一種發射綠光的有機發光材料及其制備方法與流程
本發明涉及有機發光材料技術領域,涉及一種發射綠光的有機發光材料及其制備方法。
背景技術:
有機發光二極管由于其自發光、全固態、寬視角、響應速度快、驅動電壓低、低能耗、效率高、可彎曲等諸多優點,成為研究的熱點。為實現全彩的熒光發射,紅、綠、藍三基色的熒光材料在有機發光器件領域必不可少。
2,1,3-苯并噻二唑作為電子給體常被應用于光電材料領域,由于在新型光學以及電子學材料中的潛在應用,使得這個物質在光電學和有機電致發光材料方面受到廣泛的關注,基于此結構涌現出較多的紅色發光材料。另外D-π-A構型的有機分子由于其分子內電荷轉移(ICT)能產生量子效率較高的化合物,正被廣泛應用于有機發光材料方面。
從目前研究的情況來看,藍光材料、紅光材料研究眾多,但是高效率、色度純、結構簡單的綠光材料較少,這在一定程度上限制了有機發光器件的發展。
技術實現要素:
針對現有技術不足,本發明提供一種發射綠光的有機發光材料及其制備方法,解決了現有技術中高效率、色度純、結構簡單的綠光材料較少的技術問題。
為實現以上目的,本發明通過以下技術方案予以實現:
一種發射綠光的有機發光材料,所述有機發光材料為4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑,具有式(I)所示的結構:
一種發射綠光的有機發光材料的制備方法,包括以下步驟:
S1、將2,1,3-苯并噻二唑加入裝有40-60mlHBr溶液的燒瓶中,再向燒瓶中滴加25-35mlHBr溶液,邊滴加邊攪拌,滴加完后加熱至100-200℃回流4-8h,冷卻,加入飽和的亞硫酸鈉溶液,再過濾、重結晶即得到4,7-二溴-2,1,3-苯并噻二唑;
S2、在氮氣氛圍下,向裝有甲苯、K2CO3水溶液的燒瓶中加入4,7-二溴-2,1,3-苯并噻二唑、3,5-二叔丁基苯硼酸、Cs2CO3、四三苯基膦鈀,加熱至溫度為100-150℃,反應10-36h,冷卻,得到反應混合物;
S3、將步驟S2制得的反應混合物萃取2-4次,再洗滌、干燥、減壓蒸餾,得到粗產物,再洗脫、提純,得到4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑。
優選的,步驟S2所述4,7-二溴-2,1,3-苯并噻二唑與3,5-二叔丁基苯硼酸的摩爾比為1:2-4。
優選的,步驟S2所述4,7-二溴-2,1,3-苯并噻二唑與四三苯基膦鈀的摩爾比為1:0.02-0.05。
優選的,步驟S2所述加熱至溫度為120-140℃。
優選的,步驟S2所述反應時間為20-30h。
優選的,步驟S1、步驟S2所述冷卻均冷卻至室溫。
優選的,所述步驟S3將制得的反應混合物用CH2Cl2萃取三次,有機層用鹽水洗滌之后得到的粗產物,再將粗產物用二氯甲烷和石油醚作為洗脫劑洗脫,再進行硅膠層析柱提純,即可。
本發明4,-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑的合成路線如下:
本發明提供一種發射綠光的有機發光材料及其制備方法,與現有技術相比優點在于:
本發明發射綠光的有機發光材料為4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑,該材料是一種色度純、結構簡單、熒光量子產率較高、溶解性好的綠光材料,是理想的綠光發光材料,在有機電致顯示領域有潛在的應用;
本發明發射綠光的有機發光材料的制備方法操作過程簡單,反應條件比較溫和,產物分離提純簡單,產率較高,產率能夠達到90%,所制備的綠光材料屬于小分子發光材料,在發光器件中具有很好的應用前景。
附圖說明
圖1為本發明綠光材料4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑在甲苯中的熒光發射光譜圖;
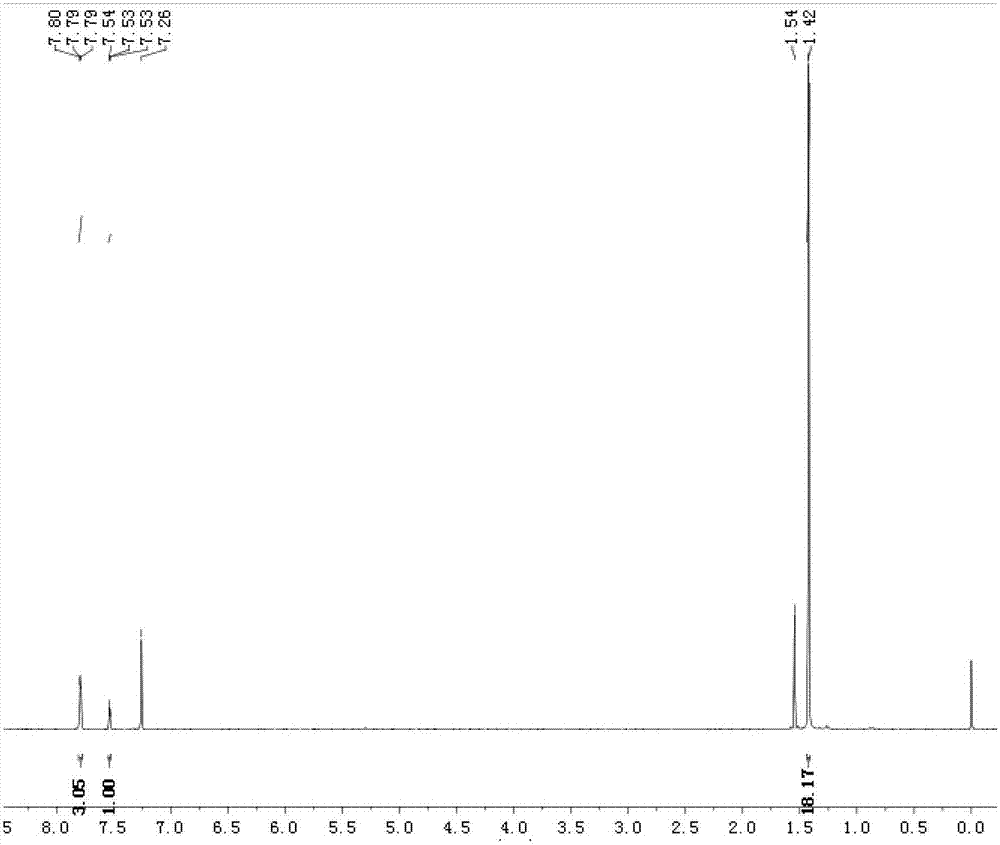
圖2為本發明綠光材料4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑的核磁共振氫譜圖。
具體實施方式
為使本發明實施例的目的、技術方案和優點更加清楚,下面結合本發明實施例對本發明實施例中的技術方案進行清楚、完整地描述,顯然,所描述的實施例是本發明一部分實施例,而不是全部的實施例。基于本發明中的實施例,本領域普通技術人員在沒有作出創造性勞動前提下所獲得的所有其他實施例,都屬于本發明保護的范圍。
實施例1:
本實施例4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑的制備方法,包括以下步驟:
S1、在250ml的圓底燒瓶中裝有50mlHBr溶液(48%),再加入3g(22.00mmol)2,1,3-苯并噻二唑,在恒壓漏斗中將10g(65.00mmol)Br2溶于30ml HBr溶液(48%),滴加至的圓底燒瓶中,邊滴加邊劇烈攪拌,全部滴加完后加熱至150℃回流6小時,反應結束后冷卻至室溫,加入飽和的亞硫酸鈉溶液,將析出的固體過濾,得到淡黃色的粗產物,將此粗產物在活性炭存在的條件下用正己烷重結晶得到4,7-二溴-2,1,3-苯并噻二唑6.08g,白色固體,計算產率為94%;
S2、在氮氣保護下,向裝有50ml甲苯,25ml K2CO3水溶液(8.0g,57.9mmol)的250ml的兩口圓底燒瓶中加入1.94g(6.6mmol)4,7-二溴-2,1,3-苯并噻二唑、3.096g(13.2mmol)3,5-二叔丁基苯硼酸、2g(6.1mmol)Cs2CO3、0.289g(0.25mmol)四三苯基膦鈀,加熱至溫度為100℃,反應24h,冷卻,得到反應混合物;
S3、將步驟S2制得的反應混合物倒入水中,用CH2Cl2萃取3次,將得到的有機層用鹽水洗滌之后,再用無水Na2SO4進行干燥,之后減壓蒸餾除去溶劑,得到粗產物,將粗產物用二氯甲烷和石油醚作為洗脫劑的溶劑進行洗脫,硅膠層析柱提純,得到4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑2.98g。制得的4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑為綠色固體。產率88%。1HNMR(400MHz,CDCl3),δ[ppm]:7.81-7.78(m,6H),7.55-7.52(t,2H),1.42(s,36H)。
將本實施例制得的4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑做熒光發射光譜實驗和核磁共振實驗,結果如圖1和圖2所示。
實施例2:
本實施例4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑的制備方法,包括以下步驟:
S1、在250ml的圓底燒瓶中裝有60mlHBr溶液(48%),再加入3g(22.00mmol)2,1,3-苯并噻二唑,在恒壓漏斗中將10g(65.00mmol)Br2溶于35ml HBr溶液(48%),滴加至的圓底燒瓶中,邊滴加邊劇烈攪拌,全部滴加完后加熱至200℃回流8小時,反應結束后冷卻至室溫,加入飽和的亞硫酸鈉溶液,將析出的固體過濾,得到淡黃色的粗產物,將此粗產物在活性炭存在的條件下用正己烷重結晶得到4,7-二溴-2,1,3-苯并噻二唑6.08g,白色固體,計算產率為92%;
S2、在氮氣保護下,向裝有50ml甲苯,25ml K2CO3水溶液(8.0g,57.9mmol)的250ml的兩口圓底燒瓶中加入1.94g(6.6mmol)4,7-二溴-2,1,3-苯并噻二唑、6.192g(26.4mmol)3,5-二叔丁基苯硼酸、2g(6.1mmol)Cs2CO3、0.587g(0.50mmol)四三苯基膦鈀,加熱至溫度為120℃,反應30h,冷卻,得到反應混合物;
S3、將步驟S2制得的反應混合物倒入水中,用CH2Cl2萃取2次,將得到的有機層用鹽水洗滌之后,再用無水Na2SO4進行干燥,之后減壓蒸餾除去溶劑,得到粗產物,將粗產物用二氯甲烷和石油醚作為洗脫劑的溶劑進行洗脫,硅膠層析柱提純,得到4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑2.88g。制得的4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑為綠色固體。產率85%。1HNMR(400MHz,CDCl3),δ[ppm]:7.81-7.78(m,6H),7.55-7.52(t,2H),1.42(s,36H)。
實施例3:
本實施例4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑的制備方法,包括以下步驟:
S1、在250ml的圓底燒瓶中裝有40mlHBr溶液(48%),再加入3g(22.00mmol)2,1,3-苯并噻二唑,在恒壓漏斗中將10g(65.00mmol)Br2溶于25ml HBr溶液(48%),滴加至的圓底燒瓶中,邊滴加邊劇烈攪拌,全部滴加完后加熱至100℃回流4小時,反應結束后冷卻至室溫,加入飽和的亞硫酸鈉溶液,將析出的固體過濾,得到淡黃色的粗產物,將此粗產物在活性炭存在的條件下用正己烷重結晶得到4,7-二溴-2,1,3-苯并噻二唑6.08g,白色固體,計算產率為95%;
S2、在氮氣保護下,向裝有50ml甲苯,25ml K2CO3水溶液(8.0g,57.9mmol)的250ml的兩口圓底燒瓶中加入1.94g(6.6mmol)4,7-二溴-2,1,3-苯并噻二唑、3.87g(16.5mmol)3,5-二叔丁基苯硼酸、2g(6.1mmol)Cs2CO3、0.289g(0.25mmol)四三苯基膦鈀,加熱至溫度為130℃,反應24h,冷卻,得到反應混合物;
S3、將步驟S2制得的反應混合物倒入水中,用CH2Cl2萃取3次,將得到的有機層用鹽水洗滌之后,再用無水Na2SO4進行干燥,之后減壓蒸餾除去溶劑,得到粗產物,將粗產物用二氯甲烷和石油醚作為洗脫劑的溶劑進行洗脫,硅膠層析柱提純,得到4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑3.05g。制得的4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑為綠色固體。產率90%。1HNMR(400MHz,CDCl3),δ[ppm]:7.81-7.78(m,6H),7.55-7.52(t,2H),1.42(s,36H)。
實施例4:
本實施例4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑的制備方法,包括以下步驟:
S1、在250ml的圓底燒瓶中裝有50mlHBr溶液(48%),再加入3g(22.00mmol)2,1,3-苯并噻二唑,在恒壓漏斗中將10g(65.00mmol)Br2溶于30ml HBr溶液(48%),滴加至的圓底燒瓶中,邊滴加邊劇烈攪拌,全部滴加完后加熱至150℃回流6小時,反應結束后冷卻至室溫,加入飽和的亞硫酸鈉溶液,將析出的固體過濾,得到淡黃色的粗產物,將此粗產物在活性炭存在的條件下用正己烷重結晶得到4,7-二溴-2,1,3-苯并噻二唑6.08g,白色固體,計算產率為94%;
S2、在氮氣保護下,向裝有50ml甲苯,25ml K2CO3水溶液(8.0g,57.9mmol)的250ml的兩口圓底燒瓶中加入1.94g(6.6mmol)4,7-二溴-2,1,3-苯并噻二唑、4.644g(19.8mmol)3,5-二叔丁基苯硼酸、2g(6.1mmol)Cs2CO3、0.3468g(0.30mmol)四三苯基膦鈀,加熱至溫度為140℃,反應36h,冷卻,得到反應混合物;
S3、將步驟S2制得的反應混合物倒入水中,用CH2Cl2萃取3次,將得到的有機層用鹽水洗滌之后,再用無水Na2SO4進行干燥,之后減壓蒸餾除去溶劑,得到粗產物,將粗產物用二氯甲烷和石油醚作為洗脫劑的溶劑進行洗脫,硅膠層析柱提純,得到4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑2.78g。制得的4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑為綠色固體。產率82%。1HNMR(400MHz,CDCl3),δ[ppm]:7.81-7.78(m,6H),7.55-7.52(t,2H),1.42(s,36H)。
綜上所述,本發明發射綠光的有機發光材料為4,7-二(3,5-二叔丁基苯基)-2,1,3-苯并噻二唑,該材料是一種色度純、結構簡單、熒光量子產率較高、溶解性好的綠光材料,是理想的綠光發光材料,在有機電致顯示領域有潛在的應用;
本發明發射綠光的有機發光材料的制備方法操作過程簡單,反應條件比較溫和,產物分離提純簡單,產率較高,所制備的綠光材料屬于小分子發光材料,在發光器件中具有很好的應用前景。
以上實施例僅用以說明本發明的技術方案,而非對其限制;盡管參照前述實施例對本發明進行了詳細的說明,本領域的普通技術人員應當理解:其依然可以對前述各實施例所記載的技術方案進行修改,或者對其中部分技術特征進行等同替換;而這些修改或者替換,并不使相應技術方案的本質脫離本發明各實施例技術方案的精神和范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!