核酸擴增的制作方法
對于用于核酸擴增的方法和試劑的需求日益增加。生成特定核酸的多個拷貝通常是必要的或有用的,以便核酸可用于給定的應用。例如,為了分析感興趣的核酸的核苷酸序列,在分析該序列之前經常復制核酸以增加它的拷貝數。在另一個實例中,為了確定樣品中特定核酸的存在或不存在,可在一定條件下處理樣品以使得如果特定核酸存在于該樣品中則它可被擴增。在另一個實例中,用作探針的核酸可進行重復拷貝以生成大量含有與原始核酸模板相同的序列的核酸,從而生成核酸的許多拷貝,該拷貝可用作探針。
已知多種用于核酸擴增的方法。例如,聚合酶鏈反應(“PCR”)(參見,例如,美國專利號4,683,202)是一種用于核酸擴增的普遍方法。為了成功地進行PCR反應,該反應必須在重復多個循環的多個不同溫度下進行。這需要用于重復地改變PCR反應的溫度的硬件或其他機構。用于核酸擴增的另一種方法被稱為環介導等溫擴增(“LAMP”)(參見,例如,美國專利號6,410,278)。LAMP反應可在等溫下進行,但通常包括四種不同引物的使用,這些引物識別靶核酸上總計六種不同的序列。
為促進生成擴增的核酸以用于使用擴增的核酸的多個和增加數量的應用,需要用于核酸擴增的新的方法和試劑。
援引并入
本說明書中提到的所有出版物、專利和專利申請均通過引用而以相同程度并入本文,猶如特別地且單獨地指出每個單獨的出版物、專利或專利申請通過引用而并入。然而,在本公開的內容與本文通過引用并入的文獻的內容之間沖突的情況下,以本公開的內容為準。
技術實現要素:
本文提供了涉及核酸擴增和多聯體生成的方法和組合物。
在一些實施方式中,本文提供了用于生成包含雙鏈核酸模板的兩個或更多個拷貝的多聯體的方法,該方法包括:(A)在使得合成與雙鏈核酸模板的第一鏈退火的第一引物的第一拷貝的延伸產物的條件下,用第一引物的第一拷貝和聚合酶處理包含雙鏈核酸模板的一級雙鏈核酸,其中第一引物包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包括:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且第一引物的第一拷貝的模板結合區與雙鏈核酸模板的第一鏈退火,(B)在使得合成與步驟(A)的第一引物的第一拷貝的延伸產物退火的第二引物的延伸產物的條件下,用第二引物和聚合酶處理步驟(A)的第一引物的第一拷貝的延伸產物,其中第二引物包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包含:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,第二引物的尾區包含與第一引物的尾區的核苷酸序列互補的核苷酸序列,如果將所述序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊并且第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,第二引物的模板結合區與步驟(A)的第一引物的第一拷貝的延伸產物退火,并且第二引物的延伸產物含有5’末端核苷酸、3’末端核苷酸以及包含3’末端核苷酸的3’末端區,其中該3’末端區含有與在5’至3’方向讀取的第二引物的尾區的核苷酸序列相同的核苷酸序列,且3’末端區的最后的核苷酸是第二引物的延伸產物的3’末端核苷酸,(C)在使得合成與步驟(B)的第二引物的延伸產物退火的第一引物的第二拷貝的延伸產物的條件下,用第一引物的第二拷貝和聚合酶處理步驟(B)的第二引物的延伸產物,以產生包含步驟(B)的第二引物的延伸產物和第一引物的第二拷貝的延伸產物的二級核酸的第一拷貝,其中第一引物的第二拷貝的延伸產物含有5’末端核苷酸、3’末端核苷酸以及包含3’末端核苷酸的3’末端區,其中該3’末端區含有與在5’至3’方向讀取的第一引物的尾區的核苷酸序列相同的核苷酸序列,并且該3’末端區的最后的核苷酸是第二引物的延伸產物的3’末端核苷酸,(D)將至少步驟(C)重復另外一次或多次以生成步驟(C)的二級核酸的至少第二拷貝,(E)在使得二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的3’末端區與二級核酸的第二拷貝的第二引物的延伸產物的3’末端區退火的條件下,處理步驟(C)的二級核酸的第一拷貝以及步驟(D)的二級核酸的第二拷貝,以產生包含二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物以及二級核酸的第二拷貝的第二引物的延伸產物的交換結構,(F)在使得合成二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的延伸產物以及合成二級核酸的第二拷貝的第二引物的延伸產物的延伸產物的條件下,用聚合酶處理步驟(E)的交換結構,以產生包含步驟(A)的雙鏈核酸模板的兩個拷貝的多聯體,其中該多聯體包含二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的延伸產物以及二級核酸的第二拷貝的第二引物的延伸產物的延伸產物。
在一些實施方式中,本文提供了用于生成包含多核苷酸模板或其類似序列的兩個或更多個拷貝的多聯體的方法,該方法包括:(A)在使得合成與多核苷酸模板退火的第一引物的第一拷貝的延伸產物的條件下,用第一引物的第一拷貝和聚合酶處理包含多核苷酸模板的一級核酸,其中第一引物包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包括:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且第一引物的第一拷貝的模板結合區與多核苷酸模板退火,(B)在使得合成與步驟(A)的第一引物的第一拷貝的延伸產物退火的第二引物的延伸產物的條件下,用第二引物和聚合酶處理步驟(A)的第一引物的第一拷貝的延伸產物,其中第二引物包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,(ii)模板結合區,其包含:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,第二引物的尾區包含與第一引物的尾區的核苷酸序列互補的核苷酸序列,如果將所述序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊以及第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,第二引物的模板結合區與步驟(A)的第一引物的第一拷貝的延伸產物退火,并且第二引物的延伸產物含有5’末端核苷酸、3’末端核苷酸以及包含3’末端核苷酸的3’末端區,其中該3’末端區含有與在5’至3’方向讀取的第二引物的尾區的核苷酸序列相同的核苷酸序列,且3’末端區的最后的核苷酸是第二引物的延伸產物的3’末端核苷酸,(C)在使得合成與步驟(B)的第二引物的延伸產物退火的第一引物的第二拷貝的延伸產物的條件下,用第一引物的第二拷貝和聚合酶處理步驟(B)的第二引物的延伸產物,以產生包含步驟(B)的第二引物的延伸產物和第一引物的第二拷貝的延伸產物的二級核酸的第一拷貝,其中第一引物的第二拷貝的延伸產物含有5’末端核苷酸、3’末端核苷酸以及包含3’末端核苷酸的3’末端區,其中該3’末端區含有與在5’至3’方向讀取的第一引物的尾區的核苷酸序列相同的核苷酸序列,并且該3’末端區的最后的核苷酸是第二引物的延伸產物的3’末端核苷酸,(D)將至少步驟(C)重復另外一次或多次以生成包含步驟(B)的第二引物的延伸產物和步驟(C)的第一引物的第二拷貝的延伸產物的二級核酸的至少第二拷貝,(E)在使得二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的3’末端區與二級核酸的第二拷貝的第二引物的延伸產物的3’末端區退火的條件下,處理步驟(C)的二級核酸的第一拷貝以及步驟(D)的二級核酸的第二拷貝,以產生包含二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物以及二級核酸的第二拷貝的第二引物的延伸產物的交換結構,(F)在使得合成二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的延伸產物以及合成二級核酸的第二拷貝的第二引物的延伸產物的延伸產物的條件下,用聚合酶處理步驟(E)的交換結構,以產生包含步驟(A)的多核苷酸模板的兩個拷貝的多聯體,其中該多聯體包含二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的延伸產物以及二級核酸的第二拷貝的第二引物的延伸產物的延伸產物。在一些實施方式中,步驟(A)的核酸聚合酶是DNA聚合酶。在一些實施方式中,步驟(A)的核酸聚合酶是逆轉錄酶。
在一些實施方式中,本文提供了用于生成包含雙鏈核酸模板的兩個或更多個拷貝的多聯體的方法,該方法包括:(A)制備反應混合物,其包含:(i)包含雙鏈核酸模板的一級核酸,(ii)分離的核酸聚合酶,(iii)第一引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(a)尾區,其包含:(1)引物的5’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(3)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(b)模板結合區,其包括:(1)引物的3’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(3)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,其中模板結合區與核酸模板的第一鏈互補,(iv)第二引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(a)尾區,其包含:(1)引物的5’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(3)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(b)模板結合區,其包含:(1)引物的3’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(3)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且其中模板結合區與核酸模板的第二鏈互補,并且其中如果將所述序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊并且第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,第二引物的尾區含有與第一引物的尾區的核苷酸序列互補的核苷酸序列,以及(B)在沒有熱循環的情況下將反應混合物溫育至少3分鐘。
在一些實施方式中,本文提供了用于生成包含多核苷酸模板的兩個或更多個拷貝的多聯體的方法,該方法包括:(A)制備反應混合物,其包含:(i)包含多核苷酸模板的核酸,(ii)分離的核酸聚合酶,(iii)第一引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(a)尾區,其包含:(1)引物的5’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(3)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(b)模板結合區,其包括:(1)引物的3’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(3)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且其中模板結合區與多核苷酸模板互補,(iv)第二引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(a)尾區,其包含:(1)引物的5’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(3)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(b)模板結合區,其包含:(1)引物的3’末端核苷酸,(2)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(3)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且其中模板結合區與互補于多核苷酸模板的核苷酸序列互補,并且其中如果將所述引物的序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊并且第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,第二引物的尾區含有與第一引物的尾區的核苷酸序列互補的核苷酸序列,以及(B)在不高于80℃的溫度下將反應混合物溫育至少3分鐘。
在一些實施方式中,本文提供了用于生成包含雙鏈核酸模板的兩個或更多個拷貝的多聯體的方法,該方法包括:將包含雙鏈核酸模板的雙鏈核酸分子的第一拷貝和第二拷貝與聚合酶一起溫育,以產生包含與交換結構的第二鏈的延伸產物退火的交換結構的第一鏈的延伸產物的多聯體,其中該多聯體包含雙鏈核酸模板的兩個拷貝,其中雙鏈核酸分子包含各自含有多個核苷酸的第一鏈和第二鏈,第一鏈包含5’末端核苷酸和3’末端核苷酸,并含有5’至3’方向的通用格式的區域:A1-B-A2,第二鏈包含5’末端核苷酸和3’末端核苷酸,并含有5’至3’方向的通用格式的區域:C1-D-C2,區域B包含雙鏈核酸模板的第一鏈的核苷酸序列,區域D包含雙鏈核酸模板的第二鏈的核苷酸序列,在雙鏈核酸分子中,區域A1與C2退火,B與D退火,且A2與C1退火,生成了包含雙鏈核酸分子的第一拷貝的第一鏈以及雙鏈核酸分子的第二拷貝的第二鏈的交換結構,其中第一鏈的A2區域與第二鏈的C2區域退火,合成了交換結構的第一鏈的延伸產物,并合成了交換結構的第二鏈的延伸產物。
在實施方式中,本文提供了拷貝多核苷酸模板的方法,該方法包括:在包含第一引物的多個拷貝和第二引物的多個拷貝的反應混合物中溫育多核苷酸模板,其中:第一引物包含第一區域和第二區域,其中第一引物的第二區域包含與多核苷酸模板的第一部分互補的核苷酸序列;第二引物包含第一區域和第二區域,其中第二引物的第二區域包含與配偶體核苷酸序列互補的核苷酸序列,其中該配偶體核苷酸序列與多核苷酸模板的第二部分互補;并且在多核苷酸模板與第一引物的多個拷貝和第二引物的多個拷貝一起溫育時,形成至少一條多聯體鏈,其中該多聯體鏈包含5’端和3’端,并且包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列,其中:C’表示第二引物的第一區域的核苷酸序列,T表示多核苷酸模板的核苷酸序列或其類似序列,且X表示任何數目和序列的核苷酸。
在一些實施方式中,在本文提供的包括形成包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列的多聯體鏈的方法中,該多聯體鏈是第一多聯體鏈,并且還形成了第二多聯體鏈,其中該第二多聯體鏈包含5’端和3’端,并且包含具有5’至3’方向的通用結構C-X’-T’-C-T’-C的核苷酸序列,其中:C表示第一引物的第一區域的核苷酸序列,T’表示與多核苷酸模板互補的核苷酸序列,且X’表示與X的核苷酸序列互補的核苷酸序列。
在實施方式中,本文提供了測定生物樣品中的靶多核苷酸模板的方法,該方法包括:A)在包含第一引物的多個拷貝和第二引物的多個拷貝的反應混合物中溫育生物樣品或其部分,其中:第一引物包含第一區域和第二區域,其中第一引物的第二區域包含與多核苷酸模板的第一部分互補的核苷酸序列;第二引物包含第一區域和第二區域,其中第二引物的第二區域包含與配偶體核苷酸序列互補的核苷酸序列,其中該配偶體核苷酸序列與多核苷酸模板的第二部分互補;并且在多核苷酸模板與第一引物的多個拷貝和第二引物的多個拷貝一起溫育時,形成至少一條多聯體鏈,其中該多聯體鏈包含5’端和3’端,并且包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列,其中:C’表示第二引物的第一區域的核苷酸序列,T表示多核苷酸模板的核苷酸序列或其類似序列,且X表示任何數目和序列的核苷酸;以及B)在A)溫育步驟開始后在一個或多個點測量A)的反應混合物中擴增的核酸的量。在實施方式中,測量反應混合物中擴增的核酸的量可包括確定反應混合物中的熒光的水平。在實施方式中,該方法可進一步包括確定反應混合物中的核酸擴增的轉變時間。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器(vessel)或試劑盒中,X可含有具有5’至3’方向的通用結構[(C’-T)N]的序列,其中C’表示第二引物的第一區域的核苷酸序列,T表示多核苷酸模板的核苷酸序列或其類似序列,且N為0至2000之間的任何整數。在實施方式中,N可以是0至10、0至100、0至1000、0至5000、0至10,000、1至10、1至100、1至1000、1至2000、1至5000或1至10,000之間的任何整數。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,X可含有不多于0、1、2、3、4、5、6、7、8、9、10、15、20、25、50、100、500、1000、10,000、50,000、100,000或500,000個核苷酸。在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、容器或試劑盒中,X可含有至少1、2、3、4、5、6、7、8、9、10、15、20、25、50、100、500、1000、10,000、50,000、100,000或500,000個核苷酸。在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、容器或試劑盒中,X可含有至少1、2、3、4、5、6、7、8、9、10、15、20、25、50、100、500、1000、10,000、50,000、100,000個核苷酸,并且不多于2、3、4、5、6、7、8、9、10、15、20、25、50、100、500、1000、10,000、50,000、100,000或500,000個核苷酸。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,在至少一個C’與T之間,存在并非C’或T序列的一部分的一個或多個額外的核苷酸。所述一個或多個額外的核苷酸可以是,例如,1至10、1至20、1至100或1至1000個核苷酸。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,至少一個C’或T序列可缺失一個或多個核苷酸。在2個或更多個核苷酸缺失的情況下,缺失的核苷酸可以是鄰近的,或者可以在分開的位置。所述一個或多個缺失的核苷酸可以是,例如,1至10、1至20、1至100或1至1000個核苷酸。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,至少一個C’或T序列可具有一個或多個點突變。在存在兩個或更多個點突變的情況下,點突變可以是鄰近的,或者可以在分開的位置。所述一個或多個點突變可以是,例如,1至10、1至20、1至100或1至1000個點突變。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,核苷酸序列具有以下特點中的兩個或全部三個:i)在至少一個C’與T之間,存在并非C’或T序列的一部分的一個或多個額外的核苷酸;ii)至少一個C’或T序列缺失一個或多個核苷酸;以及iii)至少一個C’或T序列含有一個或多個點突變。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,在多核苷酸模板是RNA分子的實施方式中,T可表示與多核苷酸模板的RNA序列類似的DNA序列的核苷酸序列。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,該多聯體鏈進一步包含位于最5’的C’序列的5’的一個或多個核苷酸。所述一個或多個核苷酸可以是,例如,1至10、1至20、1至100或1至1000個核苷酸。
在實施方式中,在本文提供的包含多聯體鏈(其包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,該多聯體鏈進一步包含位于最3’的C’序列的3’的一個或多個核苷酸。所述一個或多個核苷酸可以是,例如,1至10、1至20、1至100或1至1000個核苷酸。
在實施方式中,本文提供了生成包含雙鏈核酸模板的至少兩個拷貝的多聯體的方法,該方法包括:在反應混合物中溫育至少第一模板分子和第二模板分子,其中:第一模板分子包含第一核酸鏈和第二核酸鏈,其中:第一模板分子的第一核酸鏈包含具有5’至3’方向的通用結構H’-S-Y1-H’的核苷酸序列,其中:H’表示第一同源序列的核苷酸序列,S表示雙鏈核酸模板的第一鏈的核苷酸序列,且Y1表示任何數目和序列的核苷酸;并且第一模板分子的第二核酸鏈包含具有5’至3’方向的通用結構H-Y1’-S’-H的核苷酸序列,其中:H表示第二同源序列的核苷酸序列,其中第一同源序列與第二同源序列彼此互補,Y1’表示與Y1的核苷酸序列互補的核苷酸序列,且S’表示雙鏈核酸模板的第二鏈的核苷酸序列,其中雙鏈核酸模板的第一鏈和第二鏈彼此互補;并且第二模板分子包含第一核酸鏈和第二核酸鏈,其中:第二模板分子的第一核酸鏈包含具有5’至3’方向的通用結構H’-S-Y2-H’的核苷酸序列,其中:H’表示第一同源序列的核苷酸序列,S表示雙鏈核酸模板的第一鏈的核苷酸序列,且Y2表示任何數目和序列的核苷酸;且第一模板分子的第二核酸鏈包含具有5’至3’方向的通用結構H-Y2’-S’-H的核苷酸序列,其中:H表示第二同源序列的核苷酸序列,Y2’表示與Y2的核苷酸序列互補的核苷酸序列,且S’表示雙鏈核酸模板的第二鏈的核酸序列;并且在反應混合物中的第一模板分子與第二模板分子一起溫育時,形成包含雙鏈核酸模板的至少兩個拷貝的至少一個多聯體,其中多聯體包含第一多聯體鏈和第二多聯體鏈,其中第一多聯體鏈包含5’端和3’端,并包含具有5’至3’方向的通用結構H’-S-Y2-H’-S-Y1-H’的核苷酸序列,其中H’、Y1、S和Y2中的每一個均表示如上所述的核苷酸序列;并且其中第二多聯體鏈包含5’端和3’端,并包含具有5’至3’方向的通用結構H-Y1’-S’-H-Y2’-S’-H的序列,其中,H’、Y1、S和Y2中的每一個均表示如上所述的核苷酸序列。
在實施方式中,在本文提供的包含第一多聯體鏈(其包含具有5’至3’方向的通用結構H’-S-Y2-H’-S-Y1-H’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,Y1和Y2中的至少一個或兩者可表示0個核苷酸。
在實施方式中,在本文提供的包含第一多聯體鏈(其包含具有5’至3’方向的通用結構H’-S-Y2-H’-S-Y1-H’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,Y1可含有具有5’至3’方向的通用結構[(H’-S)N1]的序列,其中H’和S表示如上所述的核苷酸序列,且N1是0至2000之間的任何整數。
在實施方式中,在本文提供的包含第一多聯體鏈(其包含具有5’至3’方向的通用結構H’-S-Y2-H’-S-Y1-H’的核苷酸序列)的方法、反應混合物、容器或試劑盒中,Y2可含有具有5’至3’方向的通用結構[(H’-S)N2]的序列,其中H’和S表示如上所述的核苷酸序列,且N2是0至2000之間的任何整數。
在實施方式中,在本文提供的包含第一模板分子和第二模板分子的方法、反應混合物、容器或試劑盒中,第一模板分子和第二模板分子兩者均為雙鏈DNA分子。
在實施方式中,在本文提供的包含第一模板分子的第一核酸鏈的方法、反應混合物、容器或試劑盒中,其中第一核酸鏈包含具有5’至3’方向的通用結構H’-S-Y1-H’的核苷酸序列,其中H’表示第一同源序列的核苷酸序列,第一同源序列可含有不多于4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、40、50、60、70、80、90或100個核苷酸。在實施方式中,第一同源序列可含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、40、50、60、70、80、90或100個核苷酸。在實施方式中,第一同源序列可含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、40、50、60、70、80、90或100個且不多于5、6、7、8、9、10、11、12、13、14、15、20、25、30、40、50、60、70、80、90、100或200個核苷酸。
在實施方式中,本文提供的反應混合物、容器或試劑盒包含核酸聚合酶。在實施方式中,核酸聚合酶是具有鏈置換活性的DNA聚合酶。在實施方式中,核酸聚合酶是RNA聚合酶。在實施方式中,核酸聚合酶是逆轉錄酶。在實施方式中,反應混合物、容器或試劑盒包含多于一種核酸聚合酶,諸如具有鏈置換活性的DNA聚合酶和逆轉錄酶兩種酶。在實施方式中,本文提供的反應混合物、容器或試劑盒包含核苷酸和緩沖液。
在實施方式中,在本文提供的包含多核苷酸模板的方法、反應混合物、容器或試劑盒中,多核苷酸模板是單鏈分子。在實施方式中,在本文提供的包含多核苷酸模板的方法、反應混合物、容器或試劑盒中,多核苷酸模板包含雙鏈核酸模板的一條鏈。在實施方式中,在本文提供的包含多核苷酸模板的方法、反應混合物、容器或試劑盒中,多核苷酸模板是DNA或RNA分子。
在實施方式中,在本文提供的包含核酸模板的方法、反應混合物、容器或試劑盒中,核酸模板是RNA或DNA分子。在實施方式中,核酸模板可以是單鏈或雙鏈分子。
在實施方式中,在本文提供的包括溫育反應混合物的方法中,在溫育反應混合物的過程中,反應混合物的溫度不超過90、85、80、75、70、65、60、55、50、45、40、37、35、30、25或20℃。在實施方式中,在本文提供的方法中,該方法的所有步驟均在不高于90、85、80、75、70、65、60、55、50、45、40、37、35、30、25或20℃的溫度下進行。在實施方式中,本文提供的反應混合物、容器或試劑盒保持不高于90、85、80、75、70、65、60、55、50、45、40、37、35、30、25、或20℃的溫度。在實施方式中,本文提供的方法在沒有熱循環的情況下進行。
在實施方式中,在本文提供的包含含有第一部分的多核苷酸模板的方法、反應混合物、容器或試劑盒中,第一部分含有不多于5、10、15、20、25、30、35、40、50、60、70、80、90、100或200個核苷酸。在實施方式中,在本文提供的包含含有第一部分的多核苷酸模板的方法、反應混合物、容器或試劑盒中,第一部分含有至少5、10、15、20、25、30、35、40、50、60、70、80、90、100或200個核苷酸。在實施方式中,在本文提供的包含含有第一部分的多核苷酸模板的方法、反應混合物、容器或試劑盒中,第一部分含有至少5、10、15、20、25、30、35、40、50、60、70、80、90或100個且不多于10、15、20、25、30、35、40、50、60、70、80、90、100或200個核苷酸。
在實施方式中,在本文提供的包含含有第一區域的引物的方法、反應混合物、容器或試劑盒中,第一區域含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、或100個核苷酸。在實施方式中,在本文提供的包含含有第一區域的引物的方法、反應混合物、容器或試劑盒中,第一區域含有不多于4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有第一區域的引物的方法、反應混合物、容器或試劑盒中,第一區域含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80或90個且不多于5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有第一區域的第一引物和含有第一區域的第二引物的方法、反應混合物、容器或試劑盒中,第一引物和第二引物兩者均可具有以上所述的任何特征。在實施方式中,在本文提供的包含含有第一區域的第一引物和含有第一區域的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的第一區域和第二引物的第一區域可含有相同數目的核苷酸。在實施方式中,在本文提供的包含含有第一區域的第一引物和含有第一區域的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的第一區域和第二引物的第一區域可含有不同數目的核苷酸。
在實施方式中,在本文提供的包含含有第二區域的引物的方法、反應混合物、容器或試劑盒中,第二區域含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、或100個核苷酸。在實施方式中,在本文提供的包含含有第二區域的引物的方法、反應混合物、容器或試劑盒中,第二區域含有不多于4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有第二區域的引物的方法、反應混合物、容器或試劑盒中,第二區域含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80或90個且不多于5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有第二區域的第一引物和含有第二區域的第二引物的方法、反應混合物、容器或試劑盒中,第一引物和第二引物兩者均可具有以上所述的任何特征。在實施方式中,在本文提供的包含含有第二區域的第一引物和含有第二區域的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的第二區域和第二引物的第二區域可含有相同數目的核苷酸。在實施方式中,在本文提供的包含含有第二區域的第一引物和含有第二區域的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的第二區域和第二引物的第二區域可含有不同數目的核苷酸。
在實施方式中,在本文提供的包含含有第二區域的第二引物和包含第二部分的多核苷酸模板的方法、反應混合物、容器或試劑盒中,第二引物的第二區域的核苷酸序列與多核苷酸模板的第二部分的核苷酸序列相同。
在實施方式中,在本文提供的包含含有尾區的引物的方法、反應混合物、容器或試劑盒中,尾區含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有尾區的引物的方法、反應混合物、容器或試劑盒中,尾區含有不多于4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有尾區的引物的方法、反應混合物、容器或試劑盒中,尾區含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80或90個且不多于5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有尾區的第一引物和含有尾區的第二引物的方法、反應混合物、容器或試劑盒中,第一引物和第二引物兩者均可具有以上所述的任何特征。在實施方式中,在本文提供的包含含有尾區的第一引物和含有尾區的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的尾區和第二引物的尾區可含有相同數目的核苷酸。在實施方式中,在本文提供的包含含有尾區的第一引物和含有尾區的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的尾區和第二引物的尾區可含有不同數目的核苷酸。
在實施方式中,在本文提供的包含含有模板結合區的引物的方法、反應混合物、容器或試劑盒中,第二區域含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有模板結合區的引物的方法、反應混合物、容器或試劑盒中,模板結合區含有不多于4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有模板結合區的引物的方法、反應混合物、容器或試劑盒中,模板結合區含有至少4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80或90個且不多于5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90或100個核苷酸。在實施方式中,在本文提供的包含含有模板結合區的第一引物和含有模板結合區的第二引物的方法、反應混合物、容器或試劑盒中,第一引物和第二引物兩者均可具有以上所述的任何特征。在實施方式中,在本文提供的包含含有模板結合區的第一引物和含有模板結合區的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的模板結合區和第二引物的模板結合區可含有相同數目的核苷酸。在實施方式中,在本文提供的包含含有模板結合區的第一引物和含有模板結合區的第二引物的方法、反應混合物、容器或試劑盒中,第一引物的模板結合區和第二引物的模板結合區可含有不同數目的核苷酸。
在實施方式中,在本文提供的包含多核苷酸模板的方法、反應混合物、容器或試劑盒中,多核苷酸模板可含有至少8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000或5000個核苷酸。在實施方式中,在本文提供的包含多核苷酸模板的方法、反應混合物、容器或試劑盒中,多核苷酸模板可含有不多于8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000、5000或10,000個核苷酸。在實施方式中,在本文提供的包含多核苷酸模板的方法、反應混合物、容器或試劑盒中,多核苷酸模板可含有至少8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000或5000個且不多于9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000、5000或10,000個核苷酸。
在實施方式中,在本文提供的包含雙鏈核酸模板的方法、反應混合物、容器或試劑盒中,雙鏈核酸模板的每一條鏈可含有至少8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000或5000個核苷酸。在實施方式中,在本文提供的包含雙鏈核酸模板的方法、反應混合物、容器或試劑盒中,雙鏈核酸模板的每一條鏈可含有不多于8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000、5000或10,000個核苷酸。在實施方式中,在本文提供的包含雙鏈核酸模板的方法、反應混合物、容器或試劑盒中,雙鏈核酸模板的每一條鏈可含有至少8、9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000或5000個且不多于9、10、11、12、13、14、15、20、25、30、35、40、50、60、70、80、90、100、200、500、1000、2000、5000或10,000個核苷酸。
在實施方式中,本文提供的反應混合物、容器或試劑盒不含有重組酶。
在實施方式中,本文提供的方法、反應混合物、容器或試劑盒可含有或包含引物的多個拷貝。所述多個拷貝可以是,例如,引物的至少5、10、15、20、50、100、500、1000、10,000、100,000或1,000,000個拷貝。
在實施方式中,本文提供的反應混合物或容器可包含來自受試者的生物樣品的至少一部分。該生物樣品可以是,例如,唾液、血液、尿液、臉頰拭子或鼻拭子。該受試者可以是人。
在一些實施方式中,本文提供的方法的所有步驟均在不高于70、65、60、65、60、55、50、45、40、35、30、25、20、15或10℃的溫度下進行。在一些實施方式中,本文提供的方法的一些步驟在不高于70、65、60、65、60、55、50、45、40、35、30、25、20、15或10℃的溫度下進行。
在一些實施方式中,本文提供的方法的兩個或更多個步驟在相同的反應混合物中同時進行。在一些實施方式中,本文提供的方法的所有步驟均在相同的反應混合物中同時進行。
在一些實施方式中,在本文提供的方法中,在該方法開始后的5、10、15、20、30、40、50、60、70、80、90、120或180分鐘內核酸模板擴增了至少10、100、1000、10,000、100,000或1,000,000倍。在一些實施方式中,在本文提供的方法中,在該方法開始后的5、10、15、20、30、40、50、60、70、80、90、120或180分鐘內反應混合物中核酸模板的拷貝數增加了至少10、100、1000、10,000、100,000或1,000,000倍。
在實施方式中,本文提供的核酸模板可以是單鏈或雙鏈核酸模板。
在實施方式中,本文提供了一種容器,該容器包含在其中流體連通的:第一引物,其中該第一引物包含第一區域和第二區域,并且其中第一引物的第二區域包含與多核苷酸模板的第一部分互補的核苷酸序列;第二引物,其中該第二引物包含第一區域和第二區域,并且其中第二引物的第二區域包含與配偶體核苷酸序列互補的核苷酸序列,其中該配偶體核苷酸序列與多核苷酸模板的第二部分互補;以及至少一條多聯體鏈,其中該多聯體鏈包含5’端和3’端,并且包含具有5’至3’方向的通用結構C’-T-C’-T-X-C’的核苷酸序列,其中:C’表示第二引物的第一區域的核苷酸序列,T表示多核苷酸模板的核苷酸序列或其類似序列,且X表示任何數目和序列的核苷酸。
在一些實施方式中,本文提供了一種容器,該容器包含在其中流體流通的:(A)分離的核酸聚合酶,(B)包含至少第一鏈的核酸模板,(C)第一引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包括:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,其中模板結合區與核酸模板的第一鏈互補,以及(D)第二引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包含:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且其中模板結合區與互補于核酸模板的第一鏈的核苷酸序列互補,并且其中如果將引物的序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊并且第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,第二引物的尾區含有與第一引物的尾區的核苷酸序列互補的核苷酸序列。
在實施方式中,本文提供了一種試劑盒,其包含兩個或更多個流體隔離的器皿(container),該器皿共同包含:第一引物,其中第一引物包含第一區域和第二區域,并且其中第一引物的第二區域包含與多核苷酸模板的第一部分互補的核苷酸序列;第二引物,其中第二引物包含第一區域和第二區域,并且其中第二引物的第二區域包含與配偶體核苷酸序列互補的核苷酸序列,其中該配偶體核苷酸序列與核苷酸模板的第二部分互補;以及分離的具有鏈置換活性的DNA聚合酶;其中:第一引物的第一區域和第二引物的第一區域互補。
在一些實施方式中,本文提供了一種用于檢測包含至少第一鏈的感興趣的靶核酸的試劑盒,該試劑盒包含兩個或更多個流體隔離的器皿,該器皿共同包含:(A)分離的核酸聚合酶,(B)第一引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包括:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,其中模板結合區與靶核酸的第一鏈互補,以及(C)第二引物,其包含5’末端核苷酸、3’末端核苷酸以及兩個區域:(i)尾區,其包含:(a)引物的5’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,(c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,以及(ii)模板結合區,其包含:(a)引物的3’末端核苷酸,(b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,(c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸,并且其中模板結合區與互補于靶核酸的第一鏈的核苷酸序列互補,并且其中如果將引物的序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊并且第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,第二引物的尾區含有與第一引物的尾區的核苷酸序列互補的核苷酸序列。
在一些實施方式中,本文提供的試劑盒包含具有感興趣的靶核酸的核苷酸序列的核酸。
在一些實施方式中,本文提供的反應混合物、容器或試劑盒包含核酸染料。
在一些實施方式中,在本文提供的包含分離的核酸聚合酶的容器或試劑盒中,分離的核酸聚合酶是DNA聚合酶。在一些實施方式中,在本文提供的包含分離的核酸聚合酶的容器或試劑盒中,分離的核酸聚合酶是逆轉錄酶。在一些實施方式中,在本文提供的包含分離的核酸聚合酶的容器或試劑盒中,該容器或試劑盒包含DNA聚合酶和逆轉錄酶兩者。
在一些實施方式中,在本文提供的包含核酸聚合酶的方法、容器或試劑盒中,該核酸聚合酶具有鏈置換活性。
在一些實施方式中,本文提供的方法包括用核酸染料處理一個或多個反應組分或該方法的步驟。
在一些實施方式中,在本文提供的包含核酸模板的方法、容器或試劑盒中,模板是DNA分子。在一些實施方式中,在本文提供的包含核酸模板的方法、容器或試劑盒中,模板是RNA分子。
在一些實施方式中,在本文提供的包含第一引物的方法、容器或試劑盒中,第一引物的尾區包含至少4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20個核苷酸。在一些實施方式中,在本文提供的包含第一引物的方法、容器或試劑盒中,第一引物的尾區包含不多于4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50或60個核苷酸。
在一些實施方式中,在本文提供的包含第二引物的方法、容器或試劑盒中,第二引物的尾區包含至少4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20個核苷酸。在一些實施方式中,在本文提供的包含第二引物的方法、容器或試劑盒中,第二引物的尾區包含不多于4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50或60個核苷酸。
在一些實施方式中,在本文提供的包含第一引物的方法、容器或試劑盒中,第一引物的模板結合區包含至少4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20個核苷酸。在一些實施方式中,在本文提供的包含第一引物的方法、容器或試劑盒中,第一引物的模板結合區包含不多于4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50或60個核苷酸。
在一些實施方式中,在本文提供的包含第二引物的方法、容器或試劑盒中,第二引物的模板結合區包含至少4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20個核苷酸。在一些實施方式中,在本文提供的包含第二引物的方法、容器或試劑盒中,第二引物的模板結合區包含不多于4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50或60個核苷酸。
在一些實施方式中,在本文提供的其中RNA分子是模板分子或一級核酸的方法和組合物中,模板的擴增可以指對應于RNA分子的DNA鏈的拷貝的生成。
在一些實施方式中,本文提供的方法包括測量來自包括本方法的測定的熒光信號。
在一些實施方式中,核酸連接酶可包含在本文提供的方法或組合物中。在一些實施方式中,相比于如果核酸連接酶不包含在反應中,當連接酶包含在反應混合物中用于本文提供的方法時,采用本文提供的方法可更快速地擴增核酸模板。在實施方式中,本文提供的反應混合物、容器或試劑盒可含有具有連接酶活性的酶。
在實施方式中,本文提供了測定樣品中的病原體的方法,該方法包括進行如本文提供的方法以從病原體中擴增核酸。在實施方式中,在本文提供的組合物或方法中使用的靶核酸可以是來自病原體的核酸。在實施方式中,在本文提供的方法中使用的第一和第二引物可各自含有與病原體的核酸中的序列互補的區域,或者與互補于病原體核酸中的序列的序列互補的區域。在實施方式中,病原體的核酸可以是DNA或RNA。病原體可包括但不限于病毒、細菌、真菌和原生生物。樣品可來自受試者,并可具有本文其他地方所述的任何樣品特征。
在實施方式中,本文提供的用于核酸擴增的方法可用于人體或動物體外部的診斷方法。例如,樣品可從人或動物中獲得,并且可用本文提供的用于核酸擴增的方法測定樣品中感興趣的靶核酸。
在實施方式中,本文提供的方法可包括:a)在反應混合物中提供一種或多種用于進行如本文所述的方法的試劑(例如,第一引物、第二引物、核酸模板、核酸聚合酶、核苷酸、緩沖液、水等中的一種或多種),以及b)在基本等溫的溫度下溫育反應混合物,其中在溫育期間反應混合物的溫度偏離中心溫度不多于或少于20、15、10、9、8、7、6、5、4、3、2或1攝氏度。在實施方式中,中心溫度可以是,例如,30、35、40、45、50、55、60、65、70、75或80攝氏度。
在實施方式中,本文提供的方法可以在基本等溫的溫度下進行。在實施方式中,基本等溫的溫度可以是30、35、40、45、50、55、60、65、70、75或80攝氏度加或減20、15、10、9、8、7、6、5、4、3、2或1攝氏度中的任何溫度。
在實施方式中,本文提供的方法可在一個或多個溫度下進行,該溫度均不超過90、85、80、75、70、65、60、55、50、45、40、35、30、或25攝氏度。
在本文提供的包含含有第一區域的第一引物和含有第一區域的第二引物的組合物和方法中,其中第一引物的第一區域與第二引物的第一區域互補,在實施方式中,第一引物的第一區域和第二引物的第一區域含有核苷酸序列,使得雙鏈結構不會形成限制酶識別序列,該雙鏈結構根據沃森-克里克(Watson-Crick)堿基配對原則通過第一引物的第一區域與第二引物的第一區域退火而形成。
在本文提供的包含核酸聚合酶的組合物和方法中,在實施方式中,該核酸聚合酶具有3’至5’外切核酸酶活性。
除非上下文另外明確指出,本文中對生成多核苷酸模板或核酸模板的拷貝或擴增多核苷酸模板或核酸模板的提及包括生成含有多核苷酸模板/核酸模板的序列的拷貝,以及生成含有多核苷酸模板/核酸模板的類似序列的拷貝。例如,如果多核苷酸模板是RNA,則生成模板的拷貝可包括生成這樣的拷貝,該拷貝是含有多核苷酸模板的RNA序列的DNA形式的DNA分子(即,在DNA序列中,含有T而非U)。
附圖說明
在附圖中,
圖1為本文提供的方法的總的示意圖;圖1A-1K示出了本方法的步驟和特征。圖1包含以下的核苷酸序列:103:AACGGTTGCTC(SEQ ID NO:1);104:GAGCAACCGTT(SEQ ID NO:2);105:ATGGGAGC(SEQ ID NO:3);106:CCATAACG(SEQ ID NO:4);111:ATGGGAGCAACCGTT(SEQ ID NO:5);112:CCATAACGGTTGCTCCCAT(SEQ ID NO:6);113:ATGGGAGCAACCGTTATGG(SEQ ID NO:7);121:CCATAACGGTTGCTCCCATAACGGTTGCTCCCAT(SEQ ID NO:8);122:ATGGGAGCAACCGTTATGGGAGCAACCGTTATGG(SEQ ID NO:9)。
圖2A示出了與本文提供的方法一起使用的某些引物的核苷酸序列。圖2A包含以下的核苷酸序列:P1引物,37個核苷酸:CGCCGGATGGCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:10);P1引物,35個核苷酸:CCGGATGGCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:11);P1引物,33個核苷酸:GGATGGCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:12);P1引物,31個核苷酸:ATGGCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:13);P1引物,30個核苷酸:TGGCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:14);P1引物,29個核苷酸:GGCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:15);P1引物,28個核苷酸:GCTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:16);P1引物,27個核苷酸:CTCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:17);P1引物,26個核苷酸:TCTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:18);P1引物,25個核苷酸:CTTGGGAAACCAAACCGTACCAACC(SEQ ID NO:19);P1引物,24個核苷酸:TTGGGAAACCAAACCGTACCAACC(SEQ ID NO:20);P1引物,23個核苷酸:TGGGAAACCAAACCGTACCAACC(SEQ ID NO:21);P2引物,36個核苷酸:GTTTCCCAAGAGCCATCCGGCGATGCGGAATGTACC(SEQ ID NO:22);P2引物,34個核苷酸:GTTTCCCAAGAGCCATCCGGATGCGGAATGTACC(SEQ ID NO:23);P2引物,32個核苷酸:GTTTCCCAAGAGCCATCCATGCGGAATGTACC(SEQ ID NO:24);P2引物,30個核苷酸:GTTTCCCAAGAGCCATATGCGGAATGTACC(SEQ ID NO:25);P2引物,29個核苷酸:GTTTCCCAAGAGCCAATGCGGAATGTACC(SEQ ID NO:26);P2引物,28個核苷酸:GTTTCCCAAGAGCCATGCGGAATGTACC(SEQ ID NO:27);P2引物,27個核苷酸:GTTTCCCAAGAGCATGCGGAATGTACC(SEQ ID NO:28);P2引物,26個核苷酸:GTTTCCCAAGAGATGCGGAATGTACC(SEQ ID NO:29);P2引物,25個核苷酸:GTTTCCCAAGAATGCGGAATGTACC(SEQ ID NO:30);P2引物,24個核苷酸:GTTTCCCAAGATGCGGAATGTACC(SEQ ID NO:31);P2引物,23個核苷酸:GTTTCCCAAATGCGGAATGTACC(SEQ ID NO:32);以及P2引物,22個核苷酸:GTTTCCCAATGCGGAATGTACC(SEQ ID NO:33)。
圖2B為示出了根據本文提供的方法進行的反應的結果的圖。
圖3A和3B示出了與本文提供的方法一起使用的某些引物的核苷酸序列。圖3A包含以下的核苷酸序列:C5:ATGGCTCTTGGGAAACTGAAACCGTACCAACC(SEQ ID NO:34);D5:GTTTCCCAAGAGCCATGGATGCGGAATGTACC(SEQ ID NO:35);C6:GGCTCTTGGGAAACTGAAACCGTACCAACC(SEQ ID NO:36);D6:GTTTCCCAAGAGCCGGATGCGGAATGTACC(SEQ ID NO:37);C7:CTCTTGGGAAACTGAAACCGTACCAACC(SEQ ID NO:38);D7:GTTTCCCAAGAGGGATGCGGAATGTACC(SEQ ID NO:39);C8:TCTTGGGAAACTGAAACCGTACCAACC(SEQ ID NO:40);D8:GTTTCCCAAGAGGATGCGGAATGTACC(SEQ ID NO:41);C9:CTTGGGAAACTGAAACCGTACCAACC(SEQ ID NO:42);D9:GTTTCCCAAGGGATGCGGAATGTACC(SEQ ID NO:43);C10:TTGGGAAACTGAAACCGTACCAACC(SEQ ID NO:44);D10:GTTTCCCAAGGATGCGGAATGTACC(SEQ ID NO:45);C11:TGGGAAACTGAAACCGTACCAACC(SEQ ID NO:46);D11:GTTTCCCAGGATGCGGAATGTACC(SEQ ID NO:47);C12:GGGAAACTGAAACCGTACCAACC(SEQ ID NO:48);以及D12:GTTTCCCGGATGCGGAATGTACC(SEQ ID NO:49)。圖3B包含以下的核苷酸序列:A1:ATGGCTCTTGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:50);B1:GTTTCCCAAGAGCCATACAGGGATGCGGAATGTACC(SEQ ID NO:51);A2:GGCTCTTGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:52);B2:GTTTCCCAAGAGCCACAGGGATGCGGAATGTACC(SEQ ID NO:53);A3:CTCTTGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:54);B3:GTTTCCCAAGAGACAGGGATGCGGAATGTACC(SEQ ID NO:55);A4:TCTTGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:56);B4:GTTTCCCAAGAACAGGGATGCGGAATGTACC(SEQ ID NO:57);A5:CTTGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:58);B5:GTTTCCCAAGACAGGGATGCGGAATGTACC(SEQ ID NO:59);A6:TTGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:60);B6:GTTTCCCAAACAGGGATGCGGAATGTACC(SEQ ID NO:61);A7:TGGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:62);B7:GTTTCCCAACAGGGATGCGGAATGTACC(SEQ ID NO:63);A8:GGGAAACTGCCTGAAACCGTACCAACC(SEQ ID NO:64);以及B8:GTTTCCCACAGGGATGCGGAATGTACC(SEQ ID NO:65)。
圖3C和3D為示出了根據本文提供的方法進行的反應的結果的圖。
圖4為示出了根據本文提供的方法進行的反應的結果的圖。
圖5為示出了根據本文提供的方法進行的反應的結果的圖。
圖6為示出了根據本文提供的方法進行的反應的結果的圖。
圖7為示出了根據本文提供的方法進行的反應中生成的產物的核苷酸序列的序列比對。圖7包含以下的核苷酸序列(按從比對中的頂部序列到比對中的底部序列的順序):SEQ ID NO:66:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGA;SEQ ID NO:67:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:68:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:69:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:70:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACTGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:71:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:72:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:73:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:74:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGG GAAGACCAAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:75:
TCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAATTCTTGAGAGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:76:
GAACCCACTAACAGTAGAAGTACCATACATTTGTACAGAAGGGGAAGACCAAATGAACCCACTAACAGTAGAAGTACCATACATTT;SEQ ID NO:77:
TCTTGAGAGAACCCACTAACTCTTGAGAGAACCCACTAAC;以及SEQ ID NO:78:GGAAGACCAAATTCTTGAGA。
需要注意的是,附圖和其中的元件不必要按形狀或比例繪制。例如,為便于呈現或使呈現清楚,附圖中元件的形狀或比例可進行簡化或修改。應進一步理解,附圖和其中的元件僅用于示例性說明目的,不應理解為以任何方式進行限制。
具體實施方式
盡管本發明包括各種修改和替代形式,但其具體實施方式通過附圖中的示例示出并將在本文中詳細描述。然而,應理解,并非意在將本發明限于所公開的特定形式,而是相反,本發明覆蓋如由權利要求所限定的本發明的精神和范圍內的所有修改、等同項和替代方案。
在一些實施方式中,本文提供了涉及核酸擴增和多聯體生成的方法和組合物。
在本文提供的方法中,核酸多聯體的生成還增加了該多聯體中的核酸模板/特定核酸的拷貝數。因此,本文中對用于生成多聯體的方法和組合物的提及還適用于核酸的擴增。
如本文所用的,“多核苷酸”指的是含有兩個或更多個核苷酸的聚合鏈。“多核苷酸”包括引物、寡核苷酸、核酸鏈等。多核苷酸可含有標準或非標準核苷酸。通常,多核苷酸在鏈的一個末端(“5’末端”)含有5’磷酸并在鏈的另一末端(“3’末端”)含有3’羥基基團。多核苷酸的最5’核苷酸在本文中可被稱為多核苷酸的“5’末端核苷酸”。多核苷酸的最3’核苷酸在本文中可被稱為多核苷酸的“3’末端核苷酸”。
在含有5’末端核苷酸和3’末端核苷酸的多核苷酸的上下文中如本文所用的術語“下游”指的是比多核苷酸中的參考位置更接近3’末端核苷酸的該多核苷酸中的位置。例如,在具有序列5’ATAAGC 3’的引物中,“G”在“T”和全部“A”的下游。
在含有5’末端核苷酸和3’末端核苷酸的多核苷酸的上下文中,如本文所用的術語“上游”指的是比多核苷酸中的參考位置更接近5’末端核苷酸的該多核苷酸中的位置。例如,在具有序列5’ATAAGC 3’的引物中,“T”在“G”、“C”以及最接近“G”的兩個“A”的上游。
如本文所用的,“核酸”包括DNA和RNA兩者,包括含有非標準核苷酸的DNA和RNA。“核酸”含有至少一個多核苷酸(“核酸鏈”)。核酸可以是單鏈或雙鏈的。
如本文所用的,“多聯體”指的是在其內含有特定核酸的兩個或更多個拷貝的核酸分子,其中這些拷貝串聯連接。在該多聯體內,特定核酸的拷貝可彼此直接連接,或者它們可間接地連接(例如,在特定核酸的拷貝之間可具有核苷酸)。在一個實例中,該特定核酸可以是雙鏈核酸模板的核酸,以使得多聯體可含有該雙鏈核酸模板的兩個或更多個拷貝。在另一個實例中,該特定核酸可以是多核苷酸模板的核酸,以使得多聯體可含有該多核苷酸模板的兩個或更多個拷貝。
如本文所用的,“靶”核酸或分子指的是感興趣的核酸。靶核酸/分子可以是任何類型,包括單鏈或雙鏈DNA或RNA(例如,mRNA)。
如本文所用的,“互補”序列指的是這樣的兩個核苷酸序列,這兩個核苷酸序列在彼此反平行對齊時,含有按照標準堿基配對原則(例如,A-T、G-C或A-U)可彼此配對的多個單獨的核苷酸堿基,使得含有該序列的分子可彼此特異性地退火。對于被認為“互補”的序列,不必要兩個序列中的每一個核苷酸堿基均能夠彼此配對。例如,如果當兩個序列對于互補而最佳對齊時,該兩個序列中至少30%、40%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、98%、99%或100%的核苷酸堿基可彼此配對,則該序列可被認為是互補的。此外,當兩個序列的總長度彼此明顯不同時,該序列仍可被認為“互補”。例如,如果當15個核苷酸的引物與含有數百個核苷酸的更長的多核苷酸的特定區域反向平行對齊時,該引物的多個單獨的核苷酸堿基可與更長的多核苷酸中的核苷酸堿基配對,則該15個核苷酸的引物可被認為與該含有數百個核苷酸的更長的多核苷酸“互補”。此外,“互補”序列可含有一種或多種核苷酸類似物或核堿基類似物。
如本文所用的,當應用于蛋白質、核酸或其他生物分子時,術語“分離的”指的是已從其天然存在的環境的組分中純化或分離的分子(例如,從其天然產生的細胞中純化的蛋白質)。“分離的”分子可與其他分子相接觸(例如,作為反應混合物的一部分)。如本文所用的,“分離的”分子還包括具有天然存在的氨基酸或核苷酸序列的重組產生的蛋白質或核酸。“分離的”核酸包括在細胞中包含的編碼多肽的核酸分子,該細胞通常在例如該核酸分子在與天然細胞不同的染色體位置時表達多肽。在一些實施方式中,“分離的”多肽被純化為至少50%、60%、70%、80%、90%、95%、98%或100%的同質性,如通過多肽的SDS-PAGE以及隨后的考馬斯藍、銀或其他蛋白質染色方法所顯示的。
除非上下文中另外明確指出,如本文所用的,描述為含有模板或其他核酸的“序列”的核酸分子也可被認為含有該模板或其他核酸本身(例如,被描述為含有模板的序列的分子也可以被描述為含有該模板)。
如本文所用的,當第一多核苷酸被描述為與第二多核苷酸“退火”等時,第一多核苷酸全部或其任何部分可與第二多核苷酸退火,反之亦然。
如本文所用的,提及在某一條件下或采用其他對象等“處理”給定對象指的是直接或間接地將給定對象暴露于所提及的條件或其他對象。因此,盡管“處理”步驟可包括不同的相關操作(例如,將酶加入到容器中,振動容器等),但并非每一個“處理”步驟都需要不同的相關操作。例如,包括一種或多種試劑的反應可設置在容器中,并且一旦反應已經開始,則多個事件或步驟可以在容器中發生而不進一步人為或機械干預容器中的內容物。在容器中進行的這些多個事件或步驟中的一個或多個可以被描述為“處理”容器中的對象,即使在反應開始后不單獨地干預容器中的內容物。
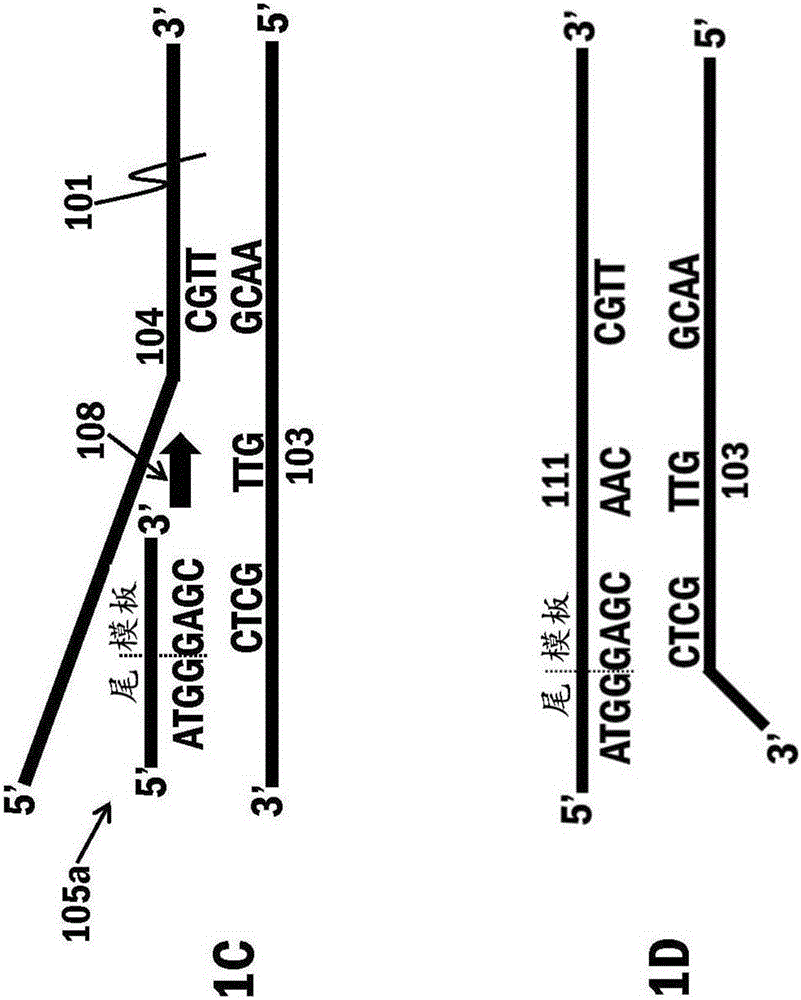
可參考圖1對本文提供的方法和組合物的實施方式進行描述。可提供一級核酸101(圖1A)。一級核酸101可含有核酸模板102的序列。核酸模板102可以是含有第一鏈103和第二鏈104的雙鏈核酸。在圖1中,雙鏈核酸模板的第一鏈103具有5’至3’方向的示例性核苷酸序列AACGGTTGCTC(SEQ ID NO:1)。第一鏈103還包含5’末端核苷酸(最5’的A)和3’末端核苷酸(最3’的C)。第二鏈104具有5’至3’方向的示例性核苷酸序列GAGCAACCGTT(SEQ ID NO:2)。第二鏈104還包含5’末端核苷酸(最5’的G)和3’末端核苷酸(最3’的T)。
還可提供第一引物105和第二引物106(圖1B)。在圖1中,第一引物105具有5’至3’方向的示例性核苷酸序列ATGGGAGC(SEQ ID NO:3)。第一引物還包含5’末端核苷酸(最5’的A)和3’末端核苷酸(最3’的C)。第二引物106具有5’至3’方向的示例性核苷酸序列CCATAACG(SEQ ID NO:4)。第二引物還包含5’末端核苷酸(最5’的C)和3’末端核苷酸(最3’的G)。雖然圖1的核酸模板102是11個核苷酸的長度并具有示例性核苷酸序列,但這些是示例性的,并不被認為是限制。
第一引物105可包含兩個區域:i)尾區以及ii)模板結合區(“模板”區)。第一引物105的尾區可包含三個部分:a)引物的5’末端核苷酸,b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,以及c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸。在圖1中,第一引物105的尾區具有5’至3’方向的示例性核苷酸序列:ATGG,在該序列中,引物的5’末端核苷酸為A,中間部分為中間的TG,且最內核苷酸為最3’的G。第一引物105的模板結合區可包含三個部分:a)引物的3’末端核苷酸,b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,以及c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸。在圖1中,第一引物105的模板結合區具有5’至3’方向的示例性核苷酸序列:GAGC,在該序列中,引物的3’末端核苷酸為C,中間部分為中間的AG,且最內核苷酸為最5’的G。
第二引物106可包含兩個區域:i)尾區以及ii)模板結合區。第一引物106的尾區可包含三個部分:a)引物的5’末端核苷酸,b)最內核苷酸,其中該最內核苷酸在5’末端核苷酸的下游,以及c)5’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸。在圖1中,第二引物106的尾區具有5’至3’方向的示例性核苷酸序列:CCAT,在該序列中,引物的5’末端核苷酸為最5’的C,中間部分為中間的CA,且最內核苷酸為T。第二引物106的模板結合區可包含三個部分:a)引物的3’末端核苷酸,b)最內核苷酸,其中該最內核苷酸在3’末端核苷酸的上游,以及c)3’末端核苷酸與最內核苷酸之間的中間部分,該中間部分包含一個或多個核苷酸。在圖1中,第二引物106的模板結合區具有5’至3’方向的示例性核苷酸序列:AACG,在該序列中,引物的3’末端核苷酸為G,中間部分為中間的AC,且最內核苷酸為最5’的A。
在一些實施方式中,如果將引物的序列對齊使得第二引物的5’末端核苷酸與第一引物的尾區的最內核苷酸對齊并且第一引物的5’末端核苷酸與第二引物的尾區的最內核苷酸對齊,則第二引物的尾區可含有與第一引物的尾區的核苷酸序列互補的核苷酸序列。例如,在圖1中,第二引物106的尾區具有5’至3’方向的核苷酸序列CCAT,并且第一引物105的尾區具有5’至3’方向的核苷酸序列ATGG。當第二引物的5’末端核苷酸(C)與第一引物的尾區的最內核苷酸(G)對齊并且第一引物的5’末端核苷酸(A)與第二引物的尾區的最內核苷酸(T)對齊107時,這些序列是互補的(圖1B)。
應注意,雖然第二引物的尾區可含有與第一引物的尾區的核苷酸序列互補的核苷酸序列,但通常由第一引物與第二引物退火而形成的產物對于本文提供的方法或組合物不是期望的或有用的。因此,在一些實施方式中,可以采取步驟來最小化第一引物-第二引物退火產物的形成。這樣的步驟可包括,例如,在開始本文提供的方法之前不在引物可相互作用持續延長的時間段的條件下對第一引物和第二引物進行預溫育。
可在使得第一引物的第一拷貝105a的模板結合區與核酸模板的第一鏈103退火(圖1C)并且形成第一引物的第一拷貝的延伸產物111(圖1D)的條件下,用第一引物的第一拷貝105a和聚合酶108處理一級核酸101。聚合酶108可催化第一引物的第一拷貝的延伸產物111的形成。該聚合酶可具有鏈置換活性。在合成第一引物的第一拷貝的延伸產物111的過程中,聚合酶可從核酸模板的第一鏈103置換核酸模板的第二鏈104。通常,由第一引物的第一拷貝105a的3’端生成延伸產物。在生成第一引物的第一拷貝的延伸產物111的過程中,第一引物的第一拷貝105a可與合成的延伸產物共價連接,使得第一引物的第一拷貝變為本文描述為“第一引物的第一拷貝的延伸產物”的分子的一部分。第一引物的第一拷貝的延伸產物111與核酸模板的第一鏈103互補。在一些實施方式中,當第一引物的第一拷貝105a與核酸模板的第一鏈103退火時,模板結合區而非第一引物的第一拷貝105a的尾區與核酸模板的第一鏈退火。
在一些實施方式中,使得第一引物的第一拷貝105a的模板結合區與核酸模板的第一鏈103退火并形成第一引物的第一拷貝的延伸產物111的條件可包括足以支持基于聚合酶的核酸合成的任何條件。針對基于聚合酶的核酸合成的示例性條件是本領域已知的并提供于例如,Molecular Cloning:A Laboratory Manual,M.R.Green and J.Sambrook,Cold Spring Harbor Laboratory Press(2012)中,該文獻通過引用全文并入本文。在實施方式中,第一引物或第二引物的模板結合區可支持由核酸聚合酶進行的引物的模板依賴性延伸,這可從引物的3’端延伸引物。
可在使得第二引物106的模板結合區與第一引物的第一拷貝的延伸產物111退火(圖1E)并形成第二引物的延伸產物112(圖1F)的條件下,用第二引物106和聚合酶108處理第一引物的第一拷貝的延伸產物111。聚合酶108可催化第二引物106的延伸產物的形成。該聚合酶可具有鏈置換活性。聚合酶可以是與用于生成第一引物的第一拷貝的延伸產物111的聚合酶相同類型的聚合酶,或者它可以是不同類型的聚合酶。在合成第二引物的延伸產物112的過程中,聚合酶可從第一引物的第一拷貝的延伸產物111置換核酸模板的第一鏈103。通常,由第二引物106的3’端生成延伸產物。在生成第二引物的延伸產物112的過程中,第二引物106可與合成的延伸產物共價連接,使得第二引物變為本文描述為“第二引物的延伸產物”的分子的一部分。第二引物的延伸產物112與第一引物的第一拷貝的延伸產物111互補。在一些實施方式中,當第二引物106與第一引物的第一拷貝的延伸產物111退火時,模板結合區而非第二引物106的尾區與第一引物的第一拷貝的延伸產物111退火。第二引物的延伸產物112含有5’末端核苷酸、3’末端核苷酸以及3’末端區。3’末端區的最后的核苷酸(T)是第二引物的延伸產物的3’末端核苷酸(T),并且該3’末端區含有與在5’至3’方向讀取的第二引物的尾區的核苷酸序列(CCAT)相同的核苷酸序列。
在一些實施方式中,使得第二引物106的模板結合區與第一引物的第一拷貝的延伸產物111退火并形成第二引物的延伸產物112的條件可包括足以支持基于聚合酶的核酸合成的任何條件,包括本文其他地方討論的任何條件。該條件可與用于生成第一引物的第一拷貝的延伸產物111的條件相同,或者它們可以是不同的條件。
可在使得第一引物的第二拷貝105b的模板結合區與第二引物的延伸產物112退火(圖1G)并形成第一引物的第二拷貝的延伸產物113(圖1H)的條件下,用第一引物的第二拷貝105b和聚合酶108處理第二引物的延伸產物112。聚合酶108可催化第一引物的第二拷貝的延伸產物113的形成。該聚合酶可具有鏈置換活性。聚合酶可以是與用于生成第一引物的第一拷貝的延伸產物111或第二引物的延伸產物112的聚合酶相同類型的聚合酶,或者它可以是不同類型的聚合酶。在合成第一引物的第二拷貝的延伸產物113的過程中,聚合酶可從第二引物的延伸產物112置換第一引物的第一拷貝的延伸產物111。通常,由第一引物的第二拷貝105b的3’端生成延伸產物。在生成第一引物的第二拷貝的延伸產物113的過程中,第一引物的第二拷貝105b可與合成的延伸產物共價連接,使得第一引物的第二拷貝變為本文描述為“第一引物的第二拷貝的延伸產物”的分子的一部分。第一引物的第二拷貝的延伸產物113與第二引物的延伸產物112互補。在一些實施方式中,當第一引物的第二拷貝105b與第二引物的延伸產物112退火時,第一引物的第二拷貝105b的模板結合區和尾區均與第二引物的延伸產物112退火。第一引物的第二拷貝的延伸產物113含有5’末端核苷酸、3’末端核苷酸以及3’末端區。3’末端區的最后的核苷酸(G)是第二引物的延伸產物的3’末端核苷酸(G),并且該3’末端區含有與在5’至3’方向讀取的第一引物的尾區的核苷酸序列(ATGG)相同的核苷酸序列。
在一些實施方式中,使得第一引物的第二拷貝105b的模板結合區與第二引物的延伸產物112退火并形成第一引物的第二拷貝的延伸產物113的條件可包括足以支持基于聚合酶的核酸合成的任何條件,包括本文其他地方討論的任何條件。該條件可與用于生成第一引物的第一拷貝的延伸產物111或第二引物的延伸產物112的條件相同,或者它們可以是不同的條件。
第一引物的第二拷貝的延伸產物113的生成可導致生成包含第一引物的第二拷貝的延伸產物113和第二引物的延伸產物112的分子,該分子在本文中可被稱為“二級核酸”115。在二級核酸115內,第一引物的第二拷貝的延伸產物113可與第二引物的延伸產物112退火。此外,二級核酸115含有核酸模板102的序列。該二級核酸115具有比單獨核酸模板102長的核苷酸長度,因為除核酸模板102的序列之外,它還可包含第一引物和第二引物的尾區的序列及其互補序列。具體而言,二級核酸115可具有第一端區域116和第二端區域117。第一端區域116可包含第二引物的延伸產物112的3’末端區及其互補序列。第二端區域117可包含第一引物的第二拷貝的延伸產物113的3’末端區及其互補序列。
可形成或提供二級核酸115的第一拷貝115a和第二拷貝115b(圖1I)。二級核酸115的第一拷貝115a和第二拷貝115b可采用通過其可生成具有二級核酸115的通用結構的核酸的任何方法生成,包括本文其他地方討論的任何方法。例如,如上文所述的用于由一級核酸101生成二級核酸115的全部過程可重復兩次,以便生成該二級核酸的第一拷貝115a和第二拷貝115b。在另一個實例中,二級核酸的第一拷貝115a和第二拷貝115b可由第一引物的第一拷貝的延伸產物111的單一拷貝生成。在這一實例中,第二引物的延伸產物的兩個拷貝112a、112b可由第一引物的第一拷貝的延伸產物111的單一拷貝生成,這在從第一引物的第一拷貝的延伸產物111的單一拷貝置換第二引物的延伸產物的第一拷貝112a時,可能發生,從而允許由第一引物的第一拷貝的延伸產物111的單一拷貝生成第二引物的延伸產物的第二拷貝112b。然后,例如,第一引物的第二拷貝的延伸產物113a、113b可分別由第二引物的延伸產物的各個拷貝112a、112b生成。也可進行用于生成二級核酸的第一拷貝115a和第二拷貝115b的另外的程序并將該程序與本文提供的方法一起使用。
可在使得二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物113a的3’末端區與二級核酸的第二拷貝的第二引物的延伸產物112b的3’末端區退火的條件下,處理二級核酸的第一拷貝115a和第二拷貝115b,以產生包含這些鏈的交換結構118(圖1J)(為簡單起見,未示出鏈113b和112a)。可在使得形成兩個組分鏈112b、113a的延伸產物(該延伸產物在本文中可分別稱為“第一多聯體鏈”121和“第二多聯體鏈”122)的條件下,用聚合酶進一步處理交換結構118。第一多聯體鏈121和第二多聯體鏈122可退火在一起并可共同被稱為多聯體120(圖1K)。多聯體120可含有核酸模板102的兩個或更多個拷貝。在多聯體120內,核酸模板102的兩個或更多個拷貝中的一些或全部可通過第一引物105和第二引物106的尾區的序列彼此分隔開,其中尾區的序列彼此退火。例如,在圖1K的多聯體120中,雙鏈核酸模板的第一鏈的第一拷貝通過5’-3’順序的序列CCAT與雙鏈核酸模板的第一鏈的第二拷貝分隔開。CCAT還是第二引物106的尾區的5’-3’順序的序列。類似地,在圖1K的多聯體120中,雙鏈核酸模板的第二鏈的第一拷貝通過5’-3’順序的序列ATGG與雙鏈核酸模板的第二鏈的第二拷貝分隔開。ATGG還是第一引物105的尾區的5’-3’順序的序列。在多聯體內,第一多聯體鏈的CCAT與第二多聯體鏈的ATGG退火。
在一些實施方式中,使得形成交換結構118或交換結構的鏈的延伸產物的條件可包括足以支持基于聚合酶的核酸合成的任何條件,包括本文其他地方討論的任何條件。該條件可與如用于生成第一引物的第一拷貝的延伸產物111、第二引物的延伸產物112或第一引物的第二拷貝的延伸產物111的條件相同,或者它們可以是不同的條件。
在一些實施方式中,本文提供的多聯體可根據圖1I-1K中的總體概述的過程進一步增加長度。例如,可處理如圖1K所示的多聯體分子120中的兩個,使得它們形成與圖1J中所示的結構相似的交換結構(除了具有更長的鏈),隨后生成包含核酸模板102的四個拷貝的更大的多聯體分子。在另一實例中,二級核酸115和多聯體120可形成交換結構,隨后生成含有核酸模板102的三個拷貝的更大的多聯體分子。在一些實施方式中,在本文提供的方法中,可同時生成多個不同長度的多個不同的多聯體。
在實施方式中,可參考圖8對本文提供的方法和組合物進行描述。多核苷酸模板800(圖8A)可以是用于擴增的靶標。多核苷酸模板800是單一核苷酸鏈。該多核苷酸模板鏈可作為游離的單鏈分子存在,或者它可作為雙鏈分子的一部分存在,在該雙鏈分子中該多核苷酸模板鏈與其互補鏈退火。多核苷酸模板800可以是DNA或RNA。
多核苷酸模板800可含有至少第一部分801(也用“(i)”表示)和第二部分802(也用“(ii)”表示)。第一部分801和第二部分802可各自含有任何數目的核苷酸,諸如各自少于1000、500、400、300、200、100、90、80、70、60、50、40、30、20、15、10、9、8、7、6、5、4或3個核苷酸或各自至少1000、500、400、300、200、100、90、80、70、60、50、40、30、20、15、10、9、8、7、6、5、4或3個核苷酸。第一部分801和第二部分802可含有相同或不同數目的核苷酸。在一些實施方式中,除第一部分801和第二部分802之外,多核苷酸模板800還可含有其他部分。在其他實施方式中,第一部分801和第二部分802可構成多核苷酸模板800的全部。多核苷酸模板800可具有本文其他地方所述的核酸模板的長度。多核苷酸模板800可以是一級核酸的一部分。多核苷酸模板可存在于從受試者獲得的樣品中。
多核苷酸模板800可在含有第一引物810和第二引物820的反應混合物中進行溫育(圖8B)。通常,該反應混合物含有每個引物的多個拷貝,例如,每個引物的至少4、5、6、10、15、20、50、100、1000、10,000、100,000或1百萬個拷貝或更多個拷貝。第一引物810可具有第一區域811(也用“(i)”表示)和第二區域812(也用“(ii)”表示)。第一引物的第一區域811可具有5’端,并且第一引物的第二區域812可具有3’端。第一引物的第一區域可具有與第一引物的第二區域的核苷酸序列不同的核苷酸序列。第二引物820可具有第一區域821(也用“(i)”表示)和第二區域822(也用“(ii)”表示)。第二引物的第一區域821可具有5’端,并且第二引物的第二區域822可具有3’端。第二引物的第一區域可具有與第二引物的第二區域的核苷酸序列不同的核苷酸序列。
第一引物的第二區域812可具有與多核苷酸模板的第一部分801的核苷酸序列互補的核苷酸序列。在圖8中,多核苷酸模板的第一部分801的核苷酸序列由字母A表示,并且第一引物的第二區域812的核苷酸序列由字母A’表示,其中A和A’彼此互補。第二引物的第二區域822可具有與配偶體核苷酸序列830互補的核苷酸序列,其中配偶體核苷酸序列830與多核苷酸模板的第二部分802的核苷酸序列互補。在圖8中,多核苷酸模板的第二部分802的核苷酸序列由字母B表示,配偶體核苷酸序列830的核苷酸序列由字母B’表示,并且第二引物的第二區域822的核苷酸序列由字母B表示,其中B和B’彼此互補。換言之,如圖8所示,多核苷酸模板的第二部分802的核苷酸序列(B)可與第二引物的第二區域822的核苷酸序列(B)相同。通過采用本文提供的組合物和方法,可生成配偶體核苷酸序列830,例如,作為來自第一引物的3’端的延伸產物的一部分。在實施方式中,第一引物的第一區域811可與第二引物的第一區域821互補。在圖8中,第一引物的第一區域的核苷酸序列由字母C表示,并且第二引物的第一區域的核苷酸序列由字母C’表示,其中C和C’彼此互補。
在實施方式中,圖8的第一引物和第二引物可分別具有本文其他地方所述的第一引物和第二引物的任何特征(例如,如圖1中的)。而且,在實施方式中,圖8的第一引物的第一區域可具有本文其他地方所述的第一引物的尾區的任何特征。在實施方式中,圖8的第一引物的第二區域可具有本文其他地方所述的第一引物的模板結合區的任何特征。在實施方式中,圖8的第二引物的第一區域可具有本文其他地方所述的第二引物的尾區的任何特征。在實施方式中,圖8的第二引物的第二區域可具有本文其他地方所述的第二引物的模板結合區的任何特征。
在實施方式中,含有多核苷酸模板800和第一引物810的至少兩個拷貝以及第二引物820的至少兩個拷貝的反應混合物可含有一個或多個可支持如本文其他地方所述的基于聚合酶的核酸合成的其他組分(例如,聚合酶、核苷酸、緩沖液、水等)。相似地,含有多核苷酸模板800和第一引物810的至少兩個拷貝以及第二引物820的至少兩個拷貝的反應混合物可在本文其他地方所述的用于支持核酸模板的擴增或多聯體的生成的任何反應條件下進行溫育。
在實施方式中,在如本文所述在反應混合物中溫育多核苷酸模板800和第一引物810的至少兩個拷貝以及第二引物820的至少兩個拷貝時,可形成一個或多個多聯體鏈(圖8C)。在實施方式中,形成的多聯體鏈840可具有5’和3’端,并可具有含有5’至3’方向的通用結構C’-T-C’-T-X-C’的序列,其中C’是第二引物的第一區域的核苷酸序列,T是多核苷酸模板的序列或其類似序列,并且X是任何數目和序列的核苷酸。因此,如由多聯體鏈的通用結構所示的,多聯體鏈可含有多核苷酸模板的序列或其類似序列的至少兩個拷貝,其中多核苷酸模板的序列的拷貝由至少第二引物的第一區域的序列分隔開。在實施方式中,T可以是多核苷酸模板的類似序列。如本文所用的,多核苷酸模板的“類似序列”指的是含有作為多核苷酸模板的相似序列,而非含有多核苷酸模板中的核苷酸的一個或多個相似的核苷酸的序列。因此,例如,如果多核苷酸模板含有RNA序列,則其類似序列可以是相同序列的DNA形式(即,RNA序列中的尿嘧啶在類似的DNA序列中是胸腺嘧啶),或反之亦然。繼續該實例,如果多核苷酸模板含有5’UACCUG 3’的RNA序列,則類似的序列是5’TACCTG 3’的DNA序列。
在實施方式中,在含有5’至3’方向的通用結構C’-T-C’-T-X-C’的序列中,X是零個核苷酸(即,X的任一側上的T和C序列直接連接)。在其他實施方式中,X是少于10,000、5000、4000、3000、2000、1000、500、400、300、200、100、90、80、70、60、50、40、30、20、15、10、9、8、7、6、5、4或3個核苷酸。X中的核苷酸(如果有)可具有任何序列。在實施方式中,X含有具有5’至3’方向的通用結構[(C’-T)N]的序列,其中C’是第二引物的第一區域的核苷酸序列,T是多核苷酸模板的序列或其類似序列,并且N是小于1000、500、200、100、50或10的任何整數,諸如1至500、1至200、1至100、1至50或1至10之間的整數。例如,如果當X含有5’至3’方向的通用結構[(C’-T)N]的序列時“N”是3,則在結構C’-T-C’-T-X-C’的X位置上存在3個連續重復的(C’-T),使得相應的結構可以寫成:C’-T-C’-T–C’-T–C’-T–C’-T-C’,其中,帶下劃線的C’和T是式[(C’-T)3]的C’-T的重復。因此,例如,根據本文提供的組合物和方法,可形成含有多核苷酸模板的數十或數百個拷貝的多聯體鏈。在實施方式中,如圖8所提供的多聯體鏈可具有本文其他地方所述的多聯體鏈的任何特征。而且,在一些實施方式中,在生成多聯體鏈的過程中,在具有通用結構C’-T-C’-T-X-C’的序列中的C’或T的一個或多個位置處,可在C’與T之間插入少量的核苷酸(例如,15個或更少、10個或更少、5個或更少、或3個或更少)。而且,在一些實施方式中,在生成多聯體鏈的過程中,在具有通用結構C’-T-C’-T-X-C’的序列中的C’或T的一個或多個位置處,少量的核苷酸(例如,15個或更少、10個或更少、5個或更少、或3個或更少)可從C’或T序列中缺失。因此,根據本文提供的方法生成的多聯體鏈可包括具有如本文提供的通用結構的鏈,但該鏈可在多聯體鏈的不同序列組分之間的一個或多個接合點(即,模板序列與引物序列/T和C’之間的接合)處添加或去除少量核苷酸。而且,在實施方式中,如本文提供的多聯體鏈可在含有多聯體(該多聯體含有具有通用結構C’-T-C’-T-X-C’的序列)的分子的5’或3’端含有附加的核苷酸(例如,多達3、5、10、20、50、100、500、1000個或更多個附加的核苷酸)。在實施方式中,通用結構C’-T-C’-T-X-C’的C’可具有本文其他地方所述的第二引物的尾區的任何特征(例如,長度、序列)。在實施方式中,通用結構C’-T-C’-T-X-C’的T可具有本文其他地方所述的多核苷酸模板鏈的任何特征(例如,長度、序列)。
在實施方式中,根據本文提供的方法生成的多聯體鏈840可以是單鏈分子的一部分。在其他實施方式中,根據本文提供的方法生成的多聯體鏈840可以是雙鏈多聯體的一部分,在該雙鏈多聯體中多聯體鏈840與互補于多聯體鏈850的鏈退火。雖然圖8C描繪了含有具有5’至3’方向的通用結構C’-T-C’-T-X-C’(鏈840)或C-T’-C-T’-X’-C(鏈850)的序列的多聯體鏈(其中X是0個核苷酸),但根據圖8的示意圖生成的多聯體鏈可具有上文或本文其他地方所述的多聯體鏈的任何特征。而且,關于圖8C,序列A和B是模板鏈的一部分,并且因此不在通用結構C’-T-C’-T-X-C’或C-T’-C-T’-X’-C中單獨用符號表示。
根據本文提供的方法和組合物生成的多聯體可以是任何長度的核苷酸。在一些實施方式中,本文生成的多聯體分子可以是至少30、40、50、60、70、80、90、100、150、200、250、300、400、500、600、700、800、900、1000、1500、2000、3000、4000、5000、6000、7000、8000、9000、10,000、15,000、20,000或25,000個核苷酸的長度。在一些實施方式中,本文生成的多聯體分子可以是不多于30、40、50、60、70、80、90、100、150、200、250、300、400、500、600、700、800、900、1000、1500、2000、3000、4000、5000、6000、7000、8000、9000、10,000、15,000、20,000或25,000個核苷酸的長度。在一些實施方式中,本文生成的多聯體分子可具有選自最小值為30、40、50、60、70、80、90、100、150、200、250、300、400、500、600、700、800、900、1000、1500、2000、3000、4000、5000、6000、7000、8000、9000、10,000、15,000或20,000個核苷酸的長度且最大值為40、50、60、70、80、90、100、150、200、250、300、400、500、600、700、800、900、1000、1500、2000、3000、4000、5000、6000、7000、8000、9000、10,000、15,000、20,000或25,000個核苷酸的長度的范圍的長度。在一些實施方式中,根據本文提供的方法或組合物生成的至少一些多聯體具有上文所述的特征。在一些實施方式中,根據本文提供的方法或組合物生成的至少10%、20%、30%、40%、50%、60%、70%、80%、90%或95%的多聯體具有上文所述的特征。
根據本文提供的方法和組合物生成的多聯體可含有核酸模板或特定核酸的任何數目的拷貝。在一些實施方式中,本文生成的多聯體分子可含有核酸模板或特定核酸的至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、60、70、80、90或100個拷貝。在一些實施方式中,本文生成的多聯體分子可含有核酸模板或特定核酸的不多于2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、60、70、80、90或100個拷貝。在一些實施方式中,本文生成的多聯體分子可具有核酸模板或特定核酸的選自最小值為2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、60、70、80或90個拷貝且最大值為3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、60、70、80、90或100個拷貝的范圍的多個拷貝。在一些實施方式中,根據本文提供的方法或組合物生成的至少一些多聯體具有上文所述的特征。在一些實施方式中,根據本文提供的方法或組合物生成的至少10%、20%、30%、40%、50%、60%、70%、80%、90%或95%的多聯體具有上文所述的特征。
本文提供的方法的過程可以采用多種不同方式進行監測。在實施方式中,可測定反應的核酸擴增產物(例如,產物的量或其生成速率)。在其他實施方式中,可測定反應的聚合酶沿核酸模板的活性(例如,聚合酶沿模板鏈的移動)。因此,在一些實施方式中,由于由方法產生的產物的積累(可能在該方法的步驟期間或完成后)或由于在方法的步驟期間發生的可檢測事件,使得可觀察到本文提供的方法的事件。
可測定擴增的核酸的存在,例如,通過檢測反應產物(擴增的核酸或反應副產物)或通過檢測與反應進展相關的探針。
在一些實施方式中,可通過用染料將產物染色來鑒定反應產物。在一些實施方式中,染料在與核酸結合時比未與核酸結合時可具有更大的熒光。在實施方式中,染料可插入雙鏈核酸或它可與核酸的外部區域結合。可與本文提供的方法和組合物一起使用的核酸染料包括,例如,花青染料、染料、Gold、Green I、Green II、溴化乙錠、二氫乙錠、BlueViewTM、染料、染料、染料、染料、染料、染料、染料、染料、染料、碘化丙啶、碘化己啶(hexidium iodide)、亞甲藍、DAPI、吖啶橙、奎納克林(quinacrine)、吖啶二聚體(acridine dimer)、9-氨基-6-氯-2-甲氧基吖啶、雙苯酰亞胺染料、Hoechst染料、7-氨基放線菌素D、放線菌素D、羥芪巴脒、派洛寧Y(pyronin Y)、DiamondTM染料、GelRedTM、GelGreenTM和LDS 751。
在一些實施方式中,可通過分析擴增反應的濁度來鑒定反應產物。例如,在實施方式中,增加的濁度可能與反應產物和反應副產物(例如,與鎂復合的焦磷酸)的形成相關。
在一些實施方式中,可通過分離根據本文方法通過凝膠電泳進行的反應并隨后用核酸染料將凝膠染色來鑒定反應產物。該染料可以是本文公開的或本領域以其他方式已知的任何核酸染料。
在一些實施方式中,本領域已知的用于檢測核酸或用于生成核酸的任何方法或組合物可與本文提供的方法和組合物一起使用。
在一些實施方式中,含有與核酸模板鏈(或具有相似或相同的序列的鏈)的一部分互補的核苷酸序列和含有熒光報道分子(熒光團)和猝滅劑中的一種或兩種的核酸探針包含在本文提供的反應中。
在實例中,核酸探針可含有在其5’或3’末端的熒光報道分子,以及在另一末端的猝滅劑。該探針可進一步具有含有按順序的至少第一、第二和第三區域的核苷酸序列,在該核苷酸序列中第一和第三區域彼此互補,并且第二區域的至少一部分與核酸模板鏈(探針“檢測序列”)的一部分互補。在一些實施方式中,第二區域的長度可大于第一或第三區域的長度。在一些實施方式中,第二區域的長度可為10至40個核苷酸,并且第一和第三區域的長度可為4至10個核苷酸。該探針可具有至少兩種不同的構型:(A)其中探針不與其檢測序列退火且第一和第三區域彼此退火的構型;該構型可以是“莖-環”結構,在該結構中第一和第三區域形成莖而第二區域形成環,以及(B)其中探針與其檢測序列退火的構型;在該構型中,第二區域或其一部分與其檢測序列退火,并且第一和第三區域彼此不退火。在探針的構型(A)中,熒光報道分子和猝滅劑(它們位于探針的相對末端/第一和第三區域的外端)可彼此緊密靠近(均在通過第一和第三區域退火形成的莖結構的末端處),以使得熒光報道分子被猝滅。在探針的構型(B)中,熒光報道分子和猝滅劑可不彼此緊密靠近,以使得熒光報道分子不被猝滅。探針可用于監測所選反應產物的積累,例如,在探針可形成莖環結構或與其檢測序列退火的反應條件下。在一些實施方式中,如果存在檢測序列,則探針可與檢測序列退火,并且探針可響應于熒光團的激發光譜的波長的光而發熒光。相反,如果不存在檢測序列,則探針可形成莖環結構,并且探針不響應于熒光團的激發光譜的波長的光而發熒光。
在另一實例中,核酸探針可在其5’或3’末端含有熒光報道分子,并且它可與含有猝滅劑的核酸引物退火。含有猝滅劑的核酸引物可在引物的位置上含有猝滅劑,使得當核酸探針與引物退火時,熒光報道分子被猝滅。探針可用于監測所選反應產物的積累,例如,在探針可與引物退火或與其檢測序列(在反應產物中)退火的反應條件下。在一些實施方式中,如果存在檢測序列,則探針可與檢測序列退火,并且探針可響應于熒光團的激發光譜的波長的光而發熒光(由此指示反應產物的存在)。相反,如果不存在檢測序列,則探針可保持與引物配對,并且探針不響應于熒光團的激發光譜的波長的光而發熒光。
在含有熒光報道分子和猝滅劑對的探針中,可選擇熒光報道分子和猝滅劑,以使得猝滅劑可有效地猝滅報道分子。在一些實施方式中,熒光報道分子與猝滅劑配對,其中熒光報道分子的發射最大值類似于猝滅劑的吸收最大值。可用作熒光報道分子的熒光團包括,例如,CAL Fluor Gold、CAL Fluor Orange、Quasar 570、CAL Fluor Red 590、CAL Fluor Red 610、CAL Fluor Red 610、CAL Fluor Red 635、Quasar670(Biosearch Technologies)、VIC、NED(Life Technologies)、Cy3、Cy5、Cy5.5(GE Healthcare Life Sciences)、Oyster 556、Oyster 645(Integrated DNA Technologies)、LCred610、LCred610、LCred640、LCred670、LCred705(Roche Applies Science)、德克薩斯紅(Texas red)、FAM、TET、HEX、JOE、TMR和ROX。可使用的猝滅劑包括,例如,DDQ-I、DDQ-II(Eurogentec)、Eclipse(Epoch Biosciences)、Iowa Black FQ、Iowa Black RQ(Integrated DNA Technologies)、BHQ-1、BHQ-2、BHQ-3(Biosearch Technologies)、QSY-7、QSY-21(分子探針)和Dabcyl。
在一些實施方式中,根據本文提供的方法進行的反應可在含有光源和光學傳感器的裝置中進行監測。在一些情況下,可將反應定位于來自光源的光路上,并且可測量由樣品吸收(例如,在混濁的反應的情況下)、由樣品散射(例如,在混濁的反應的情況下)或由樣品發射(例如,在含有熒光分子的反應的情況下)的光。在一些實施方式中,本文提供的方法可在如在2013年2月18日提交的美國專利申請系列號13/769,779中公開的設備或其中的模塊中進行或監測,該專利申請通過引用全文并入本文。
通過使用本文提供的方法,感興趣的核酸模板的特異性擴增產物可在擴增反應開始后例如30秒、1分鐘、3分鐘、5分鐘、10分鐘、15分鐘、20分鐘、30分鐘、45分鐘、60分鐘、90分鐘、120分鐘、180分鐘或240分鐘內進行鑒定。在其他實例中,當生成模板的少至10、50、100、500、1000、5000、10,000、50,000、100,000、500,000或1,000,000個拷貝時,通過使用本文提供的方法可鑒定對于感興趣的核酸模板為陽性的擴增反應。在其他實例中,通過使用本文提供的方法,可鑒定樣品中感興趣的核酸模板的存在,該樣品在該方法開始時含有感興趣的模板的少至1、2、3、4、5、10、15、20、25、30、40、50、100、200、500、1000、5000或10,000個拷貝。
在實施方式中,本文提供的方法可用于測定樣品中的感興趣的靶核酸。在某些實施方式中,可通過包括測定反應中核酸擴增的轉變時間的方法來確定樣品中感興趣的靶核酸的存在或量。轉變時間/轉變點是擴增反應被確定為對核酸模板為陽性的時間或點。轉變時間/轉變點可以通過一個或多個指標來鑒定,例如,反應開始后在反應中已經生成所選量的核酸的時間,當反應的擴增速率由基線期變為指數期時的時間,或者當反應的擴增速率由指數期變為平臺期(plateau phase)時的時間等。在實施方式中,轉變時間/轉變點可以基于反應的熒光或吸光度的變化或基于反應的熒光或吸光度達到所選值來鑒定。在某些實施方式中,樣品中感興趣的靶核酸的存在或量可通過包括比較反應的核酸擴增的轉變時間來確定,該反應相對于以下反應中的一者或兩者具有未知量的感興趣的靶核酸:i)已知缺乏感興趣的靶核酸的反應(即,陰性對照);或ii)已知含有感興趣的靶核酸的反應(即,陽性對照)。在實施方式中,可測量含有感興趣的靶核酸的反應和不含有靶核酸的反應兩者的所選的轉變時間。在實施方式中,樣品中感興趣的靶核酸的存在可基于這樣的方法來確定,該方法包括評價包含可含有或可不含有感興趣的靶核酸的樣品的反應的轉變點與具有感興趣狀態(例如,已知其含有或不含有感興趣的靶核酸)的已知靶核酸的一個或多個反應的轉變時間之間的時間差異。例如,如果根據本文提供的方法的反應的轉變時間比已知不含有感興趣的靶核酸的相應反應早至少3、5、10、15、20、30、40、50、60、90、120或180分鐘,則樣品可被鑒定為含有感興趣的靶核酸。在另一實例中,如果根據本文提供的方法的反應的轉變時間比已知不含有感興趣的靶核酸的相應反應晚不多于3、5、10、15、20、30、40、50、60、90、120或180分鐘,則樣品可被鑒定為含有感興趣的靶核酸。
本文提供的方法可進行任意時間長度。通常,該方法將進行足以監測例如核酸復制速率、聚合酶活性的出現或擴增產物的積累的時間長度。在一些實施方式中,本文提供的方法可進行總計少于10秒、30秒、1分鐘、5分鐘、10分鐘、20分鐘、30分鐘、45分鐘、1小時、2小時、3小時、4小時、6小時、8小時、12小時、16小時或24小時,到該時間時測量核酸復制速率、聚合酶活性的出現或擴增產物的積累。
本文提供的方法可以以各種方式終止。在一個實施方式中,方法的步驟可在濃度降低時或該方法的一個或多個步驟中包含的一種或多種試劑(例如,dNTP)完全消耗時結束。在另一個實施方式中,方法的步驟可在該方法的一個或多個步驟中包含的一種或多種酶(例如,聚合酶)失活時結束。酶可通過各種方式失活。例如,由于影響酶結構的隨機事件,導致酶可隨時間逐漸失去酶活性,或者酶可暴露于加速酶活性失活的條件(例如,高熱量、極端pH等)。
在一些實施方式中,一級核酸可以是單鏈或雙鏈的。單鏈一級核酸在本文也可被稱為“一級多核苷酸”。一級核酸可以是線形或環形的。一級核酸可以包含核酸模板。在一些實施方式中,整個一級核酸可以是核酸模板。在其他實施方式中,一級核酸可以含有不是核酸模板的一部分的一個或多個核苷酸(例如,一級核酸可具有比包含在一級核酸內的核酸模板更長的長度)。在一些實施方式中,一級核酸可含有核酸模板的兩個或更多個拷貝。一級核酸可含有DNA、RNA或其混合物。雙鏈線形一級核酸可具有平端或粘端(“粘端”指的是具有突出鏈的末端,該突出鏈具有一個或多個未配對的核苷酸)。
一級核酸可以是任何長度的核苷酸。例如,一級核酸可以是至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、25、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在另一個實例中,一級核酸可以是2至100,000、5至100,000、10至100,000、15至100,000、20至100,000、25至100,000、30至100,000、50至100,000、70至100,000、100至100,000、200至100,000、2至10,000、5至10,000、10至10,000、15至10,000、20至10,000、25至10,000、30至10,000、50至10,000、70至10,000、100至10,000、200至10,000、2至5,000、5至5,000、10至5,000、15至5,000、20至5,000、25至5,000、30至5,000、50至5,000、70至5,000、100至5,000、200至5,000、2至3,000、5至3,000、10至3,000、15至3,000、20至3,000、25至3,000、30至3,000、50至3,000、70至3,000、100至3,000、200至3,000、2至1,000、5至1,000、10至1,000、15至1,000、20至1,000、25至1,000、30至1,000、50至1,000、70至1,000、100至1,000、200至1,000、2至500、5至500、10至500、15至500、20至500、25至500、30至500、50至500、70至500、100至500或200至500個核苷酸堿基的長度。
在一些實施方式中,核酸模板可以是單鏈或雙鏈的。核酸模板的單鏈在本文可被稱為“多核苷酸模板”。如本文提及的“多核苷酸模板”并不排除與其互補序列結合。換言之,“多核苷酸模板”可以是例如整個單鏈核酸模板,或者它可以是雙鏈核酸模板的一條鏈。核酸模板可以包含在一級核酸分子中。在一些實施方式中,核酸模板可構成整個一級核酸分子。在其他實施方式中,核酸模板可包含在含有不是核酸模板的一部分的一個或多個核苷酸的一級核酸中(例如,核酸模板可具有比含有核酸模板的一級核酸更短的長度)。
核酸模板可以是任何長度的核苷酸。例如,核酸模板可以是至少2、3、4、5、6、7、8、9、10、12、14、16、18、20、25、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在另一個實例中,核酸模板可以是2至100,000、5至100,000、10至100,000、15至100,000、20至100,000、25至100,000、30至100,000、50至100,000、70至100,000、100至100,000、200至100,000、2至10,000、5至10,000、10至10,000、15至10,000、20至10,000、25至10,000、30至10,000、50至10,000、70至10,000、100至10,000、200至10,000、2至5,000、5至5,000、10至5,000、15至5,000、20至5,000、25至5,000、30至5,000、50至5,000、70至5,000、100至5,000、200至5,000、2至3,000、5至3,000、10至3,000、15至3,000、20至3,000、25至3,000、30至3,000、50至3,000、70至3,000、100至3,000、200至3,000、2至1,000、5至1,000、10至1,000、15至1,000、20至1,000、25至1,000、30至1,000、50至1,000、70至1,000、100至1,000、200至1,000、2至500、5至500、10至500、15至500、20至500、25至500、30至500、50至500、70至500、100至500或200至500個核苷酸堿基的長度。
如本文所用的“引物”可以指這樣一種多核苷酸,該多核苷酸i)能夠與原始核酸鏈雜交,并且ii)充當合成新的核酸鏈的起始點,其中新的核酸鏈是引物的延伸產物并與原始鏈互補。引物可在其3’末端具有游離的–OH基團,其可充當延伸產物合成的起點。
引物可含有標準核苷酸[例如,標準DNA脫氧核糖核苷酸(脫氧腺苷單磷酸、脫氧鳥苷單磷酸、胸苷單磷酸、脫氧胞苷單磷酸)或標準RNA核糖核苷酸(腺苷單磷酸、鳥苷單磷酸、尿苷單磷酸、胞苷單磷酸)]、替代性核苷酸(例如,肌苷)、修飾的核苷酸、核苷酸類似物或其組合。例如,寡核苷酸引物可包括肽核酸、嗎啉代寡核苷酸(例如,磷二酰胺嗎啉代寡核苷酸)、鎖定核酸[參見,例如,Kaur,H,等人,Biochemistry 45(23),7347-55(2006)]、乙二醇核酸或蘇糖核酸。引物可具有骨架,包括,例如,磷酸二酯鍵、硫代磷酸酯鍵(用硫替代非橋接O)或肽鍵(作為肽核酸的一部分)。替代性核苷酸、修飾的核苷酸以及核苷酸類似物可在本文中通稱為“非標準核苷酸”。
引物中非標準核苷酸的存在可影響該引物的各種特性。在一些實施方式中,在引物中包含非標準核苷酸可增加或降低引物對其互補序列的熱力學穩定性。例如,具有增加的熱力學穩定性的引物可含有鎖定核酸。具有降低的熱力學穩定性的引物可含有,例如,肌苷(由Auer等人,Nucl.Acids Res.24;5021-5025(1996)描述的)或帶負電荷的化學基團,諸如羧酸。
本文提供的第一引物或第二引物可以是任何長度。第一引物和第二引物可含有相同數目的核苷酸或不同數目的核苷酸。在一些實施方式中,第一或第二引物可以為至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在一些實施方式中,第一或第二引物可以為不多于2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在一些實施方式中,第一或第二引物可具有選自最小值為2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750或1000個核苷酸的長度并且最大值為3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度的范圍的長度。
本文提供的第一引物或第二引物的尾區可以是任何長度。通常,針對于同一模板的第一引物和第二引物的尾區含有相同數目的核苷酸。在一些實施方式中,第一或第二引物的尾區可以為至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在一些實施方式中,第一或第二引物的尾區可以為不多于2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在一些實施方式中,第一或第二引物的尾區可具有選自最小值為2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750或1000個核苷酸的長度并且最大值為3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度的范圍的長度。
本文提供的第一引物或第二引物的模板結合區可以是任何長度。針對于同一模板的第一引物和第二引物的模板結合區可含有相同數目的核苷酸或不同數目的核苷酸。在一些實施方式中,第一或第二引物的模板結合區可以為至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在一些實施方式中,第一或第二引物的模板結合區可以為不多于2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度。在一些實施方式中,第一或第二引物的模板結合區可具有選自最小值為2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750或1000個核苷酸的長度且最大值為3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、60、70、80、90、100、150、200、250、300、350、400、500、750、1000或1500個核苷酸的長度的范圍的長度。
在一些實施方式中,引物可以是任何長度,并含有在用于包括該引物的方法或其步驟的溫度下允許該引物與其互補序列足夠穩定且特異性地退火的任何核苷酸序列。引物所需的確切長度可能依賴于多種因素,包括反應的溫度、引物的化學組成以及包括引物的反應。在一些實施方式中,引物的模板結合區可以是任何長度,并含有在用于包括該引物的方法或其步驟的溫度下允許該引物的模板結合區與其互補序列足夠穩定且特異性地退火的任何核苷酸序列。引物的模板結合區所需的確切長度可能依賴于多種因素,包括反應的溫度、引物的模板結合區的化學組成以及包括引物的反應。與缺乏非標準核苷酸的相應引物的長度相比,在引物中包含一個或多個非標準核苷酸可改變在本文提供的方法中使用的引物的所需長度。例如,如果采用本文提供的方法,期望有具有某一解鏈溫度(“Tm”)的引物,在一些實施方式中,相比于如果引物僅含有標準核苷酸,如果引物含有至少一些非標準核苷酸,具有所選Tm的引物可以具有更短的長度。通常,核苷酸序列的“解鏈溫度”指的是50%的具有核苷酸序列的核酸與其互補序列堿基配對(即在雙鏈分子中),而50%的具有核苷酸序列的核酸是單鏈形式時的溫度。
本文提供的引物可通過任何合適的方法進行制備。例如,引物可化學合成。在另一實例中,天然存在的核酸可進行分離、裂解(例如,采用限制酶)和/或修飾以生成或變為本文所述的引物的一部分。
在一些實施方式中,標記物可附接至引物。標記物包括,例如,結合配體(例如,地高辛或生物素)、酶、熒光分子/熒光團、發光的分子、猝滅劑分子或放射性同位素。在其他實施方式中,可將寡核苷酸的堿基替代為熒光類似物,諸如2-氨基嘌呤(參見,例如,Proc.Acad.Sci.USA,91,6644—6648(1994),該文獻通過引用全文并入本文)。
在一些實施方式中,使得i)第一引物的第一拷貝的模板結合區與核酸模板鏈退火,ii)第二引物的模板結合區與第一引物的第一拷貝的延伸產物退火,iii)第一引物的第二拷貝的模板結合區與第二引物的延伸產物退火,或iv)二級核酸的第一拷貝的第一引物的第二拷貝的延伸產物的3’末端區與二級核酸的第二拷貝的第二引物的延伸產物的3’末端區退火,以產生包含這些鏈的交換結構的條件,可各自包括(即,i)、ii)、iii)或iv)中的任何一個可包括)在使得雙鏈核酸分子的鏈以一定程度“呼吸(breathe)”(即經歷連接堿基對的氫鍵的局部斷裂的短暫時期)的溫度下溫育核酸,該程度足以促進引物或不同的核酸鏈進入雙鏈分子的鏈之間,并足以使引物或不同的核酸鏈與打開的雙鏈核酸分子的一條鏈退火。在一些實施方式中,方法或其步驟可在至少10、15、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、90或95℃的溫度下執行或溫育。在一些實施方式中,方法或其步驟可在不高于10、15、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、90或95℃的溫度下執行或溫育。在一些實施方式中,方法或其步驟可在10、15、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85或90℃至15、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、90或95℃之間的溫度下執行或溫育。
在一些實施方式中,對于本文提供的方法或其步驟,在低于相關潛在配對的核苷酸鏈或其區域(例如,第一引物的模板結合區與核酸模板的第一鏈配對,第二引物的模板結合區與第一引物的第一拷貝的延伸產物配對,第一引物與第二引物的延伸產物配對,第二引物的延伸產物的3’末端區與其互補序列配對,第一引物的第一拷貝的延伸產物的3’末端區與其互補序列配對,等等)的解鏈溫度(Tm)的溫度下執行步驟或方法。在一些實施方式中,對于本文提供的方法或其步驟,在高于相關潛在配對的核苷酸鏈或其區域(例如,第一引物的模板結合區與核酸模板的第一鏈配對,第二引物的模板結合區與第一引物的第一拷貝的延伸產物配對,第一引物與第二引物的延伸產物配對,第二引物的延伸產物的3’末端區與其互補序列配對,第一引物的第一拷貝的延伸產物的3’末端區與其互補序列配對,等等)的Tm的溫度下執行步驟或方法。在一些實施方式中,對于本文提供的方法或其步驟,在處于相關潛在配對的核苷酸鏈或其區域(例如,第一引物的模板結合區與核酸模板的第一鏈配對,第二引物的模板結合區與第一引物的第一拷貝的延伸產物配對,第一引物與第二引物的延伸產物配對,第二引物的延伸產物的3’末端區與其互補序列配對,第一引物的第一拷貝的延伸產物的3’末端區與其互補序列配對,等等)的Tm或在其+/-1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20或25℃或+/-1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20或25℃以內的溫度下執行步驟或方法。
在一些實施方式中,核酸聚合酶包含在本文提供的方法或組合物中。聚合酶可生成引物的延伸產物。引物及其延伸產物可與模板核酸鏈互補。通常,核酸聚合酶將在引物的3’端處引發引物的延伸產物的合成。在一些實施方式中,DNA聚合酶包含在本文提供的方法或組合物中。如本文所用的,“DNA聚合酶”指的是對DNA模板具有主要的或專一的聚合酶活性的核酸聚合酶。在一些實施方式中,逆轉錄酶包含在本文提供的方法或組合物中。如本文所用的,“逆轉錄酶”指的是可從RNA模板合成DNA鏈的核酸聚合酶。在一些實施方式中,RNA聚合酶可包含在本文提供的方法或組合物中。如本文所用的,“RNA聚合酶”指的是可從DNA或RNA模板合成RNA鏈的核酸聚合酶。
在一些實施方式中,本文提供的聚合酶可具有鏈置換活性。具有鏈置換活性的聚合酶包括,例如,exo-Bca DNA聚合酶、phi29DNA聚合酶、大腸桿菌DNA聚合酶I的Klenow片段、VentR DNA聚合酶、Deep VentR DNA聚合酶、9°Nm DNA聚合酶、Bst 2.0DNA聚合酶以及Bst DNA聚合酶的大片段。也可以使用具有鏈置換活性的其他聚合酶。
聚合酶的修飾形式也可以與本文提供的方法和組合物一起使用,條件是修飾的聚合酶具有序列依賴性核酸合成活性。聚合酶的修飾形式(“修飾的聚合酶”)可以具有,例如,100個或更少的、70個或更少的、50個或更少的、40個或更少的、30個或更少的、20個或更少的、10個或更少的、5個或更少的、4個或更少的、3個或更少的、2個或更少的或1個與聚合酶的親代形式的序列不同的氨基酸。在一些實施方式中,修飾的聚合酶可含有比親代聚合酶多或少不多于1000、700、500、400、300、200、100、50、40、30、20、10或5個氨基酸。在一些實施方式中,修飾的聚合酶可含有親代聚合酶的片段。在一些實施方式中,修飾的聚合酶可包含具有來源于聚合酶的一部分和來源于非聚合酶蛋白質的一部分的嵌合多肽。在一些實施方式中,修飾的聚合酶可具有,例如,與親代聚合酶相比提高的催化活性、提高的穩定性或提高的熱穩定性。
在一些實施方式中,本文提供的聚合酶是熱穩定的。熱穩定的聚合酶在高達25、30、35、40、45、50、55、60、65、70、75、80、85、90或95℃的溫度下可具有例如至少5、10、15、20、30、40、50、60、90、120或180分鐘的半衰期。在一些實施方式中,修飾的聚合酶可以是熱穩定的。
在一些實施方式中,本文提供的方法和其步驟包括足以支持基于聚合酶的核酸合成的條件或在該條件下進行。針對基于聚合酶的核酸合成的示例性條件是本領域已知的并提供于例如Green和Sambrook(同上)中。用于基于聚合酶的核酸合成反應的非限制性組分可包括以下的一種或多種:聚合酶(例如,以每50微升反應體積0.01至10個單位的酶,或者其中的任何范圍,包括例如,每50微升反應體積0.01-1、0.1-10、0.1-5、0.5-10、0.5-5、0.5-2、1-10或1-5個單位的酶的濃度,其中1單位的酶在75℃下將使15nmol的dNTP在30分鐘內摻入聚合產物中);模板(以每個反應至少例如1、10、100、1,000、10,000或100,000個拷貝的濃度);引物(以例如0.01至10微摩爾,或者其中的任何范圍,包括例如0.01-1、0.1-10、0.1-5、0.5-5或0.5-2微摩爾的濃度);dNTP(例如dATP、dTTP、dGTP和dCTP,以例如每個dATP、dTTP、dGTP和dCTP 50至500微摩爾,或者其中的任何范圍,包括例如每個dATP、dTTP、dGTP和dCTP 50-350、100-500、100-300、200-500或300-400微摩爾的濃度);鹽(例如KCl或乙酸鉀,以例如1至200毫摩爾,或者其中的任何范圍,包括例如1-100、1-50、1-20、1-10、10-20、10-50或10-200毫摩爾的濃度);緩沖液(例如Tris-HCl或Tris-乙酸鹽(Tris-acetate),pH 7.8-8.5,以例如1至100毫摩爾,或者其中的任何范圍,包括例如1-50、1-20、1-10、1-5、10-100、20-100或50-100毫摩爾的濃度);以及鎂離子(以例如0.1至10毫摩爾,或者其中的任何范圍,包括例如,0.1-5、0.1-1、0.5-10、0.5-5或0.5-2.5毫摩爾的濃度)。用于基于聚合酶的核酸合成反應的另外的非限制性組分可提高反應速度、提高反應的保真度或提高反應中的酶或DNA的穩定性,并且可以包括以下的一種或多種:明膠(以例如0.0001%至0.1%w/v的濃度)、BSA(以例如0.01至1微克每微升的濃度)、蔗糖(以例如0.01摩爾至0.8摩爾的濃度)、海藻糖(以例如0.01摩爾至0.8摩爾的濃度)、DMSO(以例如0.01%至10%v/v的濃度)、甜菜堿(以例如0.1至10摩爾的濃度)、甲酰胺(以例如0.1%至10%v/v的濃度)、甘油(以例如0.1%至20%v/v的濃度)、聚乙二醇(以例如0.1%至20%v/v的濃度)、非離子型去污劑[例如NP-40(以例如0.01%至1%v/v的濃度)]、Tween-20(以例如0.01%至1%v/v的濃度)或Triton X-100(以例如0.01%至1%v/v的濃度)]、銨離子[例如硫酸銨(以例如1至100毫摩爾的濃度)]和EDTA(以例如0.001至0.1毫摩爾的濃度)。其他的試劑也可存在于本文提供的基于聚合酶的核酸合成反應中。例如,可以使用足以合成RNA反應產物或含有非標準核苷酸的反應產物的試劑。足以支持基于聚合酶的核酸合成的條件可包括多個溫度和pH值。例如,基于聚合酶的核酸合成反應的pH可為例如pH 6.0至pH 10.0,諸如pH6.5、7、7.5、7.8、7.9、8、8.1、8.2、8.5、9或9.5。基于聚合酶的核酸合成反應的溫度可以是恒定的或變化的。恒定的溫度可以在例如10℃至95℃之間,諸如20、25、30、35、37、40、42、45、50、55、60、65、70、75、80或85℃。變化的溫度可以是例如10℃至95℃之間的兩個或更多個不同的溫度,諸如選自20、25、30、35、37、40、42、45、50、55、60、65、70、75、80或85℃的兩個或更多個溫度。
本文提供的方法可在多個溫度下進行。在一些實施方式中,方法的所有步驟在相同的溫度下進行。因此,諸如在PCR中的溫度循環在本文公開的方法中是不必要的。在一些實施方式中,本文提供的方法可在兩個或更多個不同的溫度下進行。在一些實施方式中,含有用于本文提供的方法的試劑的反應混合物在兩個或更多個不同的溫度下進行溫育。在一些實例中,可選擇不同的溫度來優化速率、準確度或本文提供的方法的不同步驟的其他特征。例如,可選擇溫度來提高聚合酶的酶活性。在一些實例中,可選擇不同的溫度來提高引物與模板的結合特異性或提高模板對引物的可及性(例如較高的溫度可促進雙鏈體模板核酸的分離)。在一些實施方式中,本文提供的方法的所有步驟在不高于80、70、60、50、40、30、20或10℃的溫度下進行。在一些實施方式中,本文提供的方法在20-60、30-70、40-80、20-40、30-50、40-60、50-70、60-80、30-40、35-45、40-50、45-55、50-60、55-65℃的溫度下進行。在某些實施方式中,含有靶核酸的樣品可在本文提供的方法開始之前加熱至大于40、50、60、70、80、90或95℃的溫度。在某些實施方式中,本文提供的反應混合物可在本文提供的方法開始之前或之后一次加熱至大于40、50、60、70、75、80、85、90或95℃的升高的溫度。將反應混合物加熱至升高的溫度之后,反應混合物可維持在如本文其他地方提供的較低的溫度下(例如,在40-70℃的溫度下)用于進行該方法的其余部分。在實施方式中,如果在本文提供的方法開始之前將反應混合物或樣品加熱至升高的溫度,則可在反應混合物或樣品已經加熱至升高的溫度并且反應混合物或樣品已經回到如本文提供的較低溫度之后,將核酸聚合酶添加至反應混合物或樣品中。本文公開的方法可在有或沒有熱循環儀的情況下進行。
作為一種考慮,可選擇用于本文提供的方法或其步驟的溫度以適合在該方法的步驟中使用的酶。在一些實施方式中,對于使用聚合酶的方法,選擇反應的溫度,使得該溫度不會顯著損害聚合酶的活性(例如,可選擇反應的溫度使得聚合酶具有至少24、12、6、4、3、2、1、0.75、0.5、0.25或0.1小時的半衰期)。或者,可在損害方法中使用的酶的活性的溫度下執行方法(例如,可選擇反應的溫度使得反應中的酶具有不多于24、12、6、4、3、2、1、0.75、0.5、0.25或0.1小時的半衰期)。在一些實施方式中,如果在損害一種或多種酶的活性的溫度或其他條件(例如pH)下執行方法,則可在該方法開始后以一個或多個間隔向反應中加入另外的酶以補充受損的酶的活性。
在一些實施方式中,本文提供的方法的一個或多個步驟在相同的反應容器(例如,管、尖端、器皿等)中發生。在一些實施方式中,方法的所有步驟均在相同的反應容器中發生。
用于本文提供的方法的試劑可在反應開始時一起提供,或者它們可以按順序加入,其中在一個、兩個或更多個步驟之后向反應中添加新的試劑。在一些情況下,可在反應過程期間向反應容器中添加新的試劑(例如,酶、引物),以增加可作用于底物或代替已變得失活的試劑(例如酶)的功能的試劑的量。可在本文提供的方法的反應開始后的一個或多個選定的時間間隔(例如,在反應開始后1、3、5、7、10、15、20、30、45或60分鐘)向反應中添加新的試劑。
在一些實施方式中,本文提供的方法的一個或多個步驟可同時發生。例如,在生成第一引物的第一拷貝的延伸產物的單一拷貝后,可由該第一引物的第一拷貝的延伸產物的單一拷貝按順序生成第二引物的延伸產物的多個拷貝。由于第二引物的延伸產物的拷貝由第一引物的第一拷貝的延伸產物的單一拷貝按順序生成,因此第二引物的延伸產物的單獨的拷貝可以例如,充當用于形成第一引物的第二拷貝的延伸產物的模板,是二級核酸的組分,是交換結構的組分,或者可以是用于形成第二引物/第一多聯體鏈的延伸產物的延伸產物的起始點。在另一實例中,二級核酸的兩個拷貝可在由核酸模板的第一鏈生成第一引物的第一拷貝的延伸產物的同時形成交換結構。在另一實例中,在由核酸模板的第一鏈生成第一引物的第一拷貝的延伸產物的一個拷貝的同時,由第一引物的第一拷貝的延伸產物的不同拷貝生成第二引物的延伸產物。本文提供的其他步驟也可同時發生。此外,在本文提供的包括雙鏈核酸模板的方法和組合物中,核酸模板的任一條鏈可被認為是“第一鏈”,并且本文提供的引物對的任一引物可被認為是“第一引物”。因此,在一些實例中,雙鏈核酸的兩條鏈可以根據本文提供的方法同時用作核酸的“第一鏈”,且引物對的相對引物充當不同的“第一鏈”的“第一引物”。而且,根據本文提供的方法生成的各種結構可任選地進入本文提供的方法的不同途徑。例如,在實施方式中,第一二級核酸可與第二二級核酸配對以形成如本文其他地方所述的交換結構。在其他實施方式中,第一二級核酸可被第一引物侵入,并且第二引物的延伸產物可充當用于生成第一引物的新的延伸產物的模板。為生成第一引物的新的延伸產物,置換作為二級核酸的一部分的第一引物的延伸產物。在另一實例中,在實施方式中,第一多聯體可與另一多聯體配對以形成交換結構。在其他實施方式中,第一多聯體可被第一引物侵入,并且第一多聯體鏈可充當用于生成新的第二多聯體鏈的模板。為生成新的第一多聯體鏈,置換作為多聯體的一部分的第一多聯體鏈。其他類似事件也可在本文提供的方法的過程中發生。
本文提供的反應和組合物可含有第一引物、第二引物、一級核酸、二級核酸、第一引物的第一拷貝的延伸產物、第一引物的第二拷貝的延伸產物、第二引物的延伸產物、交換結構、多聯體等的多個拷貝。因此,本文提供的方法可包括這樣的過程,其中本文提供的多個步驟同時發生,并且這樣的步驟可與相關分子的多個拷貝一起發生。
在一些實施方式中,在本文提供的方法或組合物中提供了兩組或更多組第一和第二引物,其中每一組均含有第一引物和第二引物,并且其中不同的引物組與不同的核酸模板互補。組中的第一和第二引物兩者的模板結合區可與同一雙鏈核酸模板的不同鏈互補。通常,給定組中的第一和第二引物的尾區具有不同于將在同一方法或組合物中使用的其他引物組的第一和第二引物的尾區的非互補序列,使得來自不同引物組的引物尾部不是互補的。這可能是理想的以便防止形成含有來源于不同核酸模板的鏈的雜合交換結構。或者,在兩個或更多個不同的引物組中的第一和第二引物的尾區可具有互補序列,以便形成雜合交換結構和含有來源于不同核酸模板的鏈的多聯體。在本文提供的方法或組合物中包含兩個或更多個引物組可支持在同一反應容器中同時擴增多個不同的核酸模板。這例如對于擴增樣品中感興趣的多個模板或對于測定樣品中多個不同模板的存在可能是有用的。在一些實施方式中,在本文提供的方法中提供了1、2、3、4、5、6、7、8、9、10、15、20、25、30、40、50、60、70、100、200、500組或更多組第一和第二引物,以便擴增1、2、3、4、5、6、7、8、9、10、15、20、25、30、40、50、60、70、100、200、500個或更多個不同的核酸模板或測定該核酸模板的存在。
在一些實施方式中,在本文提供的方法中,可快速擴增核酸模板。例如,在一些實施方式中,在該方法開始后0.1、0.5、1、3、5、10、15、20、30、40、50、60、90、120或180分鐘內核酸模板可擴增至少500倍。在另一實例中,在一些實施方式中,在該方法開始后0.1、0.5、1、3、5、10、15、20、30、40、50、60、90、120或180分鐘內核酸模板可擴增至少10,000倍。在另一實例中,在一些實施方式中,在該方法開始后0.1分鐘、0.5分鐘、1分鐘、3分鐘、5分鐘、10分鐘、15分鐘、20分鐘、30分鐘、40分鐘、50分鐘、60分鐘、90分鐘、2小時、3小時、4小時、6小時、8小時、12小時、16小時或24小時內,核酸模板相對于該方法開始時反應混合物中存在的核酸模板的原始量可擴增至少5、10、25、50、100、250、500、1,000、5,000、10,000、50,000、100,000、500,000或1,000,000倍。在一些實施方式中,當方法開始時,用于該方法的第一步驟的所有試劑均在含有用于該方法的反應混合物的容器中。在一些實施方式中,當方法開始時,用于該方法的所有步驟的所有試劑均在含有用于該方法的反應混合物的容器中。
在一些實施方式中,在本文提供的方法中,核酸模板可以以比線性速率更高的速率進行擴增。在一些實施方式中,在本文提供的方法中,核酸模板可以以指數方式進行擴增。在一些實施方式中,在本文提供的方法中,在該方法開始后每1、2、3、5、10、15、20、25、30、45、60、90、120、180或240分鐘,核酸模板的數目可至少加倍。在一些實施方式中,相對于該方法開始時反應中存在的核酸模板的原始量,核酸模板可擴增至少5、10、25、50、100、250、500、1,000、5,000、10,000、50,000、100,000、500,000、1,000,000或10,000,000倍。
根據本文提供的方法生成的多聯體中核酸模板的多個拷貝的存在可有助于根據本文提供的方法快速擴增核酸模板。特別地,由于核酸模板的鏈的多個拷貝可存在于單一多聯體鏈中,因此將單一聚合酶負載至單一多聯體鏈上可導致隨著聚合酶沿著該多聯體鏈移動而生成核酸模板的鏈的多個拷貝。在一些情況下,核酸聚合酶遇到并負載至核酸鏈上所需的時間可顯著影響擴增反應的總體速度。例如,如果聚合酶在復制反應期間遇到的每個核酸鏈僅含有核酸模板的鏈的單一拷貝,則在生成該模板的鏈的每個拷貝后聚合酶可能需要遇到并負載至新的模板鏈上。相比之下,通過采用多聯體,在聚合酶遇到并負載至多聯體鏈上后,它可合成模板的鏈的多個拷貝而無需使多聯體鏈留下或遇到并負載至另一條鏈上。
在一些實施方式中,本文提供了用于由單鏈或雙鏈RNA模板生成雙鏈DNA多聯體的方法和組合物。除了逆轉錄酶(例如,AMV逆轉錄酶、M-MLV逆轉錄酶、Superscript IITM逆轉錄酶、Superscript IIITM逆轉錄酶或ThermoScriptTM逆轉錄酶)也包含在本文提供的方法中外,可如本文所述執行該方法。第一引物的第一拷貝可與RNA模板退火,并且逆轉錄酶可生成第一引物的第一拷貝的延伸產物,該延伸產物通過逆轉錄的過程形成為DNA鏈。用于RNA的逆轉錄的方法和條件是本領域已知的并公開在例如RNA:A Laboratory Manual,D.Rio等人,Cold Spring Harbor Laboratory Press(2011)中,該文獻通過引用全文并入本文。在通過逆轉錄酶(由RNA鏈)生成第一引物的第一拷貝的延伸產物(為DNA鏈)后,用于生成多聯體的其余步驟可與本文其他地方所述的相同。
在一些實施方式中,本文提供的方法和組合物可包括一個或多個“暴沸(bumping)引物”。暴沸引物可與本文提供的方法和組合物一起使用,以通過例如提高從核酸模板的第一鏈置換核酸模板的第二鏈的速率,提高從第一引物延伸產物置換核酸模板的第一鏈的速率或者提高從第二引物延伸產物置換第一引物延伸產物的速率來例如提高生成反應產物的速率或特異性。如本文所用的“暴沸引物”指的是與在核酸模板的第一鏈或第二鏈上的序列互補的引物,該序列在與第一引物或第二引物的模板結合區結合的相同鏈上的序列的下游。因此,當暴沸引物與同一核酸鏈(第一引物或第二引物與該核酸鏈退火)退火時,暴沸引物的3’末端朝向第一引物或第二引物的5’末端(即,第一引物或第二引物的5’末端核苷酸和尾區)。當與核酸聚合酶一起溫育并在支持生成引物延伸產物的條件下時,暴沸引物的延伸產物可通過該聚合酶由暴沸引物的3’末端形成。由于暴沸引物的3’末端朝向第一引物或第二引物的5’末端,因此隨著暴沸引物的延伸產物的長度增加,它可最終遇到作為延伸產物的第一引物或第二引物的5’末端。聚合酶可隨后從鏈以及第一引物或第二引物的任何延伸產物中置換第一引物或第二引物。因此,暴沸引物可加快本文提供的反應。
在一些實施方式中,本文提供了含有一種或多種酶、引物或本文提供的其他試劑的容器。容器可包含能夠支持或含有液體或固體材料的任何結構,并可包括管、器皿、尖端等。在一些實施方式中,容器壁可允許光穿過壁透射。容器可以是光學透明的。容器可含有,例如,分離的核酸聚合酶、分離的DNA聚合酶、分離的逆轉錄酶、第一引物、第二引物、核酸染料或核酸探針中的任意一種或多種,如本文其他地方所述。可提供容器的任何內容物的任何數目的拷貝(例如,第一拷貝、第二拷貝、第三拷貝等)。容器的內容物可以是流體連通的。在一些實施方式中,容器可進一步含有核酸模板。在一些實施方式中,容器可進一步含有核苷酸、緩沖液、鹽、水或本文提供的用于核酸擴增的其他試劑。在一些實施方式中,容器可含有兩個或更多個引物組,其中每個引物組包含第一引物和第二引物,并且不同的引物組與不同的核酸模板互補。
可將對于本文提供的方法有用的兩種或更多種試劑包裝并作為試劑盒提供。例如,試劑盒可包含以下的任意兩種或更多種:核酸模板、第一引物、第二引物、核酸聚合酶、DNA聚合酶、逆轉錄酶、緩沖液、核酸染料、核酸探針或dNTP,如本文其他地方所述。在試劑盒內,兩種或更多種試劑可包裝于分開的容器或同一容器中。在一些實施方式中,試劑盒可進一步含有核苷酸、緩沖液、鹽、水或本文提供的用于核酸擴增的其他試劑。
在實施方式中,如本文提供的第一引物和第二引物可作為引物組一起提供。引物組可作為單獨的試劑盒或組合物提供,或者該引物組可與用于執行本文提供的方法的一種或多種其他試劑一起提供于試劑盒中。
在一些實施方式中,核酸連接酶可包含在本文提供的方法或組合物中。連接酶催化核苷酸之間(通常在一個核苷酸的5’磷酸與另一個核苷酸的3’羥基基團之間)磷酸二酯鍵的形成。相比于不包含連接酶的反應,本文提供的反應通過在反應中包含連接酶可以以更高的速率擴增靶核酸。連接酶可以例如增加存在于本文提供的反應中的多聯體的大小或數目。
核酸連接酶包括大腸桿菌DNA連接酶、Taq DNA連接酶、T3DNA連接酶、T4DNA連接酶、T7DNA連接酶、AmpligaseTM、T4RNA連接酶1和T4RNA連接酶2。
為催化連接反應,某些連接酶需要ATP(例如T4DNA連接酶)或NAD+(大腸桿菌DNA連接酶)。在一些實施方式中,連接酶可連接具有平端的核酸。在一些實施方式中,連接酶可連接具有粘端的核酸。在一些實施方式中,連接酶可連接具有平端和粘端兩者的核酸。
連接酶的修飾形式也可與本文提供的方法和組合物一起使用,條件是修飾的連接酶具有催化核苷酸之間磷酸二酯鍵的形成的能力。連接酶的修飾形式(“修飾的連接酶”)可以具有例如,100個或更少的、70個或更少的、50個或更少的、40個或更少的、30個或更少的、20個或更少的、10個或更少的、5個或更少的、4個或更少的、3個或更少的、2個或更少的、或1個與天然存在的親代連接酶形式的序列不同的氨基酸。在一些實施方式中,修飾的連接酶可含有比親代連接酶多或少不多于1000、700、500、400、300、200、100、50、40、30、20、10或5個的氨基酸。在一些實施方式中,修飾的連接酶可含有親代連接酶的片段。在一些實施方式中,修飾的連接酶可包含具有來源于連接酶的一部分和來源于非連接酶蛋白質的一部分的嵌合多肽。在一些實施方式中,修飾的連接酶可具有,例如,與親代連接酶相比提高的催化活性、提高的穩定性或提高的熱穩定性。
在一些實施方式中,本文提供的連接酶是熱穩定的。熱穩定的連接酶在高達25、30、35、40、45、50、55、60、65、70、75、80、85、90或95℃的溫度下可具有例如至少5、10、15、20、30、40、50、60、90、120或180分鐘的半衰期。在一些實施方式中,修飾的連接酶可以是熱穩定的。
在一些實施方式中,包含在本文提供的方法和組合物中的連接酶可以是在本文中被稱為“p50-Tth”的修飾的連接酶,其具有氨基酸序列:
MGHHHHHHHHHHSSGHIEGRASADGPYLQILEQPKQRGFRFRYVCEGPSHGGLPGASSEKNKKSYPQVKICNYVGPAKVIVQLVTNGKNIHLHAHSLVGKHCEDGICTVTAGPKDMVVGFANLGILHVTKKKVFETLEARMTEACIRGYNPGLLVHPDLAYLQAEGGGDRQLGDREKELIRQAALQQTKEMDLSVVRLMFTAFLPDSTGSFTRRLEPVVSDAIYDSKAPNASNLKIVRMDRTAGCVTGGEEIYLLCDKVQKDDIQIRFYEEEENGGVWEGFGDFSPTDVHRQFAIVFKTPKYKDINITKPASVFVQLRRKSDLETSEPKPFLYYPEIKDKEEVQRKRQKGSSGTSGGGSGGGMTLEEARKRVNELRDLIRYHNYRYYVLADPEISDAEYDRLLRELKELEERFPELKSPDSPTLQVGARPLEATFRPVRHPTRMYSLDNAFNLDELKAFEERIERALGRKGPFAYTVEHKVDGLSVNLYYEEGVLVYGATRGDGEVGEEVTQNLLTIPTIPRRLKGVPERLEVRGEVYMPIEAFLRLNEELEERGERIFKNPRNAAAGSLRQKDPRITAKRGLRATFYALGLGLEEVEREGVATQFALLHWLKEKGFPVEHGYARAVGAEGVEAVYQDWLKKRRALPFEADGVVVKLDELALWRELGYTARAPRFAIAYKFPAEEKETRLLDVVFQVGRTGRVTPVGILEPVFLEGSEVSRVTLHNESYIEELDIRIGDWVLVHKAGGVIPEVLRVLKERRTGEERPIRWPETCPECGHRLLKEGKVHRCPNPLCPAKRFEAIRHFASRKAMDIQGLGEKLIERLLEKGLVKDVADLYRLRKEDLVGLERMGEKSAQNLLRQIEESKKRGLERLLYALGLPGVGEVLARNLAARFGNMDRLLEASLEELLEVEEVGELTARAILETLKDPAFRDLVRRLKEAGVEMEAKEKGGEALKGLTFVITGELSRPREEVKALLRRLGAKVTDSVSRKTSYLVVGENPGSKLEKARALGVPTLTEEELYRLLEARTGKKAEELV(SEQ ID NO:79)。連接酶p50-Tth在至少60℃的溫度下具有熱穩定的平端連接活性。連接酶p50-Tth是嵌合蛋白,其包括含His10的前導序列、來自人類NF-kappa-B蛋白登錄號NP_003989氨基酸40-366的p50序列(以斜體字表示)、柔性富甘氨酸序列以及來自嗜熱棲熱菌(Thermus Thermophilus)HB8,登錄YP_144363的Tth DNA連接酶序列(用下劃線表示)。在一些實施方式中,p50-Tth連接酶的修飾形式可與本文提供的方法和組合物一起使用(例如具有100個或更少的、70個或更少的、50個或更少的、40個或更少的、30個或更少的、20個或更少的、10個或更少的、5個或更少的、4個或更少的、3個或更少的、2個或更少的、或1個與p50-Tth連接酶不同的氨基酸)。在實施方式中,與本文提供的組合物或方法一起使用的連接酶可以是描述于2013年3月15日提交的美國臨時專利申請號61/802,124或2014年3月15日提交的PCT申請號PCT/US14/30003中的連接酶,這兩個專利申請均通過引用全文并入本文用于所有目的。
本文提供的用于擴增核酸模板/生成含有該模板的至少兩個拷貝的多聯體的各種方法和組合物可實現先前已通過用于等溫的依賴熱循環儀的核酸擴增的其他方法和組合物實現的許多功能。根據本文提供的方法用于擴增的核酸模板在本文也可稱為“靶核酸”等。本文提供的方法和組合物可用于,例如感興趣的核酸的分離和克隆、基因表達分析、核酸的診斷鑒定、新型核酸的合成、核酸探針合成和標記、受試者的法醫學鑒定、受試者的等位基因鑒定、遺傳篩查、核酸測序以及相關的應用。靶核酸分子可以是任何類型,包括單鏈或雙鏈DNA或RNA(例如,mRNA)。靶核酸可以是任何類型或功能(例如,編碼蛋白質的序列、調節序列、內含子等)。靶核酸可以是整個基因或其一部分。
在一些實施方式中,本文提供的方法或組合物可用于檢測樣品中靶核酸的量(包括靶標的存在或不存在),測量在所選時間段內由樣品形成的靶標的擴增產物的量,或確定由樣品生成模板的一定數目的拷貝所必需的時間量。可與本文提供的方法和組合物一起使用的樣品在本文其他地方進行了描述,并且可包括,例如受試者的體液、分泌物或組織。在實施方式中,可在測定中使用樣品之前處理樣品以根據本文提供的方法擴增樣品中的靶核酸。樣品的處理可包括如本文其他地方所述的任何處理步驟,并可包括例如聲處理或化學裂解步驟。
在一些實施方式中,可執行本文提供的方法以在同一反應容器中同時測定至少2、3、4、5、6、7、8、9、10、12、15、20、25、30、35、40、45、50、75、100種或更多種不同的靶核酸。通常,對于每種感興趣的靶核酸,提供了第一引物和第二引物,每一個均與核酸靶標的鏈或其互補序列互補。可通過例如使用對不同靶核酸中的檢測序列具有序列特異性的核酸探針和不同的熒光團,來監測在同一容器中不同靶核酸的擴增。
在一些實施方式中,本文提供的方法或組合物可用于檢測靶核酸中感興趣的特定核苷酸的存在或不存在(例如,在突變或SNP的情況下)。例如,可選擇與靶核酸中包括感興趣的核苷酸或與之相鄰的區域選擇性結合的第一或第二引物。該引物可設計為使得其選擇性地:i)當該區域含有感興趣的核苷酸時與該區域結合,或ii)當該區域含有感興趣的核苷酸時不與該區域結合。可用所選引物來執行如本文所述的方法,并且擴增反應的結果可提供關于靶核酸中感興趣的核苷酸存在或不存在的信息。例如,如果第一引物的模板結合區被設計為具有與包含感興趣的特定核苷酸(例如突變)的靶核酸中的序列互補的核苷酸序列,則用所選引物從樣品中成功擴增靶核酸可表明該樣品含有具有感興趣的特定核苷酸的靶核酸。在一些實施方式中,用于分析靶核酸中感興趣的核苷酸的引物可在該引物的3’末端含有關鍵核苷酸(即對應于靶核酸中感興趣的核苷酸的同一位置的核苷酸)。在這樣的情況下,引物的3’末端核苷酸的退火可能依賴于靶核酸中感興趣的核苷酸的存在。如果引物的3’末端核苷酸不與靶核酸中的核苷酸退火(例如由于核苷酸之間的錯配),則該錯配可顯著影響核酸聚合酶由引物合成延伸產物。因此,在一些實施方式中,具有對應于感興趣的核苷酸的3’末端核苷酸的引物可用于確定靶核酸中特定核苷酸的存在或不存在。在這樣的實施方式中,在一些情況下可選擇在引物的3’末端的關鍵核苷酸與靶核酸中感興趣的核苷酸互補,并且在一些其他情況下可選擇在引物的3’末端的關鍵核苷酸與靶核酸中感興趣的核苷酸不互補。感興趣的核苷酸可代表例如靶核酸的野生型形式、突變體形式或多態性。
本文提供的方法和組合物可用于從可含有核酸的任何樣品中擴增核酸。樣品的實例可包括各種流體樣品。在一些情況下,樣品可以是來自受試者的體液樣品。樣品可包含一個或多個流體組分。在一些情況下,可提供固體或半固體樣品。樣品可包括從受試者采集的組織。樣品可包括受試者的體液、分泌物或組織。樣品可以是生物樣品。該生物樣品可以是體液、分泌物或組織樣品。生物樣品的實例可以包括但不限于,血液、血清、唾液、尿液、胃液和消化液、淚液、糞便、精液、陰道液、來源于腫瘤組織的間質液、眼部液體、汗液、粘液、耳垢、油、腺體分泌物、呼氣、脊髓液、毛發、指甲、皮膚細胞、血漿、鼻拭子或鼻咽洗液、脊髓液、腦脊髓液、組織、咽喉拭子、活檢物、胎盤液、羊水、臍帶血、重點流體(emphatic fluid)、腔液、痰、膿、微生物群、胎糞、母乳或其他排泄物。樣品可以由人或動物提供。樣品可以來自植物、微生物(例如病毒、細菌)或其他生物物質。
在一些實施方式中,本文提供的方法和組合物可在服務點位置(例如受試者的家中或工作地點、食品雜貨店、藥店、診所或學校等)執行或使用。本文提供的方法和組合物可允許快速擴增來自受試者的樣品中的核酸,以便幫助診斷或治療受試者。例如,此處提供的方法和組合物可用于檢測來自受試者的樣品中來自病原體如病毒(例如流感病毒)或細菌(例如鏈球菌屬(streptococcus))的核酸的存在。
本文公開的測定和方法可在用于處理樣品的裝置或系統上執行。本文公開的測定和方法可容易地并入用于處理樣品的裝置或用于處理樣品的系統中并在其中使用,該裝置或系統可以是自動化的測定裝置或者可以是自動化的測定系統。這樣的裝置以及這樣的系統可用于實施本文公開的方法。例如,裝置可用于接收樣品。裝置可用于制備或用于處理樣品。裝置可用于對樣品進行測定。裝置可用于從樣品獲得數據。裝置可用于傳送從樣品中獲得的數據。裝置可用于處理或測定樣品之后處置樣品。
裝置可以是系統的一部分,該系統的組件可以是樣品處理裝置。裝置可以是樣品處理裝置。樣品處理裝置可配置為促進樣品的采集、制備用于臨床檢驗的樣品或執行使用一種或多種試劑的方法,如本文所公開的。樣品處理裝置可配置為從樣品獲得數據。樣品處理裝置可配置為傳送從樣品中獲得的數據。樣品處理裝置可配置為分析來自樣品的數據。樣品處理裝置可配置為與另一裝置或實驗室或附屬于實驗室的個體通信,以分析從樣品中獲得的數據。
樣品處理裝置可配置為放置在受試者體內或受試者上。樣品處理裝置可配置為直接或間接地接納來自受試者的樣品。樣品可以是,例如,血液樣品(例如,由手指針刺或由靜脈穿刺獲得的樣品或動脈血樣品)、尿液樣品、活檢樣品、組織切片、糞便樣品或其他生物樣品;水樣品、土壤樣品、食物樣品、空氣樣品;或其他樣品。血液樣品可以包括,例如,全血、血漿或血清。樣品處理裝置可通過裝置的外殼接收來自受試者的樣品。樣品采集可發生在樣品采集地點或其他地方。可在樣品采集地點向裝置提供樣品。
在一些實施方式中,樣品處理裝置可配置為接收或容納筒匣。在一些實施方式中,樣品處理裝置可包含筒匣。該筒匣可從樣品處理裝置中移除。在一些實施方式中,可向樣品處理裝置的筒匣提供樣品。或者,可向樣品處理裝置的另一部分提供樣品。筒匣和/或裝置可包含可配置為容納樣品的樣品采集單元。
筒匣可包含樣品,并可包含用于在處理或測試樣品中使用的試劑、用于在處理或測試樣品中使用的一次性用品或其他材料。筒匣可包含本文公開的用于執行本文公開的方法的試劑。將筒匣放置在樣品處理裝置上或將筒匣插入樣品處理裝置之后,筒匣的一個或多個組件可與樣品處理裝置的其他組件流體連通。例如,如果樣品在筒匣收集,則樣品可轉移至樣品處理裝置的其他部分。類似地,如果在筒匣上提供了一種或多種試劑,則該試劑可轉移至樣品處理裝置的其他部分,或者樣品處理裝置的其他組件可得到該試劑。在一些實施方式中,筒匣的試劑或組件可保持在筒匣上。在一些實施方式中,不包含需要裝管或需要維護(例如,人工或自動維護)的流體元件。
樣品或試劑可轉移至裝置,諸如樣品處理裝置。樣品或試劑可在裝置內轉移。樣品或試劑的這種轉移可在不提供從筒匣到裝置的連續流體途徑的情況下完成。樣品或試劑的這種轉移可在不提供裝置內的連續流體途徑的情況下完成。在實施方式中,樣品或試劑的這種轉移可以通過樣品處理系統(例如移液管)來完成;例如,樣品、試劑或其等分試樣可被吸入頂端開放的轉移組件,諸如移液管尖端,該轉移組件可以可操作地連接到樣品處理系統,該樣品處理系統將該尖端以及包含在該尖端內的樣品、試劑或其等分試樣一起轉移至樣品處理裝置之上或之內的位置。樣品、試劑或其等分試樣可放置在樣品處理裝置之上或之內的位置。樣品和試劑或多種試劑可使用樣品處理系統以相似的方式進行混合。筒匣的一個或多個組件可以以自動化方式轉移至樣品處理裝置的其他部分,反之亦然。
裝置,諸如樣品處理裝置,可具有流體處理系統。流體處理系統可進行或可幫助進行運輸、稀釋、提取、等分、混合以及對于流體如樣品的其他操作。在一些實施方式中,流體處理系統可包含在裝置外殼內。流體處理系統可允許流體的采集、遞送、處理和/或運輸,干燥試劑的溶解,液體和/或干燥試劑與液體的混合,以及非流體組分、樣品或材料的采集、遞送、處理和/或運輸。該流體可以是樣品、試劑、稀釋液、洗液、染料或可被裝置使用的任何其他流體,并且可以包括但不限于均勻流體、不同的液體、乳液、懸浮液和其他流體。流體處理系統(包括但不限于移液管)還可用于在裝置周圍運輸容器(其中含有或不含有流體)。流體處理系統可分配或抽吸流體。樣品可包含漂浮在流體內的一個或多個微粒或固體物質。
在實施方式中,流體處理系統可包含移液管、移液管尖端、注射器、毛細管或其他組件。流體處理系統可具有含內表面和外表面以及開放端的部分。流體處理系統可包括移液管(其可包含移液管主體和移液管的管嘴)并且可包括移液管尖端。移液管尖端可以從或不可以從移液管管嘴上拆除。在實施方式中,流體處理系統可使用與移液管尖端配對的移液管;移液管尖端可以是一次性的。尖端在與移液管配對時,可形成流體密封。移液管尖端可使用一次、兩次或更多次。在實施方式中,流體處理系統可使用具有或不具有移液管尖端的移液管或相似裝置來抽吸、分配、混合、運輸或以其他方式處理流體。需要時,可從流體處理系統分配流體。在從例如移液管尖端的孔口中分配之前流體可包含在移液管尖端內。在實施方式或情況中,在使用期間,可分配全部流體;在其他實施方式或情況中,在使用期間,可分配尖端內流體的一部分。移液管可選擇性地抽吸流體。移液管可抽吸所選量的流體。移液管可以能夠致動攪拌機構以混合尖端或容器內的流體。移液管可合并尖端或容器,從而產生連續的流動回路以用于包括非液體形式的材料或試劑的混合。移液管尖端還可通過多個流體的同時或順序計量遞送來促進混合,諸如在兩段式底物反應中。
流體處理系統可包括一個或多個流體隔離的或液壓獨立的單元。例如,流體處理系統可包含一個、兩個或更多個移液管尖端。移液管尖端可被配置為接納并限制流體。尖端可以是彼此流體隔離或彼此液壓獨立的。包含在每個尖端內的流體可以與其他尖端內的流體以及與裝置內的其他流體為流體隔離或液壓獨立的。流體隔離或液壓獨立的單元可以是相對于裝置的其他部分和/或彼此可移動的。流體隔離或液壓獨立的單元可以是單獨可移動的。流體處理系統可以包含一個或多個基部或支持體。基部或支持體可支持一個或多個移液管或移液管單元。基部或支持體可將流體處理系統的一個或多個移液管彼此連接。
樣品處理裝置可配置為對從受試者獲得的樣品執行處理步驟或操作。樣品處理可包括樣品制備,包括,例如,樣品稀釋、將樣品分為等分試樣、提取、與試劑接觸、過濾、分離、離心或其他的預備或處理操作或步驟。樣品處理裝置可配置為對樣品執行一個或多個樣品制備操作或步驟。任選地,樣品可制備用于化學反應和/或物理處理步驟。樣品制備操作或步驟可包括以下的一個或多個:離心、分離、過濾、稀釋、富集、純化、沉淀、溫育、移液、運輸、色譜分析、細胞裂解、細胞計數、粉碎、研磨、活化、超聲處理、微柱處理、用磁珠處理、用納米顆粒處理或其他樣品制備操作或步驟。例如,樣品制備可包括將血液分離為血清和/或微粒部分或者將任何其他樣品分離為各個組分的一個或多個步驟。樣品制備可包括稀釋和/或濃縮樣品如血液樣品或其他生物樣品的一個或多個步驟。樣品制備可包括向樣品中加入抗凝劑或其他成分。樣品制備還可包括樣品的純化。在實施方式中,所有的樣品處理、制備或測定操作或步驟均由單一裝置執行。在實施方式中,所有的樣品處理、制備或測定操作或步驟均在單一裝置的外殼內執行。在實施方式中,大多數的樣品處理、制備或測定操作或步驟由單一裝置執行,并且可在單一裝置的外殼內執行。在實施方式中,許多的樣品處理、制備或測定操作或步驟由單一裝置執行,并且可在單一裝置的外殼內執行。在實施方式中,樣品處理、制備或測定操作或步驟可由多于一個裝置執行。
樣品處理裝置可配置為對樣品運行一個或多個測定,并從該樣品獲得數據。樣品處理裝置可執行本文提供的方法以及附加的測定。測定可包括一種或多種物理或化學處理,并可包括運行一個或多個化學或物理反應。樣品處理裝置可配置為對體液的小樣品執行一個、兩個或更多個測定。可在具有一定體積的樣品上進行一個或多個化學反應,如本文其他地方所述。例如,可在具有小于飛升(femtoliter)體積的丸劑中進行一個或多個化學反應。在實例中,樣品采集單元被配置為接收相當于單滴或更少的血液或間質液體積的體液樣品。在實施方式中,樣品的體積可以是小體積,其中小體積可以是小于約1000μL、或小于約500μL、或小于約250μL、或小于約150μL、或小于約100μL、或小于約75μL、或小于約50μL、或小于約40μL、或小于約20μL、或小于約10μL、小于約5μL、小于約1μL、小于約0.5μL、小于約0.1μL的體積或其他的小體積。在實施方式中,對單一樣品執行全部的樣品測定操作或步驟。在實施方式中,所有的樣品測定操作或步驟均由單一裝置執行。在實施方式中,所有的樣品測定操作或步驟均在單一裝置的外殼內執行。在實施方式中,大多數的樣品測定操作或步驟由單一裝置執行,并且可在單一裝置的外殼內執行。在實施方式中,許多的樣品測定操作或步驟由單一裝置執行,并且可在單一裝置的外殼內執行。在實施方式中,樣品處理、制備或測定操作或步驟可由多于一個裝置執行。
樣品處理裝置可配置為對樣品進行多個測定。在一些實施方式中,樣品處理裝置可以配置為執行本文提供的方法以及一個、兩個或更多個附加測定。在實施方式中,樣品處理裝置可配置為對單一樣品進行多個測定。在實施方式中,樣品處理裝置可配置為對單一樣品進行多個測定,其中該樣品是小樣品。例如,小樣品可以具有為小于約1000μL、或小于約500μL、或小于約250μL、或小于約150μL、或小于約100μL、或小于約75μL、或小于約50μL、或小于約40μL、或小于約20μL、或小于約10μL、小于約5μL、小于約1μL、小于約0.5μL、小于約0.1μL的小體積或其他小體積的樣品體積。樣品處理裝置可以能夠對單一樣品進行多重測定。多個測定可同時運行;可按順序運行;或者一些測定可同時運行而其他測定按順序運行。一個或多個對照測定和/或校準物(例如,包括具有用于測定/測試的校準物的對照的配置)也可并入裝置中;對照測定和對校準物的測定可與對樣品進行的測定同時進行,或可在對樣品進行的測定之前或之后進行,或以其任何組合方式進行。在實施方式中,所有的樣品測定操作或步驟均由單一裝置執行。在實施方式中,全部多個樣品測定操作或步驟均在單一裝置的外殼內執行。在實施方式中,多個測定中的大多數的樣品測定操作或步驟由單一裝置執行,并且可在單一裝置的外殼內執行。在實施方式中,多個測定中的許多的樣品測定操作或步驟由單一裝置執行,并且可在單一裝置的外殼內執行。在實施方式中,樣品處理、制備或測定操作或步驟可由多于一個裝置執行。
在實施方式中,全部多個測定可在短的時間段內進行。在實施方式中,這樣的短的時間段包括少于約三小時、或少于約兩小時、或少于約一小時、或少于約40分鐘、或少于約30分鐘、或少于約25分鐘、或少于約20分鐘、或少于約15分鐘、或少于約10分鐘、或少于約5分鐘、或少于約4分鐘、或少于約3分鐘、或少于約2分鐘、或少于約1分鐘或其他短的時間段。
樣品處理裝置可配置為檢測與樣品相關的一種或多種信號。樣品處理裝置可配置為鑒定樣品的一個或多個特性。例如,樣品處理裝置可配置為檢測樣品中一種分析物(例如靶核酸)或多種分析物或疾病狀況的存在或濃度(例如,在體液、分泌物、組織或其他樣品中或通過體液、分泌物、組織或其他樣品)。或者,樣品處理裝置可配置為檢測一種或多種可被分析以檢測樣品中一種或多種分析物(其可以指示疾病狀況)或疾病狀況的存在或濃度的信號。信號可在裝置上或另一位置進行分析。運行臨床檢驗可以包括或可以不包括對收集的數據的任何分析或比較。
可在有或沒有樣品的情況下進行化學反應或其他處理步驟。可由裝置制備或運行的步驟、測試或測定的實例可包括但不限于,免疫測定、核酸測定(例如本文所提供的方法)、基于受體的測定、細胞計數測定、比色測定、酶測定、電泳測定、電化學測定、光譜測定、色譜測定、顯微測定、地形測定(topographic assay)、量熱測定、濁度測定、凝集測定、放射性同位素測定、粘度測定、凝聚測定、凝固時間測定、蛋白質合成測定、組織學測定、培養測定、摩爾滲透壓濃度測定和/或其他類型的測定,離心、分離、過濾、稀釋、富集、純化、沉淀、粉碎、溫育、移液、運輸、細胞裂解或其他樣品制備操作或步驟或其組合。可由裝置制備或運行的步驟、測試或測定可包括成像,包括顯微鏡檢查、細胞計數以及制備或使用圖像的其他技術。可由裝置制備或運行的步驟、測試或測定可進一步包括對樣品的組織學、形態學、運動學、動力學和/或狀態的評估,該評估可包括對細胞的這種評估。
裝置可以能夠在短的時間量內進行所有的機載步驟(例如,由單一裝置執行的步驟或操作)。裝置可以能夠在短的時間量內對單一樣品進行所有的機載步驟。例如,從受試者樣品采集到傳輸數據和/或分析可能花費約3小時或更少、2小時或更少、1小時或更少、50分鐘或更少、45分鐘或更少、40分鐘或更少、30分鐘或更少、20分鐘或更少、15分鐘或更少、10分鐘或更少、5分鐘或更少、4分鐘或更少、3分鐘或更少、2分鐘或更少、或1分鐘或更少的時間。從將樣品接納在裝置內到傳輸數據和/或關于這樣的樣品的裝置分析的時間量可能依賴于對樣品執行的步驟、測試或測定的類型或數目。從將樣品接納在裝置內到傳輸數據和/或關于這樣的樣品的裝置分析的時間量可能花費約3小時或更少、2小時或更少、1小時或更少、50分鐘或更少、45分鐘或更少、40分鐘或更少、30分鐘或更少、20分鐘或更少、15分鐘或更少、10分鐘或更少、5分鐘或更少、4分鐘或更少、3分鐘或更少、2分鐘或更少或1分鐘或更少的時間。
裝置可配置為準備樣品以供處置或配置為在樣品的處理或測定后處置樣品,諸如生物樣品。
在實施方式中,樣品處理裝置可配置為傳送從樣品獲得的數據。在實施方式中,樣品處理裝置可配置為通過網絡進行通信。樣品處理裝置可包括可與網絡接合的通信模塊。樣品處理裝置可經由有線連接或無線地連接至網絡。該網絡可以是局域網(LAN)或廣域網(WAN)諸如因特網。在一些實施方式中,該網絡可以是個人局域網。該網絡可包括云。樣品處理裝置可連接至網絡而無需中間裝置,或者可能需要中間裝置將樣品處理裝置連接至網絡。樣品處理裝置可以通過網絡與另一裝置通信,該另一裝置可以是任何類型的聯網裝置,包括但不限于個人計算機、服務器計算機或膝上型計算機;個人數字助理(PDA),諸如Windows CE裝置;電話,諸如蜂窩電話、智能電話(例如,iPhone、Android、Blackberry等)或位置感知的便攜式電話(例如GPS);漫游裝置,諸如聯網的漫游裝置;無線裝置,諸如無線電子郵件裝置或能夠與計算機網絡無線通信的其他裝置;或可以通過網絡而可能通信并處理電子交易的任何其他類型的網絡裝置。這樣的通信可包括向云計算基礎設施或可被其他裝置訪問的任何其他類型的數據存儲基礎設施提供數據。
樣品處理裝置可以向例如衛生保健專業人員、健康護理專業場所諸如實驗室或其附屬機構提供關于樣品的數據。實驗室、衛生保健專業人員或受試者中的一個或多個可具有能夠接收或訪問由樣品處理裝置提供的數據的網絡裝置。樣品處理裝置可配置為向數據庫提供關于樣品的數據。樣品處理裝置可配置為向電子病歷系統、向實驗室信息系統、向實驗室自動化系統或其他系統或軟件提供關于樣品的數據。樣品處理裝置可以以報告的形式提供數據。
實驗室、裝置或其他實體或軟件可對關于樣品的數據進行實時分析。軟件系統可進行化學分析和/或病理分析,或者這些可分布在實驗室、臨床以及專業或專家人員的組合中。分析可包括樣品的定性和/或定量評估。數據分析可包括隨后的樣品的定性和/或定量評估。任選地,報告可基于原始數據、預處理的數據或分析的數據生成。可制作這樣的報告以便維持從樣品獲得的數據的機密性、關于從中獲得樣品的受試者的身份和其他信息、數據的分析以及其他機密信息。報告和/或數據可傳輸至衛生保健專業人員。可向數據庫、電子病歷系統、向實驗室信息系統、向實驗室自動化系統或其他系統或軟件提供由樣品處理裝置獲得的數據或對這樣的數據的分析或報告。
可使用或可與本文公開的方法、組合物或其他試劑一起使用的試劑、測定、方法、試劑盒、裝置和系統的實例的描述和公開內容可發現于,例如,美國專利8,088,593;美國專利8,380,541;2013年2月18日提交的美國專利申請序列號13/769,798;2013年2月18日提交的美國專利申請序列號13/769,779;2011年9月26日提交的美國專利申請序列號13/244,947;2012年9月25日提交的PCT/US2012/57155;2011年9月26日提交的美國申請序列號13/244,946;2011年9月26日提交的美國專利申請13/244,949;以及2011年9月26日提交的美國申請序列號61/673,245,這些專利和專利申請的公開內容均通過引用全文并入于此。
本申請要求2013年3月15日提交的美國臨時專利申請號61/800,606的權益和優先權,該專利申請的公開內容通過引用全文并入于此用于所有目的。
實施例
提供以下實施例僅僅是為了說明性目的,并非旨在以任何方式限制本發明。
實施例1-用可變尾區長度的引物擴增模板核酸
使用如本文提供的方法擴增靶核酸。準備反應以測定靶核酸T124A1的102核苷酸部分,其是A型流感病毒血凝素(HA3)基因(RNA分子)的464核苷酸部分。在SEQ ID NO:89中提供了T124A1的核苷酸序列。制備第一引物(“P1”)的12個變體和第二引物(“P2”)的12個變體。圖2A中提供了全部引物變體的序列。所有的引物均含有15個核苷酸長度的模板結合區。第一引物的所有變體的模板結合區的序列為:CAAACCGTACCAACC(SEQ ID NO:80)(在5’-3’方向)。第二引物的所有變體的模板結合區的序列為:ATGCGGAATGTACC(SEQ ID NO:81)(在5’-3’方向)。不同的引物變體含有范圍為8至22個核苷酸長度特別是8、9、10、11、12、13、14、15、16、18、20或22個核苷酸長度的尾區。第一引物的尾區具有堿基序列:CGCCGGATGGCTCTTGGGAAAC(SEQ ID NO:82)(在5’-3’方向)。堿基序列為22個核苷酸的長度;第一引物的較短尾區具有相同的序列,從尾區的5’端減去適當數目的核苷酸(例如具有18個核苷酸長度的尾區的引物具有含有與堿基序列減去堿基序列的前4個核苷酸(CGCC)相同的序列的尾區)。第二引物的尾區具有堿基序列:GTTTCCCAAGAGCCATCCGGCG(SEQ ID NO:83)(在5’-3’方向)。堿基序列為22個核苷酸的長度;第一引物的較短尾區具有相同的序列,從尾區的3’端減去適當數目的核苷酸(例如具有18個核苷酸長度的尾區的引物具有含有與堿基序列減去堿基序列的最后4個核苷酸(GGCG)相同的序列的尾區)。
制備150微升的反應混合物,每一個含有:50mM乙酸鉀,20mM Tris-乙酸鹽(pH 7.9),10mM乙酸鎂,1mM DTT,30μg牛血清白蛋白(BSA),0.8M甜菜堿,各為1.4mM的dATP、dTTP、dGTP和dCTP,2uM 59(Life Technologies),0.8單位/μl Bst DNA聚合酶(New England BioLabs),0.016單位/μl AMV逆轉錄酶(New England Biolabs),1單位/μl鼠核糖核酸酶抑制劑(New England Biolabs),0.8μM的第一引物變體,0.8μM的第二引物變體以及每微升100,000個拷貝T124A1模板,并在59℃下在CFX 96Touch儀器(Bio-Rad)中溫育100分鐘。測定的轉變點使用采用CFX Manager軟件(Bio-Rad)的單一閾值方法來確定并示于圖2B中。X軸提供了反應中使用的第一和第二引物的尾區的核苷酸長度,而Y軸提供了測定的轉變時間(以分鐘計)。對于每一個尾區核苷酸長度,示出了兩個相鄰的條:左邊的條是含有模板的反應的轉變時間,而右邊的條是沒有模板的反應[“無模板對照”(“NTC”)]的轉變時間。對于超過90分鐘的轉變時間,不顯示條。如圖2B所示,在這些反應條件下,具有8-15個核苷酸并且尤其是8-11個核苷酸的尾區的引物支持最快的轉變時間。無模板對照反應最后顯示轉變時間;這是由于隨著時間的推移形成了背景非特異性產物。
實施例2-用可變尾區長度和可變模板結合區長度的引物擴增模板核酸
使用如本文提供的方法擴增靶核酸。準備反應以測定靶核酸T124A1,該靶核酸T124A1在上文實施例1中進行了描述。制備兩個不同組的第一引物和第二引物對組。在第一組的引物對中,每一個引物均具有20個核苷酸長度的模板結合區(“20核苷酸模板結合區”組)。在第二組的引物對中,每一個引物均具有16個核苷酸長度的模板結合區(“16核苷酸模板結合區”組)。在各組中,制備具有8個不同尾區長度的第一和第二引物對組:7、8、9、10、11、12、14和16個核苷酸。圖3提供了針對16核苷酸模板結合區組(圖3A)和20核苷酸模板結合區組(圖3B)的不同的引物對組的核苷酸序列。在圖3A和3B中,“尾”序列指尾區,而“引物”區指引物的模板結合區。引物的序列以5’-3’方向顯示。
制備110微升的反應混合物,每一個含有:50mM乙酸鉀,20mM Tris-乙酸鹽(pH 7.9),10mM乙酸鎂,1mM DTT,30μg牛血清白蛋白(BSA),0.8M甜菜堿,各為1.4mM的dATP、dTTP、dGTP和dCTP,2uM 59(Life Technologies),0.8單位/μl Bst DNA聚合酶(New England BioLabs),0.016單位/μl AMV逆轉錄酶(New England Biolabs),1單位/μl鼠核糖核酸酶抑制劑(New England Biolabs),0.8μM的第一引物變體,0.8μM的第二引物變體以及每微升100,000個拷貝T124A1模板,并在56℃下在CFX 96Touch儀器(Bio-Rad)中溫育100分鐘。測定的轉變點示于圖3C(20核苷酸模板結合區組)和3D(16核苷酸模板結合區組)中。在圖3C和3D中,X軸提供了反應中使用的第一和第二引物的尾區的核苷酸長度,而Y軸提供了測定的轉變時間(以分鐘計)。對于每一個尾區核苷酸長度,示出了兩個相鄰的條:左邊的條是含有模板的反應的轉變時間,而右邊的條是沒有模板的反應的轉變時間。如圖3所示,在這些反應條件下,含有具有相對較短尾區的引物的反應顯示了更快的轉變時間以及含模板的反應與沒有模板的反應的轉變時間之間的更大的分離。例如,對于16bp和20bp引物,含有具有7、8或9個核苷酸的尾區長度的引物的反應顯示了比含有具有12、14或16個核苷酸的尾區長度的引物的反應更快的轉變時間。
實施例3-在可變的溫度下擴增模板核酸
使用如本文提供的方法擴增靶核酸。準備反應以測定在上文實施例1中描述的靶核酸T124A1。第一引物“RLX0892”(序列:5’TTGGGAAACCAAACCGTACCAACC 3’)(SEQ ID NO:20)和第二引物“RLX0893”(序列:5’GTTTCCCAAATGCGGAATGTACC 3’)(SEQ ID NO:32)用于擴增T124A1。這兩種引物均具有9核苷酸尾區,RLX0892具有15核苷酸模板結合區而RLX0893具有14核苷酸模板結合區。RLX0892的尾區為:5’TTGGGAAAC 3’(SEQ ID NO:84)而RLX0893的尾區為:5’GTTTCCCAA 3’(SEQ ID NO:85)。
制備80微升的反應混合物,每一個含有:50mM乙酸鉀,20mM Tris-乙酸鹽(pH 7.9),10mM乙酸鎂,1mM DTT,20μg牛血清白蛋白(BSA),0.8M甜菜堿,各為1.4mM的dATP、dTTP、dGTP和dCTP,2uM 59(Life Technologies),0.8單位/μl Bst DNA聚合酶(New England BioLabs),0.016單位/μl AMV逆轉錄酶(New England Biolabs),1單位/μl鼠核糖核酸酶抑制劑(New England Biolabs),0.8μM的第一引物RLX0892,0.8μM的第二引物RLX0893以及每微升10,000、1,000、100或0個拷貝T124A1模板,并一式三份在52、52.7、54、55.9、58.4、60.3、61.4或62℃下在CFX 96Touch儀器(Bio-Rad)中溫育100分鐘。測定的轉變點示于圖4中。X軸提供了反應的溫育溫度,而Y軸提供了測定的轉變時間(以分鐘計)。對于各個溫度,示出了4個相鄰的條,從左至右為:10,000個拷貝模板/微升、1000個拷貝模板/微升、100個拷貝模板/微升或無模板對照。如圖4所示,在這些反應條件下,該試驗在52-62℃的整個溫度范圍內在1000個拷貝模板/微升下,并且在一些溫度下在至少低至100個拷貝模板/微升的模板濃度下有效地擴增了模板。
實施例4-在人基因組DNA的存在下擴增模板核酸
使用如本文提供的方法擴增靶核酸。在人DNA的存在下準備反應以測定靶核酸T124A1(上文所述的)。使用第一引物“RLX0892”(上文所述的)和第二引物“RLX0893”(上文所述的)來擴增T124A1。
制備160微升的反應混合物,每一個含有:50mM乙酸鉀,20mM Tris-乙酸鹽(pH 7.9),10mM乙酸鎂,1mM DTT,20μg牛血清白蛋白(BSA),0.8M甜菜堿,各為1.4mM的dATP、dTTP、dGTP和dCTP,0.4x 59(Life Technologies),0.8單位/μl Bst DNA聚合酶(New England BioLabs),0.016單位/μl AMV逆轉錄酶(New England Biolabs),1單位/μl鼠核糖核酸酶抑制劑(New England Biolabs),0.8μM的第一引物RLX0892,0.8μM的第二引物RLX0893,和每微升1,000、100或0個拷貝T124A1模板,以及0、1、2.5、5或10納克的人基因組DNA,并在56℃下在CFX 96Touch儀器(Bio-Rad)中溫育100分鐘。測定的轉變點示于圖5中。X軸提供了反應中人基因組DNA(“hDNA”)的量,而Y軸提供了測定的轉變時間(以分鐘計)。對于hDNA的每個量,示出了4個相鄰的條,從左至右為:1000個拷貝模板/微升、100個拷貝模板/微升或無模板。如圖5所示,在這些反應條件下,該試驗在至少10ng hDNA的存在下在1000個拷貝模板/微升下有效地擴增了模板。而且,反應中加入hDNA僅引起了NTC轉變時間相對較小的降低,即使在5或10ng hDNA的濃度下。
實施例5-從病毒裂解物洗脫液擴增模板核酸
使用如本文提供的方法從含有靶標的兩個不同樣品中擴增靶核酸。在以下兩個樣品中制備靶核酸T124A1:1)含有分離的T124A1RNA分子(如在實施例1中的)的樣品,以及2)含有從甲型流感H3N2病毒樣品中分離的核酸的樣品。T124A1是HA3基因的一部分,并因此被預期存在于從甲型流感H3N2病毒中分離的核酸的樣品中。根據制造商的說明用Chemagic病毒DNA/RNA試劑盒(PerkinElmer)制備甲型流感病毒裂解物。通過qPCR定量兩個不同樣品中的T124A1的濃度,并且稀釋樣品以將樣品中T124A1的濃度歸一化。使用第一引物“RLX0892”和第二引物“RLX0893”擴增T124A1。
制備25微升的反應混合物,每一個含有:50mM乙酸鉀,20mM Tris-乙酸鹽(pH 7.9),10mM乙酸鎂,1mM DTT,20μg牛血清白蛋白(BSA),0.8M甜菜堿,各為1.4mM的dATP、dTTP、dGTP和dCTP,2uM 59(Life Technologies),0.8單位/μl Bst DNA聚合酶(New England BioLabs),0.016單位/μl AMV逆轉錄酶(New England Biolabs),1單位/μl鼠核糖核酸酶抑制劑(New England Biolabs),0.8μM的第一引物RLX0892,0.8μM的第二引物RLX0893以及每微升10,000、1000或0個拷貝T124A1模板,并在56℃下在CFX 96Touch儀器(Bio-Rad)中溫育100分鐘。測定的轉變點示于圖6中。X軸提供了反應中的模板拷貝數/微升,而Y軸提供了測點的轉變點(以分鐘計)。對于模板拷貝數/微升的各個量,示出了2個相鄰的條,從左至右為:分離的T124A1和甲型流感病毒裂解物。還示出了NTC的轉變點。如圖6中所示,在這些反應條件下,該試驗有效地擴增了分離的T124A1模板以及甲型流感病毒裂解物中的T124A1模板。
實施例6-模板核酸的擴增
使用如本文提供的方法擴增靶核酸。準備反應以測定T129D1的54核苷酸部分,其為乙型流感病毒血凝素(HA)基因(RNA分子)的298核苷酸部分。在SEQ ID NO:90中提供了T129D1的核苷酸序列。第一引物“A8”(核苷酸序列:5’TCTTGAGAGAACCCACTAAC 3’)(SEQ ID NO:86)和第二引物“B8”(核苷酸序列:5’TCTCAAGAATTTGGTCTTCC 3’)(SEQ ID NO:87)用于擴增T129D1。在這兩種引物中,前8個核苷酸(從5’末端)是尾區,而最后的12個核苷酸是模板結合區。這些引物一起靶向T129D1的54核苷酸部分。
制備100微升的反應混合物,其含有:50mM乙酸鉀,20mM Tris-乙酸鹽(pH7.9),10mM乙酸鎂,1mM DTT,20μg牛血清白蛋白(BSA),0.8M甜菜堿,各為1.4mM的dATP、dTTP、dGTP和dCTP,0.4x 59(Life Technologies),0.8單位/μl Bst DNA聚合酶(New England BioLabs),0.016單位/μl AMV逆轉錄酶(New England Biolabs),1單位/μl鼠核糖核酸酶抑制劑(New England Biolabs),0.8μM的第一引物A8,0.8μM的第二引物B8以及每微升100,000T129D1模板,并在58℃下在CFX 96Touch儀器(Bio-Rad)中溫育100分鐘。100分鐘后,從反應中取出樣品并將其連接入克隆載體。使用針對于克隆位點的載體特異性引物對含有反應產物的載體進行測序。多個示例性測序反應的結果的一部分示于圖7中。測序結果表明形成了具有期望的結構的多聯體。特別地,在這些實例中,在反應產物的單一鏈中,存在來自T129D1基因的靶向的54核苷酸序列的多個拷貝,這些拷貝由A8引物的尾區的序列(5’TCTTGAGA 3’)(SEQ ID NO:88)分隔開。在圖7中,僅顯示了T129D1的第二次(從左至右)出現的一部分;序列在圖中所示的核苷酸之外繼續。
除非另外指出,本文提供的核苷酸和氨基酸序列是人工序列。
盡管本文中已經示出并描述了本發明的優選實施方式,但對于本領域技術人員顯而易見的是,這些實施方式僅以示例的方式提供。前述的描述并非詳盡的或將本發明限于所公開的精確的實施方式,并且根據以上教導在不脫離本發明的情況下其他的修改和變化是可能的。無論優選與否的任何特征均可與無論優選與否的任何其他特征相組合。還應當理解,雖然出于方便的目的,本文中已經使用有限數目的術語和短語描述了本文提供的發明,但本發明也可以使用本文未提供的同樣準確描述本發明的其他術語和短語進行描述。所附權利要求書不應被解釋為包括裝置加功能的限定,除非這樣的限定在給定的權利要求中使用短語“用于…的裝置”而被明確闡述。應當理解,如此處的說明書和隨后的權利要求書全文中所使用,“一個”、“一種”和“該”的含義包括復數指代對象,除非上下文另有明確規定。例如,提及“測定”可以指一個測定或多個測定。此外,如此處的說明書和隨后的權利要求書全文中所使用,“之中”的含義包括“之中”和“之上”,除非上下文另有明確規定。如在此處的說明書和隨后的整個權利要求書中所用的,描述為含有第二個對象的“至少一部分”的第一對象可含有所有量的/完整的第二對象。如在此處的說明書和隨后的整個權利要求書中所用的,術語“包含”、“包括”和“含有”以及相關的時態是包含在內且開放式的,并且不排除附加的、未敘述的要素或方法步驟。而且,在一些情況下,拓寬詞語和短語諸如“一個或多個(一種或多種)”、“至少”、“但不限于”或其他類似的短語的存在不應被理解為在這類拓寬短語可能不存在的情況下意味著較窄的情況是有意或需要的。最后,如此處的說明書和隨后的權利要求書全文中所使用,“或”的含義同時包括結合的和分離的,除非上下文另有明確規定。因此,除非上下文另外明確規定,術語“或”包括“和/或”。
本文檔包含受到版權保護的材料。版權所有者(本文的申請人)不反對對專利文件或專利公開內容中的任何一個的摹本復制,因為它們出現于美國專利商標局專利文件或記錄中,但除此之外保留任何所有的版權。以下聲明應當適用:Copyright 2013-14Theranos,Inc。
- 還沒有人留言評論。精彩留言會獲得點贊!