一種連續制備大顆粒硅溶膠的方法與流程
本發明涉及化學技術領域,具體涉及電子化學品領域,特別涉及一種連續制備大顆粒硅溶膠的方法。
背景技術:
大顆粒硅溶膠是指平均顆粒大小≧80nm的硅溶膠,是一種重要的精密拋光耗材,也可以用于其他多個領域。隨著電子產業的興起,大顆粒硅溶膠在藍寶石襯底、硅晶圓片等精密拋光和集成電路多層布線時的化學機械平坦化(cmp)工藝中的作用越來越大,市場對其需求也越來越大。
目前制備大顆粒硅溶膠的方法主要有離子交換法和直接酸化法。其基本原理為:
離子交換法采用水玻璃為原料,經過離子的交換、硅酸的制備、晶種的制備、粒子的增長反應、濃縮和純化等步驟而制備出硅溶膠產品。離子交換法需要一步步地將粒子增大,耗費大量時間,效率低下,而且再生離子交換樹脂時會產生大量的含酸廢水,每個步驟對硅溶膠最終的品質均有直接的影響,離子交換法生產大顆粒硅溶膠很難做成連續化生產模式。另一種方法是直接酸化法,一般采用稀水玻璃為原料,經過離子交換法去除鈉離子,制備晶核,再經過直接酸化、晶粒長大等步驟制備出硅溶膠,用此種方法制備出的硅溶膠雜質離子含量高,穩定性差,產品質量差,并且制備產品過程復雜,耗時較長,效率低下,也無法連續化。綜上所述,目前正常生產大顆粒硅溶膠的方法都是間歇式的,時間長、效率低、成本較高,并且產品質量不穩定,生產過程中有大量的廢水需要處理,環境壓力大。
技術實現要素:
鑒于現有技術制備大顆粒硅溶膠方法存在的產品過程復雜,無法連續化生產的缺陷,本發明提供一種連續制備大顆粒硅溶膠的方法。
本發明的技術方案是:一種連續制備大顆粒硅溶膠的方法,包括下列步驟:
(1)配制堿性水溶液a液,
(2)將烷氧基硅烷加入高純酸性水溶液中,通過水解反應制得無色透明硅酸水解液前驅體b液,
(3)在第一反應容器內加入步驟(1)制備的堿性溶液a液,加熱至沸騰回餾,
(4)并將步驟(2)制備的硅酸水解液前驅體b液和步驟(1)制備的堿性溶液a液,同時連續地滴加在步驟(3)的第一反應容器的堿性溶液中a液,在該條件下二氧化硅顆粒成核生長;
通過連續滴加裝置,在反應器中不斷滴加硅酸水解液與堿性液體,使二氧化硅顆粒不斷長大,通過控制滴加硅酸水解液和堿性溶液的速度、時間與增減連續反應裝置中反應器的數量,可以調節硅溶膠的顆粒大小,
(5)將第一反應容器中制備得到的硅溶膠導入到第二反應容器,并將步驟(2)制備的硅酸水解液前驅體b液和步驟(1)制備的堿性溶液a液,同時連續地滴加在步驟(3)的第二反應容器的堿性溶液中a液,在該條件下二氧化硅顆粒成核生長;
(6)將第二反應容器中制備得到的硅溶膠導入到第n反應容器,并將步驟(2)制備的硅酸水解液前驅體b液和步驟(1)制備的堿性溶液a液,同時連續地滴加在步驟(3)的第n反應容器的堿性溶液中a液,在該條件下二氧化硅顆粒成核生長;其中n≥1;
(7)最后將第n反應容器的硅溶膠導出,得到成品;在整個生產過程中從第一反應容器到第n反應容器的反應,都是在連續滴加硅酸水解液前驅體b液和堿性溶液a液,進行反應。
本發明的一優選技術方案中,所述烷氧基硅烷選自四甲氧基硅烷或者四乙氧基硅烷或其混合;所述其中酸性溶液中的酸選自鹽酸、硝酸、硫酸。
本發明的一優選技術方案中,步驟(2)中,水、h+與烷氧基硅烷的摩爾比為4:0.002~0.005:0.5~2。
本發明的一優選技術方案中,所述堿性水溶液選自氫氧化鉀、碳酸鉀、氫氧化鈉、有機鉀鹽比如甲醇鉀,乙醇鉀等。所述堿性水溶液的濃度為0.01%~10%。
本發明的一優選技術方案中,步驟(2)中,將烷氧基硅烷連續加入高純酸性水溶液中,通過水解反應制得無色透明硅酸水解液前驅體。
本發明的一優選技術方案中,為使反應中產生的二氧化硅核繼續生長,在滴加過程中連續加熱被滴加物料,蒸出部分水以及醇;本發明中,第n反應器1≤n≤10。
本發明的制備工藝與傳統的水玻璃制備工藝相比,既不需要用大量的離子交換樹脂,將水玻璃轉換成硅酸,又不需要間隙式的進料出料,耗費大量時間。連續法制備大顆粒硅溶膠時其快速性與連續性的優點非常明顯,效率高,產品質量穩定,成本低,根據顆粒大小可得不同濃度的硅溶膠,硅溶膠的平均顆粒大小在80nm至200nm可調。
本發明的方法通過不斷地滴加堿性溶液與硅酸前驅體,以達到連續進料、連續出料、二氧化硅顆粒連續生長的目的;而且該硅溶膠具有除鉀或鈉離子外其他所有金屬雜質含量低的品質,而鉀離子對大多數電子產品的拋光基本無影響。與水玻璃法間隙式進出料系統相比,其特點是進出料連續、高效、成本低,質量控制更加容易實現。
本發明的優點是:
1.連續法制備硅溶膠,可以在有限的空間與時間內連續地生產出所需要粒徑的大顆粒硅溶膠,與間隙法相比,生產效率大大提高。
2.本發明不需溶劑為媒介,也不需要用離子交換樹脂把水玻璃轉換成硅酸,不產生大量廢液,更不需要在進料、出料時由于階段性的升溫降溫,浪費大量的能源。
3.制得的硅溶膠純度高,其中主要的穩定劑可以為鉀離子,除了鉀以外的各金屬離子含量小于1ppm,也可以是鈉離子。而以鉀離子為穩定劑的硅溶膠對電子產品的拋光的影響比鈉離子小。
附圖說明
下面結合附圖及實施例對本發明作進一步描述:
圖1為本現有技術的水玻璃法的制備方法流程示意圖。
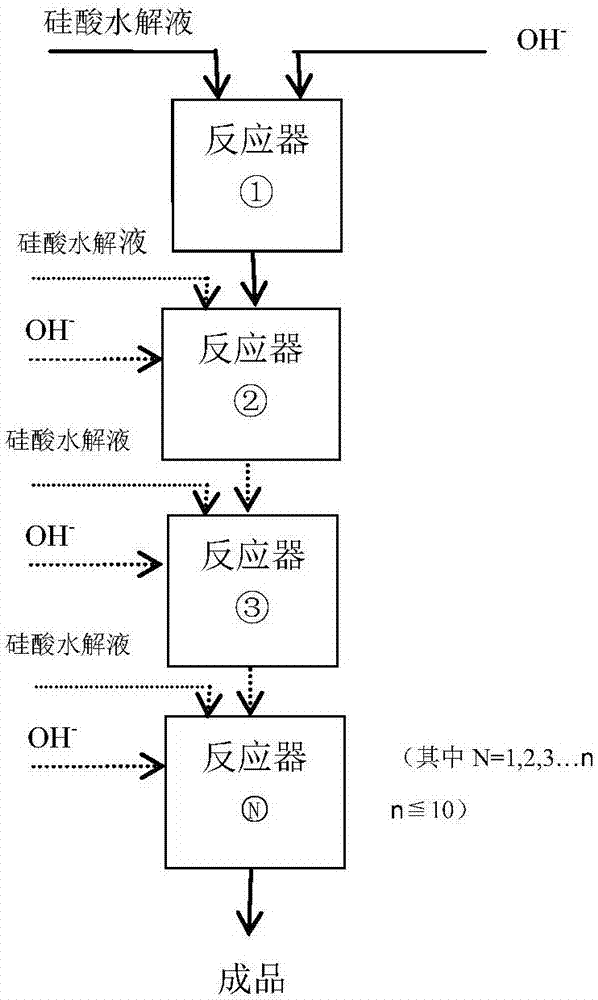
圖2為本發明的連續制備大顆粒硅溶膠的方法流程示意圖;
圖3為本發明實施例1制備得到硅溶膠顆粒的sem測試圖。
圖4為本發明實施例2制備得到硅溶膠顆粒的sem測試圖。
具體實施方式
為使本發明的上述目的、特征和優點能夠更加明顯易懂,下面結合附圖對本發明的具體實施方式做詳細的說明。在下面的描述中闡述了很多具體細節以便于充分理解本發明。但是本發明能夠以很多不同于在此描述的其它方式來實施,本領域技術人員可以在不違背本發明內涵的情況下做類似改進,因此本發明不受下面公開的具體實施例的限制。
除非另有定義,本文所使用的所有的技術和科學術語與屬于本發明的技術領域的技術人員通常理解的含義相同。本文中在本發明的說明書中所使用的術語只是為了描述具體的實施例的目的,不是旨在于限制本發明。本文所使用的術語“及/或”包括一個或多個相關的所列項目的任意的和所有的組合。
以下結合附圖描述本發明具體實施方式。
實施例1:
溶液a:0.1%的氫氧化鉀水溶液
溶液b:將水、硫酸(98%)、四甲基硅烷(tmos)按照4:0.002:1的比例流入一管式反應器,混合均勻后從管式反應器中連續流出。
在反應器①中加入溶液a,加熱至沸騰回餾,然后將溶液a與溶液b同時勻速滴入反應器①中,持續勻速滴加。當反應器①中的硅溶膠流出至反應器②后,加熱此液體至沸騰回餾,然后開始同時勻速滴加溶液a與溶液b至反應器②中,持續勻速滴加。與此同時反應器①中的反應繼續進行,硅溶膠不停地從反應器①流入反應器②中。當反應器②中的硅溶膠開始流入反應器③后,在反應器③中重復之前在反應器②中的操作。10h后從反應器③中流出的二氧化硅溶膠趨于穩定。24h后與72h后分別從流出的硅溶膠中取樣,兩次得到的硅溶膠粒徑、固含量與ph均相同。固含量35%,ph=8.4,通過sem測試,平均粒徑大小為85nm。24h的樣品的sem測試如圖3所示。
實施例2:
溶液a:0.1%的氫氧化鉀水溶液
溶液b:將水、硫酸(98%)、四甲基硅烷(tmos)按照4:0.002:1的比例流入一管式反應器,混合均勻后從管式反應器中連續流出。
在反應器①中加入溶液a,加熱至沸騰回餾,然后將溶液a與溶液b同時勻速滴入反應器①中,持續勻速滴加。當反應器①中的硅溶膠流出至反應器②后,加熱此液體至沸騰回餾,然后開始同時勻速滴加溶液a與溶液b至反應器②中,持續勻速滴加。與此同時反應器①中的反應繼續進行,硅溶膠不停地從反應器①流入反應器②中。當反應器②中的硅溶膠開始流入反應器③后,在反應器③中重復之前在反應器②中的操作。反應器①與反應器②中的反應繼續進行。當反應器③中的硅溶膠開始流入反應器④中時,在反應器④中重復之前在反應器②中的操作。14h后從反應器④中流出的二氧化硅溶膠趨于穩定。24h后與100h后分別從流出的硅溶膠中取樣,兩次得到的硅溶膠粒徑、固含量與ph均相同。固含量40%,ph=8.8,通過sem測試,平均粒徑大小為103nm。24h的樣品的sem測試如圖4所示。
以上顯示和描述了本發明的基本原理、主要特征和本發明的優點。本行業的技術人員應該了解,本發明不受上述實例的限制,上述實例和說明書中描述的只是說明本發明的原理,在不脫離本發明精神和范圍的前提下本發明還會有各種變化和改進,這些變化和改進都落入要求保護的本發明范圍內。本發明要求保護范圍由所附的權利要求書及其等同物界定。
- 還沒有人留言評論。精彩留言會獲得點贊!