一種新的合成晶體材料EMM?26、其制備及其用途的制作方法
本發明涉及一種新的合成晶體材料EMM-26及其制備方法。本發明還涉及多孔形式的EMM-26在有機轉化和吸附過程中的用途。
背景技術:
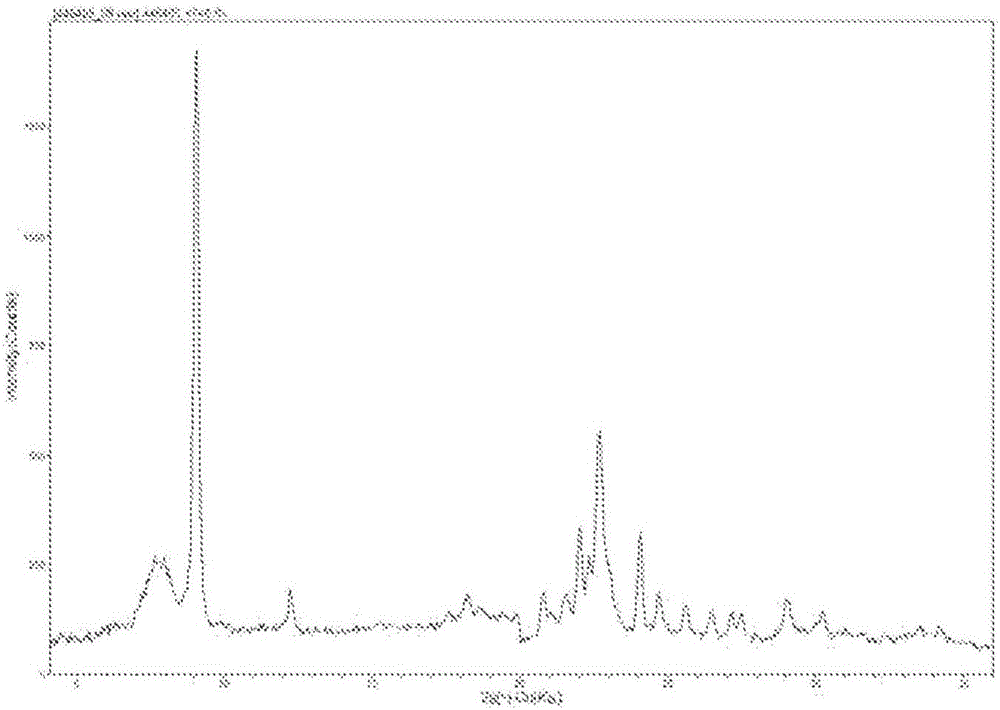
:已知天然和合成的沸石材料兩者都可用作吸附材料,并對各種不同類型的烴類轉化反應具有催化性能。特定沸石材料正如通過X-射線衍射所確定的,是具有確定晶體結構的有序、多孔的結晶金屬硅酸鹽,其中存在大量較小空腔,所述空腔可能通過大量更小的通道或孔隙互相連接。在特定沸石材料中,這些空腔和孔隙的尺寸均勻。由于這些孔隙的尺寸使其接受特定尺寸的分子的吸附并拒絕更大尺寸的分子的吸附,因此這些材料已開始被稱為“分子篩”,并以利用這些性質的各種方式得到利用。這些天然和合成的分子篩兩者包括許多種含正離子的結晶硅酸鹽和其中硅被其他四價元素部分或完全代替的取代的硅酸鹽。這些硅酸鹽可以被描述為SiO4四面體和任選的三價元素氧化物例如AlO4和/或BO4的四面體的剛性三維構架,其中所述四面體通過氧原子的共享而交聯,由此使總的三價元素和硅原子對氧原子的局部比為~1:~2。所述含有三價元素的四面體的電價通過在所述晶體中包含陽離子例如堿金屬或堿土金屬陽離子而得以平衡。這可以表示為其中三價元素例如鋁對各種陽離子例如Ca/2、Sr/2、Na、K或Li的數目之比約等于1。以常規方式使用離子交換技術,可以將一種類型的陽離子用另一種類型的陽離子完全或部分交換。利用這種陽離子交換,可以通過陽離子的適當選擇來改變給定硅酸鹽的性質。現有技術已導致形成多種合成沸石。這些沸石中的許多用字母或其他方便的符號命名,例如沸石A(美國專利號2,882,243)、沸石X(美國專利號2,882,244)、沸石Y(美國專利號3,130,007)、沸石ZK-5(美國專利號3,247,195)、沸石ZK-4(美國專利號3,314,752)、沸石ZSM-5(美國專利號3,702,886)、沸石ZSM-11(美國專利號3,709,979)、沸石ZSM-12(美國專利號3,832,449)、沸石ZSM-20(美國專利號3,972,983)、ZSM-35(美國專利號4,016,245)、沸石ZSM-23(美國專利號4,076,842)、沸石MCM-22(美國專利號4,954,325)和沸石MCM-35(美國專利號4,981,663)等等。目前存在超過200種已知的被國際沸石聯合會(InternationalZeoliteAssociation)認可的沸石構架結構。對于具有與已知材料不同的性質,用于改進許多有機化合物轉化和吸附過程的性能的新的結構,存在著需求。每種結構具有獨特的孔隙、通道和籠尺寸,這提供了如上所述的特定性質。EMM-26是一種具有獨特構架結構的新的合成晶體材料,具有由四面體配位原子的10元環限定的二維孔隙系統,其孔隙尺寸為EMM-26可用于有機化合物轉化和/或吸附過程。發明概述因此,在一個方面中,本發明涉及一種新的合成晶體材料EMM-26,其在特定形式下表現出微孔性并具有通過橋接原子相連的四面體原子(T)的獨特構架。所述EMM-26的四面體原子構架由以下面表1中示出的方式連接最近的四面體(T)原子來限定。在一個或多個實施方式中,所述EMM-26的四面體原子構架可以由具有下面表2中列出的以埃為單位的原子坐標的晶胞所限定,其中每個坐標位置可以在±1埃內變化:在一些實施方式中,EMM-26至少在其合成后原樣(as-synthesized)的形式下可以通過包括在下面的表3中列出的線的X-射線衍射圖案來鑒定。在一個或多個實施方式中,EMM-26在其合成后原樣的形式下可以具有包含下式、基本上由下式構成或者為下式的組成:aHal:bQ:cX2O3:YO2:zH2O,其中Hal是鹵素離子;Q是選自1,6-雙(N-甲基-吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的有機結構導向劑,X是三價元素,Y是四價元素,a是具有等于或大于0至小于或等于0.2的值的數,b是具有大于0至小于或等于0.10的值的數,0.015<c<0.125,并且z是具有大于或等于0至小于或等于0.15的值的數。在一些實施方式中,X可以包含硼和/或鋁,并且Y可以包含硅和/或鍺。在其他實施方式中,EMM-26在其合成后原樣的形式下可以具有下述組成:mM:bQ:cX2O3:YO2:zH2O,其中M是堿金屬或堿土金屬;Q是選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的有機結構導向劑,X是三價元素,Y是四價元素,m是具有等于或大于0至小于或等于0.1的值的數,b是具有大于0至小于或等于0.10的值的數,0.015<c<0.125,并且z是具有大于或等于0至小于或等于0.15的值的數。在一些實施方式中,X可以包含硼和/或鋁,并且Y可以包含硅和/或鍺。在另一方面中,本發明涉及一種用于生產EMM-26的方法,所述方法包括:提供包含水、四價元素Y的氧化物、三價元素X的氧化物的源和選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的結構導向劑(Q)的反應混合物;將所述反應混合物在足以形成EMM-26晶體的溫度下加熱足夠時間;以及任選但優選地從所述反應混合物純化和/或分離EMM-26晶體產物。在又一方面中,本發明涉及一種用于從包含二氧化碳與烷烴、氧、氮、SOx和NOx中的一者或多者的混合物中分離二氧化碳的方法,所述方法包括使所述混合物與多孔形式的EMM-26接觸以選擇性吸附所述二氧化碳,以便形成與所述二氧化碳混合物相比具有較低二氧化碳含量的產物料流。附圖說明圖1示出了實施例1的產物的X-射線衍射圖案。圖2示出了實施例1的產物的掃描電子顯微照相(SEM)圖像。圖3示出了實施例2的產物的X-射線衍射圖案。圖4示出了實施例3的制造后原樣的、煅燒后原樣(as-calcined)的和臭氧處理過的產物的X-射線衍射圖案。圖5示出了實施例3的制造后原樣的產物的SEM圖像。圖6示出了實施例3的制造后原樣的和臭氧處理過的產物的11BMASNMR波譜。圖7示出了實施例4的制造后原樣的產物的SEM圖像。圖8示出了實施例6的產物的X-射線衍射圖案。圖9示出了實施例6的制造后原樣的產物的SEM圖像。圖10是繪制與二氧化硅-CHA和二氧化硅-DDR構架類型的沸石的等效容量相比,實施例3的煅燒后原樣的EMM-26產物對CO2、CH4和N2的相對吸附容量的圖。圖11是比較了實施例3和6的煅燒后原樣的EMM-26產物對CO2、CH4和N2的相對吸附容量的圖。具體實施方式EMM-26是一種具有獨特晶體構架結構的新的物質組合物,其具有由四面體配位原子的10元環限定的二維孔隙系統,在特定形式、特別是其合成后原樣的形式下,EMM-26的孔隙可以被額外構架材料(extra-frameworkmaterial)部分或完全阻斷。在其多孔形式下,EMM-26可用于有機化合物轉化和/或吸附過程。在一些實施方式中,EMM-26的獨特晶體結構可以由每個晶胞中四面體配位的原子之間的連接限定。具體來說,EMM-26的每個晶胞可以具有通過橋接原子相連的四面體(T)原子的構架,其中所述四面體原子構架可以由以下面表1中示出的方式連接最近的四面體(T)原子來限定。表1四面體配位的原子是能夠具有四面體配位的原子,包括但不限于下述原子中的一種或多種:硼(B),鋰(Li),鈹(Be),鋁(Al),磷(P),硅(Si),鎵(Ga),鍺(Ge),鋅(Zn),鉻(Cr),鎂(Mg),鐵(Fe),鈷(Co),鎳(Ni),錳(Mn),砷(As),銦(In),銅(Cu),錫(Sn),銻(Sb),鈦(Ti)和鋯(Zr)。橋接原子是能夠連接兩個四面體配位的原子的原子,其實例包括但不限于下述原子中的一種或多種:氧(O),氮(N),氟(F),硫(S),硒(Se)和碳(C)。EMM-26構架中優選的四面體原子可以包含選自B、Al、Si和Ge中的一種或多種元素。EMM-26的完整結構可以通過在完全相連的三維構架中連接多個如上所定義的晶胞來建立。一個晶胞中的四面體配位的原子可以連接到所有與它相鄰的晶胞中的特定四面體配位的原子。盡管表1列出了給定EMM-26晶胞的所有四面體配位的原子的連接,但所述連接可能不是連接到同一晶胞中的特定原子,而是連接到相鄰晶胞。可以設置表1中列出的所有連接,使得它們連接到最近的四面體配位的原子,不論它們是在同一晶胞中還是在相鄰晶胞中。另外地或可選地,EMM-26的結構可以由晶胞中每個四面體配位的原子的位置的x、y和z(笛卡爾)坐標限定。在這種構造中,每個四面體配位的原子可以鍵合到橋接原子,所述橋接原子進而可以鍵合到相鄰的四面體配位的原子。由于四面體配位的原子可能因其他晶體力(例如因無機或有機物質的存在)和/或因四面體配位原子和/或橋接原子的選擇而四處移動,因此在本文中對報道的x、y和z坐標位置暗示了±1.0埃的范圍。當T=硅并且橋接原子是氧時,EMM-26的四面體配位的原子(T-原子)的典型的以埃為單位的近似x、y和z坐標位置列于下面的表2中。表2EMM-26的合成后原樣的和煅燒后原樣的形式可以具有特征性的X-射線衍射(XRD)圖案,其基本反射線可以在表3(合成后原樣的形式)和表4(煅燒后的形式)中表示。隨著具體組成及其在結構中的載量,可能出現變化。因此,在表3和4中,相對強度和d-間距被表示成范圍。表3表4表3和4中的XRD圖案使用帶有X’celerator檢測器的PANalyticalX’Pert衍射儀,利用CuKα輻射來測量,并使用了下述參數:Bragg-Brentano幾何,~45kV和~40mA的管電壓和電流,~1/8°的固定發散狹縫和抗散射狹縫,~0.04弧度的Soller狹縫,和~0.017°的步長。在一個或多個實施方式中,EMM-26在其合成后原樣的形式下可以具有下述組成:aHal:bQ:cX2O3:YO2:zH2O,其中Hal是鹵素離子,例如氯離子或氟離子;Q是選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的有機結構導向劑,X是三價元素,Y是四價元素,a是具有等于或大于0至小于或等于0.2的值的數,b是具有大于0至小于或等于0.10的值的數,0.015<c<0.125,并且z是具有大于或等于0至小于或等于0.15的值的數。在一些實施方式中,X可以包含硼和/或鋁,并且Y可以包含硅和/或鍺。在另外的或可選的實施方式中,EMM-26在其合成后原樣的形式下可以具有下述組成:mM:bQ:cX2O3:YO2:zH2O,其中M是堿金屬或堿土金屬;Q是選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的有機結構導向劑,X是三價元素,Y是四價元素,m是具有等于或大于0至小于或等于0.1的值的數,b是具有大于0至小于或等于0.10的值的數,0.015<c<0.125,并且z是具有大于或等于0至小于或等于0.15的值的數。在一些實施方式中,X可以包含硼和/或鋁,并且Y可以包含硅和/或鍺。在上述有機結構導向劑中,1,6-雙(N-甲基吡咯烷)己烷雙陽離子具有下述結構式:并且1,6-雙(N-甲基哌啶)己烷雙陽離子具有下述結構式:上述二季銨化合物可以使用已知技術,通過N-甲基吡咯烷和N-甲基哌啶分別與1,6-二溴己烷的反應容易地合成。所述新的晶體材料EMM-26可以從包含水、優選為硅和/或鍺的四價元素Y的氧化物、優選為硼和/或鋁的三價元素X的氧化物的源和選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的結構導向劑(Q)的反應混合物制備。所述四價元素Y的適合的源可以取決于所選的元素Y,并且在Y包含或者是硅和/或鍺的優選實施方式中,可以包括二氧化硅的膠體懸浮液、鍛制二氧化硅、沉淀二氧化硅、堿金屬硅酸鹽、四烷基原硅酸酯、氧化鍺等或其組合。所述三價元素X的適合的源同樣可以取決于所選的元素,并且在X包含或者是硼和/或鋁的情況下,可以包括硼酸和水溶性硼酸鹽、水合氧化鋁和水溶性鋁鹽例如硝酸鋁等及其組合。另外地或可選地,可以使用X和Y的組合的源,其可以包括例如鋁硅酸鹽沸石如沸石Y,以及粘土或處理過的粘土例如偏高嶺土。Q的適合的源是相關的二季銨化合物的氫氧化物、氯化物、溴化物和/或其他鹽。在一些實施方式中,當存在時,所述反應混合物可能包含一種或多種鹵素(Hal)離子的源,優選為氯離子和/或氟離子。在這種實施方式中,所述反應混合物可以具有以氧化物的摩爾比計在下述范圍內的組成:在一些實施方式中,所述反應混合物可以包含一種或多種氫氧根離子的源。在這種實施方式中,所述反應混合物可以具有以氧化物的摩爾比計在下述范圍內的組成:所述反應混合物也可以含有來自于以前的合成的晶體材料例如EMM-26的晶種,理想情況下其量為所述反應混合物的約0.01重量ppm至約10,000重量ppm,例如約100重量ppm至約5,000重量ppm。EMM-26從上述合成混合物的結晶化可以在適合的反應容器例如聚丙烯罐或帶有特氟龍內襯的或不銹鋼高壓釜中,在靜態或攪拌條件下,在約100℃至約200℃例如約130℃至約180℃的溫度下,進行足以使結晶化在所使用的溫度下發生的時間,例如約2小時至約168小時或約5天至約40天。隨后,可以從液體/混合物分離所述晶體并回收。可以對通過本發明的方法生產的合成后原樣的EMM-26進行后續處理,以除去在其合成中使用的部分或全部有機導向劑Q。這可以方便地通過熱處理來實施,其中可以將所述合成后原樣的材料在至少約370℃的溫度下加熱至少~1分鐘,并且通常不超過約24小時。盡管可以將低于大氣壓和/或高于大氣壓的壓力用于所述熱處理,但出于方便的原因,大氣壓力通常可能是期望的。所述熱處理可以在高達約925℃的溫度下進行。另外地或可選地,有機導向劑Q可以通過用臭氧處理來移除(參見例如,Parikh等,微孔和介孔材料(MicroporousandMesoporousMaterials)76(2004)17–22)。根據需要并取決于材料的X2O3/YO2摩爾比,所述合成后原樣的EMM-26中的任何堿金屬或堿土金屬陽離子可以根據本領域中公知的技術,通過與其他陽離子的離子交換來替換。優選的替換陽離子可以包括金屬離子、氫離子、氫前體例如銨離子,及其混合物。特別優選的陽離子可以包括為特定烴類轉化反應定制催化活性的那些陽離子。這些陽離子可以包括但可能不限于氫、稀土金屬和元素周期表的第2至15族的金屬。當在本文中使用時,元素周期表的編號方案公開在化學與工程新聞(ChemicalandEngineeringNews),63(5),27(1985)中。本發明的產物可以與加氫組分例如鉬、錸、鎳、鈷、鉻、錳和/或貴金屬例如鉑或鈀密切組合,在其中可以執行加氫-脫氫功能。這些組分可以通過共結晶、以所述結構中的三價元素X例如鋁的程度交換到組合物中、在組合物中浸漬、與組合物密切物理混合或通過本領域中已知的任何適合的方法,進入到所述組合物中。這些組分,例如在鉑的情況下,可以通過用含有鉑金屬離子的溶液處理硅酸鹽,浸漬到產物催化劑組合物中/其上。因此,適合用于此目的鉑化合物包括氯鉑酸、二氯化鉑和含有鉑胺絡合物的各種化合物。本發明的晶體材料當用作吸附劑和/或催化劑時,通常應該是脫水的,至少是部分地脫水的。這可以通過在氣氛例如空氣、氮氣等下,并在大氣壓、低于大氣壓或高于大氣壓的壓力下,加熱到約200℃至約370℃范圍內的溫度約30分鐘至約48小時之間完成。另外地或可選地,脫水可以在室溫(~20-25℃)下,僅僅通過將EMM-26置于真空中來進行,但是為了獲得足夠量的脫水,可能需要更長的時間。本文中描述的EMM-26可例如在從包含二氧化碳和一種或多種烷烴例如甲烷、乙烷、丙烷和/或丁烷的混合物中和/或包含二氧化碳和氧、氮、H2S、SOx和/或NOx的混合物中分離二氧化碳的操作中用作吸附劑。所述分離方法可以利用EMM-26的平衡選擇性、EMM-26的動力學選擇性或EMM-26的平衡和動力學選擇性兩者,所述選擇性對于二氧化碳來說超過所述混合物的其他組分。特別地,B2O3對SiO2的摩爾比為約0.125至約0.033的EMM-26材料,在~1atm(~100kPa)下對CO2通常可以具有約0.8mmol/g至約2.0mmol/g的吸附容量。可選地或此外,特別是在其鋁硅酸鹽形式下,EMM-26可用作催化劑以促進一種或多種有機化合物轉化過程,包括許多目前在商業/工業上重要的過程。如在有機化合物(烴)轉化過程中使用的許多催化劑的情況下那樣,可以希望將對有機轉化過程中使用的溫度和其他條件有抗性的另一種材料并入本發明的EMM-26。這種材料可以包括有活性和無活性材料及合成的或天然存在的沸石,以及無機材料例如粘土、二氧化硅和/或金屬氧化物例如氧化鋁。后者可以是天然存在的或呈凝膠狀沉淀物或凝膠的形式,包括二氧化硅與金屬氧化物的混合物。與本發明的EMM-26聯合使用的、即在所述新晶體的合成期間與其組合和/或存在的有活性的材料的使用,可以在特定有機轉化過程中傾向于改變所述轉化和/或催化劑的選擇性。無活性的材料可以適合地充當稀釋劑以控制給定過程中的轉化的量,使得可以以經濟有序的方式獲得產物而不需使用其他(更昂貴的)控制反應速率的手段。這些材料可以被并入到天然存在的粘土例如膨潤土和高嶺土中,以提高催化劑在商業化運行條件下的壓碎強度。所述材料即粘土、氧化物等,可以起到催化劑的粘合劑的作用。提供具有良好的壓碎強度的催化劑可以是期望的,因為在商業化使用中,可能希望阻止催化劑碎裂成粉末狀材料(磨損)。這些粘土和/或氧化物粘合劑通常僅用于提高催化劑的壓碎強度的目的。可以與本發明的EMM-26復合的天然存在的粘土可以包括但不限于蒙脫土和高嶺土家族,所述家族包括亞膨潤土類和通常被稱為Dixie、McNamee、Georgia和Florida粘土的高嶺土類,或其中主要礦物質成分是埃洛石、高嶺石、地開石、珍珠石或富硅高嶺石的其他粘土。這些粘土可以以最初挖掘出的原始狀態使用,或首先進行煅燒、酸處理或化學改性。另外地或可選地,可用于與EMM-26復合的粘合劑包括無機氧化物例如二氧化硅、氧化鋯、二氧化鈦、氧化鎂、氧化鈹、氧化鋁及其混合物。可選地或除了上述材料之外,本發明的EMM-26可以與多孔基質材料復合,所述多孔基質材料例如二氧化硅-氧化鋁、二氧化硅-氧化鎂、二氧化硅-氧化鋯、二氧化硅-氧化釷、二氧化硅-氧化鈹、二氧化硅-二氧化鈦,和/或一種或多種三元組合物例如二氧化硅-氧化鋁-氧化釷、二氧化硅-氧化鋁-氧化鋯、二氧化硅-氧化鋁-氧化鎂和二氧化硅-氧化鎂-氧化鋯。EMM-26和無機氧化物基質的相對比例可以廣泛變化,其中EMM-26含量在復合材料的約1重量%至約90重量%的范圍內,并且更通常,特別是當所述復合材料以珠子的形式制備時,在所述復合材料的約2重量%至約80重量%的范圍內。示例性的基質含量范圍可以包括約10重量%至約50重量%。另外地或可選地,本發明可以有利地包括一個或多個下述實施方式。實施方式1.一種合成的晶體材料,其具有通過橋接原子相連的四面體原子(T)的構架,所述四面體原子構架由以表1中示出的方式連接最近的四面體(T)原子來限定。實施方式2.一種合成的晶體材料,其具有通過橋接原子相連的四面體原子(T)的構架,所述四面體原子構架由具有表2中列出的以埃為單位的原子坐標的晶胞所限定,其中每個坐標位置可以在±1埃內變化。實施方式3.一種合成的多孔晶體材料,所述晶體材料在其煅燒后原樣的形式下包含包括表4中列出的d-間距和相對強度的X-射線衍射圖案。實施方式4.一種合成的多孔晶體材料,所述晶體材料在其合成后原樣的形式下包含包括表3中列出的d-間距和相對強度的X-射線衍射圖案。實施方式5.根據前述實施方式中任一項所述的晶體材料,其中所述四面體原子包含選自Li、Be、B、Al、P、Si、Ga、Ge、Zn、Cr、Mg、Fe、Co、Ni、Cu、Mn、As、In、Sn、Sb、Ti和Zr中的一種或多種元素,例如選自B、Al和Si中的一種或多種元素。實施方式6.根據前述實施方式中任一項所述的晶體材料,其中所述橋接原子包含選自O、N、F、S、Se和C中的一種或多種元素,例如包含氧。實施方式7.根據實施方式1-2和4-6中任一項所述的晶體材料,其具有下述組成:aHal:bQ:cX2O3:YO2:zH2O,其中Hal是鹵素離子;Q是選自1,6-雙(N-甲基-吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的有機結構導向劑,X是三價元素,Y是四價元素,a是具有等于或大于0至小于或等于0.2的值的數,b是具有大于0至小于或等于0.10的值的數,0.015<c<0.125,并且z是具有大于或等于0至小于或等于0.15的值的數。實施方式8.根據實施方式1-2和4-6中任一項所述的晶體材料,其具有下述組成:mM:bQ:cX2O3:YO2:zH2O,其中M是堿金屬或堿土金屬;Q是選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的有機結構導向劑,X是三價元素,Y是四價元素,m是具有等于或大于0至小于或等于0.1的值的數,b是具有大于0至小于或等于0.10的值的數,0.015<c<0.125,并且z是具有大于或等于0至小于或等于0.15的值的數。實施方式9.根據實施方式7或實施方式8所述的晶體材料,其中X包含硼并且Y包含硅,任選地具有約0.125至約0.033的B2O3對SiO2的摩爾比,并任選地在約1atm(約100kPa)下對CO2具有約0.8mmol/g至約2.0mmol/g的吸附容量。實施方式10.一種用于獨立地制備晶體材料或制備根據前述實施方式中任一項所述的晶體材料的方法,所述方法包括下列步驟:(a)提供反應混合物,其包含:水、四價元素Y的氧化物、三價元素X的氧化物的源,任選的鹵素離子源,任選的氫氧根離子源和選自1,6-雙(N-甲基吡咯烷)己烷雙陽離子和1,6-雙(N-甲基哌啶)己烷雙陽離子中的一者或多者的結構導向劑(Q);(b)將所述反應混合物在包括100℃至200℃的溫度的結晶條件下加熱,直至形成所述晶體材料的晶體;(c)回收在(b)中產生的晶體;以及任選地(d)處理在(c)中回收的晶體以除去至少一部分所述結構導向劑(Q)。實施方式11.一種合成的多孔晶體材料,其通過實施方式10所述的方法生產。實施方式12.一種用于從包含二氧化碳與烷烴、氧、氮、H2S、SOx和NOx中的一者或多者的混合物中分離二氧化碳的方法,所述方法包括使所述混合物與實施方式1-9和11中任一項或多項所述的多孔晶體材料接觸。實施方式13.一種用于從包含二氧化碳和甲烷的混合物中分離二氧化碳的方法,所述方法包括使所述混合物與實施方式1-9和11中任一項或多項所述的多孔晶體材料接觸。現在將參考下面的實施例和附圖更具體地描述本發明。實施例實施例1在密封的~1.5-mL不銹鋼反應容器中,使用硼酸作為硼源、LudoxAS-40TM作為二氧化硅源、HCl作為鹵素離子源和1,6-雙(N-甲基吡咯烷)己烷氫氧化物作為結構導向劑Q,使用下述摩爾比制備反應混合物:Q/Si≈0.2;Si/B≈5;HCl/Si≈0.10;且H2O/Si≈35。將所述反應混合物在對流烘箱中,在翻滾條件(約30rpm)下,在~160℃下加熱~56天。通過三次離心、傾析、重懸浮和用去離子水清洗的一系列操作,逐步建立樣品。產物的粉末XRD給出了圖1的圖案,并顯示出產物是新的相EMM-26與無定形材料和少量沸石β雜質的混合物。圖2提供了該產物的SEM圖像,并顯示出產物看起來包含長度為5微米左右、寬度為~1-2微米并且厚度為約0.3微米的大晶體。實施例2重復實施例1,區別在于使用1,6-雙(N-甲基哌啶)己烷氫氧化物作為結構導向劑Q,不向反應混合物添加HCl,并且將反應混合物加熱~28天。產物的粉末XRD(圖3)顯示所述產物是在實施例1中觀察到的新的相EMM-26的純的形式。所述粉末XRD圖案可以在具有a≈19.43、b≈15.75和的C心斜方晶胞上索引。實施例3將約1.67克1,6-雙(N-甲基吡咯烷)己烷氫氧化物的溶液(~25.8重量%)與~5.39克去離子水在~23-mL鋼制Parr高壓釜的特氟龍內襯中混合。接下來將約0.19克硼酸添加至所述溶液并混合,直至幾乎完全溶解。然后向所述混合物添加~2.25gLudoxAS-40TM,添加~1.50克~1NHCl并混合,以產生具有下述摩爾組成的相對均勻的懸浮液:Q/Si≈0.1;Si/B≈5;HCl/Si≈0.10;且H2O/Si≈35。向所述懸浮液添加約0.04克來自于實施例1的產物的晶種,然后將所述內襯加蓋,密封在~23-mL高壓釜內部,并在翻滾條件(約40rpm)下在~160℃下加熱。在~14天后取出反應器,淬火,并通過過濾分離固體,用去離子水徹底清洗,干燥,并使用粉末XRD進行分析。圖4(下方的XRD圖案)示出了新的相EMM-26的粉末衍射圖案,并且圖5示出了所述相的SEM圖像。將一部分從實施例3生產的制造后原樣的產物在馬弗爐內,在氮氣氣氛下以~4℃/min的速度從環境溫度(~20-25℃)加熱至~400℃,然后在空氣中以~4℃/min的速度加熱至~550℃,然后在空氣中在~550℃下保持~2小時。圖4的中間的XRD圖案似乎顯示出在煅燒后衍射強度的相當可觀的損失和峰位置的遷移。然而,觀察到粉末衍射圖案在煅燒后仍保留。將另一部分實施例3的制造后原樣的產物用臭氧處理,以便分解/除去沸石結構中堵塞的有機物。將薄的產物床置于具有來自于臭氧發生器的~3500cm3/min的空氣流速的水平管式爐中。所述臭氧發生器產生具有約1%臭氧的空氣流。在~30分鐘的時間段內,將所述產物在含有臭氧的料流存在下從環境溫度(~20-25℃)加熱至~300℃。將溫度在~300℃保持~4小時,停止臭氧發生,然后使所述爐冷卻至室溫(~20-25℃)。圖4的上部XRD圖案示出了臭氧處理的產物的粉末衍生圖案。在這里可以看到,所述臭氧處理的材料的圖案中的峰似乎具有與制造后原樣的材料的峰相同的位置。制造后原樣的和臭氧處理過的材料兩者的圖案可以在相似的C心斜方晶胞上索引。圖6示出了所述新的EMM-26相的制造后原樣的和臭氧處理過的版本的11BMASNMR波譜。在-3.3ppm附近的共振據信是由四面體配位的硼造成的,并且以11.5ppm附近為中心的寬的特征據信是由非四面體配位的硼造成的。在臭氧處理后,約53%的硼似乎是非四面體的。實施例4在~23-mL鋼制Parr高壓釜的去了皮重的特氟龍內襯中,將~0.99克四甲基原硅酸酯和~2.93克1,6-雙(N-甲基-吡咯烷)己烷氫氧化物的氫氧化物溶液([OH]≈1.11mmol/克)混合在一起。使所述懸浮液部分水解約20分鐘,然后添加~0.13克~50%HF溶液和~0.033克硼酸并混合,以產生相對均勻的糊料。將所述特氟龍內襯置于通風罩中,使其過夜(~8-16小時)蒸發。然后向混合物添加另外的去離子水,以將H2O/Si的摩爾比調整到~10。添加約0.01克來自于實施例3的制造后原樣的產物的晶種,以產生具有下述組成的凝膠:Q/Si≈0.25;Si/B≈12;F/Si≈0.5;且H2O/Si≈10。將所述特氟龍內襯加蓋,密封在鋼制Parr高壓釜內,然后在~23-mL的翻滾(~50rpm)的高壓釜中在~150℃下加熱~22天。然后將高壓釜從烘箱取出并淬火至環境溫度(~20-25℃)。通過過濾分離固體,用去離子水徹底清洗,干燥,并使用粉末XRD進行分析。粉末XRD顯示所述樣品似乎是具有少量沸石β的EMM-26。圖7示出了所述產物的SEM圖像。實施例5重復實施例4,區別在于所述合成使用~7的H2O/Si摩爾比和~20的Si/B摩爾比進行,并將所述反應混合物在~175℃加熱~14天。粉末XRD顯示所述產物是EMM-26與沸石β的混合物。實施例6重復實施例5,區別在于使用~12的Si/B摩爾比,并將所述反應混合物僅僅加熱~7天。粉末XRD(圖8)顯示所述產物是純的EMM-26。圖9示出了所述產物的SEM圖像。在這些圖像中的晶體通常比圖5和圖7中的晶體更厚。實施例7與對二氧化硅-CHA和二氧化硅-DDR構架類型的沸石的等效容量相比,關于實施例3的煅燒后原樣的EMM-26產物對CO2、CH4和N2的相對吸附容量進行了一系列實驗。在測量之前,將所述沸石在真空下(例如不超過~0.01托)在~400℃下除氣。吸附等溫線在來自于康塔儀器公司(QuantachromeInstruments)的自動體積測量儀Autosorb-1TM中測量。結果示出在圖10中,其中吸附攝取值基于干樣品的重量。此外,表5列出了在~800托的相應氣體的分壓下試驗的每種沸石的平衡CO2/CH4吸附選擇性(SCO2/CH4)和平衡CO2/N2吸附選擇性(SCO2/N2)。表5樣品和處理SCO2/CH4SCO2/N2~400℃除氣的EMM-26~22.6~15.5~400℃除氣的DDR~3.4~8.2~400℃除氣的CHA~3.8~10.7實驗數據顯示,CO2似乎可以進入EMM-26的孔隙結構,并且正如所測量的,EMM-26的平衡CO2/CH4和CO2/N2吸附選擇性似乎高于二氧化硅DDR和二氧化硅CHA沸石的相應值。實施例8使用實施例6的煅燒后原樣的EMM-26產物重復實施例7的吸附實驗。在圖11中繪制兩組實驗的結果,其中樣品A對應于實施例3的產物,樣品B對應于實施例6的產物。可以看到,實施例6的產物似乎具有比實施例3的產物更高的吸附容量。實施例9遵照在“納米多孔材料中的擴散(DiffusioninNanoporousMaterials)”,J.Karger,D.N.Ruthven,D.N.Theodorou,Wiley-VCH,2012p.227[Karger等]中描述的已確立的方法,使用分子動力學模擬,對CO2和CH4在EMM-26結構中的擴散進行了建模。在NVT套件中,使用Nose恒溫器在不同溫度下進行了平衡分子動力學模擬。用于CO2分子的分子模型從J.J.Potoff,J.I.Siepmann,美國化學工程師會志(AIChEJournal),47(2001),1676獲取,用于CH4分子的分子模型從C.D.Wick,M.G.Martin,J.L.Siepmann,物理化學雜志B(J.Phys.Chem.B)104(2000)8008獲取。使用O.Talu,A.L.Myers,膠體和表面A:物理化學工程方面(ColloidsandSurfacesA:Physicochem.Eng.Aspects)187–188(2001)83中所描述的與沸石構架的相互作用,使用Lorentz-Berthelot組合規則。沸石構架上的電荷被鑒定為是Si(+2)和O(-1)。自擴散系數使用愛因斯坦關系式從分子的均方位移來計算[參見Karger等]。模擬預測了CO2在環境溫度(~300°K)和低載量(<~1mmol/克)下的擴散率在1E-10m2/sec至1E-9m2/sec之間。模擬預測了CH4的擴散率慢得多。CH4的估算擴散率約為1E-13m2/sec。這些模擬使用剛性構架結構來進行。預期在使用更加現實的柔性構架模型例如在R.Awati,P.I.Ravikovitch,D.S.Sholl,物理化學雜志C(J.Phys.Chem.C)117(2013)13462中所公開的模型時,CH4的擴散率將約為1e-12m2/sec至1e-11m2/sec。模擬結果表明,EMM-26應該是高度動力學選擇性的,被定義為CO2對CH4的擴散率之比的分離系數大于~10,更可以大于~100,并且可以甚至大于~500。盡管已參考特定實施方式對本發明進行了描述和說明,但本領域普通技術人員將理解,本發明將會產生不一定在本文中說明的變化。因此,出于確定本發明的真實范圍的目的,應該只參考權利要求書。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1