一種新型鋰電池正極材料的制作方法
本發明屬于材料技術領域,具體涉及一種含v6b20簇化合物的新型鋰電池正極材料。
背景技術:
鋰離子電池作為新一代的綠色儲能電池,包含工作電壓高,比容量大,循環性能優異,無記憶效應以及無污染等一系列優點。相對負極材料,鋰離子電池的正極材料比容量偏低,所以發展鋰離子電池的關鍵在于尋找更加優異的正極材料。正極材料的研究主要集中在第四周期的ti、v、mn、fe、co、ni這幾種可變價過渡金屬的鋰氧化合物上。正極材料經歷了從最開始的tis2、mos2等,到現在市場上常見的licoo2、lifepo4,再到近來引起廣泛研究的磷酸釩鹽(如li3v2(po4)3、livpo4f、livopo4)正極材料和三元混合材料。
多硼釩氧簇化合物由于含有可變價態的v,具有在電化學方面的廣泛應用。作為探索性試驗,本文將含有li+的多硼釩氧簇化合物作為鋰離子正極材料研究其電化學性能。由于其結構特點作為正極材料有以下優點:1,v具有較高的氧化還原電位從而獲得高的工作電壓;2,多硼釩氧簇陰離子所帶負電荷高,可以容納大量的抗衡陽離子li+,從而獲得高的比容量;3,多硼釩氧簇陰離子體積較大,容易形成較大的孔道,本發明所合成的化合物中存在直徑6?的孔道,有利于li+的擴散,從而獲得好的倍率性能。
技術實現要素:
本發明的目的在于提供一種新型的鋰電池正極材料及其制備方法,該鋰電池正極材料,具有優良的電化學性能,較高的首次充放電比容量,良好的離子電導率。本發明的原料相對廉價易得、制備方法簡單、材料結構清晰準確。
所述一種鋰電池正極材料,其是由以下質量分數的原料組分組成的:正極活性材料:80~85wt%,導電材料:10~15wt%,粘接材料:5~10wt%。其正極材料為[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2,導電材料為導電炭,粘接材料為n-甲基-吡咯烷酮。
所述正極材料的具體制備步驟為:
(1)正極活性材料的合成:稱取原釩酸鈉0.2196g,硼酸1.2006g,草酸0.3636g,乙酸銅0.1518g,氫氧化鋰0.1531g,加入6ml蒸餾水,攪拌混合均勻,然后緩慢滴加0.5ml乙二胺,置于磁力攪拌器上攪拌加熱,加熱至沸騰,當釜內溶液剩余2-3ml時停止加熱,使反應物充分溶解,趁熱將反應混合液移入23.00ml的聚四氟乙烯內襯的反應釜中,在160°c下恒溫120個小時。從烘箱中取出反應釜使其自然冷卻,24小時后抽濾得到綠色正六邊形的片狀晶體。(按釩計算其產率約為68%)。
(2)活性材料的預處理。將晶體材料研磨成粉末,并將粉末置于120°c的真空干燥箱中干燥24小時,以便最大程度的去除材料中的水分。
(3)正極材料的制備。按照重量分數計,由以下組分按照所示比例制備而成,正極活性材料:80~85%,導電材料:10~15%,粘接材料:5~10%。所述正極材料為[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2,所述導電材料為導電炭,粘結材料為n-甲基-吡咯烷酮。
本發明的顯著優點在于:
1:制備方法簡單。只需要將反應原料、蒸餾水以及有機配體置于反應釜中,
并將反應釜置于烘箱中,控制好反應的溫度以及時間,使得反應在較低的溫度下(160℃)下進行,最終得到反應產物。
2:原料豐富,容易獲取,而且價格較低,有應用潛力。
3:該正極材料具有較高的首次放電比容量(89.1mah/g)。
附圖說明
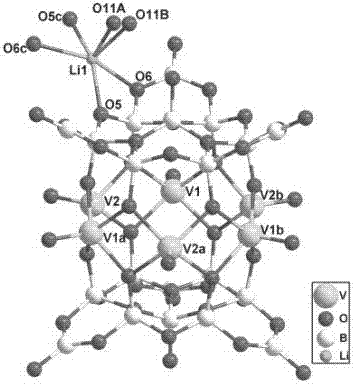
圖1是化合物[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2的晶體結構圖。
圖2是化合物[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2的紅外譜圖。
圖3是化合物[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2的紫外可見固體漫反射光譜圖。
圖4是電池的循環伏安曲線。
圖5是電池的充放電曲線。
圖6是電池的交流阻抗曲線。
具體實施方式
為進一步公開而不是限制本發明,以下結合實例對本發明作進一步的詳細說明。
實施例1
本新型鋰電池正極材料制備方法,步驟如下:
(1)活性材料的合成。稱取原釩酸鈉0.2196g,硼酸1.2006g,草酸0.3636g,乙酸銅0.1518g,氫氧化鋰0.1531g,加入6ml蒸餾水,攪拌混合均勻,然后緩慢滴加0.5ml乙二胺,置于磁力攪拌器上攪拌加熱使反應物充分溶解,趁熱將反應混合液移入23.00ml的聚四氟乙烯內襯的反應釜中,在160℃下恒溫120個小時。從烘箱中取出反應釜使其自然冷卻,24小時后抽濾得到綠色正六邊形的片狀晶體。(按釩計算其產率約為68%)。
(2)活性材料的預處理。將晶體材料研磨成粉末,并將粉末置于120℃的真空干燥箱中干燥24小時,以便最大程度的去除材料中的水分。
(3)正極材料的制備。按照重量分數計,由以下組分按照所示比例制備而成,活性材料:80~85wt%,導電材料:10~15wt%,粘接材料:5~10wt%。所述正極材料為[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2,所述導電材料為導電炭,粘接材料為n-甲基-吡咯烷酮。
應用:以[li(h2o)]2{[li(h2o)]3[v6b20o39(oh)11]}(h2o)2、導電炭,粘結劑以7:2:1的質量比例混合均勻涂于鋁正極片,與鋰負極片組裝成扣式電池。
活性物質的單晶衍射解析
x-射線單晶衍射法是目前測定單晶結構最常用且有效的方法。本文的化合物是在福州大學物理化學國家重點學科公共測試中心的rigakur-axis-paridweissenbergeip衍射儀上,于293(2)k溫度下,采用石墨單色化的mo靶kα射線(λ=0.71073?)以ω-2θ掃描方式在一定范圍內進行晶體晶胞參數的測定和衍射強度數據的收集。然后,用直接法確定化合物中重原子的坐標,再用多輪差傅立葉合成法確定其它原子的坐標,對所有能進行各向異性的原子利用最小二乘法各向異性修正。化合物中的氫原子通過差傅立葉合成或者理論加氫所得,參與結構因子計算,但不參加結構精修。
活性物質的表征
(1)紅外光譜表征
化合物的紅外光譜是在物理化學國家重點學科perkin-elmerspectrum2000ft-ir光譜儀進行的。在室溫下,采用kbr壓片,掃描范圍400~4000cm-1,掃描10次。從圖2可以看出,3440cm-1,3220cm-1附近出現的寬吸收峰歸屬于νas(o-h)振動吸收峰。1031cm-1為bo4四面體中的δ(b-o)的振動吸收峰,777cm-1為v-oμ的反對稱伸縮振動,663cm-1為v-oμ的對稱伸縮振動峰。由于化學環境的不同,使一些特征峰出現較大的位移或分裂。νas(v=ot)特征吸收峰的峰位置受多方面因素的影響。v的氧化態對νas(v=ot)峰位置的影響比較明顯,隨著氧化態的升高,νas(v=ot)頻率越高。化合物中v為+4價,其νas(v=ot)峰位于930cm-1左右。
(2)紫外可見固體漫反射光譜表征
本發明中化合物的紫外-可見光譜是在我校國家化肥催化劑研究工程中心的perkin-elmerlambda900型紫外-可見光譜儀測試得到,掃描波長為200-800nm。從圖3可以看出,263nm,293nm兩個強的吸收譜帶為oμ→v之間的荷移躍遷峰。420nm、560nm和710nm附近出現了v(iv)的d-d躍遷。
正極材料的電化學性能測試與分析
(1)電池的循環伏安曲線的測試與分析
電池進行了循環伏安曲線(cv)的測試,電壓范圍為2~4.6v,掃描速度為1mv/s,從圖4上可以發現,2.6v附近出現了較平緩的還原峰,3.12v附近出現了較平緩的氧化峰,由于v(v)具有d0穩定的電子組態,v(v)到v(iv)的還原反應所需能量較高,影響活性物質氧化還原的可逆性,對應于放電過程中較緩慢的嵌鋰過程。
(2)電池的充分電測試與分析
圖5為電流密度30ma/g下電池的首次充放電曲線,電池具有較高的首次放電比容量(89.1mah/g)。圖5為電池在30ma/g電流密度下的充放電曲線,從圖中可以看出電池的首次放電比容量為89.1mah/g,與活性物質的理論比容量89.8mah/g非常接近。經過25次循環后電池比容量基本保持在35.4mah/g左右,可能由于化合物在氧化還原過程中結構發生變化,失去了連接簇單元的li+,剩下位于孔道中的li+,其剩下理論比容量為35.9mah/g,與實驗值非常接近。
(3)電池的交流阻抗測試與分析
圖6為電池進行了交流阻抗(eis)的測試,頻率范圍在0.01hz~100khz,振幅為5mv,從圖上可以發現,eis譜包含一個圓弧和一條斜線,斜線反應了li+在活性材料內部的擴散電阻;圓弧代表電池的內阻,對應氧化還原反應阻抗
總之,本發明的新型材料完全具備成為鋰電池正極材料的條件,為新型鋰離子電池正極材料找到了一個新的方向,而且一步水熱合成法也為鋰電池正極材料的研究提供了一種新的合成途徑。
表1化合物的晶體學數據
- 還沒有人留言評論。精彩留言會獲得點贊!