鋰離子電池及其制造方法與流程
本申請公開了鋰離子電池及其制造方法。
背景技術:
在專利文獻1中,公開了一種使用了lini0.5mn1.5o4作為正極活性物質的非水電解液鋰離子電池。lini0.5mn1.5o4的相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的高電位。通過使用這樣的高電位型的正極活性物質,可容易地提高鋰離子電池的工作電壓。但是,在使用了高電位型的正極活性物質的情況下,存在這樣的問題:因非水電解液的分解而在電池內產生氣體。
為了解決該問題,對鋰離子電池的正極進行了各種研究。例如,在專利文獻2~4中,提出了用含鈮氧化物等被覆正極活性物質的表面。另外,在專利文獻5中,提出了在構成正極的正極合劑中混合含鈮氧化物。根據專利文獻2~5所公開的技術,認為利用含鈮氧化物等能減小正極活性物質與非水電解液直接接觸的面積,抑制了正極活性物質與非水電解液的反應,能抑制非水電解液的分解。或者,認為在正極合劑中,含鈮氧化物作為負催化劑起作用,正極活性物質的活性下降,能抑制非水電解液的分解。
現有技術文獻
專利文獻1:特開2012-124026號公報
專利文獻2:特開2015-144108號公報
專利文獻3:特開2015-204256號公報
專利文獻4:特開2011-070789號公報
專利文獻5:特開2004-319268號公報
技術實現要素:
發明所要解決的課題
專利文獻2~5任一者都公開了抑制正極活性物質與非水電解液的反應的技術。但是,本發明人新發現,高電壓型的鋰離子電池中的非水電解液的分解不僅僅由其與正極活性物質的反應引起。即認為,為了進一步抑制由非水電解液的分解引起的氣體的產生,需要專利文獻2~5所公開的那樣的“正極活性物質的表面修飾”、“正極合劑中的負催化劑的混合”以外的方法。
鑒于以上,在本申請中,公開了一種可抑制由非水電解液的分解引起的氣體的產生的鋰離子二次電池及其制造方法。
用于解決課題的手段
本發明人推定,在使用了高電位型的正極活性物質的鋰離子電池中,由于以下機理,非水電解液分解并產生氣體。
(1)在正極合劑中,存在與正極活性物質相接觸的導電材料。
(2)在正極活性物質處于高電位時,與該正極活性物質相接觸的導電材料也處于高電位。
(3)在處于高電位的導電材料與非水電解液相接觸時,在導電材料的表面,非水電解液分解,產生氣體。
在以往完全沒有考慮過上述的推定機理。本發明人基于上述的推定機理反復進行了各種研究,結果發現,通過用含鈮氧化物被覆導電材料的表面,實際上能顯著抑制氣體的產生。
基于以上的認識,作為用于解決上述課題的手段之一,本申請公開了一種鋰離子電池,其具備正極、非水電解液和負極,所述正極包含導電材料、被覆所述導電材料的表面的層狀含鈮氧化物、以及相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質。
“被覆所述導電材料的表面的層狀含鈮氧化物”是指含鈮氧化物以順著導電材料的表面形狀的方式連續被覆導電材料的表面。即,是指膜狀的含鈮氧化物被覆導電材料的表面的形態、含鈮氧化物以層狀在導電材料的表面沉積的形態。但是,含鈮氧化物不需要被覆導電材料的全部表面,一部分也可以成為不連續的層。就這一點而言,本公開的鋰離子電池與以往的電池(正極活性物質被表面修飾的形態,或導電材料和含鈮氧化物被單純混合的形態)明顯不同。
“含鈮氧化物”是指包含鈮作為構成氧化物的元素。在含鈮氧化物中,除了鈮和氧以外,可以包含鈮和氧以外的元素。
“相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質”是指含鋰氧化物活性物質的鋰的吸留和放出的電位的一部分相對于金屬鋰的氧化還原電位成為4.5v以上。即,可以說,含鋰氧化物活性物質為鋰離子電池的正極活性物質、且在4.5v(相對于li/li+)以上具有電位平坦部。
“含鋰氧化物”是指包含鋰作為構成氧化物的元素。“含鋰氧化物”只要是相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的活性物質,關于鋰及氧以外的構成要素、組成比就不特別限定。
在本公開的鋰離子電池中,優選所述層狀含鈮氧化物的厚度為0.4nm以上。
在本公開的鋰離子電池中,優選所述層狀含鈮氧化物的厚度為0.4nm以上5nm以下。
在本公開的鋰離子電池中,優選所述導電材料包含碳材料。
作為用于解決上述課題的手段之一,本申請公開了一種鋰離子電池的制造方法,該制造方法具備:第1工序,用層狀含鈮氧化物被覆導電材料的表面來形成復合體;第2工序,將所述復合體與相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質進行混合來得到正極合劑;第3工序,使用所述正極合劑來制作正極;和第4工序,使用所述正極、非水電解液和負極來制作發電元件。
在本公開的制造方法中,優選在所述第1工序中,通過原子層沉積法(ald)、用所述層狀含鈮氧化物被覆所述導電材料的表面。
發明效果
根據本公開的鋰離子電池,可抑制由非水電解液的分解引起的氣體的產生。
附圖說明
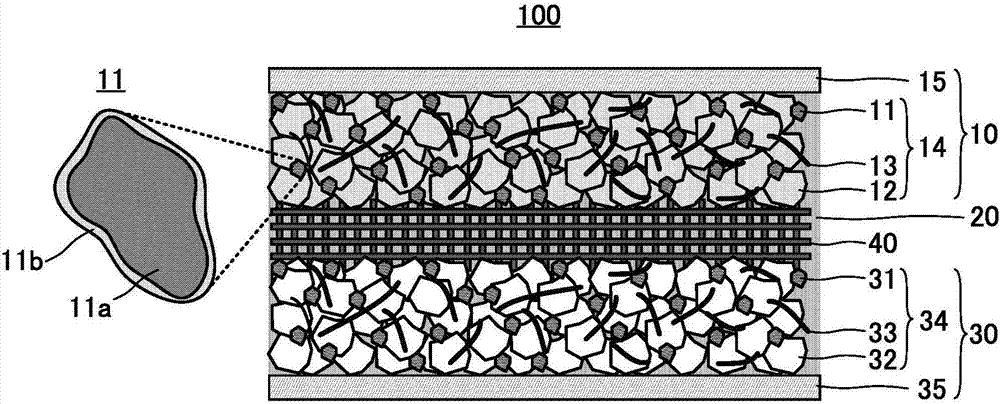
圖1是用于說明鋰離子電池100的構成的示意圖。
圖2是用于說明鋰離子電池的制造方法(s100)的流程的圖。
圖3是示出實施例3中使用的復合體(導電材料及層狀含鈮氧化物)的斷面的haadf-stem圖像的圖。
圖4是示出實施例3中使用的復合體(導電材料及層狀含鈮氧化物)的表面的haadf-stem圖像及元素分析結果的圖。
附圖標記說明
100鋰離子電池
10正極
14正極合劑層
11復合體
11a導電材料
11b層狀含鈮氧化物
12含鋰氧化物活性物質
13粘合劑
15正極集電體
20非水電解液
30負極
34負極合劑層
31導電材料
32負極活性物質
33粘合劑
35正極集電體
40分隔體
具體實施方式
1.鋰離子電池100
圖1中公開的鋰離子電池100具備正極10、非水電解液20和負極30,正極10包含導電材料11a、被覆導電材料11a的表面的層狀含鈮氧化物11b、以及相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質12。
1.1.正極10
1.1.1.導電材料11a
正極10包含導電材料11a。作為導電材料11a,可使用包含氣相生長碳纖維、乙炔黑(ab)、科琴黑(kb)、碳納米管(cnt)、碳納米纖維(cnf)等碳材料的導電材料、包含可耐受非水電解液鋰離子電池使用時的環境的金屬材料的導電材料。特別地,優選包含碳材料的導電材料。導電材料11a可以僅單獨使用1種,也可以混合2種以上來使用。
導電材料11a優選為粒子狀或纖維狀。在導電材料11a為粒子狀的情況下,優選其一次粒徑為5nm以上100nm以下,優選長寬比(aspectratio)不到2。粒子狀的導電材料11a的一次粒徑的下限更優選為10nm以上,進一步優選為15nm以上,上限更優選為80nm以下,進一步優選為65nm以下。這是由于通過使用這樣的粒子狀的導電材料11a,能使正極10的導電性進一步改善。在導電材料11a為纖維狀的情況下,優選其纖維直徑為10nm以上1μm以下,優選長寬比為20以上。纖維狀的導電材料11a的纖維直徑的下限優選為30nm以上,更優選為50nm以上,上限更優選為700nm以下,更優選為500nm以下。另外,纖維狀的導電材料的長寬比的下限優選為30以上,更優選為50以上。
正極10中的導電材料11a的含量不特別限定。例如,將導電材料11a、后述的含鋰氧化物活性物質12和粘合劑13的合計設為100質量%,包含優選2質量%以上、更優選為5質量%以上、進一步優選7質量%以上的導電材料11a。上限不特別限定,但優選為15質量%以下,更優選為13質量%以下,進一步優選為10質量%以下。只要導電材料11a的含量為這樣的范圍,就能得到離子傳導性及電子傳導性進一步優異的正極10。
1.1.2.層狀含鈮氧化物11b
正極10包含被覆導電材料11a的表面的層狀含鈮氧化物11b。例如,如圖1所示,正極10包含以順著導電材料11a的表面形狀的方式連續被覆導電材料11a的表面的含鈮氧化物11b。換句話說,膜狀的含鈮氧化物11b被覆著導電材料11a的表面。或者,含鈮氧化物11b以層狀沉積于導電材料11a的表面。這樣,正極10包含導電材料11a與含鈮氧化物11b的復合體11。
予以說明,也可以說圖1中示出的復合體11具有以導電材料11a為核、以含鈮氧化物11b為殼的核殼結構。但是,在復合體11中,含鈮氧化物11b不需要被覆導電材料11a的全部表面,一部分可以成為不連續的層。換句話說,在復合體11中,導電材料11a的表面的一部分可以露出。在這樣的情況下,優選導電材料11a的表面的50%以上被覆有層狀含鈮氧化物11b。更優選70%以上,進一步優選90%以上。
“含鈮氧化物”是包含鈮作為構成元素的氧化物。“含鈮氧化物”除了鈮和氧以外,可以包含鈮和氧以外的元素。例如,作為鈮和氧以外的元素,可以包含選自鋰、碳和氮中的1種以上的元素。
作為“含鈮氧化物”的具體例,可舉出氧化鈮、鈮酸鋰等。它們能進一步抑制由非水電解液的分解引起的氣體的產生。
層狀含鈮氧化物11b優選厚度為0.4nm以上。這是由于能進一步抑制由非水電解液的分解引起的氣體的產生。該厚度的上限不特別限定,即使為任意厚度,也能抑制由非水電解液的分解引起的氣體的產生。但是,根據本發明人的認識,在將層狀含鈮氧化物11b的厚度設為5nm以下的情況下,除了能抑制由非水電解液的分解引起的氣體的產生的效果以外,還取得了能減小正極10的電阻這樣的新效果。即,層狀含鈮氧化物11b特別優選厚度為0.4nm以上5nm以下。
予以說明,關于導電材料11a的表面是否被覆有層狀含鈮氧化物11b,可通過利用使用了掃描透射電子顯微鏡的高角度散射暗場法(haadf-stem法)取得haadf-stem圖像等來容易地確認。
1.1.3.含鋰氧化物活性物質12
正極10包含相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質12。含鋰氧化物活性物質12的鋰的吸留及放出的電位的一部分相對于金屬鋰的氧化還原電位成為4.5v以上。即,可以說,含鋰氧化物活性物質12為鋰離子電池100的正極活性物質、且在4.5v(相對于li/li+)以上具有電位平坦部。含鋰氧化物活性物質12可以僅單獨使用1種,也可以混合2種以上來使用。
“含鋰氧化物”是指包含鋰作為構成氧化物的元素。“含鋰氧化物”只要是相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的活性物質,其種類就不特別限定。例如,通過制成包含選自鎳、錳和鈷中的1種以上的元素作為鋰和氧以外的元素的含鋰氧化物,可構成這樣的高電位型的活性物質12。
作為“含鋰氧化物”的具體例,可舉出尖晶石型結構的鋰鎳錳復合氧化物、層狀結構的鋰鎳鈷錳氧化物或橄欖石型結構的鈷橄欖石等。特別優選尖晶石結構的鋰鎳錳復合氧化物。這是由于可制成電位更高的正極活性物質。
含鋰氧化物活性物質12的形狀不特別限定。例如,優選采用粒子狀、薄膜狀。在使含鋰氧化物活性物質12為粒子狀的情況下,其一次粒徑優選為1nm以上100μm以下。下限更優選為10nm以上,進一步優選為100nm以上、特別優選為500nm以上,上限更優選為30μm以下,進一步優選為10μm以下。予以說明,含鋰氧化物活性物質12可以是一次粒子彼此聚集而形成二次粒子。在該情況下,二次粒子的粒徑不特別限定,但通常為3μm以上50μm以下。下限優選為4μm以上,上限優選為20μm以下。如果含鋰氧化物活性物質12的粒徑為這樣的范圍,則能得到離子傳導性和電子傳導性進一步優異的正極10。
正極10中的含鋰氧化物活性物質12的含量不特別限定。例如,將上述的導電材料11a、含鋰氧化物活性物質12和后述的粘合劑13的合計設為100質量%,包含優選80質量%以上、更優選85質量%以上、進一步優選90質量%以上的含鋰氧化物活性物質12。上限不特別限定,但優選98質量%以下、更優選97質量%以下、進一步優選為95質量%以下。如果含鋰氧化物活性物質12的含量為這樣的范圍,則能得到離子傳導性和電子傳導性進一步優異的正極10。
予以說明,正極10可以是一部分包含含鋰氧化物活性物質12以外的正極活性物質。例如,可以包含相對于金屬鋰的氧化還原電位的上限電位不到4.5v(相對于li/li+)的正極活性物質。但是,從更容易提高鋰離子電池的工作電壓的觀點考慮,正極10所包含的正極活性物質中,優選80質量%以上為含鋰氧化物活性物質12。
1.1.4.粘合劑13
正極10任意地包含粘合劑13。粘合劑13可采用任一種在鋰離子電池中使用的粘合劑。例如,為丁苯橡膠(sbr)、羧甲基纖維素(cmc)、丙烯腈-丁二烯橡膠(abr)、丁二烯橡膠(br)、聚偏氟乙烯(pvdf)、聚四氟乙烯(ptfe)等。粘合劑13可以僅單獨使用1種,也可以混合2種以上來使用。正極10中的粘合劑13的含量不特別限定,例如設為與以往的鋰離子電池的正極所包含的粘合劑同等量即可。
正極10具備包含上述的導電材料11a、層狀含鈮氧化物11b和含鋰氧化物活性物質12的正極合劑層14。正極合劑層14的厚度不特別限定,例如優選為0.1μm以上1mm以下,更優選為1μm以上100μm以下。
1.1.5.正極集電體15
將上述的正極合劑層14與正極集電體15連接,由此可經由端子等(未圖示)從正極集電體15將電能取出至外部。正極集電體15包含含有選自例如cu、ni、al、v、au、pt、mg、fe、ti、co、cr、zn、ge、in中的一種或兩種以上的元素的金屬材料。正極集電體15的形狀不特別限定,可采用箔狀、網狀等各種形狀。
1.2.非水電解液20
鋰離子電池100具備非水電解液20。在非水電解液鋰離子電池中,通常在正極的內部、負極的內部以及在正極與負極之間存在非水電解液,由此確保了正極與負極之間的鋰離子傳導性。
非水電解液20通常含有鋰鹽。作為鋰鹽,例如可舉出lipf6、libf4、liclo4及liasf6等無機鋰鹽;和licf3so3、lin(cf3so2)2、lin(c2f5so2)2及lic(cf3so2)3等有機鋰鹽等。鋰鹽可僅單獨使用1種,也可以混合2種以上來使用。
非水電解液20通常含有溶解上述鋰鹽的非水溶劑。作為非水溶劑,例如可舉出碳酸亞乙酯(ec)、碳酸亞丙酯(pc)、碳酸亞丁酯(bc)等環狀酯(環狀碳酸酯);γ-丁內酯;環丁砜;n-甲基吡咯烷酮(nmp);1,3-二甲基-2-咪唑啉酮(dmi);碳酸二甲酯(dmc)、碳酸二乙酯(dec)、碳酸甲乙酯(emc)等鏈狀酯(鏈狀碳酸酯);乙酸甲酯、乙酸乙酯等乙酸酯類;2-甲基四氫呋喃等醚;等。非水溶劑可以僅單獨使用1種,也可以混合2種以上來使用。
非水電解液20中的鋰鹽的濃度例如優選在0.3mol/l以上5.0mol/l以下的范圍內,更優選在0.8mol/l以上1.5mol/l以下的范圍內。如果鋰鹽的濃度過低,則有可能高倍率時的容量下降。如果鋰鹽的濃度過高,則有可能粘度增高,低溫下的容量下降。予以說明,作為非水電解液20,也可以使用例如離子性液體等低揮發性液體。
1.3.負極30
負極30采用與以往的鋰離子電池的負極同樣的構成即可。例如,負極30包含導電材料31、負極活性物質32和粘合劑33。在負極30中,負極活性物質32是必須的,導電材料31和粘合劑33是任意的。在負極30中,通過這些負極活性物質層32等形成負極合劑層34,將該負極合劑層34與負極集電體35連接,可經由端子等(未圖示)從該集電體將電能取出至外部。負極活性物質32可吸留和放出鋰離子即可。例如,可舉出包含碳材料的活性物質、包含氧化物的活性物質和包含金屬的活性物質等。作為碳材料,例如可舉出石墨、中間相碳微球(mcmb)、高取向性石墨(hopg)、硬碳、軟碳等。作為氧化物,例如可舉出nb2o5、li4ti5o12和氧化硅等。作為金屬,例如可舉出li、in、al、si、sn和它們的合金等。負極活性物質32的形狀例如可設為粒子狀或薄膜狀。在負極活性物質32為粒子狀的情況下,優選其一次粒徑為1nm以上100μm以下。下限更優選為10nm以上,進一步優選為100nm以上,特別優選為500nm以上,上限更優選為30μm以下,進一步優選為10μm以下。予以說明,負極活性物質32可以是一次粒子彼此聚集而形成二次粒子。在該情況下,二次粒子的粒徑不特別限定,但通常為3μm以上50μm以下。下限優選為4μm以上,上限優選為20μm以下。負極合劑層34中的負極活性物質32的含量例如可設為40質量%以上99質量%以下。關于導電材料31、粘合劑33,適當地選擇并使用作為正極10的導電材料11a、粘合劑13而例示的導電材料、粘合劑即可。導電材料31和導電材料11a可以包含相互不同的材料。關于粘合劑33和粘合劑13也同樣。負極合劑層34中的導電材料31和粘合劑33的含量不特別限定。負極集電體35包含含有選自例如cu、ni、al、v、au、pt、mg、fe、ti、co、cr、zn、ge、in中的一種或兩種以上的元素的金屬材料。負極集電體35的形狀不特別限定,可采用箔狀、網狀等各種形狀。
1.4.分隔體40
鋰離子電池100可以在正極10與負極30之間具備分隔體40。在鋰離子電池100中,該分隔體40、正極10和負極30都浸漬在非水電解液20中。分隔體40可采用任一種以往的非水電解液鋰離子電池中所使用的分隔體。分隔體40例如為多孔膜即可。分隔體40可以由有機材料構成,也可以由無機材料構成。作為分隔體40的具體例,可舉出聚丙烯(pp)或聚乙烯(pe)的單層型的有機多孔膜,pp/pe/pp的層疊型的有機多孔膜等。分隔體40的厚度不特別限定,但優選為0.1μm以上1000μm以下,更優選為0.1μm以上300μm以下。
通過以上的正極10、非水電解液20和負極30構成發電元件,制成鋰離子電池100。鋰離子電池100由于正極10包含被覆導電材料11a的表面的層狀含鈮氧化物11b,因此能抑制在導電材料11a的表面由非水電解液的分解引起的氣體的產生。
2.鋰離子電池100的制造方法
鋰離子電池100例如可通過圖2中公開的方法來制造。圖2中公開的制造方法(s100)具備:第1工序(s1),用層狀含鈮氧化物11b被覆導電材料11a的表面來形成復合體11;第2工序(s2),將復合體11與相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質12進行混合來得到正極合劑;第3工序(s3),使用正極合劑來制作正極10;和第4工序(s4),使用正極10、非水電解液20和負極30來制作發電元件。
2.1.第1工序(s1)
在s1中,用層狀含鈮氧化物11b被覆導電材料11a的表面制成復合體11。s1可通過各種方法來實施。例如,可舉出通過原子層沉積法(ald)、化學氣相生長法(cvd)、濺射法等在導電材料11a的表面將含鈮氧化物11b進行成膜的方法,在導電材料11a的表面吹付(噴き付ける)含鈮氧化物的前體溶液之后使其干燥的方法等。其中優選ald。這是由于通過增加或減少前體供給和清洗(purge)的循環數,可容易控制層狀含鈮氧化物11b的厚度。根據ald,可在導電材料11a的表面均勻地設置厚度5nm以下的非常薄的層狀含鈮氧化物11b。
予以說明,在ald中,認為在導電材料11a的表面的官能團部分優先形成核。例如,在導電材料11a包含碳材料(例如乙炔黑)的情況下,認為在點在(分散存在)于導電材料11a的表面的邊緣部分(石墨烯結構的末端部分)優先進行核的形成和核的生長。因此,也認為難以在導電材料11a的整個表面將均勻的層進行成膜。實際上,在使氧化鋁沉積于乙炔黑的表面的情況下,形成氧化鋁點在于乙炔黑的表面這樣的狀態,形成間隙多的層。但是,本發明人進行了專心研究,結果,只有含鈮氧化物,令人意外地,對于碳材料那樣的邊緣部分點在的表面,可通過ald在該整個表面將厚度不到5nm的均勻的層進行成膜(參照圖3)。
2.2.第2工序(s2)
在s2中,將復合體11與相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質12進行混合來得到正極合劑。予以說明,除了復合體11和活性物質12以外,還可以混合粘合劑13。另外,可以進一步加入溶劑來形成漿料狀。復合體11、活性物質12和粘合劑13的混合比如上所述。s2可通過各種混合方法來實施。例如,作為混合方法,除了使用了研缽的基于手動的混合以外,也可以使用振動機、超聲波分散器、攪拌裝置等來進行機械混合。但是,如果過分增大s2中的混合能,則復合體11被破碎,導致含鈮氧化物11b從復合體11剝落。可以在考慮向復合體11賦予的能量的同時選擇混合方法。
2.3.第3工序(s3)
在s3中,使用正極合劑來制作正極10。在正極合劑為包含溶劑的漿料狀的情況下,使用刮刀等將該漿料涂覆于正極集電體15的表面,其后使其干燥,由此可容易地制作在正極集電體15的表面具備了正極合劑層14的正極10。另一方面,在正極合劑不包含溶劑的情況下,例如在正極合劑為粉體狀的情況下,通過將粉體與正極集電體15一起一邊任意地加熱一邊進行壓制成形,可容易地制作在正極集電體15的表面具備了正極合劑層14的正極10。
2.4.第4工序(s4)
在s4中,使用正極10、非水電解液20和負極30制作發電元件。例如,將正極10和負極30收容在電池殼體的預定部位。在此,可以用正極10和負極30夾持分隔體40,形成層疊體,將該層疊體收容在電池殼體的預定部位。然后,在殼體內填充非水電解液20以將正極10和負極30浸漬在非水電解液20中,由此可制作發電元件。其后,將電池殼體進行密封等,得到鋰離子電池100。
予以說明,關于非水電解液20、負極30的制作方法,與以往同樣。例如,可參照專利文獻1~5所公開的那樣的方法。在此省略詳細的說明。
實施例
1.鋰離子電池的制作
以下那樣地操作,制作了根據實施例1~7、參考例1和比較例1~3的鋰離子電池。
<實施例1>
(導電材料的被覆)
利用ald裝置(picosun公司制),在導電材料(乙炔黑,デンカ公司制,粒子狀:粒徑約50nm)的表面將氧化鈮進行成膜,得到了復合體。使用乙氧基鈮作為鈮源,使用水作為氧源。成膜時,使乙氧基鈮的溫度為200℃、使水的溫度為20℃、使反應槽的溫度為200℃。將乙氧基鈮的投入、吹掃、水的投入、以及吹掃設為1個循環(成膜速率:
(正極合劑的制作)
使用研缽,將復合體、含鋰氧化物活性物質(lini0.5mn1.5o4)混合,進一步添加溶解在n-甲基吡咯烷酮(nmp)中的聚偏氟乙烯(pvdf)粘合劑(クレハ公司制),使用攪拌器使其混合·分散,制作了正極合劑漿料。在正極合劑漿料中,將含鋰氧化物活性物質、復合體和粘合劑的質量比設為85:10:5。
(正極的制作)
使用刮刀,將正極合劑漿料涂覆于正極集電體(鋁箔,厚度15μm)的表面,在空氣中于約80℃下進行干燥以除去nmp,其后在120℃下真空干燥10小時。其后,將正極合劑層與正極集電體壓制以相互壓接,得到了正極。正極合劑層的厚度為約30μm。
(鋰離子電池的制作)
將正極、負極(石墨)和非水電解液(在將ec及emc以體積比3:7混合的混合溶劑中以濃度1mol/l溶解了作為鋰鹽的六氟磷酸鋰(lipf6)的溶液)分別封入層壓袋內,制作了鋰離子電池。
<實施例2~6>
除了使ald中的循環數變化為25循環、50循環、75循環、125循環、175循環以外,與實施例1同樣地操作,制作了復合體,與實施例1同樣地操作,制作了正極合劑、正極和鋰離子電池。在實施例2~6中,復合體中的層狀氧化鈮的厚度分別為約1nm、約2nm、約3nm、約5nm、約7nm。
<實施例7>
(導電材料的被覆)
利用ald裝置(picosun公司制),在導電材料(乙炔黑,デンカ公司制,粒子狀:粒徑約50nm)的表面將鈮酸鋰進行成膜,得到了復合體。使用乙氧基鈮作為鈮源,使用叔丁氧基鋰作為鋰源,使用水作為氧源。成膜時,將乙氧基鈮的溫度設為200℃、將叔丁氧基鋰的溫度設為140℃、將水的溫度設為20℃、將反應槽的溫度設為235℃。將乙氧基鈮的投入、吹掃、叔丁氧基鋰的投入、吹掃、水的加入、以及吹掃設為1個循環(成膜速率:
(正極合劑、正極和鋰離子電池的制作)
除了改變復合體之外,與實施例1同樣地操作,制作了正極合劑、正極和鋰離子電池。
<參考例1>
除了作為含鋰氧化物活性物質使用下述的復合活性物質以外,與實施例2同樣地操作,制作了正極合劑、正極和鋰離子電池。
(復合活性物質的制作)
在與實施例2同樣的條件下在含鋰氧化物活性物質的表面將氧化鈮進行成膜(25個循環),得到了復合活性物質。在復合活性物質中,層狀氧化鈮的厚度為約1nm。
<比較例1>
除了不進行導電材料的被覆以外,與實施例1同樣地操作,制作了正極合劑、正極和鋰離子電池。
<比較例2>
(導電材料的被覆)
利用ald裝置(picosun公司制),在導電材料(乙炔黑,デンカ公司制,粒子狀:粒徑約50μm)的表面用氧化鋁進行被覆,得到了復合體。使用三甲基鋁作為鋁源,使用水作為氧源。成膜時,將三甲基鋁的溫度設為20℃、將水的溫度設為20℃、將反應槽的溫度設為200℃。將三甲基鋁的投入、吹掃、水的投入、以及吹掃設為1個循環(成膜速率:
(正極合劑、正極和鋰離子電池的制作)
除了改變復合體之外,與實施例1同樣地操作,制作正極合劑、正極和鋰離子電池。
<比較例3>
除了將ald中的循環數設為30個循環以外,與比較例2同樣地操作,制作了復合體,與比較例2同樣地操作,制作了正極合劑、正極和鋰離子電池。
2.鋰離子電池的評價
關于制作的鋰離子電池,通過以下方法進行評價。
<復合體的表面狀態的觀察>
關于實施例3中使用的復合體,使用掃描透射電子顯微鏡(日本電子公司制),利用高角度散射暗場法(haadf-stem法)取得了haadf-stem圖像。將結果示于圖3、4。予以說明,圖3是對樹脂埋入后的復合體的斷面進行觀察得到的圖像。圖3(a)和圖3(b)只是觀察區域不同,都是實施例3中使用的復合體的斷面的haadf-stem圖像。圖4是對樹脂埋入前的復合體的斷面進行觀察得到的圖像。圖4(b)是對存在于由圖4(a)的箭頭表示的范圍的元素數進行分析得到的圖。圖4(b)的橫軸左端對應于箭頭的基端,橫軸右端對應于箭頭的前端。由圖4(b)可知復合體的“表面”存在的元素比。
在圖3、4中,在由白色表示的部分包含重金屬(nb)。如從圖3、4可知的那樣,通過ald能在導電材料的表面將層狀氧化鈮均勻地成膜而未使其聚集。關于根據實施例1、2、4~7和參考例1的復合體也是同樣的,能在導電材料的表面將層狀氧化鈮、層狀鈮酸鋰成膜而未使其聚集。
<充放電試驗>
將使鋰離子從正極脫離(放出)的過程作為“充電”,將使鋰離子插入(吸留)于正極的過程作為“放電”,使用充放電試驗裝置(北斗電工公司制,hj-1001sm8a)進行充放電試驗。將電流值設為1/3c,在溫度25℃下、在從3.5v至4.9v的范圍內重復充電和放電,將第三次循環的放電容量作為初始容量。其后,在將soc調整為60%后,以5c倍率放電10秒,從此時的曲線電壓差計算出電池電阻。將結果示于下述表1。
另外,在溫度60℃、電流值2c下、在從3.5v至4.9v的范圍內進行10個循環的充電和放電,從層壓袋的膨脹量估算在電池內產生的氣體量。將結果示于下述表1。
【表1】
如從表1中示出的結果可知的那樣,根據實施例1~7和參考例1的鋰離子電池與根據比較例1的鋰離子電池相比,能顯著抑制在電池的充電和放電時在導電材料的表面由非水電解液的分解引起的氣體的產生。另外,由實施例1~7可知,越增大層狀含鈮氧化物的厚度,氣體產生量變得越小,另一方面,單元(cell)電阻變得越大。作為單元電阻增大的原因,認為是由于導電材料的界面電子電阻增大,電子的供給慢,自導電材料的電子的供給變得律速(速率受控)。即,由實施例1~7的結果可知,在使層狀含鈮氧化物的厚度為0.4nm以上5.0nm以下的情況下,能抑制氣體的產生,同時將單位電阻維持得較低。另一方面,由參考例1的結果可知,通過用層狀含鈮氧化物不僅被覆導電材料而且還被覆正極活性物質的表面,能進一步抑制氣體產生量。但是,還可知在用層狀含鈮氧化物被覆了正極活性物質的表面的情況下,導致單元電阻過度地上升。
另外,由比較例1~3可知,即使在用氧化鋁被覆了導電材料的表面的情況下,也能抑制氣體的產生量。但是,在用氧化鋁進行被覆時,得不到用含鈮氧化物進行被覆時那樣程度的顯著效果。
如上所述,可知通過使用包含導電材料、被覆所述導電材料的表面的層狀含鈮氧化物、以及相對于金屬鋰的氧化還原電位的上限電位為4.5v(相對于li/li+)以上的含鋰氧化物活性物質的正極來構成鋰離子電池,能顯著抑制由在使用了高電位型活性物質時發生的非水電解液的分解引起的氣體的產生。
產業上的利用可能性
根據本發明的鋰離子電池可作為一次電池、二次電池在各種電源中使用。例如,可適合用作車載用的電源。
- 還沒有人留言評論。精彩留言會獲得點贊!