一種電極材料、其制備方法及用途與流程
本發明屬于二次電池和能源材料技術領域,涉及一種電極材料、其制備方法及用途,尤其涉及一種含有羥基苯磺酸和/或羥基苯磺酸鹽的有機電極材料、其制備方法及該電極材料在離子型電池的用途。
背景技術:
二十一世紀以來,能源問題已成為制約各國經濟發展的主要問題。煤、石油和天然氣等傳統化石能源是目前支撐社會發展的主要能源。但是,化石能源不僅儲量問題日漸突出,而且帶來了嚴重的環境污染。因此,發展清潔的可再生能源成為人類社會可持續發展的關鍵。在目前的儲能體系中,化學儲能電池因其高效便捷,無地域限制等特點脫穎而出,成為世界范圍內研究的熱點。
鋰離子電池由于能量密度大、循環壽命長、工作電壓高、無記憶效應和自放電小等優點在目前儲能材料市場中獨占鰲頭。而鈉離子電池鈉源豐富,可以從海水和鹽湖中提取,為電池的可持續發展提供了可能。目前,對于鋰離子和鈉離子電池的研究大部分集中在無機材料上,但是大部分無機材料生產成本高,資源有限且涉及環境污染問題,阻礙了其進一步的發展。而有機化合物具有種類繁多含量豐富、氧化還原電位調節范圍寬、能發生多電子反應以及容易循環等優點,成為了電池材料領域研究的新方向。
目前,對于鋰/鈉離子電池有機負極材料的研究有了一定的進展。Q.Deng等研究了有機小分子鹽2,5-二羥基對苯二甲酸二鋰鹽(Li2DHTP)以及對應的有機酸2,5-二羥基對苯二甲酸(DHTPA)作為鋰離子負極材料的電化學行為。Li2DHTP循環100圈后,容量保持在165mAh g-1,庫倫效率為98%,倍率性能較好,雖然DHTPA具有優異的Li+存儲能力,但是其循環穩定性不佳(Q.J.Deng et al,J.Electroanal.Chem.,761(2016)74–79)。Zhao等研究了對苯二甲酸鈉(Na2C8H4O4)的嵌鈉性能。在0.1~0.2V,0.1C倍率條件下該材料具有270mAhg-1的比容量。通過將材料與20%的科琴黑超導電碳(KB碳)進行球磨,能有效減小粒徑,增加其導電性。為了改善倍率性能,作者對Na2C8H4O4進行了Al2O3包覆,包覆后的材料能有效減少SEI膜的形成,有利于電極結構的保持,從而改善循環壽命。未處理的對苯二甲酸鈉初始容量為258mAh g-1,50次循環后衰減至192mAh g-1,包覆后的材料初始比容量為255mAh g-1,50次后保持在211mAh g-1(L.Zhao,J.Zhao,Y.S.Hu,H.Li,Z.Zhou,M.AMmand,L.Chen,Adv.Energy Mater.,2(2012)962–965)。但是上述材料依然存在比容量低和循環穩定性不佳的問題,為了適應高比能量和壽命長的鋰/鈉離子電池的發展需要,開發比容量高、循環穩定性好、簡單易得的新型鋰/鈉離子電池有機負極材料是離子電池發展并產業化的重要途徑和需求。
技術實現要素:
針對上述問題以及新型綠色有機電池的需要,本發明的目的是提供一種比容量高、循環穩定性好且簡單易得的有機電極材料、其制備方法及用途。本發明的有機電極材料既可以用于鋰離子電池又適用于鈉離子電池的制備,得到的鋰離子電池和鈉離子電池均表現出非常好的電化學性能,且該有機電極材料的制備方法簡單,易于實施,有利于推廣。
為達上述目的,本發明采用以下技術方案:
第一方面,本發明提供一種有機電極材料,所述有機電極材料中包含活性物質,所述活性物質為羥基苯磺酸、羥基苯磺酸鹽、苯磺酸、苯磺酸鹽、苯二磺酸或苯二磺酸鹽中的任意一種或至少兩種的混合物。
本發明中,有機電極材料為有機正極材料或有機負極材料中的任意一種,優選為有機負極材料。
優選地,以有機電極材料的總質量為100%計,所述活性物質的質量百分比為50%~90%,例如50%、52%、55%、56%、58%、60%、65%、68%、70%、72.5%、75%、77%、79%、81%、83.5%、85%、88%或90%等。
本發明所述“羥基苯磺酸”為本領域常用的羥基苯磺酸,對羥基的個數和位置,以及苯磺酸基的個數和位置不作限定,例如可以是4,5,6-三羥基苯-1,3-二磺酸、4,5-二羥基苯-1,3-二磺酸或對羥基苯磺酸等,優選為4,5,6-三羥基苯-1,3-二磺酸。
本發明所述“苯二磺酸”例如可以是1,3苯二磺酸等。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸的制備方法為:向1,2,3-三羥基苯中加入濃硫酸(即質量分數在70%以上的硫酸),室溫(即15~32℃)攪拌反應,充分析出白色固體后,過濾,干燥,得到白色粉末狀的4,5,6-三羥基苯-1,3-二磺酸。
本發明所述“羥基苯磺酸鹽”為本領域常用的羥基苯磺酸的金屬鹽,例如4,5,6-三羥基苯-1,3-二磺酸鹽、4,5-二羥基苯-1,3-二磺酸鹽和對羥基苯磺酸鹽等。
優選地,所述羥基苯磺酸鹽、苯磺酸鹽和苯二磺酸鹽獨立地選自各自的堿金屬鹽、堿土金屬鹽或IIIA族金屬鹽中的任意一種或至少兩種的組合,即羥基苯磺酸堿金屬鹽、羥基苯磺酸堿土金屬鹽、羥基苯磺酸IIIA族金屬鹽、苯磺酸堿金屬鹽、苯磺酸堿土金屬鹽、苯磺酸IIIA族金屬鹽、苯二磺酸堿金屬鹽、苯二磺酸堿土金屬鹽或苯二磺酸IIIA族金屬鹽中的任意一種或至少兩種的組合。
進一步優選地,所述羥基苯磺酸鹽為4,5,6-三羥基苯-1,3-二磺酸鹽,優選為4,5,6-三羥基苯-1,3-二磺酸堿金屬鹽、4,5,6-三羥基苯-1,3-二磺酸堿土金屬鹽或4,5,6-三羥基苯-1,3-二磺酸IIIA族金屬鹽中的任意一種或至少兩種的組合。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸堿金屬鹽的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與堿金屬鹽反應,充分析出白色固體后,過濾,干燥,得到白色粉末狀的4,5,6-三羥基苯-1,3-二磺酸堿金屬鹽。
優選地,4,5,6-三羥基苯-1,3-二磺酸堿金屬鹽的制備過程中,所述堿金屬鹽包括氯化鈉、溴化鈉、碘化鈉、碳酸鈉、碳酸氫鈉、硝酸鈉、硫酸鈉、磷酸鈉、磷酸氫二鈉、氯化鋰、溴化鋰、碘化鋰、碳酸鋰、碳酸氫鋰、硝酸鋰、硫酸鋰、磷酸鋰或磷酸氫二鋰中的任意一種或至少兩種的組合,但又不限于上述列舉的堿金屬鹽,其他可達到相同效果的堿金屬鹽也可用于本發明。
優選地,4,5,6-三羥基苯-1,3-二磺酸堿土金屬鹽的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與堿土金屬鹽反應,充分析出白色固體后,過濾,干燥,得到白色粉末狀4,5,6-三羥基苯-1,3-二磺酸堿土金屬鹽。
優選地,4,5,6-三羥基苯-1,3-二磺酸堿土金屬鹽的制備過程中,所述堿土金屬鹽包括氯化鎂、溴化鎂、碘化鎂、碳酸鎂、硝酸鎂、硫酸鎂或磷酸鎂中的任意一種或至少兩種的組合,但又不限于上述列舉的堿土金屬鹽,其他可達到相同效果的堿土金屬鹽也可用于本發明。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸堿金屬鹽的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與IIIA族金屬鹽反應,過濾,干燥,得到白色粉末狀的4,5,6-三羥基苯-1,3-二磺酸IIIA族金屬鹽。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸IIIA族金屬鹽的制備過程中,所述IIIA族金屬鹽包括氯化鋁、溴化鋁、碘化鋁、硝酸鋁、硫酸鋁中的任意一種或至少兩種的組合。
本發明中,4,5,6-三羥基苯-1,3-二磺酸鹽的化學組成為其中,M為金屬陽離子,n為金屬元素的自身特性所決定的金屬陽離子M具有的常規價態數(比如,堿金屬如Na的陽離子決定的常規價態數為1,則n=1;堿土金屬如Mg的陽離子決定的常規價態數為2,則n=2;IIIA族金屬如Al的陽離子決定的常規價態數為3,則n=3)。
優選地,M=Li,n=1;M=Na,n=1;M=Mg,n=2;M=Al,n=3。
作為本發明所述有機電極材料的優選技術方案,所述羥基苯磺酸鹽為4,5,6-三羥基苯-1,3-二磺酸二鈉和/或4,5,6-三羥基苯-1,3-二磺酸二鋰。
所述“4,5,6-三羥基苯-1,3-二磺酸二鈉和/或4,5,6-三羥基苯-1,3-二磺酸二鋰”指:可以是4,5,6-三羥基苯-1,3-二磺酸二鈉,也可以是4,5,6-三羥基苯-1,3-二磺酸二鋰,還可以是4,5,6-三羥基苯-1,3-二磺酸二鈉和4,5,6-三羥基苯-1,3-二磺酸二鋰的混合物。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸二鈉的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與鈉鹽反應,充分析出白色固體后,過濾,干燥,得到4,5,6-三羥基苯-1,3-二磺酸二鈉。
優選地,所述鈉鹽包括但不限于氯化鈉、溴化鈉、碘化鈉、碳酸鈉、碳酸氫鈉、硝酸鈉、硫酸鈉、磷酸鈉或磷酸氫二鈉中的任意一種或至少兩種的混合物,其他可達到相同效果的鈉鹽也可用于本發明。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸二鋰的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與鋰鹽反應,充分析出白色固體后,過濾,干燥,得到4,5,6-三羥基苯-1,3-二磺酸二鋰。
優選地,所述鋰鹽選自但不限于氯化鋰、溴化鋰、碘化鋰、碳酸鋰、碳酸氫鋰、硝酸鋰、硫酸鋰、磷酸鋰或磷酸氫二鋰中的任意一種或至少兩種的混合物,其他可達到相同效果的鋰鹽也可用于本發明。
作為本發明所述有機電極材料的又一優選技術方案,所述羥基苯磺酸鹽為4,5,6-三羥基苯-1,3-二磺酸鎂鹽。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸鎂鹽的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與鎂鹽反應,充分析出白色固體后,過濾,干燥,得到4,5,6-三羥基苯-1,3-二磺酸鎂鹽。
優選地,所述鎂鹽選自但不限于氯化鎂、溴化鎂、碘化鎂、硝酸鎂或硫酸鎂中的任意一種或至少兩種的混合物,其他可達到相同效果的鎂鹽也可用于本發明。
作為本發明所述有機電極材料的另一優選技術方案,所述羥基苯磺酸鹽為4,5,6-三羥基苯-1,3-二磺酸鋁鹽。
優選地,所述4,5,6-三羥基苯-1,3-二磺酸鋁鹽的制備方法為:將4,5,6-三羥基苯-1,3-二磺酸溶于水,與鋁鹽反應,充分析出白色固體后,過濾,干燥,得到4,5,6-三羥基苯-1,3-二磺酸二鋁。
優選地,所述鋁鹽選自但不限于氯化鋁、溴化鋁、碘化鋁、硝酸鋁、硫酸鋁中的任意一種或至少兩種的混合物,其他可達到相同效果的鋁鹽也可用于本發明。
作為本發明所述有機電極材料的優選技術方案,所述有機電極材料中還包含導電添加劑。
優選地,所述導電添加劑包括導電石墨、乙炔黑、炭納米管、super P、或科琴黑(又名KB碳)中的任意一種或至少兩種的組合,但又不限于上述列舉的導電添加劑,其他本領域常用的導電添加劑也可用于本發明。
優選地,以有機電極的總質量為100%計,所述導電添加劑的質量百分比小于或等于50%,例如為50%、45%、42%、40%、35%、30%、38%、24%、20%、15%、12%、10%或5%等。
優選地,所述有機電極的原料組分中還包含粘結劑。
優選地,所述粘結劑為聚偏氟乙烯(Polyvinylidene fluoride,PVDF)。
優選地,以有機電極的總質量為100%計,所述粘結劑的質量百分比小于或等于50%,例如為50%、43%、40%、35%、30%、35%、30%、25%、20%、15%、13%、9%或5%等。
第二方面,本發明提供一種有機電極,所述有機電極的原料組分中包含第一方面所述的有機電極材料。
“所述有機電極的原料組分”指:制備有機電極使用的原料。
本發明的有機電極為有機正極或有機負極。
第三方面,本發明提供如第二方面所述的有機電極的制備方法,所述方法包括以下步驟:在持續研磨的研缽中,分別加入活性物質、導電添加劑和溶有粘結劑的N-甲基吡咯烷酮溶液,繼續研磨至得到均勻的漿料,將漿料涂于金屬箔上,得到有機電極。
第四方面,本發明提供如第二方面所述有機電極的用途,所述有機電極用于離子型電池,優選作為鋰離子電池或鈉離子電池的有機電極。
與已有技術相比,本發明具有如下有益效果:
(1)本發明提供了一種全新的有機電極材料,為電極材料帶來了新的研究范圍和研究方向。其既可以用于制備鋰離子電池的電極,又可以用于制備鈉離子電池的電極,其不同于傳統的有機硫化物、有機自由基化合物及有機共軛羰基化合物等,應用于鋰/鈉離子電池的電極,可以表現出非常好的嵌脫鋰/鈉的性能,倍率性能優良,充放電比容量高,且穩定性高,以羥基苯磺酸作為活性物質制備得到的鋰離子電池的首次放電容量可達2272mAh g-1;二圈庫倫效率可達97%;在100mA g-1的電流密度下循環100圈庫倫效率可達100%,放電容量為924mAh g-1,放電容量保持率達70%;2Ag-1的大電流密度進行充放電,容量可以達到780mAh g-1,倍率性能較好。以羥基苯磺酸作為有機電極材料制備得到的鈉離子電池的首次放電容量可達1505mAh g-1,二圈庫倫效率可達86%,循環100圈(前10圈的電流密度為10mA g-1,后90圈的電流密度為50mA g-1)庫倫效率可達98%,放電容量為500mAh g-1,放電容量保持率可達72%,倍率性能較好;5Ag-1的大電流密度進行充放電,容量可以達到195mAh g-1,倍率性能較好。以羥基苯磺酸鹽作為有機電極材料制備得到的鋰離子電池的首次放電容量在362mAh g-1以上,二圈庫倫效率在72%以上。
(2)本發明的有機電極材料的制備方法簡單,工藝易控,制備電極材料的原料儲藏豐富,成本低廉,且對環境沒有危害,滿足可持續發展的要求,且適于工業化生產,具有廣闊的應用前景。
附圖說明
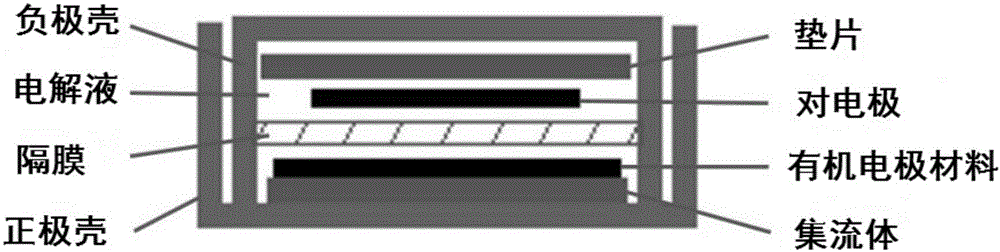
圖1為本發明的高性能有機鋰離子電池或有機鈉離子半電池的結構示意圖,其中的有機電極材料包含活性物質、導電添加劑以及粘結劑。
圖2a、圖2b和圖2c分別為采用實施例一中的C6H6O9S2負極片制成的鋰離子半電池的恒電流充放電曲線、充放電循環曲線以及倍率性能曲線;
其中,圖2b中的左箭頭對應左側縱坐標,右箭頭對應右側縱坐標。
圖3a、圖3b和圖3c分別為采用實施例一中的C6H6O9S2負極片制成的鈉離子半電池的恒電流充放電曲線、充放電循環曲線以及倍率性能曲線;
其中,圖3b中的左箭頭對應左側縱坐標,右箭頭對應右側縱坐標。
圖4為采用實施例二中的C6H4O9S2Li2負極片制成的鋰離子半電池的恒電流充放電曲線。
圖5為采用實施例二中的C6H4O9S2Li2負極片制成的鈉離子半電池的恒電流充放電曲線。
圖6為采用實施例三中的C6H4O9S2Na2負極片制成的鋰離子半電池的恒電流充放電曲線。
圖7為采用實施例三中的C6H4O9S2Na2負極片制成的鈉離子半電池的恒電流充放電曲線。
具體實施方式
下面結合附圖并通過具體實施方式來進一步說明本發明的技術方案。
實施例一
C6H6O9S2的制備:
稱量60mmol的1,2,3-三羥基苯,倒入反應瓶中,加入200mL的濃硫酸,得到白色固體。室溫下攪拌48h使其反應充分。過濾,干燥得到C6H6O9S2白色粉末。
C6H6O9S2負極片的制備:
以C6H6O9S2作為有機負極材料,稱量120mg的C6H6O9S2粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40min,然后涂于銅箔上制備得到C6H6O9S2負極片。
鋰離子半電池的組裝:
將制備的C6H6O9S2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H6O9S2為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1mol L-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鋰離子半電池結構參見圖1,當圖1為鋰離子半電池時,對電極為鋰片。
鈉離子半電池的組裝:
將制備的C6H6O9S2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H6O9S2為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
將上述組裝的鋰離子電池進行放電容量、循環性能以及倍率性能測試,測試條件為:在100mAg-1的電流密度以及3~0.01V的充放電范圍。測得恒電流充放電曲線如圖2a所示,充放電循環曲線如圖2b所示,倍率性能曲線如圖2c所示。
由圖2a可以看出,首次放電容量為2272mAh g-1,首次充電容量為1434mAhg-1;第二圈的放電容量為1397mAh g-1,第二圈的充電容量為1355mAh g-1,庫倫效率=第二圈充電容量/第二圈放電容量,為97%。
由圖2b可以看出,100mAg-1的電流密度下循環100圈后,放電容量為924mAh g-1,充電容量為924mAh g-1,庫倫效率=放電容量/充電容量,為100%,放電容量保持率達70%。
由圖2c可以看出,2Ag-1的大電流密度進行充放電,容量可以達到780mAhg-1,倍率性能較好。
將上述組裝的鈉離子半電池進行放電容量、循環性能以及倍率性能測試,測試條件為:在10mAg-1的電流密度以及3~0.01V的充放電范圍。測得恒電流充放電曲線如圖3a所示,充放電循環曲線如圖3b所示,倍率性能曲線如圖3c所示。
由圖3a可以看出,首次放電容量為1505mAh g-1,首次充電容量為1003mAhg-1;第二圈的放電容量為992mAh g-1,第二圈的充電容量為853mAh g-1,庫倫效率=充電容量/放電容量,為86%。
由圖3b可以看出,先在10mAg-1的電流密度循環10圈再在50mAg-1的電流密度循環90圈后,庫倫效率為98%,放電容量保持率達72%。
由圖3c可以看出,5Ag-1的大電流密度進行充放電,容量可以達到195mAhg-1,倍率性能良好。
實施例二
C6H4O9S2Li2的制備:
稱量10mmol實施例一合成的C6H6O9S2,加入5mL的蒸餾水,室溫下攪拌2min使其溶解,繼續加入20mL的飽和氯化鋰溶液,攪拌5min,出現白色固體,繼續攪拌12h,使其反應充分,過濾,干燥,得到C6H4O9S2Li2。
C6H4O9S2Li2負極片的制備:
以C6H4O9S2Li2作為有機負極材料,稱量120mg的C6H4O9S2Li2粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40min,然后涂于銅箔上制備得到C6H4O9S2Li2負極片。
有機鋰離子半電池的組裝:
將制備的C6H4O9S2Li2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O9S2Li2為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1mol L-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鋰離子電池結構參見圖1。當圖1為鋰離子電池時,對電極為鋰片。
有機鈉離子半電池的組裝:
將制備的C6H4O9S2Li2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O9S2Li2為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
圖4為采用C6H4O9S2Li2負極片制成的鋰離子半電池的恒電流充放電曲線,可以看出在100mA g-1的電流密度和3~0.01V的充放電范圍條件下,首次放電容量為675mAh g-1,首次充電容量為392mAh g-1;第二圈的放電容量為409mAhg-1,第二圈的充電容量為391mAh g-1,庫倫效率=充電容量/放電容量,為96%。
從圖5為采用C6H4O9S2Li 2負極材片制成的鈉離子半電池的恒電流充放電曲線,可以看出在10mAg-1的電流密度和3~0.01V的充放電范圍條件下,首次放電容量為461mAh g-1,首次充電容量為167mAh g-1;第二圈的放電容量為227mAh g-1,第二圈的充電容量為174mAh g-1,庫倫效率=充電容量/放電容量,為77%。
實施例三
C6H4O9S2Na2的制備:
稱量10mmol實施例一合成的C6H6O9S2,加入5mL的蒸餾水,室溫下攪拌2min使其溶解,繼續加入20mL的飽和氯化鈉溶液,攪拌5min,出現白色固體,繼續攪拌12h,使其反應充分,過濾,干燥,得到C6H4O9S2Na2。
C6H4O9S2Na2負極片的制備:
以C6H4O9S2Na2作為有機負極材料,稱量120mg的C6H4O9S2Na2粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40分鐘,然后涂于銅箔上制備得到C6H4O9S2Na2負極片。
有機鋰離子半電池的組裝:
將制備的電極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O9S2Na2為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1molL-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鋰離子半電池結構參見圖1。當圖1為鋰離子半電池時,對電極為鋰片。
有機鈉離子半電池的組裝:
將制備的C6H4O9S2Li2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O9S2Li2為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
圖6為采用C6H4O9S2Na2負極片制成的鋰離子半電池的恒電流充放電曲線,可以看出在100mAg-1的電流密度和3~0.01V的充放電范圍的條件下,首次放電容量為366mAh g-1,首次充電容量為176mAh g-1;第二圈的放電容量為188mAh g-1,第二圈的充電容量為170mAh g-1,庫倫效率=充電容量/放電容量,為90%。
圖7為采用C6H4O9S2Na2負極片制成的鈉離子半電池的恒電流充放電曲線,可以看出在10mAg-1的電流密度和3~0.01V的充放電范圍的條件下,首次放電容量為362mAh g-1,首次充電容量為142mAh g-1;第二圈的放電容量為215mAhg-1,第二圈的充電容量為156mAh g-1,庫倫效率=充電容量/放電容量,為72%。
實施例四
C6H4O9S2Mg的制備:
稱量10mmol實施例一合成的C6H6O9S2,加入5mL的蒸餾水,室溫下攪拌2min使其溶解,繼續加入20mL的飽和氯化鎂溶液,攪拌5min,出現白色固體,繼續攪拌12h,使其反應充分,過濾,干燥,得到C6H4O9S2Mg。
C6H4O9S2Mg負極片的制備:
稱量120mg的C6H4O9S2Mg粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40分鐘,然后涂于銅箔上制備C6H4O9S2Mg負極片。
有機鋰離子半電池的組裝:
將制備的C6H4O9S2Mg負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O9S2Mg為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1mol L-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。電池結構如圖1所示。鋰離子半電池結構參見圖1。當圖1為鋰離子半電池時,對電極為鋰片。
有機鈉離子半電池的組裝:
將制備的C6H4O9S2Mg負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O9S2Mg為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
實施例五
[C6H4O9S2]3Al2的制備:
稱量10mmol實施例一合成的C6H6O9S2,加入5mL的蒸餾水,室溫下攪拌2min使其溶解,繼續加入20mL的飽和氯化鋁溶液,攪拌5min,出現白色固體,繼續攪拌12h,使其反應充分,過濾,干燥,得到[C6H4O9S2]3Al2。
[C6H4O9S2]3Al2負極片的制備:
稱量120mg的C6H3O9S2Al粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40分鐘,然后涂于銅箔上制備[C6H4O9S2]3Al2負極片。
有機鋰離子半電池的組裝:
將制備的[C6H4O9S2]3Al2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H3O9S2Al為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1mol L-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。電池結構如圖1所示。鋰離子半電池結構參見圖1。當圖1為鋰離子半電池時,對電極為鋰片。
有機鈉離子半電池的組裝:
將制備的[C6H4O9S2]3Al2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,[C6H4O9S2]3Al2為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
實施例六
4,5-二羥基苯-1,3-二磺酸(C6H6O8S2)負極片的制備:
以C6H6O8S2作為有機負極材料,稱量120mg的C6H6O8S2粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40min,然后涂于銅箔上制備得到C6H6O8S2負極片。
鋰離子半電池的組裝:
將制備的C6H6O8S2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H6O8S2為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1mol L-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鋰離子半電池結構參見圖1,當圖1為鋰離子半電池時,對電極為鋰片。
鈉離子半電池的組裝:
將制備的C6H6O8S2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H6O8S2為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
實施例七
4,5-二羥基苯-1,3-二磺酸鈉(C6H4O8S2Na2)的制備:
稱量10mmol實施例一合成的C6H6O8S2,加入5mL的蒸餾水,室溫下攪拌2min使其溶解,繼續加入20mL的飽和氯化鈉溶液,攪拌5min,出現白色固體,繼續攪拌12h,使其反應充分,過濾,干燥,得到C6H4O8S2Na2。
C6H4O8S2Na2負極片的制備:
以C6H4O8S2Na2作為有機負極材料,稱量120mg的C6H4O8S2Na2粉末放入瑪瑙研缽中,研磨5min,稱量60mg的導電添加劑例如乙炔黑放入瑪瑙研缽中,繼續研磨5min,再加入溶有PVDF粘結劑的N-甲基吡咯烷酮溶液5mL(溶液濃度為15mg/mL),繼續研磨40分鐘,然后涂于銅箔上制備得到C6H4O8S2Na2負極片。
有機鋰離子半電池的組裝:
將制備的電極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O8S2Na2為工作電極,金屬鋰為對電極,Celgard 2300為隔膜。電解液為1molL-1的LiPF6(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鋰離子半電池結構參見圖1。當圖1為鋰離子半電池時,對電極為鋰片。
有機鈉離子半電池的組裝:
將制備的C6H4O8S2Na2負極片在氬氣手套箱(水、氧含量小于0.1ppm)中組裝電池,C6H4O8S2Na2為工作電極,金屬鈉為對電極,grade GF/F為隔膜。電解液為1mol L-1的NaClO4(溶劑為EC與DEC的混合物,EC與DEC的體積比是1:1)。鈉離子半電池結構參見圖1。當圖1為鈉離子半電池時,對電極為鈉片。
申請人聲明,本發明通過上述實施例來說明本發明的詳細方法,但本發明并不局限于上述詳細方法,即不意味著本發明必須依賴上述詳細方法才能實施。所屬技術領域的技術人員應該明了,對本發明的任何改進,對本發明產品各原料的等效替換及輔助成分的添加、具體方式的選擇等,均落在本發明的保護范圍和公開范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!