一種摻雜硅錳酸鋰/碳復合材料及制備方法與流程
本發明涉及一種硅錳酸鋰材料及制備方法,特別涉及一種摻雜硅錳酸鋰/碳復合材料及制備方法。
背景技術:
鋰離子電池的性能很大程度上取決于正極材料的選擇。目前應用于鋰離子電池的正極材料主要包括層狀過渡金屬氧化物(LiMO2)、尖晶石型錳酸鋰(LiMn2O4)和橄欖石型磷酸鐵鋰(LiFePO4)。上述的幾種材料都存在不同的缺陷:層狀過渡金屬氧化物、尖晶石型錳酸鋰和橄欖石型磷酸鐵鋰能量密度低、導電性差。研究能量密度高、安全性好、環境友好、成本低廉的鋰離子電池正極材料成為該領域目前的研究熱點。
硅酸錳鋰是一種新型的聚陰離子型鋰離子電池正極材料,因其具有理論比容量高(333mAhg-1)、能量密度高、原料來源廣泛、環境友好等優點而受到廣泛的關注。然而循環穩定性差、電子電導率和離子擴散率低的特點嚴重制約了其電化學性能的發揮,阻礙了進一步的研究和生產。
技術實現要素:
本發明旨在提供一種摻雜的硅錳酸鋰/碳復合材料及制備方法,使該復合材料在用于鋰離子電池正極材料時,以提升循環穩定性和導電性,并提升高倍率下的電化學性能。本發明采用以下方案:
一種硅錳酸鋰/碳復合材料,硅錳酸鋰中還摻有硼元素,材料的化學式為:Li2MnSiO4Bx/C,其中0<x≤0.10,其中碳占材料總質量的5%~20%;材料為正交晶系,晶格常數b值大于
經Rietveld精修,發現該摻雜復合材料的Pmn21空間群的含量大于95wt%,使得其材料電化學性能更佳。
制備上述硅錳酸鋰/碳復合材料的方法,包括以下步驟:
(Ⅰ)將泊洛沙姆(英文名:Poloxamer,聚氧乙烯聚氧丙烯醚嵌段共聚物)F127加入至無水乙醇或水中,形成溶液;將硅酸四乙酯和可溶于水的酸溶于水中,酸的加入量按照使體系初始pH值在1~3之內來計算,水解反應一定時間后,一般為20-50min,按摻雜硅錳酸鋰化合物的化學式的摩爾比向體系中加入相應量的水溶性錳鹽、水溶性鋰鹽和硼酸,混合至體系澄清,再向其中加入酚醛樹脂水溶液,形成溶膠;將形成的溶膠與泊洛沙姆F127溶膠混合,之后于30-40℃靜置至少12h,得到前驅體凝膠;將凝膠在空氣氣氛下100-150℃處理12-24h后,經粉碎得到前驅體粉末;水溶性錳鹽如:硝酸錳、氯化錳、硫酸錳、乙酸錳等,水溶性鋰鹽如:硝酸鋰、氯化鋰、硫酸鋰、乙酸鋰等。
(Ⅱ)在保護氣氛下熱處理步驟(Ⅰ)所制得的前驅體粉末,制得摻雜硅酸錳鋰/C復合材料。
制備方法在采用以下工藝條件時更優:
泊洛沙姆F127用量為每摩爾溶膠反應物中加入100~200克泊洛沙姆F127,其溶液的濃度為100~200g/L。
第Ⅰ步中的可溶于水的酸為鹽酸、硫酸、硝酸、磷酸或乙酸中的一種。加入酚醛樹脂水溶液的質量濃度為20%-50%,其加入量按照酚醛樹脂水溶液與硅酸有機酯的質量比(1~2):1之比例確定。
第Ⅱ步的熱處理工藝條件為,升溫速率1-5℃/min,保溫溫度為700℃,保溫時間8~12h;所述的保護氣氛為氮氣、氬氣、氫氣與氮氣混合氣氛或氫氣與氬氣混合氣氛。
與現有技術相比,本發明制備的硼摻雜硅酸錳鋰/碳復合正極材料,在硅酸錳鋰中摻雜硼系聚陰離子,使得晶體結構發生擇優生長,由于硼系聚陰離子的支柱效應使準層狀材料硅酸錳鋰的電化學循環穩定性得到了大幅提升。而B的摻雜影響了材料的晶格常數發生變化,這種變化有利于充放電過程中鋰離子的嵌入和脫出,同時硼的摻雜改性使活性物質中載流子增加,從而有利于導電性的提升,本發明的材料在高倍率下電化學性能表現較現有材料為優。
具體實施方式
實施例1
第1步:將1.6g泊洛沙姆F127在30℃下溶于10mL無水乙醇中待用。取0.01mol硅酸四乙酯和0.5mL 0.2mol/L的稀鹽酸溶液溶于1mL水中,攪拌進行水解反應直至溶液不再分層,硅酸四乙酯完全溶解,反應時間約為30min,隨后按摩爾比加入0.01mol的硝酸錳、0.02mol硝酸鋰和0.03g硼酸,攪拌一段時間至體系澄清,再向其中加入2.5g的20wt%酚醛樹脂水溶液,將形成的溶膠與之前制備的泊洛沙姆F127乙醇溶膠混合,30℃下攪拌1h得到穩定的溶膠體系,將上述溶膠體系于30℃靜置12h得到前驅體凝膠,再將凝膠在空氣氣氛下150℃處理24h后,磨碎得到前驅體粉末;
第2步:在氬氣氣氛保護下熱處理第1步制得的前驅體粉末,熱處理的工藝為以5℃/min速率升溫至700℃,保溫8h,自然冷卻。
經以上步驟制得的材料為:Li2MnSiO4B0.05/C復合材料,經XRD檢測分析,復合材料為正交晶系,晶格常數b值為經Rietveld精修分析,材料的Pmn21空間群的含量為96.52wt%;復合材料中碳的質量占材料總質量的8.8%。
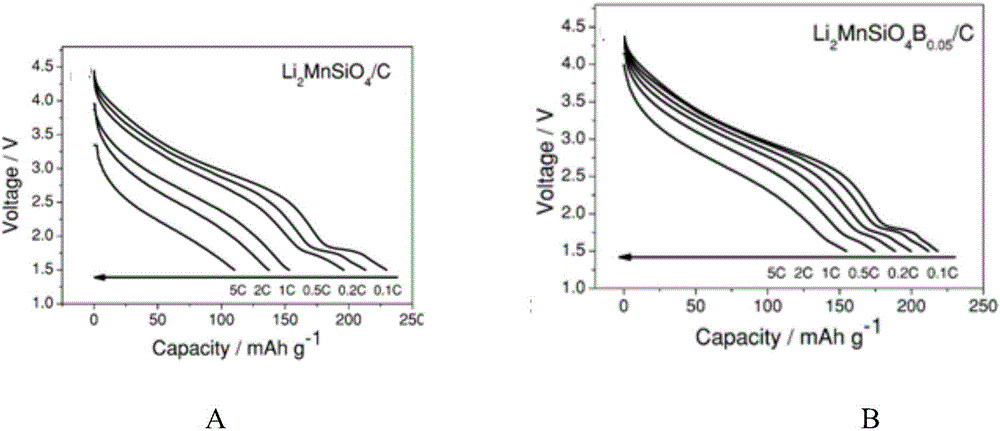
分別采用上述制備方法得到的Li2MnSiO4B0.05/C復合材料和不摻雜的Li2MnSiO4/C的復合材料作為正極,按現有方法組裝成鋰離子電池進行測試。在0.2C電流密度下的測試結果如圖1所示,不摻雜材料和摻雜材料的初始放電比容量分別為203mAhg-1和205.1mAhg-1,但在循環60圈后,比容量分別為25.5mAhg-1和85.7mAhg-1,采用本發明的方法的摻雜復合材料的循環性能有大幅提升。不摻雜材料和摻雜材料的分別制作的電池在低0.1C電流密度下恒流充電至4.6V——在4.6V恒壓充電2h后,依次0.2C、0.5C、1C、2C、5C下放電,其測試結果如圖2所示,其中圖2A為不摻雜復合材料的測試結果,圖2B為摻雜復合材料的測試結果。從圖中可以看出,兩種材料的電池在0.2C電流密度下的放電比容量分別為216.8mAhg-1和229.6mAhg-1;隨電流密度的增大,未摻雜材料制作的電池其放電比容量急劇降低,5C倍率下放電比容量只有110.3mAhg-1;而摻雜的復合材料制作的電池在5C倍率下放電比容量還可達到146.7mAhg-1,摻雜材料制作電池的倍率性能也得到了顯著的提高。
實施例2
第1步:將1g泊洛沙姆F127在30℃下溶于10mL水中待用。取0.01mol硅酸四乙酯和1mL 0.2mol/L的稀硝酸溶液溶于1mL水中,調整體系的pH至攪拌進行水解反應直至溶液不再分層,硅酸四乙酯完全溶解,反應時間約為50min,隨后按摩爾比加入0.01mol的硝酸錳、0.02mol硝酸鋰和0.06g硼酸,攪拌一段時間至體系澄清,再向其中加入2.5g 20wt%酚醛樹脂水溶液,將形成的溶膠與之前制備的泊洛沙姆F127水溶膠混合,30℃下攪拌1h得到穩定的溶膠體系,將上述溶膠體系于30℃靜置12h得到前驅體凝膠,再將凝膠在空氣氣氛下150℃處理24h后,磨碎得到前驅體粉末;
第2步:在氮氣和氫氣的混合氣氛保護下熱處理第1步制得的前驅體粉末,熱處理的工藝為以5℃/min速率升溫至700℃,保溫8h,自然冷卻。
經以上步驟制得的材料為:Li2MnSiO4B0.1/C復合材料,經XRD檢測分析,復合材料為正交晶系,晶格常數b值為經精修分析,材料的Pmn21空間群的含量為97.03wt%;復合材料中碳的質量占材料總質量的8.6%。
- 還沒有人留言評論。精彩留言會獲得點贊!