鈉離子二次電池的制作方法
本發明涉及含有作為正極活性物質的含鈉過渡金屬氧化物的鈉離子二次電池,所述含鈉過渡金屬氧化物可逆地負載鈉離子。
背景技術:
近年來,將自然能轉化為電能的技術日益受到關注。對作為能夠儲存大量電能的高能量密度電池的非水電解質二次電池的需求日益增加。在非水電解質二次電池之中,鋰離子二次電池具有重量輕和電動勢高的優點。然而,隨著非水電解質二次電池的市場擴大,鋰資源的價格日益上升。
含有便宜的鈉的鈉離子二次電池的開發已經取得了進展。含有含鈉離子的熔融鹽的熔融鹽電池也是有前景的。鈉離子二次電池使用鈉離子;因此,鈉離子二次電池生產成本低、熱穩定性好、相對容易確保安全性、并且適合在高溫下持續使用。
專利文獻1公開了含有作為正極活性物質的含鈉過渡金屬氧化物和作為電解質的含鈉離子的熔融鹽的鈉熔融鹽電池。
現有技術文獻
專利文獻
專利文獻1:日本特開2012-182087號公報
技術實現要素:
發明要解決的技術問題
在鈉離子二次電池如鈉熔融鹽電池中,通過正極和負極的活性物質反復吸藏和放出鈉離子而進行充放電。然而,在過充電狀態下,放出在正常充放電期間不從正極活性物質放出的、與不可逆容量相當的量的鈉離子。因此,負極活性物質不能完全吸藏很多鈉離子,從而容易造成鈉的析出。
因此,目的是抑制鈉離子二次電池在過充電期間的鈉析出。
解決技術問題的技術手段
本發明的一個方面涉及鈉離子二次電池,其包含含有正極活性物質的正極、含有負極活性物質的負極、置于所述正極與所述負極之間的隔膜、和電解質,
所述電解質為含有鈉離子的非水電解質,
所述正極活性物質含有可逆地吸藏和放出鈉離子的含鈉過渡金屬氧化物,
所述負極活性物質含有選自由可逆地吸藏和放出鈉離子的第一材料和與鈉合金化的第二材料構成的組中的至少一種,
在滿充電狀態的所述含鈉過渡金屬氧化物中,鈉原子對過渡金屬原子之比,即Na/MT滿足Na/MT≤0.3,且
所述負極的可逆容量和不可逆容量的總計Cnt對所述正極的可逆容量和不可逆容量的總計Cpt之比,即Cnt/Cpt滿足1≤Cnt/Cpt。
發明的效果
在所述鈉離子二次電池中,即使在過充電期間也抑制鈉的析出。
附圖說明
[圖1]為示意性顯示本發明的一種實施方式的鈉離子二次電池的縱剖面圖。
[圖2]為示意性顯示本發明的一種實施方式的包含鈉離子二次電池的充放電系統的方框圖。
具體實施方式
[發明的實施方式的說明]
首先,下面將列出和說明本發明的實施方式。
本發明的一種實施方式的鈉離子二次電池包含(1)含有正極活性物質的正極、含有負極活性物質的負極、置于所述正極與所述負極之間的隔膜、和電解質,所述電解質為含有鈉離子的非水電解質。所述正極活性物質含有可逆地吸藏和放出鈉離子的含鈉過渡金屬氧化物。所述負極活性物質含有選自由可逆地吸藏和放出鈉離子的第一材料和與鈉合金化的第二材料構成的組中的至少一種。在滿充電狀態的所述含鈉過渡金屬氧化物中,鈉原子對過渡金屬原子之比,即Na/MT滿足Na/MT≤0.3。所述負極的可逆容量和不可逆容量的總計Cnt對所述正極的可逆容量和不可逆容量的總計Cpt之比,即Cnt/Cpt滿足1≤Cnt/Cpt。
如上所述,在這種實施方式中,將在滿充電狀態下滿足比率Na/MT≤0.3的含鈉過渡金屬氧化物用作正極活性物質。換句話說,使用可以可逆地深度充放電的正極活性物質;因此,可以減小正極的不可逆容量。此外,負極的可逆容量和不可逆容量的總計Cnt大于等于正極的可逆容量和不可逆容量的總計Cpt。因此,即使在過充電期間與不可逆容量相當的量的鈉離子從正極活性物質完全放出,所述鈉離子仍在負極中穩定地吸藏(或插入)或合金化。因此,可以抑制鈉的析出。如上所述的正極活性物質的使用還可以增加能量密度。
滿充電狀態是指鈉離子二次電池的充電率(SOC)為100%的狀態,換句話說,鈉離子二次電池在進行可逆地充放電的范圍內被充電到預定的充電終止電壓的狀態。充電終止電壓是鈉離子二次電池的電池特性之一并由制造商根據例如活性物質的種類設定。鈉離子二次電池通常由電壓控制電路如充電器控制,以免充電到大于預定充電終止電壓的電壓(換句話說,超過100%的充電率)。然而,電池可以因為例如充電器的劣化或故障、和/或使用者使用不當而被過充電。在本發明的實施方式中,以在滿充電狀態下的比率Na/MT滿足Na/MT≤0.3的方式設定滿充電狀態(SOC:100%)。
當滿足Na/MT≤0.3時,Na/MT可以滿足Na/MT=0。在本發明中,正極活性物質中含有的過渡金屬氧化物根本上是含鈉過渡金屬氧化物。因此,即使在充放電改變Na/MT并且包含Na/MT=0的狀態的情況下,正極活性物質中含有的過渡金屬氧化物仍被稱為“含鈉過渡金屬氧化物”。
通過制作包含金屬鈉對電極的半電池并進行充放電可以確定負極的可逆容量和不可逆容量的總計Cnt。
可以將當所有鈉原子從正極放出時的容量估算為正極的可逆容量和不可逆容量的總計Cpt。在本說明書中,正極的不可逆容量可以包含緩沖容量。
(2)含鈉過渡金屬氧化物優選含有Ni、Ti和Mn作為過渡金屬原子。所述含鈉過渡金屬氧化物易于具有小的不可逆容量。
(3)在優選實施方式中,含鈉過渡金屬氧化物為由式(1):NaxTiyNizMn1-y-zO2(其中x因充放電而變動并且滿足0≤x≤0.67、0.15≤y≤0.2、0.3≤z≤0.35)表示的化合物。所述化合物尤其具有小的不可逆容量和高能量密度。
在式(1)中,因充放電而變動的x的范圍包括x=0。在這種情況下,由式(1)表示的化合物被稱為含鈉過渡金屬氧化物。x可以在0<x≤0.67的范圍內。
(4)優選比率Cnt/Cpt滿足1≤Cnt/Cpt≤1.3。在這種情況下,在提高耐過充電性的同時,抑制了無助于正常充放電(即可逆的充放電)的負極容量(和體積)的過度增加,從而進一步增加能量密度。
(5)當將與電解質中含有的鈉離子總量相當的容量表示為Ce時,Cnt優選滿足Cnt≥(Cpt+Ce)。過充電的進行可以使正極停止放出鈉離子,從而使得在正極進行副反應等。即使在正極進行副反應的同時,在負極仍發生充電反應,使得電解質中的鈉離子吸藏在負極中或與負極合金化。電解質含有大量鈉離子,從而引起鈉容易析出的狀態。即使在這種狀態下,當滿足Cnt≥(Cpt+Ce)時,仍有效抑制鈉的析出。
Ce相當于使電解質中含有的所有鈉離子被吸藏或合金化的負極(或正極)的容量。
(6)優選地,所述電解質含有70質量%以上的離子液體,并且所述離子液體含有陰離子和鈉離子。這樣的電解質也被稱為熔融鹽電解質。具有如上所述高離子液體含量的熔融鹽電解質具有高粘度,使得鈉離子不易移動(即,離子傳導性低)。因而,特別易于在電池中發生鈉的析出。在本發明的實施方式中,即使當使用易于發生顯著的鈉析出的熔融鹽電解質時,仍抑制過充電期間的鈉析出。因此,所述鈉離子二次電池(鈉熔融鹽電池)具有良好的耐過充電性。
熔融鹽電池是指包含熔融鹽電解質的電池。熔融鹽電解質是指主要由離子液體組成的電解質。在前述的實施方式中,所述熔融鹽電解質含有70質量%以上的離子液體。離子液體被定義為熔融狀態的鹽(熔融鹽)并且是含有陰離子和陽離子的液態離子性物質。鈉熔融鹽電池是指含有鈉離子傳導性的熔融鹽作為電解質的電池,鈉離子作為參與充放電反應的載流子。
(7)優選第一材料為選自由軟碳、硬碳和含堿金屬的鈦氧化物構成的組中的至少一種。優選第二材料含有選自由鋅、銦、錫、硅、磷、銻、鉛和鉍構成的組中的至少一種。在這些材料中,穩定地進行鈉離子的吸藏和放出。或者,穩定地進行鈉的合金化和去合金化。因此,這些材料適用于本發明實施方式的鈉離子二次電池。
[發明實施方式的詳情]
下面將適當地參考附圖對本發明實施方式的鈉離子二次電池的具體例子進行說明。本發明不限于這些例子。本發明旨在包括在權利要求的范圍內和與所述范圍等價的含義內的任何修改。
鈉離子二次電池包括正極、負極、置于正極與負極之間的隔膜、和含有鈉離子的電解質。
下面將進一步對鈉離子二次電池的構成要素進行詳細說明。
(正極)
(正極活性物質)
正極中的正極活性物質含有含鈉過渡金屬氧化物。由電化學地吸藏和放出(或插入和脫離)鈉離子的法拉第反應提供所述含鈉過渡金屬氧化物的容量。在所述含鈉過渡金屬氧化物處于充電率(SOC)為100%的狀態下,比率Na/MT滿足Na/MT≤0.3。Na/MT為在處于充電率(SOC)為100%的狀態下的含鈉過渡金屬氧化物中的鈉原子對過渡金屬原子之比。
例如,可以將亞鉻酸鈉(NaCrO2)用作在鈉離子二次電池中可逆地吸藏和放出鈉離子的正極活性物質。然而,在亞鉻酸鈉的情況下,即使以在進行可逆的充放電的范圍內使比率Na/MT最小化的方式來設定滿充電狀態(SOC=100%),所述比率Na/MT在充電率(SOC)為100%的狀態下也為約0.5。所述活性物質具有相對大的不可逆容量。因此,在過充電期間容易放出大量鈉離子,使得易于發生顯著的鈉析出。為了可靠地防止在過充電期間的鈉析出,負極需要具有與正極的不可逆容量相當的容量。如果為了達到正極與負極之間的容量平衡而過度增加負極的容量,則能量密度顯著減少。因此通常將負極容量設定為正極的可逆容量的約1.1倍至約1.2倍是現實的。
相比之下,在本發明的實施方式中,使用含有在充電率(SOC)為100%的狀態下比率Na/MT為0.3以下的含鈉過渡金屬氧化物的正極活性物質,即不可逆容量小的正極活性物質。因此,在過充電期間從正極活性物質放出的鈉離子的量減少。即使不使用過大的負極,也抑制鈉離子的析出。此外,上述含鈉過渡金屬氧化物的使用也增加了可逆的充放電的深度,從而增加能量密度。
理論上,比率Na/MT隨著含鈉過渡金屬氧化物中的過渡金屬原子的比率的增加而相對降低。然而,事實上,含鈉過渡金屬氧化物中的過渡金屬原子的比率基本上恒定。因此,比率Na/MT(特別是在P2型層狀晶體結構或O3型層狀晶體結構的情況下)可以被認為是含鈉過渡金屬氧化物中的Na的比率。
在充電率(SOC)為100%的狀態下,比率Na/MT為0.3以下并且可以為0.2以下或0.1以下。當比率Na/MT減小時,含鈉過渡金屬氧化物的不可逆容量(進而正極活性物質和正極的不可逆容量)減小,因此提高抑制過充電期間的鈉析出的效果。此外,能量密度增加。在充電率(SOC)為100%的狀態下比率Na/MT滿足0≤Na/MT并且可以滿足0<Na/MT、0.05≤Na/MT或0.1≤Na/MT。所述上限值和下限值可以自由組合在一起。在充電率(SOC)為100%的狀態下比率Na/MT可以滿足0≤Na/MT≤0.3、0≤Na/MT≤0.2、0.05≤Na/MT≤0.3、或0.1≤Na/MT≤0.3。
含鈉過渡金屬氧化物中含有的過渡金屬元素為選自由Ti、V、Mn、Fe、Co和Ni構成的組中的至少一種(優選至少兩種)。根據需要,所述過渡金屬元素還可以含有Cr。作為含鈉過渡金屬氧化物,優選含有Ni、Ti和Mn作為過渡金屬原子的材料。根據需要,可以含有其它過渡金屬原子(V、Fe、Co和/或Cr)和/或其它原子(主族元素等等)。
含有Ni、Ti和Mn的含鈉過渡金屬氧化物易于具有小的不可逆容量且因此是有利的,因為在充電率(SOC)為100%的狀態下比率Na/MT減小。特別地,使用由式(1):NaxTiyNizMn1-y-zO2(x因充放電而變動并且滿足0≤x≤0.67、0.15≤y≤0.2、0.3≤z≤0.35)表示的化合物作為所述含鈉過渡金屬氧化物是特別有利的,因為在充電率(SOC)為100%的狀態下比率Na/MT減小。
由式(1)表示的化合物易于具有Na2/3Ti1/6Ni1/3Mn1/2O2的晶體結構(即P2型層狀結構)。因此,穩定地進行充放電。
鈉原子的比率x在放電期間增加且在充電期間減少。在充電率(SOC)為100%的狀態下的鈉原子的比率x與所述在充電率(SOC)為100%的狀態下的比率Na/MT相當(鈉原子的比率x與鈉原子對過渡金屬原子的比率Na/MT相當)。
含鈉過渡金屬氧化物也包括其中式(1)中的Ni、Ti和Mn中的至少一種被其它過渡金屬原子、主族元素等置換的化合物。
可以單獨使用一種含鈉過渡金屬氧化物。或者,可以組合使用兩種以上的含鈉過渡金屬氧化物。在由式(1)表示的化合物之中,NaxTi1/6Ni1/3Mn1/2O2因其不可逆容量小和能量密度高而是優選的。
可以通過已知方法制備含鈉過渡金屬氧化物。可以通過例如下述方法制備含鈉過渡金屬氧化物:在惰性氣體氣氛中對Na化合物(例如,氧化物、氫氧化物和/或碳酸鹽)和過渡金屬化合物(例如,氧化物、氫氧化物和/或碳酸鹽)的混合物進行燒制。在含鈉過渡金屬氧化物含有多種過渡金屬原子的情況下,可以使用含有各種過渡金屬原子的多種化合物。或者,可以使用含有多種過渡金屬原子的化合物(例如,復合氧化物)。
根據需要,正極活性物質可以含有除含鈉過渡金屬氧化物以外的活性物質(具體而言,可逆地吸藏和放出鈉離子的材料)。正極活性物質中的含鈉過渡金屬氧化物的比率例如為80質量%至100質量%并且優選為90質量%至100質量%。正極活性物質可以單獨由所述含鈉過渡金屬氧化物組成。
(其它)
負極的可逆容量和不可逆容量的總計Cnt對正極的可逆容量和不可逆容量的總計Cpt之比,即Cnt/Cpt滿足1≤Cnt/Cpt。比率Cnt/Cpt的增加具有提高耐過充電特性的傾向。然而,比率Cnt/Cpt的過度增加需要使用具有為正極的不可逆容量而準備的較大容量的負極,導致電池中不用于可逆充放電(正常充放電)的負極體積較大。
因此,從增加電池的能量密度的觀點考慮,比率Cnt/Cpt例如優選為1.5以下,并且可以為1.4以下或1.3以下。比率Cnt/Cpt可以滿足1≤Cnt/Cpt、1<Cnt/Cpt或1.1≤Cnt/Cpt。這些上限值和下限值可以自由組合在一起。比率Cnt/Cpt可以滿足例如1≤Cnt/Cpt≤1.5、1≤Cnt/Cpt≤1.3、1<Cnt/Cpt≤1.3、1.1≤Cnt/Cpt≤1.5、或1.1≤Cnt/Cpt≤1.3。
正極可以含有正極活性物質(或含有正極活性物質的正極混合物)和負載所述正極活性物質(或所述正極混合物)的正極集電器。
正極集電器可以由金屬箔或金屬多孔體(由金屬纖維形成的無紡布和/或金屬多孔片)形成。作為金屬多孔體,可以使用具有三維網狀骨架(特別是中空骨架)的金屬多孔體。考慮到在正極電位下的穩定性,正極集電器的材料例如優選為鋁和/或鋁合金,但不特別地限于它們。金屬箔具有例如10μm至50μm的厚度。金屬多孔體具有例如100μm至2000μm的厚度。
除正極活性物質外,正極混合物還可以含有導電助劑和/或粘結劑。可以通過將正極混合物涂布或填充到正極集電器、進行干燥、并任選地在厚度方向上進行壓制(或軋制)而形成正極。通常以含有分散介質的漿料的形式使用正極混合物。作為分散介質,使用有機溶劑如N-甲基-2-吡咯烷酮(NMP)和/或水。
導電助劑的例子包括但不特別地限于炭黑、石墨、碳纖維(例如,氣相生長碳纖維)和/或碳納米管。從增加導電性的觀點考慮,可以用導電助劑包覆正極活性物質的粒子。可以通過將導電助劑涂布于正極活性物質粒子的表面、機械化學加工(包括機械融合加工)等進行利用導電助劑的包覆。
相對于100質量份的正極活性物質,導電助劑的量可以在例如1質量份至25質量份的范圍內適當選擇,并且可以為5質量份至20質量份。
粘結劑的例子包括但不特別地限于氟樹脂,如聚偏二氟乙烯和聚四氟乙烯;聚烯烴樹脂;橡膠狀聚合物,如苯乙烯-丁二烯橡膠;聚酰胺樹脂(例如,芳族聚酰胺);聚酰亞胺樹脂,如聚酰亞胺和聚酰胺-酰亞胺;聚乙烯基吡咯烷酮;聚乙烯醇;和/或纖維素醚(羧烷基纖維素及其鹽,如羧甲基纖維素及其鈉鹽)。
從容易確保高粘著性和容量的觀點考慮,相對于100質量份的正極活性物質,粘結劑的量可以在例如約0.5質量份至約15質量份的范圍內選擇,并且可以優選為1質量份至12質量份,但不特別地限于此。
(負極)
負極含有負極活性物質。負極可以含有負極集電器和負載在所述負極集電器上的負極活性物質(或負極混合物)。
負極集電器可以由如在正極集電器中所述的金屬箔或金屬多孔體形成。優選的負極集電器的材料的例子包括但不特別地限于銅、銅合金、鎳、鎳合金和不銹鋼,因為它們不與鈉合金化并且在負極電位下穩定。負極集電器的厚度可以在正極集電器中所述的范圍內適當選擇。
所述負極活性物質的例子包括可逆地負載鈉離子的材料。所述材料的例子包括可逆地吸藏和放出(或插入和脫離)鈉離子的材料(第一材料);和與鈉合金化(具體而言,可逆的合金化和去合金化)的材料(第二材料)。所述第一材料和第二材料各自為由法拉第反應提供容量的材料。
第一材料的例子包括碳質材料和/或金屬化合物。碳質材料的例子包括易石墨化碳(軟碳)和/或難石墨化碳(硬碳)。金屬化合物的例子包括鈦化合物,例如含鋰的鈦氧化物,如鈦酸鋰(例如,Li2Ti3O7和/或Li4Ti5O12);和含鈉的鈦氧化物(例如,含堿金屬的鈦氧化物),如鈦酸鈉(例如,Na2Ti3O7和/或Na4Ti5O12)。在含鋰的鈦氧化物(或含鈉的鈦氧化物)中,鈦和/或鋰(或鈉)可以部分地被其它元素置換。作為第一材料,可以使用選自由軟碳、硬碳和含堿金屬的鈦氧化物構成的組中的至少一種。
第二材料的例子包括含有選自由鋅、銦、錫、硅、磷、銻、鉛和鉍構成的組中的至少一種的材料。所述材料的例子包括含有前述元素的金屬、合金和化合物。
可以單獨使用一種負極活性物質。或者,可以組合使用兩種以上的負極活性物質。在這些材料之中,從容易獲得高能量密度的觀點考慮,優選第一材料,例如前述的化合物(如含鈉的鈦氧化物)和/或碳質材料(如硬碳)。
Cnt可以大于等于Cpt。從進一步有效抑制過充電期間的鈉離子析出的觀點考慮,優選Cnt≥(Cpt+Ce)。在這種情況下,即使進行過充電而引起電解質中的鈉離子參與充電的狀態,鈉離子仍吸藏在負極中或與負極合金化。
Ce例如為0.01mAh至1×Cpt mAh并且可以為0.1mAh至1mAh或0.2mAh至0.8mAh。
正如正極的情況那樣,可以通過例如將含有負極活性物質的負極混合物涂布或填充到負極集電器、進行干燥并任選地在厚度方向上進行壓制(或軋制)而形成負極。作為負極,可以使用通過使用氣相法例如蒸發或濺射在負極集電器的表面上沉積負極活性物質的膜而制造的部件。可以將片狀金屬或合金直接用作負極。可以將通過將片狀金屬或合金與集電器壓接而制造的部件用作負極。
除負極活性物質之外,負極混合物還可以含有導電助劑和/或粘結劑。粘結劑(粘著劑)和導電助劑可以各自從為正極而例示的那些中適當選擇。用于負極活性物質的粘結劑(粘著劑)和導電助劑的量可以從為正極而例示的范圍中適當選擇。通常以含有分散介質的漿料(或糊料)的形式使用負極混合物。分散介質可以從為正極而例示的那些中適當選擇。
(隔膜)
作為隔膜,例如可以使用由樹脂和/或無紡布構成的微孔膜。可以考慮電池的工作溫度選擇隔膜的材料。微孔膜或無紡布的纖維中含有的樹脂的例子包括聚烯烴樹脂、聚苯硫醚樹脂、聚酰胺樹脂(如芳族聚酰胺樹脂)、和/或聚酰亞胺樹脂。無紡布中含有的纖維可以為無機纖維,如玻璃纖維。隔膜可以含有無機填料,如陶瓷粒子。
隔膜的厚度沒有特別限制,并且可以在例如約10μm至約300μm的范圍內選擇。
(電解質)
作為電解質,使用含有鈉離子的非水電解質。所使用的非水電解質的例子包括其中鈉離子和陰離子的鹽(鈉鹽)溶解在非水溶劑(有機溶劑)中的電解質(有機電解質);和含有陽離子(含鈉離子的陽離子)和陰離子的離子液體(熔融鹽電解質)。
考慮到低溫性質等,優選使用含有非水溶劑(有機溶劑)的電解質。從使電解質的分解最小化的觀點考慮,優選使用含有離子液體的電解質。可以使用含有離子液體和非水溶劑的電解質。
電解質中的鈉鹽或鈉離子的濃度可以在例如0.3mol/L至10mol/L的范圍內適當選擇。
(有機電解質)
除非水溶劑(有機溶劑)和鈉鹽之外,有機電解質還可以含有例如離子液體和/或添加劑。電解質中的非水溶劑和鈉鹽的總含量例如為60質量%以上,優選為75質量%以上,并且更優選為85質量%以上。電解質中的非水溶劑和鈉鹽的總含量可以例如為100質量%以下,或者95質量%以下。這些下限值和上限值可以自由組合在一起。電解質中的非水溶劑和鈉鹽的總含量可以例如為60質量%至100質量%或75質量%至95質量%。
鈉鹽中含有的陰離子(第一陰離子)的種類的例子包括但不特別地限于含氟酸的陰離子[例如含氟磷酸根陰離子,如六氟磷酸根離子,和含氟硼酸根陰離子,如四氟硼酸根離子];含氯酸的陰離子[例如高氯酸根離子];含草酸根的含氧酸的陰離子[例如草酸根合硼酸根離子,如雙(草酸根合)硼酸根離子(B(C2O4)2-),和草酸根合磷酸根離子,例如三(草酸根合)磷酸根離子(P(C2O4)3-)];氟代烷烴磺酸根陰離子[如三氟甲烷磺酸根離子(CF3SO3-)];和雙(磺酰)胺陰離子。
可以單獨使用一種鈉鹽。或者,可以組合使用兩種以上具有不同的第一陰離子的鈉鹽。
所述雙(磺酰)胺陰離子的例子包括雙(氟磺酰)胺陰離子(FSA)、雙(三氟甲磺酰)胺陰離子(TFSA)、(氟磺酰)(全氟烷基磺酰)胺陰離子[如(FSO2)(CF3SO2)N-]、和雙(全氟烷基磺酰)胺陰離子[如N(SO2CF3)2-和N(SO2C2F5)2-]。其中,特別優選FSA和/或TFSA。
非水溶劑沒有特別限制。可以使用用于鈉離子二次電池的已知非水溶劑。考慮到離子傳導性可以優選使用的非水溶劑的例子包括環狀碳酸酯,如碳酸亞乙酯、碳酸亞丙酯和碳酸亞丁酯;鏈狀碳酸酯,如碳酸二甲酯、碳酸二乙酯和碳酸甲乙酯;和環狀碳酸酯,如γ-丁內酯。可以單獨使用一種非水溶劑。或者,可以組合使用兩種以上的非水溶劑。
(熔融鹽電解質)
在將含有離子液體的熔融鹽電解質用作電解質的情況下,除含有陽離子和陰離子的離子液體之外,電解質還可以含有例如非水溶劑和/或添加劑。電解質優選具有70質量%以上的離子液體含量。電解質的離子液體含量優選為70質量%至100質量%并且可以為80質量%至100質量%或90質量%至100質量%。在本發明的這種實施方式中,即使在離子液體含量高的情況下,也抑制過充電期間的鈉析出。
除了鈉離子(第二陽離子)之外,熔融鹽電解質(或它的陽離子)還可以含有除鈉離子以外的陽離子(第三陽離子)。第三陽離子的例子包括有機陽離子和除鈉離子以外的無機陽離子。熔融鹽電解質(或它的陽離子)可以含有第三陽離子中的一種或者可以以組合的方式含有兩種以上的第三陽離子。
有機陽離子的例子包括衍生自脂族胺、脂環族胺和芳族胺的陽離子(如季銨陽離子);含氮的陽離子,例如具有含氮雜環的陽離子(即,衍生自環狀胺的陽離子);含硫的陽離子;和/或含磷的陽離子。
在含氮的有機陽離子之中,特別優選季銨陽離子和具有作為含氮雜環骨架的吡咯烷、吡啶或咪唑骨架的陽離子。
含氮的有機陽離子的具體例子包括四烷基銨陽離子,例如四乙銨陽離子(TEA)和甲基三乙銨陽離子(TEMA);1-甲基-1-丙基吡咯烷陽離子(MPPY或Py13)和1-丁基-1-甲基吡咯烷陽離子(MBPY或Py14);和/或1-乙基-3-甲基咪唑陽離子(EMI)和1-丁基-3-甲基咪唑陽離子(BMI)。
無機陽離子的例子包括除鈉離子以外的堿金屬離子(如鉀離子);堿土金屬離子(如鎂離子和鈣離子);和/或銨離子。
熔融鹽電解質(或它的陽離子)優選含有有機陽離子。含有有機陽離子的離子液體的使用降低了熔融鹽電解質的熔點和/或粘度。這容易增加鈉離子傳導性并且容易確保高容量。熔融鹽電解質(或它的陽離子)可以含有有機陽離子和無機陽離子作為第三陽離子。
作為陰離子,優選使用雙(磺酰)胺陰離子。雙(磺酰)胺陰離子可以從為有機電解質而例示的陰離子中適當選擇。在雙(磺酰)胺陰離子之中,特別優選FSA和/或TFSA。
離子液體含有鈉離子(第二陽離子)和陰離子(第二陰離子)的鹽(第二鹽),并且可以根據需要含有第三陽離子和陰離子(第三陰離子)的鹽(第三鹽)。第二鹽可以由一種鹽或者兩種以上具有不同的第二陰離子的鹽組成。第三鹽可以由一種鹽或者兩種以上具有不同的第三陽離子和/或不同的第三陰離子的鹽組成。第二和第三陰離子可以從前述的陰離子中適當選擇。
在第二鹽之中,例如特別優選鈉離子和FSA的鹽(Na·FSA)、和/或鈉離子和TFSA的鹽(Na·TFSA)。
第三鹽的具體例子包括Py13和FSA的鹽(Py13·FSA)、PY13和TFSA的鹽(Py13·TFSA)、Py14和FSA的鹽(Py14·FSA)、PY14和TFSA的鹽(Py14·TFSA)、BMI和FSA的鹽(BMI·FSA)、BMI和TFSA的鹽(BMI·TFSA)、EMI和FSA的鹽(EMI·FSA)、EMI和TFSA的鹽(EMI·TFSA)、TEMA和FSA的鹽(TEMA·FSA)、TEMA和TFSA的鹽(TEMA·TFSA)、TEA和FSA的鹽(TEA·FSA)、和TEA和TFSA的鹽(TEA·TFSA)。這些第三鹽可以單獨或以兩種以上的組合使用。
第二鹽占第二鹽和第三鹽的總計的比率(即,鈉離子占鈉離子和第三陽離子的總計的比率)可以取決于鹽的種類在5摩爾%至95摩爾%的范圍內適當選擇。
在第三陽離子為有機陽離子的情況下,第二鹽的比率優選為10摩爾%以上、15摩爾%以上、20摩爾%以上、或25摩爾%以上,并且更優選為30摩爾%以上、或40摩爾%以上。第二鹽的比率優選為65摩爾%以下并且更優選為55摩爾%以下。熔融鹽電解質具有相對低的粘度,因而容易獲得高容量。這些下限值和上限值可以自由組合在一起來設定優選范圍。例如,第二鹽的比率可以為10摩爾%至65摩爾%、15摩爾%至55摩爾%、或25摩爾%至55摩爾%。
可以通過熔融鹽電解質的組成來調節鈉熔融鹽電池的工作溫度。鈉熔融鹽電池可以在-20℃至大于90℃的溫度的寬溫度范圍內工作。
可以通過例如以下步驟制造鈉離子二次電池:(a)形成包含正極、負極和置于正極與負極之間的隔膜的電極組的步驟,和(b)將電極組和電解質收容在電池殼中的步驟。
圖1為示意性顯示本發明的一種實施方式的鈉離子二次電池的縱剖面圖。鈉離子二次電池包含堆疊型電極組、電解質(未示出)、和收容這些部件的棱柱形鋁電池殼10。電池殼10包括具有開口頂部和封閉底部的殼主體12;和封閉所述頂部開口的蓋體13。
當組裝鈉熔融鹽電池時,將正極2和負極3在隔膜1置于其間的狀態下進行堆疊以形成電極組,并將該電極組插入電池殼10的殼主體12中。然后通過將電解質注入殼主體12中,進行用電解質填充構成電極組的隔膜1、正極2和負極3之間的空隙的步驟。或者,當電解質為熔融鹽電解質時,可以用熔融鹽電解質浸滲電極組,然后可以將含有熔融鹽電解質的電極組收容在殼主體12中。
在蓋體13的中央設置當電池殼10的內壓增加時用于釋放內部產生的氣體的安全閥16。將貫穿蓋體13的外部正極端子14相對于安全閥16設置在蓋體13的一側部。將貫穿蓋體13的外部負極端子設置在蓋體13的另一側部。
堆疊型電極組包含多個正極2、多個負極3、和置于其間的多個隔膜1,正極2和負極3各自具有矩形片形狀。在圖1中,各個隔膜1具有袋狀,以便包圍相對應的一個正極2。然而,各個隔膜的形狀沒有特別限制。將多個正極2和多個負極3在電極組中的堆疊方向上交替堆疊。
可以將正極引線片2a布置在各正極2的端部。將多個正極2的正極引線片2a集束起來并與設置在電池殼10的蓋體13上的外部正極端子14連接,使得所述多個正極2并聯連接。同樣地,可以將負極引線片3a布置在各負極3的端部。將多個負極3的負極引線片3a集束起來并與設置在電池殼10的蓋體13上的外部負極端子連接,使得所述多個負極3并聯連接。優選將正極引線片2a的束和負極引線片3a的束在束之間保持距離從而彼此不接觸的情況下布置在電極組的一個端面的左側和右側。
外部正極端子14和外部負極端子各自為柱狀的并且至少在外部露出部分中具有螺紋槽。將螺母7與各端子的螺紋槽嚙合,并旋緊以將螺母7固定于蓋體13。將凸緣部8布置在各端子在電池殼10內部的部分中。旋緊螺母7,使得在其間具有墊圈9的狀態下將凸緣部8固定于蓋體13的內表面。
電極組不限于堆疊型,并且可以通過在隔膜置于其間的狀態下卷繞正極和負極而形成。從防止在負極上析出金屬鈉的觀點考慮,負極的尺寸可以大于正極的尺寸。
通常在預定的電壓范圍內進行鈉離子二次電池的充放電。具體而言,將鈉離子二次電池充電到預定的上限電壓(充電終止電壓),且將鈉離子二次電池放電到預定的終止電壓(放電終止電壓)。通常通過包含鈉離子二次電池的充放電系統中的充電控制單元和放電控制單元控制充電和放電。本發明的實施方式包括充放電系統,其包含鈉離子二次電池、控制鈉離子二次電池充電的充電控制單元、和控制鈉離子二次電池放電的放電控制單元。放電控制單元可以包含消耗由鈉離子二次電池供應的電力的負載裝置。
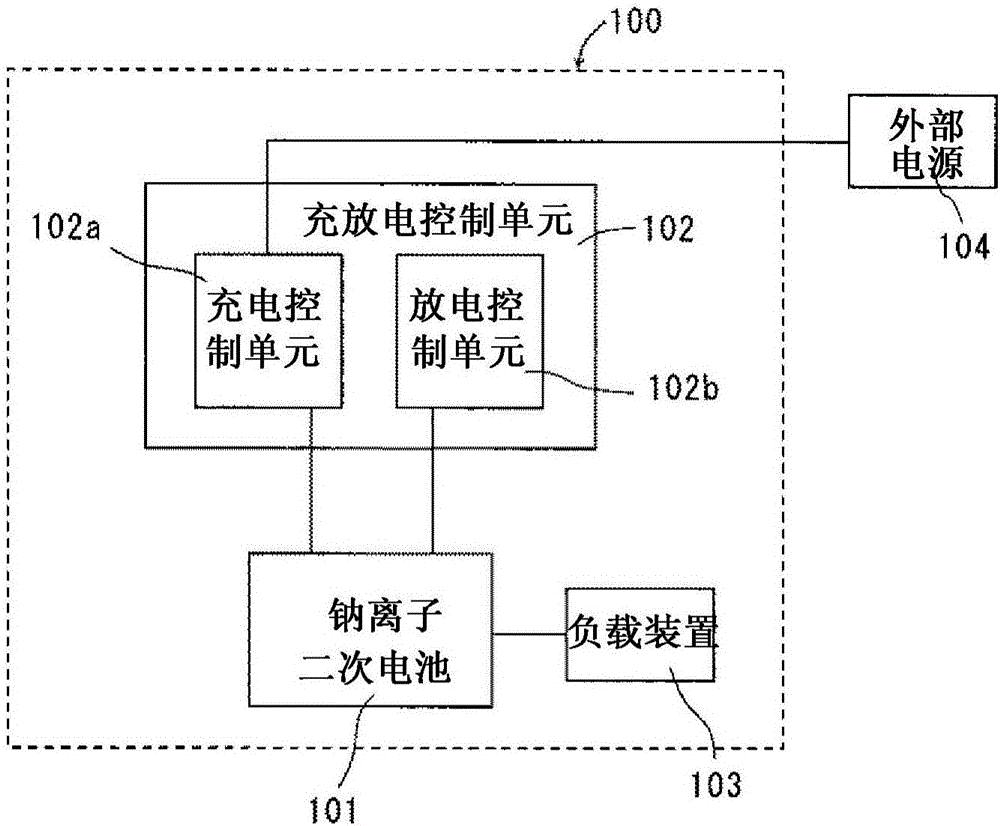
圖2為示意性顯示本發明的一種實施方式的充放電系統的方框圖。
充放電系統100包含鈉離子二次電池101、控制鈉離子二次電池101充放電的充放電控制單元102、和消耗由鈉離子二次電池101供應的電力的負載裝置103。充放電控制單元102包含控制例如鈉離子二次電池101的充電期間的電流和/或電壓的充電控制單元102a,和控制例如鈉離子二次電池101的放電期間的電流和/或電壓的放電控制單元102b。充電控制單元102a與外部電源104和鈉離子二次電池101連接。放電控制單元102b與鈉離子二次電池101連接。負載裝置103與鈉離子二次電池101連接。
關于前述的實施方式,進一步公開了以下附錄。
(附錄1)
鈉離子二次電池包含
含有正極活性物質的正極、含有負極活性物質的負極、置于所述正極與所述負極之間的隔膜、和電解質,
所述電解質為含有鈉離子的非水電解質,
所述正極活性物質含有可逆地吸藏和放出鈉離子的含鈉過渡金屬氧化物,
所述負極活性物質含有選自由可逆地吸藏和放出鈉離子的第一材料和與鈉合金化的第二材料構成的組中的至少一種,
在滿充電狀態的所述含鈉過渡金屬氧化物中,鈉原子對過渡金屬原子之比,即Na/MT滿足Na/MT≤0.3,且
所述負極的可逆容量和不可逆容量的總計Cnt對所述正極的可逆容量和不可逆容量的總計Cpt之比,即Cnt/Cpt滿足1≤Cnt/Cpt。
在附錄1的電池中,即使在過充電期間也抑制鈉的析出。
(附錄2)
在附錄1的鈉離子二次電池中,所述含鈉過渡金屬氧化物含有由式(1):NaxTiyNizMn1-y-zO2(其中x因充放電而變動并且滿足0≤x≤0.67、0.15≤y≤0.2、0.3≤z≤0.35)表示的化合物,并且比率Cnt/Cpt滿足1≤Cnt/Cpt≤1.3。
在這種情況下,確保了高耐過充電性,并且使能量密度進一步增加。
(附錄3)
充放電系統包含附錄1或2所述的鈉離子二次電池、控制所述鈉離子二次電池充電的充電控制單元、和控制所述鈉離子二次電池放電的放電控制單元。
在所述充放電系統中,即使當所述鈉離子二次電池處于過充電狀態時,也抑制鈉的析出。
[實施例]
下面將基于實施例和比較例對本發明進行具體說明。然而,本發明不限于下述的這些實施例。
<實施例1>
(1)含鈉過渡金屬氧化物Na2/3Ti1/6Ni1/3Mn1/2O2的合成
以使得獲得的含鈉過渡金屬氧化物具有前述組成的比例將碳酸鈉、氫氧化鎳、氧化鈦和碳酸錳混合在一起。將獲得的混合物在空氣氣氛中于900℃下燒制12小時以合成Na2/3Ti1/6Ni1/3Mn1/2O2。通過X射線衍射光譜確認燒制產物的組成。
(2)正極的制作
將在(1)中制備的Na2/3Ti1/6Ni1/3Mn1/2O2(正極活性物質)、乙炔黑(導電助劑)、和聚偏二氟乙烯(粘結劑)與NMP混合在一起以制備正極混合物糊料。在這種情況下,正極活性物質對導電助劑對粘結劑的質量比為100:10:5。將正極混合物糊料涂布到厚度為20μm的鋁箔表面、充分干燥、并壓制,制作成厚度為約52μm的正極。將正極沖孔成直徑為12mm的硬幣型。
(3)負極的制作
首先,將100質量份硬碳(負極活性物質)和4質量份聚偏二氟乙烯(粘結劑(粘著劑))與N-甲基-2-吡咯烷酮混合在一起以制備負極混合物糊料。將獲得的負極混合物糊料涂布到厚度為20μm的銅箔的表面、充分干燥、并壓制,制作成厚度為100μm的負極。將負極沖孔成直徑為12mm的硬幣型。
(4)鈉熔融鹽電池的制作
在0.3Pa的減壓下于90℃以上對硬幣型正極、負極和隔膜進行加熱,由此充分進行干燥。隨后,將硬幣型負極放入淺的圓筒形的Al/不銹鋼覆層殼中。在硬幣型隔膜置于其間的狀態下將硬幣型正極放置在所述硬幣型負極上。將預定量的熔融鹽電解質注入所述殼中。然后用在周緣具有絕緣墊的淺的圓筒形的Al/不銹鋼覆層密封板密封所述殼的開口。結果,向在殼底部與密封板之間的包含負極、隔膜和正極的電極組施加壓力,導致所述部件彼此接觸。從而制作硬幣型鈉熔融鹽電池A1。作為隔膜,使用由聚烯烴構成的微孔膜(NPS,厚50μm,由日本板硝子株式會社制造)。作為熔融鹽電解質,使用0.014g含有摩爾比為40:60的Na·FSA和Py13·FSA的離子液體(熔融鹽電解質的離子液體含量:100質量%)。從所使用的熔融鹽電解質中含有的鈉離子的總量求出Ce,結果為0.69mAh。
(5)評價
(a)Cpt,Cnt/Cpt,和Cnt/(Cpt+Ce)
除了使用了在(3)中制作的負極和作為對電極的鈉電極之外,與(3)中一樣制作了鈉熔融鹽電池(半電池)。作為鈉電極,使用了將金屬鈉接合在鋁箔上的硬幣型電極(厚度:50μm,直徑:12mm)。將獲得的半電池保持在25℃下。將其中將電池在0.1C下充電至0.02V、然后在0.1C下放電至1.5V的循環重復兩次,從而求出負極的可逆容量和不可逆容量。計算其總計Cnt。
將正極的可逆容量和不可逆容量的總計Cpt作為當所有鈉原子從正極放出時的容量計算出。與所制作的正極不能可逆地進行充放電的部分的容量相當的比率Na/MT為0.1。
從Cnt、Cpt和Ce值計算Cnt/Cpt和Cnt/(Cpt+Ce)。
(b)能量密度
將在(4)中制作的鈉熔融鹽電池保持在25℃下。使用其中在0.1C下將電池充電到充電終止電壓(4.0V)并在0.1C下放電到2.0V的充放電循環進行了充放電,以在充電率(SOC)為100%的狀態下比率Na/MT為預定值(在實施例1中為0.3)的方式設定所述充電終止電壓。求出第一個循環時的放電容量(初始電池容量)。將所述初始容量(Ah)除以正極、負極和隔膜的總體積(L)來求出能量密度(Ah/L)。從所述正極和負極的尺寸計算它們的體積(表觀體積)。
(c)耐過充電試驗
在25℃下將在(4)中制作的鈉熔融鹽電池充電到滿充電狀態(SOC:100%)。在測定電池溫度的同時,在0.5C下將電池從滿充電狀態過充電4小時。求出過充電期間的電池溫度最大值(最高溫度)(℃)。
<實施例2>
除了通過調節正極混合物糊料的涂布量按表1中所示改變正極厚度之外,與實施例1中一樣制作了正極。除了使用了獲得的正極之外,與實施例1中一樣制作了鈉熔融鹽電池A2。進行了評價。然而,在這種情況下,比率Na/MT在充電率(SOC)為100%的狀態下變為0.1。因此,在能量密度的評價中,將充電終止電壓設定為4.3V。
<比較例1>
除了使用了亞鉻酸鈉代替Na2/3Ti1/6Ni1/3Mn1/2O2之外,與實施例1中一樣制作了正極。除了使用了獲得的正極之外,與實施例1中一樣制作了鈉熔融鹽電池B1。進行了評價。然而,在這種情況下,亞鉻酸鈉在滿充電狀態下的比率Na/MT為0.5。因此,在能量密度的評價中,以在充電率(SOC)為100%的狀態下的比率Na/MT為0.5的方式將充電終止電壓設定為3.5V。與所制作的正極不能可逆地進行充放電的部分的容量相當的比率Na/MT為0.5。
<比較例2>
除了通過調節正極混合物糊料的涂布量按表1中所示改變正極厚度之外,與比較例1中一樣制作了正極。除了使用了獲得的正極之外,與比較例1中一樣制作了鈉熔融鹽電池B2。進行了評價。
<比較例3>
除了通過調節正極混合物糊料的涂布量按表1中所示改變正極厚度之外,與實施例1中一樣制作了正極。除了使用了獲得的正極之外,與實施例1中一樣制作了鈉熔融鹽電池B3。進行了評價。
表1顯示實施例和比較例的結果。
如表1中所示,其中比率Cnt/Cpt為1以上的實施例的電池A1和A2的結果證明了:所述電池具有高能量密度。即使在過充電期間,也抑制電池溫度上升。即,所述電池具有良好的耐過充電性。
其中比率Cnt/Cpt小于1的比較例的電池B1和B3的結果證明了,雖然所述電池在一定程度上具有高能量密度,但在過充電期間的電池溫度高于180℃。即,所述電池具有顯著低的耐過充電性。在比較例的電池B2中,雖然比率Cnt/Cpt為1以上,但在滿充電狀態下的比率Na/MT大于0.3。正極具有大的不可逆容量。電池具有低的能量密度。此外,在電池B2中,電池溫度上升到85℃。
在比較例的電池B1至B3中,電池溫度在過充電期間升高的原因大概是鈉在過充電期間在負極上析出,從而導致在正極與負極之間的內部短路。
產業實用性
本發明的一種實施方式的鈉離子二次電池具有良好的耐過充電性,因此對例如大型家用和工業用蓄電設備以及電動車輛和混合動力車輛用電源是有用的。
標號說明
1 隔膜
2 正極
2a 正極引線片
3 負極
3a 負極引線片
7 螺母
8 凸緣部
9 墊圈
10 電池殼
12 殼主體
13 蓋體
14 外部正極端子
16 安全閥
100 充放電系統
101 鈉離子二次電池
102 充放電控制單元
102a 充電控制單元
102b 放電控制單元
103 負載裝置
104 外部電源
- 還沒有人留言評論。精彩留言會獲得點贊!