一種采用生物膜干涉技術驗證抗體親和富集可行性的方法及其應用與流程
本發明屬于生物,具體涉及一種采用生物膜干涉技術驗證抗體親和富集可行性的方法及其應用。
背景技術:
1、生物制品中的宿主細胞殘留蛋白(hcp,host?cell?protein)會導致過敏反應或潛在毒性等不良臨床反應風險,因此必須建立合適的hcp檢測驗證方法來嚴格控制生物制品的質量。當前,廣泛被使用于hcp檢測的方法是雙抗體夾心酶聯免疫法(elisa),但不是所有hcps都可以作為抗原產生抗體,由于hcp成分不一、每一種蛋白成分含量也不一致,作為免疫原產生抗體的能力也不相同,所以由此制備的抗hcp抗體并不能完全檢測hcp中所有成分,因此會有“漏檢”,所以需要評估hcp?elisa試劑盒中抗體的覆蓋率(coverage)。為評估hcp?elisa檢測試劑盒中多克隆抗體的覆蓋率,本領域已經開發了各種技術,包括:采用雙向電泳(two-dimensional?electrophoresis,2-de)和蛋白質免疫印跡(western?blot,wb)技術結合的方法、采用熒光差異印跡電泳技術(2d-dibe,differential?in?blotelectrophoresis)、抗體親和富集-雙向電泳(aae,antibody?affinity?extraction)-2d,抗體親和富集-質譜分析(aae-ms)等。
2、其中,傳統的基于免疫印跡(western?blot,wb)的hcp抗體覆蓋率驗證方法,包括雙向凝膠電泳-免疫印跡(2d-wb)、雙向差異熒光印跡(2d-dibe)等;由于hcp覆蓋率低、重復性差等問題,逐漸無法滿足nda、bla等注冊申報的要求。而抗體親和富集(affinityantibody?extraction,aae)方法,突破了wb方法的局限性,將抗hcp抗體偶聯到固體基材上,然后上樣hcp樣品,富集過程中hcp抗體可捕獲識別hcp,而未識別的hcp則被流穿,通過多次重復循環,直到沒有額外的hcp結合為止;最后通過低ph等條件洗脫、富集hcp。將富集前的hcp和富集后hcp進行二維電泳-染色分析(aae-2d)或質譜分析(aae-ms),計算抗體的覆蓋率,進一步更真實準確地反應hcp抗體覆蓋率。
3、“生物膜干涉技術”(biolayer-interferometry,bli)是一種通過檢測干涉光譜的位移變化來檢測傳感器表面反應的技術;當一束可見光從光譜儀射出后,在傳感器末端的光學膜層的兩個界面會形成兩束反射光譜,并形成一束干涉光譜。任何由于分子結合或解離而形成的膜層厚度和密度變化,能夠通過干涉光譜的位移值而體現,并通過這個位移值作出實時的反應監測圖譜。因此。開發一種基于生物膜干涉技術完全模擬抗體親和富集整個過程,進而驗證抗體親和富集可行性的方法具有重要的應用價值。
技術實現思路
1、針對現有技術存在的不足,本發明的目的在于提供一種采用生物膜干涉技術驗證抗體親和富集可行性的方法及其應用。本發明利用生物膜干涉技術完全模擬抗體親和富集整個過程,進而驗證抗體親和富集可行性。不但可以實時提供結合數據,產生更多抗體親和富集相互作用的活性和行為的信息。還能簡化實際操作、減少驗證時間。
2、為達到此發明目的,本發明采用以下技術方案:
3、第一方面,本發明提供一種采用生物膜干涉技術驗證抗體親和富集可行性的方法,所述方法包括:
4、(1)采用生物素標記anti-cho?hcp抗體,所述生物素與anti-cho?hcp抗體的摩爾比為1:(1-10),例如可以是1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9或1:10等;
5、(2)采用檢測緩沖液潤濕傳感器,平衡傳感器,并將所述生物素標記的anti-chohcp抗體采用鏈酶親和素固定在傳感器上;
6、(3)將hcp蛋白溶液與所述生物素標記的anti-cho?hcp抗體結合;
7、(4)采用洗脫緩沖液洗脫hcp蛋白;
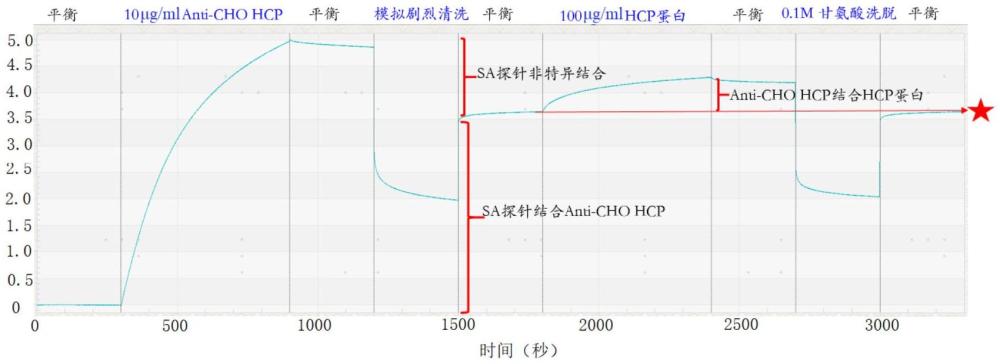
8、(5)統計上述步驟中octet系統采集的數據,親和素探針抓取生物素化anti-chohcp抗體、以及結合hcp蛋白均有明顯的上升信號,并且經過洗脫后的hcp蛋白信號與起始點信號一致;證明抗體親和富集的可行性及準確性;所述抗體親和富集的方法為鏈霉素親和素磁珠結合實驗方法。
9、優選地,步驟(1)中,所述生物素包括:生物素n-羥基磺基琥珀酰亞胺酯。
10、優選地,步驟(1)中,所述標記的反應條件為:反應溫度為4-37℃,例如可以是4℃、6℃、8℃、10℃、12℃、14℃、16℃、18℃、20℃、22℃、24℃、26℃、28℃、30℃、32℃、34℃、36℃或37℃等,反應時間為1-3h,例如可以是1h、2h或3h等。
11、優選地,步驟(1)中,所述標記后還包括:通過過濾去除過量的生物素后。
12、優選地,步驟(2)中,所述檢測緩沖液按濃度計包括:pbs+0.02-0.1%?tween-20,例如可以是0.02%、0.04%、0.06%、0.08%或0.1%等。
13、本發明中,分別使用含有0%(v/v)、0.02%(v/v)、0.1%(v/v)和0.5%(v/v)吐溫-20的磷酸鹽緩沖液進行實驗,使用含有0.02%(v/v)tween-20的磷酸緩沖液能獲得較優的檢測效果。
14、優選地,步驟(2)中,所述平衡傳感器的時間為200-500s,例如可以是200s、250s、300s、350s、400s、450s或500s等。
15、優選地,步驟(2)中,所述生物素標記的anti-cho?hcp抗體的固定量為5-40μg/ml,例如可以是5g/ml、10g/ml、15g/ml、20g/ml、25g/ml、30g/ml、35g/ml或40g/ml等。
16、本發明中,在固化中盡可能多的配體會使檢測信號最大化,但是這種方法也有可能產生不希望的假象。諸如分子擁擠、親合力、非特異性結合和/或傳質等效應都會影響觀察到的結合動力學。相反,如果太少配體被固定時,檢測信號可能非常低,導致數據跡線分離不良和信噪比不足。因此,本發明經過優化,所述生物素標記的anti-cho?hcp抗體的固定量為5-40μg/ml時,能獲得較好的實驗效果。
17、優選地,步驟(2)中,所述生物素標記的anti-cho?hcp抗體與親和素探針的固定時間為500-800s,例如可以是500s、550s、600s、650s、700s、750s或800s等。
18、優選地,步驟(2)中,所述生物素標記的anti-cho?hcp抗體固定后,還包括模擬劇烈清洗的步驟。
19、本發明中,模擬劇烈清洗以去除非特異性吸附影響,排除實驗干擾。
20、優選地,所述模擬劇烈清洗采用的緩沖液為0.1-0.5m甘氨酸,例如可以是0.1m、0.2m、0.3m、0.4m或0.5m等,ph2.0-3.0,例如可以是2、2.5或3等。
21、優選地,所述模擬劇烈清洗的時間為200-500s,例如可以是200s、250s、300s、350s、400s、450s或500s等。
22、優選地,所述模擬劇烈清洗前后還包括采用檢測緩沖液平衡傳感器的步驟。
23、優選地,所述平衡傳感器的時間為200-500s,例如可以是200s、250s、300s、350s、400s、450s或500s等。
24、優選地,步驟(3)中,所述hcp蛋白的濃度范圍為50-1000nm,例如可以是50nm、100nm、200nm、300nm、400nm、500nm、600nm、700nm、800nm、900nm或1000nm等。
25、優選地,步驟(3)中,所述hcp蛋白的溶液的溶劑按濃度計包括:pbs+0.02-0.1%tween-20,例如可以是0.02%、0.04%、0.06%、0.08%或0.1%等。
26、優選地,步驟(3)中,所述hcp蛋白與所述生物素標記的anti-cho?hcp抗體結合的時間為500-800s,例如可以是500s、550s、600s、650s、700s、750s或800s等。
27、優選地,步驟(3)中,所述hcp蛋白與所述生物素標記的anti-cho?hcp抗體結合的轉速設置為500-2000rpm,例如可以是500rpm、1000rpm、1500rpm或2000rpm等。
28、優選地,步驟(3)中,所述hcp蛋白與生物素標記的anti-cho?hcp抗體結合后,還包括采用檢測緩沖液平衡傳感器的步驟。
29、優選地,所述平衡傳感器的時間為200-500s,例如可以是200s、250s、300s、350s、400s、450s或500s等。
30、優選地,步驟(4)中,所述洗脫緩沖液為:0.05-0.5m甘氨酸,例如可以是0.05m、0.1m、0.15m、0.2m、0.25m、0.3m、0.35m、0.4m、0.45m或0.5m等,ph?2.0-2.5,例如可以是2.0、2.1、2.2、2.3、2.4或2.5。
31、優選地,步驟(4)中,所述洗脫的時間為200-500s,例如可以是200s、250s、300s、350s、400s、450s或500s等。
32、優選地,步驟(4)中,所述洗脫的轉速設置為500-2000rpm,例如可以是500rpm、1000rpm、1500rpm或2000rpm等。
33、優選地,步驟(4)中,所述洗脫后還包括采用檢測緩沖液平衡傳感器的步驟。
34、優選地,所述平衡傳感器的時間為200-500s,例如可以是200s、250s、300s、350s、400s、450s或500s等。
35、優選地,所述方法包括:
36、(1)采用生物素標記anti-cho?hcp抗體,所述生物素與anti-cho?hcp抗體的摩爾比為1:(1-10);所述標記的反應條件為:反應溫度為4-37℃,反應時間為1-3h;標記后通過過濾去除過量的生物素;
37、(2)采用檢測緩沖液潤濕傳感器,平衡傳感器200-500s,所述檢測緩沖液按濃度計包括:pbs+0.02-0.1%?tween-20;并將所述生物素標記的anti-cho?hcp抗體采用鏈酶親和素固定在傳感器上,固定時間為500-800s;所述生物素標記的anti-cho?hcp抗體的固定量為5-40μg/ml;固定后采用檢測緩沖液平衡傳感器200-500s,采用0.1-0.5m甘氨酸,ph?2.0-3.0緩沖液模擬劇烈清洗200-500s;再采用檢測緩沖液平衡傳感器200-500s;
38、(3)將濃度范圍為50-1000nm的一系列hcp蛋白溶液與所述生物素標記的anti-chohcp抗體結合500-800s,轉速設置為500-2000rpm;所述hcp蛋白的溶液的溶劑按濃度計包括:pbs+0.02-0.1%?tween-20;采用檢測緩沖液平衡傳感器200-500s;
39、(4)采用洗脫緩沖液洗脫hcp蛋白200-500s,轉速設置為500-2000rpm;所述洗脫緩沖液為:0.05-0.5m甘氨酸,ph?2.0-2.5;洗脫后采用檢測緩沖液平衡傳感器200-500s;
40、(5)統計上述步驟中octet系統采集的數據,親和素探針抓取生物素化anti-chohcp抗體、以及結合hcp蛋白均有明顯的上升信號,并且經過洗脫后的hcp蛋白信號與起始點信號一致;證明抗體親和富集的可行性及準確性;所述抗體親和富集的方法為鏈霉素親和素磁珠結合實驗方法。
41、本發明中,所述鏈霉素親和素磁珠結合實驗方法包括:
42、對用于hcp檢測的多克隆抗體進行生物素化,所述多克隆抗體與生物素之間的摩爾比為1:(1-10),所述生物素化的反應條件為:反應溫度為4-37℃,反應時間為1-3h,將生物素化的多克隆抗體固定于連接有鏈霉親和素的固體基材上;采用所得固體基材從待測溶液中捕獲富集hcp蛋白,再進行洗脫。
43、第二方面,本發明提供第一方面所述的采用生物膜干涉技術驗證抗體親和富集可行性的方法在評估hcp?elisa試劑盒中抗體的覆蓋率中應用。
44、本發明所述的數值范圍不僅包括上述列舉的點值,還包括沒有列舉出的上述數值范圍之間的任意的點值,限于篇幅及出于簡明的考慮,本發明不再窮盡列舉所述范圍包括的具體點值。
45、相對于現有技術,本發明具有以下有益效果:
46、本發明利用生物膜干涉技術完全模擬抗體親和富集整個過程,進而驗證抗體親和富集可行性。不但可以實時提供結合數據,產生更多抗體親和富集相互作用的活性和行為的信息。還能簡化實際操作、減少驗證時間。
- 還沒有人留言評論。精彩留言會獲得點贊!