用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法與流程
本發明涉及一種無損檢測測量技術的技術領域,具體涉及一種用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法。
背景技術:
活性氧的產量是光動力治療過程中把握劑量的一個關鍵,主要是通過基于直接或間接監測單線態氧產率、產量而獲得治療劑量信息。但目前無論是基于單線態氧發光檢測方法,還是基于單線態氧捕捉,或者其他間接劑量監測方式,這些技術都存在信號弱,靈敏度低,實時性差,或不易檢測,與活性氧產率相關程度低等各種限制,而且使用探針直接捕捉單線態氧的檢測方式不僅對單線態氧形成了淬滅和消耗,而且檢測的精確度也會受到影響,因而不能提供精確、實時的、易于實施的光動力劑量監測。
技術實現要素:
本發明的目的在于:克服現有技術的不足,提供一種用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法,全新的納米藥物高效輸運和腫瘤治療及監測體系,為高精度、高效治療腫瘤提供了一種可行性方案;提出了替代比率法檢測單線態氧的新思路,通過選擇性檢測與單線態氧同步產生的氧自由基,利用其和單線態氧在產出上的比率關系,反推單線態氧的產率產量,從而巧妙地避免了光動力反應中單線態氧直接檢測的諸多難題,實現了在不影響單線態氧產生的基礎上,高靈敏地監測光動力劑量,進行精準治療;提出了與光動力反應同步的耦合反饋式單線態氧精確檢測的新途徑,首次直接將單線態氧的產生和檢測整合在同一個納米探針上實現了一體化、直接耦合檢測,直接反饋劑量信息;本發明利用上轉換納米材料的優異的光學特性,同步實現了基于近紅外光的光敏劑激發和檢測探針的熒光激發,產生的紅色熒光也有利于攜帶的劑量信息高效穿透組織,該方法可提供治療劑量的精確監測和高效控制。
本發明所采取的技術方案是:
用于光動力反應活性氧的替代比率式耦合檢測裝置,包括計算機、數據采集卡、控制盒、近紅外光激光器、光纖、準直器、擴束鏡、ccd、濾光系統、采集鏡頭、跟蹤驅動系統和三維電動平臺,所述計算機與數據采集卡電連接,所述數據采集卡通過控制盒與近紅外光激光器電連接,所述近紅外激光器通過光纖與擴束鏡光信號連接,所述光纖上設有準直器,所述數據采集卡通過ccd與采集鏡頭光信號連接,并且ccd位于采集鏡頭的成像交點處,所述ccd通過濾光系統與采集鏡頭光信號連接,所述數據采集卡通過跟蹤驅動系統與三維電動平臺電連接,所述擴束鏡和采集鏡頭分別設于三維電動平臺上,還包括設于三維電動平臺一側的樣品臺,并且所述樣品臺位于擴束鏡和采集鏡頭的正下方。
本發明更進一步改進方案是,所述計算機為帶有采集控制軟件和圖像分析重建軟件以及電機控制軟件的計算機。
本發明更進一步改進方案是,所述的采集控制軟件和圖像分析重建軟件均為matlab軟件;所述的電機控制軟件為labview軟件。
本發明更進一步改進方案是,所述三維電動平臺包括前后移動平臺、左右移動平臺和上下移動平臺,所述前后移動平臺、左右移動平臺和上下移動平臺由各自的步進電機分別驅動。
本發明更進一步改進方案是,所述三維電動平臺的前后移動平臺、左右移動平臺和上下移動平臺的各自移動最小步距均為10μm。
本發明更進一步改進方案是,所述跟蹤驅動系統的最大跟蹤工作范圍為5cm。
本發明更進一步改進方案是,所述三維電動平臺由裝有電機控制軟件的計算機控制實現伺服跟蹤;每采集完一次光熒光信號,圖像分析重建軟件分析圖像得出樣品位置變動信息,并控制三維電動平臺進行位置校正,圖像分析重建軟件利用比值計算出單線態氧數據后,將結果和設定的閾值相比較,比較結果轉變為控制激光強度和照射時間的信號,輸出至激光控制盒控制激光。
本發明更進一步改進方案是,所述近紅外光激光器發出的激光為連續激光,功率在0~20w的范圍內,波長在700nm~1000nm的范圍內。
本發明更進一步改進方案是,所述擴束鏡的透光波長在650~1050nm的范圍內。
本發明更進一步改進方案是,所述濾光系統為693nm帶通的濾光片。
利用如上所述的用于光動力反應活性氧的替代比率式耦合檢測裝置進行檢測的方法,包括以下步驟:
1)使用溶劑熱法合成納米粒子:將定量的稀土氧化物充分溶解后,置于燒瓶內除水除氧,在氬氣保護下溫控加熱,并通過多次結晶技術形成核殼結構的近紅外激發的上轉換納米粒子;
2)將雙羧基聚乙二醇peg和不飽和磷脂分子用edc和nhs活化后,共價連接形成pl-peg-cooh,層析提純待用;將光敏劑rosebengal和pl-peg-cooh的羧基分別用dec和nhs活化,再按照5:1的摩爾比例混合,然后和步驟1)中制備得到的納米粒子混合孵育反應,離心去上清,三遍后用二氯甲烷溶解備用;靶向分子使用c(rgdyk),pl-peg-cooh經dec和nhs活化后和rgd共價連接,層析提純,將pl-peg-rgd加去離子水震蕩溶解備用;稱取一定量的探針分子hydro-ir-676,加少許二氯甲烷溶解,振搖至近澄清,將其與上述納米粒子混合并超聲,旋轉蒸發儀去除二氯甲烷,得膠體狀懸液,離心三次去游離的探針分子后按比例加適量pl-peg-rgd和pl-peg去離子水溶液,震蕩過夜,從而將步驟1)中制備得到的納米粒子構建成納米探針;
3)將步驟2)中所制備的納米探針用pbs溶液溶解后放入1ml一次性培養皿中,蓋好上蓋后,在蓋上做圖形標記,將培養皿放在樣品臺上;
4)計算機通過控制盒使近紅外光激光器發出激光,通過準直器和擴束鏡調整激光光斑面積、以使激光光斑覆蓋整個培養皿,調整采集鏡頭的位置,使培養皿在ccd上成像最清晰且處于中間位置;
5)近紅外激光經上轉換納米粒子轉換后,發出兩種波長的可見光,短波長的可見光用于激發光敏效應,從而產生單線態氧,長波長的可見光用于激發檢測探針的熒光;激光啟動后,被照射納米探針吸收的激光,經由上轉換納米粒子激發產生氧自由基分子檢測分子和光敏劑分子,光敏劑分子在短波長的可見光照射下發生光動力效應從而產生單線態氧和氧自由基分子,氧自由基分子檢測分子和氧自由基分子在長波長的可見光照射下發出熒光信號,熒光信號被同側的采集鏡頭接收,然后通過濾光片濾除干擾光后被ccd接收,之后信號被數據采集卡采集,數據采集卡再將數據傳輸并儲存到帶有采集控制軟件和圖像分析重建軟件的計算機中;
6)計算機利用圖像分析重建軟件對數據采集卡所采集的熒光信號數據進行成像,根據熒光強度、熒光變化率對所成的像的對應區域做統計學分析,得到平均值,并根據單線態氧和氧自由基的已知比率對相對應的部分做比值,由此可以定量出單線態氧產量和產量信息,通過圖像特征分析獲得樣品移動信息;
7)獲得的產量信息和預設的閾值比較,比較結果輸出到控制激光功率的控制盒以控制激光輸出功率;獲得的移動信息,輸出到跟蹤驅動系統,控制三維電動平臺跟蹤樣品的位置。
本發明更進一步改進方案是,所述步驟1)中,上轉換納米粒子經3-氨丙基三乙氧基硅烷處理后帶氨基基團,電鏡等檢測控制平均粒徑為50nm,光譜儀檢測上轉換光譜和發光量子效率。
本發明更進一步改進方案是,所述步驟2)中,整個操作過程避光操作。
本發明更進一步改進方案是,所述步驟5)中,光敏劑分子和氧自由基檢測分子共定于納米粒子表面,光敏反應產生的主產物:單線態氧用于治療,副產物:氧自由基檢測分子被直接捕獲檢測,以熒光形式報告產量信息。
本發明更進一步改進方案是,所述步驟6)中,計算機利用圖像分析重建軟件對數據采集卡所采集的熒光信號數據進行成像所采用的數據處理方法為最大值投影算法。
光動力過程中在光敏劑主要產生單線態氧的同時(ⅱ型反應),會通過電子轉移產生一定比例的氧自由基(ⅰ型反應),如下:
3s*+rh→sh*+r*sh*+3o2→1s+o2?
3s*+rh→s*‐+rh*+s*‐+3o2→1s+o2?
(s光敏劑,3o2基態氧,o2?超氧陰離子,*激發態。)
因此,通過測量副產物氧自由基的量再根據其與單線態氧產量的比率關系反推,即可獲得主要產物單線態氧的產出,該方法我們稱之為替代比率法。替代比率法是一種非直接的檢測方法,是一種影響小,又不失精確度的新的檢測思路。另外,為避免檢測和被檢測分子二者定位差異的干擾,在光動力治療過程中,活性氧(包括單線態氧和氧自由基)產生后,在其擴散和淬滅之前,立即由鄰近的探針分子完成在位檢測,實現活性氧產物的直接耦合檢測,檢測結果更加準確,實時。
在激光的激發下,氧自由基檢測探針被氧化發出熒光,產物越多熒光越強,熒光信號經ccd檢測后輸至采集卡和電腦。
熒光變化率、強度檢測可依據下式實現:
熒光變化率:
熒光強度:
其中t為時間,k為常數,c為與初始熒光有關的常數,c為探針濃度,iex為激發光強度,v為探測體積。熒光變化率為時間t1到t2間隔的平均近似,和單線態氧的產率相關。其中,與熒光強度相關的檢測體積以及激發光強度均通過參數控制視為不變項。
本發明的有益效果在于:
第一、本發明的用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法,全新的納米藥物高效輸運和腫瘤治療及監測體系,為高精度、高效治療腫瘤提供了一種可行性方案。
第二、本發明的用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法,提出了替代比率法檢測單線態氧的新思路,通過選擇性檢測與單線態氧同步產生的氧自由基,利用其和單線態氧在產出上的比率關系,反推單線態氧的產率產量,從而巧妙地避免了光動力反應中單線態氧直接檢測的諸多難題,實現了在不影響單線態氧產生的基礎上,高靈敏地監測光動力劑量,進行精準治療。
第三、本發明的用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法,提出了與光動力反應同步的耦合反饋式單線態氧精確檢測的新途徑,首次直接將單線態氧的產生和檢測整合在同一個納米探針上實現了一體化、直接耦合檢測,直接反饋劑量信息。
第四、本發明的用于光動力反應活性氧的替代比率式耦合檢測裝置及其檢測方法,本發明利用上轉換納米材料的優異的光學特性,同步實現了基于近紅外光的光敏劑激發和檢測探針的熒光激發,產生的紅色熒光也有利于攜帶的劑量信息高效穿透組織,該方法可提供治療劑量的精確監測和高效控制。
附圖說明:
圖1為本發明檢測裝置結構的示意圖。
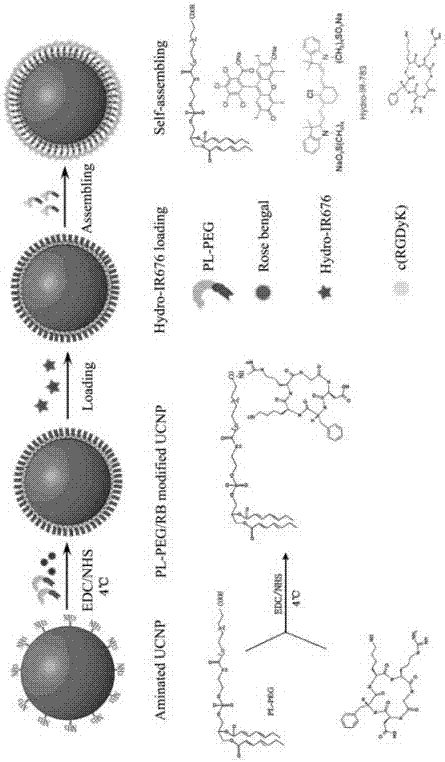
圖2為本發明中納米探針及其構建納米粒子構建示意圖。
圖3為實施例1中樣品檢測反應之后1min和10min的熒光圖像。
具體實施方式:
如圖1可知,本發明包括計算機1、數據采集卡2、控制盒3、近紅外光激光器4、光纖5、準直器6、擴束鏡7、ccd8、濾光系統、采集鏡頭10、跟蹤驅動系統11和三維電動平臺12,所述計算機1與數據采集卡2電連接,所述數據采集卡2通過控制盒3與近紅外光激光器4電連接,所述近紅外激光器4通過光纖5與擴束鏡7光信號連接,所述光纖5上設有準直器6,所述數據采集卡通過ccd8與采集鏡頭10光信號連接,并且ccd8位于采集鏡頭10的成像交點處,所述ccd通過濾光系統與采集鏡頭10光信號連接,所述數據采集卡2通過跟蹤驅動系統11與三維電動平臺12電連接,所述擴束鏡7和采集鏡頭10分別設于三維電動平臺12上,還包括設于三維電動平臺12一側的樣品臺13,并且所述樣品臺13位于擴束鏡7和采集鏡頭10的正下方。
所述計算機1為帶有采集控制軟件和圖像分析重建軟件以及電機控制軟件的計算機。
所述的采集控制軟件和圖像分析重建軟件均為matlab軟件;所述的電機控制軟件為labview軟件。
所述三維電動平臺12包括前后移動平臺、左右移動平臺和上下移動平臺,所述前后移動平臺、左右移動平臺和上下移動平臺由各自的步進電機分別驅動。
所述三維電動平臺12的前后移動平臺、左右移動平臺和上下移動平臺的各自移動最小步距均為10μm。
所述跟蹤驅動系統11的最大跟蹤工作范圍為5cm。
所述三維電動平臺12由裝有電機控制軟件的計算機1控制實現伺服跟蹤;每采集完一次光熒光信號,圖像分析重建軟件分析圖像得出樣品位置變動信息,并控制三維電動平臺12進行位置校正,圖像分析重建軟件利用比值計算出單線態氧數據后,將結果和設定的閾值相比較,比較結果轉變為控制激光強度和照射時間的信號,輸出至激光控制盒控制激光。
所述近紅外光激光器4發出的激光為連續激光,功率在0~20w的范圍內,波長在700nm~1000nm的范圍內。
所述擴束鏡7的透光波長在650~1050nm的范圍內。
所述濾光系統為693nm帶通的濾光片9。
如圖2可知,利用如上所述的用于光動力反應活性氧的替代比率式耦合檢測裝置進行檢測的方法,包括以下步驟:
1)使用溶劑熱法合成納米粒子:將定量的稀土氧化物充分溶解后,置于燒瓶內除水除氧,在氬氣保護下溫控加熱,并通過多次結晶技術形成核殼結構的近紅外激發的上轉換納米粒子;
2)將雙羧基聚乙二醇peg和不飽和磷脂分子用edc和nhs活化后,共價連接形成pl-peg-cooh,層析提純待用;將光敏劑rosebengal和pl-peg-cooh的羧基分別用dec和nhs活化,再按照5:1的摩爾比例混合,然后和步驟1)中制備得到的納米粒子混合孵育反應,離心去上清,三遍后用二氯甲烷溶解備用;靶向分子使用c(rgdyk),pl-peg-cooh經dec和nhs活化后和rgd共價連接,層析提純,將pl-peg-rgd加去離子水震蕩溶解備用;稱取一定量的探針分子hydro-ir-676,加少許二氯甲烷溶解,振搖至近澄清,將其與上述納米粒子混合并超聲,旋轉蒸發儀去除二氯甲烷,得膠體狀懸液,離心三次去游離的探針分子后按比例加適量pl-peg-rgd和pl-peg去離子水溶液,震蕩過夜,從而將步驟1)中制備得到的納米粒子構建成納米探針;
3)將步驟2)中所制備的納米探針用pbs溶液溶解后放入1ml一次性培養皿中,蓋好上蓋后,在蓋上做圖形標記,將培養皿放在樣品臺上;
4)計算機1通過控制盒2使近紅外光激光器4發出激光,通過準直器6和擴束鏡7調整激光光斑面積、以使激光光斑覆蓋整個培養皿,調整采集鏡頭10的位置,使培養皿在ccd8上成像最清晰且處于中間位置;
5)近紅外激光經上轉換納米粒子轉換后,發出兩種波長的可見光,短波長的可見光用于激發光敏效應,從而產生單線態氧,長波長的可見光用于激發檢測探針的熒光;激光啟動后,被照射納米探針吸收的激光,經由上轉換納米粒子激發產生氧自由基分子檢測分子和光敏劑分子,光敏劑分子在短波長的可見光照射下發生光動力效應從而產生單線態氧和氧自由基分子,氧自由基分子檢測分子和氧自由基分子在長波長的可見光照射下發出熒光信號,熒光信號被同側的采集鏡頭10接收,然后通過濾光片9濾除干擾光后被ccd8接收,之后信號被數據采集卡2采集,數據采集卡2再將數據傳輸并儲存到帶有采集控制軟件和圖像分析重建軟件的計算機1中;
6)計算機1利用圖像分析重建軟件對數據采集卡2所采集的熒光信號數據進行成像,根據熒光強度、熒光變化率對所成的像的對應區域做統計學分析,得到平均值,并根據單線態氧和氧自由基的已知比率對相對應的部分做比值,由此可以定量出單線態氧產量和產量信息,通過圖像特征分析獲得樣品移動信息;
7)獲得的產量信息和預設的閾值比較,比較結果輸出到控制激光功率的控制盒3以控制激光輸出功率;獲得的移動信息,輸出到跟蹤驅動系統11,控制三維電動平臺12跟蹤樣品的位置。
所述步驟1)中,上轉換納米粒子經3-氨丙基三乙氧基硅烷處理后帶氨基基團,電鏡等檢測控制平均粒徑為50nm,光譜儀檢測上轉換光譜和發光量子效率。
所述步驟2)中,整個操作過程避光操作。
所述步驟5)中,光敏劑分子和氧自由基檢測分子共定于納米粒子表面,光敏反應產生的主產物:單線態氧用于治療,副產物:氧自由基檢測分子被直接捕獲檢測,以熒光形式報告產量信息。
所述步驟6)中,計算機1利用圖像分析重建軟件對數據采集卡2所采集的熒光信號數據進行成像所采用的數據處理方法為最大值投影算法。
實施例1
本發明包括計算機1、數據采集卡2、控制盒3、近紅外光激光器4、光纖5、準直器6、擴束鏡7、ccd8、濾光系統、采集鏡頭10、跟蹤驅動系統11和三維電動平臺12,所述計算機1與數據采集卡2電連接,所述數據采集卡2通過控制盒3與近紅外光激光器4電連接,所述近紅外激光器4通過光纖5與擴束鏡7光信號連接,所述光纖5上設有準直器6,所述數據采集卡通過ccd8與采集鏡頭10光信號連接,并且ccd8位于采集鏡頭10的成像交點處,所述ccd通過濾光系統與采集鏡頭10光信號連接,所述數據采集卡2通過跟蹤驅動系統11與三維電動平臺12電連接,所述擴束鏡7、ccd8和濾光系統和采集鏡頭10分別設于三維電動平臺12上,還包括設于三維電動平臺12一側的樣品臺13,并且所述樣品臺13位于擴束鏡7和采集鏡頭10的正下方。
所述計算機1為帶有采集控制軟件和圖像分析重建軟件以及電機控制軟件的計算機。
所述的采集控制軟件和圖像分析重建軟件均為matlab軟件;所述的電機控制軟件為labview軟件。
所述的數據采集卡2的型號為ni公司生產的pci2400。
所述的光纖5為激光功率光纖,數值孔徑為0.22、光纖接頭為sma905,光纖芯徑為200μm。
所述的納米探針為50nm的負載有光敏劑和氧自由基檢測劑的上轉換納米粒子。
所述的ccd8為可見光ccd。
所述三維電動平臺12包括前后移動平臺、左右移動平臺和上下移動平臺,所述前后移動平臺、左右移動平臺和上下移動平臺由各自的步進電機分別驅動。
所述三維電動平臺12的前后移動平臺、左右移動平臺和上下移動平臺的各自移動最小步距均為10μm。
所述跟蹤驅動系統11為三維光電跟蹤系統,最大跟蹤工作范圍為5cm,最小分辨率為橫向為1mm,縱向為2mm。
所述三維電動平臺12由裝有電機控制軟件的計算機1控制實現伺服跟蹤;每采集完一次光熒光信號,圖像分析重建軟件分析圖像得出樣品位置變動信息,并控制三維電動平臺12進行位置校正,圖像分析重建軟件利用比值計算出單線態氧數據后,將結果和設定的閾值相比較,比較結果轉變為控制激光強度和照射時間的信號,輸出至激光控制盒控制激光。
所述近紅外光激光器4發出的激光為連續激光,功率在0~20w的范圍內,波長在700nm~1000nm的范圍內。
所述擴束鏡7的焦距為4.6mm,透光波長在650~1050nm的范圍內。
所述濾光系統為693nm帶通的濾光片9。
合成上轉換納米粒子
使用溶劑熱法合成納米粒子。將定量的稀土氧化物充分溶解后,置于燒瓶內除水除氧,在氬氣保護下溫控加熱,最后通過多次結晶技術形成核殼結構的980nm近紅外激發的上轉換納米粒子。納米粒子(nayf4:yb,er@nayf4:yb)特征為:980nm光激發,可見光發射;經3-氨丙基三乙氧基硅烷(aptes)處理后帶氨基基團。電鏡等檢測控制平均粒徑在50nm,光譜儀檢測上轉換光譜和發光量子效率。
光敏納米探針構建:
將雙羧基聚乙二醇peg(2000)和不飽和磷脂(1,2-didocosahexaenoyl-sn-glycero-3-phosphocholine,c52h80no8p)分子用edc和nhs活化后,共價連接形成pl-peg-cooh,層析提純待用。將光敏劑rosebengal和pl-peg-cooh的羧基分別用dec和nhs活化,再按照5:1的摩爾比例混合,然后和納米粒子混合孵育反應,離心去上清,三遍后用二氯甲烷溶解備用。靶向分子使用c(rgdyk),pl-peg-cooh經dec和nhs活化后和rgd共價連接,層析提純,將pl-peg-rgd加去離子水震蕩溶解備用。稱取一定量的探針分子hydro-ir-676,加少許二氯甲烷溶解,振搖至近澄清,將其與上述納米粒子混合并超聲,旋轉蒸發儀去除二氯甲烷,得膠體狀懸液,離心三次去游離的探針分子后按比例加適量pl-peg-rgd和pl-peg去離子水溶液,震蕩過夜。操作過程中注意避光。所得到的檢測探針為hydro-ir-676氧自由基熒光探針;所述的樣品為活體生物組織,測量目標為光動力反應的劑量。
然后將所制備的hydro-ir-676氧自由基熒光探針用pbs溶液溶解后放入1ml一次性培養皿中,蓋好上蓋后,在蓋上做圖形標記,將培養皿放在樣品臺上;計算機1通過控制盒2使近紅外光激光器4發出980nm的激光,通過準直器6和擴束鏡7調整激光光斑面積、以使激光光斑覆蓋整個培養皿,調整采集鏡頭10的位置,使培養皿在ccd8上成像最清晰且處于中間位置;接著上轉換納米粒子,能夠被980nm或800nm近紅外激光激發發出545nm和654nm波長的可見光,短波長的可見光用于激發光敏效應,從而產生單線態氧,長波長的可見光用于激發檢測探針的熒光;激光啟動后,被照射納米探針吸收的激光,經由上轉換納米粒子激發產生氧自由基分子檢測分子和光敏劑分子,光敏劑分子在短波長的可見光照射下發生光動力效應從而產生單線態氧和氧自由基分子,氧自由基分子檢測分子和氧自由基分子在長波長的可見光照射下發出熒光信號,熒光信號被同側的采集鏡頭10接收,然后通過濾光片9濾除干擾光后被ccd8接收,之后信號被數據采集卡2采集,數據采集卡2再將數據傳輸并儲存到帶有采集控制軟件和圖像分析重建軟件的計算機1中;之后,計算機1利用圖像分析重建軟件對數據采集卡2所采集的熒光信號數據進行成像,根據熒光強度、熒光變化率對所成的像的對應區域做統計學分析,得到平均值,并根據單線態氧和氧自由基的已知比率對相對應的部分做比值,由此可以定量出單線態氧產量和產量信息,通過圖像特征分析獲得樣品移動信息;再將獲得的產量信息和預設的閾值比較,比較結果輸出到控制激光功率的控制盒3以控制激光輸出功率;獲得的移動信息,輸出到跟蹤驅動系統11,控制三維電動平臺12跟蹤樣品的位置。
如圖3可知,反應10min后的熒光亮度明顯強于反應1min后的熒光強度。因此論證了可以通過本發明檢測出氧自由基分子產量的不同,從而可以得出單線態氧的對應產量的變化。實際應用的時候,可以進行多次不同量的定量實驗,從而標定不同熒光光亮度代表的氧自由基分子的產量值,及各自對應單線態氧的產量,然后在實際檢測過程中通過被檢測樣品的熒光強度與各標定的熒光強度進行比對,從而得出實際檢測的樣品中的單線態氧的產量,進而可以得出其治療效果,為高精度、高效治療腫瘤提供了一種可行性方案。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 生產5?氨基乙酰丙酸的谷氨酸棒桿菌工程菌株及構建的制造方法與工藝
- 一種Pb2+摻雜的紫外長余輝發光材料及其制備方法與制造工藝
- TMC/京尼平/pDNA納米載體及其制備方法和應用與制造工藝
- 一種治療痔瘡的制劑及其制備方法與制造工藝
- 一種麒麟菜有效成分的提取方法與制造工藝
- 基于苯基取代氟硼二吡咯及二苯胺基茚并芴的雙光子熒光染料及其合成方法與制造工藝
- 苯并[c,d]吲哚若丹復合份菁及其合成方法和應用與制造工藝
- 一種具有水溶性及聚集誘導發射效應的熒光探針和納米粒及制備方法和應用與制造工藝
- 一種ZnPc?UCNP?PEG?G納米復合物的制備方法與制造工藝
- 一種基于納米載體的化療?熱療型骨修復材料及制備和應用的制造方法與工藝