豬疾病多聯快速檢測試紙條的制作方法
本實用新型總體涉及動物疫病快速診斷試紙條,具體涉及一種可同時檢測豬瘟、藍耳病和O型口蹄疫病毒抗體的免疫層析試紙條。
背景技術:
豬瘟(classical swine fever,CSF)俗稱爛腸瘟,是感染豬的一種急性、熱性、高度接觸性傳染病。豬瘟會導致患病豬發燒、厭食、腹瀉、死亡等,可造成母豬流產、仔豬大批死亡。豬繁殖與呼吸綜合征(porcine reproductive and respiratory syndrome,PRRS)由于發病豬出現耳朵發紺癥狀,又稱藍耳病。藍耳病主要感染繁殖母豬和仔豬,引起免疫抑制,對豬鏈球菌病有誘發作用。口蹄疫(foot and mouth disease,FMD)是一種多宿主傳染病,豬、牛、羊等偶蹄類動物最易感。豬O型口蹄疫發病率高,傳播迅速,可造成母豬流產、仔豬大批死亡。豬瘟、高致病性豬藍耳病和口蹄疫是對養豬業危害最嚴重的三種豬病,被世界動物衛生組織(OIE)列為A類傳染病和法定申報動物疫病,我國也將其列為一類傳染病。目前,我國針對這三種豬病采取強制免疫與疫情監測相結合的凈化策略,疫苗免疫成為影響疫病防控的關鍵,而針對疫苗建立合適的評價手段具有重要意義。
目前,疫苗免疫效果評價主要依賴ELISA方法。國內外有許多動物疫病血清抗體檢測試劑,如美國愛德士(IDEXX)和韓國金諾(JBT)的豬瘟阻斷ELISA試劑盒,中國獸醫藥品監察所的豬瘟間接ELISA試劑盒。ELISA敏感性高,可平行檢測多份樣品,但是該方法耗時較長,間接ELISA需要約2h,阻斷ELISA需要2~3h。此外,ELISA檢測需要使用酶標儀等儀器,只能適用于具有實驗硬件支持的機構,無法在臨床一線等簡陋條件下開展免疫監測。因此,研發病毒抗體快速檢測手段對于豬病臨床診斷與免疫監測具有重要意義,而基于免疫層析原理的膠體金試紙條檢測技術操作簡單,檢測時間短,成為重要 的血清學監測手段。
技術實現要素:
本實用新型所要解決的問題是克服現有技術的不足,提供一種可同時檢測豬瘟、藍耳病、O型口蹄疫病毒抗體的膠體金試紙條。該試紙條不需專業人員操作,不需借助任何儀器,檢測耗時短且制備簡單。
本實用新型所要解決的技術問題是通過以下技術方案實現的:
一種豬疾病多聯快速檢測試紙條,試紙條包括底板、包被膜、玻璃纖維膜、吸水紙和樣品墊。其中,包被膜的底面粘貼在底板上,包被膜正面的兩端分別粘貼玻璃纖維膜和吸水紙。在玻璃纖維膜遠離吸水紙一端的正面粘貼樣品墊。在包被膜上設有檢測線I、II、III和質控線。
檢測線I、II、III分別包被豬瘟、藍耳病、豬O型口蹄疫病毒rED蛋白,質控線包被兔抗豬IgG抗體。所述玻璃纖維膜上噴涂SPA蛋白膠體金顆粒標記偶聯物。
本實用新型試紙條采用雙抗原夾心法,當被檢樣品中含有豬瘟、藍耳病和豬O型口蹄疫病毒抗體時,則在樣品墊處與SPA膠體金顆粒標記偶聯物結合,分別形成“SPA偶聯物—病毒抗體復合物”,并在吸水紙的作用下向前滲透泳動。當復合物到達檢測線I,豬瘟病毒抗體與rED1蛋白發生特異性結合,形成“SPA偶聯物—豬瘟病毒抗體—rED1復合物”,在包被膜上出現肉眼可見的色帶。當復合物到達檢測線II,藍耳病病毒抗體與rED2蛋白發生特異性結合,形成“SPA偶聯物—藍耳病病毒抗體—rED2復合物”,在包被膜上出現肉眼可見的色帶。當復合物到達檢測線III,O型口蹄疫病毒抗體與rED3蛋白發生特異性結合,形成“SPA偶聯物—口蹄疫病毒抗體—rED3復合物”,在包被膜上出現肉眼可見的色帶。當被檢樣品中不含豬瘟、藍耳病、O型口蹄疫病毒抗體時,SPA膠體金顆粒標記偶聯物泳動至質控線,與兔抗豬IgG抗體結合,在包被膜上出現肉眼可見的色帶。檢測時,吸取待檢血清樣品1滴,加入加樣孔,觀察檢測線I、II、III和質控線是否出現紅色色帶,從而判定動物體內是否含有豬瘟病毒、豬藍耳病病毒和豬O型口蹄疫病毒抗體。
本實用新型的積極效果是:
1、本實用新型試紙條結合膠體金技術和膜層析技術,操作便捷,不需要儀器,結果判讀簡單。相對于ELISA,試紙條原輔料更為簡單,成本低,有益于推廣應用。采集一份血清樣品,可同時檢測豬瘟、豬藍耳病和豬O型口蹄疫病毒抗體。能夠滿足基層組織、農戶對于重大疫病診斷的需求。
2、本實用新型采用酵母真核表達系統制備試紙條上的檢測用抗原蛋白。酵母為真核表達宿主,蛋白翻譯后加工修飾機制更完善,表達蛋白活性高。
3、本實用新型采用雙抗原夾心法,不受樣品的宿主來源限制,除檢測豬瘟、藍耳病和豬O型口蹄疫病毒抗體外,還可用于多種動物O型口蹄疫病毒檢測。
附圖說明
圖1為本實用新型試紙條的側面結構示意圖。圖中1:底板;2:包被膜;3:玻璃纖維膜;4:吸水紙;5:樣品墊。
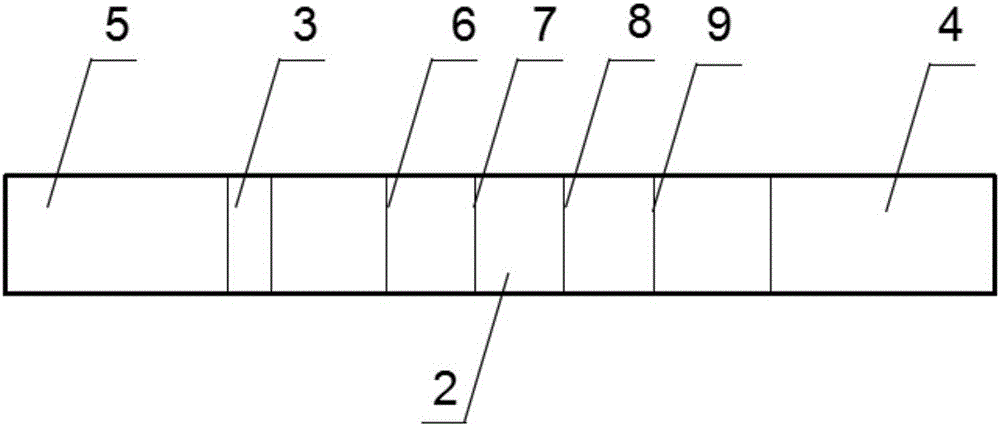
圖2為圖1的正面結構示意圖。圖中6:檢測線I;7:檢測線II;8:檢測線III;9:質控線。
具體實施方式
下面結合附圖具體介紹本實用新型的豬疾病多聯快速檢測試紙條。本領域技術人員應該理解,下面描述的實施例只是為了更好地理解本實用新型,并不用來限制本實用新型。
如圖1所示,根據本實用新型的豬疾病多聯快速檢測試紙條包括底板1、包被膜2、玻璃纖維膜3、吸水紙4和樣品墊5。其中,包被膜2粘貼在底板1上面,包被膜2正面的兩端分別粘貼玻璃纖維膜3和吸水紙4。在玻璃纖維膜3遠離吸水紙4的一端的正面粘貼樣品墊5。底板1通常為PVC材質,包被膜2為硝酸纖維素膜(NC膜)。在玻璃纖維膜3上涂覆有膠體金標記SPA蛋白。
如圖2所示,在包被膜上設有檢測線I 6、檢測線II 7、檢測線III 8和質控線9,檢測線I 6包被豬瘟病毒主要抗原區(rED1),檢測線 II 7包被藍耳病病毒主要抗原區(rED2),檢測線III 8包被O型口蹄疫病毒主要抗原區(rED3),質控線9包被兔抗豬IgG抗體。所述檢測線I 6、檢測線II 7、檢測線III 8和質控線9在包被膜2上呈4條線平行排列,依據檢測線I 6、檢測線II 7、檢測線III 8和質控線9是否出現紅色色帶來進行結果判定。
下述實施例中的主要原材料來源為:豬瘟病毒主要抗原區(rED1)、藍耳病病毒主要抗原區(rED2)、O型口蹄疫病毒主要抗原區(rED3)、豬瘟病毒抗體陽性血清、藍耳病病毒抗體陽性血清、豬O型口蹄疫病毒陽性血清為鄭州中道生物技術有限公司制備并對外提供。其中3種抗原為畢赤酵母真核系統表達,3種陽性血清均為商品化疫苗免疫動物制備。其它試劑和材料均是來源于商業途徑。所述實驗方法,若無特別說明,均為常規實驗方法。
本實用新型的試紙條的具體制備方法如下:
1.1豬瘟、藍耳病、O型口蹄疫病毒主要抗原區(rED)的制備
根據所檢測的病原體,檢索NCBI數據庫并選擇相應參考基因:豬瘟病毒(AF531433.1)、藍耳病病毒(EU807840.1)、O型口蹄疫病毒(JQ973889)。設計3對引物,分別擴增豬瘟、藍耳病和O型口蹄疫病毒主要抗原區基因:
(1)豬瘟病毒rED1:
P1:5'-TTTGAATTCAGACTAGCCTGCAAGGAAGATTAC-3';
P2:5'-TATGCGGCCGCGTTGAAGTCGAAGCCACACC-3';
(2)豬藍耳病病毒rED2:
P3:5'-TTTGAATTCATGCCAAACAACAACGGTAA-3';
P4:5'-TTTGCGGCCGCAGCAGATGGGGAAGCAGTGA-3';
(3)豬O型口蹄疫病毒rED3:
P5:5'-TTTGAATTCACCAGCACCGGTGAAAGCGC-3';
P6:5'-TTTGCGGCCGCCAGGCTCTGTTTCACCGGGG-3'。
根據畢赤酵母密碼子偏好性,對目的基因進行密碼子優化,優化后的基因序列由金唯智生物公司合成。構建重組酵母菌pGAPZαA-GS115,并在YPD培養基中進行1L體積的發酵表達。收集發酵液上清透析過夜,然后進行蛋白活性分析。三種病毒的主要抗 原區經酵母表達后有很好的抗原活性,經Western blot鑒定能與相應的陽性血清發生特異性結合。
1.2包被膜2的制備
在硝酸纖維素膜上分別噴涂豬瘟病毒主要抗原區(rED1)、藍耳病病毒主要抗原區(rED2)、O型口蹄疫病毒主要抗原區(rED3)和兔抗豬IgG抗體,并呈4條線平行排列,分組組成檢測線I 6、檢測線II 7、檢測線III 8和質控線9。37℃烘干處理2h,置裝有干燥劑的密封袋中保存備用。
檢測線I 6:調試噴膜儀,噴液量為1μL/cm,用包被緩沖液稀釋豬瘟病毒主要抗原區(rED1),濃度為2.5mg/mL,用噴膜儀噴涂劃線。
檢測線II 7:調試噴膜儀,噴液量為1μL/cm,用包被緩沖液稀釋藍耳病病毒主要抗原區(rED2),濃度為3.0mg/mL,用噴膜儀噴涂劃線。
檢測線II 8:調試噴膜儀,噴液量為1μL/cm,用包被緩沖液稀釋O型口蹄疫病毒主要抗原區(rED3),濃度為3.0mg/mL,用噴膜儀噴涂劃線。
質控線9:調試噴膜儀,噴液量為1μL/cm,用包被緩沖液稀釋兔抗豬IgG抗體,濃度為1mg/mL,用噴膜儀噴涂劃線。
所述包被緩沖液配方:稱取牛血清白蛋白0.01g,十二水合磷酸氫二鈉30.072g,磷酸二氫鉀2.176g,用超純水溶解,并定容至1000mL。
包被膜2上所劃4條線應細致均勻,相鄰兩線間隔0.4-1.0cm。
1.3玻璃纖維膜3的制備
(1)膠體金溶液的制備
將雙蒸水置于磁力攪拌器上加熱至沸騰,迅速加入濃度為1%的氯金酸溶液至終濃度為0.02%。煮沸5min,之后加入濃度為1%的檸檬酸三鈉溶液,加樣體積為氯金酸溶液的1.8倍。煮沸10min后,冷卻至室溫,再用雙蒸水調整氯金酸濃度為0.02%,常溫避光保存備用。
(2)膠體金標記SPA玻璃纖維膜3的制備
用5M碳酸鉀調節膠體金溶液PH至7.5-8.0,按60ug抗體/mL膠 體金溶液的比例加入SPA蛋白,混勻后靜置5min。再按5%體積的量加入10%牛血清白蛋白溶液,混勻后靜置5min。10000r/min離心30min,棄去上清,用標記洗滌液洗滌1次。沉淀用十分之一初始膠體金體積的金標蛋白保存液溶解,然后按照每毫升溶液鋪10cm2的量噴涂于玻璃纖維膜3上。真空干燥3h,置裝有干燥劑的密封袋中保存備用。
所述10%牛血清白蛋白溶液:取牛血清白蛋白100g,用雙蒸水定容至1000mL。
所述標記洗滌液:取牛血清白蛋白4g,聚乙二醇8000 2g,聚乙烯吡咯烷酮2g,蔗糖2g,Tris 1.211g,用雙蒸水定容至1000mL,并調節PH至8.1。
所述金標蛋白保存液:取牛血清白蛋白25g,聚乙二醇8000 5g,Tris 10.2g,氫氧化鈉2.5g,吐溫20 7.5mL,用雙蒸水定容至1000mL,并調節PH至8.5。
1.4大板組條
各組份規格(長×寬):底板1(30cm×7.6cm)、包被膜2(30cm×2.0cm)、樣品墊3(30cm×3.0cm)、涂覆膠體金標記SPA蛋白的玻璃纖維膜3(30cm×0.7cm)和吸水紙4(30cm×3.2cm)。
各組份按組合方式如下:將包被膜2粘貼在底板1上面,包被膜2正面的兩端分別粘貼玻璃纖維膜3和吸水紙4。在玻璃纖維膜3遠離吸水紙4的一端的正面粘貼樣品墊5。即在底板1上按順序依次粘貼包被膜2、玻璃纖維膜3、吸水紙4、樣品墊5。
1.5切條
用切條機將大板切成單條,每條寬度為3-5mm。
下面再詳細描述本實用新型的試紙條檢測原理和結果判定。
2.1試紙條檢測原理
本實用新型試紙條采用雙抗原夾心法,當被檢樣品中含有豬瘟、藍耳病和豬O型口蹄疫病毒抗體時,則在樣品墊5處與SPA膠體金顆粒標記偶聯物結合,分別形成“SPA偶聯物—病毒抗體復合物”,并在吸水紙4的作用下向前滲透泳動。當復合物到達檢測線I 6,豬瘟病毒抗體與rED1蛋白發生特異性結合,形成“SPA偶聯物—豬瘟病 毒抗體—rED1復合物”,在包被膜2上出現肉眼可見的色帶。當復合物到達檢測線II 7,藍耳病病毒抗體與rED2蛋白發生特異性結合,形成“SPA偶聯物—藍耳病病毒抗體—rED2復合物”,在包被膜2上出現肉眼可見的色帶。當復合物到達檢測線III 8,O型口蹄疫病毒抗體與rED3蛋白發生特異性結合,形成“SPA偶聯物—口蹄疫病毒抗體—rED3復合物”,在包被膜2上出現肉眼可見的色帶。當SPA膠體金顆粒標記偶聯物泳動至質控線9,與兔抗豬IgG抗體結合,在包被膜上出現肉眼可見的色帶。檢測時,吸取待檢血清樣品1滴,加入加樣孔,觀察檢測線和質控線是否出現紅色色帶,從而判定動物體內是否含有豬瘟病毒、豬藍耳病病毒和豬O型口蹄疫病毒抗體。
2.2試紙條結果判定
陽性結果判定:當質控線9出現紅色條帶,檢測線I 6、II 7、III 8分別出現紅色條帶時,分別代表豬瘟、藍耳病和O型口蹄疫病毒抗體陽性。
陰性結果判定:當質控線9出現紅色條帶,而檢測線I 6、II 7、III 8無紅色條帶出現時,表明豬瘟、藍耳病和O型口蹄疫病毒抗體陰性。
無效結果:當質控線9不出現紅色條帶時,檢測結果無效。
- 還沒有人留言評論。精彩留言會獲得點贊!