一種抗Sm抗體IgG測定試劑盒(化學發光法)及其制備方法與流程
本發明涉及體外診斷免疫檢測領域,具體地,本發明提供了一種抗Sm抗體IgG測定試劑盒(化學發光法)及其制備方法。
背景技術:
抗Sm 抗體,以病人名字(Smith) 命名,在這位診斷為紅斑狼瘡的病人血清中,首次發現了該抗體,因此命名。以后大量的報道證實在紅斑狼瘡病人血清中,存在此種抗體,屬于一類抗核抗體。Sm系統中的主要蛋白質抗原為B、B'、D、E蛋白,分子量11~29kD,此外還有A、A'、B"、C、F、G以及68kD、150kD等蛋白質。這些蛋白質與含鳥苷十分豐富的小核RNAs(snRNAs)即UsnRNAs形成復合物。目前在哺乳動物中發現至少有13種UsnRNAs,即U1~U13 snRNAs。Sm抗原由U1、U2、U5、U4/U6與上述蛋白質構成小核核糖核蛋白(U1、U2、U5、U4/U6 snRNP),它在異質性核RNA(hn RNA)向成熟信使RNA(mRNA)的轉化中起重要作用。DNA轉錄的hnRN由編碼片段外顯子(exons)和間斷插入的非編碼片段內含子(introns)組成,hnRNA向mRNA轉化時,U1、U2、U5、U4/U6 RNP分子的RNA部分在切掉非編碼的序列(內含子)、重新連接編碼的RNA序列(外顯子)中起重要作用。經過此種剪接,產生成熟的mRNA,進入細胞質,在核糖體上翻譯成蛋白。已證實抗Sm抗體可進入活的淋巴細胞,可能在與靶抗原結合后干擾其功能,使細胞增殖受抑制,分泌細胞因子(IFN-γ,IL-2等)減少,并誘導細胞凋亡。
目前認為,抗Sm抗體和抗dsDNA一樣,對SLE有高度特異性,且不論是否活動期,抗Sm均可陽性,故可作為SLE的標志性抗體。
臨床檢測抗Sm抗體IgG的主要方法為酶聯免疫吸附法,但該方法存在著下述的不足之處:
(1) 使用12×8型、6×8型、8×12型或整板型96孔專用微孔板作為抗原包被用具和反應容器,在使用時只能分成12批次、6批次、8批次或整板一次使用,無法進行獨立的、單人份的檢測;
(2) 定量測定所用的試劑種類較多,每一種檢測試劑都要用試劑瓶來盛裝,并且每使用一種試劑時都需要更換吸液嘴來分別加注到微孔板的微孔中,不但試劑瓶種類多,加注試劑的操作也極為繁瑣;
(3) 缺少對檢測信息的相應標注,只能通過查看試劑盒外包裝盒的標識才能了解或知悉檢測試劑的生產批號及有效期信息,而且所知悉的信息在檢測過程中不受控,具有很大的隨意性;
(4) 檢測試劑在檢測過程中處于開放的空間,容易引起各種試劑之間的交叉污染而影響檢測結果的準確性;
(5) 檢測過程多采用手工操作,試劑或樣本的加量不很精確,操作過程極為繁瑣和復雜,容易發生操作差錯,檢測結果的準確度和精密度較差;
(6) 在檢測項目成套試劑的數量配置及使用上均為項目數×48/96人份,如果需要檢測10個項目,則試劑的配置及使用數須為10×48/96人份,如果只有一份樣本需要檢測10個不同的項目,也需要配置10×48/96人份的試劑,存在著不夠經濟合理的缺點。
技術實現要素:
目前抗Sm抗體IgG檢測技術存在以下缺點:檢測成本高、檢測靈敏度低、檢測線性范圍窄、重現性低、不能定量、操作復雜等。
本發明正是為了克服以上所述缺點,公開了一種檢測成本低、靈敏度高、檢測線性范圍廣、重現性高、可以定量、操作簡單的抗Sm抗體IgG測定試劑盒(化學發光法)及其制備方法。本發明首先制備化學發光免疫分析試劑盒,主要包括:Sm抗原包被的磁顆粒、鼠抗人IgG包被的吖啶酯以及抗Sm抗體IgG校準品;然后利用全自動化學發光免疫分析儀對校準品進行檢測,繪制標準曲線,內置于電腦軟件,測試實際樣本,根據樣本發光值計算樣本濃度;最后對抗Sm抗體IgG全自動化學發光免疫分析系統進行性能(靈敏度、線性、精密度、干擾性)的評價。
本發明與目前技術相比,具有以下優點:
1、本發明選擇吖啶酯作為標記材料,并應用于化學發光免疫分析系統,該發光體系為直接化學發光,與傳統的酶促化學發光相比,該反應不需要酶的參與,更加節約成本;
2、本發明選用的吖啶酯化學發光免疫分析系統檢測靈敏度高,能夠達到0.33AU/mL,相比其它的抗Sm抗體IgG檢測方法靈敏度至少提高了3倍;
3、本發明選用的吖啶酯化學發光免疫分析系統線性范圍寬,能達到3-165 ng/mL,其它的抗Sm抗體IgG化學發檢測方法的檢線性范圍為20-135 ng/mL;
4、本發明選用的吖啶酯化學發光免疫分析系統重復性高,批內及批間差均在5%以內,這是其它化學發光免疫分析系統難以達到的;
5、本發明的化學發光免疫分析系統已實現樣本的定量,通過內置標準曲線到測試軟件,只需測試樣本就可直接得到樣本的濃度值;
6、本發明的化學發光免疫分析系統已實現全自動化,試劑及樣本的添加全有儀器完成,操作更加簡便,減少了人為的誤差。
附圖說明
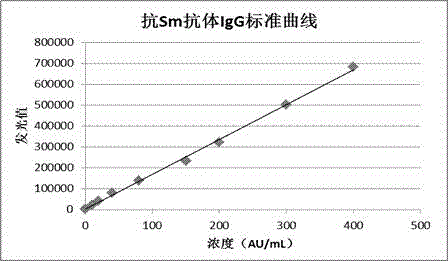
圖1為實施例3得到的抗Sm抗體IgG標準曲線圖。
具體實施方式
實施例1:抗Sm抗體IgG測定試劑盒(化學發光法)制備方法
(1)Sm抗原包被的納米磁珠制備:
取50mg羧基化的磁微粒(粒徑為0.05-1um)懸浮液,磁分離去上清,用0.02 M,pH為5.5 MES緩沖液重懸,加入0.5-2mL新配置的10 mg/mL的EDC水溶液,活化磁珠表面羧基,加入3-5 mg Sm抗原,室溫下混懸2-10 h,磁分離,去除上清,用含2% BSA 的0.1 M pH為8.0的Tris緩沖液重懸到1mg/mL,得到Sm抗原包被的磁顆粒,每瓶5mL分裝保存于4℃備用。
(2)鼠抗人IgG標記的吖啶酯的制備:
取50 uL 5mg/mL的鼠抗人IgG,加入150 uL 0.1-0.2 M pH 9.0-9.5的碳酸鹽緩沖液,混勻,然后加入1-2 uL 5 mg/mL的吖啶酯混勻,室溫下避光反應,1-2 h后取出,用2 mL的zeba離心脫鹽柱脫鹽處理,脫鹽過程中首先分別用純凈水及TBS緩沖液進行處理,最后加入得到的鼠抗人IgG標記的吖啶酯溶液,收集離心管中的液體至保存管得到鼠抗人IgG標記的吖啶酯,每瓶5 mL分裝保存于4℃備用。
(3)抗Sm抗體IgG校準品的制備:
用標準品緩沖液(50 mM Tris,5% BSA,0.15% NaCl,pH 7.4)將抗Sm抗體IgG配置成濃度為0 AU/mL、20 AU/mL、200 AU/mL,每瓶1 mL分裝,4 ℃保存備用。
(4)化學發光預激發液的配制:
量取1.0升純化水,依次加入80uL質量分數為20%的雙氧水(H2O2)、1.0克疊氮化鈉、1.5克吐溫20,搖勻后避光存放。
(5)化學發光激發液的配制:
量取1.0升純化水,依次加入0.6克氫氧化鈉、0.5克PC300、0.5g疊氮化鈉、1.5克Triton 405,搖勻后避光存放。
實施例2:抗Sm抗體IgG測定試劑盒(化學發光法)檢測方法:
本發明以全自動化學發光免疫分析儀為檢測工具,本發明的方法學模式為間接法,即儀器加入10 uL的樣品用樣本稀釋液10倍稀釋后取10ul、然后加入50 uL的Sm抗原包被的磁顆粒反應10min后,進行磁分離;再依次加入50 uL的測試稀釋液與50ul的鼠抗人IgG標記的吖啶酯,反應10 min后,進行磁分離,儀器將反應混合物送入暗室,依次加入50uL化學發光預激發液、50uL化學發光激發液進行發光反應,最后記錄發光強度,從標準曲線計算出被測樣品的 抗Sm抗體IgG含量。
實施例3:抗Sm抗體IgG測定試劑盒(化學發光法)性能評價
檢測曲線見附圖1。
靈敏度的檢測:
參照CLSI EP17-A 文件推薦實驗方案,計算抗Sm抗體IgG測定試劑盒(化學發光法)的靈敏度,求得的靈敏度為0.33 AU/ mL。
線性的檢測:
對濃度為12.5 AU/mL、25 AU/mL、50AU/mL、100 AU/mL、200 AUmL標準品做線性分析,計算線性相關系數,r=0.9996,另外,該試劑盒對抗Sm抗體IgG樣品檢測的線性范圍為10-200 AU/mL。
精密度測定:
取濃度為30 AU/mL及150 AU/mL兩個抗Sm抗體IgG樣品,每個樣本每個濃度各做3個平行,用三批試劑盒進行檢測,計算試劑盒批內及批間差,結果表明該試劑盒批內及批間差均小于5%。
干擾性實驗:
取混合血清分別添加干擾物包括: 結合膽紅素、游離膽紅素、血紅蛋白、抗壞血酸、甘油酯,添加比例按照 1: 20 進行,分別測定混合血清及添加了各種干擾物后混合血清的測值,計算二者之間的偏差,以 ±10%為可接受范圍。結果表明,干擾性均達到 NCCLS 的文件標準,可用于臨床實驗室抗Sm抗體IgG的準確評估。
實施例4:抗Sm抗體IgG測定試劑盒(化學發光法)的靈敏度對比實驗
分別用化學發光檢測方法和傳統的酶聯免疫吸附法對濃度為0 AU/mL的校準品或樣本稀釋液為樣本進行檢測,重復測定20次,得出20次測量結果的RLU值(相對發光值),計算其平均值(M)和標準差(SD),得出M+2SD,將該發光值代入校準曲線計算得到相應的濃度值。采用化學發光檢測方法得到的濃度值為0.33 AU/ml,相對于傳統的酶聯免疫吸附法最低檢測限1 RU/ml,提高了3倍。
- 還沒有人留言評論。精彩留言會獲得點贊!