一種用于檢測乳鐵蛋白含量的適配體及其應用的制作方法
本發明屬于生物檢測技術領域,具體涉及一種使用熒光偏振法對乳鐵蛋白進行檢測的適配體及其應用。
背景技術:
熒光偏振技術作為一種簡單可靠的信號傳導手段,可以基于熒光基團的分子質量的變化提供關于分子取向、遷移和作用過程的信息。熒光偏振分析法具有很多的優勢:第一,它是一種均相分析方法且靈敏度高,無需分離等復雜操作,結果重現性好;第二,響應時間快,可以實時監測分子間相互作用;第三,可以與酶標儀等儀器聯用,可以實現自動化高通量測定;第四,熒光偏振依賴于兩個垂直方向上的熒光強度的比值,與熒光絕對強度無關,熒光偏振值對熒光的波動及光漂白不敏感,從而成為在復雜生物樣品中均相測定目標分子的理想分析方法。因此,熒光偏振技術在熒光傳感應用中受到廣泛的研究關注。
乳鐵蛋白是一種極具廣闊市場前景的功能性蛋白,它主要存在于哺乳動物的乳汁中,其含量與動物的種屬息息相關,以人乳、牛乳為典型代表。研究表明,乳鐵蛋白具有多種生物學活性。它具有參與鐵代謝、抗腫瘤、抗氧化、抗菌、阻斷氧自由基、免疫調節及抗炎癥、促進細胞增長、減少內臟脂肪等多種功能。且由于乳鐵蛋白是一種可被嬰兒攝入的、安全極高的天然乳成分,其在日本被批準為食品添加劑,在美國被納入一般認為安全物質之中。加之,乳鐵蛋白廣泛的生物學功能深受國內外食品相關企業的高度重視,在我國GB 14880—2012《食品營養強化劑使用標準》中,乳鐵蛋白也被列為一種新型營養強化劑并規定了其在相關乳制品中的含量標準。因而,能否建立快速準確的乳鐵蛋白檢測技術對于食品安全來說至關重要。目前,適合不同類型生物樣品中乳鐵蛋白的檢測技術主要有分光光度法、高效液相色譜法、酶聯免疫吸附法、高效親和色譜法、高效毛細血管電泳法以及表面等離子共振技術等檢測技術,但這些方法依然存在前處理過程復雜、實際樣品回收率低、穩定性差等特點,因此建立出一種能夠全面實現準確、快速、無需對樣品進行前處理的全自動乳鐵蛋白檢測方法十分重要且緊迫。
技術實現要素:
本發明所要解決的技術問題是提供一種用于檢測乳鐵蛋白含量的適配體。
本發明還要解決的技術問題是提供上述適配體在檢測乳鐵蛋白中的應用。
為解決上述技術問題,本發明采用的技術方案如下:
一種用于檢測乳鐵蛋白含量的適配體,所述適配體的核苷酸序列如SEQ ID NO.5~65所示,所述的適配體優選SEQ ID NO.6、SEQ ID NO.18、SEQ ID NO.20、SEQ ID NO.35。
上述用于檢測乳鐵蛋白含量的適配體在檢測乳鐵蛋白中的應用。
一種熒光偏振法測量陰性蛋白含量的方法,包括如下步驟:
(1)繪制標準曲線:向10μL、40nM~4000nM異硫氰酸熒光素標記的適配體溶液中加入100μL不同濃度的陰性蛋白標準樣品,混勻,所述適配體的核苷酸序列為SEQ ID NO.1~61中的任一種,25℃~40℃下反應5~120min,用酶標儀檢測,激發波長為480nm,發射波長為528nm,繪制標準曲線;
(2)樣品檢測:將異硫氰酸熒光素標記的適配體與待測樣品混合,按照步驟(1)的條件檢測。
其中,所述異硫氰酸熒光素標記的適配體的濃度為40nM~4000nM;
其中,所述待測樣品的濃度為0.78~50μg/mL。
其中,所述的陰性蛋白為乳鐵蛋白、α-乳白蛋白、β-乳球蛋白、BSA,優選乳鐵蛋白。
有益效果:
本發明以FITC標記的適配體為探針,通過乳鐵蛋白與探針的特異性結合使熒光偏振信號發生改變,且乳鐵蛋白濃度對數值與熒光偏振信號呈線性變化,從而實現對乳鐵蛋白的定量檢測。該種熒光偏振法靈敏度高,抗干擾性非常強,可以有效避免假陽性信號,實現對復雜樣品中目標物的測量,如牛奶中乳鐵蛋白的測量,該方法檢測的線性范圍為0.78~50μg/mL。
附圖說明
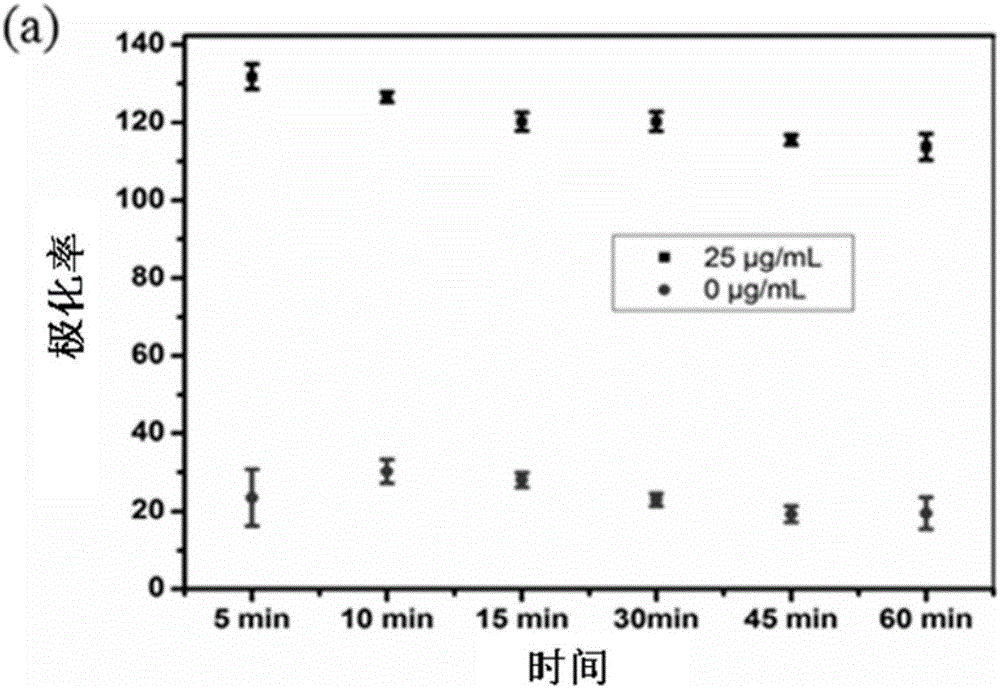
圖1熒光偏振法反應時間優化圖。
圖2不同濃度乳鐵蛋白與熒光偏振信號關系圖。
圖3熒光偏振法對乳鐵蛋白特異性檢測圖。
圖4熒光偏振法對乳鐵蛋白檢測線性圖。
圖5其他適配體對乳鐵蛋白熒光偏振檢測線性圖。
具體實施方式
根據下述實施例,可以更好地理解本發明。然而,本領域的技術人員容易理解,實施例所描述的內容僅用于說明本發明,而不應當也不會限制權利要求書中所詳細描述的本發明。
實施例1:乳鐵蛋白適配體篩選
乳鐵蛋白適配體篩選的具體步驟,包括芯片制備、正負篩過程、PCR擴增等詳細過程,具體如下所述,其中:
文庫:5′-TAMRA-GACAGGCAGGACACCGTAAC-N40-CTGCTACCTCCCTCCTCTTC-3′
TARMA修飾的前向引物:5′-TARMA-GACAGGCAGGACACCGTAAC-3′
生物素化的后向引物:5′Biotin-GAAGAGGAGGGAGGTAGCAG-3′
(1)芯片制備:利首先利光刻掩模與化學腐蝕相結合的技術制作微流控通道模板作為PDMS通道制做磨具;后稱取質量比為10:1的PDMS前聚體與固化劑充分混合,抽真空后澆到微流控通道模板上經固化后得到PDMS微流控通道;使用點樣儀在玻璃基片點制濃度為5mg/mL的乳鐵蛋白和陰性蛋白微陣列,并對PDMS和點樣后的玻璃基片同時等離子處理,之后緊密貼合共同作為篩選芯片,用于接下來的每輪篩選;篩選準備:將步驟(1)得到的篩選芯片放入恒溫水浴箱中37℃下孵育蛋白2h;再通入20mg/mlBSA和0.01mM隨機序列短鏈ssDNA(20nt)在37℃條件下封閉1h;之后用150μL,1×PBST溶液清洗正負篩通道;
(2)第一輪篩選:將0.5nmol,125μL原始文庫在95℃加熱5min,并立即在冰上冷凍10s;再用注射泵以2.5μL/min流速將文庫輸進正篩通道,在常溫條件下反應50min;之后以15μL/min流速通入150μL,1×PBS緩沖溶液以除去正篩通道中未結合的ssDNA序列;輕輕撕掉PDMS層,使用Luxscan~10K/A微陣列掃描儀掃描芯片;最后用DPEC水在95℃下加熱5min洗脫乳鐵蛋白結合的ssDNA序列,所得溶液在50℃條件下高純氮吹干至體積為69μL;
(3)PCR擴增過程:將步驟(2)所得溶液分為體積均為23μL的3份相同溶液,每份依次加入25μL,2×Taq聚合酶,1μL,20μM TAMRA標記的前向引物和1μL,20μM生物素化的后向引物,混合均勻后進行PCR擴增;PCR的熱循環過程如下:94℃5min;循環94℃30s,60.5℃30s,72℃30s過程10輪,72℃5min終止反應;該步驟獲得的產物稀釋10倍后作為模板進行再一次擴增:取5μL稀釋后PCR產物與25μL,2×SYBRPremix Ex TaqTM酶,1μL,20μM TAMRA標記的前向引物,1μL,20μM生物素化的后向引物以及18μL DPEC水充分混合均勻,PCR擴增每進行一輪便取10μL樣品至微孔板中用BioTek檢測其熒光信號,熒光信號最高者作為最佳輪數,剩余產物均擴增該輪數;
(4)分離純化:將步驟(4)得到的PCR產物與600μL Promega磁珠充分混勻,在搖床上快速搖動1h后除去上清液;再加入25μL,50mM NaOH渦旋5min將磁珠上連接的雙鏈解離;吸取上層清液并依次加入12.5μL 100mM HCl,25μL H2O,62.5μL2×PBSM中和,所得的溶液作為下一輪篩選的次級文庫,其含量約為40pmol;
(5)第二輪篩選:用泵以2.5μL/min流速將文庫輸進負篩通道,在常溫條件下反應50min;再用泵以2.5μL/min流速將文庫輸進正篩通道,在常溫條件下反應50min;接著以15μL/min流速通入150μL 1×PBS緩沖溶液除去正篩通道中未反應的鏈;輕輕撕掉PDMS層,使用Luxscan~10K/A微陣列掃描儀掃描芯片;最后用無核水在95℃下加熱5min洗脫蛋白結合的鏈,所得溶液在60℃吹干至體積為92μL,留作PCR擴增;
(6)重復步驟(4)、(5)、(6)至第八輪篩選;
(7)將篩選的第五、六、七輪PCR擴增產物送至上海生工測序,每輪隨機選取120條測序,再用IDT軟件對得到的鏈進行二級結構分析,最終獲得最佳的適配體。
實施例2:熒光偏振法對乳鐵蛋白標準樣品進行檢測:
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N2(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入100μL濃度為25μg/mL的乳鐵蛋白標準樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
實施例3:熒光偏振法反應時間優化
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N2(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入100μL濃度為25μg/mL的乳鐵蛋白標準樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下分別反應5min、10min、15min、20min、25min、30min、35min、40min、45min、50min、55min、60min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
圖1為不同時間條件下熒光偏振信號與空白溶液中熒光偏振信號圖。
實施例4:不同濃度乳鐵蛋白與熒光偏振信號關系
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N2(堿基序列:CGGTGCATCTATGGCTACTAGCTTTTCCTGCCTATACTAC)溶液中分別加入100μL濃度為0.19μg/mL,0.39μg/mL 0.78μg/mL,1.56μg/mL,3.12μg/mL,6.25μg/mL、12.5μg/mL、25μg/mL、50μg/mL的乳鐵蛋白標準樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
(3)通過分析,發現分析熒光偏振信號隨乳鐵蛋白濃度的對數值呈線性變化,得到標準曲線,由標準曲線計算得到樣品中乳鐵蛋白的濃度。
圖2為加入不同濃度乳鐵蛋白的熒光偏振值圖,圖d為標準曲線圖(R=0.988)。
實施例5:熒光偏振法對乳鐵蛋白特異性檢測
(1)在五份10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N2(堿基序列:CGGTGCATCTATGGCTACTAGCTTTTCCTGCCTATACTAC)溶液中分別將加入100μL25μg/mL的乳鐵蛋白、100μL 500μg/mL α-乳白蛋白、100μL 500μg/mL β-乳球蛋白、100μL 500μg/mL BSA和100μL PBS溶液,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
圖3為該種熒光偏振法對乳鐵蛋白、α-乳白蛋白、β-乳球蛋白、BSA的特異性檢測圖。
實施例6:檢測乳鐵蛋白含量的方法
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N2(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入稀釋25-100倍的牛奶樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
(3)對比標準曲線得到牛奶樣品中乳鐵蛋白的濃度,具體見圖4。
實施例7:檢測乳鐵蛋白含量的方法
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N6(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入稀釋25-100倍的牛奶樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
(3)對比標準曲線得到牛奶樣品中乳鐵蛋白的濃度,具體見圖5(a)。
實施例8:檢測乳鐵蛋白含量的方法
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N14(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入稀釋25-100倍的牛奶樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
(3)對比標準曲線得到牛奶樣品中乳鐵蛋白的濃度,具體見圖5(b)。
實施例9:檢測乳鐵蛋白含量的方法
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N16(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入稀釋25-100倍的牛奶樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
(3)對比標準曲線得到牛奶樣品中乳鐵蛋白的濃度,具體見圖5(c)。
實施例10:檢測乳鐵蛋白含量的方法
(1)在10μL,250nM FITC(異硫氰酸熒光素)標記的適配體N31(堿基序列:AGGCAGGACACCGTAACCGGTGCATCTATGGCTACTAGCTTTTCCTGCCT)溶液中加入稀釋25-100倍的牛奶樣品,充分混勻。
(2)將步驟(1)的混合液置于96微孔板中37℃條件下反應15min,用BioTeK酶標儀直接掃描,激發波長為480nm,發射波長為528nm。
(3)對比標準曲線得到牛奶樣品中乳鐵蛋白的濃度,具體見圖5(d)。
本發明將熒光偏振方法應用于乳鐵蛋白的分析檢測中,當乳鐵蛋白的濃度在0.78μg/mL~50μg/mL之間,熒光偏振信號強度與乳鐵蛋白濃度的對數之間具有很好的相關性,相關系數為0.988。同時,本發明能快速高通量檢測乳鐵蛋白,不僅可以避免假陽性信號的產生而且可以防止外界環境的干擾,信號采集方式簡單快速。
- 還沒有人留言評論。精彩留言會獲得點贊!