肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球及應用的制作方法
本發明屬于熒光免疫層析
技術領域:
,具體涉及一種肌紅蛋白熒光免疫層析試紙條用的活化熒光乳膠微球及其制備和應用。
背景技術:
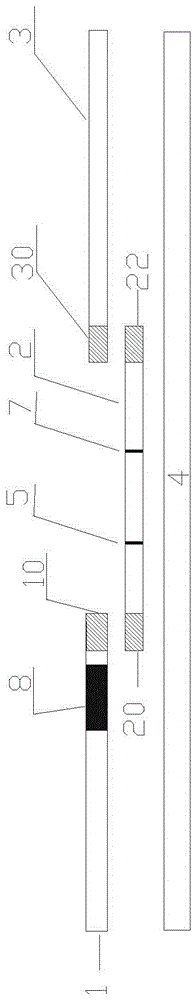
:熒光免疫層析試紙條(試劑卡)因其快速便捷的特性,廣泛用于快檢領域。待測物抗體標記熒光乳膠微球,乳膠微球在液相中存在著表面電子斥力和范德華力使得液相中的乳膠顆粒保持均勻分布。但是噴涂于玻璃纖維素膜并烘干后隨著溶液被蒸發干,表面張力推動乳膠顆粒間無限靠近導致分子間斥力消失,范德華力增大,最終使得多個乳膠分子團聚成大大小小不同的顆粒。當免疫層析時加入樣本復溶乳膠微球時,乳膠微球不再均勻分散導致層析失敗。因此本領域多采用熒光免疫層析試劑盒,含試紙條加上樣本緩沖液。增加了檢測復雜度。或者由于乳膠微球部分凝聚,使得檢測靈敏度降低,檢測結果出現假陰性。另外,乳膠微球的不穩定,也會使得熒光試紙條的穩定性差,不便于保存以及運輸。肌紅蛋白(Myoglobin)是一種存在于心肌和骨骼肌細胞質的蛋白質。它為肌細胞運送氧氣,同時也可以作為一個儲氧囊。肌紅蛋白分子量為17.8kD,因此肌細胞受損后該蛋白可迅速進入血液循環。測定血清中的肌紅蛋白是診斷急性心肌梗塞(AMI)、再梗塞以及溶栓治療后成功再灌入診斷的指標之一。濃度在癥狀出現后約兩個小時肌紅蛋白濃度升高,因此可作為診斷心肌梗塞的早期指標。根據不同的再灌入治療措施,在梗塞形成開始之后,血液循環中的肌紅蛋白濃度在梗塞發生后4到12小時可達到高峰,約24小時之后下降至正常水平。骨骼肌受損后以及腎功能嚴重障礙也可導致肌紅蛋白濃度升高。技術實現要素:本發明所要解決的技術問題是:熒光免疫層析試紙條的熒光乳膠微球在烘干后,容易團聚,分散不均勻,從而導致層析失敗或使得檢測靈敏度降低。為了解決上述技術問題,本發明提供了一種肌紅蛋白熒光免疫層析試紙條用的活化熒光乳膠微球及其制備,應用該活化熒光乳膠微球制備的肌紅蛋白干式熒光免疫層析試紙條,本試紙條可用于體外定量測定人血清、血漿或全血中肌紅蛋白的含量。本發明的試紙條可以解決熒光乳膠微球在噴涂、烘干玻璃纖維素膜時發生團聚的現象,以便制備標記物墊,從而得到干式熒光免疫層析試紙條,無需稀釋液配置檢測試劑盒。本發明提供的肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球的制備方法,包括如下步驟:1)取表面活性劑加入pH為8~10的緩沖溶液中,再加入二甲基甲酰胺、N,N’-二環己基碳二亞胺和N-羥基琥珀酰亞胺;2)取氨基表面的熒光乳膠微球的分散液,以緩沖溶液調pH至8~10后,加入到步驟1)所得的混合物中,攪拌反應,反應完畢后,離心去除上清液,得到活化熒光乳膠微球;其中,所述表面活性劑為氨基酸型表面活性劑和硬脂酸鹽的混合物,氨基酸型表面活性劑與硬脂酸鹽的重量比為2~6:1。優選地,所述硬脂酸鹽為硬脂酸鈉,所述氨基酸行表面活性劑為N-十二烷基丙氨酸。更優選地,N-十二烷基丙氨酸與硬脂酸鈉重量比為3:1。。優選地,所述表面活性劑與所述氨基表面的熒光乳膠微球的質量比為500~2000:1。優選地,步驟1)和步驟2)中所述的緩沖溶液為碳酸緩沖液;步驟2)中的攪拌反應時間為2~4小時,溫度為20~30℃;氨基表面的熒光乳膠微球為氨基聚苯乙烯熒光微球。本發明還提供上述的制備方法得到的肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球。本發明還提供上述的肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球的標記物工作液的制備方法:取肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球分散于微球緩沖液中,得到標記物工作液;表面活化的熒光乳膠微球在標記物工作液中所占的比例為0.5~2wt%;其中,微球緩沖液的制備方法為:將BSA、生物防腐劑、雷米邦A和甜菜堿溶于0.01M、pH7.4的磷酸緩沖液中。優選地,BSA(牛血清蛋白)、生物防腐劑、雷米邦A和甜菜堿在所述微球緩沖液中的濃度均為0.1wt%。本發明還提供肌紅蛋白熒光免疫層析試紙條的標記物墊的制備方法,包括如下步驟:1)活化熒光乳膠微球標記的兔IgG的制備:取上述制備方法得到的標記物工作液,離心,棄上清液后,用標記緩沖液復溶,并且同時加入碳二亞胺和兔IgG,攪拌反應,然后離心,棄上清液,最后用標記稀釋液復溶;2)活化熒光乳膠微球標記的標記用鼠抗人肌紅蛋白單克隆抗體的制備方法:取上述制備方法得到的標記物工作液,離心,棄上清液后用標記緩沖液復溶,并且同時加入碳二亞胺和標記用鼠抗人肌紅蛋白單克隆抗體,攪拌反應,然后離心,棄上清液,最后用標記稀釋液復溶;3)取步驟1)所得分散液和步驟2)所得分散液,混合,噴涂于玻璃纖維之上,烘干;所述標記緩沖液的配方為:碳酸鈉4.33g、碳酸氫鈉2.96g,溶于1000mL水中;所述標記稀釋液的配方為:檸檬酸三鈉7.33g、檸檬酸4.44g、氫氧化鈉1g,溶于1000mL水中。本發明提供一種肌紅蛋白熒光免疫層析試紙條,包括上述的標記物墊、包被墊和吸收墊,其中所述標記物墊搭接于包被墊的一端上,吸收墊搭接于包被墊的另一端上,包被墊上設有質控線和檢測線,質控線上包被有羊抗兔IgG的抗體,檢測線上包被有包被用鼠抗人肌紅蛋白單克隆抗體。本發明能夠達到如下技術效果:1、本發明研究發現經特定的表面活性劑活化的熒光乳膠微球在烘干時保持顆粒間的相對距離不易團聚。層析過程時,加入樣本能即刻復溶并順利層析,以便制備干式熒光免疫層析試紙條(試劑卡),方便用戶使用,且檢測結果穩定、準確、可靠。2、本發明通過實驗篩選出適合用于肌紅蛋白熒光免疫層析試紙條的熒光乳膠微球的特定表面活性劑組合。采用特定的表面活性劑事先處理化學修飾的熒光乳膠微球,處理后的乳膠微球標記肌紅蛋白抗體,用于制備肌紅蛋白熒光免疫層析試紙條的標記物墊,實現乳膠微球均勻噴涂,無團聚現象。并且,在加入待測樣本后,標記的熒光乳膠微球可以快速的、順利實現層析,無需特殊樣本稀釋液或者緩沖液處理試紙條。3、本發明所制備的肌紅蛋白干式熒光免疫層析試紙條,穩定性強,操作簡便,用戶友好,檢測結果準確、可靠,靈敏度高。附圖說明圖1是本發明的肌紅蛋白熒光免疫層析試劑卡的截面分解結構示意圖。圖2是本發明的肌紅蛋白熒光免疫層析試劑卡的俯視結構示意圖。圖3是肌紅蛋白標準曲線的建立。圖4全血樣本中肌紅蛋白含量測定曲線。圖5是實施例4的試紙條的熒光信號曲線。圖6是實施例5的試紙條的熒光信號曲線。圖7是實施例6的試紙條的熒光信號曲線。圖8是對比例的試紙條的熒光信號曲線。具體實施方式下面結合附圖和具體實施例對本發明作進一步說明,以使本領域的技術人員可以更好的理解本發明并能予以實施,但所舉實施例不作為對本發明的限定。本發明提供了一種肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球,包括如下步驟:1)取表面活性劑加入pH為8~10的緩沖溶液中,加入二甲基甲酰胺、N,N’-二環己基碳二亞胺和N-羥基琥珀酰亞胺,攪拌反應;2)取氨基表面的熒光乳膠微球的分散液,以緩沖溶液調pH至8~10后,加入到步驟1)所得的混合物中,攪拌反應,反應完畢后,離心去除上清液,得到活化熒光乳膠微球;所述表面活性劑為氨基酸型表面活性劑和硬脂酸鹽的混合物,氨基酸型表面活性劑與硬脂酸鹽的重量比為2~6:1。本發明采用氨基酸型表面活性劑和硬脂酸鹽(陰離子型和兩性表面活性劑混合)通過共價偶聯的方法修飾乳膠微球外表面,使其具有疏水性。采用處理后的活化熒光乳膠微球標記肌紅蛋白抗體。熒光乳膠微球標記的肌紅蛋白抗體與熒光乳膠微球標記的兔IgG混勻后噴涂在玻璃纖維素膜上制備成標記物墊1,包被墊2(硝酸纖維素膜)靠近質控線的一端覆蓋上吸水墊,靠近檢測線的另一端覆蓋標記物墊,用于制備干式熒光免疫層析試劑卡,檢測線上包被包被用肌紅蛋白抗體。加入待測樣本后,肌紅蛋白與熒光乳膠微球標記的肌紅蛋白抗體接觸反應,乳膠微球能夠保持分散狀態不團聚,且在接觸待測樣本后可迅速、均勻分散,并沿著硝酸纖維素膜快速層析。本發明以下實施例中所用的熒光乳膠微球是指被化學修飾的氨基表面的聚苯乙烯熒光微球,直徑100-500nm。一、活化熒光乳膠微球的制備實施例11)取表面活性劑(7.5mgN-十二烷基丙氨酸,2.5mg硬脂酸鈉)首先溶解在0.5MpH9.6的碳酸緩沖液(H值到9.6),再加入在0.1ml的DMF中,0.1ml的DMF中,加入N,N’-二環己基碳二亞胺(DCC)1mg和0.6mgN-羥基琥珀酰亞胺(NHS)后室溫攪拌3小時。2)將1ml含1%固體物的氨基表面的熒光乳膠微球溶液用0.5MpH9.6的碳酸緩沖液調PH值到9.6后加入到步驟1)中,繼續攪拌反應3小時。既得活化的乳膠微球。3)用高速離心機將熒光乳膠微球反應液高速離心分離,去除反應溶液上清液,用1mL微球緩沖液復溶熒光乳膠微球,形成標記物工作液。微球磷酸緩沖液配制:0.01MpH7.4的磷酸緩沖液,含0.1wt%BSA,含0.1wt%生物防腐劑,含0.1wt%雷米邦A,含0.1wt%甜菜堿。微球磷酸緩沖液提供一定的例子強度和PH值,使微球均勻分散。實施例2本實施例的操作方法與實施例1類似,不同之處在于,步驟1)中表面活性劑為:9mgN-十二烷基丙氨酸,1.5mg硬脂酸鈉。實施例3本實施例的操作方法與實施例1類似,不同之處在于,步驟1)中表面活性劑為:6mgN-十二烷基丙氨酸,3mg硬脂酸鈉。二、以肌紅蛋白熒光免疫層析試紙條為例對實施例1~3制備的活化熒光乳膠微球的應用及效果進行說明。實施例4采用實施例1得到的標記物工作液制備的熒光免疫層析試紙條1)熒光乳膠微球標記的兔IgG:取5mL實施例1得到的標記物工作液,用離心機離心30min(轉速為10000r/min),離心完后棄上清液,用5mL標記緩沖液復溶,再加入1mg的兔IgG混勻,另加入5mg碳化二亞胺,室溫攪拌反應1h,然后離心15min(轉速為10000r/min),棄上清液,用10mL的標記物稀釋液稀釋復溶混勻后備用。2)熒光乳膠微球標記的標記用鼠抗人肌紅蛋白單克隆抗體取10mL實施例1得到的標記物工作液,用離心機離心30min(轉速為10000r/min),離心完后棄上清液,用10mL標記緩沖液復溶,再加入2mg的標記用鼠抗人肌紅蛋白單克隆抗體混勻,另加入10mg碳化二亞胺,室溫攪拌反應1h,然后離心15min(轉速為10000r/min),棄上清液,用20mL的標記物稀釋液稀釋復溶混勻后備用。步驟1)和2)中標記緩沖液的配方為:碳酸鈉4.33g、碳酸氫鈉2.96g,溶于1000mL水中;標記稀釋液的配方為:檸檬酸三鈉7.33g、檸檬酸4.44g、氫氧化鈉1g,溶于1000mL水中。3)標記物墊制備步驟2)得到的熒光乳膠微球標記的標記用待測物抗體與步驟1)得到的熒光乳膠微球標記的兔IgG混勻,二者體積比例為2:1。然后將混勻的熒光乳膠微球按1微升/厘米的量均勻噴涂在玻璃纖維素紙上轉置45℃的烘干箱烘干2小時即完成標記物墊的制備。4)包被液制備:取包被用鼠抗人肌紅蛋白單克隆抗體加入磷酸鹽緩沖液中,制成檢測線包被液;取羊抗兔IgG加入磷酸鹽緩沖液中,制成質控線包被液。該磷酸鹽緩沖液的配方為:0.99g磷酸二氫鈉,5.16g磷酸氫二鈉溶于1000mL純化水中。5)包被墊的處理:檢測線包被液在包被墊上劃線包被形成檢測線,質控線包被液在在包被墊上劃線包被形成質控線,然后干燥。6)試紙條組裝:將干燥好的標記物墊和剪裁好的吸收墊(吸水紙),按包被墊(硝酸纖維素膜)靠近質控線的一端覆蓋上吸收墊,靠近檢測線的另一端覆蓋標記物墊的要求進行貼條。按切條機標準操作規程進行操作,切成4mm±0.1mm寬的試紙條。如圖1和2所示,試紙條包括:包被墊2(硝酸纖維素膜),其兩端各設有一連接段(如圖所示第一連接段20、第二連接段22),兩連接段中間為檢測段21,檢測段21表面設有檢測線5和質控線7;標記物墊1(玻璃纖維素膜),其一端設有連接段10,標記物墊的連接段10覆蓋并固定于包被墊2的第一連接段20上;標記物墊1上噴涂有標記物8,具體在一實施方式中,是在靠近連接段10附近(距連接段2mm,標記物沿包被墊長度方向的長度為5mm)噴涂標記物8(含有熒光乳膠微球標記的兔IgG和熒光乳膠微球標記的標記用鼠抗人肌紅蛋白單克隆抗體)。吸收墊3(吸水紙),其一端設有連接段30,吸收墊的連接段30覆蓋并固定于包被墊2的第二連接段22上;底板4,包被墊2、標記物墊1和吸收墊3均固定于底板上。本試紙條在使用時用一株鼠抗人肌紅蛋白單克隆抗體(包被用鼠抗人肌紅蛋白單克隆抗體)在硝酸纖維素膜上劃線包被,作為測試線,用羊抗兔多抗在硝酸纖維素膜上劃線包被制成質控線。將乳膠熒光微球標記的另一株鼠抗人肌紅蛋白單克隆抗體(標記用鼠抗人肌紅蛋白單克隆抗體)與乳膠熒光微球標記的兔IgG混勻后噴涂在玻璃纖維素膜上制備成標記物墊。硝酸纖維素膜靠近質控線的一端覆蓋上吸水墊,靠近測試線的另一端覆蓋標記物墊。往標記物墊上加入標準品或待測血樣,抗原就會與標記物混合反應并沿著硝酸纖維素膜層析,分別與測試線和質控線反應。當測試結果有效時,質控線顯示一定光強度。這時測試線上的光信號強度比質控線光信號強度的比值(T/C)與樣本濃度成正相關,通過標準曲線計算即可得出待測樣品濃度。(一)本實施例制得的試紙條校準曲線及待測樣本的測定將50ul校準品或者待測樣本緩慢滴加在標記物墊上。在室溫條件下靜置15分鐘反應,反應結束后將試紙條放入到Savant-100熒光免疫層析分析儀中檢測。校準品的每個濃度點重復做3遍,取T/C面積比的平均值后與濃度生成一條標準曲線(線性范圍10-500ng/mL)。標準曲線測定結果如下表所示,標準曲線如附圖3所示。線性x1x2x3x4x59.70128.54280.65370.85487.708.49124.15280.45378.51512.1010.41130.55240.54384.78467.29平均值9.53127.75267.21378.05489.03SD0.973.2723.106.9722.43CV10.18%2.56%8.64%1.85%4.59%理論值平均值x111.239.53x2130.34127.75x3249.44267.21x4368.55378.05x5487.65489.03取線性范圍內的3個樣本重復檢測15次,其變異系數(CV%)應不高于15.0%,來驗證試紙條的重復性:收集臨床樣本200例,與德國羅氏(ROCHE)醫學診斷產品肌紅蛋白檢測試劑盒(電化學發光法)進行對比檢測,樣本檢測值如附圖4所示,可見當r>0.975時,證明與德國羅氏(ROCHE)醫學診斷產品的檢測結果等同,具有同樣的有效性。(二)關于熒光乳膠微球的分散性和涌動性試紙條的層析完成后,使用儀器采集包被墊的檢測段21上的熒光信號,其將檢測段沿長度方向平分為300段,每段為單位輸出電信號(熒光強度)。共計輸出300個電信號,如圖5所示。圖5中,縱坐標:FluonescenceIntensity發光強度;橫坐標:檢測段21的位置長度(檢測段21靠近第二連接段22的一側邊為0);橫坐標50-100測的是質控線7,取值是50-100此段的峰面積。橫坐標200-250測的是檢測線5,取值是200-250此段的峰面積。從圖5中可看出,表面活化的熒光乳膠微球易形成單分散狀態,提高微球涌動性能。當血液移動至抗原的檢測線時,待測物和試劑的復合物便可以進行充分的特異性結合(200-250段峰值)。峰清晰,檢測段21上除了檢測線與質控線之外無熒光微球殘留。本實施例制得的試紙條,檢測靈敏度高、特異性強、發光效率高且能夠定量反應血液中檢測物的濃度。實施例5采用實施例2得到的標記物工作液制備的熒光免疫層析試紙條本實施例的熒光免疫層析試紙條與實施例4類似,區別在于步驟1)和2)中使用實施例2得到的標記物工作液取代實施例1得到的標記物工作液。對熒光乳膠微球的分散性和涌動性進行檢測,方法同實施例4,結果見圖6,本實施例制得的熒光免疫層析試紙條的具有如下效果:表面活化的熒光乳膠微球易形成單分散狀態,提高微球涌動性能。當血液移動至抗原的檢測線時,待測物和試劑的復合物便可以進行充分的特異性結合(200-250段峰值)。峰清晰,檢測段21上除了檢測線與質控線之外無熒光微球殘留。本實施例制得的試紙條,檢測靈敏度高、特異性強、發光效率高且能夠定量反應血液中檢測物的濃度。實施例6采用實施例3得到的標記物工作液制備的熒光免疫層析試紙條本實施例的熒光免疫層析試紙條與實施例4類似,區別在于步驟1)和2)中使用實施例3得到的標記物工作液取代實施例1得到的標記物工作液。對熒光乳膠微球的分散性和涌動性進行檢測,方法同實施例4,結果見圖7,本實施例制得的熒光免疫層析試紙條的具有如下效果:表面活化的熒光乳膠微球易形成單分散狀態,提高微球涌動性能。當血液移動至抗原的檢測線時,待測物和試劑的復合物便可以進行充分的特異性結合(200-250段峰值)。峰清晰,檢測段21上除了檢測線與質控線之外無熒光微球殘留。本實施例制得的試紙條,檢測靈敏度高、特異性強、發光效率高且能夠定量反應血液中檢測物的濃度。對比例本對比例的熒光免疫層析試紙條與實施例5類似,區別在于步驟1)和2)中使用市售的氨基聚苯乙烯熒光微球分散液取代實施例1得到的標記物工作液。分散性和涌動性檢測方法同實施例1,檢測結果見圖8,從圖8可看出:1.未活化微球,爬膜效果差。乳膠微球易凝聚,同時因其疏水性,易發生非特異性吸附,造成顆粒聚并。2.在檢測時的層析過程中,強大的吸附性凝聚成團的熒光微球很難再形成單分散微球層析。3.因包被墊(NC膜)是多孔網狀結構膜,因此可能與較大顆粒發生不利于層析檢測的非特異性吸附以及導致大顆粒熒光微球釋放性差。4.致NC膜前(檢測線5到第一連接段20之間的檢測段21)端有明顯大量熒光微球殘留。圖8中的200-300段,測試峰難以分辨。以上所述實施例僅是為充分說明本發明而所舉的較佳的實施例,本發明的保護范圍不限于此。本
技術領域:
的技術人員在本發明基礎上所作的等同替代或變換,均在本發明的保護范圍之內。本發明的保護范圍以權利要求書為準。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1
- 基于量子點的CA15?3免疫層析試紙條的制備方法與制造工藝
- 肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球及應用的制造方法與工藝
- 鐵蛋白熒光免疫層析檢測卡用活化熒光乳膠微球的制造方法與工藝
- 全程C?反應蛋白熒光免疫層析用活化熒光乳膠微球的制造方法與工藝
- 一種微流控芯片上基于熒光量子點磁性富集并分離結核分枝桿菌TB的方法及裝置與制造工藝
- 25?羥基維生素D熒光免疫層析用活化熒光乳膠微球的制造方法與工藝
- 25?羥基維生素D3熒光免疫層析用活化熒光乳膠微球的制造方法與工藝
- 降鈣素原熒光免疫層析檢測卡用活化熒光乳膠微球的制造方法與工藝
- 一種改變量子點熒光色的方法與制造工藝
- 一種基于熒光免疫層析技術的定量檢測計算方法與制造工藝
- 一種基于碳量子點的熒光面料及其制備方法與制造工藝
- 基于量子點的CA15?3免疫層析試紙條的制備方法與制造工藝
- 肌紅蛋白熒光免疫層析試紙條用活化熒光乳膠微球及應用的制造方法與工藝
- 鐵蛋白熒光免疫層析檢測卡用活化熒光乳膠微球的制造方法與工藝
- 全程C?反應蛋白熒光免疫層析用活化熒光乳膠微球的制造方法與工藝
- 一種微流控芯片上基于熒光量子點磁性富集并分離結核分枝桿菌TB的方法及裝置與制造工藝
- 25?羥基維生素D熒光免疫層析用活化熒光乳膠微球的制造方法與工藝
- 25?羥基維生素D3熒光免疫層析用活化熒光乳膠微球的制造方法與工藝
- 降鈣素原熒光免疫層析檢測卡用活化熒光乳膠微球的制造方法與工藝
- 一種改變量子點熒光色的方法與制造工藝