試樣用夾持器的制作方法
本發明涉及在腫瘤部位識別裝置中使用的試樣用夾持器。
背景技術:
近年來的日本迎來了快速的老齡化社會,癌癥患者數有增加的趨勢。特別是淋巴結轉移是重要的預后因素之一,因此,在決定患者的治療方法的方面,準確地診斷淋巴結轉移的有無是重要的。特別地,從原發灶離開的癌細胞最先到達的淋巴結被稱為前哨淋巴結。到達前哨淋巴結的癌細胞的數量起初是有限的,因此,對前哨淋巴結進行調查,若癌細胞的轉移極少,則可以認為基本沒有從前哨淋巴結轉移至末端的淋巴結。
作為術前的淋巴結轉移診斷法,已知有ct(計算機斷層攝影,computedtomography)、fdg-pet(氟脫氧葡萄糖正電子發射斷層攝影,fluorodeoxyglucosepositronemissiontomography)等,但現狀是在診斷精度的方面仍然不夠充分。另外,術中、術后的淋巴結轉移的診斷使用病理組織診斷,但通常僅根據從單一的切割面得到的標本來診斷轉移的有無,因此有時會漏掉小的轉移灶,其診斷精度不能說是充分的。此外,在術中的快速檢查中,到診斷為止至少需要約30分鐘,而且需要由病理醫生做出判斷,因此,也有可能因病理醫生個人的技能差異而使診斷結果產生差異。此外,鑒于病理醫生本身不足的目前的現狀,需要不依靠病理醫生的判斷而能夠以高精度進行淋巴結轉移的診斷的新方法。
目前,在包括消化系統領域在內的廣泛領域內,癌癥的檢測正在應用使用5-氨基乙酰丙酸(5-ala)的光線力學方法。5-ala是也存在于生物體內的氨基酸的一種,其為水溶性,能夠經口、局部地給藥。從體外給用5-ala時,在正常細胞中快速代謝為血紅素,但在癌細胞中,由于代謝酶的活性的差異而選擇性地蓄積作為代謝產物的原卟啉ix(ppix)。在此,血紅素觀察不到熒光,另一方面,ppix為熒光物質,因此,通過對該光進行檢測,能夠進行癌癥的診斷(參考專利文獻1、非專利文獻1)。
現有技術文獻
專利文獻
專利文獻1:國際公開第2013/002350號
非專利文獻
非專利文獻1:“使用5-氨基乙酰丙酸(5-ala)的消化系統癌癥轉移淋巴結的診斷”,京都府立醫科大學雜志,122卷,no.4(2013)
技術實現要素:
發明所要解決的問題
上述內容在現階段還處于實驗室水平的研究階段,設想在實際應用于人的診斷時會產生各種問題。本申請人目前正在進行通過對存在于試樣的腫瘤部位的ppix所發出的熒光進行分光檢測而進行腫瘤部位和非腫瘤部位的識別的裝置的開發。在該開發過程中,本發明人發現,為了精度良好地進行腫瘤部位的識別,使收容試樣的夾持器承擔一定的要求,從而完成了本發明。
本發明的目的在于提供在腫瘤部位識別裝置中使用的試樣用夾持器,其是能夠精度良好地進行腫瘤部位的識別的夾持器。
用于解決問題的方法
本發明為一種試樣用夾持器,其為在通過對試樣照射從光源部射出的激發光、對存在于上述試樣的腫瘤部位的卟啉類所發出的熒光進行分光檢測而進行上述腫瘤部位和非腫瘤部位的識別的腫瘤部位識別裝置中使用的試樣用夾持器,其特征在于,
具備收容上述試樣的收容部、和用于使從上述試樣用夾持器的外側射出的上述激發光透射而對收容在上述收容部內的上述試樣照射該激發光的窗部,
至少上述窗部由低自體熒光性材料構成。
需要說明的是,本說明書中的“卟啉類”是指在卟啉環上帶有取代基的化合物,例如除了ppix以外,還存在由ppix生成的光-原卟啉(ppp)等原卟啉類。
在使用腫瘤部位識別裝置對試樣中是否包含腫瘤部位進行檢測時,首先,對作為受試者的患者給用5-ala。在正常細胞中,5-ala被吸收時,利用細胞內線粒體代謝為作為卟啉類之一的原卟啉ix(以下適當記載為“ppix”),生物合成為血紅素。但是,惡性腫瘤細胞與正常細胞相比,ppix生成過程中的酶(pbg脫氨酶)活性高,催化由ppix生物合成血紅素的酶(亞鐵螯合酶)活性低。因此,在惡性腫瘤細胞中,5-ala被吸收時,在該細胞中大量蓄積ppix。
ppix是熒光物質,而血紅素不是熒光物質。因此,通過對試樣照射規定的激發光并對從試樣發出的熒光進行受光分析,能夠進行腫瘤部位和非腫瘤部位的識別。
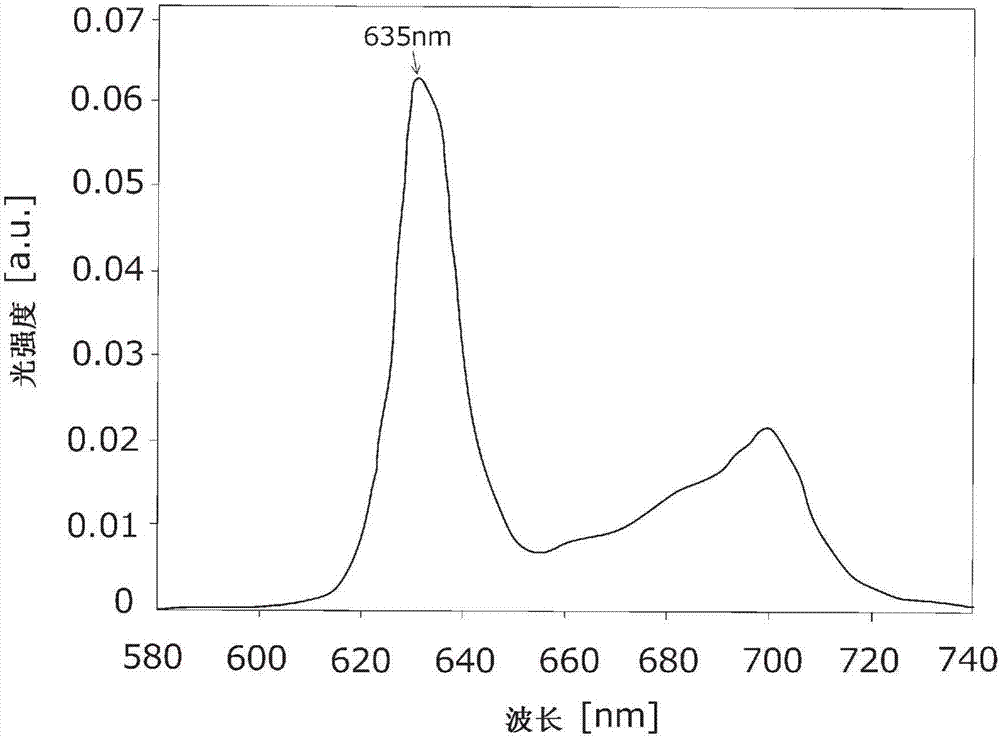
圖1a是示出ppix的吸收光譜的圖。另外,圖1b是示出ppix的熒光光譜的圖。ppix對規定波長的激發光顯示出高吸光度。具體而言,如圖1a所示,對波長370nm以上且450nm以下的光顯示出高吸光度,特別是對波長385nm以上且425nm以下的光顯示出極高的吸光度。而且,對ppix照射上述波長范圍的光時,如圖1b所示,從ppix放射出以635nm附近作為峰值、包含620nm以上且710nm以下的波長成分的熒光。
作為腫瘤部位識別裝置,需要能夠射出包含在上述波段內的波長的激發光的光源部、和接收從ppix放射出的熒光的受光部。另外,需要用于將試樣設置到裝置中的機構。
作為試樣,假設淋巴結的切片等活檢材料。在將這樣的活檢材料設置到裝置中時,為了不產生污染裝置等問題,本申請人想出了預先將試樣收容在規定的夾持器內并將該夾持器設置到裝置的規定位置的方法。
該夾持器具有收容部,在使用時將試樣載置于該收容部內。另外,在夾持器上設置有使從裝置內的光源部射出的激發光透射的窗部。通過使激發光從窗部透射而照射到試樣上,若試樣中含有ppix,則該ppix被激發而發出熒光。通過對設置在裝置側的受光部中接收到的光進行分光分析,能夠根據來自ppix的熒光的波長的光的強度對腫瘤部位和非腫瘤部位進行識別。
但是,在上述的構成下,激發光先從夾持器的窗部透射后照射到試樣上。因此,假如由于在夾持器的窗部一部分激發光被吸收并被激發而導致從該部位發出熒光,則在裝置的受光部接收到該熒光,結果,有可能誤將應該為非腫瘤部位的部位認定為腫瘤部位。
但是,根據本發明,將使激發光透射的夾持器的窗部利用低自體熒光性的材料構成,因此,由于夾持器所發出的熒光而誤將非腫瘤部位判斷為腫瘤部位的可能性降低,能夠精度良好地進行腫瘤部位的識別。
在此,低自體熒光性的材料是指,夾持器的自體熒光的強度與來自要測定的試樣中蓄積的卟啉類的熒光的強度相比低至能夠忽略的程度的材料。列舉一例來說,夾持器的自體熒光的強度相對于從要測定的試樣發出的來自卟啉類的熒光的強度優選為10%以下。但是,對于從試樣發出的來自卟啉類的熒光的強度的影響小的自體熒光強度的范圍可以根據測定的精度進行適當變更。
更具體而言,在試樣用夾持器中,可以將上述窗部利用芳香族聚碳酸酯樹脂、聚苯乙烯樹脂、環狀烯烴類樹脂或丙烯酸類樹脂中的一種或多種構成。
作為對熒光或熒光標記的檢查物的熒光的變化進行分光光學檢測時的支撐體,通常使用玻璃、硅。但是,在以用于保持作為活檢材料的試樣的支撐體(容器)進行研究的情況下,存在如下問題:玻璃的微細加工繁雜,而且經不起落下等的沖擊,在制造、輸送、檢查過程中非常容易損傷。另外,活檢材料有可能對人體、環境造成不良影響,因此期望在檢查后連同夾持器一起進行焚燒處理。但是,若利用玻璃、硅形成夾持器,則在焚燒時會在焚燒爐內產生融著,焚燒時活檢材料的一部分也可能漏出到外部。
如上所述,通過將夾持器利用樹脂構成,可耐受落下等的沖擊,并且能夠進行注射成形,也能夠容易地進行焚燒處理。而且,通過利用上述各樹脂構成夾持器的窗部,能夠形成即使從裝置照射激發光也幾乎不發出ppix的熒光波段即620nm以上且710nm以下、特別是620nm以上且650nm以下的波段的熒光的構成。由此,可實現耐久性和環境性優良、容易制造并且不會使腫瘤部位檢測的精度降低的試樣用夾持器。
作為更具體的一例,可以將包含收容試樣的收容部的底面的部位設定為窗部。此時,可以形成在裝置中具備用于插入夾持器的插入口并且在比插入口更靠下方的位置具備光源部和受光部的構成。此時,若從光源部向夾持器的收容部的底面射出激發光,則該激發光從窗部透射而照射到試樣上。試樣中蓄積有ppix時,來自ppix的熒光從窗部通過,被導入到受光部。
但是,窗部并不一定限定于收容部的底面側。可以從試樣的上方照射激發光,也可以從試樣的側方照射激發光,還可以從試樣的整個外周進行照射。即,只要為在夾持器中在射出激發光的光源部的射出端與試樣之間的位置具備由低自體熒光性的材料構成的窗部的構成即可。
另外,不限于窗部,也可以將夾持器整體利用上述低自體熒光性材料構成。
另外,如上所述,激發光經由窗部照射到試樣上。因此,假如激發光在窗部被大量吸收,則需要提高激發光的強度。因此,窗部優選由對激發光具有高透光性的材料構成。例如,可以將窗部利用對波長370nm以上的光的透光率為80%以上的材料構成。
需要說明的是,作為收容到夾持器內的試樣,除了淋巴結以外,還可以假設病理斷端等。另外,上述的裝置也可以用于印片細胞診斷。
發明效果
通過將試樣收容到本發明的試樣用夾持器內并安裝到腫瘤部位識別裝置中,能夠精度良好地進行腫瘤部位的識別。
附圖說明
圖1a是示出ppix的吸收光譜的圖。
圖1b是示出ppix的熒光光譜的圖。
圖2是示意性地示出腫瘤部位識別裝置的外觀的圖。
圖3是示意性地示出腫瘤部位識別裝置的內部構成的框圖。
圖4a是試樣用夾持器的立體圖的一例。
圖4b是試樣用夾持器的基體部的俯視圖的一例。
圖4c是試樣用夾持器的蓋部的俯視圖的一例。
圖5是試樣用夾持器的立體圖的另一例。
具體實施方式
[裝置概要]
在試樣用夾持器的說明之前,先對利用該夾持器的腫瘤部位識別裝置的構成進行說明。
圖2是示意性地示出裝置的外觀的圖。另外,圖3是示意性地示出裝置內部的構成的框圖。需要說明的是,圖2和圖3是示出腫瘤部位識別裝置的一例的圖,利用本發明的夾持器的裝置不拘泥于該圖的內容。
如圖2所示,腫瘤部位識別裝置10(以下,有時適當稱為“裝置10”)具備夾持器安裝口11和顯示部12。夾持器安裝口11是用于安裝試樣用夾持器1的機構。另外,顯示部12對應于顯示由腫瘤部位識別裝置10判定的結果的監視器。需要說明的是,在此,示出了在腫瘤部位識別裝置10的主體上設置有顯示部12的構成,但也可以采用在裝置10的主體上不設置顯示部12而在其他監視器顯示判定結果的構成。
如圖3所示,裝置10具備光源部21、濾光片22、分色鏡23、物鏡24、濾光片25、受光部26、運算處理部27。需要說明的是,在圖3的示例中,假設了仿照圖2使裝置10具備顯示部12的構成。
光源部21例如由汞燈、發光二極管元件、激光二極管元件等構成。濾光片22具有從由光源部21射出的光中選擇性地使特定波長的光透射的功能,例如可以由電介質多層膜等構成。在此,以濾光片22具有選擇性地使波長390nm的光透射的功能的情況進行說明,但只要具有選擇性地使385nm以上且425nm以下的特定波段的光透射的功能即可。
分色鏡23具有使規定波段的光反射、使其他規定波段的光透射的功能,例如可以由電介質多層膜等構成。在此,以分色鏡23具有使波長390nm的光反射、使波長620nm以上的光透射的功能的情況進行說明。需要說明的是,該分色鏡23只要具有使利用濾光片22選擇出的波長的光反射、至少使從試樣2發出的熒光的峰值波長附近的光透射的功能即可。
從光源部21射出、從濾光片22透射后的波長390nm的激發光31被分色鏡23反射,導入到物鏡24。然后,從物鏡24通過后的光從夾持器1的規定區域(以下,適當記載為“窗部52”)透射,照射到收容于夾持器1中的試樣2上。試樣2中蓄積有ppix時,ppix被該波長390nm的激發光31激發,發出熒光32。熒光32從夾持器1的窗部52透射,與激發光反向行進,導入到物鏡24。然后,從分色鏡23透射,入射到濾光片25。
濾光片25具有從入射的光中選擇性地使規定波長的光透射的功能。在此,以濾光片25具有選擇性地使波長635nm的光透射的功能的情況進行說明,但只要具有選擇性地使圖1b所示的ppix的熒光光譜的峰值波長635nm附近的規定波長的光透射的功能即可。
從濾光片25透射后的波長635nm的熒光在受光部26被接收。受光部26例如可以由ccd相機等攝像裝置構成。受光部26將接收的光的強度與試樣2內的位置信息一起輸出到運算處理部27。運算處理部27例如由微型計算機等構成,對各位置的光強度是否超過規定的閾值進行判定。然后,運算處理部27將光強度超過規定閾值的部位判斷為腫瘤部位、將光強度為閾值以下的部位判斷為非腫瘤部位。然后,將該判斷結果輸出到顯示部12。
顯示部12基于從運算處理部27輸送的腫瘤部位的坐標信息,顯示例如在試樣2的圖像上的規定位置實施表示其為腫瘤部位的標記或顯色而得到的圖像數據。另外,在不存在被運算處理部27判斷為腫瘤部位的區域的情況下,可以將該內容的信息顯示于顯示部12。
檢查員通過目視確認顯示部12,由此能夠獲知在試樣2中是否存在腫瘤部位,并且在存在腫瘤部位的情況下能夠容易地獲知其存在部位。另外,通過設定為例如在裝置10上設置操作按鈕、將收容有試樣2的夾持器1安裝到裝置10中并按下該操作按鈕時從光源部21射出激發光的結構,能夠利用裝置10自動地進行試樣2的腫瘤部位識別判定,可消除由檢查員的技術導致的判斷結果的偏差,并且也不需要病理醫生的判斷。
需要說明的是,分色鏡23是出于為了使裝置10小型化而將激發光31和熒光32的光路部分共用的目的設置的,但在裝置10中,分色鏡23不是一定需要的構成。另外,濾光片22可以與光源部21一體化。濾光片25也可以與受光部26一體化。圖3所示的裝置10的構成只不過是一例,只要是實現相同功能的構成,則可以進行各種設計變更,這是不言而喻的。
[夾持器]
接著,對夾持器1的構成進行說明。圖4a是夾持器1的立體圖的一例。如圖4a所示,夾持器1包含基體部42和蓋部43而構成。圖4b是基體部42的俯視圖的一例,圖4c是蓋部43的俯視圖的一例。
基體部42和蓋部43由鉸鏈部51連接,蓋部43以相對于基體部42可旋轉的方式構成。在基體部42設置有用于將試樣2收容到規定部位的收容部41。該收容部41的深度比其周圍更深,即使在收容部41內收容有試樣2的狀態下將蓋部43與基體部42重疊,試樣2也不會被蓋部43壓碎。需要說明的是,圖4b中示意性地示出了在收容部41內收容有試樣2的狀態。
如參考圖3所說明的那樣,在裝置10中,激發光31從夾持器1透射,照射到試樣2上。在此,在圖4a中,從與蓋部43相反的一側對基體部42照射激發光31,從基體部42的規定部位透射,激發光被導入到收容在收容部41內的試樣2中。在夾持器1的基體部42,激發光所透射的區域對應于“窗部52”(參考圖3)。
在本實施方式中,作為一例,以基體部42由聚苯乙烯樹脂構成的情況進行說明。
低自體熒光性的材料是指,從基體部42發出的自體熒光的強度與從試樣2發出的來自ppix的波長635nm附近的熒光32的強度相比低至能夠忽略的程度的材料(列舉一例為10%以下)。但是,對于從試樣2發出的來自ppix的波長635nm附近的熒光32的強度的影響小的、從基體部42發出的自體熒光的強度可以根據測定的精度進行適當變更。
石英、聚苯乙烯樹脂、聚甲基戊烯(polymethylpentene:pmp)、聚甲基丙烯酸甲酯樹脂(polymethylmethacrylate:pmma)、芳香族聚碳酸酯樹脂、環狀烯烴類樹脂(環烯烴聚合物、環烯烴共聚物)、聚對苯二甲酸乙二醇酯(polyethyleneterephthalate:pet)的熒光的強度極低,這些材料符合低自體熒光性材料。
在此,假設將基體部42利用發出相對于從試樣2發出的來自ppix的波長635nm附近的熒光32的強度為10%以上的自體熒光的材料構成的情況。此時,從光源部21射出激發光31時,該激發光31如上所述從基體部42的窗部52透射,被導入到試樣2中。若試樣2中存在有ppix,則會發出來自該ppix的波長635nm附近的熒光32。但是,通過對基體部42照射激發光31,從基體部42也會發出自體熒光。該自體熒光的波段與來自ppix的熒光32重疊,因此,在受光部26接收兩者的熒光,結果,有可能誤將應該為非腫瘤部位的部位認定為腫瘤部位。
與此相對,在本實施方式中,將基體部42利用聚苯乙烯樹脂構成,因此,即使對基體部42照射波長390nm附近的激發光,該基體部42自身也幾乎不產生波長635nm附近的熒光。因此,在受光部26中接收的波長635nm附近的光為來自試樣2中含有的ppix的熒光。因此,能夠基于該熒光的強度進行試樣2的腫瘤部位識別。
從同樣的觀點出發,基體部42不限于由聚苯乙烯樹脂構成,也可以由芳香族聚碳酸酯樹脂、環狀烯烴類樹脂、丙烯酸類樹脂等低自體熒光性的材料構成。
在此,如上所述,激發光31從基體部42的窗部52透射,照射到試樣2上。因此,假如基體部42由大量吸收激發光31的材料構成,則為了對試樣2照射足以使ppix發出熒光的光量的激發光31,需要增大從光源部21射出的激發光31的強度。因此,基體部42優選由對激發光31具有高透光性的材料構成。更詳細而言,基體部42對激發光31的透光率優選為70%以上,更優選為80%以上。
在此,關于波長390nm附近的激發光的透光率,聚苯乙烯樹脂為89.5%、芳香族聚碳酸酯樹脂為89.4%、環狀烯烴類樹脂為90.9%、丙烯酸類樹脂為91.2%,另外,除此以外的作為上述低自體熒光性材料的樹脂均顯示出80%以上。通過利用這些材料構成基體部42,幾乎不吸收激發光31,并且幾乎不產生包含來自ppix的熒光32的峰值波長的成分的熒光。因此,能夠在將光源部21設定為低輸出的同時以高精度進行腫瘤部位識別。
需要說明的是,在上述的實施方式中,使基體部42由低自體熒光性的材料構成,但只要至少窗部52的區域由低自體熒光性材料構成即可。反過來,不僅是基體部42,蓋部43也可以由低自體熒光性材料構成。
[其他實施方式]
以下,對其他實施方式進行說明。
<1>在專利文獻1中記述了如下內容:通過對ppix照射規定波長的光,將其轉換為光-原卟啉(ppp)。其概略如下所述。
ppp的熒光光譜的峰值波長為675nm附近,與ppix的熒光光譜的峰值波長635nm不同。在此,若將用于產生熒光而照射的光稱為“第一激發光”、將用于使ppix轉換為ppp而照射的光稱為“第二激發光”,則可以根據在照射第二激發光之前照射第一激發光而得到的熒光的光譜和在照射第二激發光之后照射第一激發光而得到的熒光的光譜的變化的方式來確定ppix。更具體而言,可以將波長635nm附近的熒光強度與波長675nm附近的熒光強度的比率在第二激發光的照射前后變化至超過規定閾值的程度的部位判斷為腫瘤部位。
在裝置10中,可以基于上述方法進行腫瘤部位識別。在將夾持器2由上述的聚苯乙烯樹脂、芳香族聚碳酸酯樹脂、環狀烯烴類樹脂和丙烯酸類樹脂構成的情況下,即使對該夾持器2照射激發光(第一激發光、第二激發光),也幾乎不會發出包含波長635nm附近和波長675nm附近的成分的熒光,因此能夠精度良好地進行ppix的識別。
需要說明的是,也可以將腫瘤部位識別裝置10作為用于基于來自ppix和ppp以外的卟啉類的熒光強度進行腫瘤部位的判定的裝置來利用。
<2>在圖3所示的裝置10中,可以設定為如下構成:對于從ppix發出的熒光32,利用受光部26接收多種不同波長的熒光32并進行分析。這種情況下,可以設定為例如如下構成:裝置10具備濾光片更換機構,并且準備與各波長對應的多個濾光片25,在利用該濾光片更換機構更換濾光片25的同時在受光部26接收光。另外,也可以設定為如下構成:利用光學系統按照各波長將光路分支,可以在受光部26同時接收不同波長的熒光32。
另外,在圖3所示的裝置10中,可以利用多種不同波長的激發光31。特別是在使用其他實施方式<1>中記載的方法的情況下,假設利用第一激發光和第二激發光。這種情況下,可以在利用濾光片更換機構更換濾光片22的同時對夾持器1進行照射,也可以利用光學系統按照各波長將光路分支并對夾持器1進行照射。
<3>圖5是試樣用夾持器的立體圖的另一例。如圖5所示,夾持器1可以具備密封構件(密封部)61。由此,在將蓋部43重疊到基體部42上時,能夠利用密封構件61進行封印,能夠將收容在收容部41內的試樣2完全地密閉,從而防止污染。
<4>在上述的實施方式中,以夾持器1具備基體部42和蓋部43的構成進行了說明。但是,夾持器1也可以為不具備蓋部43的構成。這種情況下,為了使載置在基體部42上的試樣2不會落下、或者使試樣2中含有的生理鹽水等液體不會流出,可以采用將基體部42的外緣用壁包圍的構成。此外,將夾持器1安裝到裝置10內時,也可以采用在裝置10內將覆蓋基體部42的包圍構件安裝到基體部42的上方或外周的構成。
標號說明
1:試樣用夾持器
2:試樣
10:腫瘤部位識別裝置
11:夾持器安裝口
12:顯示部
21:光源部
22:濾光片
23:分色鏡
24:物鏡
25:濾光片
26:受光部
27:運算處理部
31:激發光
32:熒光
41:收容部
42:基體部
43:蓋部
51:鉸鏈部
52:窗部
61:密封構件(密封部)
- 還沒有人留言評論。精彩留言會獲得點贊!