用于診斷、預后和確認先兆子癇的方法與組合物與流程
本申請要求于2014年7月30日提交的美國臨時專利申請62/031,132、于2014年7月31日提交的美國臨時專利申請62/031,834和于2015年2月11日提交的美國臨時專利申請62/115,077的權益和優先權。每個前述專利申請的內容和公開通過引用整體并入本文。
相關領域
本公開涉及提供先兆子癇的診斷和預后。
發明背景
先兆子癇(pe)是嚴重的妊娠多系統并發癥,對母親和嬰兒有不良影響。該障礙的發生率是美國和全世界所有妊娠的約5-8%,并且該障礙占美國所有孕產婦死亡的18%。先兆子癇的病因和發病機制仍不確定,并且當前pe的實驗室標志和臨床癥狀發生在疾病過程的晚期,有時使得確定pe和臨床管理決策很困難。具體地,區分先兆子癇與妊娠癥狀的并發癥(例如妊娠高血壓、慢性高血壓和妊娠糖尿病,其中每一種需要不同的治療選擇)是關鍵的。更早和更可靠的診斷、預后、確認和監測疾病將導致更及時和個性化的先兆子癇治療,并且因此將顯著促進對先兆子癇發病機理的理解。
發明概述
本公開提供了用于在任何受試者、優選妊娠受試者中確認先兆子癇的方法,包括:評估來源于受試者的樣品中的多個生物標志物以計算指數或以確認受試者是否患有先兆子癇,其中該確認具有大于90%的靈敏度、大于90%的特異性或大于0.9的接受者操作特征曲線(roc和/或auc)下的面積。
本公開提供了用于確認受試者、優選妊娠受試者中的先兆子癇的測試,其中該測試能夠以至少0.80、0.85、0.90、0.91、0.92、0.93、0.94、0.95、0.96、0.97、0.98、0.99、0.995或更大的roc值辨別沒有患有pe但具有與pe相關的一個或多個癥狀的受試者與患有pe的受試者。與pe相關的一個或多個癥狀可以是糖尿病(例如妊娠糖尿病、i型或ii型糖尿病)、高于正常葡萄糖水平、高血壓(例如慢性或非慢性高血壓)、過度或突然的體重增加、高于正常體重、肥胖、高于正常體重指數(bmi)、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產(nulliparity)、異常巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、先前妊娠的pe、腎病、血栓形成傾向或其任何組合。
本公開提供了用于確認受試者、優選妊娠受試者中的先兆子癇的測試,其中該測試能夠以至少80%、85%、90%、95%、96%、97%、98%、99%、99.5%或更高的靈敏度、特異性和/或陰性預測值(npv)辨別沒有患有pe但具有與pe相關的一個或多個癥狀的受試者與患有pe的受試者。與pe相關的一個或多個癥狀可以是糖尿病(例如妊娠糖尿病、i型或ii型糖尿病)、高于正常葡萄糖水平、高血壓(例如慢性或非慢性高血壓)、過度或突然的體重增加、高于正常體重、肥胖、高于正常體重指數(bmi)、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、先前妊娠的pe、腎病、血栓形成傾向或其任何組合。
本公開提供了用于確認受試者、優選妊娠受試者中的先兆子癇的方法,包括對來源于受試者的樣品進行測試,其中該測試包括測量多個標志物的水平,并使用水平以至少80%、85%、90%、95%、96%、97%、98%、99%、99.5%或更高的靈敏度、特異性和/或陰性預測值(npv)值或者以至少0.80、0.85、0.90、0.91、0.92、0.93、0.94、0.95、0.96、0.97、0.98、0.99、0.995或更大的roc值確認pe。與pe相關的一個或多個癥狀可以是糖尿病(例如妊娠糖尿病、i型或ii型糖尿病)、高于正常葡萄糖水平、高血壓(例如慢性或非慢性高血壓)、過度或突然的體重增加、高于正常體重、肥胖、高于正常體重指數(bmi)、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、先前妊娠的pe、腎病、血栓形成傾向或其任何組合。
本公開還提供了用于確認受試者、優選妊娠受試者是否沒有患有先兆子癇的方法,該方法包括:評估來源于受試者的樣品以確定樣品中多個生物標志物的水平,使用多個生物標志物的水平以計算代表受試者沒有患有先兆子癇的可能性的指數;并且基于該指數,確認受試者是否沒有患有先兆子癇。
一種用于確認受試者、優選妊娠受試者是否確實患有先兆子癇的方法,該方法包括:(a)評估來源于受試者的樣品以確定樣品中多種生物標志物的水平,(b)使用多個生物標志物的水平以計算代表受試者患有先兆子癇的可能性的指數;和(c)基于該指數,確認受試者是否確實患有先兆子癇。
本公開還提供了用于確認受試者、優選妊娠受試者是否沒有患有先兆子癇的方法,該方法包括:(a)評估來源于受試者的樣品以確定樣品中生物標志物的水平;和(b)使用該生物標志物的水平以計算代表受試者沒有患有先兆子癇的可能性的指數;其中該生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(pikachurin)(egflam)或血紅素。
本公開提供了用于確認受試者、優選妊娠受試者是否確實患有先兆子癇的方法,該方法包括:(a)評估來源于受試者的樣品以確定樣品中生物標志物的水平;和(b)使用該生物標志物的水平以計算代表受試者確實患有先兆子癇的可能性的指數;其中該生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)或血紅素。
本公開還提供了用于確認具有至少一個與pe相關的癥狀的受試者、優選妊娠受試者是否患有pe的方法,該方法包括:(a)評估來源于受試者的樣品以確定樣品中的一個或多個生物標志物的水平;和(b)使用一個或多個生物標志物的水平計算代表女性確實患有pe的可能性的指數,以計算指數,其中一個或多個生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)或血紅素。
本公開還提供了用于確認沒有至少一個與pe相關的癥狀的受試者、優選妊娠受試者是否沒有患有pe的方法,該方法包括:(a)評估來源于受試者的樣品以確定樣品中一個或多個生物標志物的水平;和(b)使用一個或多個生物標志物的水平計算表示受試者沒有患有pe的可能性的指數,以計算指數,其中一個或多個生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)或血紅素。
本公開還提供了用于診斷或確認受試者、優選妊娠受試者中存在先兆子癇的方法,該方法包括:(a)進行多個不同的測定,所述測定確定來源于受試者的樣品中纖連蛋白的水平;和(b)評估樣品并使用來自多個不同測定的水平以診斷或確認先兆子癇的存在并計算指數。
本公開還提供了用于確認受試者、優選妊娠受試者沒有患有先兆子癇的方法,該方法包括:進行多個不同的測定,所述測定確定來源于受試者的樣品中纖連蛋白的水平;以及評估樣品并使用來自多個測定的水平以確認受試者沒有患有先兆子癇并計算指數。
本公開還提供了用于診斷或確認受試者、優選妊娠受試者中存在先兆子癇的方法,該方法包括:(a)進行至少一個測定,所述測定利用結合纖連蛋白的抗體或選擇性結合與該抗體相同的纖連蛋白的抗原,其中該抗體的結合決定來源于受試者的樣品中纖連蛋白的水平;和(b)評估樣品并使用來自至少一個測定的纖連蛋白的水平來診斷或確認先兆子癇的存在并計算指數。
本公開還提供了用于診斷或證實受試者、優選妊娠受試者中存在先兆子癇的方法,該方法包括:(a)測量來源于受試者的樣品中sflt-1和plgf(plgf)的比率水平和多個不同生物標志物的水平,其中不同的生物標志物中沒有一個是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)或血紅素;和(b)評估樣品并使用來自步驟(a)的水平來確定診斷或確認存在先兆子癇的指數并計算指數。
本公開還提供了通過評估來源于受試者、優選妊娠受試者的樣品用于診斷、監測、表征或確認先兆子癇的方法,其通過使用至少2、3、4、5、6、7、8、9或10個選自圖5a-5f(或表2)的標志物(例如生物標志物),以計算指數值,其中指數值用于在受試者中確定診斷、相對水平或表征先兆子癇。
本公開還提供了用于確認受試者、優選妊娠受試者,沒有患有先兆子癇的方法,該方法由以下組成:測量來源于受試者的樣品中sflt-1和plgf的比率水平和多個不同生物標志物的水平,其中不同的生物標志物中沒有一個是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)或血紅素;和評估樣品并使用來自步驟(a)的水平來確定確認不存在先兆子癇的指數并計算指數。
本公開還提供了用于區分患有先兆子癇的受試者與沒有患有先兆子癇但具有與先兆子癇相關的癥狀的受試者的方法。與先兆子癇相關的此類癥狀包括例如慢性高血壓、妊娠高血壓、自身免疫性疾病和/或妊娠糖尿病。本文的方法和測試具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或99.5%的特異性、靈敏度和/或陰性預測值(npv)。本文的方法和測試優選以至少0.8、0.85、0.9或0.95的roc值或在曲線下的面積區分患有先兆子癇的受試者與沒有患有先兆子癇但具有與先兆子癇相關的癥狀的受試者。本文的方法包括測量來源于受試者的樣品中的多個不同生物標志物(例如,諸如選自圖5a-5f(或表2)中的列表的那些生物標志物)的水平,使用不同指數的水平產生指數,并且使用該指數作為確認先兆子癇的存在、先兆子癇的不存在和/或先兆子癇的嚴重性的手段。
本公開還提供了用于確認受試者、優選妊娠受試者中先兆子癇的存在、不存在或嚴重性的方法,該方法包括:使用選擇性結合纖連蛋白的單克隆抗體以測定來源于樣品的纖連蛋白的水平,基于該水平產生指示先兆子癇的存在、不存在或嚴重性和含有指數的報告;評估樣品;并且基于該指數,提示先兆子癇的治療,其中治療涉及阿司匹林、早產、用抗高血壓或抗先兆子癇藥物或臥床休克治療。
本公開還提供了用于確認來源于受試者、優選妊娠受試者的樣品中先兆子癇的存在、不存在或嚴重性的方法,該方法包括:利用針對至少一個纖連蛋白elisa試劑盒中纖連蛋白抗體的抗原的抗體來分析和評估來源于受試者的樣品。
本公開還提供了用于確認受試者、優選妊娠受試者中先兆子癇的存在、不存在或嚴重性的方法,該方法包括:進行至少一個測定,其利用選擇性結合纖連蛋白、纖連蛋白的一部分(portion)、纖連蛋白的一部分(part)或纖連蛋白的片段的抗體,其中抗體的結合決定來源于受試者的樣品中纖連蛋白的水平;評估樣品;并使用來自至少一個測定的纖連蛋白的水平來確認先兆子癇的存在、不存在或嚴重性并計算指數。
本公開還提供了用于確認受試者、優選女性受試者中不存在先兆子癇的測試,其中該測試測量來自來源于受試者的樣品的一個或多個生物標志物,其中該測試具有至少0.8的總體roc值。在一些實例中,該測試測量來自來源于受試者的樣品的一個或多個生物標志物,其中該測試具有至少0.7、0.8、0.85、0.9、0.95、0.96、0.97、0.98、0.99或更大的總體roc值。在一些實例中,該測試測量來自來源于受試者的樣品的一個或多個生物標志物,并且具有至少0.81、0.82、0.83、0.84、0.85、0.86、0.87、0.88、0.89、0.9、0.91、0.92、0.93、0.94、0.95、0.96、0.97、0.98、0.99、0.995或更大的總體roc值。
本公開還提供了用于確認、診斷、預測、監測或表征受試者、優選妊娠受試者中先兆子癇的試劑盒,所述試劑盒包含至少兩種試劑,其特異性用于測定來源于受試者的樣品中纖連蛋白的水平。
本公開還提供了商業方法,其包括確定受試者、優選妊娠受試者中先兆子癇的存在、不存在、預測、嚴重性或特征的步驟,所述方法包括以下步驟:(a)評估來源于受試者的樣品中的sflt-1、plgf的水平和多個不同的生物標志物,其中不同的生物標志物中沒有一個是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)或血紅素,(b)測定生物標志物指數值,所述指數包含sflt-1/plgf和加上多個不同的生物標志物,(c)采用所述生物標志物指數提供先兆子癇測定、先兆子癇診斷確認、確認先兆子癇不存在、先兆子癇的預后或先兆子癇的特征,和(d)提供報告以換取費用,其中報告基于所述生物標志物的分析指示指數值,并且指定所述受試者是否處于低先兆子癇風險、高先兆子癇風險或患有先兆子癇。
本公開還提供了用于確認、診斷、預后、監測或表征受試者、優選妊娠受試者中先兆子癇的系統,包括:(a)輸入模塊,其用于接收作為sflt-1、plgf和多個不同的生物標志物的輸入水平,(b)處理器,其任選地被配置為對所述水平進行對數變換以獲得對數變換水平,將每個對數變換水平標準化為標準化水平,將每個標準化水平調整為加權標準化水平,總計每個經調整的水平,平均每個經調整的水平;并基于所述評分提供先兆子癇指數,其中指數評分包括sflt-1/plgf并加上多個不同生物標志物。在一些情況下,對數變換是自然對數變換、常用對數變換、二元對數變換、有理數對數變換或無理數對數變換。在一些示例中,對數變換是log2、log10或loge變換。在一些情況下,對數變換是logb,其中對數底是任何實數(包括自然數、有理數或無理數)。
本公開還提供了用于確認受試者、優選妊娠受試者沒有患有先兆子癇的方法,包括:評估來源于受試者的樣品中的多個生物標志物以確認受試者沒有患有先兆子癇,其中該確認具有大于90%的特異性或具有0.9的auc并用于計算指數。
本公開的一些實施方案是:
1.一種用于確定先兆子癇的嚴重性或用于確認女性受試者中存在或不存在先兆子癇的方法,包括:
a)測量來源于妊娠女性的樣品中一個或多個生物標志物的水平;
b)基于一個或多個生物標志物的水平計算指數;和
c)基于指數,確認妊娠女性是否正經歷先兆子癇或妊娠女性是否沒有正經歷先兆子癇。
2.一種用于診斷、預后(pronging)、監測、表征、確定先兆子癇的嚴重性或確認女性受試者中存在或不存在先兆子癇的方法,包括:
a)測量來源于妊娠女性的樣品中一個或多個生物標志物的水平;
b)將一個或多個生物標志物的水平與各自的重組蛋白水平進行比較;和
c)基于比較,確認妊娠女性是否正經歷先兆子癇或妊娠女性是否沒有正經歷先兆子癇。
3.權利要求2的方法,還包括基于一個或多個生物標志物的水平計算指數。
4.一種用于診斷、預后、監測、表征、確定先兆子癇的嚴重性或確認女性受試者中存在或不存在先兆子癇的方法,包括:
a)測量來源于妊娠女性的樣品中纖連蛋白(fn)和兩個或更多個生物標志物的水平,其中兩個或更多個生物標志物中的至少兩種不同于纖連蛋白,
b)基于纖連蛋白和兩個或更多個生物標志物的水平計算指數;和
c)基于比較,確認女性受試者是否正經歷先兆子癇或女性受試者是否沒有正經歷先兆子癇。
5.權利要求4的方法,其中兩個或更多個生物標志物選自sflt-1、p1gf、adam-12、hpx和papp-a。
6.權利要求4的方法,其中一個或多個生物標志物是sflt-1、p1gf和papp-a。
7.權利要求4的方法,其中一個或多個生物標志物是sflt-1、p1gf、papp-a和adam-12。
8.權利要求4的方法,其中一個或多個生物標志物是sflt-1、p1gf、papp-a和hpx。
9.權利要求4的方法,其中一個或多個生物標志物是p1gf、papp-a和adam-12。
10.權利要求4的方法,其中一個或多個生物標志物是sflt-1和p1gf。
11.權利要求4的方法,其中一個或多個生物標志物是p1gf和papp-a。
12.權利要求4的方法,其中一個或多個生物標志物是sflt-1、p1gf和adam-12。
13.權利要求4的方法,其中一個或多個生物標志物是sflt-1和adam-12。
14.權利要求4、5、6、7、8、9、10、11、12或13的方法,還包括將指數與閾值進行比較。
15.一種用于確認女性受試者中先兆子癇或不存在先兆子癇的方法,包括:
a)使用選擇性結合纖連蛋白(fn)或fn片段的單克隆抗體測量來源于女性受試者的樣品中fn或fn片段的水平;和
b)確認女性受試者是否正經歷先兆子癇或女性受試者是否沒有正經歷先兆子癇,其中該確認基于比較。
16.如權利要求15的方法,還包括測量來源于女性受試者的樣品中兩個或更多個生物標志物的水平。
17.權利要求16的方法,其中兩個或更多個生物標志物選自sflt-1、p1gf、adam-12、hpx和papp-a。
18.權利要求16的方法,其中一個或多個生物標志物是sflt-1、p1gf和papp-a。
19.權利要求16的方法,其中一個或多個生物標志物是sflt-1、p1gf、papp-a和adam-12。
20.權利要求16的方法,其中一個或多個生物標志物是sflt-1、p1gf、papp-a和hpx。
21.權利要求16的方法,其中一個或多個生物標志物是p1gf、papp-a和adam-12。
22.權利要求16的方法,其中一個或多個生物標志物是sflt-1和p1gf。
23.權利要求16的方法,其中一個或多個生物標志物是p1gf和papp-a。
24.權利要求16的方法,其中一個或多個生物標志物是sflt-1、p1gf和adam-12。
25.權利要求16的方法,其中一個或多個生物標志物是sflt-1和adam-12。
26.權利要求15的方法,還包括基于結合的單克隆抗體的水平計算指數。
27.權利要求16、18、19、20、21、22、23、24或25的方法,還包括基于結合的單克隆抗體和兩個或更多個生物標志物的水平計算指數。
28.權利要求26或27的方法,還包括將指數與閾值進行比較,其中指數指示女性受試者中存在或不存在先兆子癇。
29.一種用于診斷、預后、表征、監測、確定先兆子癇的嚴重性或確認女性受試者中先兆子癇或不存在先兆子癇的方法,包括:
a)測量來源于妊娠女性的樣品中sflt、p1gf和一個或多個生物標志物的水平,其中一個或多個生物標志物僅不同于vegf,其中vegf不包括vegfr-1。
b)基于sflt、p1gf和一個或多個生物標志物的水平計算指數;和
c)基于指數,確認女性受試者是否正經歷先兆子癇或女性受試者是否沒有正經歷先兆子癇。
30.權利要求29的方法,其中一個或多個生物標志物選自纖連蛋白(fn)、adam-12、hpx和papp-a。
31.權利要求29的方法,其中一個或多個生物標志物是adam-12
32.權利要求29的方法,其中一個或多個生物標志物是papp-a。
33.權利要求29的方法,其中一個或多個生物標志物是纖連蛋白(fn)。
34.權利要求29的方法,其中一個或多個生物標志物是纖連蛋白(fn)和papp-a。
35.權利要求29的方法,其中一個或多個生物標志物是纖連蛋白(fn)和adam-12。
36.權利要求29的方法,其中一個或多個生物標志物是纖連蛋白(fn)、adam-12和papp-a。
37.權利要求29的方法,其中一個或多個生物標志物是纖連蛋白(fn)、hpx和papp-a。
38.權利要求29、30、32、33、34、35、36或37的方法,還包括將指數與閾值進行比較。
39.一種用于診斷、預后、表征、監測、確定先兆子癇的嚴重性或確認女性受試者中先兆子癇或不存在先兆子癇的方法,包括:
a)在兩個不同的測定中測量至少一個纖連蛋白(fn)片段的水平,其中測定確定來源于妊娠女性的樣品中的fn水平;和
b)基于在兩個不同測定中測量的fn水平,診斷、預后、表征、監測、確定先兆子癇的嚴重性或確認女性受試者中先兆子癇或不存在先兆子癇。
40.權利要求39的方法,其中不同的測定中的每一個測定利用不同的單克隆抗體。
41.權利要求40的方法,還包括測量來源于妊娠女性的樣品中一個或多個生物標志物的水平,其中一個或多個生物標志物不同于纖連蛋白(fn)。
42.權利要求41的方法,其中一個或多個生物標志物選自sflt-1、p1gf、adam-12、hpx和papp-a。
43.權利要求40的方法,其中一個或多個生物標志物是sflt-1和p1gf。
44.如權利要求40的方法,其中一個或多個生物標志物是sflt-1、p1gf和papp-a。
45.權利要求40的方法,其中一個或多個生物標志物是sflt-1、p1gf和adam-12。
46.權利要求41、43、44或45的方法,還包括基于結合的單克隆抗體和兩個或更多個生物標志物的水平計算指數。
47.如權利要求1、3或46的方法,還包括將指數與閾值進行比較。
48.權利要求14、28、38、47的方法,其中指數通過實函數算法計算,用于對包括一個或多個變量乘以一個或多個對應的權重因子的一個或多個生物標志物的水平進行總計,
其中一個或多個生物標志物水平中的每一個的水平被輸入到一個或多個變量的具體變量中,
其中對應的權重因子對于每個具體變量是獨特的,
其中對應的權重因子中的至少一個不同于一。
49.權利要求48的方法,其中算法包括至少一個二元運算。
50.權利要求49的方法,其中至少一個二元運算是除法。
51.權利要求49的方法,其中至少一個二元運算是加法或減法。
52.權利要求1、3、4、15、29或39的方法,還包括產生指示存在或不存在先兆子癇的報告。
53.權利要求1、3、4、15、29或39的方法,其中方法不包括測量血壓、血糖水平、尿蛋白水平、家族性先兆子癇史或體重增加。
54.權利要求1、3、4、15、29或39的方法,其中女性受試者被診斷為具有由以下組成的組的至少一個癥狀:高于140/90mmhg的血壓、高于100mg/dl的空腹血糖水平、在24小時收集中尿蛋白水平超過5克或者至少分開四小時收集的兩個隨機尿樣的尿蛋白水平超過3+、一周中體重增加超過兩磅、血小板水平在妊娠中期低于155,000(每微升)或在妊娠晚期過程中低于145,000(每微升)、在24小時內少于400毫升的少尿、高于25的體重指數、先兆子癇家族史或家族性先兆子癇、孕產婦先兆子癇史、肺水腫、紫紺和視力變化。
55.權利要求1或2的方法,其中一個或多個生物標志物選自sflt-1、p1gf、纖連蛋白(fn)、adam-12、hpx和papp-a。
56.權利要求1、3、4、15、29或39的方法,其中生物標志物不包括鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)和血紅素。
57.權利要求14、38或47的方法,其中比較是將一個或多個生物標志物與單個妊娠女性或經歷pe的一組妊娠女性和未經歷pe的一組妊娠女性的比較。
58.權利要求57的方法,其中單個妊娠女性是正被測試的女性。
59.權利要求57的方法,其中比較包括將一個或多個生物標志物與各自的重組蛋白指數值進行比較。
60.權利要求1、3、4、15、29或39的方法,其中生物標志物包括一個或多個蛋白質或蛋白質片段。
61.權利要求1、3、4、15、29或39的方法,其中生物標志物包括多核苷酸。
62.權利要求1、3、4、15、29或39的方法,其中測量是通過選自由以下組成的組的方法的測量:免疫測定、質譜、色譜、比濁法、輻射狀免疫擴散和單向輻射狀免疫擴散測定。
63.權利要求1、3、4、15、29或39的方法,其中測量是通過免疫測定的測量。
64.權利要求63的方法,其中免疫測定選自elisa、夾心elisa、競爭性elisa和igm抗體捕獲elisa。
65.一種用于診斷、預后、監測、表征、確定先兆子癇的嚴重性或用于確認妊娠女性中存在或不存在先兆子癇的試劑盒,該試劑盒包含:至少兩個不同的試劑,其特異性用于測定來自妊娠女性的樣品中纖連蛋白的水平(fn)。
66.權利要求65的試劑盒,其還包含兩個或更多個試劑,其測量來源于女性受試者的樣品中兩個或更多個生物標志物的水平。
67.權利要求66的試劑盒,其中兩個或更多個生物標志物是sflt-1、p1gf和papp-a。
68.權利要求66的試劑盒,其中兩個或更多個生物標志物是sflt-1、p1gf、papp-a和adam-12。
69.權利要求66的試劑盒,其中兩個或更多個生物標志物是sflt-1、p1gf、papp-a和hpx。
70.權利要求66的試劑盒,其中兩個或更多個生物標志物是p1gf、papp-a和adam-12。
71.權利要求66的試劑盒,其中兩個或更多個生物標志物是sflt-1和p1gf。
72.權利要求66的試劑盒,其中兩個或更多個生物標志物是p1gf和papp-a。
73.權利要求66的試劑盒,其中兩個或更多個生物標志物是sflt-1、p1gf和adam-12。
74.權利要求66的試劑盒,其中兩個或更多個生物標志物是sflt-1和adam-12。
75.權利要求65或66的試劑盒,其中該試劑盒不包括測量選自由以下組成的組的生物標志物的水平的試劑:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離βhpc和血紅素。
76.一種用于確認妊娠女性中存在或不存在先兆子癇的試劑盒,該試劑盒包含
a)第一試劑,其特異性用于測定papp-a水平;和
b)第二試劑,其特異性用于測定adam12。
77.權利要求76的試劑盒,其還包含測量來源于女性受試者的樣品中一個或多個生物標志物的水平的一個或多個試劑。
78.權利要求77的試劑盒,其中一個或多個生物標志物是sflt-1、p1gf和纖連蛋白(fn)。
79.權利要求77的試劑盒,其中一個或多個生物標志物是p1gf和纖連蛋白(fn)。
80.權利要求76或77的試劑盒,其中該試劑盒不包括測量選自由以下組成的組的生物標志物的水平的試劑:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離βhpc和血紅素。
81.一種用于診斷、預后、監測、表征、確定先兆子癇的嚴重性或用于確認妊娠女性中存在或不存在先兆子癇的試劑盒,該試劑盒包含:
a)第一試劑,其特異性用于測定sflt-1或p1gf之一的水平;
b)第二試劑,其特異性用于測定纖連蛋白(fn);和
c)第三試劑,其特異性用于測定生物標志物的水平,該生物標志物的水平不同于由第一和第二試劑測定的生物標志物的水平。
82.權利要求81的試劑盒,其中第一試劑測定sflt-1的水平,第三試劑測定p1gf的水平,并且該試劑盒還包含測定不同于sflt-1、p1gf和fn的生物標志物的水平的第四試劑。
83.權利要求82的試劑盒,其中第四試劑測定papp-a、hpx或adam12的水平。
84.權利要求81、82或83的試劑盒,其中該試劑盒不包括測量選自由以下組成的組的生物標志物的水平的試劑:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離βhpc和血紅素。
85.一種用于確認妊娠女性中存在或不存在先兆子癇的試驗,其中該試驗測量來自來源于妊娠女性的樣品的一個或多個生物標志物并且具有至少0.8或更大的總體roc值。
86.權利要求85的測試,其中總體roc值為至少0.9或更大。
87.權利要求85的測試,其中總體roc值為至少0.95或更大。
88.權利要求85的測試,其中總體roc值為至少0.98或更大。
89.權利要求85的測試,其中總體roc值為至少0.984或更大。
90.一種具有用于診斷、預后、表征、監測、確定先兆子癇的嚴重性或確認女性受試者中存在或不存在先兆子癇的可執行邏輯的計算機可讀介質,包括:
(a)輸入字段,其用于提供一個或多個生物標志物水平,
(b)算法,其用于相對于訓練集調整一個或多個生物標志物的水平,從而提供一個或多個經調整的生物標志物水平;
(c)算法,其包括使用經調整的生物標志物水平執行至少一個二元運算,其中該算法是得到指數值的實函數;和
(d)輸出字段,其呈現指數值,其中指數值指示診斷、預后、表征、監測、確定先兆子癇的嚴重性或確認女性受試者中存在或不存在先兆子癇。
91.一種具有用于確認女性受試者中存在或不存在先兆子癇的可執行邏輯的計算機可讀介質,包括:
(e)輸入字段,其用于提供一個或多個生物標志物水平,
(f)算法,其用于相對于對照值調整一個或多個生物標志物水平,從而提供一個或多個經調整的生物標志物水平;
(g)算法,其包括加上或減去一個或多個經調整的生物標志物水平,其中該算法是得到指數值的實函數;和
(h)輸出字段,其呈現指數值,其中指數值指示女性受試者中存在或不存在先兆子癇。
92.一種具有用于確認女性受試者中存在或不存在先兆子癇的可執行邏輯的計算機可讀介質,包括:
(i)輸入字段,其用于提供一個或多個生物標志物水平,
(j)算法,其用于相對于對照值調整一個或多個生物標志物水平,從而提供一個或多個經調整的生物標志物水平;
(k)算法,其包括一個或多個經調整的生物標志物水平中兩個之間的比率,其中該算法是得到指數值的實函數;和
(l)輸出字段,其呈現指數值,其中指數值指示女性受試者中存在或不存在先兆子癇。
93.權利要求90、91或92的計算機可讀介質,其中實函數是復雜統計算法。
94.權利要求90、91或92的計算機可讀介質,其中實函數包括至少一個附加二元運算。
95.權利要求94的計算機可讀介質,其中實函數包括乘以對應的權重因子的變量。
96.權利要求95的計算機可讀介質,其中一個或多個生物標志物中每個生物標志物的水平被輸入到對應于具體生物標志物的具體變量,并且其中對應的權重因子對于每個具體變量是獨特的或對于兩個變量的每個具體比率是獨特的。
97.權利要求90的計算機可讀介質,還包括用于對一個或多個經調整的生物標志物水平中的每一個進行平均的算法。
權利要求90的計算機可讀介質,其中計算機可讀介質還包括用于執行水平的對數變換以獲得對數變換水平的算法;用于將每個對數變換水平標準化為標準化水平的算法;用于將每個標準化水平調整為加權標準化水平的算法。
98.一種具有用于診斷、預后、監測、表征、確定先兆子癇的嚴重性或用于確認妊娠女性中存在或不存在先兆子癇的可執行邏輯的計算機可讀介質,包括:
(a)輸入字段,其用于提供一個或多個生物標志物水平,
(b)調整算法,其用于相對于對應的對照值調整一個或多個生物標志物中的每一個的水平,其中該調整算法提供一個或多個經調整的生物標志物水平;
(c)實函數算法,其用于操作一個或多個經調整的生物標志物水平的,包括一個或多個變量乘以一個或多個對應的權重因子,
其中一個或多個經調整的生物標志物水平中的每一個的水平被輸入到一個或多個變量的具體變量中,
其中對應的權重因子對于每個具體變量是獨特的,其中對應的權重因子中的至少一個不同于一;和
(d)輸出字段,其呈現指數值,其中指數值指示女性受試者中存在或不存在先兆子癇。
99.權利要求90、91、92或98的計算機可讀介質,其中使用訓練集來產生對照值。
100.權利要求98的計算機可讀介質,其中訓練集基于模型。
101.權利要求98的計算機可讀介質,其中訓練集基于從受試者獲得的實際值。
102.權利要求98的計算機可讀介質,其中對象是至少150個受試者或更多受試者。
103.權利要求98的計算機可讀介質,其中實際受試者包括復雜受試者。
104.權利要求98的計算機可讀介質,其中復雜受試者包括用于訓練集的總受試者的至少10%。
105.權利要求98的計算機可讀介質,其中算法包括至少一個二元運算。
106.權利要求105的計算機可讀介質,其中至少一個二元運算是除法。
107.權利要求105的計算機可讀介質,其中至少一個二元運算是加法或減法。
本公開的一些實施方案是:
1.一種用于確認女性受試者中存在或不存在先兆子癇的方法,該方法包括:
a)測量來源于女性受試者的樣品中一個或多個生物標志物的水平;
b)基于一個或多個生物標志物的水平計算指數;和
c)基于指數,確認女性受試者中存在或不存在先兆子癇。
2.權利要求1的方法,其中一個或多個生物標志物的測量水平包括測量三個或更多個生物標志物的水平。
3.權利要求1的方法,其中一個或多個生物標志物的測量水平包括測量四個或更多個生物標志物的水平。
4.權利要求1的方法,其中一個或多個生物標志物的測量水平包括測量五個或更多個生物標志物的水平。
5.一種用于確認女性受試者中存在或不存在先兆子癇的方法,該方法包括:
a)測量來源于女性受試者的樣品中一個或多個生物標志物的水平;
b)將一個或多個生物標志物的水平與各自的重組蛋白水平或標準值進行比較;和
c)基于比較,確定女性受試者中存在或不存在先兆子癇。
6.權利要求5的方法,還包括基于一個或多個生物標志物的水平計算指數。
7.一種用于確認女性受試者中存在或不存在先兆子癇的方法,該方法包括:
a)測量來源于女性受試者的樣品中纖連蛋白(fn)和兩個或更多個生物標志物的水平,其中兩個或更多個生物標志物中的至少兩個不同于纖連蛋白,
b)基于fn和兩個或更多個生物標志物的水平計算指數;和
c)基于指數,確定女性受試者中存在或不存在先兆子癇。
8.權利要求7的方法,其中兩個或更多個生物標志物選自sflt-1、p1gf、adam-12、hpx和papp-a。
9.權利要求7的方法,其中生物標志物是sflt-1、p1gf和papp-a。
10.權利要求7的方法,其中生物標志物是sflt-1、p1gf、papp-a和adam-12。
11.權利要求7的方法,其中生物標志物是sflt-1、p1gf、papp-a和hpx。
12.權利要求7的方法,其中生物標志物是p1gf、papp-a和adam-12。
13.權利要求7的方法,其中生物標志物是sflt-1和p1gf。
14.權利要求7的方法,其中生物標志物是p1gf和papp-a。
15.權利要求7的方法,其中生物標志物是sflt-1、p1gf和adam-12。
16.權利要求7的方法,其中生物標志物是sflt-1和adam-12。
17.權利要求7的方法,其中生物標志物是p1gf、adam-12、sflt1、papp-a2和hpx。
18.權利要求7、8、9、10、11、12、13、14、15、16或17的方法,還包括將指數與閾值進行比較。
19.一種用于確認女性受試者中存在或不存在先兆子癇的方法,該方法包括:
a)使用選擇性結合纖連蛋白(fn)或fn片段的單克隆抗體測量來源于女性受試者的樣品中fn或fn片段的水平;
b)將纖連蛋白(fn)或fn片段的水平與各自的重組蛋白水平或與標準值進行比較;和
c)基于比較,確認存在或不存在先兆子癇。
20.權利要求19的方法,還包括測量來源于女性受試者的樣品中兩個或更多個生物標志物的水平。
21.權利要求20的方法,其中兩個或更多個生物標志物選自sflt-1、p1gf、adam-12、hpx和papp-a。
22.權利要求20的方法,其中生物標志物是sflt-1、p1gf和papp-a。
23.權利要求20的方法,其中生物標志物是sflt-1、p1gf、papp-a和adam-12。
24.權利要求20的方法,其中生物標志物是sflt-1、p1gf、papp-a和hpx。
25.權利要求20的方法,其中生物標志物是p1gf、papp-a和adam-12。
26.權利要求20的方法,其中生物標志物是sflt-1和p1gf。
27.權利要求20的方法,其中生物標志物是p1gf和papp-a。
28.權利要求20的方法,其中生物標志物是sflt-1、p1gf和adam-12。
29.權利要求20的方法,其中生物標志物是sflt-1和adam-12。
30.權利要求20的方法,其中生物標志物是p1gf、fn、adam-12、sflt1、papp-a2和hpx。
31.權利要求19的方法,還包括基于結合的單克隆抗體的水平計算指數。
32.權利要求20、22、23、24、25、26、27、28或29的方法,還包括基于(1)結合的單克隆抗體和(2)兩個或更多個生物標志物的水平計算指數。
33.權利要求31或32的方法,還包括將指數與閾值進行比較,其中指數指示女性受試者中存在或不存在先兆子癇。
34.一種用于確認女性受試者中存在或不存在先兆子癇的方法,該方法包括:
a)測量來源于女性受試者的樣品中sflt、p1gf和一個或多個生物標志物的水平,其中一個或多個生物標志物不同于vegf,其中vegf不包括vegfr-1;
b)基于sflt、p1gf和一個或多個生物標志物的水平計算指數;和
c)基于指數,確定女性受試者中存在或不存在先兆子癇。
35.權利要求34的方法,其中一個或多個生物標志物選自纖連蛋白(fn)、adam-12、hpx和papp-a。
36.權利要求34的方法,其中生物標志物是adam-12。
37.權利要求34的方法,其中生物標志物是papp-a。
38.權利要求34的方法,其中生物標志物是纖連蛋白(fn)。
39.權利要求34的方法,其中生物標志物是纖連蛋白(fn)和papp-a。
40.權利要求34的方法,其中生物標志物是纖連蛋白(fn)和adam-12。
41.權利要求34的方法,其中生物標志物是纖連蛋白(fn)、adam-12和papp-a。
42.權利要求34的方法,其中生物標志物是纖連蛋白(fn)、hpx和papp-a。
43.權利要求34的方法,其中生物標志物是fn、adam-12、papp-a2和hpx。
44.權利要求34、35、36、37、38、39、40、41或42的方法,還包括將指數與閾值進行比較。
45.一種用于確認女性受試者中存在或不存在先兆子癇的方法,該方法包括:
a.測量由以下組成的生物標志物的水平:sflt和p1gf;
b.基于sflt和p1gf的水平計算指數;和
c.基于指數,確認女性受試者中存在或不存在先兆子癇。
46.權利要求45的方法,其中計算包括將sflt和p1gf的測量水平各自乘以獨特的權重因子,以及將一個或多個二元函數應用于sflt和p1gf的加權測量水平。
47.一種用于診斷、預后、表征、監測、確定女性受試者中先兆子癇的嚴重性、確認女性受試者中存在先兆子癇或確認女性受試者中不存在先兆子癇的方法,該方法包括:
a)在兩個不同的測定中測量至少一個纖連蛋白(fn)片段的水平,其中測定確定來源于女性受試者的樣品中fn的水平;和
b)基于在兩個不同測定中測量的至少一個fn片段的水平,診斷、預后、表征、監測、確定女性受試者中先兆子癇的嚴重性、確認女性受試者中存在先兆子癇或確認女性受試者中不存在先兆子癇。
48.權利要求47的方法,其中兩個不同測定中的每一個測定使用不同的單克隆抗體。
49.權利要求48的方法,還包括測量來源于女性受試者的樣品中一個或多個生物標志物的水平,其中一個或多個生物標志物不同于纖連蛋白(fn)。
50.權利要求49的方法,其中生物標志物選自sflt-1、p1gf、adam-12、hpx和papp-a。
51.權利要求49的方法,其中生物標志物是sflt-1或p1gf。
52.權利要求49的方法,其中生物標志物是sflt-1、p1gf或papp-a。
53.權利要求49的方法,其中生物標志物是sflt-1、p1gf或adam-12。
54.權利要求49的方法,其中生物標志物是p1gf、adam-12、sflt1、papp-a2和hpx。
55.權利要求49、50、51、52、53或54的方法,還包括基于(1)結合的單克隆抗體和(2)一個或多個生物標志物的水平計算指數。
56.權利要求1、5、7、34或47的方法,其中測量包括:
用對待測生物標志物具有親和力的抗體包被免疫測定板;和
用非特異性阻斷蛋白包被免疫測定板。
57.權利要求56的方法,還包括:
將標記的生物標志物與樣品混合得到混合物;并將混合物加入免疫測定板。
58.權利要求56的方法,還包括:
將樣品引入免疫測定板;和
將綴合的二抗引入免疫測定板。
59.權利要求1、6或55的方法,還包括將指數與閾值進行比較。
60.權利要求7、18、31、32、33、34、44或59的方法,其中指數通過用于總計測量的生物標志物水平的實函數算法計算,其中算法包括將一個或多個變量乘以一個或多個對應的權重因子,
其中生物標志物水平中每一個的水平被輸入到一個或多個變量中的具體變量中,
其中對應的權重因子對于每個具體變量是獨特的,
其中一個或多個對應的權重因子中的至少一個不同于一。
61.權利要求60的方法,其中算法包括至少一個二元運算。
62.權利要求61的方法,其中至少一個二元運算是除法。
63.權利要求61的方法,其中至少一個二元運算是加法或減法。
64.權利要求60的方法,其中一個或多個權重因子是兩個生物標志物的測量水平的比率。
65.權利要求1、5、7、19、34或47的方法,還包括產生指示女性受試者中存在或不存在先兆子癇的報告。
66.權利要求1、5、7、19、34或47的方法,其中該方法不包括考慮血壓、血糖水平、尿蛋白水平、先兆子癇家族史或體重增加。
67.權利要求1、5、7、19、34或47的方法,其中女性受試者具有以下組中的至少一種癥狀:高于140/90mmhg的血壓、高于100mg/dl的空腹血糖水平、在24小時收集中尿蛋白水平超過5克或者至少分開四小時收集的兩個隨機尿樣的尿蛋白水平超過3+、一周中體重增加超過兩磅、血小板水平在妊娠中期低于155,000(每微升)或在妊娠晚期過程中低于145,000(每微升)、在24小時內少于400毫升的少尿、高于25的體重指數、先兆子癇家族史、肺水腫、紫紺和視力變化。
68.權利要求1或5的方法,其中一個或多個生物標志物選自sflt-1、p1gf、纖連蛋白(fn)、adam-12、hpx和papp-a。
69.權利要求1、5、7、19、34或47的方法,其中生物標志物不包括鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)和血紅素。
70.權利要求18、44或59的方法,其中比較包括將生物標志物與(1)患有先兆子癇的單個妊娠女性或妊娠女性組的生物標志物和(2)沒有患有先兆子癇的妊娠女性組的生物標志物進行比較。
71.權利要求70的方法,其中單個妊娠女性是女性受試者。
72.權利要求70的方法,其中比較包括將生物標志物與各自的重組蛋白指數值進行比較。
73.權利要求1、5、7、19、34或47的方法,其中生物標志物包括一個或多個蛋白質或蛋白質片段。
74.權利要求1、5、7、19、34或47的方法,其中生物標志物包括多核苷酸。
75.權利要求1、5、7、19、34或47的方法,其中測量包括利用免疫測定、質譜、色譜、比濁法、輻射狀免疫擴散或單向輻射狀免疫擴散測定。
76.權利要求1、5、7、19、34或47的方法,其中測量包括通過免疫測定測量。
77.權利要求76的方法,其中免疫測定選自elisa,夾心elisa,競爭性elisa和igm抗體捕獲elisa。
78.一種用于診斷、預后、監測、表征、確定女性受試者中先兆子癇的嚴重性、確認女性受試者中存在先兆子癇或確認女性受試者中不存在先兆子癇的試劑盒,該試劑盒包含:至少兩種不同的特異性用于測定來源于女性受試者的樣品中纖連蛋白(fn)的水平的試劑。
79.權利要求78的試劑盒,還包括兩個或更多個用于測量來源于女性受試者的樣品中兩個或更多個生物標志物的水平的試劑。
80.權利要求79的試劑盒,其中生物標志物是sflt-1、p1gf和papp-a。
81.權利要求79的試劑盒,其中生物標志物是sflt-1、p1gf、papp-a和adam-12。
82.權利要求79的試劑盒,其中生物標志物是sflt-1、p1gf、papp-a和hpx。
83.權利要求79的試劑盒,其中生物標志物是p1gf、papp-a和adam-12。
84.權利要求79的試劑盒,其中生物標志物是sflt-1和p1gf。
85.權利要求79的試劑盒,其中生物標志物是p1gf和papp-a。
86.權利要求79的試劑盒,其中生物標志物是sflt-1、p1gf和adam-12。
87.權利要求79的試劑盒,其中生物標志物是sflt-1和adam-12。
88.權利要求79的試劑盒,其中生物標志物是p1gf、fn、adam-12、sflt1、papp-a2和hpx。
89.權利要求78或79的試劑盒,其中該試劑盒不包括用于測量選自以下生物標志物的水平的試劑:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離βhpc和血紅素。
90.一種用于確認女性受試者中存在或不存在先兆子癇的試劑盒,該試劑盒包括:
a)特異性用于測定papp-a水平的第一試劑;和
b)特異性用于測定adam12水平的第二試劑。
91.權利要求90的試劑盒,其還包含一個或多個用于測量來源于女性受試者的樣品中一個或多個生物標志物的水平的試劑。
92.權利要求91的試劑盒,其中生物標志物是sflt-1、p1gf和纖連蛋白(fn)。
93.權利要求91的試劑盒,其中生物標志物是p1gf和纖連蛋白(fn)。
94.權利要求90或91的試劑盒,其中該試劑盒不包括用于測量選自以下生物標志物的水平的試劑:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離βhpc和血紅素。
95.一種用于診斷、預后、監測、表征、確定女性受試者中先兆子癇的嚴重性、確認女性受試者中存在先兆子癇或確認女性受試者中不存在先兆子癇的試劑盒,該試劑盒包括:
a)特異性用于測定sflt-1或p1gf之一的水平的第一試劑;
b)特異性用于測定纖連蛋白(fn)的第二試劑;和
c)特異性用于測定不同于由第一和第二試劑測定的生物標志物的生物標志物的水平的第三試劑。
96.權利要求95的試劑盒,其中第一試劑特異性用于測定sflt-1的水平,第三試劑特異性用于測定p1gf的水平,并且試劑盒還包括特異性用于測定不同于sflt-1、p1gf和fn的生物標志物的水平的第四試劑。
97.權利要求96的試劑盒,其中第四試劑特異性用于測定papp-a、hpx或adam12的水平。
98.權利要求95、96或97的試劑盒,其中該試劑盒不包括特異性用于測定選自以下生物標志物的水平的試劑:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離βhpc和血紅素。
99.一種用于確認女性受試者中存在或不存在先兆子癇的測試,其中該測試測量來源于女性受試者的樣品的一個或多個生物標志物,其中與所述生物標志物相關的接受者操作特征(roc)值為至少0.8。
100.權利要求99的測試,其中roc值為至少0.9。
101.權利要求99的測試,其中roc值為至少0.95。
102.權利要求99的測試,其中roc值為至少0.98。
103.權利要求99的測試,其中roc值為至少0.984。
104.一種用于確認受試者中存在或不存在先兆子癇的測試,其中該測試測量來源于受試者的樣品中一個或多個生物標志物,其中與所述生物標志物相關的接受者操作特征(roc)值大于與sflt/p1gf相關的roc值。
105.權利要求104的測試,其中女性受試者表現出先兆子癇的臨床癥狀。
106.權利要求104的測試,其中測試包括測量sflt/p1gf的測量水平的比率。
107.權利要求104的測試,其中sflt/p1gf的測量水平的比率是經標準化的、原始的、經調整的或其組合。
108.一種用于診斷、預后、表征、監測、確定女性受試者中先兆子癇的嚴重性、確認女性受試者中存在先兆子癇或確認女性受試者中不存在先兆子癇的系統,該系統包括:
(a)輸入模塊,其用于接收一個或多個生物標志物的輸入水平;
(b)處理器,其被配置為:
執行將一個或多個生物標志物的水平相對于訓練集進行調整的第一算法,從而提供一個或多個經調整的生物標志物水平;和
執行使用經調整的生物標志物水平應用至少一個二元運算的第二算法,其中第二算法是得到指數值的實函數;和
(c)輸出模塊,其用于輸出指數值,其中指數值指示用于女性受試者中先兆子癇的診斷、預后、表征、監測的方面、嚴重性的確定、存在的確認或不存在的確認。
109.一種用于確認女性受試者中存在或不存在先兆子癇的系統,該系統包括:
(a)輸入模塊,其用于接收一個或多個生物標志物的輸入水平;
(b)處理器,其被配置為:
執行將一個或多個生物標志物的水平相對于對照值進行調整的第一算法;和
執行加上或減去一個或多個經調整的生物標志物水平的第二算法,其中第二算法是得到指數值的實函數;和
(c)輸出模塊,其用于輸出指數值,其中指數值指示女性受試者中不存在或存在先兆子癇。
110.一種用于確認女性受試者中存在或不存在先兆子癇的系統,該系統包括:
(a)輸入模塊,其用于接收兩個或更多個生物標志物的輸入水平;
(b)處理器,其被配置為:
執行將兩個或更多個生物標志物的水平相對于對照值進行調整的第一算法,從而提供兩個或更多個經調整的生物標志物水平;和
執行計算兩個或更多個經調整的生物標志物水平中的兩個之間的比率的第二算法,其中第二算法是得到指數值的實函數;和
(c)輸出模塊,其用于輸出指數值,其中指數值指示女性受試者中存在或不存在先兆子癇。
111.權利要求108、109或110的系統,其中實函數包括復雜統計算法。
112.權利要求108、109或110的系統,其中實函數包括至少一個二元運算。
113.權利要求112的系統,其中實函數包括將變量乘以對應的權重因子。
114.權利要求113的系統,其中每個生物標志物的水平被輸入到對應于生物標志物的具體變量中,并且其中對應的權重因子對于每個變量是獨特的或對于每兩個變量的比率是獨特的。
115.權利要求108的系統,其中處理器還被配置為執行對一個或多個經調整的生物標志物水平中的每一個進行平均的第三算法。
116.權利要求108的系統,其中處理器還被配置為執行對水平應用對數變換以獲得對數變換水平的第三算法;將每個對數變換水平標準化為標準化水平的第四算法;以及將每個標準化水平調整為加權標準化水平的第五算法。
117.一種用于診斷、預后、監測、表征、確定女性受試者中先兆子癇的嚴重性、確認女性受試者中存在先兆子癇或確認女性受試者中不存在先兆子癇的系統,該系統包括:
(a)輸入模塊,其用于接收一個或多個生物標志物的輸入水平;
(b)處理器,其被配置為:
執行將一個或多個生物標志物中的每一個的水平相對于對應的對照值進行調整的算法,由此提供一個或多個經調整的生物標志物水平;
執行實函數算法,其通過將一個或多個變量乘以一個或多個對應的權重因子來操作一個或多個經調整的生物標志物水平,其中一個或多個經調整的生物標志物水平中的每一個的水平被輸入到一個或多個變量中的具體變量中,其中對應的權重因子對于每個具體變量是獨特的,其中對應的權重因子中的至少一個不同于一;和
(c)輸出模塊,其用于輸出指數值,其中指數值指示女性受試者中先兆子癇的診斷、預后、表征、監測的方面、嚴重性的確定、存在的確認或不存在的確認。
118.權利要求109、110或117的系統,其中,使用訓練集來產生對照值。
119.權利要求117的系統,其中訓練集基于模型。
120.權利要求117的系統,其中訓練集基于從受試者獲得的實際值。
121.權利要求120的系統,其中受試者包括至少150個受試者。
122.權利要求120的系統,其中受試者包括復雜受試者。
123.權利要求122的系統,其中復雜受試者包括用于訓練集的所有受試者的至少10%。
124.權利要求117的系統,其中算法應用至少一個二元運算。
125.權利要求124的系統,其中至少一個二元運算是除法。
126.權利要求124的系統,其中至少一個二元運算是加法或減法。
127.一種用于確認受試者中先兆子癇的測試,其中該測試能夠以至少為0.8的接受者操作特征(roc)值辨別沒有先兆子癇但具有一個或多個與先兆子癇相關的癥狀的受試者與患有先兆子癇的受試者。
128.權利要求127的測試,其中roc值為至少0.9。
129.權利要求127的測試,其中與先兆子癇相關的一個或多個癥狀選自糖尿病、高于正常葡萄糖水平、高血壓、過度或突然的體重增加、超重、肥胖、高于正常體重指數、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果、先前先兆子癇發作、先兆子癇家族史、腎病和血栓形成傾向。
130.權利要求129的測試,其中糖尿病是妊娠糖尿病、i型或ii型糖尿病。
131.權利要求129的測試,其中高血壓是慢性高血壓。
132.一種用于確認受試者中先兆子癇的測試,其中該測試能夠以至少80%的敏感性辨別沒有先兆子癇但具有一個或多個與先兆子癇相關的癥狀的受試者與患有先兆子癇的受試者。
133.一種用于確認受試者中先兆子癇的測試,其中該測試能夠以至少80%特異性辨別沒有先兆子癇但具有一個或多個與先兆子癇相關的癥狀的受試者與患有先兆子癇的受試者。
134.一種用于確認受試者中先兆子癇的測試,其中該測試能夠以至少為80%的陰性預測值(npv)辨別沒有先兆子癇但具有一個或多個與先兆子癇相關的癥狀的受試者與患有先兆子癇的受試者。
135.權利要求132、133或134的測試,其中與先兆子癇相關的一個或多個癥狀選自糖尿病、高于正常葡萄糖水平、高血壓、過度或突然的體重增加、超重、肥胖、高于正常體重指數、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果、先前先兆子癇發作、先兆子癇家族史、腎病和血栓形成傾向。
136.權利要求135的測試,其中糖尿病是妊娠糖尿病、i型或ii型糖尿病。
137.權利要求135的測試,其中高血壓是慢性高血壓。
138.權利要求135的測試,其中靈敏度為至少90%。
139.權利要求133的測試,其中特異性為至少90%。
140.權利要求134的測試,其中npv為至少90%。
141.一種用于確認先兆子癇的方法,該方法包括對來源于女性受試者的樣品進行測試,其中測試包括測量多個標志物的水平,并使用多個標志物的水平來以至少為0.90的接受者操作特征(roc)值確認先兆子癇。
142.如權利要求141的方法,其中roc值為至少0.95。
143.一種用于確認先兆子癇的方法,該方法包括對來源于女性受試者的樣品進行測試,其中測試包括測量多個標志物的水平,并使用多個標志物的水平來以至少為80%的特異性確認先兆子癇。
144.權利要求143的方法,其中特異性為至少90%。
145.一種用于確認先兆子癇的方法,該方法包括對來源于女性受試者的樣品進行測試,其中測試包括測量多個標志物的水平,并使用多個標志物的水平來以至少為80%的靈敏度確認先兆子癇。
146.權利要求145的方法,其中靈敏度為至少90%。
147.一種用于確認先兆子癇的方法,該方法包括對來源于女性受試者的樣品進行測試,其中測試包括測量多個標志物的水平,并使用所述水平來以至少為80%的陰性預測值確認先兆子癇。
148.權利要求147的方法,其中陰性預測值為至少90%。
149.權利要求127-140中任一項的測試,其中樣品選自全血、尿液、血清和血漿。
150.權利要求141-148中任一項的方法,其中樣品選自全血、尿液、血清和血漿。
151.權利要求1-7、31、34、60、141、143或147中任一項的方法,其中生物標志物包括第1組的生物標志物。
152.權利要求30、126或131-134中任一項的測試,其中生物標志物包括第1組的生物標志物。
153.權利要求108-110或116中任一項的系統,其中生物標志物包括第1組的生物標志物。
154.權利要求78、90或95中任一項的試劑盒,其中生物標志物包括第1組的生物標志物。
155.一種包含指令的計算機可讀介質,指令在由計算機系統執行時使得計算機系統:
在第一時間點接收與來源于受試者的第一生物樣品中的多個先兆子癇生物標志物的第一水平有關的第一數據集;
對第一水平進行第一分析以獲得受試者中先兆子癇的第一評估;
在第二時間點接收與來源于受試者的第二生物樣品中的多個先兆子癇生物標志物的第二水平有關的第二數據集;
對第二水平進行第二分析以獲得受試者中先兆子癇的評估;
將第一評估與第二評估進行比較;和
基于比較確認先兆子癇或缺乏先兆子癇。
156.一種用于診斷或確認受試者中先兆子癇的方法,該方法包括:
檢測來源于受試者的生物樣品中的sflt、pig和結合于畢赤霉素抗體的蛋白質或蛋白質片段的蛋白質水平;和
使用檢測到的蛋白質水平計算先兆子癇指數評分,其中先兆子癇評分指示受試者中存在或不存在先兆子癇。
157.權利要求156的方法,還包括診斷或確認受試者中的先兆子癇。
158.權利要求156的方法,其中計算包括將檢測的蛋白質水平乘以獨特的權重因子,以及將一個或多個二元函數應用于加權的檢測蛋白質水平。
159.權利要求3的方法,其中四個或更多個生物標志物中的每一個選自sflt-1、p1gf、abfn、papp-a、takfn、adam-12和hpx,其中四個或更多個生物標志物中的每一個彼此不同。
160.權利要求5或49的方法,其中一個或多個生物標志物包括四個或更多個生物標志物,其中四個或更多個生物標志物中的每一個選自sflt-1、p1gf、abfn、papp-a、takfn、adam-12和hpx,其中四個或更多個生物標志物中的每一個彼此不同。
161.權利要求7或20的方法,其中兩個或更多個生物標志物包括四個或更多個生物標志物,其中四個或更多個生物標志物中的每一個選自sflt-1、p1gf、abfn、papp-a、takfn、adam-12和hpx,其中四個或更多個生物標志物中的每一個彼此不同。
162.權利要求79的試劑盒,其中兩個或更多個生物標志物包括四個或更多個生物標志物,其中四個或更多個生物標志物中的每一個選自sflt-1、p1gf、abfn、papp-a、takfn、adam-12和hpx,其中四個或更多個生物標志物中的每一個彼此不同。
通過引用并入
本說明書中提及的所有出版物、專利和專利申請通過引用并入本文,其程度如同每個單獨出版物、專利或專利申請被具體和單獨地指明通過引用并入。
附圖簡要說明
當結合附圖閱讀時,從下面的詳細描述可以最好地理解本公開。要強調的是,根據通常的實踐,附圖的各種特征不是按比例的。相反,為了清楚起見,各種特征的尺寸被任意地擴大或縮小。附圖中包括以下附圖。
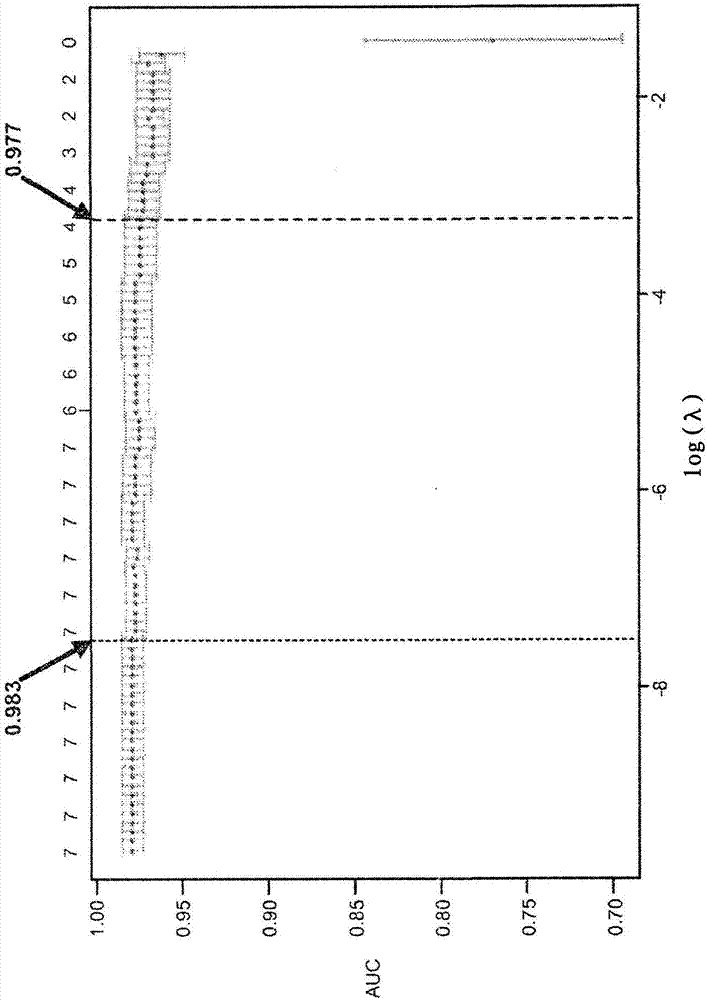
圖1描繪了具有數量增加的標志物的一系列懲罰模型的性能。該圖顯示了平均交叉驗證性能和對應的標準誤差。頂部的數字表示模型的大小,而箭頭標識具有最高曲線的下面積(auc)的模型和具有最大1-se(模型選擇的“1-se”規則)內的平均auc的模型。
圖2描述了具有不包括sflt-1/plgf的數量增加的標志物的一系列處罰模型的性能。該圖顯示了平均交叉驗證性能和對應的標準誤差。頂部的數字表示模型的大小,而箭頭標識具有最高auc的模型和具有最大1-se(模型選擇的“1-se”規則)內的平均auc的模型。
圖3是描述具有2x一式兩份的hi和lo質量對照的32個樣品的一式兩份模板的圖。
圖4是描述具有3x一式三份的hi和lo質量對照的20個樣品的一式三份模板的圖。
圖5a-5f提供了各種pe生物標志物的列表(也參見表2)。
圖6是20個化合物的主要單元的示意圖。
發明詳述
本文提供了用于確認先兆子癇診斷、確認“先兆子癇(pre-eclampsia)”或“先兆子癇(preeclampsia)”或“pe”的存在和/或不存在、預測受試者將發展pe的可能性、確定和/或確認pe的嚴重性、確定未妊娠的受試者如果受試者變為妊娠的受試者其發展pe的易感性,以及監測已經診斷患有pe的受試者的pe進展的方法、組合物、系統和軟件,所有這些比傳統的pe測試具有更大的靈敏度、特異性、置信度、準確度或曲線下的面積。
方法涉及分析來源于受試者的一個或多個樣品以確認一個或多個pe生物標志物的存在、不存在、數量和/或構象。來源于受試者的樣品可以是全血、尿液、血清、血漿和生物來源的其他液體樣品或來源于其的細胞及其后代。樣品可以在其采購后以任何方式操作,例如通過用試劑處理、增溶或富集某些組分。“標志物”或“生物標志物”是與不會獲得先兆子癇的個體相比,在將獲得或患有先兆子癇的個體的樣品中以不同方式表示的任何生物實體。如果例如在不同的水平(例如蛋白質、rna或dna的量)、不同的三維狀態(天然形式、錯誤折疊、替代構象)或不同的排列(例如,復雜物、聚集體、錯誤折疊組裝體)發現生物標志物,則以不同方式表示生物標志物。
pe生物標志物可以是蛋白質、蛋白質片段、肽、多核苷酸、基因(dna)或基因片段、rna轉錄物或其他形式的rna,例如snrna、sirna和微rna。本申請中使用的術語“蛋白質”、“肽”和“多肽”是可以互換的。“多肽”是指氨基酸的聚合物,并且包括翻譯后修飾的多肽、糖基化多肽、乙酰化多肽、磷酸化多肽等。
本文考慮的pe生物標志物的實例包括但不限于圖5a-5f(或表2)中列出的標志物。
可以通過獲得“先兆子癇譜”、“pe譜”或“譜”來進行pe的存在、不存在、監測或預測。pe譜是患者樣品中一個或多個先兆子癇生物標志物的水平。pe生物標志物可以通過測量蛋白質水平或表達水平來確定。pe譜可以包括表1所示的pe生物標志物的以下組(小組)中的任何一個或多個。
表1
pe譜的其他示例包括以下中的任何一個或多個:
·sflt1/p1gf的比率和選自fn、papp-a、hpx和adam12的至少一種生物標志物,
·至少兩個選自p1gf、adam12、fn、papp-a和hpx的生物標志物。
·fn、fg和至少一個或兩個選自hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、p1gf和adam12的生物標志物。
·hpx與fn、fg、sflt-1、papp-a、vegf(不包括vegf-r1)、p1gf和/或adam12組合
·sflt-1與fn、fg、hpx、papp-a、vegf(不包括vegf-r1)、p1gf和/或adam12組合。
·papp-a與fn、fg、hpx、sflt-1、vegf(不包括vegf-r1)、p1gf和/或adam12組合。
·可以與fn、fg、hpx、papp-a、sflt-1、p1gf和/或adam12組合測量vegf(不包括vegf-r1)。
·p1gf與fn、fg、hpx、papp-a、sflt-1、vegf(不包括vegf-r1)和/或adam12組合。
·adam12與fn、fg、hpx、papp-a、sflt-1、p1gf和/或vegf(不包括vegf-r1)組合。
·sflt-1、p1gf、fn、fg和pappa-a;
·sflt-1、p1gf、adam12和fn、fg;
·sflt-1、p1gf、pappa-a和fn、fg;
·sflt-1、p1gf、hpx、papp-a和fn、fg;
·p1gf、adam12、papp-a、fn、fg;
·sflt-1、p1gf和fn、fg、p1gf、fn、fg、papp-a
·fn、fg、sflt-1、p1gf和fn、fg;
·sflt-1、fn、fg和adam12;
·p1gf、fn、fg和papp-a;
·p1gf和adam12;
·fn、fg和adam12、hpx、fn、fg、和adam12、hpx、adam12和pappa、hpx和pappa、sflt-1和p1gf.
本文的任何pe生物標志物譜或小組可任選地不包括一個或多個以下生物標志物:鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)和血紅素。
在一些情況下,該生物標志物小組包括至少2、3、4、5、6、7、8、9、10或15個生物標志物。優選地,本公開的方法包括測定本文所述的一個或多個小組的蛋白質水平。當小組包括sflt1和plgf的比率時,比率可以是sflt-1和p1gf的原始水平的比率、sflt-1和plgf的標準化或經調整的水平(例如,相對于持家基因,例如abl1、gapdh、pgk1、或相對于整個小組中的信號)的比率、平均水平的比率或與對照相比的水平的比率(例如,純化、重組蛋白)。
當分析多個pe生物標志物時,可以使結果經受提供單個分數(例如pe分數)的算法或pe評分函數。先兆子癇評分是代表患者樣品中的一個或多個先兆子癇生物標志物的單一度量值。可以在給受試者或受試者的保健服務提供商的報告中報告pe評分。
pe評分可以作為pe指數報告。“pe指數”或“指數”是指示確認pe的可能性、pe的嚴重性或發展pe的可能性的程度的度量系統。可以使用分類算法從pe評分計算pe指數。受監督和不受監督的分類過程的示例于jain,“statisticalpatternrecognition:areview”,ieeetransactionsonpatternanalysisandmachineintelligence,vol.22,no.1,january2000中。
pe評分或指數可以指示pe診斷的診斷、預后或確認。除了pe評分或pe指數,報告還可以提供一套建議的治療或當前治療有效性的評估。本文所使用的術語“診斷”(“diagnosing”或“diagnosis”)是指確定受試者是否患有pe。本文所使用的術語“確認”(“confirming”或“confirmation”)一般包括確定懷疑患有pe或先前診斷為患有pe的受試者是否患有pe。本文使用的術語“預后”(“prognosing”或“prognosis”)一般包括預測受試者中pe的可能病程,例如pe嚴重性增加的可能性或受試者對治療的響應性。本文所使用的術語“治療”(“treating”或“treatment”)一般是指獲得所需的藥理學和/或生理學效果。該效果可以在以下方面是預防性的:完全或部分預防疾病或其癥狀(例如,降低發病的可能性)、降低疾病的發病率或嚴重性,和/或在以下方面是治療性的:部分或完全治愈疾病,和/或可歸因于疾病的不良效果。在確定pe評分時,通過獲得例如光密度(od)值來獲得生物標志物的原始水平。原始數據可以用于使用本文的方法確定樣品中生物標志物的濃度,所述方法可包括與標準曲線的比較。標準曲線可以具有決定系數。在一些情況下,決定系數可以是r2值,例如,本文所述的方法可以使用≥0.5、0.6、0.7、0.75、0.8、0.85、0.9或0.95的r2值。在示例性情況下,使用本文方法的標準曲線的r2≥0.95。可以使用本領域普通技術人員已知的統計方法來評估數據的附加情況。諸如softmaxpro的軟件可以用于執行本文所述的至少一些計算和分析。落在標準曲線范圍之外的采集數據不會被進一步分析或計算。
生物標志物的原始水平可任選地相對于例如空白、對照或本文所述的另一樣品進行標準化。在一些情況下,標準化可以包括從樣品的od值中減去空白、對照或另一個樣品的od值。標準化還可以包括首先取樣品的od的平均值(average)、平均數(mean)或中值(median),并且其次取空白、對照或另一個樣品的平均值、平均數或中值od,然后將這兩個od值相減。
在一些情況下,將個體樣品的原始od值,一組樣品的平均值、平均數或中值od值,一個空白、一個對照、另一個樣品、一組空白、一組對照或另一組樣品的原始od值進行對數變換。通常,對數變換可以包括與標準曲線的比較。
生物標志物水平可以相對于以下的一個或多個進行調整:來源于如下更詳細討論的訓練集的對照,在妊娠前被測試的受試者,在pe發作前被測試的受試者,來自沒有患有pe的妊娠受試者的平均數值,來源于指定實驗室受試者的值,計算值,對應的純化生物標志物或對應的重組生物標志物,來源于沒有患有pe或沒有pe癥狀的妊娠受試者的樣品的對照水平,來源于未被診斷為患有pe或沒有pe癥狀的妊娠受試者的樣品的對照水平,來源于具有(或被診斷為具有)pe癥狀(例如妊娠癥狀的并發癥)但沒有患有(或未被診斷為患有)pe的妊娠受試者樣品的對照水平,來源于沒有患有pe但具有一個或多個先兆子癇癥狀的妊娠受試者(例如,具有復雜妊娠的妊娠受試者)的樣品的對照水平,所述先兆子癇癥狀例如糖尿病(例如,妊娠糖尿病、i型或ii型糖尿病)、高于正常葡萄糖水平、高血壓(例如慢性或非慢性高血壓)、高于正常體重、肥胖、高于正常體重指數(bmi)、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、先前妊娠的pe、腎病、血栓形成傾向或其任何組合;來源于未被診斷患有pe但具有一個或多個例如上述那些先兆子癇癥狀的妊娠受試者樣品(例如,具有復雜妊娠的懷孕受試者)的對照水平。
當對照值來源于訓練集時,訓練集可以基于理論模型、從受試者獲得的實際(測量)值或兩者的組合。優選地,訓練集基于從至少10、50、100、150、200、250、300、400或500個受試者獲得的實際值。更優選地,訓練集中至少5、10、20、30、40、50或60%的受試者患有pe,而其余受試者是懷孕的并且沒有患有pe。
在一種情況下,通過將每個生物標志物水平(或標準化水平)乘以權重因子或“權重”來調整pe生物標志物水平,以達到加權水平。
然后使用算法、函數、實函數、多項式等計算生物標志物評分或生物標志物指數。此類算法在本文中稱為pe評分函數。pe評分函數中每個生物標志物的權重可以是獨特的。每個生物標志物的權重可以是正或負實數。權重可以是兩個或更多個生物標志物的比率。pe評分函數可以是包括諸如加法、減法、乘法和除法的二元運算的實函數算法。在一些情況下,pe評分函數包括至多一個、兩個、三個、四個、五個、六個或七個二元運算。在一些情況下,所有二元運算是變量的加法或減法(變量是生物標志物值,無論是經調整的還是未經調整的)。在一些情況下,二元運算包括變量的至少一個除法。在一些情況下,二元運算僅包括變量的一個除法。在一些實例中,二元運算不包括變量的除法。在一些情況下,二元運算不包括變量的乘法。
pe評分函數可以是線性的、指數的、對數的、二次的或其任何組合。
用于確定pe評分的pe評分函數可以根據下式表示:
pe評分=a0+a1(比率)+a2(sflt-1)+a3(p1gf)+a4(fn1)+a5(fn2)+a6(pappa)+a7(hpx)+a8(adam12)+a9(fg)+an(選自表1的生物標志物或生物標志物的比率),其中,(i)a0是零或至多-0.5、-1、-5、-10、-20、-30、-40、-50、-60、-70、-80、-90、-100、-110、-120、-130、-140、或-150或者a0是零,(ii)a1是至少0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09或0.10,(iii)a2是零或至少-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、0.001、0.01、0.05、0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0或5.0,(iv)a3是零或至少-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、0.001、0.01、0.05、0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0或5.0,(iv)a4是零或至少2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5、11.0、11.5、12.0、12.5、13.0、13.5、14.0、14.5、15.0或15.5,(v)a5是零或至少-13.0、-12.0、-11.0、-10.0、-9.0、-8.0、-7.0、-6.0、-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、0.001、0.01、0.05、0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0或5.0,(vi)a6是零或至少-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、-0.5、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5或8.0,(vii)a7是零或至少0.01、0.05、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.2、1.3、1.4、1.5、1.6、1.7、1.8、2.0或2.5,(viii)a8是零或至少-13.0、-12.0、-11.0、-10.0、-9.0、-8.0、-7.0、-6.0、-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、0.001、0.01、0.05、0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5、11.0、11.5、12.0、12.5、13.0、13.5、14.0、14.5、15.0或15.5,(ix)a9是零或至少-13.0、-12.0、-11.0、-10.0、-9.0、-8.0、-7.0、-6.0、-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、0.001、0.01、0.05、0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5、11.0、11.5、12.0、12.5、13.0、13.5、14.0、14.5、15.0或15.5,(x)an是零或至少-13.0、-12.0、-11.0、-10.0、-9.0、-8.0、-7.0、-6.0、-5.0、-4.0、-3.5、-3.0、-2.5、-2.0、-1.5、-1.0、0.001、0.01、0.05、0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5、11.0、11.5、12.0、12.5、13.0、13.5、14.0、14.5、15.0或15.5,以及(xi)比率可以是兩個或更多個生物標志物的任意比率,包括,例如sflt-1/p1gf、p1gf/sflt-1、(sflt-1)/(不包括vegf-r1的vegf)、(不包括vegf-r1的vegf)/p1gf、(不包括vegf-r1的vegf)/sflt-1、p1gf/(不包括vegf-r1的vegf);(xii)fn1表示由第一抗體檢測的纖連蛋白的同種型,fn2表示由第二抗體檢測的纖連蛋白同種型,其中兩種同種型可以相同或不同,并且其中兩種抗體不同。
提供用于確定pe評分的線性模型的非限制性示例如下:l=-52.651+0.214*比率-0.877plgf-0.715*hpx-0.884*adam12+pappa*3.85+4.473*fn;l=-46.789+0.018*比率-0.879*plgf-0.587*hpx-0.973*adam12+pappa*3.121+4.007*fn;l=-49.789+0.012*比率-0.984*plgf-0.652*hpx-0.968*adam12+pappa*3.22+4.105*fn;l=-50.789+0.019*比率-0.977plgf-0.695*hpx-0.910*adam12+pappa*3.62+4.351*fn;l=-48.989+0.022*比率-0.998plgf-0.731*hpx-0.971*adam12+pappa*3.41+4.317*fn;l=-58.899+0.014*比率-0.912*plgf-0.486*hpx-0.853*adam12+pappa*2.191+4.097*fn;l=-49.211+0.017*比率-0.974plgf-0.785*hpx-0.957*adam12+pappa*3.68+4.324*fn;l=-48.789+0.011*比率-0.899*plgf-0.487*hpx-0.873*adam12+pappa*2.121+4.007*fn;l=-52.838+0.009*比率-0.942*plgf-0.533*hpx-0.899*adam12+pappa*2.460+4.212*fn;l=-51.828+0.119*比率-0.762*plgf-0.618*hpx-0.711*adam12+pappa*2.243+5.921*fn;l=-47.298+0.122*比率-1.298*plgf-0.723*hpx-0.932*adam12+pappa*1.920+3.929*fn;l=-47.562+1.292*比率-0.298*plgf-0.722*hpx-0.921*adam12+pappa*3.291+4.118*fn。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-20.0484+0.1478(比率)+3.2970(pappa);l=-20.1484+0.0478(比率)+3.0970(pappa);l=-21.0484+2.1478(比率)+4.2970(pappa);l=-20.3484+0.4478(比率)+3.5970(pappa);l=-77.6525+0.1405(比率)+5.1705(fn1);l=-79.6525+1.0405(比率)+7.1705(fn1);l=-78.7525+0.2405(比率)+6.2705(fn1);和l=-78.6525+0.0405(比率)+6.1705(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-77.0827+9.0491(比率)+8.5207(plgf)+7.1632(fn1);l=-79.0827+0.1491(比率)+0.2207(plgf)+6.3632(fn1);l=-78.0827+0.0491(比率)+0.5207(plgf)+6.1632(fn1);l=-76.0827+0.4491(比率)+0.6207(plgf)+6.7632(fn1);
l=-87.8431+0.0422(比率)+0.9659(hpx)+6.3886(fn1).l=-86.8431+0.1422(比率)+0.8659(hpx)+6.2886(fn1);l=-88.8431+0.1422(比率)+1.9659(hpx)+7.3886(fn1);和=-85.8431+0.2422(比率)+0.3659(hpx)+6.4886(fn1);
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-49.0767+0.0462(比率)+3.2997(fn2)+3.8873(pappa);l=-48.0767+0.0462(比率)+2.2997(fn2)+2.8873(pappa);l=-48.1767+0.2462(比率)+2.3997(fn2)+2.4873(pappa)和l=-48.5767+0.6462(比率)+2.7997(fn2)+2.9873(pappa)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-85.7092+0.0492(比率)-5.8358(fn2)+12.7388(fn1);l=-85.1092+0.2492(比率)-5.3358(fn2)+12.4388(fn1);l=-86.7092+0.1492(比率)-6.8358(fn2)+13.7388(fn1);和l=-85.5092+0.6492(比率)-5.7358(fn2)+12.8388(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-68.2829+1.0405(比率)+2.0848(adam12)+3.1148(fn1);l=-88.2829+2.0405(比率)+3.0848(adam12)+4.1148(fn1);l=-79.2829+0.1405(比率)+0.2848(adam12)+7.1148(fn1);和l=-78.2829+0.0405(比率)+0.0848(adam12)+6.1148(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-12.2190+2.0500(比率)+3.7240(pappa)+4.2174(fn1);l=-82.2190+0.0500(比率)+2.7240(pappa)+5.2174(fn1);l=-22.2190+3.0500(比率)+4.7240(pappa)+6.2174(fn1);和l=-32.2190+4.0500(比率)+5.7240(pappa)+7.2174(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-29.9815+4.0348(sflt1)-5.5288(fn2)+16.2160(fn1);l=-39.9815+4.0348(sflt1)-5.5288(fn2)+17.2160(fn1);l=-19.9815+2.0348(sflt1)-3.5288(fn2)+14.2160(fn1);和l=-59.9815+3.0348(sflt1)-7.5288(fn2)+12.2160(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-12.4750+-3.8232(plgf)+4.8961(pappa)+6.7670(fn1)l=-92.4750+-2.8232(plgf)+2.8961(pappa)+5.7670(fn1)l=-22.4750+-3.8232(plgf)+4.8961(pappa)+7.7670(fn1);和l=-32.4750+-4.8232(plgf)+5.8961(pappa)+9.7670(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-14.0940+0.0441(比率)+2.4773(sflt1)+3.5748(plgf)+4.8088(fn1);l=-24.0940+3.0441(比率)+4.4773(sflt1)+5.5748(plgf)+6.8088(fn1);l=-74.0940+0.0441(比率)+0.4773(sflt1)+0.5748(plgf)+5.8088(fn1);和l=-34.0940+4.0441(比率)+5.4773(sflt1)+6.5748(plgf)+7.8088(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-70.3822+1.0796(比率)-3.7798(sflt1)+4.8134(fn2)+6.2025(pappa);l=-77.3822+0.0796(比率)-2.7798(sflt1)+3.8134(fn2)+5.2025(pappa);l=-71.3822+2.0796(比率)-3.7798(sflt1)+4.8134(fn2)+6.2025(pappa);和l=-72.3822+3.0796(比率)-4.7798(sflt1)+5.8134(fn2)+7.2025(pappa)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-70.3510+1.0348(比率)+2.4503(sflt1)-3.5868(fn2)+14.8250(fn1);l=-78.3510+0.0348(比率)+1.4503(sflt1)-7.5868(fn2)+13.8250(fn1);l=-71.3510+2.0348(比率)+3.4503(sflt1)-4.5868(fn2)+15.8250(fn1);和l=-72.3510+3.0348(比率)+4.4503(sflt1)-5.5868(fn2)+16.8250(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-74.5657+0.0300(比率)+0.8356(sflt1)-0.5594(adam12)+5.9467(fn1);l=-72.5657+0.0370(比率)+0.2756(sflt1)-0.3894(adam12)+4.6467(fn1);l=-79.5657+0.0350(比率)+0.8756(sflt1)-0.5894(adam12)+5.6467(fn1);和l=-67.5657+0.0230(比率)+0.4756(sflt1)-0.1494(adam12)+4.7867(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-100.6298+1.0845(比率)+-3.8124(sflt1)+4.0643(pappa)+6.5308(fn1);l=-108.6298+0.0845(比率)+-2.8124(sflt1)+5.0643(pappa)+6.5308(fn1);l=-101.6298+2.0845(比率)+-3.8124(sflt1)+4.0643(pappa)+5.5308(fn1);和l=-102.6298+3.0845(比率)+-4.8124(sflt1)+6.0643(pappa)+7.5308(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-41.5704+2.0489(比率)+3.1839(plgf)+4.2834(fn2)+5.8683(pappa);l=-42.5704+3.0489(比率)+4.1839(plgf)+5.2834(fn2)+6.8683(pappa);l=-40.5704+1.0489(比率)+2.1839(plgf)+3.2834(fn2)+4.8683(pappa);l=-47.5704+0.0489(比率)+0.1839(plgf)+2.2834(fn2)+2.8683(pappa);l=-80.6889+1.0607(比率)+2.6545(plgf)-3.9105(fn2)+14.8608(fn1);l=-85.6889+0.0607(比率)+0.6545(plgf)-5.9105(fn2)+12.8608(fn1);l=-81.6889+2.0607(比率)+3.6545(plgf)-4.9105(fn2)+15.8608(fn1);和l=-82.6889+3.0607(比率)+4.6545(plgf)-6.9105(fn2)+17.8608(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-77.8703+0.0491(比率)+0.5191(plgf)+0.0523(adam12)+6.1300(fn1);l=-71.8703+2.0491(比率)+3.5191(plgf)+4.0523(adam12)+5.1300(fn1);l=-72.8703+3.0491(比率)+4.5191(plgf)+5.0523(adam12)+7.1300(fn1);和l=-70.8703+1.0491(比率)+2.5191(plgf)+3.0523(adam12)+4.1300(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-81.9135+0.0433(比率)+0.3154(plgf)+1.7019(pappa)+5.2189(fn1);l=-81.9125+0.0533(比率)+0.2154(plgf)+2.7019(pappa)+5.2199(fn1);l=-82.9125+0.0553(比率)+0.3154(plgf)+2.8019(pappa)+4.2199(fn1);和l=-71.9125+0.0633(比率)+0.2254(plgf)+2.7519(pappa)+5.2399(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-49.5169+0.0464(比率)+0.1807(hpx)+2.3236(fn2)+2.8744(pappa);l=-47.5169+0.1464(比率)+0.1857(hpx)+2.4236(fn2)+2.6744(pappa);l=-45.2169+0.0344(比率)+0.2707(hpx)+1.2236(fn2)+2.4544(pappa);和l=-48.5169+0.0564(比率)+0.2807(hpx)+2.1236(fn2)+2.7744(pappa)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-68.9243+0.0583(比率)-0.7927(hpx)-6.2143(fn2)+10.7478(fn1);l=-78.9243+0.0483(比率)-0.6927(hpx)-6.0143(fn2)+12.7478(fn1);l=-77.9243+0.0583(比率)-0.7727(hpx)-6.1243(fn2)+11.8478(fn1);和l=-79.9243+0.1483(比率)-0.6227(hpx)-6.2143(fn2)+12.9478(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-88.0679+0.0309(比率)+0.5208(hpx)+2.6887(pappa)+5.2737(fn1);l=-97.0679+0.0589(比率)+0.6708(hpx)+2.7787(pappa)+5.2937(fn1);l=-77.0679+0.0609(比率)+0.6308(hpx)+2.8787(pappa)+5.3937(fn1);和l=-87.0679+0.0509(比率)+0.6208(hpx)+2.6787(pappa)+5.2937(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-53.7575+0.0542(比率)+3.2134(fn2)-1.5150(adam12)+3.6894(pappa);l=-56.7575+0.0342(比率)+4.0134(fn2)-1.4160(adam12)+3.7094(pappa);l=-55.7575+0.0442(比率)+3.0134(fn2)-1.4150(adam12)+3.6094(pappa);和l=-45.7575+0.0443(比率)+3.2134(fn2)-1.6150(adam12)+3.6084(pappa)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-85.1599+0.0529(比率)-6.5276(fn2)+0.8455(adam12)+13.1454(fn1);l=-85.1499+0.0509(比率)-6.5286(fn2)+0.8435(adam12)+13.1434(fn1);l=-85.1399+0.0409(比率)-6.2286(fn2)+0.7435(adam12)+13.0434(fn1);和l=-87.1499+1.0509(比率)-8.5286(fn2)+1.8435(adam12)+11.1434(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-94.7950+0.0632(比率)-7.5691(fn2)+3.0857(pappa)+13.8372(fn1);l=-95.7950+0.1632(比率)-7.5491(fn2)+3.2857(pappa)+15.8372(fn1);l=-94.8950+0.0642(比率)-7.5591(fn2)+3.0957(pappa)+13.2372(fn1);和l=-94.7960+0.0631(比率)-7.5791(fn2)+4.0857(pappa)+11.8372(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-91.5034+0.0566(比率)-1.8810(adam12)+3.5597(pappa)+6.1198(fn1);l=-92.5034+0.0466(比率)-1.8910(adam12)+3.6597(pappa)+6.2198(fn1);l=-93.5034+0.0467(比率)-1.7910(adam12)+3.6797(pappa)+7.2198(fn1);和l=-82.5034+0.0476(比率)-1.9910(adam12)+4.6597(pappa)+6.5198(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-73.6418+2.3065(sflt1)-1.3341(plgf)-7.4383(fn2)+13.0395(fn1);l=-72.3418+2.2365(sflt1)-1.3131(plgf)-7.4332(fn2)+13.3595(fn1);l=-71.6418+2.1065(sflt1)-1.1141(plgf)-7.1382(fn2)+13.1595(fn1);和l=-72.6418+2.2065(sflt1)-1.3141(plgf)-7.4382(fn2)+13.0595(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-103.5305+-0.3764(sflt1)-3.3328(plgf)+3.4350(pappa)+6.3890(fn1);l=-105.5305+-0.6564(sflt1)-3.5928(plgf)+3.4550(pappa)+6.5890(fn1);l=-104.5305+-0.6764(sflt1)-3.3928(plgf)+3.4850(pappa)+6.4890(fn1);和l=-104.4305+-0.6464(sflt1)-3.4928(plgf)+3.4450(pappa)+6.4490(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-74.1756+3.9467(sflt1)-8.4664(fn2)-2.4423(adam12)+15.3474(fn1);l=-75.1756+3.9167(sflt1)-8.7664(fn2)-2.4923(adam12)+15.3674(fn1);l=-76.1756+3.9667(sflt1)-8.6664(fn2)-2.4623(adam12)+15.6674(fn1);和l=-73.1756+3.9367(sflt1)-8.7364(fn2)-2.4323(adam12)+13.3674(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-76.5467+2.6634(sflt1)-3.2682(adam12)+1.9649(pappa)+6.6178(fn1);l=-68.5467+2.6634(sflt1)-3.2682(adam12)+1.6349(pappa)+6.6178(fn1);l=-74.5467+2.4634(sflt1)-3.4282(adam12)+1.9449(pappa)+6.4178(fn1);l=-78.5467+2.5634(sflt1)-3.2282(adam12)+1.9349(pappa)+6.1178(fn1)
l=-78.8718-2.6772(plgf)-1.7373(hpx)+2.9707(pappa)+5.5077(fn1);l=-75.8618-2.5762(plgf)-1.5573(hpx)+2.9507(pappa)+5.5557(fn1);l=-77.8618-2.6772(plgf)-1.5673(hpx)+2.9106(pappa)+5.5056(fn1);和l=-78.8618-2.6762(plgf)-1.5373(hpx)+2.9107(pappa)+5.5057(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-109.2319-3.7617(plgf)-6.7308(fn2)+3.5194(pappa)+13.6500(fn1);l=-107.2319-3.5617(plgf)-6.3308(fn2)+3.4194(pappa)+13.6700(fn1);l=-108.2319-3.6617(plgf)-6.6308(fn2)+3.2194(pappa)+11.6500(fn1);和l=-119.2319-3.7117(plgf)-6.1308(fn2)+3.5114(pappa)+13.7500(fn1)。
另外的用于確定pe評分的線性模型的非限制性示例包括:l=-112.4589-2.7282(plgf)-2.7122(adam12)+4.4379(pappa)+7.6259(fn1);l=-113.4589-2.7281(plgf)-2.7121(adam12)+4.4279(pappa)+7.6159(fn1);l=-114.4589-2.7381(plgf)-2.7221(adam12)+4.5379(pappa)+7.7159(fn1);和l=-133.4589-2.8281(plgf)-2.7131(adam12)+4.5279(pappa)+7.6169(fn1)。
在一些情況下,使用線性和指數模型來使用以下算法來確定概率:pe=1/(1+exp(-l))。
然后可以總計小組中所有生物標志物的加權水平,并且在一些情況下,例如在sflt和plgf的水平中,加權水平可以形成比率。加權水平和任選比率的總和得到單個加權水平或“pe評分”。每個生物標志物可以具有獨特的權重因子,或者生物標志物的組合可以具有獨特的權重因子。在一些情況下,可通過類似于先兆子癇特征(signature)所述的方法測定先兆子癇評分,例如,患者樣品中的一個或多個先兆子癇標志物中的每一個的水平可以如上進行log2、loge或log10變換和標準化,用于產生先兆子癇譜。
用于計算評分的加權水平可以由參考數據集、“訓練數據集”或“訓練集”來定義。訓練集可以基于模型、從受試者獲得的實際值或其組合。訓練集可包括被診斷為具有pe癥狀的受試者。訓練集可以包括具有pe癥狀但沒有患有pe的受試者。訓練集可以包括具有pe的癥狀但沒有患有pe并且患有一個或多個其他病癥的受試者(例如,患有妊娠并發癥的受試者),例如糖尿病(例如妊娠糖尿病、i型或ii型糖尿病)、高于正常葡萄糖水平、高血壓(例如慢性或非慢性高血壓)、高于正常體重、肥胖、高于正常體重指數(bmi)、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、先前妊娠的pe、腎病、血栓形成傾向或其任何組合。訓練集可以包括診斷為患有一個或多個疾病的pe受試者(例如,患有妊娠并發癥的受試者),例如糖尿病(例如妊娠糖尿病、i型或ii型糖尿病)、高于正常葡萄糖水平、高血壓(例如慢性或非慢性高血壓)、高于正常體重、肥胖、高于正常體重指數(bmi)、異常體重增加、異常血壓、水潴留、遺傳因素、異常蛋白尿、頭痛、水腫、異常蛋白質/肌酐比、異常血小板計數、應激、未經產、異常巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、先前妊娠的pe、腎病、血栓形成傾向或其任何組合。訓練集可以包括至少30、40、50、60、70、80、90、100、150、200、250、300、350或400個受試者。訓練集可以包括來自具有正常妊娠的至少15、50、100、150、200或250個受試者和患有pe的至少15、50、100、150、200或250個妊娠受試者的數據。在一些情況下,多于5%、10%、15%、20%、25%、30%、35%、40%、45%或50%的先兆子癇受試者具有至少一種其他病況(例如高血壓、糖尿病、超重等)。
在一些情況下,用于提供本文所述的“先兆子癇指數”的pe的分類不基于例如血壓、體重增加、水潴留、遺傳因素、蛋白尿、頭痛、水腫、蛋白質/肌酐比、血小板計數、應激、先前妊娠的pe、未經產、年齡,年齡小于20歲,年齡大于35歲、種族,非洲裔美國人和菲律賓人、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作(例如pe的個人病史)、pe的家族史、妊娠數、流產數、體重指數(bmi)、妊娠糖尿病、i型糖尿病、肥胖、葡萄糖水平、當前和過去的藥物、應激、(受試者或其家庭成員的)妊娠前的pe、慢性高血壓、腎病和血栓形成傾向。在一些實例中,pe的分類不基于剛才提到的任何妊娠特征。在一些實例中,pe的分類基于剛才提到的妊娠特征中的至少一個。在一些情況下,pe指數可以基于女性受試者的妊娠期。
本文所述的“報告”是電子或有形文檔,其包括提供與受試者相關的信息的報告元素。受試者報告任選地包括以下中的一個或多個:關于受試者的信息、pe譜、pe評分、pe指數、pe確認、pe診斷、pe預后、pe監測狀態和/或建議的治療。受試者報告還可以包括以下中的一個或多個:1)關于測試設施的信息;2)服務提供商信息;3)患者數據;4)樣品數據;5)評估報告,其可以包括各種信息,包括:a)采用的參考值,和b)測試數據,其中測試數據可以包括例如蛋白質水平測定;和6)其他特征。該報告可用于pe的陽性確認、pe的陰性確認、pe的診斷、pe的特征、pe的進展、pe的嚴重性或pe的預后。pe的陽性確認是指具有pe癥狀的受試者被確認為患有pe的情況。pe的陰性確認是指沒有pe癥狀的受試者被確認為沒有患有pe的情況。這樣的報告可以包括生物標志物、pe評分或pe指數評分的相對權重或特征值。該報告可以包括關于治療的建議(例如,臥床休息、阿司匹林、飲用額外的水、低鹽飲食、控制血壓的藥物、皮質類固醇或早期遞送的建議)。
受試者和樣品
術語“生物樣品”和“樣品”包括血液、尿液、血清、血漿和生物來源的其他液體樣品或來源于其的細胞。一旦從受試者得到樣品,其可以直接使用、冷凍或在合適的培養基中短時間維持。可以使來源于血液的樣品凝塊,并分離和收集血清以用于測定。
2μl至2,000μl的血液、血清或尿液的樣品體積可能足以確定pe評分。在一些實例中,樣品體積范圍為10μl至1,750μl、20μl至1,500μl、40μl至1,250μl、60μl至1000μl、100μl至900μl、200μl至800μl、400μl至600μl。在一些情況下,樣品體積為2-10ml或0.5-5ml或至多10、9、8、7、6、5、4、3、2或1ml。
所分析的受試者可能具有零個或至少一個、兩個、三個、四個或五個因子,這些因素混淆了先兆子癇的診斷。在一些情況下,混淆因子可以選自:高血壓、35歲以上的年齡、高于正常體重、快速體重增加、大于20周的妊娠期、民族性、糖尿病(i型或ii型)、高蛋白尿、腎病、自身免疫疾病、受試者在早期妊娠中的先前pe、以及pe的家族史或孕產婦pe史。
在實施本發明方法中,評估來自受試者的樣品以獲得一個或多個pe生物標志物的水平表示。一個或多個pe生物標志物的水平可用于提供例如如下更詳細描述的pe譜、pe特征、pe評分或pe指數。
可以以多種方式處理受試者樣品,以便增強先兆子癇標志物的檢測。例如,當樣品是血液時,可以在測定之前從樣品中除去紅細胞(例如通過離心)。此類處理可用于降低使用親和試劑檢測先兆子癇標志物水平的非特異性背景水平。先兆子癇標志物的檢測也可以通過使用本領域熟知的程序(例如酸沉淀、醇沉淀、鹽沉淀、疏水沉淀、過濾(使用能夠保留分子大于30kd的過濾器,例如centrim30tm)或親和純化)得到增強。在一些情況下,調整測試樣品和對照樣品的ph并保持在接近中性的ph(例如ph6.5-8.0)。這樣的ph調整將防止復合物形成,從而提供樣品中標志物水平的更準確的定量。在樣品是尿液的情況下,調整樣品的ph并濃縮樣品以增強標志物的檢測。可以使用本領域普通技術人員已知的方法調整ph,例如向堿性或中性ph樣品中加入酸或向酸性或中性ph樣品中加入堿。
可以在測定樣品中至少一種生物標志物的水平之前,將緩沖劑和/或其他試劑加入樣品中以促進樣品的制備。在一些情況下,緩沖劑和/或其他試劑可以包括至少但不限于以下之一:乙二胺四乙酸(edta)、磷酸鹽緩沖鹽水、hanks平衡鹽溶液、ficoll、氯化鈉、檸檬酸鈉、二氧化硅、凝血酶、茶堿(tehophylline)、腺苷、雙嘧達莫、抑蛋白酶多肽(aprotinine)、肝素、肝素鋰、氟化物、草酸鉀、檸檬酸三鈉、檸檬酸和/或葡萄糖(dextrose)。緩沖劑和/或其他試劑可以在惰性基質中混合,例如凝膠、水、鹽水等。
在具體情況下,可以使用血清分離管(serumseparatortube,sst)收集血液樣品。sst可以含有緩沖劑和/或其他試劑。在另一具體情況下,可以使用可含有緩沖劑和/或試劑的clot-2血清分離管收集血液樣品。sst和/或clot-2管可以從諸如bectondickenson的制造商獲得,然而可以使用任何類似的管。在一些情況下,可以使用本領域普通技術人員已知的方法、試劑或化學品處理樣品,使得樣品的組分變成彼此分離。有時,分離血液樣品,使得血清在包含樣品頂部的層中。
受試者樣品通常在妊娠中期或晚期過程中從個體獲得。“妊娠”是指在哺乳動物中懷孕的持續時間,例如在子宮中從受孕直到出生的發育期。受試者樣品可以在妊娠早期,例如在妊娠34周時或之前,例如在妊娠的第20-34周、在妊娠的第24-34周、在妊娠的第30-34周得到。受試者樣品可以在妊娠后期,例如在妊娠的第34、35、36、37或38周后得到。
可以從樣品來源于受試者的時間后不久或至少2、3或4周測定pe譜、特征、評分或指數。在一些情況下,從樣品來源于受試者的時間起最多1、2、3或4天測定pe譜、特征、評分或指數。
一旦從受試者得到樣品,可以加工樣品(例如,分離血漿或血清)。樣品或其部分可以進一步稀釋。樣品或樣品的一部分可以稀釋至少5倍、10倍、50倍、100倍、500倍、1,000倍、5,000倍、10,000倍、15,000倍、20,000倍、30,000倍、35,000倍、40,000倍、45,000倍、50,000倍、55,000倍、60,000倍、65,000倍、70,000倍、75,000倍或80,00倍。
用于檢測生物標志物的技術。
當生物標志物是差異表達的蛋白質水平時,可以通過測量一個或多個蛋白質、蛋白質片段、肽、核酸轉錄物(例如mrna)、基因或基因片段的水平或量來檢測生物標志物。
使用本文的方法和操作方案測定的每個生物標志物可以具有閾值。通常,生物標志物的閾值是測定、方法或操作方案中生物標志物的性能。在一些情況下,本文所述的方法、操作方案和測定可以是準確的、靈敏的和特異性的,并且可以用作陽性或陰性預測值。本文所述的方法、方案和測定可以是至少70%、75%、80%、85%、90%、95%或99%準確的。本文所述的方法、操作方案和測定可以是至多70%、75%、80%、85%、90%、95%或至多99%準確的。本文所述的方法、操作方案和測定可以是至少70%、75%、80%、85%、90%、95%或99%靈敏的。本文所述的方法、操作方案和測定可以是至多70%、75%、80%、85%、90%、95%或約99%靈敏的。本文所述的方法、操作方案和測定可以是至少70%、75%、80%、85%、90%、95%、99%或更高的特異性。本文所述的方法、操作方案和測定可以是至多70%、75%、80%、85%、90%、95%、99%或更低的特異性。本文所述的方法、操作方案和測定可具有至少70%、75%、80%、85%、90%、95%、99%或更高的陽性預測值。本文所述的方法、操作方案和測定可具有至多70%、75%、80%、85%、90%、95%、99%或更低的陽性預測值。本文所述的方法、操作方案和測定可具有至少70%、75%、80%、85%、90%、95%、99%或更高的陰性預測值。本文所述的方法、操作方案和測定可具有至多70%、75%、80%、85%、90%、95%、99%或更低的陰性預測值。
在一些情況下,使用本文所述的方法和操作方案測定的生物標志物可以高于標準曲線樣品的最低濃度存在于樣品中。在其他情況下,使用本文所述的方法和操作方案測定的生物標志物可以低于標準曲線樣品的最低濃度存在于樣品中。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物可以高于標準曲線樣品的最高濃度存在于樣品中。在其他情況下,使用本文所述的方法和操作方案測定的生物標志物可以低于標準曲線樣品的最高濃度存在于樣品中。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物可以高于高質量對照樣品的最低濃度存在于樣品中。在其他情況下,使用本文所述的方法和操作方案測定的生物標志物可以低于高質量對照樣品的最低濃度存在于樣品中。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物可以高于高質量對照樣品的最高濃度存在于樣品中。在其他情況下,使用本文所述的方法和操作方案測定的生物標志物可以低于高質量對照樣品的最高濃度存在于樣品中。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物可以高于低質量對照樣品的最低濃度存在于樣品中。在其他情況下,使用本文所述的方法和操作方案測定的生物標志物可以低于低質量對照樣品的最低濃度存在于樣品中。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物可以高于低質量對照樣品的最高濃度存在于樣品中。在其他情況下,使用本文所述的方法和操作方案測定的生物標志物可以低于低質量對照樣品的最高濃度存在于樣品中。
通常,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加約2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000倍。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500、10,000倍或更多。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加至多2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或小于10000倍。
通常,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低約2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000倍。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000倍或更多。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低至多2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000倍或更低。
通常,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加約百分之2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加至少百分之2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間增加至多百分之2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000或更少。
通常,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低約百分之2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低至少百分之2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000或更多。在一些情況下,使用本文所述的方法和操作方案測定的生物標志物的水平可以在第一測定和第二測定之間降低至多百分之2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、125、150、175、200、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1250、1500、1750、2000、2500、5000、7500或10000或更少。
可以結合臨床測量來考慮本文所述的方法和操作方案。臨床測量可以與以下但不限于的相關:總血壓、舒張壓、收縮壓、平均動脈血壓、通過例如浸漬棒法或24小時收集法檢測的蛋白尿、體重指數、腫脹、腹壓、子宮搏動指數、子宮多普勒測量、循環游離dna、循環游離胎兒dna、胎兒dna和/或血小板減少、胎兒異常、妊娠期、母親年齡、懷孕期間先兆子癇的在先病例、種族或民族性、母親或更遠的先兆子癇史、多胎、首次分娩和受試者的吸煙史。
本公開提供了用于診斷或確認受試者中存在先兆子癇的方法,包括:進行至少兩個不同的測定,其測定來自受試者的樣品中纖連蛋白的水平;以及評估樣品并使用來自多個測定的水平來診斷或確認先兆子癇的存在并計算指數。在一些情況下,該方法還包括基于指數建議用于先兆子癇的治療,治療選自阿司匹林、早產或臥床休息。
本公開提供了用于診斷或確認受試者中存在先兆子癇的方法,包括:評估來源于受試者的樣品中sflt-1和plgf的比率的水平和多個生物標志物的水平,其中不同的生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素;和評估樣品并使用來自前一步驟的水平來確定診斷或確認存在先兆子癇的指數和計算指數。在一些情況下,該方法進一步包括基于該指數,建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。在一些情況下,該方法還包括使用樣品對每個生物標志物重復進行相同的測定。在一些情況下,該方法還包括使用來源于多個相同測定中的每一個的水平確定每個生物標志物的平均水平。在一些情況下,該方法還包括對平均水平進行log2、loge或log10變換。在一些情況下,該方法還包括將每個生物標志物的水平與該生物標志物的標準曲線進行比較。在一些情況下,該方法進一步包括對每個生物標志物加權,其中加權包括將數字提供到多項式中,使得每個標志物具有不同的權重。在一些情況下,計算包括確定經調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的原始水平的比率。在一些情況下,計算包括確定經與對照相比調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的原始水平的比率。
本公開提供了用于診斷或確認受試者中存在先兆子癇的方法,包括:評估來源于受試者的樣品中sflt-1和plgf的比率和多個生物標志物的水平的水平,其中不同的生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素;和評估樣品并使用來自步驟(a)的水平來確定診斷或確認存在先兆子癇的指數。在一些情況下,多個生物標志物選自sflt-1、p1gf、fn和papp-a;sflt-1、p1gf、fn、adam12和papp-a;sflt-1、p1gf、papp-a和fn;sflt-1、p1gf、hpx、fn和papp-a;p1gf、adam12、fn和papp-a;p1gf、fn和papp-a;sflt-1、p1gf和fn;p1gf、fn和papp-a;sflt-1、p1gf、fn和adam12;sflt-1、p1gf和fn;p1gf、sflt-1和fn;sflt-1、fn和adam12;p1gf、fn和papp-a。在一些情況下,該方法進一步包括基于該指數,建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。在一些情況下,該方法還包括使用樣品對每個生物標志物重復進行相同的測定。在一些情況下,該方法還包括使用來源于多個相同測定中的每一個的水平確定每個生物標志物的平均水平。在一些情況下,該方法還包括對平均水平進行log2、loge或log10變換。在一些情況下,該方法還包括將每個生物標志物的水平與該生物標志物的標準曲線進行比較。在一些情況下,該方法進一步包括對每個生物標志物加權,其中加權包括將數字提供到多項式中,使得每個標志物具有不同的權重。在一些情況下,計算包括確定經調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的原始水平的比率。在一些情況下,計算包括確定經與對照相比調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的原始水平的比率。
檢測試劑和抗體
本公開包括可用于測定本文公開的多個生物標志物的水平的檢測試劑和抗體。通常,檢測試劑可以包括用于進行elisa的試劑。
可用于elisa操作方案的市售抗體試劑盒的實例包括但不限于抗p1gf(由uscnlifescienceinc.、roche和r&dsystems分銷)、抗sflt-1(由bosterbio.、r&dsystems、mybiosource.com、antibodies-online、biotrendchemikaliengmbh和enzolifesciences分銷)、抗papp-a(由r&dsystems、raybiotech、ibljapan、drginternational、abnova、uscnlifescience、novusbio、rapidtest、mybiosource、antibodies-online.com、fisherscientific、elabscience、sigmaaldrich、cusabio、anshlabs、demeditec、alpco、amsbio、novateinbio、creativebiomart、biorbyt、biomaticcorporation分銷)、抗vegf(由amsbio、mybiosource、abnova、antibodies-online.com、unitedstatesbiological、biomatikcorporation、cloud-clonecorp、biovendor、bosterimmunoleader、enzolifesciences、fitzgerald、abnova、avivasystemsbiology和creativebiomart分銷)、抗纖連蛋白(由biovendor、bosterimmunoleader、qedbioscience、ebioscience、biorbyt、fitzgerald、amsbio、mybiosource、novateinbio、abnova、avivasystemsbiology、creativebiomart、antibodies-online.com、abcam、novusbiologicals、unitedstatesbiological、eiaab(hongkong)companylimited、biomatikcorporation、cloud-clonecorp分銷)、抗血纖蛋白原(molecularinnovations、fitzgerald、amsbio、biorbyt、mybiosource、novateinbio、abnova,creativebiomart,avivasystemsbiology,antibodies-online.com,abcam、novusbiologicals、unitedstatesbiological、eiaab(hongkong)companylimited、biomatikcorporation、cloud-clonecorp分銷)和抗adam12(由bosterimmunoleader、amsbio、mybiosource、abnova、creativebiomart、antibodies-online.com、genetex、biorbyt、unitedstatesbiological、eiaab(hongkong)companylimited、r&dsystems和cloud-clonecorp分銷)。
方法包括使用本文所述的一個elisa試劑盒和/或抗體檢測本文所述的一個生物標志物的水平。在一些情況下,方法包括使用本文所述的兩個elisa試劑盒和/或抗體檢測本文所述的一個生物標志物的水平。在其他情況下,方法包括使用本文所述的三個elisa試劑盒和/或抗體檢測本文所述的一個生物標志物的水平。在其他情況下,方法包括使用本文所述的四個elisa試劑盒和/或抗體檢測本文所述的一個生物標志物的水平。在其他情況下,方法包括使用本文所述的五個elisa試劑盒和/或抗體檢測本文所述的一個生物標志物的水平。在其他情況下,方法包括使用本文所述的多于五個elisa試劑盒和/或抗體檢測本文所述的一個生物標志物的水平。通常,使用一個、三個、四個、五個或多于五個elisa試劑盒獨立地測量一個生物標志物。在一些情況下,一個、兩個、三個、四個、五個或多于五個elisa試劑盒可以是相同或不同的elisa試劑盒。
方法包括使用本文所述的兩個elisa試劑盒和/或抗體檢測本文所述的兩個生物標志物的水平。在其他情況下,方法包括使用本文所述的三個elisa試劑盒和/或抗體檢測本文所述的兩個生物標志物的水平。在其他情況下,方法包括使用本文所述的四個elisa試劑盒和/或抗體檢測本文所述的兩個生物標志物的水平。在其他情況下,方法包括使用本文所述的五個elisa試劑盒和/或抗體檢測本文所述的兩個生物標志物的水平。在其他情況下,方法包括使用本文所述的多于五個elisa試劑盒和/或抗體檢測本文所述的兩個生物標志物的水平。通常,使用兩個、三個、四個、五個或多于五個elisa試劑盒獨立地測量兩個生物標志物。在一些情況下,兩個、三個、四個、五個或多于五個elisa試劑盒可以是相同或不同的elisa試劑盒。
在其他情況下,方法包括使用本文所述的三個elisa試劑盒和/或抗體檢測本文所述的三個生物標志物的水平。在其他情況下,方法包括使用本文所述的四個elisa試劑盒和/或抗體檢測本文所述的三個生物標志物的水平。在其他情況下,方法包括使用本文所述的五個elisa試劑盒和/或抗體檢測本文所述的三個生物標志物的水平。在其他情況下,方法包括使用本文所述的多于五個elisa試劑盒和/或抗體檢測本文所述的三個生物標志物的水平。通常,使用三個、四個、五個或多于五個elisa試劑盒獨立地測量三個生物標志物。在一些情況下,三個、四個、五個或多于五個elisa試劑盒可以是相同或不同的elisa試劑盒。
在其他情況下,方法包括使用本文所述的四個elisa試劑盒和/或抗體檢測本文所述的四個生物標志物的水平。在其他情況下,方法包括使用本文所述的五個elisa試劑盒和/或抗體檢測本文所述的四個生物標志物的水平。在其他情況下,方法包括使用本文所述的多于五個elisa試劑盒和/或抗體檢測本文所述的四個生物標志物的水平。通常,使用四個、五個或多于五個elisa試劑盒獨立地測量四個生物標志物。在一些情況下,四個、五個或多于五個elisa試劑盒可以是相同或不同的elisa試劑盒。
在某些情況下,針對所選擇的生物標志物的抗體可以是單克隆抗體。在一些情況下,針對所選生物標志物的抗體可以是多克隆抗體。特別感興趣的是針對選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的多個生物標志物的抗體。此類抗體可以是單克隆抗體或多克隆抗體。此類抗體可以是市售的或由使用者使用本領域普通技術人員已知的方法產生。
本領域普通技術人員已知的任何市售抗體可以用于檢測本文列出的生物標志物,并且可以與本發明方法組合使用。例如,市售的抗體可以包括但不限于抗p1gf(由amb、novusbiologicals、nordicbiosite或tebubiologicals分銷)、抗hpx(由sinobiological、pierce、sigmaaldrich、origene、lifespan、proteintechgroup、abdsertotec、biorad、thermofisher、agrisera、angio-proteomie、enzolifesciences、avivasystemsbiology、everestbiotech、r&dsystems、st.john'slaboratory、abbiotec、biorbyt、acrisantibodies、mybiosource、amsbio、abgent、santacruzbiotechnology、creativebiomart、novateinbio、raybiotech、genetex、unitedstatesbiological、abcam、cedarlanelabs、gallusimmunotech、abnova和cloud-clonecorp分銷)、抗sflt-1(由cellsignalingtechnology、lifespanbiosciences、antibodies-online.com、sinobiological、abdserotec、proteintechgroup、bosterimmunoleader、thermofischerscientific、merckmillipore、agrisera、atlasantibodies、fitzgerald、avivasystemsbiology、angio-proteomie、ebioscience、genway、biorbyt、r&dsystems、lifetechnologies、st.john'slaboratory、abbiotec、acrisantibodies、mybiosource、amsbio、santacruzbiotechnology、creativebiomart、origene、novateinbio、raybiotech、novusbiologicals、prosci、genetex、unitedstatesbiological、abbexa、abcam、bioworldtechnologyinc.、abnova、springbioscience和cloud-clonecorp分銷)、抗papp-a(由lifespanbiosciences、thermofisherscientific、abdserotec、bio-rad、merckmillipore、antibodies-online.com、r&dsystems、genway、atlasantibodies、abbiotec、amsbio、mybiosource、santacruzbiotechnology、avivasystemsbiology、biorbyt、creativebiomart、novateinbio、raybiotech、genetex、unitedstatesbiological、fitzgerald、novusbiologicals、abcam、bbisolutions、abnova和cloud-clonecorp分銷)、抗vegf(由cellsignalingtechnology、lifespanbiosciences、antibodies-online.com、epigentek、angio-proteomie、avivasystemsbiology、r&dsystems、st.john'slaboratory、thermofisherscientificinc.、biorbyt、acrisantibodies、mybiosource、santacruzbiotechnology、genetex、unitedstatesbiological、abbexa、fitzgerald、novusbiologicals、abcam、bioworldtechnologyinc.、abnova、sinobiological、merckmillipore、avivasystemsbiology、origene、lifetechnologies、amsbio、abgent、creativebiomart、raybiotech、iblamerica、bosterimmunoleader、atlasantibodies、bioworldtechnologyinc.和cloud-clonecorp分銷)、抗纖連蛋白(由proteintechgroup、fitzgerald、lifespanbiosciences、bosterimmunoleader、abcam、qedbioscience、sinobiological、abdserotech、bio-rad、protenbiotechnikgmbh、beckmancoulter、antibodies-online.com、takara、merckmillipore、atlasantibodies、agrisera、thermofisherscientific,inc.、rockland、immuquest、enzolifesciences、avivasystemsbiology、genway、ebioscience、biorbyt、r&dsystems、amsbio、st.john'slaboratory、abbiotec、acrisantibodies、mybiosource、santacruzbiotechnology、novusbiologicals、creativebiomart、novateinbio、raybiotech、genetex、prosci、unitedstatesbiological、abbexa、abcam、cedarlanelabs、molecularinnovations、southernbiotech、bioworldtechnologyinc.、gallusimmunotech、abnova、alfaaesar和cloud-clonecorp分銷)、抗血纖蛋白原(由lifespanbiosciences、antibodies-online、abdserotec、bio-rad、abseabiotechnology、thermofischerscientificinc.、merckmillipore、agrisera、atlasantibodies、avivasystemsbiology、enzolifesciences、rockland、genway、r&dsystems、st.john'slaboratory、abbiotec、amsbio、acrisantibodies、mybiosource、abgent、biorbyt、santacruzbiotechnology、creativebiomart、origene、novateinbio、raybiotech、genetex、prosci、unitedstatesbiological、fitzgerald、cedarlanelabs、novusbiologicals、molecularinnovations、haematologictechnologiesinc.、dako、oxfordbiomedicalresearch、gallusimmunotech、bioworldtechnologyinc.、abnova、nordicimmunologicallaboratories,和cloud-clonecorp分銷)以及抗adam12(由lifespanbiosciences、sinobiological、abdserotec、bio-rad、thermofischerscientificinc.、merckmillipore、antibodies-online.com、atlasantibodies、enzolifesciences、everestbiotech、angio-proteomie、avivasystemsbiology、proteintechgroup、genway、r&dsystems、st.john'slaboratory、acrisantibodies、mybiosource、amsbio、santacruzbiotechnology、biorbyt、creativebiomart、origene、novateinbio、raybiotech、genetex、prosci、unitedstatesbiological、fitzgerald、novusbiologicals、abcam、abnova和cloud-clonecorp分銷)。
可以使用本領域普通技術人員已知的方法產生特異性結合本文所列的任何生物標志物的單克隆抗體。這些方法包括kohler和milstein(nature,256:495-497,1975)和campbell("monoclonalantibodytechnology,theproductionandcharacterizationofrodentandhumanhybridomas",于burdon等人編輯,laboratorytechniquesinbiochemistryandmolecularbiology,volume13,elseviersciencepublishers,amsterdam,1985中)的方法,以及huse等人描述的方法(science,246,1275-1281,1989)。
單克隆抗體可以從培養的雜交瘤細胞的上清液或通過將雜交瘤細胞腹膜內接種到小鼠中誘導的腹水制備。這些方法描述于kohler和milstein(eur.j.immunol,6,511-519,1976)中。宿主動物或培養的抗體產生細胞的免疫途徑和時間表可以遵循本領域普通技術人員已知的用于抗體刺激和產生的途徑和時間表。通常,將小鼠用作測試模型,然而,任何哺乳動物受試者或來自其的產生抗體的細胞可用于生產哺乳動物(包括人)雜交細胞系。
免疫后,免疫淋巴細胞可與骨髓瘤細胞融合以產生可無限培養的雜交細胞系,以產生單克隆抗體。例如,可以選擇淋巴細胞用于融合,并且可以從淋巴結組織或免疫動物的脾中分離淋巴細胞。鼠骨髓瘤細胞系可以例如從美國典型培養物保藏中心(atcc;manassas,va)獲得。還描述了人骨髓瘤和小鼠-人異源骨髓瘤細胞系(kozbor等人,j.immunol.,133:3001-3005,1984;brodeur等人,monoclonalantibodyproductiontechniquesandapplications,marceldekker,inc.,newyork,pp.51-63,1987)。
雜交細胞系可以在體外維持并以任何量的常規方式儲存和保存,包括在液氮下冷凍和儲存。冷凍的細胞系可以無限期地復蘇和培養。分泌的抗體可以通過常規方法例如沉淀、離子交換色譜、親和色譜等從組織培養物上清液中回收。抗體可以來自以下免疫球蛋白類別中的任一種:igg、igm、iga、igd或ige及其亞類,并且優選地是igg抗體。
在某些情況下,可以包括第一抗體組,其被特異性設計為與所選擇的生物標志物相互作用。例如,第一抗體組可以設計為與選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的蛋白質相互作用。
在一些情況下,除抗體之外的檢測試劑可用于實施本文所述的方法。檢測試劑特異性結合本文所述的生物標志物。除了抗體之外,檢測試劑還可以包括適配體、fc片段、fab片段、fab2片段、scfv結構域、雙抗體、非抗體配體、小分子、肽、多肽、蛋白質、納米顆粒、親和體等。
本公開提供了用于診斷或確認受試者中先兆子癇的存在的方法,包括:進行至少兩個不同的測定,其測定來源于受試者的樣品中纖連蛋白的水平;以及評估樣品并使用來自多個測定的水平來診斷或確認先兆子癇的存在并計算指數。在一些情況下,該方法進一步包括基于該指數,建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。
本公開提供了用于診斷或確認受試者中存在先兆子癇的方法,包括:測量來源于受試者的樣品中sflt-1和plgf的比率的水平和多個生物標志物的水平,其中生物標志物中沒有一個是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素;以及評估樣品并使用來自第一步驟的水平來確定診斷或確認存在先兆子癇的指數并計算指數。在一些情況下,該方法還包括基于指數建議用于先兆子癇的治療的步驟,該治療涉及阿司匹林、早產或臥床休息。在一些情況下,該方法還包括使用樣品對每個生物標志物重復進行相同的測定。在一些情況下,該方法還包括使用來源于多個相同測定中的每一個的水平確定每個生物標志物的平均水平。在一些情況下,該方法還包括對平均水平進行log2、loge或log10變換。在一些情況下,該方法還包括將每個生物標志物的水平與該生物標志物的標準曲線進行比較。在一些情況下,該方法進一步包括對每個生物標志物加權,其中加權包括將數字提供到多項式中,使得每個標志物具有不同的權重。在一些情況下,計算包括確定經調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的原始水平的比率。在一些情況下,計算包括確定經與對照相比調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的原始水平的比率。
本公開提供了用于診斷或確認受試者中存在先兆子癇的方法,包括:測量來源于受試者的樣品中sflt-1和plgf的比率的水平和多個生物標志物的水平,其中生物標志物中沒有一個是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素;以及評估樣品并使用來自第一步驟的水平來確定診斷或確認存在先兆子癇的指數并計算指數。在一些情況下,多個生物標志物選自sflt-1、p1gf、fn和papp-a;sflt-1、p1gf、fn、adam12和papp-a;sflt-1、p1gf、papp-a和fn;sflt-1、p1gf、hpx、fn和papp-a;p1gf、adam12、fn和papp-a;p1gf、fn和papp-a;sflt-1、p1gf和fn;p1gf、fn和papp-a;sflt-1、p1gf、fn和adam12;sflt-1、p1gf和fn;p1gf、sflt-1和fn;sflt-1、fn和adam12;p1gf、fn和papp-a。在一些情況下,該方法進一步包括基于該指數,建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。在一些情況下,該方法還包括使用樣品對每個生物標志物重復進行相同的測定。在一些情況下,該方法還包括使用來源于多個相同測定中的每一個的水平確定每個生物標志物的平均水平。在一些情況下,該方法還包括對平均水平進行log2、loge或log10變換。在一些情況下,該方法還包括將每個生物標志物的水平與該生物標志物的標準曲線進行比較。在一些情況下,該方法進一步包括對每個生物標志物加權,其中加權包括將數字提供到多項式中,使得每個標志物具有不同的權重。在一些情況下,計算包括確定經調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定sflt-1和p1gf的原始水平的比率。在一些情況下,計算包括確定經與對照相比調整的sflt-1和p1gf水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的標準化水平的比率。在一些情況下,計算包括確定與對照相比sflt-1和p1gf的原始水平的比率。
測量方法
測定蛋白質或肽的水平的方法包括但不限于酶免疫測定(eia)、例如酶倍增免疫測定技術(emit)、酶聯免疫吸附測定(elisa)、夾心elisa、競爭性elisa、igm抗體捕獲elisa(macelisa)和微粒酶免疫測定(meia);毛細管電泳免疫測定(ceia)、放射免疫測定(ria);免疫放射測定(irma);熒光偏振免疫測定(fpia)或化學發光測定(cl)。這樣的測定可以是自動化的。免疫測定也可以與激光誘導熒光結合使用。脂質體免疫測定,例如流動注射脂質體免疫測定和脂質體免疫傳感器,也適用于本公開。另外,其中蛋白質/抗體復合物的形成導致增加的光散射的濁度測定法適合用于本公開的方法中,光散射作為標志物濃度的函數被轉換為峰值速率信號。
elisa測定方法的一個實例是競爭性elisa。在該方法中,首先用標記的靶(例如,生物素化的血色素結合蛋白)暴露靶的抗體。隨后將抗體暴露于未標記的靶(例如,血色素結合蛋白)。當將標記的靶和未修飾的靶引入抗體時,兩組靶競爭抗體上的結合位點。可獲得的靶越多,與抗體結合的標記靶的量越少。隨后,將檢測來自標記的靶的可檢測信號。標記可以包括放射性同位素(例如14c、3h、32p、33p、35s、125i和131i)、熒光劑、磷光體、化學發光劑、顯色染料、酶、抗體、顆粒如磁性顆粒、量子點、重元素、核磁共振(nmr)可檢測的同位素,可以通過質譜法檢測的分子或包括綴合物的特異性結合分子。標記可以直接連接到靶,或通過間隔臂(例如聚乙二醇或烴)連接。綴合物的實例包括但不限于鈣調蛋白結合蛋白(cbp)和鈣調蛋白、生物素和抗生物素蛋白的組合、生物素和鏈霉抗生物素蛋白的組合、生物素和
在elisa和基于elisa的測定和/或操作方案中,可以將一個或多個對目的蛋白質特異性的抗體固定在選擇的固體表面,優選顯示蛋白質親和力的表面,例如聚苯乙烯微量滴定板的孔上。在洗滌以除去沒有完全吸附的材料后,用非特異性“封閉”蛋白包被測定板孔,非特異性“封閉”蛋白相對于測試樣品已知是抗原性中性的,例如牛血清白蛋白(bsa)、酪蛋白或牛奶粉的溶液。這允許封閉固定表面上的非特異性吸附位點,從而減少由抗原非特異性結合到表面上引起的背景。洗滌去除未結合的封閉蛋白后,在有利于免疫復合物(抗原/抗體)形成的條件下使固定表面與待測樣品接觸。這樣的條件包括用稀釋劑例如在磷酸鹽緩沖鹽水(pbs)/tween或pbs/triton-x100中的bsa或牛γ-球蛋白(bgg)稀釋樣品,其也傾向于有助于減少非特異性背景,樣品在約25℃-27℃的數量級的溫度下孵育約2-4小時(盡管可以使用其他溫度)。孵育后,洗滌抗血清接觸的表面以除去非免疫復合材料。示例性洗滌程序包括用溶液如pbs/吐溫、pbs/triton-x100或硼酸鹽緩沖劑洗滌。然后可以通過使結合的免疫復合物經受不同于第一抗體的對靶具有特異性的第二抗體并檢測第二抗體的結合來確定免疫復合物形成的發生和量。在某些情況下,第二抗體將具有相關酶,例如脲酶、過氧化物酶或堿性磷酸酶,其在與適當的顯色標記孵育后將產生顏色沉淀。例如,可以使用脲酶或過氧化物酶綴合的抗人igg一段時間并且在有利于形成免疫復合物的條件下(例如,在室溫下在含有pbs(例如pbs/吐溫)的溶液中孵育2小時)。在與第二抗體孵育并洗滌以除去未結合的物質后,標記的量,例如通過與顯色標記如尿素和溴甲酚紫孵育(在脲酶標記的情況下)或2,2'-連氮基-二-(3-乙基-苯并噻唑啉)-6-磺酸(abts)和h2o2(在過氧化物酶標記的情況下)被定量。然后通過測量顏色產生的程度來實現定量,例如使用可見光譜分光光度計。
定量后,數據可以以光學單位表示,例如,如果使用可見光譜分光光度計量化數據,則表示為光密度或od值。在一些情況下,根據如上所述的與第二抗體一起使用的反應性底物,數據可以表示為吸光度、發射、放射性計數等。在任何情況下,可以從含有可檢測底物的任何孔定量的光學單元中減去從不含可檢測底物(例如空白)的任何孔定量的光學單元的量值。該值可以是經調整的光學單位值或經調整的od,并且包括在本文所述的進一步的計算中。在一些情況下,可以不從含有可檢測底物的任何孔定量的光學單元中減去從不含可檢測底物(例如空白)的任何孔定量的光學單元的量值。該值可以是原始光學單位值或原始od,并且包括在本文所述的進一步的計算中。
或者,可以使用用于測量樣品中一個或多個蛋白質水平的基于非elisa的方法。代表性實例包括但不限于質譜、色譜、蛋白質組陣列、xmaptm微球技術、流式細胞術、蛋白質印跡、光譜術、比濁法、輻射狀免疫擴散技術、單向免疫擴散測定、蛋白質消化和肽分析(例如由appliedproteomics描述的方法和系統)和免疫組織化學。
質譜法可以包括任何質譜(massspectrometric,ms)技術,其可以獲得關于肽的質量的精確信息,并且優選地還可以獲得所選肽的片段化和/或(部分)氨基酸序列的精確信息(例如,在串聯質譜,ms/ms;或源后衰變,tofms),在本文中是有用的。合適的肽ms和ms/ms技術和系統本身是眾所周知的,并且可以在本文中使用,以及與質譜聯用的液相色譜(lc-ms)和與串聯質譜聯用的二維液相色譜(2d-lc-ms/ms)。適合于生物標志物肽分析的ms排列、儀器和系統可以包括但不限于基質輔助激光解吸/電離飛行時間(maldi-tof)ms;maldi-tof源后衰變(psd);maldi-tof/tof;表面增強激光解吸/電離飛行時間質譜(seldi-tof)ms;電噴霧電離質譜(esi-ms);esi-ms/ms;esi-ms/(ms)n(n是大于零的整數);esi3d或線性(2d)離子阱ms;esi三重四極ms;esi四極正交tof(q-tof);esi傅里葉變換ms系統;硅上解吸/電離(dios);二次離子質譜法(sims);大氣壓化學電離質譜(apci-ms);apci-ms/ms;apci-(ms)n;大氣壓光電離質譜(appi-ms);appi-ms/ms;和appi-(ms)n。可以使用本領域中建立的方式(例如,碰撞誘導解離(cid))實現串聯ms(ms/ms)排列中的肽離子片段化。通過質譜法對生物標志物的檢測和定量可以涉及多反應監測(mrm)。ms肽分析方法可以有利地與上游肽或蛋白質分離或分級分離方法組合,例如與色譜法和其他方法。
在一些情況下,可以在分析、測量、定量等之前衍生或修飾生物標志物蛋白。本領域普通技術人員已知的方法可用于衍生或修飾蛋白質。本文列出的蛋白質生物標志物的多態性或修飾可以使用本文所述的方法、使用本文所述的分析、測量或定量方法來鑒定。
在其他情況下,可以通過檢測患者樣品中由目標基因編碼的一個或多個rna轉錄物或其片段的量或水平以評估至少一種pe生物標志物的水平,以獲得核酸標志物表征(markerrepresentation)。可以使用任何方便的操作方案檢測樣品中的核酸水平。雖然檢測核酸的多種不同方式是已知的,例如在差異基因表達分析領域中使用的那些,一種用于產生標志物表征的代表性和方便類型的操作方案是基于陣列的基因表達譜分析操作方案。這樣的應用是雜交測定,其中使用針對要在待產生的標志物表征中待測定/分析的每種基因顯示“探針”核酸的核酸。在這些測定中,首先從待測定的初始核酸樣品制備靶核酸樣品,其中制備可包括用標記(例如信號產生系統的成員)標記靶核酸。在靶核酸樣品制備之后,使樣品在雜交條件下與陣列接觸,由此在與附著于陣列表面的探針序列互補的靶核酸之間形成復合物。然后定性或定量檢測雜交復合物的存在。
可用于產生本發明方法中使用的標志物表征的特異性雜交技術包括美國專利號5,143,854;5,288,644;5,324,633;5,432,049;5,470,710;5,492,806;5,503,980;5,510,270;5,525,464;5,547,839;5,580,732;5,661,028;5,800,992;(其公開內容通過引用并入本文);以及wo95/21265;wo96/31622;wo97/10365;wo97/27317;ep373203;和ep785280中所述的技術。“探針”核酸陣列,其中包括用于其表達正被測定的每種表型決定性基因的探針可以與來自受試者樣品的靶核酸接觸。在雜交條件下,例如嚴格雜交條件下進行接觸,然后除去未結合的核酸。本文使用的術語“嚴格測定條件”是指相容于產生具有足夠互補性的核酸結合對(例如表面結合核酸和溶液相核酸)以在測定中提供所需水平的特異性的條件,同時與在不足的互補性的結合成員之間形成結合對以降低相容性以提供所需的特異性。嚴格測定條件是雜交和洗滌條件的總和或組合(總體)。
雜交核酸的所得模式提供了關于已經被探測的每個基因的表達的信息,其中表達信息是關于基因是否被表達的,并且通常是在什么水平,其中表達數據(例如,標志物表征(例如,以轉錄組的形式))可以是定性的和定量的。
或者,可以采用用于定量樣品中一個或多個核酸水平的基于非陣列的方法,包括基于擴增操作方案的方法,例如基于聚合酶鏈反應(pcr)的測定,包括定量pcr、逆轉錄pcr(rt-pcr)、實時pcr、環介導dna等溫擴增(lamp)、鏈置換擴增(sda)、基于序列的擴增(nasba)、自我維持序列復制(3sr)、線性擴增等。
或者,可以采用用于測定在樣品中假定蛋白質的功能的功能測定、方法和操作方案,包括本領域普通技術人員已知的任何標準功能測定,其將確認或否定在樣品中假定蛋白質的存在。在一些情況下,功能測定可包括酶測定、底物測定、切割測定、比色測定、ph測定等。也可以進行溶酶體測定。
當要檢測蛋白質或肽水平時,在進行操作方案之前,可以測定樣品中蛋白質的總量或蛋白質總量的一部分。這可以使用比色測定法實現,例如bca、lowry、bradford、考馬斯、660nm等。
本文的任何測定可涉及使用標準曲線和/或質量對照,例如高質量對照、低質量對照和至少一個空白。
pe生物標志物標準品可以是與通過本文所述的方法測量的生物標志物相似或相同的純化的重組蛋白質、純化的蛋白質、合成的蛋白質、工程改造的蛋白質等。在示例性情況下,生物標志物標準品是與通過本文所述的方法測量的生物標志物相似或相同的純化的重組蛋白質。空白可以是水、緩沖劑、多于一種緩沖劑、化學品、多于一種化學品、試劑、多于一種試劑、抗體、多于一種抗體或本文所述方法的任何組分。低質量對照可以是先前分析的樣品純化的重組蛋白質、純化的蛋白質、合成的蛋白質、工程改造的蛋白質等,其具有通過本文所述的方法分析的低水平的生物標志物。高質量對照可以是先前分析的樣品、純化的重組蛋白質、純化的蛋白質、合成的蛋白質、工程改造的蛋白質等,其具有通過本文所述的方法分析的高水平的生物標志物。曲線標準品可以是由用戶或elisa的制造商提供的濃縮、稀釋或純化的蛋白質,其可用于分析總蛋白或總生物標志物水平的水平,以便計算本文中所述方法、通常是elisa方法的標準曲線。
單板的孔可以含有但不限于至少一個樣品、至少一個生物標志物標準品、至少一種曲線標準品、高質量對照、低質量對照和至少一個空白。在一些情況下,單板的孔可以含有但不限于多于一個樣品、多于一個生物標志物標準品、多于一個曲線標準品、高質量對照、低質量對照和多于一個空白。例如,單板的孔可以含有至少1、2、3、4、5、5、6、7、8、9或10個樣品;至少1、2、3、4、5、5、6、7、8、9或10種生物標志物標準品;至少1、2、3、4、5、5、6、7、8、9或10個曲線標準品;至少1、2、3、4、5、5、6、7、8、9或10個高質量對照;至少1、2、3、4、5、5、6、7、8、9或10個低質量對照;和/或至少1、2、3、4、5、5、6、7、8、9或10個空白。樣品可以是單個、一式兩份、一式三份、一式四份,或任何進一步重復的延伸。
在一個實施例中,單個elisa測定板含有一式三份的八個標準曲線樣品、六個高質量對照樣品、六個低質量對照樣品和一式三份在板上排列以避免變化的三個樣品。通常,可以使用對照代替高質量對照和/或低質量對照。在一些情況下,對照可用作內部校準。在其他情況下,可以使用對照代替生物標志物標準品。在其他情況下,可以使用對照代替標準品。例如,對照可用于產生本文所述的標準曲線。
單克隆抗體
本公開進一步提供了用于確認受試者中先兆子癇的存在、不存在或嚴重性的方法,其包括:利用選擇性結合纖連蛋白的單克隆抗體以確定來源于受試者的樣品中纖連蛋白的水平,產生報告,其基于水平指示先兆子癇的存在、不存在或嚴重性并包含指數;和評估樣品并基于指數建議用于先兆子癇的治療,所選擇的治療涉及阿司匹林、早產或臥床休息。
在一些情況下,確認、診斷、預后、監測、表征或評估受試者中先兆子癇的嚴重性的方法包括:從受試者獲得生物樣品;將生物素化的血色素結合蛋白稀釋兩倍,將生物素化的血色素結合蛋白與受試者的生物樣品混合,將該混合物加入免疫測定板中;在免疫測定測試中進行生物樣品對血紅素結合蛋白(hpx)的存在和量的分析,以及使用生物標志物水平以提供先兆子癇診斷、預后、確認、監測、表征或評估其嚴重性。在這種情況下,測定方法學例證競爭性elisa測定。生物素化的血色素結合蛋白與樣品-血色素結合蛋白競爭抗體結合位點。隨后在引入適當的綴合物形成配偶體例如抗生物素蛋白、鏈霉抗生物素蛋白、
elisa試劑盒可用于進行elisa測定。這些可以從標準商業制造商購買,例如來自mybiosource(sd,us)的含有解整聯蛋白和金屬蛋白酶結構域的蛋白12(adam12);來自abcaminc.(ma,us)的血色素結合蛋白(hpx);來自r&dsystemsinc.(mn,us)的胎盤生長因子(p1gf);和來自r&dsystemsinc.(mn,us)的可溶性fms樣酪氨酸激酶(sflt)-1。
本領域普通技術人員已知的任何市售試劑盒可以用于通過elisa方法檢測本文列出的生物標志物,并且可以與本發明方法組合使用。例如,市售試劑盒可以包括但不限于抗p1gf(由uscnlifescienceinc.,roche和r&dsystems分銷)、抗sflt-1(由bosterbio.、r&dsystems、mybiosource.com、antibodies-online、biotrendchemikaliengmbh,和enzolifesciences分銷)、抗papp-a(由r&dsystems、raybiotech、ibljapan、drginternational、abnova、uscnlifescience、novusbio、rapidtest、mybiosource、antibodies-online.com、fisherscientific、elabscience、sigmaaldrich、cusabio、anshlabs、demeditec、alpco、amsbio、novateinbio、creativebiomart、biorbyt、biomaticcorporation分銷)、抗vegf(由amsbio、mybiosource、abnova、antibodies-online.com、unitedstatesbiological、biomatikcorporation、cloud-clonecorp、biovendor、bosterimmunoleader、enzolifesciences、fitzgerald、abnova、avivasystemsbiology和creativebiomart分銷)、抗纖連蛋白(由biovendor、bosterimmunoleader、qedbioscience、ebioscience、biorbyt、fitzgerald、amsbio、mybiosource、novateinbio、abnova、avivasystemsbiology、creativebiomart、antibodies-online.com、abcam、novusbiologicals、unitedstatesbiological、eiaab(hongkong)companylimited、biomatikcorporation、cloud-clonecorp分銷)、抗血纖蛋白原(molecularinnovations、fitzgerald、amsbio、biorbyt、mybiosource、novateinbio、abnova、creativebiomart、avivasystemsbiology、antibodies-online.com、abcam、novusbiologicals、unitedstatesbiological、eiaab(hongkong)companylimited、biomatikcorporation、cloud-clonecorp分銷)和抗adam12(由bosterimmunoleader、amsbio、mybiosource、abnova、creativebiomart、antibodies-online.com、genetex、biorbyt、unitedstatesbiological、eiaab(hongkong)companylimited、r&dsystems和cloud-clonecorp分銷)。
可以使用本文所述的方法(例如使用elisa方法、操作方案、測定等)對標準曲線樣品來分析生物標志物的濃度。在對樣品或一組標準曲線樣品進行方法、操作方案和/或測定之前,每種市售或內部設計的elisa方法、操作方案和/或測定可提供包含標準曲線樣品的推薦稀釋度的說明書。在一些情況下,可以遵循市售的或內部設計的elisa方法、操作方案和/或測定的說明書,并且根據說明書稀釋標準曲線樣品。在一些情況下,標準曲線樣品可以稀釋至1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9、1:10、1:20、1:30、1:40、1:50、1:60、1:70、1:80、1:90、1:100、1:150、1:200、1:250、1:300、1:350、1:400、1:450、1:500、1:550、1:600、1:650、1:700、1:750、1:800、1:850、1:900、1:950、1:1000、1:1500、1:2000、1:2500、1:3000、1:3500、1:4000、1:10000、1:15000、1:20000、1:25000、1:30000、1:35000、1:40000、1:45000、1:50000、1:55000、1:60000、1:65000、1:70000、1:75000、1:80000、1:85000、1:90000、1:95000或1:100000、1:4500、1:5000、1:5500、1:6000、1:6500、1:7000、1:7500、1:8000、1:8500、1:9000、1:9500或1:100000的比率。在一些情況下,標準曲線樣品可以稀釋至約1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9、1:10、1:20、1:30、1:40、1:50、1:60、1:70、1:80、1:90、1:100、1:150、1:200、1:250、1:300、1:350、1:400、1:450、1:500、1:550、1:600、1:650、1:700、1:750、1:800、1:850、1:900、1:950、1:1000、1:1500、1:2000、1:2500、1:3000、1:3500、1:4000、1:10000、1:15000、1:20000、1:25000、1:30000、1:35000、1:40000、1:45000、1:50000、1:55000、1:60000、1:65000、1:70000、1:75000、1:80000、1:85000、1:90000、1:95000或1:100000、1:4500、1:5000、1:5500、1:6000、1:6500、1:7000、1:7500、1:8000、1:8500、1:9000、1:9500或約1:100000的比率。在一些情況下,可以將標準曲線樣品稀釋至小于1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9、1:10、1:20、1:30、1:40、1:50、1:60、1:70、1:80、1:90、1:100、1:150、1:200、1:250、1:300、1:350、1:400、1:450、1:500、1:550、1:600、1:650、1:700、1:750、1:800、1:850、1:900、1:950、1:1000、1:1500、1:2000、1:2500、1:3000、1:3500、1:4000、1:10000、1:15000、1:20000、1:25000、1:30000、1:35000、1:40000、1:45000、1:50000、1:55000、1:60000、1:65000、1:70000、1:75000、1:80000、1:85000、1:90000、1:95000或1:100000、1:4500、1:5000、1:5500、1:6000、1:6500、1:7000、1:7500、1:8000、1:8500、1:9000、1:9500或小于1:100000的比率。在一些情況下,標準曲線樣品可以稀釋至大于1:1、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9、1:10、1:20、1:30、1:40、1:50、1:60、1:70、1:80、1:90、1:100、1:150、1:200、1:250、1:300、1:350、1:400、1:450、1:500、1:550、1:600、1:650、1:700、1:750、1:800、1:850、1:900、1:950、1:1000、1:1500、1:2000、1:2500、1:3000、1:3500、1:4000、1:10000、1:15000、1:20000、1:25000、1:30000、1:35000、1:40000、1:45000、1:50000、1:55000、1:60000、1:65000、1:70000、1:75000、1:80000、1:85000、1:90000、1:95000或1:100000、1:4500、1:5000、1:5500、1:6000、1:6500、1:7000、1:7500、1:8000、1:8500、1:9000、1:9500或大于1:100000的比率。對于上文所列的比率,1是樣品的部分,而另一個值表示稀釋劑,其中稀釋劑可以由商業制造商提供,或稀釋劑可以由用戶提供。
數據加工和數據用途
所得數據提供了關于樣品中已經探測的每個標志物的水平的信息,其中信息是關于標志物是否存在以及通常在什么水平,并且其中數據可以是定性和定量的。因此,當檢測是定性的時,方法提供對靶標志物(例如核酸或蛋白質)是否存在于所測定的樣品中的讀數或評估,例如評價。在一些情況下,方法提供定量檢測靶標志物是否存在于所測定的樣品中,例如評估或評價所測定的樣品中的靶分析物(例如核酸或蛋白質)的實際量或相對豐度進行測定。在這種情況下,定量檢測可以是絕對的,或者如果該方法是在樣品中檢測多個不同分析物例如靶核酸或蛋白質的方法,則是相對的。
一旦已經測定了一個或多個先兆子癇標志物的水平,可以以多種方式中的任一種分析測量結果以獲得先兆子癇標志物水平表征。“生物標志物水平表征”或“基因表征”是指(一個或多個先兆子癇標志物和/或目的蛋白質輔因子)水平(例如rna、dna或蛋白質水平)的表征。
例如,可以分析先兆子癇標志物測量值以產生先兆子癇評分或指數,其可以使用邏輯回歸分析來計算。在一些情況下,可以計算至少兩個生物標志物的比率,并與用于模型中的另外的解釋變量組合。生物標志物的比率通常可以是sflt-1和p1gf的比率。在一些情況下,所生成的模型可以是懲罰模型。在其他情況下,所生成的模型可以是非懲罰的模型。樣本可能導致不準確的模型,因此,可以評估樣本外性能以確定樣本是否導致不準確的模型。在一些情況下,可以使用任何數量的方法來評估樣本外性能,包括但不限于交叉驗證方法。在一些情況下,模型的準確性取決于多個參數,包括但不限于訓練樣本對于目標群體的代表性、包括在模型中的變量的數量、生物標志物測量不確定性等。通常評估模型的樣本性能以估計未用于訓練的樣本集中的模型的誤差。
作為實例,可將先兆子癇標志物測量作為生物標志物小組進行分析。可以通過統計特征選擇過程來選擇生物標志物小組的預測成員。例如,可以通過組合遺傳算法(ga)和用于先兆子癇分類分析的所有配對(ap)支持向量機(svm)方法來選擇分析物小組。預測特征被自動確定,例如。通過迭代ga/svm,得到具有最佳分類性能的非冗余先兆子癇相關分析物的非常緊湊的集合。這些不同的分類器集合可能僅具有適度的重疊基因、蛋白質片段或蛋白質特征,但具有類似水平的準確性。
作為實例,可以分析先兆子癇標志物測量值以產生先兆子癇特征。患者樣品的先兆子癇特征可以通過本領域已知的用于計算生物標志物特征的多種方法中的任何一種來計算。例如,患者樣品中的一個或多個先兆子癇標志物中的每一種的水平可以進行log2、loge或log10變換,并且例如如上文關于產生先兆子癇標志物譜進行標準化。然后通過將標準化水平乘以權重因子或權重來加權每個標志物的標準化表達水平,以獲得一個或多個標志物中的每一個的加權表達水平。然后將加權水平總計并且在一些情況下平均以得到所分析的一個或多個先兆子癇標志物的單個加權水平。
在一些情況下,pe測試可以確認懷疑患有pe的受試者是否實際上確實患有pe。所分析的一個或多個先兆子癇標志物的單個加權水平可以確認pe的嚴重性。例如,單個加權水平可以產生高、中或低加權評分,其可以確認受試者中pe的高、中或低嚴重性。在一些情況下,高的單個加權水平確認受試者中pe的高度嚴重性。在一些情況下,中等單個加權水平確認了pe的高度嚴重性。在一些情況下,低的單個加權水平證實pe的高度嚴重性。在一些情況下,高的單個加權水平確認pe的中等嚴重性。在一些情況下,中等單個加權水平確認pe的中等嚴重性。在一些情況下,低的單個加權水平確認pe的中等嚴重性。在一些情況下,高的單個加權水平確認pe的低嚴重性。在一些情況下,中等單個加權水平確認pe的低嚴重性。在一些情況下,低的單個加權水平確認受試者中pe的低嚴重性。
所分析的一個或多個先兆子癇標志物的單個加權水平可以指示疑似患有pe的受試者患有或沒有患有pe的可能性。例如,單個加權水平可以產生高、中和低加權評分,其可以指示受試者患有或沒有患有pe的可能性。在一些情況下,高的單個加權水平指示受試者患有或沒有患有pe的可能性高。在一些情況下,中等單個加權水平指示受試者患有或沒有患有pe的可能性高。在一些情況下,低的單個加權水平指示受試者患有或沒有患有pe的可能性高。在一些情況下,高的單個加權水平指示受試者患有或沒有患有pe的中等可能性。在一些情況下,中等單個加權水平指示受試者患有或沒有患有pe的中等可能性。在一些情況下,低的單個加權水平指示受試者患有或沒有患有pe的中等可能性。在一些情況下,高的單個加權水平指示受試者患有或沒有患有pe的可能性低。在一些情況下,中等單個加權水平指示受試者患有或沒有患有pe的可能性低。在一些情況下,低的單個加權水平指示受試者患有或沒有患有pe的可能性低。
所分析的一個或多個先兆子癇標志物的單個加權水平可以指示受試者發展先兆子癇的可能性。例如,單個加權水平可以產生高、中和低加權評分,其可以指示受試者在具有任何癥狀之前發展先兆子癇的可能性。在一些情況下,高的單個加權水平表示受試者發展先兆子癇的可能性高。在一些情況下,中等單個加權水平指示受試者發展先兆子癇的可能性高。在一些情況下,低的單個加權水平表示受試者發展先兆子癇的可能性高。在一些情況下,高的單個加權水平表示受試者發展先兆子癇的中等可能性。在一些情況下,中等單個加權水平表示受試者發展先兆子癇的中等可能性。在一些情況下,低的單個加權水平指示受試者發展先兆子癇的中等可能性。在一些情況下,高的單個加權水平表示受試者發展先兆子癇的可能性低。在一些情況下,中等單個加權水平表示受試者發展先兆子癇的可能性低。在一些情況下,低的單個加權水平表示受試者發展先兆子癇的可能性低。
權重因子或權重可以通過任何統計機器學習方法例如主成分分析(pca)、線性回歸、支持向量機(svm)和/或數據集的隨機森林來確定,其可以使用獲得的樣品。例如,每個先兆子癇標志物的分析物水平可以進行log2、loge或log10轉換并加權為1(對于在先兆子癇中水平增加的那些標志物)或-1(對于先兆子癇中水平降低的那些標志物),以及測定與減少的標志物相比增加的標志物之和之間的比率以實現先兆子癇特征。先兆子癇特征是先兆子癇標志物水平表征的一個例子。
在某些情況下,多個標志物的相對權重用于確定生物標志物特征、生物標志物評分或生物標志物指數。可以比較其權重的標志物包括本文所述的任何標志物或選自包含hpx、sflt-1、papp-a、fn、fg、vegf(不包括vegf-r1)、p1gf和adam12的組的那些標志物。例如,在一些情況下,pe特征、pe評分或pe指數涉及比較sflt-1和p1gf結合至少一個其他生物標志物的水平,并確定它們的相對權重是否為至少1.5:1、2:1、2.5:1、3:1或3.5:1,其中這樣的測定指示pe的pe或pe的可能性。
pe評分或pe指數可以進一步分類為確認受試者中pe的嚴重性的值。例如,pe評分或pe指數可以產生高、中或低值,其可以確認受試者中pe的嚴重性。在一些情況下,高pe評分或pe指數可以確認受試者中pe的嚴重性高。在一些情況下,中度pe評分或pe指數確認pe的嚴重性高。在一些情況下,低pe評分或pe指數確認pe的嚴重性高。在一些情況下,高pe評分或pe指數確認pe的嚴重性中等。在一些情況下,中度pe評分或pe指數確認pe的嚴重性中等。在一些情況下,低pe評分或pe指數確認pe的嚴重性中等。在一些情況下,高pe評分或pe指數確認pe的嚴重性低。在一些情況下,中度pe評分或pe指數確認pe的嚴重性低。在一些情況下,低pe評分或pe指數確認受試者中pe的嚴重性低。
pe評分或pe指數可進一步分類為指示懷疑患有pe的受試者患有或沒有患有pe的可能性的值。例如,pe評分或pe指數可以產生高、中和低值,其可以指示受試者患有或沒有患有pe的可能性。在一些情況下,高pe分數或pe指數指示受試者患有或沒有患有pe的可能性高。在一些情況下,中等pe評分或pe指數指示受試者患有或沒有患有pe的可能性高。在一些情況下,低pe分數或pe指數指示受試者患有或沒有患有pe的可能性高。在一些情況下,高pe分數或pe指數指示受試者患有或沒有患有pe的可能性中等。在一些情況下,中等pe評分或pe指數指示受試者患有或沒有患有pe的可能性中等。在一些情況下,低pe分數或pe指數指示受試者患有或沒有患有pe的可能性中等。在一些情況下,高pe分數或pe指數指示受試者患有或沒有患有pe的可能性低。在一些情況下,中等pe評分或pe指數指示受試者患有或沒有患有pe的可能性低。在一些情況下,低pe分數或pe指數指示受試者患有或沒有患有pe的可能性低。
pe評分或pe指數可以進一步分類為可以預測受試者在癥狀發作之前發展先兆子癇的可能性的值(例如可能性高、中等或低)。在一些情況下,高pe分數或pe指數表示受試者發展先兆子癇的可能性高。在一些情況下,中等pe評分或pe指數表示受試者發展先兆子癇的可能性高。在一些情況下,低pe分數或pe指數指示受試者發展先兆子癇的可能性高。在一些情況下,高pe分數或pe指數指示受試者發展先兆子癇的可能性中等。在一些情況下,中等pe評分或pe指數表示受試者發展先兆子癇的可能性中等。在一些情況下,低pe分數或pe指數表示受試者發展先兆子癇的可能性中等。在一些情況下,高pe分數或pe指數表示受試者發展先兆子癇的可能性低。在一些情況下,中度pe評分或pe指數表示受試者發展先兆子癇的可能性低。在一些情況下,低pe分數或pe指數表示受試者發展先兆子癇的可能性低。
在一些情況下,可以使用任何數量的方法、算法和計算來加工和/或進一步分析數據,以便對單個數據點、數據集進行優先級排序并防止假陽性或假相關的結果的過擬合。如本文所描述和示出的,一些數據可能沒有被校正,例如訓練數據,其可能有時是數據的樂觀估計。另外,一些數據可以被校正,例如,校正的數據,其可以有時是數據的保守估計。在一些情況下,校正的數據是值的交叉驗證的估計,例如該值可以是曲線下面積(auc)。有時,對訓練數據評估模型的性能,提供樂觀估計。偶爾,針對不同性能度量計算對性能的樂觀估計的校正。在一些情況下,使用交叉驗證來計算校正的性能估計。在一些實例中,性能度量是曲線下面積(auc)或roc值。
數據可以用于制備模型。在一些情況下,模型被懲罰或優化。從使用懲罰數據得到的模型單獨處理生物標志物,并防止每個單個生物標志物獲得的數據或每個生物標志物的復制數據測量值控制先兆子癇指數、先兆子癇評分或先兆子癇譜。在一些情況下,在懲罰模型中使用的數據通過向一個方向或另一個方向不適當地加權先兆子癇指數、先兆子癇評分或先兆子癇譜來控制先兆子癇指數、先兆子癇評分或先兆子癇譜。在一些情況下,在懲罰模型中使用數據,使得先兆子癇指數、先兆子癇評分或先兆子癇譜沒有被不適當地加權并且防止先兆子癇指數、先兆子癇評分或先兆子癇譜從不相關因子例如受損樣品,不反映受試者的樣品等確定。在一些情況下,從數據獲得優化模型,使得校正可防止獲得的個別標志物的數據值對方程的錯誤貢獻。在一些情況下,與訓練數相比,從數據獲得的經校正和/或優化的模型可更好地預測先兆子癇指數、先兆子癇評分或先兆子癇譜。在示例性情況下,使用懲罰邏輯回歸方法來構建模型,其中懲罰方法擬合回歸模型,同時對本文所述的模型的系數的絕對值之和添加約束。約束可以防止可能與該樣品集中的結果高度相關聯的變量錯誤地影響模型。
在一些情況下,確定先兆子癇指數、先兆子癇評分或先兆子癇譜的數據計算包括sflt-1和p1gf的比率。該比率可以與或可以不與測定結果一起標準化。如本文所述,先兆子癇指數、先兆子癇評分或先兆子癇譜是可以使用本文所述的分析方法確定的生物標志物的組合。
數據可以擬合三個分開的類別,層(tier)i、層ii和層iii。層i對應于至少0.98或更大的roc值。層ii對應于0.92至0.98的roc值,而層iii對應于0.92或更小的roc值。在一些情況下,大于0.850的roc值可能在臨床上是有價值的。在一些情況下,大于0.90或0.950的roc值可能在臨床上是有價值的。在一些情況下,在層i和層ii之間沒有統計學顯著差異。在一些實例中,在層i和層ii之間存在統計學顯著差異。在一些情況下,層值可以是roc值,其可以指示方法和/或具體生物標志物或生物標志物組的數據點的靈敏度和/或特異性。在一些情況下,可以使用至少一種算法、至少一個閾值、至少隨時間的方向變化、單個受試者內的比較、受試者組內的比較或與參考標準的比較來分類數據輸出。通常,至少一個算法可以是本文所描述的算法或本領域普通技術人員已知的至少一個算法。通常,至少一個閾值可以在本文中描述或者為本領域普通技術人員所知。在一些情況下,可以基于單個參數或一組參數來設置閾值;單個參數或一組參數可以由用戶定義。通常,方向改變可以在本文中描述或者本領域普通技術人員已知。在一些情況下,方向改變可以基于單個參數或一組參數;單個參數或一組參數可以由用戶定義。通常,單個受試者內的比較可以在本文中描述或本領域普通技術人員已知。在一些情況下,單個受試者其可以與被測試的受試者相同或不同)內的比較可以基于單個參數或一組參數;單個參數或一組參數可以由用戶定義。通常,受試者組內的比較可以在本文中描述或本領域普通技術人員已知。在一些情況下,受試者組內的比較可以基于單個參數或一組參數;單個參數或一組參數可以由用戶定義。通常,與參考標準的比較可以在本文中描述或本領域普通技術人員已知。在一些情況下,與參考標準的比較可以基于單個參數或一組參數;單個參數或一組參數可以由用戶定義。參考標準可以基于實際的測試受試者、或其他實驗值、或從模型導出的理論值、或其任何組合。
在一些情況下,本公開提供了用于確認受試者中存在或不存在先兆子癇的方法,包括:評估來源于受試者的樣品中的多個生物標志物以確認受試者是否患有先兆子癇,其中該確認具有至少90、91、92、93、94、95、96、97、98、99%或更高的特異性,其用于計算指數。在一些情況下,該確認具有至少0.9、0.91、0.92、0.93、0.95、0.96、0.97、0.980、0.985、0.988、0.990、0.995、0.999或更大的auc,其用于計算指數。例如,評估來自超過一個受試者的樣品,以本文所述的特異性,確認存在或不存在pe,例如評估來自超過5、10、50、100、130、135、138、150、200、220、247、250、300、350、400、450、500或多于1000個受試者,以本文所述的特異性確認存在或不存在pe。在一些情況下,使用傳統方法將受試者評估為患有pe。在一些示例中,受試者實際上經歷pe。傳統方法包括測量蛋白尿、血壓、體重增加、血糖、血小板計數和本領域已知的傳統上用于評估pe的任何其他方法。
本公開還提供了用于區分患有先兆子癇的受試者與具有提示先兆子癇的癥狀但沒有患有先兆子癇的受試者的方法,該方法將先兆子癇與妊娠癥狀的并發癥、慢性高血壓、妊娠高血壓、自身免疫性疾病和/或妊娠糖尿病區分開,其中該方法具有至少95%的特異性或具有至少0.9的auc,該方法包括:評估來源于受試者的樣品的多個不同生物標志物的水平,產生指示存在先兆子癇、不存在先兆子癇、先兆子癇的嚴重性的指數。在一些情況下,該方法進一步包括基于指數建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。在一些情況下,自身免疫性疾病是sle或狼瘡。在一些情況下,該方法還包括對多個生物標志物中的每一個進行加權,其中加權包括將數字提供到多項式中,使得每個標志物具有不同的權重。
本公開提供了用于確認受試者中存在或不存在先兆子癇的方法,包括:評估來源于受試者的樣品中的多個生物標志物以確認受試者是否患有先兆子癇,其中該確認具有大于95%的特異性,或具有大于0.9的auc并用于計算指數。
本公開進一步提供了用于診斷或確認受試者中先兆子癇的存在的方法,包括:(a)進行至少兩個不同的測定,其測定來源于受試者的樣品中纖連蛋白的水平;和(b)評估樣品并使用來自兩種不同測定的水平來診斷或確認先兆子癇的存在并計算指數。
在一些情況下,本公開提供了用于診斷或確認受試者中存在先兆子癇的方法,包括:(a)進行至少一個測定,其利用結合纖連蛋白的抗體或選擇性結合纖連蛋白相同抗原的抗體作為抗體,其中抗體的結合決定來源于受試者的樣品中纖連蛋白的水平;和(b)評估樣品并使用來自至少一個測定的纖連蛋白的水平來診斷或確認先兆子癇的存在并計算指數。
本公開還描述了用于診斷或確認受試者存在先兆子癇或不存在先兆子癇的方法,包括:(a)評估sflt-1和plgf的比率的水平和多個不同生物標志物的水平,其中不同生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素;和(b)評估樣品并使用來自步驟(a)的水平來確定診斷或確認存在先兆子癇的指數并計算指數。
本公開還提供了用于區分患有先兆子癇的受試者與具有提示先兆子癇的癥狀但沒有患有先兆子癇的受試者的方法,該方法將先兆子癇與妊娠癥狀、慢性高血壓、妊娠高血壓、自身免疫疾病和/或妊娠糖尿病區分開,其中該方法具有至少90%的特異性或至少0.9的auc,該方法包括:評估來源于受試者的樣品的多個不同生物標志物的水平,產生指示pe存在、缺乏pe、pe特征、pe的嚴重性、pe的診斷或pe的預后的指數。
在一些情況下,本公開進一步描述了用于分析受試者的先兆子癇的診斷、預后、特征、存在、不存在或嚴重性的方法,其包括:(a)利用選擇性結合纖連蛋白的單克隆抗體,以確定來源于受試者的樣品中纖連蛋白的水平,(b)基于水平產生報告,其指示先兆子癇的存在、不存在或嚴重性并且包含指數;和(c)評估樣品并基于指數建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。
本公開還描述了用于分析來源于受試者的樣品中的先兆子癇的診斷、預后、特征、存在、不存在或嚴重性的方法,包括:利用至少一種纖連蛋白elisa試劑盒中針對纖連蛋白抗體的抗原的抗體以分析和評估來自受試者的樣品。
本公開還提供了用于診斷或確認受試者中存在先兆子癇的方法,其包括:(a)進行至少一個測定,其利用選擇性結合纖連蛋白、纖連蛋白的一部分、纖連蛋白的一部分或纖連蛋白的片段的抗體,其中抗體的結合決定來源于受試者的樣品中纖連蛋白的水平;和(b)評估樣品并使用來自一個測定的纖連蛋白的水平來診斷或確認先兆子癇的存在并計算指數。
在一些情況下,本公開描述了用于確認受試者沒有患有先兆子癇的方法,包括:評估來源于受試者的樣品中的多個生物標志物,以確認受試者沒有患有先兆子癇,其中該確認具有大于95%的特異性或具有0.9的auc,并用于計算指數。
在一些情況下,pe特征、pe評分或pe指數涉及比較fn、fg和選自以下的另一個生物標志物的水平:hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、p1gf和adam12;并確定它們的相對權重是否分別為至少3:1、5:1、10:1、20:1、30:1、50:1、50:1、100:1,其中這樣的確定表明pe或pe的可能性。
其他目的組合包括比較sflt-1和選自以下的另一個生物標志物:hpx、fn、fg、papp-a、vegf(不包括vegf-r1)、p1gf和adam12,并確定它們的相對權重是否分別為至少2:1、2.5:1、3:1、5:1、10:1、20:1、30:1、50:1、50:1、100:1,其中這樣的確定指示pe或pe的可能性。
其他目的組合包括比較p1gf和選自以下的另一個生物標志物:hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12,并確定它們的相對權重是否分別為至少2:1、2.5:1、3:1、5:1、10:1、20:1、30:1、50:1、50:1、100:1,其中這樣的確定指示pe或pe的可能性。
其他目的組合包括比較vegf(不包括vegf-r1)和選自以下的另一個生物標志物:hpx、sflt-1、papp-a、p1gf、fn、fg和adam12;并確定它們的相對權重是否分別為至少2:1、2.5:1、3:1、5:1、10:1、20:1、30:1、50:1、50:1、100:1,其中這樣的確定指示pe或pe的可能性。
作為實例,可以分析先兆子癇標志物測量值以產生先兆子癇評分。像先兆子癇特征一樣,先兆子癇評分是表示患者樣品中一個或多個先兆子癇標志物的加權水平之和的單個度量值。先兆子癇評分可以通過與上述用于先兆子癇特征的方法非常相似的方法來確定,例如患者樣品中的一個或多個先兆子癇標志物中的每一種的水平可以例如如上關于產生先兆子癇譜的描述進行log2、loge或log10變換和標準化;然后通過將標準化水平乘以權重因子或權重來對每個標志物的標準化表達水平進行加權,以獲得一個或多個標志物中的每一個的加權水平;然后對加權的水平進行求和,并且在一些情況下平均以得到所分析的一個或多個先兆子癇標志物的單個加權水平。偶爾,一個或多個先兆子癇標志物的加權水平可以隨后例如使用對數樣的反函數如雙對數ln(ln(x))、超-4-對數(super-4-logarithm)(即四對數)、超對數-4-對數(hyper-4-logarithm)(即迭代冪次)、迭代對數、朗伯w函數或分對數。
與先兆子癇特征相反,加權水平由參考數據集或訓練數據集定義。因此,先兆子癇評分由參考數據集定義。
先兆子癇指數是先兆子癇標記水平表征的實例。pe指數是指示pe的嚴重性或發展pe的可能性的程度的度量系統。它用于確定女性受試者在哪個類別中。使用分類算法從pe評分計算pe指數。分類算法的實例是本領域中眾所周知的。這些算法可以使用任何合適的統計分類(或“學習”)方法形成,該方法試圖基于數據中存在的客觀參數將數據主體分離成類。分類方法可以是受監督的或不受監督的。受監督和不受監督的分類過程的示例在jain,"statisticalpatternrecognition:areview,"ieeetransactionsonpatternanalysisandmachineintelligence,vol.22,no.1,january2000中。在受監督的分類中,將包含已知類別的實例的訓練數據提交給學習機制,學習機制學習定義每個已知類的一個或多個關系集合。然后可以將新數據應用于學習機制,其然后使用學習的關系對新數據進行分類。受監督的分類過程的實例包括線性回歸過程(例如,多元線性回歸(mlr)、偏最小二乘法(pls)回歸和主成分回歸法(pcr))、二元決策樹(例如,遞歸分配過程例如cart分類和回歸樹)、諸如反向傳播網絡的人工神經網絡、判別分析(例如,貝葉斯分類器或fischer分析)、邏輯分類器和支持向量分類器(支持向量機)。附加分類方法是遞歸分配過程。遞歸分配過程使用遞歸分配樹來對從未知樣本導出的譜進行分類。關于遞歸分配過程的進一步細節在paulse等人的美國專利申請號2002/0138208a1,“methodforanalyzingmassspectra”中提供。
在一些實施方案中,用于提供本文所述的先兆子癇指數的pe的分類不基于包括以下的組中的至少一個因素:血壓、體重增加、水潴留、遺傳因子、蛋白尿、頭痛、水腫、蛋白質/肌酐比、血小板計數、應激、先前妊娠的pe、未經產、年齡,年齡小于20歲、年齡大于35歲、種族,非洲裔美國人和菲律賓人、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作、家族史、妊娠數、流產數、體重指數(bmi)、妊娠糖尿病、i型糖尿病、肥胖、葡萄糖水平、當前和過去的藥物、應激、(受試者或其家庭成員的)妊娠前的pe、慢性高血壓、腎病或血栓形成傾向。在一些實施方案中,用于提供本文所述的先兆子癇指數的pe的分類不基于本段中剛剛描述的任何特征。
在一些實例中,用于提供本文所述的先兆子癇指數的pe的分類基于包括以下的組中的至少一個因素:血壓、體重增加、水潴留、遺傳因子、蛋白尿、頭痛、水腫、蛋白質/肌酐比、血小板計數、應激、先前妊娠的pe、未經產、年齡,年齡小于20歲、年齡大于35歲、種族,非洲裔美國人和菲律賓人、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作、家族史、妊娠數、流產數、體重指數(bmi)、妊娠糖尿病、i型糖尿病、肥胖、葡萄糖水平、當前和過去的藥物、應激、(受試者或其家庭成員的)妊娠前的pe、慢性高血壓、腎病或血栓形成傾向。
數據分析和表型的測定
在某些情況下,僅評估一個標志物的表達(例如多肽水平)以產生標志物水平表征。在一些情況下,評估多個標志物(例如,至少1、2、3、4、5、6、7、10、11、12、13、14、15個或更多個標志物)的表達。因此,在本發明的方法中,評估樣品中至少一個標志物的表達。在某些情況下,所進行的評估可以被視為蛋白質組的評估,如該術語在本領域中使用的那樣。
以這種方式達到的標志物水平表征在診斷、預后、表征、評估先兆子癇的嚴重性或確認存在或不存在先兆子癇方面找到許多用途。例如,標志物水平表征可用于預測受試者是否發展先兆子癇,診斷受試者的先兆子癇,表征診斷的先兆子癇或監測受試者對先兆子癇治療的響應性。在一些情況下,本文公開的先兆子癇標志物的特定組合的測量提供了先兆子癇預后,其相對于使用本領域已知的標準方法(例如vegf-r1(例如sflt-1)和p1gf)進行的先兆子癇預后具有改進的準確度。
在一種情況下,標志物水平表征可以基于相對權重的生物標志物用于診斷、預后、監測、表征或評估先兆子癇的嚴重性或用于確認受試者中存在或不存在先兆子癇的方法。這樣的方法包括:從受試者獲得生物樣品;對受試者的生物樣品分析p1gf、hpx、sflt-1(即vegf-r1)、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的存在和量,使用生物標志物水平提供先兆子癇診斷或預后;其中fn與生物標志物的相對權重為至少1.5、2、2.5、3、3.5、4、4.5或至少5,并且使用生物標志物水平提供先兆子癇診斷或預后;其中加權包括:生成生物標志物譜,并確定生物標志物的單個加權水平;其中譜包括表達log2、loge或log10變換和標準化;其中權重水平包括將譜與權重因子相乘,并且其中權重因子通過包括統計機器學習方法的方法來計算,所述方法可以包括例如以下任一項:主成分分析(pca)、線性回歸、支持向量機(svm)和隨機森林分析。
在一些情況下,標志物水平表征可用于基于生物標志物的相對權重診斷、預后、監測、表征、評估先兆子癇的嚴重性或確認受試者中存在或不存在先兆子癇的方法。這樣的方法包括:從受試者獲得生物樣品;對其生物樣品分析p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)和adam12的存在和量;使用生物標志物水平提供先兆子癇診斷或預后;其中fn、fg相對于生物標志物的數量的相對水平為至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、20、25、30、35、40、45、50個或更多。
本公開提供了用于確認受試者是否沒有患有先兆子癇的方法,包括:評估來源于受試者的樣品以確定樣品中多個生物標志物的水平,使用多個生物標志物的水平計算代表的受試者沒有患有先兆子癇的可能性的指數;并且基于指數,確認受試者是否沒有患有先兆子癇。在一些情況下,評估不包括比較在第一時間點來源于受試者的樣品和在第二時間點來自相同受試者的樣品。在一些情況下,評估確實包括比較在第一時間點來源于受試者的樣品和在第二時間點來自相同受試者的樣品。在一些情況下,該方法進一步包括基于該指數,建議用于先兆子癇的治療,該治療涉及阿司匹林、早產或臥床休息。有時,多個生物標志物選自:sflt-1、p1gf、fn和papp-a;sflt-1、p1gf、fn、adam12和papp-a;sflt-1、p1gf、papp-a和fn;sflt-1、p1gf、hpx、fn和papp-a;p1gf、adam12、fn和papp-a;p1gf、fn和papp-a;sflt-1、p1gf和fn;p1gf、fn和papp-a;sflt-1、p1gf、fn和adam12;sflt-1、p1gf和fn;p1gf、sflt-1和fn;sflt-1、fn和adam12;或p1gf、fn和papp-a。在一些情況下,計算還包括確定sflt-1和p1gf的水平的比率。在一些情況下,水平是經調整的、經標準化的或原始水平,或其任何組合。
在一些情況下,使用標志物水平表征是通過將其與表型測定元件例如先兆子癇表型測定元件比較,以鑒定與表型測定元件的相似性或差異,其中然后所鑒定的相似性或差異用于預測受試者是否發展先兆子癇、診斷受試者的先兆子癇、表征診斷的先兆子癇、監測受試者對先兆子癇的治療的反應性、評估先兆子癇的嚴重性等。例如,先兆子癇表型測定元件可以是來自患有或沒有患有先兆子癇的個體的樣品。這樣的樣品可以用作例如對于給定受試者的標志物表征的實驗測定中的參考或對照。作為示例,先兆子癇表型測定元件可以是代表先兆子癇狀態的標志物水平表征(例如,標志物譜、特征、評分或指數),并且可以用作參考或對照來解釋給定受試者的標志物水平表征。表型測定元件可以是陽性參考或對照。陽性參考或對照可以是來自受試者的樣品或標志物水平表征,所述受試者患有先兆子癇,或將發展先兆子癇,或患有可通過已知治療控制的先兆子癇,或患有已被確定為僅對嬰兒分娩有反應的先兆子癇。或者,表型測定元件可以是陰性參考或對照。陰性參考或對照可以是來自未發展先兆子癇的受試者或未懷孕的受試者的樣品或標志物水平表征。在一些情況下,標志物表征從與用于產生被監測個體的標志物表征的樣品的相同類型的樣品獲得。在此類情況下,表型測定元件從相同類型的樣品獲得。例如,如果正在評估個體的血清,則參考或對照優選為血清。
在某些情況下,將獲得的標志物水平表征與單個表型測定元件進行比較,以獲得關于正在測試先兆子癇的個體的信息。在某些情況下,將所獲得的標志物水平表征與多個表型測定元件進行比較。例如,所獲得的標志物水平表征可以與陰性參考和陽性參考進行比較,以獲得關于個體是否將發展先兆子癇的確認信息。在一些實例中,可將獲得的標志物水平表征與代表響應于治療的先兆子癇的參考以及代表不響應于治療的先兆子癇的參考進行比較,以便獲得關于患者是否對治療有反應的信息。
獲得的標志物水平表征和一個或多個表型測定元件的比較可以使用本領域技術人員已知的任何方便的方法進行。例如,陣列領域的技術人員將知道,可以通過例如比較表達譜的數字圖像、通過比較表達數據的數據庫等來比較陣列譜。描述比較表達譜的方式的專利包括但不限于美國專利號6,308,170和6,228,575,其公開內容通過引用并入本文。上文也描述了比較標志物水平譜的方法。類似地,elisa領域的技術人員將知道,elisa數據可以通過例如標準化為標準曲線、比較標準化值等進行比較。比較步驟產生關于所獲得的標志物水平譜與對照或參考譜相似或不相似的信息,以及采用相似性或不相似性信息來診斷、預后、監測、表征或評估先兆子癇的嚴重性、或確認存在或不存在先兆子癇以便預測先兆子癇的發病、診斷先兆子癇、監測先兆子癇患者、評估pe的嚴重性、表征pe、確認存在pe或確認pe不存在。相似性可以基于相對標志物水平、絕對標志物水平或兩者的組合。在某些情況下,使用其上存儲有程序的計算機進行相似性確定,計算機設計為接收從受試者獲得的標志物水平結果(例如來自用戶)的輸入,確定與一個或多個參考譜的相似性,以及返回例如,對于用戶(例如,實驗室技術人員、醫生、外行人、妊娠女性等)的先兆子癇預后。下面描述本公開的計算機實現的情況的進一步描述。
根據所獲得的標志物水平譜與其進行比較的參考或對照譜的類型和性質,上述比較步驟產生關于所測定的細胞或體液的多種不同類型的信息。因此,上述比較步驟可以產生先兆子癇發作的陽性或陰性預測。或者,這樣的比較步驟可產生先兆子癇的陽性或陰性診斷。或者,這樣的比較步驟可以提供先兆子癇嚴重性的表征或評估。
在一些情況下,pe標記標志物水平表征可以基于閾值。該方法還可以涉及獲得一個或多個生物標志物的水平并將水平與預定閾值(例如標準值)進行比較。這樣的閾值可以根據生物標志物的濃度來確定。
在實例中,pe的預測和/或確認的閾值可以根據與對照(例如,妊娠前或在妊娠的較早階段的相同受試者或在沒有患有pe的相同或另一個妊娠期的另一個女性)相比,測試pe或患有pe的受試者中的生物標志物的相對濃度來確定。例如,pe的指示或pe的可能性或pe的嚴重性可以是fn,濃度可以是相對于對照增加至少100倍、至少500倍、至少1,000倍、至少2,000倍、至少3,000倍、至少4,000倍、至少5,000倍、至少10,000倍、至少12,000倍、至少15,000倍、至少20,000倍、至少30,000倍、至少40,000倍、至少50,000倍、至少100,000倍或至少20,000倍;和/或vegf濃度相對于對照增加至少2倍、至少4倍、至少、至少8倍、至少10倍、至少15倍、至少20倍、至少30倍、至少40倍或至少50倍的因子;和/或濃度降低至少20倍、至少30倍、至少40倍、至少50倍、至少60倍、至少70倍、至少80倍、至少90倍、至少100倍、至少110倍、至少120、至少130、至少140或至少150倍;和/或fms樣酪氨酸激酶1(sflt1)濃度增加至少5倍、至少10倍、至少20倍、至少30倍、至少40倍、至少40倍、至少50倍、至少60倍、至少70倍或至少80倍;和/或胎盤生長因子(p1gf)濃度降低至少100倍、至少200倍、至少300倍、至少400倍、至少500倍、至少600倍、至少700倍、至少800倍、至少900倍,至少1000倍、至少1100倍、至少1200倍、至少1300倍、至少1400倍或至少1500倍;和/或adam金屬蛋白酶結構域12(adam12)濃度增加至少2倍、至少5倍、至少10倍、至少15倍、至少20倍、至少30倍、至少40倍、至少50倍、至少60倍、至少70倍、至少80倍、至少90倍或至少100倍。
在某些情況下,當診斷、預后、監測、表征或評估先兆子癇的嚴重性時,或當確認受試者中存在或不存在pe時,不考慮除了生物標志物水平之外的物理特征。在一些情況下,當確認、診斷、預后、表征或評估受試者中pe的嚴重性時,不考慮以下中的至少一種:妊娠期、血壓、體重增加、水潴留、遺傳因子、蛋白尿、頭痛、水腫、蛋白質/肌酐比、血小板計數、應激、(受試者或其家庭成員的)先前妊娠的pe、未經產、年齡,年齡小于20歲、年齡大于35歲、種族,非洲裔美國人和菲律賓人、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作、家族史、妊娠數、流產數、體重指數(bmi)、妊娠糖尿病、i型糖尿病、肥胖、葡萄糖水平、當前和過去的藥物、慢性高血壓、腎病或血栓形成傾向。
在一些情況下,當確認、診斷、預后、表征或評估受試者中pe的嚴重性時,考慮以下中的至少一種:妊娠期、血壓、體重增加、水潴留、遺傳因子、蛋白尿、頭痛、水腫、蛋白質/肌酐比、血小板計數、應激、(受試者或其家庭成員的)先前妊娠的pe、未經產、年齡,年齡小于20歲、年齡大于35歲、種族,非洲裔美國人和菲律賓人、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作、家族史、妊娠數、流產數、體重指數(bmi)、妊娠糖尿病、i型糖尿病、肥胖、葡萄糖水平、當前和過去的藥物、慢性高血壓、腎病或血栓形成傾向。
在一些情況下,在確認、診斷、預后、監測、表征或評估先兆子癇的嚴重性時考慮妊娠期。在一些情況下,妊娠期可分為早期和晚期妊娠期。在一些情況下,除了患者的妊娠期之外,可以考慮包括受試者的血壓、家族史和尿蛋白指數的其他元素。
在一些情況下,可結合上述標志物水平表征使用其他分析以提供個體的先兆子癇預后。這樣的分析是本領域眾所周知的,并考慮例如血壓、體重增加、水潴留、遺傳因素、蛋白尿、頭痛、水腫、蛋白質/肌酐比、血小板計數、應激、(受試者或其家庭成員的)先前妊娠的pe、未經產、年齡,年齡小于20歲、年齡大于35歲、種族,非洲裔美國人和菲律賓人、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作、家族史、妊娠數、流產數、體重指數(bmi)、妊娠糖尿病、i型糖尿病、肥胖、葡萄糖水平、當前和過去的藥物、慢性高血壓、腎病或血栓形成傾向以及妊娠的其他特征。
用于測量來自受試者生物樣品的生物標志物的pe的測試可以提供每個生物標志物小組分析的預測性能,如通過roc曲線分析評價的(zweig等人,receiver-operatingcharacteristic(roc)plots:afundamentalevaluationtoolinclinicalmedicine.clinicalchemistry1993;39:561-77;sing等人rocr:visualizingclassifierperformanceinr.bioinformatics2005;21:3940-1)。在某些情況下,pe特征、評分或指數可具有至少0.8、0.85、0.9、0.95、0.96、0.97、0.980、0.985、0.988、0.990、0.995、0.998或更大的累積roc值。在某些情況下,pe特征、評分或指數可具有至多0.9、0.95、0.96、0.97、0.980、0.985、0.988、0.990、0.995、0.998或更小的累積roc值。或者或另外,pe閾值、特征、評分或指數可以具有至少60%、65%、70%、75%、80%、85%、90%、91%、92%93%、94%、95%、96%、97%、98%或99%的靈敏度;和/或至少60%、65%、70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%98%或99%的特異性。或者或另外,pe閾值、特征、評分或指數可以具有至多60%、65%、70%、75%、80%、85%、90%、91%、92%、93%94%、95%、96%、97%、98%或99%的靈敏度;和/或至多60%、65%、70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%98%或99%的特異性。這樣的pe特征、評分或指數可以用于預后、診斷、監測、表征或評估pe的嚴重性、確認pe的不存在、或確認pe的存在、早期pe或晚期pe。這樣的pe特征、評分或指數優選包含高達12、11、10、9、8、7、6、5、4、3、2或1個生物標志物。roc值可適用于生物標志物特征、評分、閾值或指數。
在一些情況下,可以通過提供例如生成書面報告來提供預測、診斷、預后、監測、表征、評估pe的嚴重性或確認存在或不存在pe,所述書面報告包括包括技術人員的監測評價,例如技術人員對先兆子癇發生的預測(“先兆子癇預測”)、技術人員對先兆子癇的診斷(“先兆子癇診斷”)、技術人員對存在先兆子癇的確認(“先兆子癇陽性確認”)、技術人員對不存在先兆子癇的確認(“先兆子癇陰性確認”)、技術人員對受試者先兆子癇的監測(“先兆子癇監測”)、技術人員對受試者先兆子癇的表征(“先兆子癇表征”)或技術人員測定受試者先兆子癇的嚴重性(“評估先兆子癇的嚴重性”)。因此,本發明的方法還可以包括生成或輸出提供評估結果的報告的步驟,所述報告可以以電子介質(例如,計算機監視器上的電子顯示或可傳送的電子文件)的形式,或者以有形介質(例如,打印在紙或其他有形介質上的報告)的形式提供。
計算機系統和軟件
這些分析方法可以由本領域普通技術人員通過采用基于計算機的系統容易地執行,例如使用本領域已知的任何硬件、軟件和數據存儲介質,并且采用任何方便的用于這樣的分析的算法。例如,數據挖掘算法可以通過“云計算”、基于智能手機或基于客戶端-服務器的平臺等來應用。
本公開考慮使用計算機系統、計算機可讀介質或軟件,具有輸入模塊,其用于收集關于多個生物標志物的水平的輸入;處理器,其用于執行用于執行生物標志物水平的log2、loge或log10變換的算法,從而獲得對數變換水平;處理器,其用于執行用于將每個對數變換水平標準化為標準化水平的算法;處理器,其用于執行用于將每個標準化水平調整為加權標準化水平的算法;處理器,其用于對每個經調整的水平進行總計和任選地平均的算法;處理器,其用于基于總量提供pe評分的算法,以及處理器,其用于任選地執行用于基于先兆子癇評分提供pe指數的算法。計算機優選地生成可以提供給護理者和/或受試者女性(例如,妊娠女性)的報告。該報告中可以不包括以下任何內容、包括以下任意內容或包括所有內容:患者或受試者的姓名、測試時的妊娠期、所分析的標志物列表、樣品中測量的每個標志物的水平、生物標志物水平直接與訓練集中的那些進行比較、與訓練集中的對數轉換和標準化水平比較的生物標志物的對數轉換和標準化水平、生物標志物的對數轉換、標準化和加權數、pe評分、pe指數和推薦用于受試者的作用過程。
在一些情況下,本公開包括用于診斷、預后、監測、表征或評估先兆子癇的嚴重性、確認女性受試者中pe的存在或不存在的系統,包括:(a)輸入模塊,其用于接收作為一個或多個生物標志物,例如sflt-1,plgf和至少兩個其他不同生物標志物的輸入水平,(b)處理器,其任選地被配置為執行算法,例如(i)水平的log2、loge或log10變換以獲得對數變換水平,(ii)將每個對數變換水平標準化為標準化水平,(iii)將每個標準化水平調整為加權標準化水平,(iv)合計每個經調整的水平,(v)平均每個經調整的水平;和(c)輸出模塊,其用于基于評分輸出先兆子癇指數,其中指數評分包括sflt-1/plgf病加上另外兩個其他不同的生物標志物。在一些情況下,處理器可以執行將一個或多個生物標志物的水平相對于訓練集或對照值進行調整的算法,從而提供一個或多個經調整的生物標志物水平。處理器還可以執行使用經調整的生物標志物水平應用至少一個二元運算,加上或減去一個或多個經調整的生物標志物水平,計算兩個經調整的生物標志物水平之間的比率和/或通過將一個或多個變量乘以一個或多個對應的權重因子操作一個或多個經調整的生物標志物,其中將一個或多個經調整的生物標志物水平中的每一個的水平輸入到具體變量中,其中對應的權重因子對于每個具體變量是獨特的,其中至少對應的權重因子之一不是一。在一些情況下,算法是實函數。
在一些情況下,本公開包括含有指令的計算機可讀介質,當由計算機系統執行時,指令使得計算機系統接收關于來源于受試者的生物樣品中pe生物標志物的水平的第一數據集,并對這些水平進行分析以獲得受試者中pe的評估。在一些情況下,當由計算機系統執行時,指令可以使計算機系統第二次執行那些步驟(例如,接收關于pe生物標志物的水平的第二數據集,并且執行第二分析以獲得第二評估)。在一些情況下,可以在不同的時間點執行那些步驟。在一些情況下,指令使計算機系統將第一評估與第二評估進行比較,并基于比較來確認pe或缺乏pe。
報告
報告可以包括關于測試設施的信息,所述信息與進行樣本收集和/或數據生成的醫院、診所或實驗室相關。樣品收集可以包括從受試者獲得流體樣品,例如血液、唾液、尿液等;組織樣品,例如組織活檢等。數據生成可以包括測量在先兆子癇患者與健康個體(例如,沒有患有和/或不發展先兆子癇的個體)中差異表達或以不同水平存在的一個或多個基因的多肽濃度水平。該信息可以包括與例如測試設施的名稱和位置、進行測定和/或輸入輸入數據的實驗室技術人員的身份、進行測定和/或分析的日期和時間、樣品和/或結果數據存儲的位置、或測定中使用的試劑(例如試劑盒等)的批號有關的一個或多個細節。具有此信息的報告字段可以使用用戶提供的信息填充。
報告可以包括關于服務提供商的信息,服務提供商可以位于用戶所在的保健設施之外,或者保健設施內。這樣的信息的示例可以包括服務提供商的名稱和位置、審閱者的名稱,以及在必要或期望時進行樣本收集和/或數據生成的個人的名稱。具有此信息的報告字段可以使用用戶輸入的數據來填充,其可以從預編寫的選擇中選擇(例如,使用下拉菜單)。報告中的其他服務提供商信息可以包括關于結果和/或關于解釋報告的技術信息的聯系信息。
報告可以包括患者數據部分。患者數據部分可以包括由以下組成的列表中的一個或多個項目:患者病史和癥狀(其可以包括例如,妊娠期、血壓、蛋白尿、糖尿病、葡萄糖水平、體重指數、年齡、種族、血清型、巴氏測試結果(pap涂片)、先前先兆子癇發作、家族史、妊娠數、流產數、體重增加、水潴留、遺傳因子、頭痛、水腫、蛋白質/肌酐比、當前和過去的藥物、應激、(受試者或其家庭成員的)先前妊娠的pe、未經產、慢性高血壓、腎病或血栓形成傾向和妊娠的任何其他特征)、管理患者數據,例如識別患者的信息(例如,姓名、患者日期出生(dob)、性別、郵寄和/或居住地址、醫療記錄號(mrn)、醫療設施中的房間和/或床號、保險信息等)、訂購監測評估的患者的醫生或其他健康專業人員的姓名,以及(其與訂購醫師不同)負責患者護理的職員醫師(例如,初級保健醫師)的姓名。
報告可以包括樣品數據部分,其可以提供關于在監測評估中分析的生物樣品的信息,例如來源于患者的生物樣品的來源(例如,血液、唾液或組織類型等)、如何處理樣品(例如,儲存溫度、預備操作方案)或收集的日期和時間。通常可以使用由用戶輸入的數據來填充具有該信息的報告字段,其中一些可以作為預編寫的選擇來提供(例如,使用下拉菜單)。
報告可以包括評估報告部分,其可以包括在如本文所述的數據加工之后生成的信息。解釋性報告可以包括對受試者發展pe的可能性的預測、pe的診斷、受試者患有有pe的確認、受試者沒有患有pe的確認、受試者的pe的監測(例如,生物標志物的水平保持穩定或改變)、pe的特征、pe的嚴重性水平或其任何組合。如果生物標志物水平改變,報告可以包括這種改變的程度,以及改變在pe發生、預測或嚴重性方面的意義。解釋性報告可以包括例如蛋白質水平確定測定的結果(例如,“血清中1.5nmol/升adam12”);以及該生物標志物水平的解釋,例如預測、診斷、監測、表征、評估pe的嚴重性或確認pe的存在或不存在。在一些示例中,報告的評估部分包括建議。例如,如果結果表明先兆子癇是可能的,建議包括建議改變飲食、施用血壓藥、建議臥床休息、建議早產、施用糖尿病藥物等,如在本領域中所建議的那樣。
報告可以包括診斷、預后、特征、監測、pe的嚴重性或pe的存在或不存在的確認中的至少一個;基于對來自懷孕受試者的生物樣品中檢測到的一個或多個生物標志物的分析的生物標志物指數值。報告可以包括每個生物標志物小組分析的預測性能。在一些情況下,通過roc曲線分析評估預測性能。
還容易理解的是,報告可以包括附加元素或經修飾的元素。例如,在電子報告的情況下,報告可以含有指向內部或外部數據庫的超鏈接,其提供關于報告的所選元素的更詳細信息。例如,報告的患者數據元素可以包括到電子患者記錄的超鏈接或用于訪問這樣的患者記錄的站點,該患者記錄被保存在機密數據庫中。在一些情況下,包括超鏈接可能在醫院內系統或臨床環境中感興趣。在一些情況下,包含超鏈接可能在家庭或工作環境中感興趣。當以電子格式時,報告被記錄在合適的物理介質上,諸如計算機可讀介質,例如在計算機存儲器、zip驅動器、軟盤、usb芯片、cd、dvd或能夠存儲可檢索的磁或電子信息的任何其他存儲介質。
容易理解的是,報告可以包括上述元素中的全部或一些,條件是報告通常至少包括足以提供用戶請求的分析(例如預測、診斷、監測、表征、評估先兆子癇的嚴重性、或確認存在或不存在先兆子癇)的元素。
本公開還提供了商業方法,其包括確定受試者中先兆子癇的存在、不存在、預測、嚴重性、特征或確認受試者中存在或不存在先兆子癇的步驟。該方法包括以下步驟:評估來源于受試者的樣品中sflt-1、plgf和多個生物標志物的水平,其中多個生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素,確定生物標志物指數值,該指數包括sflt-1/plgf和加上多個生物標志物,使用生物標志物指數以提供先兆子癇確定、確認、不存在、診斷、預后、嚴重性或特征,以及提供報告以換取費用,其中該報告基于生物標志物的分析指示指數值,以及指示的范圍說明受試者是否處于pe的低風險、先兆子癇的高風險或正經歷先兆子癇。在一些情況下,該商業方法還包括傳送報告。在一些情況下,該報告含有關于受試者的信息,包括血壓、年齡、體重、孕齡、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史、蛋白尿、體重指數、腫脹、腹壓、子宮搏動指數、血小板減少、以前的先兆子癇史、以前的子癇史、首次分娩、多胎、循環游離dna、循環胎兒dna、游離dna、胎兒dna、吸煙史或相關并發因子的家族史。在一些情況下,多種生物標志物不包括內皮聯蛋白、血纖肽a、抗凝血酶iii、igfals、flt4、igfbp-5、tgf-b1、血纖肽a:d-二聚體、纖膠凝蛋白-2、纖膠凝蛋白-3、肌酐、簇集素、h2松弛素、p1gf-2、p1gf-3和人絨毛膜促性腺激素。在某些情況下,該報告是電子的。在一些情況下,該指數不受以下中至少一個的影響:血壓、年齡、體重、孕齡、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史和家族史。在一些情況下,該指數不受以下中所有的影響:血壓、體重、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史和家族史。在某些情況下,該指數不受年齡影響。有時,該指數不受胎齡影響。
在一些情況下,本公開進一步提供了商業方法,其包括確定受試者中先兆子癇的存在、不存在、預測、嚴重性或特征或確認受試者中先兆子癇的不存在或存在的步驟。該方法可以包括以下步驟:(a)評估來源于受試者的樣品中sflt-1、plgf和至少兩個其他不同生物標志物的水平,其中至少兩個其他生物標志物不是鐵蛋白(ft)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、觸珠蛋白(hp)、α-2-巨球蛋白(a2m)、載脂蛋白e(apoe)、載脂蛋白c-iii(apo-c3)、載脂蛋白a-1(apoa1)、視黃醇結合蛋白4(rbp4)、血紅蛋白(hb)、血纖蛋白原α(fga)、皮卡丘素(egflam)、游離人絨毛膜促性腺激素(游離βhcg)或血紅素,(b)確定生物標志物指數值,該指數包含sflt/plgf和加上至少兩個其他不同生物標志物,(c)使用生物標志物指數來提供先兆子癇測定、確認、不存在、診斷、預后、嚴重性或特征,和(d)提供報告以換取費用,其中該報告基于生物標志物的分析指示指數值,以及以下中的至少一個:說明受試者是否處于先兆子癇的低風險,說明受試者是否處于先兆子癇的高風險,說明受試者是否患有先兆子癇,說明受試者是否沒有患有先兆子癇,表征先兆子癇,和指示先兆子癇的嚴重性。
試劑、系統和試劑盒
還提供了用于實施一個或多個上述方法的試劑、系統和試劑盒。本發明的試劑、系統和試劑盒可以變化很大。變化可以包括孵育時間和溫度的改變。目的試劑包括特別設計用于從樣品(例如一個或多個檢測元件)產生先兆子癇標志物的上述標志物水平表征的試劑。檢測元件可以是用于檢測蛋白質、蛋白質片段的抗體或肽。檢測元件可以是用于檢測核酸的寡核苷酸。在一些情況下,檢測元件包括檢測單個先兆子癇標志物的表達的試劑,例如,檢測元件可以是包括一個或多個檢測元件(例如一個或多個更多抗體、一個或多個寡核苷酸、一組或多組pcr引物、一組或多組等溫多核苷酸擴增引物等)的試紙條、板、陣列或混合物,其可用于同時檢測至少兩個先兆子癇標志物的表達。
在一種情況下,提供了用于檢測受試者中先兆子癇的存在、不存在、預測、嚴重性或特征的試劑盒。這樣的試劑盒包括用于測量選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的多個生物標志物的多個檢測元件(分析物)。在其他情況下,使用至少2、3、4、5、6、7、8、9、10、11、12、13或14種(或更多種)不同的試劑來測量至少2、3、4、5、6、7、8、9、10、11、12、13或14個(或更多個)不同生物標志物。當提及生物標志物(例如p1gf)時,除非明確說明,否則應當理解,已知或待發現的生物標志物(例如p1gf)的所有同種型均指該生物標志物術語,例如p1gf(例如hpa18788.6[152aa]、hpa18788.1[1017aa]、hpa18788.2[1009aa]、hpa18788.3[775aa]、hpa18788.4[403aa]、hpa18788.5[375aa]或hpa18788.9[463aa])。(本文使用的p1gf等同于plgf或plgf)。當提及血色素結合蛋白(hpx)時,應當理解血紅素結合和血紅素未結合形式的血色素結合蛋白均指該生物標志物術語。
在一個實施方案中,特別適合于產生標志物水平表征(例如先兆子癇標志物)的一類試劑是特異性結合該蛋白質標志物的抗體的集合。在一些實例中,這樣的抗體可以用于elisa(例如競爭性或夾心elisa形式)。可以采用的其他分析方法學包括xmaptm微球形式、蛋白質組陣列、用于通過流式細胞術分析的懸浮液、蛋白質印跡、斑點印跡或免疫組織化學。使用它們的方法在本領域中是眾所周知的。這些抗體可以在溶液中提供。或者,它們可以預先結合到固體基質上,例如多孔皿的孔或xmap微球的表面。
在一些實施方案中,可以使用其中代表目的基因的探針核酸陣列作為試劑。本領域中已知多種不同的陣列形式,具有各種不同的探針結構、底物組合物和附著技術(例如點印跡陣列、微陣列等)。目的代表性陣列結構包括在美國專利號5,143,854;5,288,644;5,324,633;5,432,049;5,470,710;5,492,806;5,503,980;5,510,270;5,525,464;5,547,839;5,580,732;5,661,028;5,800,992;其公開內容通過引用并入本文;以及wo95/21265;wo96/31622;wo97/10365;wo97/27317;ep373203;和ep785280中所述的那些。
一種特別適合于產生基因的標志物水平表征(例如,先兆子癇基因)的試劑是設計用于選擇性擴增此類基因的基因特異性引物的集合(例如,使用基于pcr的技術,例如實時rt-pcr或等溫擴增技術,例如環介導的dna等溫擴增(lamp)、鏈置換擴增(sda)、基于序列的擴增(nasba)、自我維持序列復制(3sr)等)。基因特異性引物及其使用方法描述于美國專利5,994,076中,其公開內容通過引用并入本文。
在一些情況下,試劑盒可以包括選擇性雜交編碼所選生物標志物的多核苷酸序列的多核苷酸引物。在某些情況下,引物選擇性雜交編碼選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的蛋白質的至少兩個多核苷酸序列。這樣的引物可以是dna或rna引物。
感興趣的還有包括特異性針對至少一個基因或蛋白質的探針、引物或抗體(也稱為試劑)的探針、引物集合或抗體集合的陣列,基因或蛋白質選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12。在一些情況下,可以選擇這些基因中的多個,例如至少2、3、4、8個或更多個。
在某些情況下,探針、引物或抗體的集合包括對p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12中的一個或多個具有特異性的試劑。本發明的探針、引物或抗體集合或試劑可以包括僅對上文列出的基因、蛋白質或輔因子特異的試劑,或者它們可以包括對上文未列出的其他基因、蛋白質或輔因子特異的試劑,例如對于基因、蛋白質或輔因子特異的探針、引物或抗體,其表達模式在本領域已知與先兆子癇相關,例如sflt-1(vegf-r1)和p1gf。
本公開的系統和試劑盒可以包括上述陣列、基因特異性引物集合或蛋白質特異性抗體集合。在蛋白質特異性抗體試劑盒的情況下,系統和試劑盒可以進一步包括一個或多個另外的試劑,例如牛血清白蛋白(bsa)、酪蛋白、奶粉溶液、牛γ-球蛋白(bgg)在磷酸鹽緩沖鹽水(pbs)/吐溫或pbs/triton-x100、pbs/tween、pbs/triton-x100或硼酸鹽緩沖劑中;選擇的固體表面,優選顯示蛋白質親和力的表面,例如聚苯乙烯微量滴定板的孔;第二抗體將具有相關酶,例如脲酶、過氧化物酶或堿性磷酸酶,以及合適的顯色底物。例如,可以使用脲酶或過氧化物酶綴合的抗人igg,含有pbs的溶液如pbs/吐溫),顯色底物例如尿素和溴甲酚紫(在脲酶標記的情況下)或2,2'-連氮基-二-(3-乙基-苯并噻唑啉)-6-磺酸(abts)和h2o2(在過氧化物酶標記的情況下)。然后通過測量顏色產生的程度來實現定量,例如使用可見光譜分光光度計。
系統和試劑盒可以進一步包括在各種方法中使用的一個或多個另外的試劑,例如用于產生靶核酸、dntp和/或rntp的引物,其可以是預先混合或分開的、一個或多個獨特標記的dntp和/或rntp,例如生物素化或cy3或cy5標記的dntp、具有不同散射光譜的金或銀顆粒、或其他合成后標記試劑,例如熒光染料的化學活性衍生物、酶,例如逆轉錄酶、dna聚合酶、rna聚合酶等,各種緩沖介質,例如,雜交和洗滌緩沖劑,預制探針陣列,標記的探針純化試劑和組分,例如離心柱等,信號產生和檢測試劑,例如標記的二抗,鏈霉抗生物素蛋白-堿性磷酸酶綴合物,化學熒光或化學發光底物等。
本發明的系統和試劑盒還可以包括先兆子癇表型測定元件,該元件在許多情況下是參考或對照樣品或標志物表征,其可以例如通過合適的實驗或計算手段使用以實現基于“輸入”標志物水平譜的先兆子癇預后,例如,已經用上述標志物測定元件確定的。代表性的先兆子癇表型測定元件包括來自已知患有或沒有患有先兆子癇的個體的樣品、標志物水平表征的數據庫,例如參考或對照譜等,如上所述。
除了上述組分之外,本發明的試劑盒還將包括用于實施本發明方法的說明書。這些說明書可以以各種形式存在于本發明試劑盒中,其中一個或多個可存在于試劑盒中。可以存在這些說明的一種形式是作為在合適的介質或基材上的打印信息,例如在其上印刷信息的一片或多片紙,在試劑盒的包裝中,在包裝插頁等中。手段將是其上已記錄了信息的計算機可讀介質,例如軟盤、軟盤、usb設備、cd等。一些手段可以是可以經由因特網(即,經由云)使用以訪問移除的站點處的信息的網站地址。任何方便的手段可以存在于試劑盒中。
在某些情況下,本公開提供了用于確定受試者中pe的存在、不存在、預測、嚴重性、監測或特征的商業方法。這樣的方法包括:對受試者的生物樣品進行分析,以確定選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的一個或多個生物標志物的存在和量;確定生物標志物的權重、特征、評分或指數值;使用生物標志物權重、特征、評分或指數值來提供pe的診斷、預后、嚴重性、確認存在、確認不存在或特征,以及提供報告以換取費用。
在其他情況下,本公開提供了用于確定受試者中確定存在、確定不存在、確定預測、監測、確定嚴重性、確認存在、確認不存在或表征pe的商業方法。這樣的方法包括:對受試者的生物樣品進行分析,以確定選自p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12的一個或多個生物標志物的存在和量。在某些情況下,探針、引物或抗體的集合包括對p1gf、hpx、sflt-1、papp-a、vegf(不包括vegf-r1)、fn、fg和adam12具有特異性的試劑;確定生物標志物的權重、特征、評分或指數值;使用生物標志物權重、特征、評分或指數值來提供pe的診斷、預后、特征、確認存在、確認不存在或確定pe的嚴重性,并提供報告以換取費用。
在某些情況下,指數值基于生物標志物的分析。在一些實例中,提供范圍或閾值的指示以說明受試者是處于pe的低風險、pe的高風險還是正經歷pe。在其他情況下,指數值基于生物標志物的分析以及說明受試者是否患有輕度pe、中度pe或重度pe的范圍的指示。在一些情況下,提供確認的可靠性或確定性的指示(女性受試者是否患有pe)。
本文公開的任何方法、試劑盒、組合物、商業方法、計算機系統可以與樣品一起使用,其中樣品是血清樣品。在一些情況下,樣品來源于血液、血漿、血清、尿液、細胞或體液。在一些情況下,樣品來源于母親或胎兒。在一些情況下,樣品是陰道拭子。在一些情況下,樣品不是尿液樣品。在一些情況下,生物標志物是肽。在一些情況下,樣品中的生物標志物是肽、肽的一部分、肽的片段、含有抗原的肽、肽的一部分(其中肽的一部分含有抗原)、肽的片段(其中肽的片段含有抗原)。在一些情況下,評估包括測量至少一種rna分子的水平。在一些情況下,評估包括進行至少一個測序反應。在一些情況下,該指數不受血壓、年齡、體重、胎齡、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史或家族史的影響。在一些情況下,評估不包括比較在第一時間點來源于受試者的樣品和在第二時間點來源于相同受試者的樣品。在一些情況下,評估包括比較在第一時間點來源于受試者的樣品和在第二時間點來源于相同受試者的樣品。在一些情況下,評估步驟包括測定選自sflt-1、p1gf、vegf(不包括vegf-r1)、adam12、hpx、papp-a和fn的生物標志物的水平。在一些情況下,多個生物標志物不包括內皮聯蛋白、血纖肽a、抗凝血酶iii、igfals、flt4、igfbp-5、tgf-b1、血纖肽a:d-二聚體、纖膠凝蛋白-2、纖膠凝蛋白-3、肌酐、簇集素、h2松弛素、p1gf-2、p1gf-3和人絨毛膜促性腺激素。在一些情況下,使用識別選自sflt-1、p1gf、vegf(不包括vegf-r1)、adam12、hpx、papp-a和fn的生物標志的至少一種抗體進行測量。在一些情況下,該方法不包括預測在先兆子癇無癥狀的受試者中的先兆子癇。在一些情況下,評估不包括多普勒篩查。在一些情況下,該方法不包括檢測樣品中微泡或外來體的存在。在一些情況下,該方法準確度大于85%。在一些情況下,該方法靈敏度大于85%。在一些情況下,該方法特異性大于85%。在一些情況下,該方法準確度大于85%。在一些情況下,該方法具有大于85%的陽性預測值。在一些情況下,該方法具有大于85%的陰性預測值。在一些情況下,生物標志物與血壓、年齡、體重、妊娠期、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史、蛋白尿、體重指數、腫脹、腹壓、子宮搏動指數、血小板減少、以前的先兆子癇史、以前的子癇史、受試者的先前的分娩次數、循環游離dna、循環的胎兒dna、游離dna、胎兒dna、吸煙史或相關并發因子的家族史相關。在一些情況下,生物標志物與血壓、年齡、體重、妊娠期、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史、蛋白尿、體重指數、腫脹、腹壓、子宮搏動指數、血小板減少、以前的先兆子癇史、以前的子癇史、受試者的先前的分娩次數、循環游離dna、循環的胎兒dna、游離dna、胎兒dna、吸煙史或相關并發因子的家族史不相關。
本公開還提供了不包括先兆子癇診斷的測試,其中所述測試從來源于受試者的樣品測量一個或多個生物標志物,并且具有至少0.8、0.85、0.9、0.95、0.980、0.981、0.982、0.983、0.984、0.985、0.986、0.987、0.989、0.990、0.991、0.992、0.993、0.994、0.995、0.996、0.997、0.998、0.999或更大的總體roc值。在一些情況下,測定至少2、3、4、5、6、7、8、9、10、11、12、13或14個生物標志物。在一些情況下,測定至多2、3、4、5、6、7、8、9、10、11、12、13或14個生物標志物。在一些情況下,總體roc值不受血壓、年齡、體重、妊娠期、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史或家族史的影響。在一些情況下,樣品是血清樣品。在一些情況下,樣品來源于血液、血漿、血清、尿液、細胞或體液。在一些情況下,樣品來源于母親或胎兒。在一些情況下,樣品是陰道拭子。在一些情況下,樣品不是尿液樣品。在一些情況下,生物標志物是肽。在一些情況下,樣品中的生物標志物是肽、肽的一部分、肽的片段、含有抗原的肽、肽的一部分(其中肽的一部分含有抗原)、肽的片段(其中肽的片段含有抗原)。在一些情況下,測試的結果不受血壓、年齡、體重、妊娠期、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史或家族史的影響。在一些情況下,測試不包括比較在第一時間點來源于受試者的樣品和在第二時間點來源于同一受試者的樣品。在一些情況下,測試由比較來源于第一時間點的受試者的樣品和來源于第二時間點的相同受試者的樣品組成。在一些情況下,測試包括測定選自sflt-1、p1gf、vegf(不包括vegf-r1)、adam12、hpx、papp-a和fn的生物標志物的水平。在一些情況下,生物標志物不包括內皮聯蛋白、血纖肽a、抗凝血酶iii、igfals、flt4、igfbp-5、tgf-b1、血纖肽a:d-二聚體、纖膠凝蛋白-2、纖膠凝蛋白-3、肌酐、簇集素、h2松弛素、p1gf-2、p1gf-3和人絨毛膜促性腺激素。在一些情況下,使用識別選自sflt-1、p1gf、vegf(不包括vegf-r1)、adam12、hpx、papp-a和fn的生物標志的至少一種抗體進行測試。在一些情況下,測試不包括在無癥狀的受試者中預測先兆子癇。在一些情況下,測試不包括多普勒篩查。在一些情況下,測試不包括檢測樣品中微泡或外來體的存在。在一些情況下,測試為至少85、90、95%或更高的準確度。在一些情況下,測試為至少85、90、95%或更高的靈敏度。在一些情況下,測試為至少85、90、95%或更高的特異性。在一些情況下,測試具有至少85、90、95%的陽性預測值。在一些情況下,測試具有至少85、90、95%或更多的陰性預測值。在一些情況下,生物標志物與血壓、年齡、體重、妊娠期、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史、蛋白尿、體重指數、腫脹、腹壓、子宮搏動指數、血小板減少、以前的先兆子癇史、以前的子癇史、受試者的先前的分娩次數、循環游離dna、循環的胎兒dna、游離dna、胎兒dna、吸煙史或相關并發因子的家族史相關。在一些情況下,生物標志物與血壓、年齡、體重、妊娠期、民族性、糖尿病、腎病、自身免疫疾病、孕產婦史、蛋白尿、體重指數、腫脹、腹壓、子宮搏動指數、血小板減少、以前的先兆子癇史、以前的子癇史、受試者的先前的分娩次數、循環游離dna、循環的胎兒dna、游離dna、胎兒dna、吸煙史或相關并發因子的家族史不相關。在一些情況下,測試包括進行生物測定、功能測定、elisa、免疫測定、質譜、色譜、比濁法、輻射狀免疫擴散或單向輻射狀免疫擴散。在一些情況下,測試包括消化和測量生物標志物。在一些情況下,測試包括衍生化和測量生物標志物。在一些情況下,測試包括從樣品中的至少一個細胞分離肽。在一些情況下,測試還包括檢測多態性或對生物標志物的修飾。在一些情況下,測試還包括檢測rna和/或dna。在一些情況下,測試還包括檢測與生物標志物相關的rna和/或dna。在一些情況下,測試還包括檢測轉錄因子和/或轉錄因子輔因子。在一些情況下,測試還包括檢測與生物標志物相關的轉錄因子和/或轉錄因子輔因子。在一些情況下,測試還包括使用算法、閾值、隨時間的方向變化、將指數與單個患者進行比較、將指數與對照組比較或將指數與參考標準進行比較。在一些情況下,該測試用于確認受試者中先兆子癇的存在,其中受試者具有至少一種與先兆子癇相關的癥狀。在一些情況下,該測試用于在受試者中提供先兆子癇的診斷,其中受試者患有高血壓和蛋白尿。在一些情況下,該測試用于在受試者中提供先兆子癇的診斷,其中受試者患有高血壓。
在一些情況下,該測試用于在受試者中提供先兆子癇的診斷,其中受試者具有與先兆子癇相關的一個危險因素。在一些情況下,該測試用于確定受試者是否處于先兆子癇的風險中。在一些情況下,該測試用于量化受試者發展先兆子癇的風險。在一些情況下,該測試用于預測受試者發展先兆子癇的時間。在一些情況下,該測試用于預測先兆子癇的孕產婦和/或胎兒結果。在一些情況下,該測試用于區分輕度、中度和重度先兆子癇。在一些情況下,該測試用于確定是否hellp綜合征、早產、宮內生長限制、胎盤早剝、胎盤累積、胎兒出生體重低、胎齡低、妊娠高血壓、慢性高血壓、妊娠糖尿病、i型糖尿病、ii型糖尿病或自發流產的風險是否是受試者患有先兆子癇的結果。在一些情況下,測試還包括在非電子報告上創建電子報告。
在一些實施方案中,本公開包括排除先兆子癇診斷的測試,其中所述測試從取自受試者的樣品測量一個或多個生物標志物,并且具有至少0.8的總體roc值。在一些實施例中,該測試具有至少為0.8、0.85、0.9、0.95、0.980、0.9、0.982、0.983、0.984、0.985、0.986、0.987、0.989、0.990、0.991、0.992、0.993、0.994、0.995、0.996、0.997、0.998、0.999或更大的總體roc值。
本公開進一步提供了用于確認pe的存在、確認pe不存在、診斷、預后、監測、表征或確定受試者中先兆子癇的嚴重性的試劑盒,所述試劑盒包含用于測定來源于受試者的樣品中纖連蛋白的水平的至少兩種特異性試劑。在一些情況下,至少兩種試劑包含選擇性結合纖連蛋白的兩種不同抗體。在一些情況下,試劑盒還包含特異性用于測定樣品中sflt-1和plgf水平的試劑。在一些情況下,樣品是血清樣品。在一些情況下,樣品是血液樣品。在一些情況下,樣品不是尿液樣品。在一些情況下,試劑盒不包括檢測igfals、flt4、p1gf、p1gf-2、p1gf-3或sflt-1的試劑。
本公開還提供了用于診斷、預后、監測、表征、確定先兆子癇的嚴重性或確認受試者中存在或不存在先兆子癇的試劑盒,所述試劑盒包含特異性用于測定papp-a水平的第一試劑和特異性用于測定adam12的第二試劑。在一些情況下,試劑盒不包括檢測igfals、flt4、p1gf、p1gf-2、p1gf-3或sflt-1的試劑。在一些情況下,試劑盒不能用于預后、診斷、篩選、確定或確認唐氏綜合征。在一些情況下,試劑盒不能用于預后、診斷、篩查、確定或確認心血管疾病。在一些情況下,生物標志物不是p1gf-2或p1gf-3。
通常,本公開進一步提供用于確認pe的存在、確認pe不存在、診斷、預后、監測、表征或確定受試者中pe的嚴重性的試劑盒,所述試劑盒包含特異性用于測定來自孕婦的樣品中纖連蛋白的水平的至少兩種試劑。
在一些情況下,評估包括進行生物測定、功能測定、elisa、免疫測定、質譜、色譜、比濁法、輻射狀免疫擴散或單向輻射狀免疫擴散。在一些情況下,評估包括消化和測量生物標志物。在一些情況下,評估包括衍生化和測量生物標志物。在一些情況下,評估包括從樣品中的至少一個細胞分離肽。在一些情況下,方法還包括檢測多態性或對生物標志物的修飾。在一些情況下,方法還包括檢測rna和/或dna。在一些情況下,方法還包括檢測與生物標志物相關的rna和/或dna。在一些情況下,方法還包括檢測轉錄因子和/或轉錄因子輔因子。在一些情況下,方法還包括檢測與生物標志物相關的轉錄因子和/或轉錄因子輔因子。在一些情況下,方法還包括使用算法、閾值、閾值范圍、隨時間的方向變化、將指數與單個患者進行比較、將指數與對照組比較或將指數與參考標準。在一些情況下,該方法用于確認受試者中先兆子癇的診斷,其中受試者具有至少一種與先兆子癇相關的癥狀。在一些情況下,該方法用于在受試者中提供先兆子癇的診斷,其中受試者患有高血壓和蛋白尿。在一些情況下,該方法用于在受試者中提供先兆子癇的診斷,其中受試者患有高血壓。在一些情況下,該方法用于在受試者中提供先兆子癇的診斷,其中受試者具有與先兆子癇相關的一個危險因素。在一些情況下,該方法用于確定受試者是否處于先兆子癇的風險中。在一些情況下,該方法用于量化受試者發展先兆子癇的風險。在一些情況下,該方法用于預測受試者發展先兆子癇的時間。在一些情況下,該方法用于預測先兆子癇的孕產婦和/或胎兒結果。在一些情況下,該方法用于區分輕度、中度和重度先兆子癇。在一些情況下,該方法用于確定是否hellp綜合征、早產、宮內生長限制、胎盤早剝、胎盤累積、胎兒出生體重低、胎齡低、妊娠高血壓、慢性高血壓、妊娠糖尿病、i型糖尿病、ii型糖尿病或自發流產的風險是否是患有先兆子癇的受試者的結果。在一些情況下,該方法還包括創建電子報告。
本公開還提供了用于確認受試者中先兆子癇的存在、確認pe不存在、診斷、預后、監測、表征或確定其嚴重性的試劑盒,所述試劑盒包含特異性用于測定水平的第一試劑的papp-a和特異性用于測定adam12水平的第二試劑。在一些情況下,試劑盒不包括檢測igfals、flt4、p1gf、p1gf-2、p1gf-3或sflt-1的試劑。在一些情況下,試劑盒不能用于預后、診斷、篩查、確定或確認唐氏綜合征。在一些情況下,試劑盒不能用于預后、診斷、篩查、確定或確認心血管疾病。在一些情況下,生物標志物不是p1gf-2或p1gf-3。
應用
本文提供的方法、組合物和試劑可用于診斷、分析、區分或確認女性受試者中先兆子癇(pe)的存在或不存在。另外,本文提供的方法、組合物和試劑可用于診斷、分析、區分或確認女性受試者中的先兆子癇(pe),其中女性受試者還具有本文所述的其他癥狀。方法、組合物和試劑可用于多種應用,包括例如預測個體是否發展先兆子癇、診斷先兆子癇、確認先兆子癇的存在、不存在或嚴重性、以及監測患有先兆子癇的個體。
另外,方法、組合物和試劑可用于多種應用,包括例如預測個體是否發展先兆子癇,其具有如本文所述的其他癥狀,診斷具有如本文所述的其他癥狀的個體的先兆子癇,確認患有本文所述的其他癥狀的個體中先兆子癇的存在、不存在或嚴重性,以及監測患有先兆子癇的個體中患有本文所述的其他癥狀的個體。在一些情況下,其他癥狀可包括高血壓和蛋白尿。在其他情況下,其他癥狀可包括高血壓。
方法、組合物和試劑還可用于鑒定處于先兆子癇風險中的個體并且量化個體中先兆子癇的風險。通常,方法、組合物和試劑可用于預測先兆子癇發作的時間。在一些情況下,方法、組合物和試劑可用于預測先兆子癇進展的時間線。本文提供的方法、組合物和試劑可用于預測先兆子癇的結果,其中結果影響胎兒或其中結果影響受試者,通常是母親。在一些情況下,本文提供的方法、組合物和試劑可用于區分先兆子癇一個階段與先兆子癇另一階段。例如,先兆子癇的階段可以是輕度或嚴重的。在一些情況下,本文提供的方法、組合物和試劑可用于區分先兆子癇和子癇。通常,本文提供的方法、組合物和試劑可用于確定受試者患有先兆子癇的結果是否是hellp綜合征、早產的風險或進展、宮內生長限制的風險或進展、自發流產的風險、胎盤早剝落的風險或進展、胎盤增生的風險或進展、相對于胎齡而言具有低或高胎兒出生體重的風險和小或大尺寸的風險。本文提供的方法、組合物和試劑可進一步用于區分患有先兆子癇的患者與沒有患有先兆子癇但具有與先兆子癇相關的癥狀的患者,此類癥狀包括懷孕癥狀的并發癥、妊娠高血壓、慢性高血壓、妊娠糖尿病、i型糖尿病和/或ii型糖尿病。
本文提供的方法、組合物和試劑還可用于產生報告(通常是電子報告)以傳達本文的方法、組合物和試劑的結果。在一些情況下,報告可以傳達受試者的先兆子癇評分、先兆子癇指數和/或先兆子癇譜。
通過說明而非限制的方式提供以下實施例。
實施例
提出以下實施例以便為本領域普通技術人員提供如何制備和使用本公開的完全公開和描述,并且不旨在限制本公開的范圍,也不是它們旨在表示以下實驗是所進行的全部或獨特的實驗。已經做出努力以確保關于使用的數字(例如量、溫度等)的準確性,但是應該考慮一些實驗誤差和偏差。除非另有說明,否則份數是重量份,分子量是重均分子量,溫度是攝氏度,壓力是大氣壓或接近大氣壓。
實施例1-通過elisa分析來自正常受試者和患有先兆子癇的受試者的樣品
本實施例說明了本文所述的公開內容用于使用elisa方法進行來源于妊娠女性的一組樣品的分析的用途,其中一些樣品沒有患有先兆子癇并且其中一些樣品患有先兆子癇。本文所示的生物標志物的使用是用于診斷、預后、監測、表征、預測先兆子癇或確認女性受試者中存在或不存在先兆子癇。
設備
用于進行elisa測定的設備包括eppendorf
材料
執行方法所需的材料和試劑包括0.5ml和2ml深孔聚丙烯稀釋單元(block)、15ml和50ml聚丙烯管、5ml、10ml和25ml一次性移液管和試劑槽。將10xpbst(即具有
臨床樣品
來源于患有或沒有患有先兆子癇和/或患有多種合并癥的妊娠患者的血清樣品獲自包括
模板
可以使用含有臨床樣品、qc對照和標準品的多個不同的96孔板模板(參見圖3和圖4)。在所有情況下,列1和2含有具有2倍稀釋度的一式兩份的8點標準曲線。列12含有反向的8點標準曲線或反向一式兩份的4點標準曲線,以解決從右到左和從上到下的變異。將20份(一式三份)或32份(一式兩份)臨床血清樣品以隨機方式排列在板上。對于一式三份,樣品通過列在板上交錯,而對于一式兩份,樣品通過行沿板向下交錯。每個板含有4或6個重復的hiqc和loqc對照樣品,其策略性地排列在板上以評估從上到下和從左到右的變異。
實驗步驟
主要單元的制備。用模板編號(例如“t1master”)標記0.5ml或2ml深孔單元的正面。用移液器將每個解凍的臨床樣品混合,并且將足夠用于所有運行的測定的樣品(通常為30-500微升(μl),包括20%的平均值)加入到主要單元中。hi和loqc不添加到主要單元(僅添加到稀釋單元),因此這些孔在主要單元中保持為空的。將主要單元用板密封件密封,并在不用于制備稀釋單元時儲存在4℃。
稀釋單元的制備。所有必需的試劑和樣品在使用前在室溫下溫熱30分鐘。將2ml深孔塊的前面標記為“tx-marker”作為用于跟蹤的人可閱讀條形碼,其中“x”是被制備的模板,“marker”是被測定的蛋白質標志物。將凍干的標志物標準品用1-2ml去離子水或校準稀釋劑重構,通過攪拌輕輕混合,并允許重構至少5分鐘但至多15分鐘以制備10x或1x濃縮儲液。根據樣品中目的生物標志物的濃度范圍,使用未稀釋的血清樣品或用測定稀釋劑稀釋為1:2至1:1,000(通常為1:4、1:10、1:15、1:20或1:1000)的血清樣品(基于歷史結果)。例如,對于1:2稀釋,將120μl來自主要單元的血清加入到稀釋單元中的120μl測定稀釋劑中。如果第一濃度需要,標準溶液以1:10稀釋,然后通過在校準稀釋劑中進行1:2系列稀釋制備標準曲線。通常,對于低濃度標志物,標準曲線以50、20、10、5、2或1納克/毫升(ng/ml)開始,但是如果標志物在血清中是高濃度的,可以高達0.8、2.5或5微克/毫升(μg/ml)開始。hi和loqc對照與血清樣品相似地稀釋,或者有時由于qc對照的儲液濃度而接受較低的稀釋。通過將純化的蛋白質摻入正常或合成血清來建立qc對照,使得qc對照的od處于或接近標準曲線上的第二或第五點。
elisa操作方案。將用針對目的標志物的捕獲抗體預包被的測定板用模板編號標記,標志物標記為“tx-marker”用于跟蹤。在加入樣品之前,用50或100μl測定稀釋劑填充測定板。如上述模板所示,將樣品和標準曲線樣品加入板中。用膠條覆蓋板,并在室溫或37℃(取決于測試的標志物)孵育1、2或3小時。然后在板洗滌器上洗滌板,用每次300-400μl洗滌緩沖劑洗滌3-6次,然后在紙巾上吸干。將50至200μl針對測定稀釋劑中的目的抗原的hrp綴合的二抗加入到整個板中,用膠條覆蓋,并且取決于測試的標志物在室溫或37℃下孵育30分鐘至2小時。再次用每次300-400μl洗滌緩沖劑洗滌3-6次,然后在紙巾上吸干。在洗滌的同時,將雙組分tmb試劑(即3,3',5,5'-四甲基聯苯胺)混合在一起(等體積的兩種試劑),并將100至200μl的該試劑加入板中。取決于測試的標志物,將平板在黑暗中孵育5至28分鐘。在該孵育結束時,向整個平板中加入50μl1n硫酸以終止hrp(即辣根過氧化物酶)酶促反應。在分光光度計上在450nm讀取平板(減去570nm讀數)。
數據計算、接受和重新測試
標志物濃度的計算。使用預格式化操作方案在
測定接受標準。標準曲線的決定系數可以為r2≥0.95。使用3s控制圖隨時間跟蹤hi和loqc對照值。qc對照結果可用于警告技術團隊,額外的審查可能是適當的。標準曲線或qc對照中的任何其他變異性(邊緣效應、從左至右的變異等)由統計學家評估并在研究報告中報告。
樣品接受標準。在將其用于計算重復的總標準偏差之前,將對數轉換應用于所有標準曲線測量。去除超過4個標準偏差(sd)的任何個體測量,并且使用未排除的點計算每個濃度的平均值。
樣品再測試。如果樣品平均濃度不在標準曲線的可定量范圍內,則用必要的稀釋度變化重新測試樣品。示例性數據參見圖1和圖2。
前述內容僅僅示出了本公開的原理。應當理解,本領域技術人員將能夠設計出盡管在本文中沒有明確描述或示出但體現本公開的原理并且包括在其精神和范圍內的各種布置。此外,本文的所有實例和條件語言主要旨在幫助讀者理解本公開的原理,并且應被解釋為不限于這些具體敘述的實例和條件。此外,本文中記載原理、情況和本公開的情況以及其具體實例的所有陳述旨在包括其結構和功能等同物。另外,這樣的等同物包括當前已知的等同物和將來開發的等同物,即,開發的執行相同功能的任何元件,而不管結構如何。因此,本公開的范圍不旨在限于本文示出和描述的示例性情況。相反,本公開的范圍和精神由所附權利要求體現。
盡管本文已經示出和描述了本公開的優選情況,但是對于本領域技術人員來說顯而易見的是,這些情況僅以示例的方式提供。在不脫離本公開的情況下,本領域技術人員將想到許多變異、變化和替換。應當理解,在實踐本公開時可以采用對本文所述的本公開的情況的各種替代。意圖是所附權利要求限定本公開的范圍,并且由此涵蓋這些權利要求及其等同物的范圍內的方法和結構。
表2:各種pe生物標志物的列表。
腎素(ren)、人絨毛膜促性腺激素(hcg)、甲胎蛋白(afp)、抑制素a(inha)、激活蛋白a(inhba)、性激素結合球蛋白(shbg)、脂連蛋白(adipoq)、抗凝血酶iii(serpinc1)纖溶酶原激活物抑制劑-1(pai-1/serpine1)、纖溶酶原激活物抑制劑-2(pai-2/serpinb2)、載脂蛋白a-i(apoa1)、載脂蛋白b-100(apo)、載脂蛋白c-ii(apoc2)、載脂蛋白ciii(apoc3)、載脂蛋白e(apoe)、內皮肽(edn)、前列環素、血栓烷、胎盤生長因子-1(plgf-1)、胎盤生長因子-2(plgf-2)、胎盤生長因子-3(plgf-3)、血管內皮生長因子(vegf)、fms樣酪氨酸激酶(flt1)、可溶性fms樣酪氨酸激酶(sflt1)、血管內皮生長因子受體3(flt4)、內皮聯蛋白(eng)、可溶內皮聯蛋白(seng)、含有內皮pas結構域蛋白1(epas1)、神經激肽b、金屬肽酶抑制劑1(timp1)、金屬肽酶抑制劑(timp2)、金屬肽酶抑制劑3(timp3)、血管生成素2(angpt2)、飾膠蛋白聚糖(dcn)、肝寧結合egf樣生長因子(hbegf)、阿米洛利結合蛋白-1(abp1)、溶質載體家族21(前列腺素轉運蛋白)成員2(slc21a2)、palladin(kiaa0992)、脂蛋白脂肪酶(lpl)、胰島素樣生長因子結合蛋白復合酸不穩定亞基(igfals)、含硒蛋白質p(sepp1)、巰基氧化酶1(qsox1)、過氧化物氧還蛋白-1(prdx1)、過氧化物氧還蛋白-2(prdx2)、溶酶體原x羧肽酶(prcp)、亮氨酰-半胱氨酰氨肽酶(lnpep)、生腱蛋白-x(tnxb)、基底膜特異性硫酸乙酰肝素蛋白聚糖核心蛋白(hspg2)、細胞表面糖蛋白muc18(mcam)、磷脂酰肌醇-聚糖特異性磷脂酶d(gpld1)、kunitz型絲氨酸蛋白酶抑制劑1(spint1)、g蛋白偶聯受體126(gpr126)、c反應蛋白(crp)、磷脂酰膽堿-固醇酰基轉移酶(lcat)、robo同源物4(robo4)、胞外核苷酸焦磷酸酶/磷酸二酯酶家族成員2(enpp2)、蛋白s100-a9(s100-a9)、脂肪酸結合蛋白4(fabp4)、烯脂酰輔酶a水合酶(echs1)、δ3,5-δ2,4-二烯脂酰輔酶a異構酶(ech1)、過氧化物酶6(per6)、熱休克蛋白β-1(hsp27)、抑微管裝配蛋白(stmn)、膜聯蛋白a1(anxa)、膜聯蛋白a2(anxa2)、膜聯蛋白a4(anxa4)、前列腺素脫氫酶1(hpgd)、增殖相關蛋白2g4(pa2g4)、雌二醇17-β-脫氫酶(hsd17)、巨噬細胞加帽蛋白(capg)、缺氧誘導因子1-α(hif1a)、伴侶蛋白(cpn)、er-60蛋白酶、異檸檬酸脫氫酶1(idh1)、醛還原酶1(akr1b1)、結合至人醛糖還原酶的fidaresta鏈b、電壓依賴性陰離子選擇性通道蛋白1(vdac1)、核氯通道(nuclearcholoridechannel)、磷酸甘油酸變位酶1(pgam1)、內質網蛋白、蛋白酶體亞基α2型(psma2)、谷胱甘肽-s-轉移酶(gst)、ig重鏈v區、平滑肌肌球蛋白堿性輕鏈、腫瘤壞死因子α(tnf)、巨噬細胞集落刺激因子(m-csf)、粒細胞集落刺激因子(g-csf)、粒細胞-巨噬細胞集落刺激因子(gm-csf)、成纖維細胞生長因子(fgf)、松弛素h2(rln2)、含有ferm和pdz結構域的蛋白4(frmpd4)、生長抑素(sst)、光感受器間基質蛋白聚糖1(impg1)、c-x-c基序趨化因子9(cxcl9)、c-x-c基序趨化因子11(cxcl11)、羥基-δ-5類固醇脫氫酶3-β和類固醇δ-異構酶2(hsd3b2)、分配缺陷6同源物β(pard6b)、膽汁鹽輸出泵(abcb11)、穿膜4-結構域亞家族a成員3(ms4a3)、loc196993、bestrophin(best1)、糖基-磷脂酰肌醇錨定分子樣蛋白(gml)、細胞分裂周期2樣5(cdc2l5)、甘氨酸受體α1(glra1)、二氫嘧啶酶相關蛋白4(dpysl4)、κ型類阿片受體(oprk1)、二甲基精氨酸二甲基氨基水解酶1(ddah1)、同源異型框蛋白hox-a4(hoxa4)、同源異型框蛋白hox-a7(hoxa7)、同源異型框蛋白hox-b5(hoxb5)、促甲狀腺素釋放激素受體(trhr)、核轉換蛋白2(tnp2)、血管加壓素、胎盤蛋白13(pp13)、嗜中性粒細胞明膠酶相關脂質運載蛋白(lcn2)、干擾素γ誘導蛋白-10(ip-10)、單核細胞趨化蛋白-1(mcp-1)、細胞內粘附分子-1(icam-1)、細胞內粘附分子-3(icam-3)、血管細胞粘附分子-1(vcam-1)、白細胞介素-1(il-1)、白細胞介素-2(il-2)、白細胞介素-3(il-3)、白細胞介素-4(il-4)、白細胞介素-5(il-5)、白細胞介素-6(il-6)、白細胞介素-7(il-7)、白細胞介素-8(il-8)、白細胞介素-9(il-9)、白細胞介素-10(il-10)、白細胞介素-11(il-11)、白細胞介素-12(il-12)、白細胞介素13(il-13)、白細胞介素-27亞基β(ebi3)、凝集素、血小板衍生生長因子(pdgf)、基質金屬蛋白酶-2(mmp-2)、基質金屬蛋白酶-9(mmp-9)、基質金屬蛋白酶-12(mmp12)、基質金屬蛋白酶-23a(mifr)、基質金屬蛋白酶-23b(mifr-2)、血纖蛋白原、血纖蛋白原α(fga)、纖連蛋白-1(fn1)、蛋白s(pros1)、蛋白c(proc)、皮卡丘素(egflam)、血色素結合蛋白(hpx)、adam金屬肽酶結構域2(adam2)、adamts3、adam金屬肽酶結構域12(adam12)、adam金屬肽酶結構域12短同種型(adam12-s)、adam金屬肽酶結構域12長同種型(adam12-l)、觸珠蛋白(hp)、血清-α2-巨球蛋白(a2m)、視黃醇結合蛋白4、小誘導型細胞因子a2(ccl2)、c-c基序趨化因子5(ccl5)、組織蛋白酶b(ctsb)、組織蛋白酶c(ctsc)、組織蛋白酶d鏈h(ctsd)、血紅素加氧酶-1(hmox1)、胰島素樣生長因子結合蛋白1(igfbp1)、胰島素樣生長因子結合蛋白2(igfbp2)、胰島素樣生長因子結合蛋白-3(igfbp3)、胰島素樣生長因子結合蛋白-5(igfbp5)、胰島素樣生長因子結合蛋白-7(igfbp7)、胰島素樣生長因子-1(igf-1)、角蛋白4(krt4)、角蛋白16(krt16)、角蛋白19(krt19)、角蛋白33a(krt33a)、角蛋白40(krt40)、原血小板堿性蛋白(ppbp)、脂滴包被蛋白2(plin2)、激肽原-1(kng1)、絨毛膜促性腺激素亞基β(cgb)、半胱氨酸蛋白酶抑制劑c(cst3)、pappalysin-1(pappa1)、pappalysin-2(pappa2)、α-1b-糖蛋白(a1bg)、肌動蛋白(actb)、c4b結合蛋白β鏈(c4bp)、膽堿酯酶(bche)、絨毛膜生長催乳素激素(csh1)、凝血因子vii(f7)、凝血因子xi(f11)、細絲蛋白a(flna)、細絲蛋白b(flnb)、肝素輔因子2(hcii)、肝細胞生長因子樣蛋白(mst1)、富含組氨酸的糖蛋白(hrg)、層粘連蛋白亞基β-1(lamb1)、脂多糖結合蛋白(lbp)、絲束蛋白-2(lcp1)、組裝抑制蛋白-1(pfn1)、妊娠特異性β-1-糖蛋白(psg1)、妊娠特異性β-4-糖蛋白(psg4)、妊娠特異性β-11-糖蛋白(psg11)、受體型酪氨酸蛋白磷酸酶γ前體(ptprg)、妊娠區蛋白(pzp)、sh3結構域結合富含谷氨酸樣蛋白3(sh3bgrl3)、轉膠蛋白-2(tagln2)、踝蛋白-1(tln-1)、原肌球蛋白α-4鏈(tpm4)、vasorin(vsn)、黏著斑蛋白(vcl)、馮·維勒布蘭德因子(vwf)、鐵蛋白(ft)、鐵蛋白輕鏈、血紅蛋白(hb)、血紅素、podocin(nphs2)、nephrin(nphs1)、足萼糖蛋白(podxl)、synaptopodin(synpo)、瘦蛋白(lep)、促卵泡激素抑釋素樣3蛋白(fstl3)、β致育蛋白(ftnb)、cd33l、中性營養(neutrotrophic)酪氨酸激酶受體2(trkb)、β葡糖苷酶(bgl)、血管生成蛋白(ang)、白細胞相關ig樣受體分泌蛋白(lair)、紅細胞分化蛋白、脂肪形成抑制因子(il-11)、促腎上腺皮質激素釋放因子結合蛋白(crhbp)、α1-抗胰凝乳蛋白酶(serpina3)、細胞因子受體樣因子1(crlf1)、賴氨酰羥化酶同種型2(lh2)、斯坦尼鈣調節蛋白前體(stc)、分泌型卷曲相關蛋白(sfrp)、半乳凝素-3(lgals3)、α中性粒細胞防御素1(defa1)、膽囊收縮素前體(cck)、干擾素刺激的t細胞α化學引誘物(i-tac)、azurocidin(hbp)、精胺氧化酶(smox)、udp糖基轉移酶2家族多肽b28(ugt2b28)、中性內肽酶(nep)、cdc28蛋白激酶調節亞基2(ckshs2)、羊毛甾醇合酶(lss)、鈣/鈣調蛋白依賴性絲氨酸蛋白激酶(cask)、趨化因子(cx3c基序)受體1(cx3cr1)、酪氨酸酶相關蛋白1(tyrp1)、羥基-δ-5-類固醇脫氫酶(hsd3)、細胞色素p450家族11(cyp11)、細胞色素p450家族11亞家族a多肽1(cyp11a1)、細胞色素p450家族11亞家族b多肽1(cyp11b1)、細胞色素p4501a1(cyp1a1)、冠蛋白-2a(coro2a)、細胞色素p4502j2(cyp2j2)、paralemmin(palm)、甘油醛-3-磷酸脫氫酶(gapd)、atp結合盒亞家族a成員12(abca12)、轉錄因子eb(tfeb)、轉錄因子iie(tfiie)、突觸融合蛋白結合蛋白5樣(stxbp5l)、鳥苷肽(guca2a)、核糖體蛋白s6激酶α-2(rps6ka2)、蛋白磷酸酶1調節亞基16b(ppp1r16b)、b類堿性螺旋環螺旋蛋白2(bhlhb2)、血型糖蛋白e(gype)、星云狀小體(nebl)、富含亮氨酸的重復和免疫球蛋白樣結構域蛋白1(lrig1)、葡糖轉運蛋白3(glut3)、udp-葡糖醛酸基轉移酶2b28(ugt2b28)、核受體亞家族5組a成員2(nr5a2)、neuronatin(nnat)、鈉依賴性和氯依賴性肌酸轉運蛋白1(slc6a8)、受體酪氨酸蛋白激酶erbb-2(erbb2)、受體酪氨酸蛋白激酶erbb-3(erbb3)、唾液酸結合ig樣凝集素6(siglec6)、shc轉化蛋白3(shc3)、neurexophilin4(nxph4)、淋巴細胞抗原6d(ly6d)、前列環素合酶(ptgis)、atp依賴性rna解旋酶ddx51(ddx51)、traf3相互作用蛋白1(traf3ip1)、滋養層糖蛋白(tpbg)、轉化生長因子β3(tgfb3)、細胞周期蛋白b1(ccnb1)、驅動蛋白家族成員17(kif17)、n-myc下游介導基因1(ndrg1)、染色質的swi/snf相關的基質相關的肌動蛋白依賴調節子亞家族d成員3(smarcd3)、絲氨酸/蘇氨酸蛋白激酶chk2(chek2)、雙調蛋白(areg)、次要組織相容性抗原ha-1(ha-1)、pou結構域4類轉錄因子1(pou4f1)、前列腺干細胞抗原(psca)、膠原α-1(x)鏈(col10a1)、膠原α-3(vi)鏈(col6a3)、膠原α-3(ix)鏈(col9a3)、配對盒基因2(pax2)、配對盒基因4(pax4)、配對盒基因7(pax7)、蛛毒素受體(latrophilin)3(lphn3)、膽汁酸受體(nr1h4)、空的氣門(emptyspiracles)同源物1(emx1)、橋粒黏蛋白3(dsg3)、dna結合蛋白ikaros(znfn1a1)、黑素瘤相關抗原5(magea5)、黑色素瘤相關抗原3(magea3)、afadin和α-輔肌動蛋白結合蛋白(ssx2ip)、含有wd重復的蛋白21(wdr21)、2型食欲肽受體(hcrtr2)、nkg2-d型ii膜內在蛋白(klrk1)、hlaii類組織相容性抗原dpα1鏈(hla-dpa1)、hlaii類組織相容性抗原dpβ1鏈(hla-dpb1)、hlaii類組織相容性抗原drα鏈(hla-dra)、hlai類組織相容性抗原α鏈g(hla-g)、外周髓鞘型蛋白質2(pmp2)、鳥嘌呤核苷酸結合蛋白g(o)亞基α(gnao1)、電壓依賴性l型鈣通道亞基β-2(cacnb2)、c-jun-氨基末端激酶相互作用蛋白2(mapk8ip2)、p抗原家族成員1(page1)、gaba受體亞基β-1(gabrb1)、鈉和氯依賴性甜菜堿轉運蛋白(slc6a12)、乳凝集素(mfge8)、整合素α-l(itgal)、橋粒膠蛋白1a/1b(dsc1)、絨毛蛋白2(vil2)、網蛋白1(plec)、錨蛋白1(ank1)、波形蛋白(vim)、骨橋蛋白(spp1)、發動蛋白2(dnm2)、肌鈣黏著蛋白(cdh15)、驅動蛋白重鏈、脂肪酸合酶(fasn)、α內收蛋白(add1)、nadh-細胞色素b5還原酶(cyb5r)、二氫葉酸還原酶(dhfr)、adp-核糖基化因子樣蛋白3(arl3)、二
精氨酸血管加壓素;
和肽素;
干擾素-γ;
tnf-α;
il-10;
il-4;
β淀粉樣蛋白;
干擾素誘導型蛋白6-16;
白蛋白;
serpina1;
血漿銅藍蛋白;和
免疫球蛋白游離輕鏈
上述生物實體的同種型也被認為是生物標志物。
此類同種型包括例如sflt-2、sflt-4和sflt-5。
其他同種型包括fngenbank登錄號nm_212474.1)、fggenbank登錄號nm_000508.3(fga)和genbank登錄號nm_005141.4(fgb)、papp-a例如genbank登錄號nm_002581.3)、hpxgenbank登錄號nm_000613.2);adam12genbank登錄號nm_003474.4(同種型1)、nm_021641.3(同種型2);sflt-1例如genbank登錄號nm_001159920.1(同種型2)、nm_00160030.1(同種型3)和nm_001160031.1(同種型4));p1gf例如genbank登錄號nm_002632.5(同種型1)和nm_001207012.1(同種型2))。
在本文中被檢測試劑(例如抗體)識別的pe生物標志物的片段或部分也被認為是pe生物標志物。
- 還沒有人留言評論。精彩留言會獲得點贊!