用于紫杉醇的藥代動力學引導給藥的監測血漿中的紫杉醇濃度的方法、裝置和試劑與流程
本申請要求2014年4月4日提交的美國專利申請No.61/975,386和2014年9月17日提交的美國專利申請No.62/051,757的權益,每個申請明確地通過引用整體并入本文。
關于序列表的聲明
與本申請相關聯的序列表以文本格式代替紙質拷貝提供,并在此通過引用并入說明書中。包含序列表的文本文件的名稱為53634_SEQ.txt。文本文件為11KB;創建于2015年4月6日;并通過EFS-Web與本說明書的提交一起提交。
發明背景
最初從太平洋紫杉樹的樹皮中分離的紫杉醇已被建立為用于一系列癌癥類型(包括肺癌、卵巢癌和乳腺癌)的最有效的化療藥物之一。紫杉醇的主要限制是其低溶解度和需要配制在有毒有機溶劑(通常為聚氧乙烯化蓖麻油和脫水乙醇混合物(稱為))中。為了防止溶劑毒性,已將紫杉醇與多種賦形劑一起配制以及使用可提高疏水性藥物諸如紫杉醇的溶解度的納米顆粒遞送系統。
(紫杉醇白蛋白結合的納米顆粒制劑)在2005年被FDA批準并且是目前用于化療的紫杉醇的最佳制劑之一。其它系統已被研究用于遞送紫杉醇或正在開發中,例如使用聚合物納米顆粒、基于脂質的納米顆粒制劑、聚合物綴合物、無機納米顆粒、碳納米管、納米晶體或環糊精納米顆粒(參見例如Ping Ma等,2013,J Nanomed.Nanotechnology:4:2)。
盡管是廣泛使用的化療劑并且實際適用于所有癌癥類型,但是對的反應可低至20%。在一些患者中發現的對紫杉醇的相對不敏感性可能是低反應率的促成因素。然而,這種不敏感性可能不是低反應率的主要原因。當以各種批準的劑量(260mg/m2用于轉移性乳腺癌,125mg/m2用于胰腺癌,和100mg/m2用于肺癌)給藥時,在臨床患者樣品中監測的紫杉醇的血液濃度存在高達10倍的變化(Nyman DW等,2005,J Clin.Oncol.23,7785-93)。這種變化表明絕大多數患者可能被以太大濃度的紫杉醇施用而不正確地給藥并必須取消治療,或者施用的劑量太低從而不能從治療提供益處。即使患者對紫杉醇敏感,藥物水平不足也會使其無反應從而治療無效。低劑量組是最脆弱的患者群體,因為難以確定他們是對紫杉醇不敏感還是沒有施用足夠的紫杉醇。完全藥代動力學(PK)分析是在這種情況下的唯一方法來基于個體藥代動力學變化提供適當藥物劑量的指導。
目前沒有可用的方法來進行紫杉醇的完全PK定量而無需讓患者參加全面的臨床測試(這需要住院)。這種PK測試的典型持續時間可以是48小時的時間過程并且包括重復抽血。目前,需要使用復雜的實驗室設備來分析紫杉醇的血液濃度,包括液相色譜/質譜(LC/MS)方法。這些方法非常昂貴,目前超過120美元/樣本,設備成本在每臺儀器超過150K美元至200K美元的范圍內。還已經證明,需要在48至72小時的時間段內收集最少四個數據點以充分表征每個特定患者的PK參數。讓患者住院進行PK測試可以很容易地將每個患者的成本提高至大約10,000美元。用于證明PK引導給藥的臨床療效的充分有力的III期臨床試驗將需要500名患者(250名患者用于BSA給藥,250名患者用于PK引導給藥)。單獨的生物分析成本將為150萬美元(500個點×6個周期的化療×4個用于PK分析的血液采樣×120美元/樣品分析)。試驗的其它組成部分對每名患者的費用大約為10萬美元,總額為5000萬美元。這代表了獲得指導劑量調整以實現最佳的腫瘤反應和裝置的監管批準所必需的有意義的臨床數據的重要障礙。因此,分析和儀器的高成本對于針對具有相對窄的治療范圍的許多藥物建立治療藥物監測(TDM)具有令人望而止步的后果。
因此,仍然需要一種簡單、有效和廉價的方法來監測患者中紫杉醇的藥代動力學,從而通過為給藥策略的任何調整提供信息來適當地個性化對個體患者的治療。本發明尋求滿足這種需要并提供另外的相關優勢。
發明概述
本發明提供了用于測定治療劑的方法、裝置和組合物。在一個方面,提供了用于測定紫杉醇的方法、裝置和組合物。
在一個方面,本發明提供了用于測定液體樣品中的紫杉醇的方法。在一個實施方案中,所述方法包括:
(a)將包含紫杉醇的液體樣品施加到側流測定裝置,所述裝置包含
(i)用于接收液體樣品的樣品接收區;
(ii)檢測試劑區,其與所述樣品接收區液體連通并且按流動方向位于所述樣品接收區的下游,
其中所述檢測試劑區包含沉積在其上的檢測試劑,
其中所述檢測試劑是用可檢測的報告基團標記的結合紫杉醇的紫杉醇抗體或其片段或衍生物,并且
其中所述紫杉醇抗體或其片段或衍生物具有約104至約107的Kon和約10-3至約10-7的Koff;和
(iii)捕獲區,其與所述檢測試劑區液體連通,并按流動方向位于所述檢測試劑區的下游,
其中所述捕獲區包含固定在其上的第一和第二捕獲試劑,
其中所述第一捕獲試劑是能夠結合所述檢測試劑的紫杉醇材料(測試線),
其中所述第二捕獲試劑是能夠結合所述檢測試劑的抗體(對照線),
其中所述第一捕獲試劑按流動方向定位在所述捕獲區的上游端的下游的第一距離處,
其中所述第二捕獲試劑按流動方向定位在所述捕獲區的上游端的下游的第二距離處,
其中所述第二距離大于所述第一距離,以及
其中當Kon大于約2.0×105且Koff小于約1.0×10-3時,第一距離與第二距離的比率為約0.0至約0.4,以及
其中當Kon大于約2.0×104且Koff小于約2.0×10-4時,第一距離與第二距離的比率為約0.2至約1.0;以及
(b)使樣品從樣品接收區流動通過檢測試劑區以提供具有紫杉醇的檢測試劑;
(c)使具有紫杉醇的檢測試劑流過捕獲區,
由此第一捕獲試劑(測試線)與分析物(紫杉醇)競爭結合檢測試劑,和
由此第二捕獲試劑(對照線)結合過量的檢測試劑;以及
(d)觀察結合至第一捕獲試劑(測試線)相對于第二捕獲試劑(對照線)的檢測試劑的量。
在某些實施方案中,所述方法還包括通過定量結合至第一捕獲試劑的檢測試劑的量來測定樣品中紫杉醇的量。定量結合至第一捕獲試劑的檢測試劑的量可以包括光密度測量。
在一個實施方案中,紫杉醇抗體是3C6。在另一個實施方案中,紫杉醇抗體是8A10。在某些實施方案中,使用結合紫杉醇的兩種紫杉醇抗體或其片段或衍生物(例如3C6和8A10)。
在該方法中,紫杉醇材料是與紫杉醇競爭結合檢測試劑的紫杉醇抗原。在一個實施方案中,紫杉醇材料是紫杉醇蛋白質綴合物。
在本發明的方法中,樣品接收區與第一捕獲試劑之間的距離可改變,以優化紫杉醇檢測靈敏度。在某些實施方案中,使樣品接收區與第一捕獲試劑之間的距離最小化,以優化紫杉醇檢測靈敏度。
在某些實施方案中,所述方法還包括觀察結合至第二捕獲試劑(對照線)的過量檢測試劑的量。在這些實施方案中,所述方法還可包括通過定量結合至第二捕獲試劑的檢測試劑的量來測定樣品中紫杉醇的量。
為了增加靈敏度和動態范圍,該方法可進一步包括在第一與第二捕獲區之間的第三捕獲區,其中第三捕獲區包含能夠結合檢測試劑的紫杉醇材料。在這些實施方案中,可以通過定量結合至第三捕獲試劑的檢測試劑的量來測定紫杉醇的量。定量結合至第三捕獲試劑的檢測試劑的量可以包括光密度測量。
應當理解,本發明的方法適用于其它固相測定,包括例如表面等離子體共振(SPR)測定。
如上所述,在該方法中可以使用不止一種抗體、其片段或衍生物。在這些實施方案中,第一抗體可以具有相對高的Kon(例如大于1×104),并且第二抗體可以具有相對低的Koff(例如,小于1×10-3)。
此外,在某些實施方案中,捕獲區可包括多個捕獲位置(例如,兩條或三條線,T1、T2、T3),以在相同樣品上提供多個讀數,從而允許增加的重現性和擴展的動態范圍。
在另一個方面,本發明提供了用于治療藥物監測(TDM)引導的紫杉醇療法的方法。在一個實施方案中,本發明提供了用于監測紫杉醇療法在經診斷患有癌癥的患者中的功效的方法,包括:
(a)在第一時間點用紫杉醇治療癌癥患者;
(b)在第一時間點測定患者中紫杉醇的第一濃度,其中測定濃度包括上述用于測定紫杉醇的方法;
(c)在第二時間點用紫杉醇治療所述患者;
(d)在第二時間點測定患者中紫杉醇藥物的第二濃度,其中測定濃度包括上述用于測定紫杉醇的方法;和
(e)比較患者中紫杉醇的第一和第二濃度以測定癌癥治療的功效。
在相關實施方案中,本發明提供了用于在經診斷患有癌癥的患者中進行紫杉醇療法的PK引導給藥的方法,包括:
(a)在第一時間點用紫杉醇治療癌癥患者;
在第一時間點測定所述患者中紫杉醇的一個或多個藥代動力學參數,其中測定所述一個或多個藥代動力學參數包括上述用于測定紫杉醇的方法;
(b)使用來自第一次給藥的PK信息在第二時間點用紫杉醇治療所述患者;
(c)在第二時間點測定患者中紫杉醇的一個或多個藥代動力學參數,其中測定所述一個或多個藥代動力學參數包括上述用于測定紫杉醇的方法;和
(d)將所述受試者中的紫杉醇在第一時間點的一個或多個藥代動力學參數與在第二時間點的水平進行比較,以確認實現了適當的給藥。
在某些實施方案中,藥代動力學參數選自達到最大濃度的時間(Tmax)、濃度最大值(Cmax)、曲線下面積(AUC)、清除率(CL)、分布體積(Vd)、在末期期間的表觀分布體積(Vz)、在穩態期間的表觀分布體積(Vss)及其組合。
在其它方面,本發明提供了類似于上文中針對紫杉醇所述的那些但可用于測定其它治療劑的裝置和方法。
在一個實施方案中,本發明提供了側流裝置,其包含:
(a)用于接收液體樣品的樣品接收區;
(b)檢測試劑區,其與所述樣品接收區液體連通并且按流動方向位于所述樣品接收區的下游,
其中所述檢測試劑區包含沉積在其上的一種或多種檢測試劑;
(c)捕獲區,其與所述檢測試劑區液體連通,并且按流動方向位于所述檢測試劑區的下游,
其中所述捕獲區包含固定在其上的一種或多種捕獲試劑;和
(d)吸收區,其與捕獲區液體連通并按流動方向位于所述捕獲試劑區的下游。
如上所述,在該方法中可以使用不止一種抗體、其片段或衍生物。在這些實施方案中,第一抗體可以具有相對高的Kon(例如,大于1×104),并且第二抗體可以具有相對低的Koff(例如,小于1×10-3)。在一個實施方案中,檢測試劑包含對治療藥物具有第一親和力的第一抗體和對治療藥物具有第二親和力的第二抗體,其中第一親和力大于第二親和力。此外,在某些實施方案中,捕獲區可包括多個捕獲位置(例如,兩條或三條線,T1、T2、T3),以在相同樣品上提供多個讀數,從而允許增加的重現性和擴展的動態范圍。
在該方法中,檢測試劑是用可檢測報告基團標記的抗體,并且捕獲試劑是與治療藥物競爭結合檢測試劑的抗原,或捕獲試劑是能夠結合檢測試劑的抗體。在某些實施方案中,捕獲試劑包含第一捕獲試劑和第二捕獲試劑,所述第一捕獲試劑是與治療藥物競爭結合檢測試劑的抗原,所述第二捕獲試劑是能夠結合檢測試劑的抗體。第一捕獲試劑被固定在按流動方向第二捕獲試劑的上游。可改變樣品接收區與第一捕獲試劑之間的距離,以優化治療藥物的檢測。
在某些實施方案中,該裝置還包括固定在第一與第二捕獲試劑之間的第三捕獲試劑。在該實施方案中,第三捕獲試劑是與治療藥物競爭結合檢測試劑的抗原。
在某些實施方案中,治療劑是紫杉醇,并且檢測試劑包含選自8A10和3C6的單克隆抗體或其片段或衍生物,其中抗體或片段或衍生物結合紫杉醇。
在另一個實施方案中,本發明提供了用于測定樣品中的治療藥物的方法,其包括:
(a)將樣品施加到上述裝置的樣品接收區;和
(b)觀察結合至一種或多種固定的捕獲試劑的檢測試劑的量。
該方法還可包括通過定量結合至一種或多種固定的捕獲試劑的檢測試劑(例如,檢測試劑結合至第一捕獲位置中的捕獲試劑,檢測試劑結合至第二捕獲位置中的捕獲試劑,檢測試劑結合至第一和第二捕獲位置中的捕獲試劑,檢測試劑結合至第一、第二和第三捕獲位置中的捕獲試劑)的量來測定樣品中的治療藥物的量。
在另外的實施方案中,提供了TDM引導的治療方法。
在一個實施方案中,本發明提供了用于監測經診斷患有疾病或病癥的患者中治療性治療的功效的方法,其包括:
(a)在第一時間點用治療劑治療患者;
(b)在第一時間點測定所述患者中治療劑的第一濃度,其中測定濃度包括本文所述的方法;
(c)在第二時間點用所述治療劑治療所述患者;
(d)在第二時間點測定患者中治療劑的第二濃度,其中測定濃度包括本文所述的方法;和
(e)比較患者中的第一與第二濃度以測定治療性治療的功效。
在另一個實施方案中,本發明提供了用于在經診斷患有疾病或病癥的患者中進行治療性治療的PK-引導給藥的方法,其包括:
(a)使用來自第一給藥的PK信息在第一時間點用治療劑治療所述患者;
(b)在第一時間點測定所述患者中所述治療劑的一個或多個藥代動力學參數,其中測定一個或多個藥代動力學參數包括根據本文所述的方法測定所述治療劑;
(c)在第二時間點用所述治療劑治療所述患者;
(d)在第二時間點測定所述患者中所述治療劑的一個或多個藥代動力學參數,其中測定一個或多個藥代動力學參數包括根據本文所述的方法測定所述治療劑;和
(e)將受試者中所述治療劑在第一時間點的一個或多個藥代動力學參數與在第二時間點的水平進行比較,以確認實現了適當的給藥。
在某些實施方案中,藥代動力學參數是達到最大濃度的時間(Tmax)、濃度最大值(Cmax)、曲線下面積(AUC)、清除率(CL)、分布體積(Vd)、在末期期間的表觀分布體積(Vz)、在穩態期間的表觀分布體積(Vss)及其組合中的一個或多個。
上述方法適用于受益于治療藥物監測的疾病或病癥治療。代表性疾病或病癥包括癌癥、炎癥、高血壓、心血管病和疼痛。代表性治療劑包括紫杉醇、多西他賽、7-表紫杉醇、t-乙酰基紫杉醇、10-去乙酰基紫杉醇、10-去乙酰基-7-表紫杉醇、7-木糖基紫杉醇、10-去乙酰基-7-戊二酰基紫杉醇、7-N,N-二甲基甘氨酰紫杉醇和7-L-丙氨酰紫杉醇。
在其它方面,本發明提供了紫杉醇抗體。在一個實施方案中,本發明提供了選自8A10和3C6的單克隆抗體或其片段或衍生物,其中所述抗體、抗體片段或抗體衍生物結合紫杉醇。在某些實施方案中,單克隆抗體、抗體片段或抗體衍生物包含一個或多個與SEQ ID NO:2、4、6或8中包含的CDR具有至少95%同源性的互補決定區(CDR)。
附圖概述
當結合附圖考慮時,本發明的前述方面和許多附帶的優勢將變得更容易理解,提供參考下文的詳細描述也同樣變得更好理解。
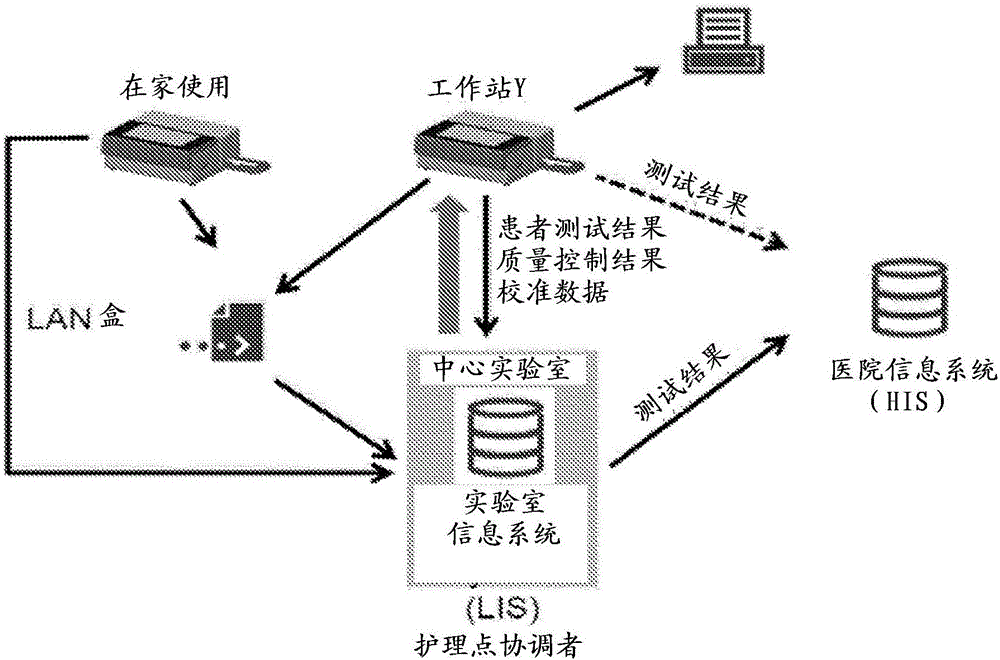
圖1是使用本發明的代表性系統和方法的藥代動力學引導給藥概念和過程的示意圖。
圖2A是根據本發明的治療藥物監測裝置的代表性工作流程的圖示。
圖2B是用于根據本發明的側流免疫測定的代表性測試條的圖示。
圖2C是根據本發明的用于紫杉醇側流免疫測定的代表性測試條的圖示。
圖3是經歷根據本發明的測定條件的代表性測試條的圖像,其中代表性分析物(紫杉醇)的量是變化的。在該測定配置中,測試條包括三個捕獲區:測試線1和測試線2顯示使用固定的抗原(呈固定的BSA-紫杉醇形式的紫杉醇)作為第一捕獲材料的捕獲;對照線顯示使用固定的抗體(山羊抗小鼠抗體,GAM)作為第二捕獲材料的捕獲。在該測定中,檢測試劑是用膠體金標記的抗紫杉醇抗體(8A10)。
圖4是說明在ELISA上本發明的完整IgG(8A10和3C6)與BSA-紫杉醇抗原的直接結合的圖。
圖5A和5B顯示了在使用如圖2C中示意性說明和如實施例3中描述的裝置進行的本發明的代表性側流測定中在T1和T2線處結合的8A10的曲線。圖5A顯示了標準曲線,即測試線與對照線(T/C)的比率相對紫杉醇濃度。對于較低濃度,8A10在T1處的比率相對T2的大差異表明當被放置得更靠近樣品端口時(其中分析物的濃度可能更高),該類抗體的靈敏度要高得多。圖5B顯示了如讀取器裝置提供的掃描的測試條的輸出強度相對于位置讀出。
圖6A和6B顯示了在使用如圖2C中示意性說明和如實施例3中描述的裝置進行的本發明的代表性側流測定中在T1和T2線處結合的3C6的曲線。圖6A示出了標準曲線,即測試線與對照線(T/C)的比率相對紫杉醇濃度。對于較低濃度,3C6在T1處的比率相對T2的相對小的差異表明對于將抗體放置得更靠近樣品端口(其中分析物的濃度可能更高),會獲得該類抗體的相對低的靈敏度改善。這類抗體的特征在于來自樣品端口的與位置無關的信號。圖6B顯示了由讀取器裝置提供的掃描的測試條的輸出強度相對于位置讀出。
圖7A和7B顯示了在使用如圖2C中示意性說明和如實施例3中描述的裝置進行的本發明的代表性側流測定中在T1和T2線處結合的組合的8A10和3C6的曲線。圖7A顯示了標準曲線,即測試線與對照線(T/C)的比率相對紫杉醇濃度。通過組合結合墊中的兩類抗體(8A10和3C6)獲得T1和T2的高靈敏度。這改善了測定的動態范圍。圖7B顯示了由讀取器裝置提供的掃描的測試條的輸出強度相對于位置讀出。
發明詳述
當今有許多治療劑處于臨床使用或開發中。困難不在于尋找治療藥物,而是在定制治療以適合患者。不考慮藥代動力學(PK)可變性的個體化醫療將導致一些患者的錯誤分類,這是由于太多的藥物暴露在假設的敏感群體中的可從較低量的施用藥物或過少的藥物暴露受益的患者中導致毒性。具有治療藥物監測(TDM)的個性化醫療消除了PK可變性,并允許根據患者的生物標志物對他們進行正確分類。
本發明提供了用于治療藥物的藥物動力學(PK)-引導給藥的護理點(point-of-care,POC)治療藥物監測(TDM)方法、裝置和相關組合物。
圖1顯示了具有醫院信息系統和/或實驗室信息系統并使得能夠將數據傳送給醫生,最終支持藥物劑量決定的裝置的系統特性、優勢和潛在連接性。本發明的方法和裝置通過在24至48小時的時間內采集手指刺血樣品收集患者的治療藥物(例如,紫杉醇)PK數據,并且PK數據由醫生訪問,所述醫生可以分析數據并確定是否應該修改治療藥物劑量。
在一個方面,本發明提供了用于一般性的免疫測定的方法和裝置,以及特別地用于紫杉醇的免疫測定的方法和裝置。一些時候,生物樣品中低水平的紫杉醇表明需要向受試者增加紫杉醇的劑量,并且生物樣品中高水平的紫杉醇表明需要降低給予受試者的紫杉醇的劑量。本發明的方法和裝置提供了可用于調整受試者的治療方案的信息。
在用于檢測和監測紫杉醇的組合物、方法和裝置的上下文中描述了本文提供的測定方法和裝置。然而,應當理解,所述組合物、方法和裝置的形式不限于此,并且容易更廣泛地應用于監測所選擇的任何分析物。
代表性測定方法和裝置
本發明提供了用于檢測或定量樣品中的分析物(例如,紫杉醇)的測定方法和裝置。
所述方法和裝置可用于測定生物樣品,諸如從已接受治療劑(例如,紫杉醇)以治療病癥的受試者(患者)獲得的樣品。在測定中使用的樣品最終是液體樣品(例如,血液、血漿、尿)。
本發明的方法是固相測定,因此適合于適應其它固相測定配置。為了舉例說明本發明,使用側流測定配置描述所述方法和裝置。應當理解,本領域已知的其它固相測定可以根據本發明的方法和裝置進行配置。
可根據本發明使用側流測定方法和裝置。取決于側流測定方法和裝置的形式,可將測定試劑布置在某些配置中。在這樣的實施方案中,一種試劑將充當“檢測試劑”,另一種試劑將充當“捕獲試劑”。在該形式中,檢測試劑通常在樣品端口與沉積捕獲試劑的位置之間的位置處沉積在結合墊上。檢測試劑通常包含可檢測標記,而捕獲試劑被固定在其在墊上的位置。因此,在操作期間,引入樣品端口中的液體樣品可沿著墊流動。樣品將首先與檢測試劑接觸,然后隨后流過捕獲試劑。
在圖2A中顯示了用于根據本發明進行側流測定的代表性裝置。參考圖2A,裝置100是盒,其包括具有樣品端口120、讀取窗口130和測試條200(參見圖2B)的殼體110。在操作中,待分析的液體樣品通過端口120被引入至測試條,并且如由流動方向所指示的沿著測試條流動(從樣品墊210至吸收墊240)。測試結果可通過經由讀取窗口130觀察測試條來查看。
測試條包括用于進行測定的幾個區域和試劑。參考圖2A和2B,代表性測試條200包括樣品墊210、結合墊220、膜230和吸收墊240。樣品墊210、綴合物墊220、膜230和吸收墊240處于液體連通,以使得被引入至樣品墊的液體樣品流過或穿過結合墊和膜到達吸收墊。可以改變測試條組件的尺寸和構造以適合待執行的特定測定。例如,組件墊和膜中的一個或多個可以重疊以促進從一個組件至下一個組件的最佳流動(樣品墊210可與結合墊220重疊,結合墊220可與膜230重疊,膜230可與吸收墊240重疊,如圖2A所示)。測試帶區域的性質不是特別關鍵的,并且這些組件的材料是本領域已知的。
代表性裝置的操作描述如下。樣品墊210接收待測試的液體樣品。樣品從樣品墊流至結合墊220。
結合墊220包括一種或多種檢測試劑(例如,對待測定的樣品中的分析物具有親和力并且被標記以便于在測定中檢測抗體的抗體)。
在某些實施方案中,將單一檢測試劑沉積在結合墊上。在其它實施方案中,將兩種或更多種檢測試劑(例如,兩種不同的抗體,諸如對待測定的分析物具有不同親和力、不同Kon速率和/或不同Koff速率的第一和第二抗體)沉積在結合墊上。第一和第二親和力不相同。在一個實施方案中,第一Kon大于第二Kon。在另一個實施方案中,第二Koff大于第一Koff。在下文中在紫杉醇測定的上下文中描述的抗體親和力、Kon和Koff速率的描述和說明可適用于一般性的治療劑測定。沉積的第一和第二抗體的量可以變化并且不必相同。
沉積在結合墊220上的檢測試劑通過液體樣品移動并與樣品一起流至膜230。當分析物存在于樣品中時,一旦樣品接觸檢測試劑,分析物與檢測試劑之間的結合開始發生。檢測試劑的捕獲發生在膜230上,其中一些檢測試劑可包括結合的分析物,并且其中一些檢測試劑可不包括結合的分析物。
膜230包括至少兩個捕獲區:用于捕獲不包括結合的分析物的檢測試劑的第一捕獲區(測試線)(參見圖2A、2B和2C中的232)和用于捕獲包括結合的分析物的過量檢測試劑的第二捕獲區(對照線)(參見圖2A、2B和2C中的238)。第一捕獲區包括有效捕獲不包括結合的分析物的檢測試劑(即,游離檢測試劑)的第一捕獲材料(例如,固定的抗原)。第二捕獲區包括有效捕獲具有或不具有結合的分析物的檢測試劑的第二捕獲材料(例如,固定的抗體)。分別由第一和第二捕獲材料捕獲的檢測試劑的量將取決于樣品中存在的分析物的量。上述測定是競爭性測定,其中分析物和第一捕獲材料競爭與檢測試劑的親和力結合。樣品中存在的分析物的量越大,由第一捕獲材料捕獲的檢測試劑的量越小。由于捕獲材料的耗盡,樣品中存在的分析物的量越少,由第一捕獲材料捕獲的檢測試劑越多,因此可由第二捕獲材料捕獲的可檢測試劑越少。第一和第二捕獲線的強度比給出了用于分析物定量的最佳值。
在某些實施方案中,捕獲區包括用于捕獲不包括結合的分析物的檢測試劑的兩個或更多個第一捕獲區(例如,圖2B和2C中的232和234)。在某些實施方案中,捕獲區包括用于捕獲檢測試劑的兩個或更多個第二捕獲區(例如,圖2B中的236和238)。
側流盒的所示方法可利用任何兼容的讀取器,其具有用于檢測來自流動盒的信號的適當靈敏度以及校準和量化這樣的信號的能力。任何讀取器的有益特征可包括易于使用的特征,包括觸摸屏、集成RFID或集成條形碼讀取器,以及容易將結果輸出至諸如存儲卡或USB棒的能力。讀取器優選具有便于語言選擇中的接口的預裝軟件。讀取器優選具有高存儲容量以便于存儲多個(諸如>1000個)結果并且可儲存>100個不同的測試方法方案。讀取器可包含連接性以便于將其集成至更大的系統中,諸如通過LAN或WLAN連接性至LIS或基于云的數據存儲和管理系統。最后,多個USB端口對于額外的連接能力(諸如以便于連接至外部打印機等)是期望的。
代表性讀取器是Qiagen's Reader ESEQuantLFR(可從Qiagen,Germany商購獲得),其已被證明是用于包含本文所述的側流盒的相容的有效讀取器。該讀取器是一種小型便攜式裝置,內置可充電電池,從而可允許其在現場操作,滿足護理點(POC)裝置的要求。使用嵌入讀取器中的共焦照相機系統掃描側流盒。板載圖像分析系統與側流盒的條形碼讀取器是完全功能性的,以使得可輕松地將分析方法上傳至裝置。
檢測試劑。在某些實施方案中,檢測試劑是如本文所述的至少一種抗體、抗體片段或抗體衍生物。檢測試劑能夠結合樣品中的分析物(例如,紫杉醇),并且當檢測試劑不結合樣品中的紫杉醇時,檢測試劑結合至捕獲試劑。
檢測試劑包括可提供能夠可靠定量的可檢測信號的部分或標記。合適的部分包括在免疫測定領域中已知的提供比色、熒光、化學發光、酶或放射性信號的那些部分。代表性部分包括提供為可視的,并且可以不需要儀器來讀取(例如,產生有色部分或酶促的有色部分或酶)的可檢測信號的那些部分。通常通過對可檢測信號的儀器分析來實現定量。在一個實施方案中,檢測試劑是用膠體金標記的抗體,其可以用肉眼觀察。
金膠體從具有單分散性質的氯化金的還原產生,其具有受控且均勻的直徑,例如40nm單分散膠體。抗體通過被動吸收與膠體金結合。
如上所述,在優選的實施方案中,使用多種(即,不止一種類型)抗體、抗體片段或抗體衍生物。在一些實施方案中,將多種(不同)抗體、抗體片段或抗體衍生物組合并沉積在測試條(即,結合墊)上的相同位置。
本文描述了兩種不同的抗紫杉醇抗體3C6和8A10。3C6抗體對紫杉醇具有高度特異性,而8A10抗體對紫杉醇的特異性較低并且通常對紫杉烷類具有更廣泛的親和力。雖然兩種抗體在常規競爭性ELISA中表現相似,但令人驚訝地發現,在固相側流測定中,由8A10提供的信號通過將第一捕獲試劑(例如,T1位置)移動更靠近樣品端口而得到改善,相比之下,3C6獨立于位置(T1或T2)。靠近樣品施加的T1暴露于較高濃度的分析物,而距離樣品施加更遠的T2暴露于較低濃度的分析物。這是令人驚訝的發現,即捕獲線的最佳放置與該方法中使用的抗體的Kon和Koff值相關。3C6的可用性允許構建多線裝置,其中將高Kon抗體(例如8A10)盡可能地接近樣品起點沉積,并沿著墊沉積低Koff抗體(例如3C6)以提供第二/第三/第四等讀出。
因此,可對側流盒裝置進行各種修改以促進或賦予各種檢測特性。例如,為了擴展裝置的動態范圍,使用多種親和抗體的多測試線(T1、T2等),可擴展測定的動態范圍和/或重現性。在下文中于代表性紫杉醇測定的上下文中描述的測試條上定位捕獲試劑(T/C)的描述和說明通常適用于在本發明的測定中的捕獲試劑的定位。
在實施例1中描述了可用于本發明的測定中的代表性檢測試劑(例如,紫杉醇抗體-膠體金綴合物)的制備。
捕獲試劑。捕獲試劑用于捕獲檢測試劑,從而允許在測定中觀察和定量可檢測的信號。如上所述,測定方法和裝置包括分別固定在第一和第二捕獲區的第一和第二捕獲材料。
在一個實施方案中,捕獲試劑是固定的分析物(例如,紫杉醇復合物),其在檢測試劑是抗體時為捕獲不包括結合的分析物的檢測試劑的固定的抗原。固定的分析物可被直接固定至測試條。或者,固定的分析物可通過接頭或載體材料固定(例如,與載體蛋白,諸如白蛋白結合的分析物)。在這樣的實施方案中,捕獲試劑是如上所述的第一捕獲材料。
在一個實施方案中,捕獲試劑是捕獲具有或不具有結合的分析物的檢測試劑的固定的抗體。在其中檢測試劑是小鼠單克隆抗體的實施方案中,捕獲試劑是抗小鼠抗體(例如,山羊抗小鼠抗體,GAM抗體)。在這樣的實施方案中,捕獲試劑是如上所述的第二捕獲材料。
可用于本發明測定中的代表性捕獲試劑(例如,BSA-紫杉醇)的制備描述于實施例1中。
替代測定配置。本文所述的本發明的側流測定法是固相免疫測定法。應當理解,可使測定和裝置的形式從上述形式倒轉過來,以使得檢測試劑是標記的抗原(例如,具有可檢測標記的BSA-紫杉醇),并且捕獲試劑是一種或多種抗體、抗體片段或抗體衍生物(即固定在捕獲區中)。在這種形式的操作中,樣品流動通過/穿過沉積的標記抗原,并隨后接觸固定的抗體、抗體片段或抗體衍生物。此時,樣品中最初存在的游離分析物(例如,紫杉醇)與標記的抗原競爭結合固定的抗體、抗體片段或抗體衍生物。如上所述,裝置可以包括固定在相同或不同位置的多種不同的抗體、抗體片段或抗體衍生物。捕獲試劑可以在相同或不同的位置。在其中測試條具有其中固定捕獲試劑的多個位置的所有實施方案中,使用可檢測那些位置中的信號的適當讀取器。
應當注意,本發明的裝置、系統、組合物和方法一般根據側流測定描述。然而,如本文所述,用于監測選擇的抗原的一般策略不必限于側流測定形式,而是可應用于其它測定形式,諸如其它固相免疫測定(表面等離子體共振測定),其在本領域中通常是公知的。因此,盡管描述介紹側流格式,但本公開內容還包括結合任何已知測定形式的裝置、系統、組合物和方法。在一些實施方案中,測定形式包括在基底上固定捕獲試劑,諸如抗原綴合物(例如,紫杉醇綴合物)或抗原結合試劑(例如,抗紫杉醇抗體、片段、衍生物)。基底可以是用于測定形式的任何已知的合適基底,諸如硝化纖維素或玻璃。在一些實施方案中,基底是納米結構。在一些實施方案中,基底可包含可將捕獲試劑固定至其的碳納米結構(諸如碳納米管)或由其組成。
代表性紫杉醇測定。圖2C是用于根據本發明的紫杉醇側流免疫測定的代表性測試條的圖示。參考圖2C,代表性測試條200包括樣品墊210、結合墊220、具有第一捕獲區232和234(T1和T2)以及第二捕獲區238(C)的膜230,和吸收墊240。如上關于圖2A和2B所述,樣品墊210、結合墊220、膜230和吸收墊240處于液體連通,以使得引入至樣品墊的液體樣品流過或穿過結合墊和膜到達吸收墊;可改變測試條組件的尺寸和構造以適合待進行的紫杉醇測定(例如,組件墊和膜中的一個或多個可以重疊以促進從一個組件至下一個組件的最佳流動,如圖2A所示)。
在一個實施方案中,本發明提供了用于測定液體樣品中的紫杉醇的方法,其包括:
(a)將包含紫杉醇的液體樣品施加至側流測定裝置,所述裝置具有
(i)用于接收液體樣品的樣品接收區;
(ii)檢測試劑區,其與所述樣品接收區液體連通并且按流動方向位于所述樣品接收區的下游,
其中所述檢測試劑區包含沉積在其上的檢測試劑,
其中所述檢測試劑是用可檢測的報道基團標記的結合紫杉醇的紫杉醇抗體或其片段或衍生物;和
(iii)捕獲區,其與所述檢測試劑區液體連通,并且按流動方向位于所述檢測試劑區的下游,
其中所述捕獲區包含固定在其上的第一和第二捕獲試劑,所述第一捕獲試劑按流動方向位于所述第二捕獲試劑的上游,
其中所述第一捕獲試劑是能夠結合所述檢測試劑的紫杉醇材料,并且
其中所述第二捕獲試劑是能夠結合所述檢測試劑的抗體;
(b)使樣品從樣品接收區流過檢測試劑區以提供具有紫杉醇的檢測試劑(例如,檢測劑與結合的紫杉醇、任選游離的檢測試劑和任選游離的紫杉醇的組合);
(c)使具有紫杉醇的檢測試劑流過捕獲區,
由此所述第一捕獲試劑結合游離檢測試劑以提供結合至所述第一捕獲試劑的檢測試劑,以及
由此所述第二捕獲試劑結合具有或不具有結合的紫杉醇的檢測試劑;以及
(d)觀察結合至第一捕獲試劑相對于第二捕獲試劑的檢測試劑的量。
在某些實施方案中,所述方法還包括通過定量結合至第一捕獲試劑的檢測試劑的量來測定樣品中紫杉醇的量。定量結合至第一捕獲試劑的檢測試劑的量包括光密度測量等。
合適的可檢測報告基團如上所述。在一個實施方案中,可檢測的報告基團是膠體金。
可用于本發明方法的紫杉醇抗體或其片段或衍生物具有大于約1X104的Kon。代表性Kon值為大于約2X104、4X104、8X104、1X105、1X106和1X107。優選范圍為約1X104至約1X107。
可用于本發明方法的紫杉醇抗體或其片段或衍生物具有小于約1X10-3的Koff。代表性Koff值為小于約1X10-3、1X10-4、1X10-5和1X10-7。優選的Koff值為約1X10-3至1X10-7。
在某些實施方案中,紫杉醇抗體或其片段或衍生物具有約1X104至約1X106的Kon和約1X10-3至約1X10-4的Koff。
用于測定Kon值和Koff值的方法在實施例4中進行了描述。
在一個實施方案中,抗體具有高的Kon和低的Koff(例如,最小Kon為2.0X105,最大Koff為1.0X10-3)。在該實施方案中,捕獲線位于0.0至0.4T/C。對于此類別,單克隆抗體工程化將集中于保持Koff恒定,同時盡可能多地增加Kon。Kon越大,抗體檢測越好。
在另一個實施方案中,抗體具有低Kon和高Koff(例如,最小Kon為2.0X104且最大Koff為2.0X10-4)。在該實施方案中,捕獲線位于0.2-1.0T/C。對于此類別,單克隆抗體工程化將集中于保持Kon恒定,同時盡可能多地降低Koff。解離速率越低,檢測抗體越好。
在某些實施方案中,紫杉醇抗體是3C6。在其它實施方案中,紫杉醇抗體是8A10。在另外的實施方案中,可使用紫杉醇抗體的組合(例如,3C6和8A10)。這些抗體在下面進行了詳細描述。
在測定中,第一捕獲區包括固定的紫杉醇材料,其用作與紫杉醇競爭結合檢測試劑的紫杉醇抗原。第一捕獲區捕獲不包括結合的紫杉醇的檢測試劑(即,游離檢測試劑)。在某些實施方案中,紫杉醇材料是紫杉醇蛋白質綴合物。合適的蛋白質綴合物包括血清白蛋白綴合物,諸如BSA-紫杉醇。
在測定中,第二捕獲區包括能夠結合檢測試劑的固定的抗體。在某些實施方案中,抗體是山羊抗小鼠抗體。
如上所述,可以通過改變在將樣品引入側流裝置(例如,樣品接收區)的點與第一捕獲試劑之間的距離來優化測定中的紫杉醇檢測靈敏度。在某些實施方案中,將樣品接收區與第一捕獲試劑之間的距離最小化,以優化紫杉醇檢測靈敏度。在某些實施例中,距離小于20mm,小于10mm,小于5mm,小于3mm,小于2mm或小于1mm。在某些實施方案中,距離為20至1mm,10至1mm,5至1mm,3至1mm或2至1mm。
優化可以被描述為T(測試線)和C(對照線)的相對定位:T/C,其被定義為從起始點到T的距離/從起始點到C的距離的比,其中起始點被定義為捕獲區的上游邊緣(圖2A-2C中膜230的上游邊緣)。T/C可以大于約0.0(即,第一捕獲試劑位于捕獲區的上游邊緣),或約0.01、約0.02、約0.04、約0.08、約0.10、約0.20、約0.40、約0.80,或小于約1.0(即,第一捕獲試劑位于捕獲區的下游邊緣,第二捕獲試劑位于第一捕獲試劑與捕獲區的下游邊緣之間)。優選地,T/C為約0.2至約0.7。
在某些實施方案中,第一距離與第二距離的比率為約0.0至約0.40。在其它實施方案中,第一距離與第二距離的比率為約0.20至約1.0。
在某些實施方案中,觀察并測量與第二捕獲試劑結合的過量檢測試劑的量。在某些實施方案中,通過使最終捕獲試劑(測試線)與第二捕獲試劑(對照線)相關來測定樣品中的紫杉醇的量。
如上所述,本發明的代表性測定法包括在不止一個第一捕獲區中的不止一種第一捕獲試劑。在這些實施方案的某些實施方案中,該方法還包括在第一(T1,圖2C中的232)與第二(C,圖2C中的238)捕獲區之間的第三捕獲區(參見T2,圖2C中的234),其中所述第三捕獲區包含能夠結合檢測試劑的紫杉醇材料。第一和第三區中的紫杉醇材料可以相同或不同。在這些實施方案的某些實施方案中,樣品中紫杉醇的量通過定量結合至第一和第二捕獲試劑的檢測試劑的量來測定。定量結合至第一和第二捕獲試劑的檢測試劑的量可以包括光密度測量。
在該方法的某些實施方案中,側流裝置還包含與捕獲試劑區液體連通并且按流動方向位于捕獲試劑區下游的吸收區。
圖3是經歷其中代表性分析物(紫杉醇)的量是變化的測定條件的代表性測試條的圖像。在這些測定配置中,膜230包括三個捕獲區:測試線1和測試線2顯示使用固定的抗原(呈固定的BSA-紫杉醇形式的紫杉醇)作為第一捕獲材料的捕獲;對照線顯示使用固定的抗體(山羊抗小鼠抗體)作為第二捕獲材料的捕獲。在該測定中,檢測試劑是用膠體金標記的抗紫杉醇抗體(8A10)。
應注意,本發明的方法和裝置可用于檢測生物樣品中紫杉醇的水平,包括紫杉醇前藥或紫杉醇的任何制劑。紫杉醇的制劑包括任何已知的促進紫杉醇遞送的試劑,諸如聚合物納米顆粒、基于脂質的納米顆粒制劑、聚合物綴合物、無機納米顆粒、碳納米管、納米晶體和環糊精納米顆粒。
根據本發明的方法和裝置的代表性側流免疫測定的描述在實施例3中進行了描述。
紫杉醇抗體
在另一個方面,本發明提供了結合紫杉醇的抗體(例如,單克隆抗體或mAb)。使用MabSelect(GE Healthcare,Pittsburgh,PA)從富含抗體的收獲培養基中純化被稱為8A10和3C6的mAb。基于它們與BSA-紫杉醇的結合來選擇mAb,所述BSA-紫杉醇是如J-G Leu等,Cancer Res.(1993)53:1388-1391中所述制備的。
在一個方面,本發明提供了選自8A10、3C6的單克隆抗體及其片段或衍生物,其中所述抗體、抗體片段或抗體衍生物結合紫杉醇。
如本文所用,術語“抗體”包括來源于任何產生抗體的哺乳動物(例如,小鼠、大鼠、兔、駱駝和靈長類動物,包括人)或者合成或重組產生的抗體及其抗體片段,其特異性結合目標靶標(例如,紫杉醇)或其部分。示例性抗體包括多克隆、單克隆和重組抗體;多特異性抗體(例如,雙特異性抗體);人源化抗體;鼠抗體;嵌合的小鼠-人、小鼠-靈長類動物、靈長類動物-人單克隆抗體;和抗獨特型抗體,并且可以是任何完整分子或其片段,諸如抗原結合片段。如本文所述,單克隆抗體是優選的,因為它們提供了選擇的抗原(諸如治療藥物(例如,紫杉醇))的結合的增加的特異性。
如本文所用,術語“抗原結合片段”是指來自全長抗體或與全長抗體相關的抗原結合或可變區。抗體片段的舉例說明性實例包括Fab、Fab'、F(ab)2、F(ab')2和Fv片段、scFv片段、雙抗體、納米抗體、線性抗體、單鏈抗體分子和由抗體片段形成的多特異性抗體。
如本文所用,“單鏈Fv”或“scFv”抗體片段包含抗體的VH和VL結構域,其中這些結構域存在于單條多肽鏈中。通常,Fv多肽還包含在VH與VL結構域之間的多肽接頭,其使scFv能夠形成抗原結合所需的結構。
如本文所用,“嵌合抗體”是重組蛋白,其含有來源于非人物種(例如,嚙齒類動物)抗體的可變結構域和互補決定區,而抗體分子的其余部分來源于人抗體。
如本文所用,“人源化抗體”是包含符合來源于被移植至人抗體框架中的非人免疫球蛋白的特異性互補決定區的最小序列的嵌合抗體。人源化抗體通常是重組蛋白,其中只有抗體互補決定區是非人來源的。
如本文所用,術語“衍生物”表示已從參照抗體產生的抗體或抗體片段。例如,有時需要修飾或增強參照抗體的結合特性。因此,可對抗體進行各種修飾,包括對編碼DNA進行突變,以改變結合性質。所得的具有改變的性質的抗體然后被稱為參照抗體的“衍生物”。例如,抗體衍生物可以是包含由施加于參照抗體(或編碼參照抗體的核酸)的親和力成熟過程產生的突變的抗體。此類突變可導致具有改變的(例如,改善的)結合親和力、選擇性等的抗體。
在一些實施方案中,抗體、抗體片段或抗體衍生物包含一個或多個與SEQ ID NO:2、4、6或8中包含的CDR具有至少95%同源性的互補決定區(CDR)。下面更詳細地描述的SEQ ID NO:2和4分別是8A10輕鏈和重鏈的可變區的氨基酸序列。也在下文更詳細描述的SEQ ID NO:6和8分別是3C6輕鏈和重鏈的可變區的氨基酸序列。每個可變區含有三個互補決定區(CDR),如下所示。在一些實施方案中,抗體、抗體片段或抗體衍生物包含與SEQ ID NO:2、4、6或8的任一個包含的1個、2個或所有3個CDR具有至少95%同源性的1個、2或所有3個互補決定區(CDR)。在一些實施方案中,抗體、抗體片段或抗體衍生物具有重鏈和輕鏈,其包含1個、2個、3個、4個、5個或所有6個由8A10可變輕鏈和重鏈區提供的CDR區(SEQ ID NO:2和4中的)。在一些實施方案中,抗體、抗體片段或抗體衍生物具有重鏈和輕鏈,其包含1個、2個、3個、4個、5個或所有6個由3C6可變輕鏈和重鏈區提供的CDR區(SEQ ID NO:6和8中的)。
在一些實施方案中,所述一個或多個CDR與SEQ ID NO:2、4、6或8的任一個中的一個或多個CDR具有至少95%、96%、97%、98%、99%或100%序列同一性。如本文所用,術語“百分比同源性”或“百分比同源的”,當與本發明實踐中使用的多肽結合使用時,被定義為在對齊序列以獲得最大百分比同源性后多肽序列中與指定的多肽的氨基酸序列同源的氨基酸殘基的百分比。當進行比較時,沒有缺口被引入生物標志物序列以實現最佳比對。氨基酸序列同源性可以例如以下列方式來測定。多肽的氨基酸序列被用于使用BLASTP程序來搜索蛋白質序列數據庫,諸如GenBank數據庫。在無缺口模式下使用程序。默認濾過用于去除由于低復雜度的區域而導致的序列同源性。使用BLASTP的默認參數。
可用于本發明的測定方法的代表性紫杉醇抗體(3C6和8A10)的生產、加工、純化、表征和優化描述于實施例2中。本發明的抗體通過用綴合于KLH的漿果赤霉素或免疫小鼠來產生。抗體概括為:3C6抗-IgG2a,k、3H5抗漿果赤霉素III IgG1、8A10抗紫杉烷IgG2a。3C6、3H5和8A10抗體的交叉反應性特征通過其針對表1中各種紫杉烷的IC50值來顯示。
表1.紫杉醇抗體的交叉反應性
為了有效地利用抗體在診斷應用中實現動態檢測范圍,需要被成功優化的兩個關鍵因素是抗體對靶向抗原的特異性和親和力。3C6和8A10單克隆抗體對紫杉醇具有高特異性和親和力,這表明這些抗體以高度均一的方式特異性結合靶向紫杉醇抗原的單個表位。這種特異性還有助于消除檢測測定中的交叉反應性問題。結合特異性,單克隆抗體還可具有針對抗原的優化的和改善的親和力,以便在診斷測試中實現動態檢測范圍,這可通過親和力成熟的過程實現。另外,可針對快速Kon選擇mAb以與快速流動測定相容。
如圖4所示,3C6和8A10單克隆抗體都具有約10nM的表觀Kd值,靈敏度極限為約100-200ng/mL。
以下實施例被提供來用于說明目的而不是限制本發明。
實施例1
測定試劑
在本實施例中,描述了在本發明的測定方法和裝置中有用的代表性檢測試劑和捕獲試劑的制備。
檢測試劑:抗體-膠體金綴合物。簡言之,將抗體(參見實施例2)在0.5X PBS中稀釋至1mg/mL,并采取以下步驟:(1)搖動或渦旋金以重懸任何沉淀的金,然后將0.5mL裸金溶膠置入10個清潔的個體試管;(2)每個管用來自提供的pH圖的pH值(或1至10)標記;(3)將pH圖用于向每個試管中添加不同量的緩沖液(以微升表示),并搖動混合;(4)將每個試管置于低速渦旋混合器上并添加抗體溶液,隨后充分混合(約2至3秒),對于20nm金,14μL的2mg/mL抗體或蛋白質溶液是最佳的;(5)一些管上的深紫色和/或黑色沉淀表明抗體或蛋白質低于其等電點,導致個體金溶液的交聯(不能用于免疫測定的交聯的溶液被丟棄;深紫色溶液大部分也是無活性的;只有具有淺紫色或無顏色變化的管可用于免疫測定);(6)使反應持續總共30分鐘;和(7)通過加入50μL封閉液停止反應。
捕獲試劑:紫杉醇-白蛋白綴合物。通常按照J-G Leu等,Cancer Res.(1993)53:1388-1391中所述,制備紫杉醇-白蛋白綴合物(例如,BSA-紫杉醇)。對于2'-半琥珀酰基紫杉醇的合成,晶體是用于將紫杉醇與載體蛋白綴合的起始材料。在室溫下將紫杉醇(20mg)和琥珀酸酐(36mg)在真空下于P2O5上干燥4小時,并溶于480μL無水吡啶中。在室溫下靜置過夜后,在真空下除去吡啶,殘余物用2mL蒸餾水洗滌一次。加入丙酮(1mL),并將蒸餾水滴加至丙酮溶液中,直至出現少量晶體(2'-半琥珀酰基紫杉醇)。將混合物在4℃下保持3小時,通過過濾回收晶體并在真空下干燥。產物收率為70%。
透析步驟除去任何未綴合的紫杉醇。將2'-半琥珀酰基紫杉醇(10mg)溶解在1mL DMSO和300μL乙腈中,然后添加50μL(35mg;0.19mmol)正-三丁胺。將混合物在冰浴中冷卻至4℃,向混合物中添加25μL(25mg;0.18mmol)氯甲酸異丁酯,將其在冰上保持30分鐘。將溶液滴加至BSA溶液[25mg,(3.73x10-4mmol)于3mL蒸餾水中,pH 9.5,在4℃下]中。用1N HCl將pH立即調節至7.5,并將混合物在4℃保持過夜,在4℃下用PBS透析過夜。
在一個示例性實施方案中,評估側流系統。將0.5mg/mL BSA-紫杉醇(測試線)和0.5mg/mL山羊抗小鼠抗體(對照線)條紋式印制至系統的膜上。使紫杉醇抗體-膠體金綴合物流過系統。抗體-膠體金綴合物結合至固定在膜上的BSA-紫杉醇并產生強信號。該信號是紫杉醇特異性的,因為當將紫杉醇添加至樣品中加標時觀察到信號減小。
實施例2
紫杉醇抗體
在本實施例中,描述了在本發明的方法和裝置中有用的代表性紫杉醇抗體的生產、加工、純化、表征和優化。
抗體生產和加工。將細胞在含有5-10%FBS和1X Pen/Strep的CCM1(Hyclone)中生長。一旦細胞達到>1×106個細胞/mL的密度,就將細胞分開(1:4)。然后將細胞冷凍并儲存在2個單獨的液氮冷凍槽中作為備份。將細胞在滾瓶中培養直至達到1×106個細胞/mL的密度。在該時刻,不再喂養培養物,每天監測細胞活力。一旦細胞活力降低至<50%,則除去細胞并收獲富含抗體的培養基。
抗體的親和純化。使用PBS,pH 7.4進行透濾,并使用50Kd截留膜將收獲的抗體濃縮10倍。MabSelect(GE Healthcare,Pittsburgh,PA)用于親和純化。針對容量和通量以及rProtein A配體的定向偶聯優化的親水性高流量瓊脂糖珠遞送了高純度和高產率的產物庫。
純化運行程序。
柱:XK 16/40(16mm i.d.,20cm床高)。
樣品:澄清的雜交瘤消耗的培養基。
上樣緩沖液A:20mM NaH2PO4,0.15M NaCl,pH7.2。
洗脫緩沖液B:0.1M檸檬酸三鈉,pH 3.6。
抗體親和力。完整IgG(8A10和3C6)與BSA-紫杉醇抗原的直接結合的結果的圖顯示于圖4中。將50μL在1x PBS中濃度為3.5μg/mL的BSA-紫杉醇抗原結合至板并在4℃下孵育過夜。用PBS/0.05%Tween 20洗滌板四次。用PBS/0.05%Tween 20中的1%BSA在室溫封閉板2小時。用PBS/0.05%Tween 20洗滌板四次。結合50μL抗體樣品(8A10和3C6)(始于300nM且滴度下降3s)。將板用PBS/0.05%Tween 20洗滌4次。結合50μL山羊抗mIgG辣根過氧化物酶(1:5000稀釋),然后添加50μL底物溶液TMB,并使顏色顯色。用50μL 1M HCl終止反應,并在450nm處讀取光密度。完整IgG(8A10和3C6)與BSA-紫杉醇抗原的直接結合的結果顯示在圖4中。
抗體優化。進行包括親和力成熟的抗體優化。該方法包括:(1)通過對從雜交瘤細胞系產生的抗體進行測序來表征抗體,(2)構建集中于CDR區的抗體文庫;(3)篩選有益突變,和(4)組合有益突變。
步驟1:克隆和表達抗紫杉醇mAb為Fab
A.從雜交瘤細胞產生的抗體(8A10和3C6)的可變區的測序。
i.總RNA提取和mRNA變性
使用QIAGEN RNeasy Mini試劑盒從兩個雜交瘤細胞(8A10和3C6)提取總RNA。將mRNA混合物(如下所述)在72℃溫育3分鐘,然后冷卻至42℃,持續2分鐘。冷卻后,將管以14,000×g短暫旋轉10秒以收集底部的內容物。
mRNA混合物
RNA模板(0.2–0.4ug) 1-2.75uL
5'-RAGE引物A 1uL
不含RNA酶的水 至3.75uL
ii.cDNA合成和5'RAGE反應
如下所示進行cDNA合成和5'RAGE反應。
iii.通過瓊脂糖凝膠電泳分析PCR反應
將PCR擴增產物在瓊脂糖凝膠上電泳以確認對應于8A10和3C6mAb的輕鏈和重鏈可變區的擴增子的存在。
iv.克隆、測序和CDR分析
將PCR陽性條帶克隆入載體中并進行測序。抗體序列分析鑒定了8A10和3C6的一條輕鏈和一條重鏈。最初對于3C6,僅鑒定了一條輕鏈并且未鑒定重鏈(異常序列)。因此,將根據從N-末端測序結果獲得的序列設計的特異性引物用于對重鏈再進行PCR。最后,完成了3C6的重鏈的鑒定。
8A10雜交瘤
8A10雜交瘤測序結果如下所示。
8A10可變輕鏈核酸序列是SEQ ID NO:1:
GAC ATT GTG ATG ACC CAG TCT CAA AAA TTC ATG TCC ATA ACACTA GGA GAG AGG GTC AGC ATC ACC TGC AAG CCC AGT CAG AAT GTGGGT TCT GCT GTA ACC TGG TGG CAA CAG AAA CCA GGA CAA TCT CCTAAA CTA CTG ATT TAC TCA GCT TCC AAT CGG TAT ACT GGA GTC CCTGAT CGC TTC ACA GGC AGT GGA TCT GGG ACA GAT TTC ACT CTC ACCATT AGT AAT GTG CAG TCT GAA GAC CTG GCA GAT TAT TTC TGT CAACAA TAT AGC AGC TAT CCG TAC ACG TTC GGA GGG GGG ACC AAG CTGGAA ATA AAA CG(SEQ ID NO:1).
編碼CDR區的序列加以下劃線。
相應的8A10可變輕鏈氨基酸序列是SEQ ID NO:2:
DIVMTQSQKFMSITLGERVSITCKPSQNVGSAVTWWQQKPGQSPKLLIYSASNRYTGVPDRFTGSGSGTDFTLTISNVQSEDLADYFCQQYSSYPYTFGGTKLEIKR(SEQ ID NO:2)。
三個CDR區加以下劃線(即,CDRL1是KPSQNVGSAVT,CDRL2是SASNRYT,CDRL3是QQYSSYPYT)。
8A10可變重鏈核酸序列是SEQ ID NO:3:
GAG GTC CAG CTG CAA CAA TCT GGA CCT GAA CTG GTG AAG CCTGGG GCT TCA GTG AAG ATT TCC TGT AAG GCT TCT GGA TAC ACG TTCACT GAC TCC ACC ATG AAC TGG GTG AAG CAG AGC CAT GGA AAG AGCCTT GAG TGG ATT GGA GAG ATT GAT CCT AAC AAT GGT GGT ACT AACTAC AAT CAG AAG TTC AAG GGC AAG GCC ACA TTG ACT GTA GAC AAGTCC TCC AGC ACA GCC TAT ATG GAG CTC CGC AGC CTG ACA TCT GAGGAC TCT GCA GTC TAT TAC TGT GCA AGA GGG GTC TGG GGC CAA GGCACC ACT CTC ACA GTC TCC TCA(SEQ ID NO:3).
編碼CDR區的序列加下劃線。
相應的8A10可變重鏈氨基酸序列是SEQ ID NO:4:
EVQLQQSGPELVKPGASVKISCKASGYTFTDSTMNWVKQSHGKSLEWIGEIDPNNGGTNYNQKFKGKATLTVDKSSSTAYMELRSLTSEDSAVYYCARGVWGQGTTLTVSS(SEQ ID NO:4)。
三個CDR區加以下劃線(即,CDRH1是GYTFTDSTMN,CDRH2是EIDPNNGGTNYNQKFKG,CDRH3是GV)。
3C6雜交瘤
3C6雜交瘤測序結果如下所示。
3C6可變輕鏈核酸序列是SEQ ID NO:5:
GAT GTT GTG ATG ACC CAA ACT CCA CTC TCC CTG CCT GTC AGTCTG GGA GAT CAA GCC TCC ATC TCT TGC AGA TCT CGT CAG AGC CTTGTA CAC AGT AAT GGA AAC ACC TAT TTA CAT TGG TAC CTG CAG AAGCCA GGC CAG TCT CCA AAG CTC CTG ATC TAC AAA GTT TCC AAC CGATTT TCT GGG GTC CCA GAC AGG TTC AGT GGT AGT GGA TCA GGG ACAGAA TTC ACA CTC GAG ATC AGC AGA GTG GAG GCT GAG GAT CTG GGAGTT TAT TTC TGC TCT CAA AGT ACA CAT GTT CCT CCG ACG TTC GGT GGAGGC ACC AAG CTG GAA ATC AAA C(SEQ ID NO:5).
編碼CDR區的序列加以下劃線。
相應的3C6可變輕鏈氨基酸序列是SEQ ID NO:6:
DVVMTQTPLSLPVSLGDQASISCRSRQSLVHSNGNTYLHWYLQKPGQSPKLLIYKVSNRFSGVPDRFSGSGSGTEFTLEISRVEAEDLGVYFCSQSTHVPPTFGGGTKLEIK(SEQ ID NO:6)。
三個CDR區帶有下劃線(即,CDRL1是RSRQSLVHSNGNTYLH,CDRL2是KVSNRFS,CDRL3是SQSTHVPPT)。
3C6可變重鏈核酸序列是SEQ ID NO:7:
GAG GTG CAG CTT CAG GAG TCG GGA CCT AGT CTC GTG AAA CCTTCT CAG ACT CTG TCC CTC ACC TGT TCT GTC ACT GGC GAC TCC ATC ACCAGT GGT TAC TGG AAC TGG ATC CGG AAA TTC CCA GGG AAT AGA CTTGAG TAC ATG GGG TAC ATA AGC TAC AGT GGT AGC ACT TAC TAC AATCCG TCT CTC AAA AGT CGA ATC TCC ATC ACT CGA GAC ACA TCC AAGAAC CAG TAC TAC CTA CAT TTG ACT TCT GTG ACT ACT GAG GAC ACAGCC ACA TAT TAC TGT GCC CAA GGG GAT GGC GCC TAC TGG GGC CAAGGC ACC ACT CTC ACA GTC TCC TCA(SEQ ID NO:7).
編碼CDR區的序列加以下劃線。
相應的3C6可變重鏈氨基酸序列是SEQ ID NO:8:
EVQLQESGPSLVKPSQTLSLTCSVTGDSITSGYWNWIRKPGNRLEYMGYISYSGSTYYNPSLKSRISITRDTSKNQYYLHLTSVTTEDTATYYCAQGDGAYWGQGTTLTVSS(SEQ ID NO:8)。
三個CDR區加以下劃線(即,CDRH1是GDSITSGYWN,CDRH2是YISYSGSTYYNPSLKS,CDRH3是GDGAY)。
表2. 8A10和3C6 mAb的N-末端測序結果與雜交瘤測序結果的比較。
B.將mAb的可變區克隆入M13工程載體中。
使用PCR,利用序列特異性引物擴增編碼mAb(即,8A10和3C6)的VL、Cκ和VH區的DNA。將所得PCR產物進行凝膠純化,并針對在lacZ啟動子控制下的基于M13的噬菌體載體內的特定位點進行限制性消化。將編碼8A10和3C6 mAb的VL、Cκ和VH區的雙鏈DNA連接至含有人IgG1的CH1區的恒定區的基因的基于噬菌體的載體中。將所述DNA轉化至大腸桿菌(E.coli)中,并詳細檢查含有噬菌體的所得噬菌斑。隨機挑取噬菌斑,分離其DNA,并測定序列。克隆8A10_1經測定具有與mAb 8A10相同的VL、Cκ和VH區的序列(未顯示)。3C6的克隆過程可根據相同的方案進行。
C.從M13工程載體產生的Fab的紫杉醇結合活性的證明。
在用IPTG誘導的同時生長XL1-Blue大腸桿菌(革蘭陰性)的克隆8A10_1噬菌體感染的培養物,通過離心收獲所述培養物,并通過滲透壓休克(periprep)釋放周質內容物。從培養物中分離釋放的Fab產物。Fab濃度通過ELISA來定量,使用紫杉醇ELISA與完整的IgG一起來進行Fab的抗原特異性結合(未顯示)。兩種完整IgG的Kd值(對于兩種抗體均為約10nM)與先前報道的Kd值相當(參見圖3)。Fab 8A10的Kd值經測定也為10nM,其與完整IgG 8A10的Kd值相同。這些結果表明,親本抗體8A10的正確可變區序列存在于本發明的Fab 8A10中,并且以Fab形式從M13工程載體正確折疊和表達。
Fab在周質制劑中表達得足夠好以證明與BSA-紫杉醇綴合物包被的孔的濃度依賴性結合。
實施例3
代表性固相競爭測定
在本實施例中,描述了證明固相競爭性測定的功效的代表性測定。該測定證明了在此類檢測形式中使用本文所述的抗紫杉醇抗體來為樣品中紫杉醇的存在提供信息性信號的有用性。結果表明,抗體的變化的放置可增強測定性能。
紫杉醇側流系統。將1.2mg/mL BSA-Pac(試驗線,T)和0.2mg/ml山羊抗小鼠抗體(對照線,C)條紋式印制至膜卡片(High-Flow Plus HF180膜卡片,Millipore)上。將抗紫杉醇抗體-膠體金綴合物吸收和干燥至結合墊(玻璃纖維墊,Millipore)。在測定中流入加標有紫杉醇(10uL)的胎牛血清(FBS)(由80μL PBS Tween追蹤)。
串聯抗體測定。使用蒸餾水重建抗體-金綴合物,然后將其添加至彼此中以制備適當的濃度。施加該串聯抗體溶液,然后干燥至測定結合墊上。
讀取器輸出:強度相對位置。掃描測試條的結果的讀出。使用Qiagen讀取器(Qiagen,Germany)讀取條。
紫杉醇標準曲線。產生測試線與對照線的比率相對紫杉醇濃度的標準曲線。
圖5A和5B顯示了在T1和T2線處結合的8A10的曲線。圖5A顯示了標準曲線,即測試線與對照線(T/C)的比率相對紫杉醇濃度。對于較低濃度,8A10在T1處的比率相對T2的大差異表明當被放置得更靠近樣品端口時(其中分析物的濃度可能更高),抗體的靈敏度要高得多。圖5B顯示了如讀取器裝置提供的掃描的測試條的輸出強度相對于位置讀出。
圖6A和6B顯示了在T1和T2線處結合的3C6的曲線。圖6A示出了標準曲線,即測試線與對照線(T/C)的比率相對紫杉醇濃度。對于較低濃度,3C6在T1處的比率相對T2的相對小的差異表明對于將抗體放置得更靠近樣品端口(其中分析物的濃度可能更高),會獲得相對低的靈敏度改善。然而,觀察到相對于T2處的信號強度的改善。圖6B顯示了由讀取器裝置提供的掃描的測試條的輸出強度相對于位置讀出。
圖7A和7B顯示了在T1和T2線處結合的組合的8A10和3C6的曲線。圖7A顯示了標準曲線,即測試線與對照線(T/C)的比率相對紫杉醇濃度。通過將靠近樣品端口的8A10的高靈敏度和與位置無關的在T2處的3C6的較高靈敏度組合,使得測定更加強健。圖7B顯示了由讀取器裝置提供的掃描的測試條的輸出強度相對于位置讀出。
在上述分析中(和在圖5-7中),圖5B、6B和7B中的T1、T2和C的位置的測量(Pos[mm])是按流動方向從測試條的下游端(例如,在55mm點處引入樣品,T2在約45mm處,T1在約40mm處,C在約35mm處)進行的。
實施例4
用于測定抗體結合特性的方法
在本實施例中,描述了用于測定抗體性質的方法。該方法由Precision Antibody,Inc.(Columbia,MD)使用Biacore測定進行。本實施例還顯示了本發明的LFA測定可如何適用于其它固相測定,諸如表面等離子體共振(SPR)測定。
在25℃下在Biacore 3000儀器(GE,Pittsburgh,PA)上進行結合實驗。通過胺偶聯(EDC/NHS)將約13,000RU的抗BSA ab(Life Technologies,A11133,lot 1637270)直接固定在CM5芯片的流動池2上。捕獲110-120RU的BSA-紫杉醇(BSA-Ag)。流動池1以相同的方式處理,但不使用配體,并用作空白表面以用于參照扣除。用1M乙醇胺封閉未被占據的位點。將分析物Ab1(8A10)和Ab2(3C6)以不同的濃度在芯片上流動。實時監測抗原與抗體的結合以獲得締合(ka)和解離(kd)速率。從觀察到的ka和kd計算平衡常數(KD)。
使用如利用2倍連續稀釋所示的分析物濃度進行全動力學分析。起始濃度為200nM,隨后為100nM、50nM、25nM、12.5nM和0nM。以一式二份運行100nM濃度以確認測定的可重現性。全動力學分析結果概述于表3中。
測定緩沖液是10mM HEPES緩沖液(pH 7.4),150mM NaCl,3mM EDTA,0.05%P20(聚氧乙烯山梨聚糖)。再生緩沖液為10mM甘氨酸緩沖液(pH2.0)。綴合緩沖液是10mM乙酸鈉緩沖液(pH5.0)。用于捕獲配體的流速為1μL/min。動力學分析的流速為50μL/min。
在實際傳感圖與從BIAnalysis軟件產生的傳感圖之間進行卡方(χ2)分析,以測定分析的準確性。1-2內的χ2值被認為是顯著的(準確的),而低于1的值是高度顯著的(高度準確的)。
三個獨立的SPR運行的概述在表4中給出。
表3.完全動力學分析
表4.SPR概述
雖然已顯示和描述了說明性實施方案,但是應當理解,在不脫離本發明的精神和范圍的情況下,可以進行各種改變。
序列表
<110> Trieu, Vuong
Park, Chulho
Lee, Cynthia
<120> 用于紫杉醇的藥代動力學引導給藥的監測血漿中的紫杉醇濃度的方法、裝置和試劑<130> ATLC-1-53634
<150> US 62/051757
<151> 2014-07-17
<150> US 61/975386
<151> 2014-04-04
<160> 8
<170> PatentIn version 3.5
<210> 1
<211> 323
<212> DNA
<213> 人工序列
<220>
<223> 合成的
<400> 1
gacattgtga tgacccagtc tcaaaaattc atgtccataa cactaggaga gagggtcagc 60
atcacctgca agcccagtca gaatgtgggt tctgctgtaa cctggtggca acagaaacca 120
ggacaatctc ctaaactact gatttactca gcttccaatc ggtatactgg agtccctgat 180
cgcttcacag gcagtggatc tgggacagat ttcactctca ccattagtaa tgtgcagtct 240
gaagacctgg cagattattt ctgtcaacaa tatagcagct atccgtacac gttcggaggg 300
gggaccaagc tggaaataaa acg 323
<210> 2
<211> 108
<212> PRT
<213> 人工序列
<220>
<223> 合成的
<400> 2
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Ile Thr Leu Gly
1 5 10 15
Glu Arg Val Ser Ile Thr Cys Lys Pro Ser Gln Asn Val Gly Ser Ala
20 25 30
Val Thr Trp Trp Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Asp Tyr Phe Cys Gln Gln Tyr Ser Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 3
<211> 333
<212> DNA
<213> 人工序列
<220>
<223> 合成的
<220>
<221> CDS
<222> (1)..(333)
<400> 3
gag gtc cag ctg caa caa tct gga cct gaa ctg gtg aag cct ggg gct 48
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
tca gtg aag att tcc tgt aag gct tct gga tac acg ttc act gac tcc 96
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Ser
20 25 30
acc atg aac tgg gtg aag cag agc cat gga aag agc ctt gag tgg att 144
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
gga gag att gat cct aac aat ggt ggt act aac tac aat cag aag ttc 192
Gly Glu Ile Asp Pro Asn Asn Gly Gly Thr Asn Tyr Asn Gln Lys Phe
50 55 60
aag ggc aag gcc aca ttg act gta gac aag tcc tcc agc aca gcc tat 240
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
atg gag ctc cgc agc ctg aca tct gag gac tct gca gtc tat tac tgt 288
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
gca aga ggg gtc tgg ggc caa ggc acc act ctc aca gtc tcc tca 333
Ala Arg Gly Val Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
100 105 110
<210> 4
<211> 111
<212> PRT
<213> 人工序列
<220>
<223> 合成的構建體
<400> 4
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Ser
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Asn Asn Gly Gly Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Val Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
100 105 110
<210> 5
<211> 337
<212> DNA
<213> 人工序列
<220>
<223> 合成的
<220>
<221> CDS
<222> (1)..(336)
<400> 5
gat gtt gtg atg acc caa act cca ctc tcc ctg cct gtc agt ctg gga 48
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
gat caa gcc tcc atc tct tgc aga tct cgt cag agc ctt gta cac agt 96
Asp Gln Ala Ser Ile Ser Cys Arg Ser Arg Gln Ser Leu Val His Ser
20 25 30
aat gga aac acc tat tta cat tgg tac ctg cag aag cca ggc cag tct 144
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
cca aag ctc ctg atc tac aaa gtt tcc aac cga ttt tct ggg gtc cca 192
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
gac agg ttc agt ggt agt gga tca ggg aca gaa ttc aca ctc gag atc 240
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Glu Ile
65 70 75 80
agc aga gtg gag gct gag gat ctg gga gtt tat ttc tgc tct caa agt 288
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
aca cat gtt cct ccg acg ttc ggt gga ggc acc aag ctg gaa atc aaa c 337
Thr His Val Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 6
<211> 112
<212> PRT
<213> 人工序列
<220>
<223> 合成的構建體
<400> 6
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Arg Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Glu Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 7
<211> 339
<212> DNA
<213> 人工序列
<220>
<223> 合成的
<220>
<221> CDS
<222> (1)..(339)
<400> 7
gag gtg cag ctt cag gag tcg gga cct agt ctc gtg aaa cct tct cag 48
Glu Val Gln Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Ser Gln
1 5 10 15
act ctg tcc ctc acc tgt tct gtc act ggc gac tcc atc acc agt ggt 96
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Asp Ser Ile Thr Ser Gly
20 25 30
tac tgg aac tgg atc cgg aaa ttc cca ggg aat aga ctt gag tac atg 144
Tyr Trp Asn Trp Ile Arg Lys Phe Pro Gly Asn Arg Leu Glu Tyr Met
35 40 45
ggg tac ata agc tac agt ggt agc act tac tac aat ccg tct ctc aaa 192
Gly Tyr Ile Ser Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
agt cga atc tcc atc act cga gac aca tcc aag aac cag tac tac cta 240
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Tyr Tyr Leu
65 70 75 80
cat ttg act tct gtg act act gag gac aca gcc aca tat tac tgt gcc 288
His Leu Thr Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
caa ggg gat ggc gcc tac tgg ggc caa ggc acc act ctc aca gtc tcc 336
Gln Gly Asp Gly Ala Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
tca 339
Ser
<210> 8
<211> 113
<212> PRT
<213> 人工序列
<220>
<223> 合成的構建體
<400> 8
Glu Val Gln Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Asp Ser Ile Thr Ser Gly
20 25 30
Tyr Trp Asn Trp Ile Arg Lys Phe Pro Gly Asn Arg Leu Glu Tyr Met
35 40 45
Gly Tyr Ile Ser Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Tyr Tyr Leu
65 70 75 80
His Leu Thr Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Gln Gly Asp Gly Ala Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser
- 還沒有人留言評論。精彩留言會獲得點贊!