一種高效定量檢測高爾基體73的試劑盒的制作方法
本發明屬生物技術領域,涉及一種檢測GP73的方法及其建立的試劑盒,特別是涉及一種定量檢測GP73的酶聯免疫試劑盒。
背景技術:
肝癌是臨床上最常見的惡性腫瘤之一,全球發病率逐年增長,已超過62.6萬/年,居于惡性腫瘤的第5位;死亡接近60萬/年,位居腫瘤相關死亡的第3位。目前,我國發病人數約占全球的55%;在腫瘤相關死亡中僅次于肺癌,位居第二。因此,肝癌嚴重威脅我國人民健康和生命。肝臟是人體最大的實質性器官,承擔人體的各類重要代謝功能,因此,肝臟一旦出現惡性腫瘤將導致未及生命的嚴重后果。又由于肝臟具有豐富的血流供應,與人體的重要結構如下腔靜脈、門靜脈、膽道系統等關系密切;肝臟惡性腫瘤發病隱匿,侵襲性生長快速,其治療甚為困難。因此,早期發現、早期診斷對肝癌的治療及其重要。目前肝癌的診斷主要依靠血清腫瘤標志物檢測,影像學和組織學檢查,其中大量的研究已經證實甲胎蛋白是目前臨床原發性肝細胞癌的最主要實驗室指標,在肝癌患者的早期,血清中有數種分子水平已經發生了明顯的變化,通過對血清中這些分子水平的定量檢查可以作為肝癌預測的一個有效手段。
AFP是目前診斷原發性肝癌最重要的腫瘤標記物,已被廣泛用于肝癌的普查、診斷、判斷治療效果和預測復發中,但AFP的敏感性和特異性較差,雖然甲胎蛋白(AFP)是診斷肝癌的重要指標之一,但其仍有一定的局限性。據文獻報道,陽性率僅為60-70%,并存在假陽性。30%至40%的HCC患者APF呈陰性或弱陽性,且急性病毒性肝炎,慢性活動性肝炎,肝硬化活動期等疾病也會出現AFP升高。
高爾基體蛋白73是新近發現的一個分子量在73kDa,定位于高爾基本上的II型跨膜糖蛋白。采用免疫組化的研究方法證實在人類的上皮細胞有著GP73和少量表達,而在正常的肝臟中,GP73僅在膽管上皮細胞表達,肝細胞基本不表達。但是病變的組織,特別是肝癌的早期,GP73呈現過表達并且其表達水平與肝癌的進展相關,在肝癌患者血清中GP73的含量是正常人的3至5倍,與臨床療效及預后有較好的相關性。
肝癌的早期的發現率低,主要與早期肝癌的癥狀不明顯以及目前市場上缺乏有效的檢測手段有關。目前臨床上用于檢測肝癌的方法包括影像學方法如PET-CT、病理活檢來驗證。PET-CT檢查費用昂貴,而侵入性活檢對患者來講是極其痛苦的。因此,有必要在目前技術上十分成熟的普通ELISA的基礎上繼續優化檢測靈敏度的工藝,開發能檢測到更低含量GP73的ELISA試劑盒。
技術實現要素:
本發明的目的是提供一種高效定量檢測GP73的方法及其建立的免疫試劑盒,該試劑盒具有特異性強、靈敏度高,檢測范圍更低、線性條件好等優點,更適合用于精確定量。
為了實現上述目的,本發明是通過以下方案予以實現的。
一種高效定量檢測GP73的免疫學方法,以抗GP73的多克隆抗體和抗GP73的單克隆抗體混合在一起作為聯合捕獲抗體,以抗GP73的單克隆抗體或抗GP73的多克隆抗體作為檢測抗體DMA,通過抗原抗體反應從而檢測GP73。
現有技術中在使用免疫學方法檢測GP73時,捕獲抗體都是僅使用一種類型的抗體,要么是單克隆抗體,要么是多克隆抗體;而本發明將抗GP73的單克隆抗體與抗GP73的多克隆抗體混合制備成捕獲抗體,以另一種抗體作為檢測抗體,這樣建立的免疫學檢測方法的敏感性和特異性更高。敏感性和特異性顯著提高的原因在于,聯合捕獲抗體在不同的溶液環境下增加了抗原抗體的結合表位,減少了假陰性,但有可能增加假陽性,所以本發明在選擇檢測抗體時,采用點陣法來作交叉實驗,篩選到的檢測抗體特異性十分強,該檢測抗體與9種肝病相關抗原蛋白無交叉反應。從而彌補了聯合捕獲抗體可能導致的假陽性。作為檢測抗體的 抗GP73的單克隆抗體為貨號為130-10311,購自美國瑞博奧生物科技有限公司。
根據本發明所述的試劑盒的進一步特征,所述抗GP73多抗是根據以下方法制備的:用純化的GP73抗原蛋白免疫SPF級新西蘭兔,得到含有抗GP73多抗的兔血清,先用硫酸銨沉淀法從兔血清中初步純化免疫球蛋白IgG,再用ProteinG/A親和柱進一步純化,得到抗GP73多抗。
所述抗GP73多克隆抗體是基于GP73抗原蛋白來制備的,所述的GP73抗原標準品是采用原核表達系統表達的蛋白,該蛋白可溶性程度高,空間構象接近天然抗原。
所述抗GP73單抗是用序列為SEQ ID NO:1的多肽來制備的。
所述抗GP73單抗可以是根據以下方法制備的:用純化的序列為SEQ ID NO:1的多肽免疫SPF級Balb/c鼠,所得小鼠脾臟與骨髓瘤細胞SP2/0融合后篩選得到雜交瘤細胞株,雜交瘤細胞分泌所得抗體用ProteinG/A親和柱進一步純化,得到抗GP73單抗。
優選地,所述抗GP73單抗是由保藏號為CCTCC NO.C2014216的雜交瘤細胞株GP73-5B4-G6-C9-C6-G4分泌的單抗。該雜交瘤細胞株保藏單位為中國典型培養物保藏中心(CCTCC),地址是中國湖北省武漢市武漢大學,保藏日期為2014年11月20日。
本發明所述的試劑盒可以是酶聯免疫試劑盒,其包括:包被所述聯合捕獲抗體的96孔微孔板,20X濃縮洗滌液,含重組人類GP73蛋白的標準品抗原干粉,用于稀釋樣本的2瓶15ml 5X濃縮稀釋液D,用于稀釋抗體和HRP-鏈親和素的15ml 5X濃縮稀釋液B,生物素化抗GP73檢測抗體,200μl 300X濃縮HRP-鏈親和素溶液,12ml TMB底物,8ml含0.2M硫酸的終止液。
根據本發明所述的酶聯免疫試劑盒的進一步特征,所述聯合捕獲抗體的包被濃度是每種抗體0.3至0.5ug/孔,所述待測血清的稀釋倍數是1:10,所述檢測抗體為抗GP73單抗DMA,濃度為0.1mg/L,所述生物素標記的檢測抗體DMA的稀釋濃度是1:5000。
實驗結果表明,該酶聯免疫試劑盒檢測抗體具有很高的特異性,與9種肝病相關抗原蛋白無交叉反應。
本發明所述的定量檢測高爾基體73(GP73)的酶聯免疫試劑盒,其優點在于:采用兩種抗體聯合包被酶標板,該試劑盒具有特異性強、檢測范圍更低、靈敏度高,靈敏度可達200pg/ml(對照組檢測值<效價檢測值的一半),而常規GP73檢測試劑盒檢測范圍的最低檢測值是0.5ng/ml(例如,北京熱景生物技術有限公司的發明專利ZL 200810181016.1中所述的定量檢測試劑盒)。
本發明所述的試劑盒可以是膠體金免疫層析檢測試劑盒,該試劑盒包括至少一個試紙條,其包括:樣品墊、標記墊、硝酸纖維素膜、吸水紙、標記墊上包被膠體金標記的抗CRP檢測抗體DMA,硝酸纖維素膜包括包被有抗鼠IgG二抗的質控區和包被有所述聯合捕獲抗體的檢測區。
根據本發明所述的膠體金免疫層析檢測試劑盒的進一步特征,所述聯合捕獲抗體的包被濃度分別為0.5~1mg/ml,用量按膜包被液量為20~25ug/30cm2;所述檢測抗體DMA的包被濃度為0.2~1mg/ml,用量按膜包被液量為0.8ug/cm2。
本發明所述的免疫層析試紙條的檢測原理是雙抗夾心法,將直徑范圍0.01~1um的膠乳微球與抗GP73單抗和各類不同的熒光素共價結合,利用熒光素在激光發作用下可以發射熒光,當此熒光膠乳標記的GP73單抗與樣本中的抗原結合形成復合物,在層析作用下移至包被膜的檢測區,在包被膜的檢測區包被有能與GP73抗原結合的聯合捕獲抗體。復合物聚積在包被膜的T線區,受到光源激發釋發出相應波長的發射光,通過熒光檢測系統捕捉的光信號轉化為數字信號,從而可用于準確定量的快速免疫檢測中。
本發明所述的試劑盒可以是時間分辨熒光免疫層析檢測試劑盒,該試劑盒包括多個檢測試劑條,所述試紙條由樣品墊,熒光微球包被的釋放墊,硝酸纖維素膜(NC膜)和吸水紙組成;其中,樣品墊用于加樣(血清或全血);釋放墊中含過量的抗GP73檢測抗體和熒光微球的復合物;NC膜上有兩道線:檢測線,又稱T線,含定量的所述聯合捕獲抗體;對照線,又稱C線,含定量的抗鼠IgG二抗。
說明書附圖
圖1是本發明所述的ELISA試劑盒檢測抗體的特異性時的抗原點陣列圖。
圖2是本發明所述的ELISA試劑盒的樣本檢測值與醫院檢測值的比較圖。
具體實施方式
為使本發明更加容易理解,下面結合具體實施例,進一步闡述本發明。應理解,這些實施例僅用于說明本發明而不用于限制本發明的范圍。
實施例1:GP73基因的分泌表達
將GP73基因序列插入載體,經測序成功后轉入大腸桿菌,表達產物經SDS-PADG驗證得到單一條帶。
GP73抗原蛋白序列與GenBank登錄號AAF44663.1的一致。
實施例2:抗GP73多抗的制備、純化及鑒定
用實施例1所述的大腸桿菌表達的GP73蛋白免疫SPF級新西蘭兔(廣東省實驗動物中心),免疫三次,每次間隔半個月。最后一次加強免疫三天后,通過心臟采血,血清析出后,先用硫酸銨沉淀法從兔血清中初步純化免疫球蛋白IgG,再用ProteinG/A親和柱進一步純化抗GP73多抗,SDS-PAGE和Western Blotting鑒定純化的抗體。
實施例3:抗GP73單抗的制備,純化及鑒定
用不同的KLH偶聯的GP73抗原多肽免疫SPF級Balb/c鼠(廣東省實驗動物中心),免疫三次,每次間隔半個月。最后一次加強免疫三天后,通過收集脾臟細胞與骨髓瘤細胞融合得到雜交瘤細胞株,雜交瘤細胞分泌所得抗體用ProteinG/A親和柱進一步純化。
根據GP73蛋白序列設計了以下3段多肽進行實驗:
SEQ ID NO:1 CKEQCEERIEEVTKKGNEAV
SEQ ID NO:2 CDGQEEEQEAAGEGRNQQ
SEQ ID NO:3 CNMDENEAESETDKQAAL
采用上述3段多肽得到3株雜交瘤細胞株,下面將采用這些雜交瘤細胞株分泌的單抗組建酶聯免疫(ELISA)試劑盒,通過直接ELISA驗證它們的靈敏度。實驗結果表明,SEQ ID NO:1多肽和SEQ ID NO:2多肽制備的單抗的靈敏度比SEQ ID NO:3多肽高。
實施例4:檢測GP73的酶聯免疫(ELISA)試劑盒
本實施例采用實施例3得到的2株雜交瘤細胞株分泌的單抗,分別對應于SEQ ID NO:1多肽、SEQ ID NO:2多肽組建酶聯免疫(ELISA)試劑盒。
1、ELISA試劑盒的組分
1)ELISA酶標板:采用吸附性能好,空白值低,批次穩定的聚苯乙烯板包被捕獲抗體,預先用封閉液處理。采用純化好的抗GP73多抗和抗GP73單抗作為捕獲抗體。包被濃度每個抗體每孔在0.3至0.5ug之間。
2)洗滌液:含0.1%Tween 20的20X濃縮洗滌液。
3)標準品:含重組人類GP73蛋白的標準品抗原干粉。
4)稀釋液:2瓶用于稀釋樣本的15ml 5X濃縮稀釋液D,1瓶用于稀釋抗體和HRP-鏈親和素的15ml 5X濃縮稀釋液B。
5)檢測抗體:生物素化抗GP73單克隆抗體,最佳稀釋濃度為0.1mg/L。
6)200μl 300X濃縮HRP-鏈親和素溶液。
7)底物:12ml TMB溶液。
8)終止液:8ml含0.2M硫酸溶液。
2、ELISA試劑盒的操作步驟
1)將所有試劑放置室溫條件(18-25℃)下平衡30分鐘,標準品和樣本都設置至少一個重復。
2)加入100μl稀釋好的標準品及樣品,蓋上封板膜室溫條件下孵育2.5個小時或者4℃過夜,放置于洗板機洗滌并倒轉微孔板在紙巾上吸干凈。
3)加入100μl稀釋好的生物素化的檢測抗體,室溫條件下孵育1個小時。
4)放置于洗板機洗滌并倒轉微孔板在紙巾上吸干凈。
5)加入100μl稀釋好的HRP-鏈親和素,孵育45分鐘。
6)重復4)的步驟。
7)加入100μl TMB反應30分鐘,再加入50μl終止液終止反應,于酶標儀450nm讀數。
8)根據檢測結果得出折線圖公式,計算待測血清的GP73含量。
實施例5:ELISA試劑盒的質量分析
本實施例采用實施例4得到的3種ELISA試劑盒,通過直接ELISA驗證它們的靈敏度。這些試劑盒采用的聯合捕獲抗體為抗GP73多抗和抗GP73單抗,其中抗GP73單抗分別對應于由SEQ ID NO:1多肽、SEQ ID NO:2多肽得到的2株雜交瘤細胞株分泌的單抗。
1)ELISA試劑盒的靈敏度
參照實施例4中的操作步驟,在第2步的微孔板中依次加入50、25、6.25、3.125、1.56、0.78、0.39、0.19、0.09、0ng/ml的GP73抗原蛋白,設兩個重復求平均值,所得檢測結果如下表1,可知其檢測靈敏度可達97pg/ml(對照組檢測值<效價檢測值的一半),而常規GP73檢測試劑盒檢測范圍的最低檢測值是0.5ng/ml。
表1:靈敏度檢測
根據包被抗體的不同分為單抗1為SEQ ID No.1多肽制備的單抗,單抗2為SEQ ID No.2多肽制備的單抗,多抗為GP73蛋白制備的多抗,聯合捕獲抗體1為單抗1與多抗組合包被,聯合捕獲抗體2為單抗2與多抗組合包被。
對比實驗表明,SEQ ID NO:1多肽制備的單抗的靈敏度比SEQ ID NO:2多肽制備的單抗的靈敏度低,但由聯合捕獲抗體1的組合的靈敏度較其他抗體組合的較高,ELISA試劑盒采用此種組合。
因此,將分泌SEQ ID NO:1多肽制備的單抗的該株雜交瘤細胞株保藏于武漢大學菌種保藏中心,保藏號為CCTCC NO:C2014216,命名為雜交瘤細胞株GP73-5B4-G6-C9-C6-G4。
2)ELISA試劑盒檢測抗體的特異性
采用芯片點陣法來建議檢證試劑盒中檢測抗體的特異性。
在硝酸素纖維膜上點上10種不同的蛋白,每種蛋白點3個重復。加入生物素標記的抗GP73檢測單抗DMA及鏈親和素連接的熒光底物,通過Odyssey掃描熒光成像,結果如圖1所示,可知檢測抗體與其它9種肝病相關抗原蛋白均無交叉反應。
實施例6:ELISA試劑盒的應用
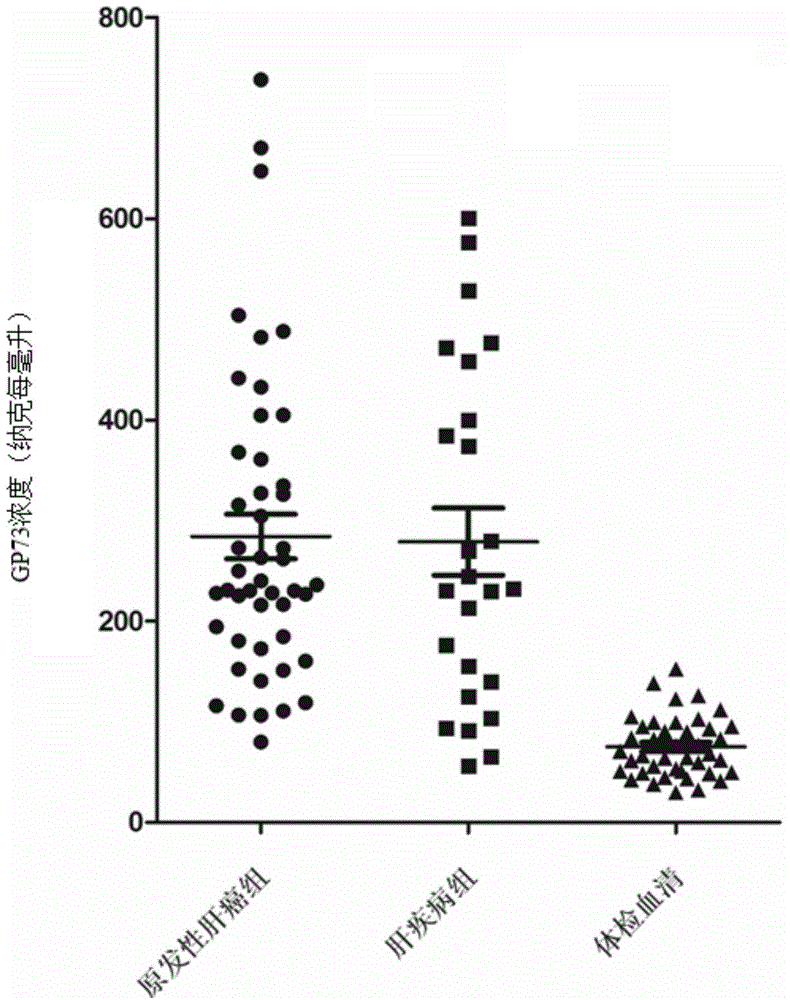
GP73定量檢測試劑盒針對同一批臨床樣本包括447例肝癌血清、25例肝病血清和41例正常人血清,結果如表2和圖2所示。
表2:試劑盒的應用
從表2的結果中可見,肝疾病組和原發性肝癌組患者的血清GP73水平相對于健康人的體檢血清水平顯著升高(P<0.0001),其中肝疾病組(包括肝炎、肝硬化等疾病)的GP73含量平均水平為278ng/ml,肝癌組平均水平為284ng/ml,與肝疾病組的差異不大,而正常人的血清含量為74.86ng/ml。
實施例7:檢測GP73的膠體金免疫層析檢測試劑盒
以上述實施例所述的聯合捕獲抗體和檢測抗體建立一種檢測GP73的膠體金免疫層析檢測試劑盒,所述試劑盒包括多個試紙條,所述試紙條由樣品墊,膠體金標記墊,硝酸纖維素膜(NC膜)和吸水紙組成,所述NC膜包被有檢測區和質控區,檢測區包被聯合捕獲抗體,質控區包被抗鼠IgG二抗;所述膠體金標記墊包被檢測抗體。
所述膠體金標記墊的制備過程為,以氯金酸-檸檬酸三鈉還原法制備活化的膠體金溶液,將檢測抗體按照100~500ug檢測抗體蛋白每100ul膠體金溶液的比例加入到膠體金溶液中,攪拌室溫反應2小時,離心洗滌2次,沉淀用膠體金溶液復溶至50ml,按0.8ug/cm2的用量涂覆在膠體金標記墊上,室溫干燥備用。
硝酸纖維素膜的制備過程為:將聯合捕獲抗體(抗GP73的單抗和多抗)和抗鼠IgG二抗用包被液調整至濃度為0.5至1mg/ml,將抗鼠IgG二抗用包被緩沖液PBS調整至濃度為0.8mg/ml,按膜包被液量為20ug/30cm2至25ug/30cm2的用量將聯合捕獲抗體噴到NC膜的檢測區,分別按膜包被液量為25ug/30cm2至30ug/27cm2的用量將抗鼠IgG噴到質控區,過夜冷凍干燥,加入干燥劑封存備用。在底板上依次相互搭接地粘貼樣品墊,膠體金標記墊,NC膜和吸水紙,按照要求切割成適當寬度的試紙條形成試劑盒。
實施例8:檢測GP73的時間分辨熒光免疫層析檢測試劑盒
以實施例中所述的聯合捕獲抗體和檢測抗體建立一種檢測GP73的時間分辨熒光免疫層析試劑盒,所述試劑盒包括多個檢測試紙條,所述試紙條由樣品墊,熒光微球包被的釋放墊,硝酸纖維素膜(NC膜)和吸水紙組成。其中,樣品墊用于加樣(血清或全血);釋放墊中含過量的抗GP73檢測抗體和熒光微球的復合物;NC膜上有兩道線:檢測線,又稱T線,含定 量的聯合捕獲抗體;對照線,又稱C線,含定量的抗鼠IgG二抗。
本試劑盒采用時間分辨熒光微球作為標記載體,將檢測抗體標記于熒光微球上,利用側向層析技術,將標記抗體的微球干燥于釋放墊上,同時在NC膜上噴制相應的聯合捕獲抗體,利用雙抗體夾心法檢測血清或全血中的GP73。當將含有待測抗原(GP73)的樣品滴在加樣區,待測樣品中的GP73與結合墊中的熒光納米微球標記的抗GP73檢測抗體結合并通過毛細作用向前層析,當達到檢測區后,與檢測線上固定的聯合捕獲抗體結合,形成微粒-抗體-抗原的抗體夾心復合物并被固定在檢測線上,而多余的熒光微球標記物繼續向前層析,與固定在質控線二抗結合。反應結束后,用紫外光源(365nm)對檢測區掃描檢測,檢測線和質控線上熒光納米微球發出高強度的熒光(615nm),且衰變時間也較長。利用延緩測量時間,待樣品基質中自然發生的短壽命熒光(1~10ns)全部衰變后,再測量微球的特異性激發熒光,這樣就可以完全排除特異本底熒光的干擾。通過檢測線和質控線熒光強度的強弱及其比值,即可分析出樣品中待測物的濃度。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 一種st2定量檢測方法及試劑盒的制作方法
- 一種定量藥粉取用盒的制作方法
- 一種層粘連蛋白(ln)測試試劑盒及其測試方法
- 一種抗核糖體P蛋白抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種阿膠膠液半成品或成品中驢、牛源性成分的定量檢測方法、組合物及試劑盒的制作方法
- 一種抗PM-Scl抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種抗LKM-1抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種抗SLA/LP抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種快速定量檢測h-fabp的時間分辨熒光免疫層析試劑及制備方法
- 一種定量檢測液體樣品中汞離子的方法及試劑盒的制作方法
- 一種定量藥粉取用盒的制作方法
- 一種層粘連蛋白(ln)測試試劑盒及其測試方法
- 一種抗核糖體P蛋白抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種阿膠膠液半成品或成品中驢、牛源性成分的定量檢測方法、組合物及試劑盒的制作方法
- 一種抗PM-Scl抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種抗LKM-1抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種抗SLA/LP抗體IgG的磁微粒化學發光定量測定試劑盒及制備和檢測方法
- 一種快速定量檢測h-fabp的時間分辨熒光免疫層析試劑及制備方法
- 一種定量檢測液體樣品中汞離子的方法及試劑盒的制作方法
- 一種軸抑制蛋白2基因突變檢測試劑及應用