負載型NiOOH電極材料及其制備方法和用途與流程
本發明涉及電極材料的制備領域,具體而言,涉及一種負載型NiOOH電極材料及其制備方法和用途。
背景技術:
面對日益嚴峻的環境問題和能源危機,探索可替代的能源存儲和轉換系統是解決這些問題的關鍵。氫能源由于其燃燒時理想的發熱值和綠色的燃燒產物被認為是一種清潔、高效、可再生的理想能源,電解水制氫是實現工業化廉價制備氫氣的重要手段。
電解水過程由兩個半反應組成:析氫反應(HER)和析氧反應(OER)。析氫反應可以在相對低的超電勢(η)下完成,而析氧反應過程在動力學的要求下則需要更高的超電勢,因為O-H鍵斷裂和隨后的O-O鍵形成需要達到高的能量勢壘。因此,制備高效穩定的OER電催化劑就顯得尤為重要。目前商用的析氧催化劑主要為IrO2和RuO2等貴金屬,其高昂的價格和稀有的儲量制約了這一過程的發展,尋找價格低廉和儲量豐富的非貴金屬催化劑成為近年來研究的熱點。
Ni基納米材料(例如NiSe,NiS,NiO等)是用于析氧反應的最有潛力的電催化劑之一,在它們的電催化過程中,NiOOH通常被認為在堿性電解質溶液中作為活性物質而起關鍵作用。在自然界中,NiOOH具有層狀結構并且以三種形式存在:α-NiOOH(斜方晶),β-NiOOH(六方晶)和γ-NiOOH(六方晶)。到目前為止,一系列的研究工作主要集中在第一列過渡金屬氧化物和氫氧化物、鈣鈦礦和硫族化物等,在這些過渡金屬催化劑中,Ni基化合物已被證明是用于堿性電解質OER的最好的電催化劑。眾所周知,鎳(氧)氫氧化物(NiOOH)是Ni(OH)2的氧化或充電狀態,許多研究報道,NiOOH中加入Fe具有很好的OER活性,但是,很少有報道研究純NiOOH的OER活性,這對研究Ni在堿性溶液中的催化機理有很好的指導作用。此外,泡沫鎳具有三維立體網狀結構,使用它作為基底可以增加電化學過程中的電荷轉移速率,基底與材料之間化學鍵的連接方式使得樣品的穩定性顯著提高。因此,仍然有需要尋找一種制備方法工藝簡單,對環境友好,反應條件溫和可控的制備方法,制備一種具有低超電勢高穩定性的電解水鎳基OER催化劑材料。
技術實現要素:
針對上述現有技術存在的問題,本發明的一個目的在于提供一種在泡沫鎳上負載豎直排列的α-NiOOH納米片結構的電極材料的制備方法,所述制備方法包括如下步驟:
1)泡沫鎳的預處理:在室溫下,將泡沫鎳在3.0M HCl溶液中超聲15min,然后依次用去離子水、無水乙醇清洗2至3次,備用。
2)鎳(Ⅱ)溶液的制備:將NiCl2·6H2O固體溶解于去離子水中,至Ni2+濃度為5mmol/L至50mmol/L,優選為10mmol/L至40mmol/L,更優選為25mmol/L。
3)丁二酮肟醇溶液的制備:稱取丁二酮肟固體溶解于無水乙醇中,至丁二酮肟濃度為5mmol/L至100mmol/L,優選為20mmol/L至80mmol/L,更優選為50mmol/L。
4)將步驟2)和3)中制備的鎳溶液和丁二酮肟醇溶液加入反應釜的聚四氟乙烯內襯中,攪拌10min后,將預處理過的泡沫鎳豎直浸入其中,預處理泡沫鎳完全浸入溶液中,擰緊釜蓋,將反應釜放入到200℃的電熱鼓風干燥箱中,并保持4至10h,優選為4至8h,更優選為6h。
5)取出反應釜自然冷卻到室溫狀態,傾倒掉上清液,用去離子水清洗掉表面沉淀物,得到長滿豎直排列Ni2Cl(OH)3納米片的泡沫鎳。
6)將得到的泡沫鎳用去離子水清洗掉表面沉淀物后,放入120至150℃的電熱鼓風干燥箱中,并保持8至12h,得到在泡沫鎳上豎直排列的α-NiOOH納米片。
優選地,在步驟4)中所述鎳(Ⅱ)與丁二酮肟的摩爾比為1:0.5至1:8,優選為1:1至1:4,更優選為1:1.5至1:3,最優選為1:2。
優選地,根據本發明的所述制備方法不使用有機溶劑或催化劑。
本發明的另一個目的在于提供一種電極材料,所述電極材料由上述制備方法制備,其中在泡沫鎳上負載有豎直排列的α-NiOOH納米片,所述α-NiOOH納米片長約0.5至1.5μm,寬度約為10-30nm,高度約為50-100nm。所述α-NiOOH納米片在泡沫鎳表面上豎直排列,有效地增加了比表面積。
本發明的另一個目的在于提供所述泡沫鎳上負載豎直排列的α-NiOOH納米片的電極材料在電解水方面的用途。
有益效果
根據本發明的所述泡沫鎳上負載豎直排列的α-NiOOH納米片的電極材料具有大的比表面積,電化學性能穩定,在電解水方面效率更高。根據本發明的所述電極材料的制備方法工藝簡單,對環境友好,反應條件溫和可控,適合大規模工業化生產。
附圖說明
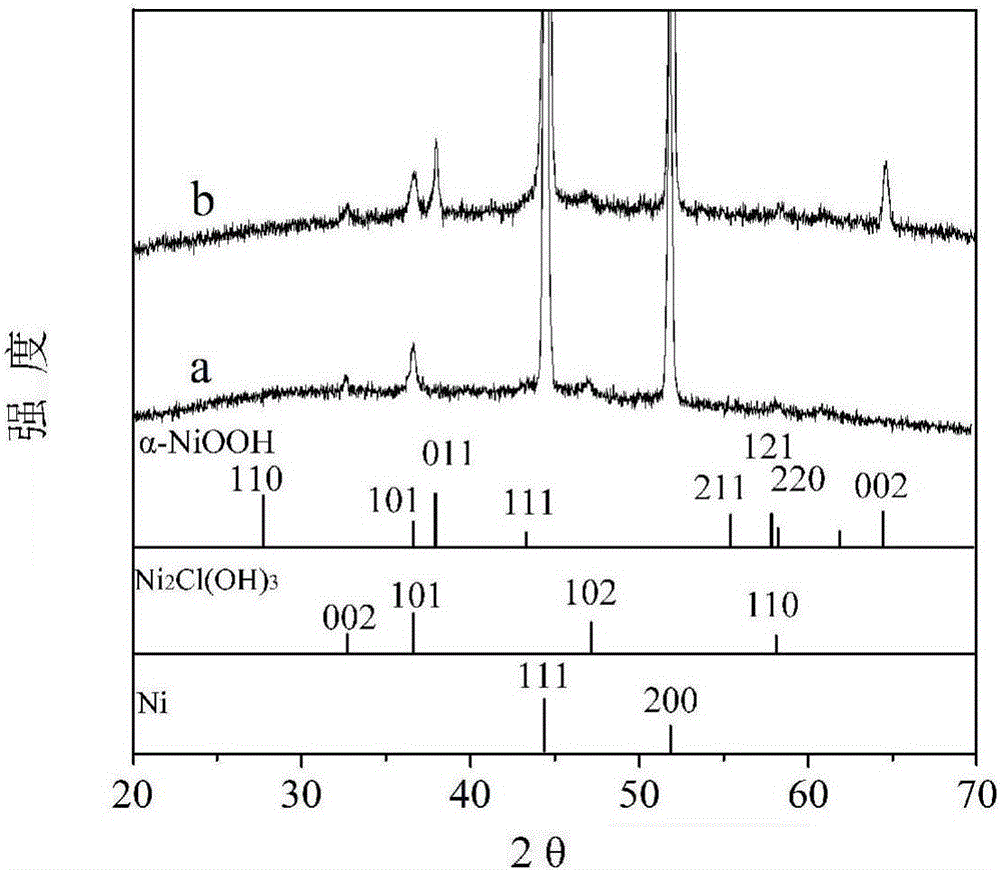
圖1為實施例1中步驟5)得到的泡沫鎳上的Ni2Cl(OH)3(曲線a)和步驟6)得到的α-NiOOH(曲線b)樣品的XRD圖。
圖2為實施例1中步驟5)得到的泡沫鎳上的Ni2Cl(OH)3的不同放大倍數的SEM圖(圖a和圖b)和EDX譜圖(c);以及步驟6)得到的α-NiOOH的不同放大倍數的SEM圖(圖d和圖e)和EDX譜圖(f)。
圖3為實施例1中步驟6)中得到的α-NiOOH納米片的TEM圖像(a),HRTEM圖像(b)和SAED圖像(c)。
圖4為實施例1中步驟6)中得到的α-NiOOH納米片的XPS圖譜,其中包括全譜(a),Ni譜(b),O譜(c);以及α-NiOOH和泡沫鎳基底(NF)的Raman圖譜(d)。
圖5a至f為實施例1步驟6)中得到的α-NiOOH/NF、實施例1步驟5)中得到的Ni2Cl(OH)3/NF、對比實施例2的Ni/NF、對比實施例1的NiO/NF和NF(泡沫鎳載體)的LSV曲線,塔菲爾曲線,阻抗譜,循環伏安曲線,電流密度-掃速圖,以及電流-時間圖。
圖6為1.50V(相對于標準氫電極)下氣體量的理論值與測量值隨時間變化曲線。
圖7為對比實施例1制備的泡沫鎳負載NiO的掃描電鏡(SEM)照片。
圖8為對比實施例1制備的泡沫鎳負載NiO的XRD譜圖。
圖9為對比實施例2制備的樣品的掃描電鏡(SEM)照片。
圖10為根據對比實施例3制備的樣品的掃描電鏡(SEM)照片。
圖11為根據對比實施例4制備的樣品的掃描電鏡(SEM)照片。
圖12為根據對比實施例5制備的樣品的掃描電鏡(SEM)照片。
具體實施方式
在根據本發明的制備方法中鎳(Ⅱ)與丁二酮肟的摩爾比為1:0.5至1:8,優選為1:1至1:4,更優選為1:1.5至1:3,最優選為1:2。當鎳(Ⅱ)與丁二酮肟的摩爾比大于1:0.5時,即二價鎳過量,則在泡沫鎳表面更易形成納米盤狀鎳,且無規則的堆疊在一起覆蓋在泡沫鎳表面;而當鎳(Ⅱ)與丁二酮肟的摩爾比小于1:8時,即二價鎳不足,則很難形成規則的鎳納米片。考慮到基材泡沫鎳的性質,優選鎳(Ⅱ)與丁二酮肟的摩爾比為為1:1.5至1:3,最優選為1:2。
以下,將詳細地描述本發明。在進行描述之前,應當理解的是,在本說明書和所附的權利要求書中使用的術語不應解釋為限制于一般含義和字典含義,而應當在允許發明人適當定義術語以進行最佳解釋的原則的基礎上,根據與本發明的技術方面相應的含義和概念進行解釋。因此,這里提出的描述僅僅是出于舉例說明目的的優選實例,并非意圖限制本發明的范圍,從而應當理解的是,在不偏離本發明的精神和范圍的情況下,可以由其獲得其他等價方式或改進方式。
在下文中,將參照附圖詳細地描述本公開的優選的實施方式。在描述之前,應當了解在說明書和所附權利要求中使用的術語,并不應解釋為局限于一般及辭典意義,而是應當基于允許發明人為最好的解釋而適當定義術語的原則,基于對應于本發明技術層面的意義及概念進行解釋。因此,在此的描述僅為說明目的的優選實例,而并非是意指限制本發明的范圍,因而應當了解的是,在不偏離本發明的精神和范圍下可以做出其他等同實施和修改。除非特別聲明,以下實施例中采用的試劑和儀器均為市售可得產品。
實施例1:泡沫鎳負載的α-NiOOH納米片的制備
1)泡沫鎳的預處理:在室溫下,將1cm×3cm的泡沫鎳在3.0M HCl溶液中超聲15min,然后依次用去離子水、無水乙醇清洗數次,放置在空氣中備用。
2)鎳(Ⅱ)溶液的制備:稱取0.5mmol的NiCl2·6H2O固體,溶解于20mL去離子水中。
3)丁二酮肟醇溶液的制備:稱取1mmol丁二酮肟固體,溶解于20mL無水乙醇中。
4)依次取上述步驟2)和3)中溶液各8mL加入反應釜的聚四氟乙烯內襯中,攪拌10min后,將預處理過的泡沫鎳豎直浸入其中,擰緊釜蓋,將反應釜放入到200℃的電熱鼓風干燥箱中,并保持6h。
5)取出反應釜自然冷卻到室溫狀態,傾倒掉上清液,用去離子水清洗掉表面沉淀物,得到長滿豎直排列Ni2Cl(OH)3納米片的泡沫鎳。
6)將步驟5)中得到的產物放入150℃的電熱鼓風干燥箱中,并保持12h,得到豎直排列的α-NiOOH納米片。
圖1為步驟5)中得到的泡沫鎳上的Ni2Cl(OH)3(曲線a)和步驟6)中得到的α-NiOOH(曲線b)樣品的XRD圖。
圖2為步驟5)中得到的泡沫鎳上的Ni2Cl(OH)3的不同放大倍數的SEM圖(圖a和圖b)和EDX譜圖(c);以及步驟6)中得到的α-NiOOH的不同放大倍數的SEM圖(圖d和圖e)和EDX譜圖(f)。
從圖1和圖2中可以看出泡沫鎳表面形成的Ni2Cl(OH)3和α-NiOOH都很好的晶化,其中α-NiOOH為斜方晶型。含Ni納米片在泡沫鎳表面均勻形成,所述α-NiOOH納米片長約0.5至1.5μm,寬度約為10-30nm,高度約為50-100nm。所述α-NiOOH納米片在泡沫鎳表面上豎直排列,有效地增加了比表面積。
圖3為步驟6)中得到的α-NiOOH納米片的TEM圖像(a),HRTEM圖像(b)和SAED圖像(c)。從圖中也可以看出形成的α-NiOOH納米片為納米薄片,長約為100至400nm,寬約100-300nm。
圖4為步驟6)中得到的α-NiOOH納米片的XPS圖譜,其中包括全譜(a),Ni譜(b),O譜(c);以及α-NiOOH和泡沫鎳基底(NF)的Raman圖譜(d)。從圖4a中可以看出,所述樣品的表面的主要元素為Ni元素和O元素,圖4b中Ni元素的2p3/2(855.1和855.9eV)和2p1/2(872.6和873.7eV)的軌道結合能數值經與文獻比對分別對應于Ni2+和Ni3+的存在,圖4c中O元素的軌道結合能(530.4eV)則說明了Ni-O鍵的存在,圖4d所述樣品中461cm-1和533cm-1處的峰表示Ni-O鍵的存在,3595cm-1處的峰表示所述樣品中OH-和水分子之間相互作用的H鍵。
對比實施例1:不同的干燥溫度
除了在步驟6)中將步驟5)中得到的產物放入升溫速率為1℃每分鐘350℃的馬弗爐中煅燒2小時以外,按照實施例1相同的方法制備泡沫鎳負載Ni的產品(NiO/NF)。
圖7為本實施例制備的泡沫鎳負載NiO的掃描電鏡(SEM)照片。圖8為本實施例制備的泡沫鎳負載NiO的XRD譜圖。從中可以看出,雖然在泡沫鎳(NF)表面也形成納米片,但該納米片為NiO,而非α-NiOOH,并且得到的納米片的形貌不規整,表面有塌陷,在作為電極使用時效率非常低。
對比實施例2:不加鎳(Ⅱ)溶液前驅體
1)泡沫鎳的預處理:在室溫下,將1cm×3cm的泡沫鎳在3.0M HCl溶液中超聲15min,然后依次用去離子水、無水乙醇清洗數次,放置在空氣中備用。
2)丁二酮肟醇溶液的制備:稱取1mmol丁二酮肟固體,溶解于20mL無水乙醇中。
3)取上述步驟2)中溶液8mL加入反應釜的聚四氟乙烯內襯中,攪拌10min后,將預處理過的泡沫鎳豎直浸入其中,擰緊釜蓋,將反應釜放入到200℃的電熱鼓風干燥箱中,并保持12h。
圖9為根據對比實施例2制備的樣品的掃描電鏡(SEM)照片,其中可以看出形成了大量Ni納米微球,而不是納米片結構。
對比實施例3:不加丁二酮肟
除了不入加丁二酮肟以外,按照實施例1相同的方法制備泡沫鎳負載型電極材料。
圖10為根據對比實施例3制備的樣品的掃描電鏡(SEM)照片,其中可以看出在未添加丁二酮肟的情況下,無法形成納米片結構。
對比實施例4:EDTA代替丁二酮肟
除了用EDTA(乙二胺四乙酸)代替丁二酮肟以外,按照實施例1相同的方法制備泡沫鎳負載型電極材料。
圖11為根據對比實施例4制備的樣品的掃描電鏡(SEM)照片,其中可以看出用EDTA代替丁二酮肟的情況下,無法形成納米片結構。
對比實施例5:乙二胺代替丁二酮肟
除了用乙二胺代替丁二酮肟以外,按照實施例1相同的方法制備泡沫鎳負載型電極材料。
圖12為根據對比實施例5制備的樣品的掃描電鏡(SEM)照片,其中可以看出用乙二胺代替丁二酮肟的情況下,無法形成納米片結構。
實驗實施例1
采用北京華科普天科技有限公司的電化學工作站(CHI 660D)測量樣品的各種電學性質。在三電極體系中,將所制備樣品作為工作電極分別進行析氧反應的線性掃描伏安測量、塔菲爾曲線測量、阻抗譜測量、活性面積測量及穩定性測量。
使用三電極體系進行電化學測試,其中所制備的樣品作為工作電極,Hg/HgO作為參比電極,Pt片作為對電極,電解質溶液為1.0M氫氧化鉀(pH=13.6)。
根據能斯特方程:ERHE=EHg/HgO+0.098+0.059×pH(25℃時汞/氧化汞電極標準電位:0.098V)ERHE=EHg/HgO+0.098+0.059×13.6=EHg/HgO+0.9004
線性掃描伏安法(LSV)是指施加在工作電極上的電勢是時間的線性函數,測量電流密度隨電勢(也即隨時間)的變化,從而在三電極體系中研究工作電極的性質。
線性掃描伏安法參數:
初始電位(V):0
終止電位(V):0.9
掃描速度(V s-1):0.002
采樣間隔(V):0.001
靜置時間(s):2
靈敏度(A/V):0.1
圖5a為實施例1步驟6)中得到的α-NiOOH/NF、實施例1步驟5)中得到的Ni2Cl(OH)3/NF、對比實施例2的Ni/NF、對比實施例1的NiO/NF和NF(泡沫鎳載體)的LSV曲線;圖5b為實施例1步驟6)中得到的α-NiOOH/NF、實施例1步驟5)中得到的Ni2Cl(OH)3/NF、對比實施例2的Ni/NF、對比實施例1的NiO/NF和NF(泡沫鎳載體)的塔菲爾曲線;圖5c為實施例1步驟6)中得到的α-NiOOH/NF、實施例1步驟5)中得到的Ni2Cl(OH)3/NF、對比實施例2的Ni/NF、對比實施例1的NiO/NF和NF(泡沫鎳載體)電極在1.50V(相對于標準氫電極)電壓下,從106到0.01Hz頻率范圍的阻抗譜;圖5d為在非法拉第效應區域(1.0-1.1V vs.標準氫電極),不同掃速下(10到100mV s-1)實施例1步驟6)中得到的α-NiOOH/NF的循環伏安曲線;圖5e為1.05V(vs.標準氫電極)電壓下,實施例1步驟6)中得到的α-NiOOH/NF的電流密度-掃速圖;圖5f為1.52V(vs.標準氫電極)電壓下,實施例1步驟6)中得到的α-NiOOH/NF的電流-時間圖。從圖中可以讀出實施例1步驟6)中得到的α-NiOOH/NF樣品在10mA/cm2處的過電勢為266mV,而對比樣品Ni2Cl(OH)3/NF在10mA/cm2處的過電勢為325mV,NiO/NF在10mA/cm2處的過電勢為326mV,Ni/NF在10mA/cm2處的過電勢為359mV;此外,與對照樣品相比,所述樣品α-NiOOH/NF的電流密度在1.50V之后迅速增大,展現了很好的電化學OER活性。
塔菲爾曲線是指符合Tafel關系的曲線,一般指極化曲線中強極化區的一段,通過斜率的大小可以反映出電化學過程中的反應動力學活性,斜率越小,反應動力學活性越高。
塔菲爾曲線是根據線性掃描極化曲線推斷而來,其中橫坐標為log(j)(毫安/平方厘米),縱坐標為電位(伏)。從圖5中可以看出實施例1步驟6)中得到的α-NiOOH/NF樣品的塔費爾斜率為76.3mV dec-1,明顯低于對比樣品Ni2Cl(OH)3/NF(154.2mV dec-1),Ni/NF(113.1mV dec-1),NiO/NF(106.6mV dec-1)和NF(142mV dec-1)。
電化學阻抗譜是用來進一步研究析氧反應的動力學催化活性的方法之一。可以從電化學阻抗譜中得到溶液阻抗和反應過程中的電荷轉移電阻。
交流阻抗法參數:
初始電平(伏):0.6
高頻(赫茲):1000000
低頻(赫茲):0.01
振幅(伏):0.005
靜置時間(秒):2
從圖5c中可以看出在1.50V(相對于標準氫電極)電壓下,所有樣品的溶液電阻電解液電阻均小于1.19Ω,α-NiOOH/NF的電荷轉移電阻為1.60Ω,而Ni2Cl(OH)3/NF(19.66Ω),Ni/NF(24.72Ω),NiO/NF(37.08Ω)泡沫鎳(42.12Ω)。較低的電荷轉移電阻值表明α-NiOOH/NF在電化學反應中具有快速的電荷轉移能力。
活性面積的測量是在非法拉第效應區域(相對于標準氫電極1.0-1.1V),測量不同掃速下的循環伏安曲線獲得,用以表征材料上活性位點數目的多少。循環伏安法參數:
初始電位(伏):0.1
高電位(伏):0.2
低電位(伏):0.1
終止電位(伏):0
掃描速度(伏/秒):0.010,0.020,0.040,0.060,0.080,0.100
掃描段數:6
采樣間隔(伏):0.001
靜置時間(秒):2
靈敏度(安/伏):0.1
分別測量0.010、0.020、0.040、0.060、0.080、0.100伏/秒掃速下的循環伏安曲線,選取1.05V(相對于標準氫電極)下的電流密度,作電流密度-掃速圖,直線斜率的一半極為活性面積值,2340μFcm-2。
穩定性曲線是利用電流-時間法在1.52V(相對于標準氫電極)電壓下,連續測量24小時獲得,用來表征材料的穩定性。
電流-時間曲線參數:
初始電位(伏):0.62
采樣間隔(秒):0.1
實驗時間(秒):86400
靜置時間(秒):0
靈敏度(安/伏):0.1
從圖5f中可以看出,在持續的電化學測量期間,樣品α-NiOOH/NF表現出了很好的穩定性。
在三電極體系中,將所制備樣品分別作為陰、陽極進行電解水過程中法拉第效率的測試。
使用三電極體系進行電解水過程中法拉第效率的測試中,工作電極和對電極均為實施例1步驟6)中得到的α-NiOOH/NF樣品,參比電極為Hg/HgO電極,在1.50V(相對于標準氫電極)電壓下電解水6小時,并收集前兩小時的氣體(用1mL的進樣針每隔20分鐘取一次氣),做出附有理論值和實驗值的產氣量-時間圖。
氣相色譜型號GC 2060,上海銳敏儀器有限公司,實驗參數:
柱溫:40℃
檢測器:120℃
進樣器:110℃
柱前壓:0.06MPa
載氣流量10mL/min
1mL進樣
圖6為1.50V(相對于標準氫電極)下氣體量的理論值與測量值隨時間變化曲線。從圖中可以看出隨著時間的變化,實際產氣量和理論值能夠很好的吻合,表明了電解水過程中的法拉第效率幾乎能達到100%,且產生的氧氣和氫氣的摩爾比為1:2。
- 還沒有人留言評論。精彩留言會獲得點贊!