一種催化硝基苯酚氫化還原的催化劑及其應用的制作方法
本發明涉及納米催化劑技術領域,具體涉及一種催化硝基苯酚氫化還原的催化劑及其應用。
背景技術:
氨基苯酚是一種重要的有機合成中間體,在制藥行業中一般用來制備撲熱息痛、維生素B、退熱冰、非那西汀等各類止痛藥物;在染料行業中一般用于制備木制品的著色劑和毛發的染色劑。另外,還可用于照像顯影劑、橡膠防老劑和尿素加成反應的抑制劑等,是一種用途廣泛的化工原料。硝基苯酚是一類高毒性、難降解、最難以治理的一類化合物,因此芳香烴類化合物廢水的凈化是我國乃至世界的技術難題。需要開發經濟綠色催化劑把硝基苯酚還原成毒性很小的氨基苯酚。雖然此類還原方法很多,但是被工業生產所廣泛采用的只有硝基苯酚電解還原法和硝基苯酚催化氫化法。硝基苯酚電解還原法對反應器的設計及工藝條件控制有較高的技術要求,且能耗較高。硝基苯酚催化氫化法原料價廉易得、生產成本低、工序少、重復利用性好,這種方法在還原過程中一般都需要高效催化劑,且能夠重復利用。
隨著納米技術的迅速崛起,已廣泛的應用在催化、醫藥、新能源和環境保護等領域。納米微粒由于尺寸小,比表面積大,表面的鍵態和電子態與顆粒內部不同,表面原子配位不全等導致表面的活性位增加,因而催化劑微粒尺寸納米化將進一步大大提高催化效率。目前用于催化硝基化合物加氫還原的多相催化劑大部分為含貴金屬(Ag、Au、Pd和Pt及其合金)納米粒子的納米催化劑。貴金屬納米催化劑盡管具有較高的催化活性,但其成本較高,且在使用過程中易于團聚或中毒失活從而降低其催化效率。因此,開發成本低廉且能高效催化的非貴金屬催化劑用于溫和條件下氫化還原硝基苯酚制氨基苯酚對降低工業生產成本具有重要作用。
技術實現要素:
針對現有技術的不足,本發明提供了一種成本低廉、催化活性高的催化硝基苯酚氫化還原的催化劑及其應用。
為實現以上目的,本發明通過以下技術方案予以實現:
一種催化硝基苯酚氫化還原的催化劑,所述催化劑為直徑在60-80nm的氯氧鉍超薄納米片,對催化還原鄰、間、對硝基苯酚制相應的氨基苯酚均具有很高的催化活性。
催化硝基苯酚氫化還原的催化劑的制備方法,步驟如下:
1)將甘露醇和聚乙烯吡咯烷酮(PVP,K-30)溶于蒸餾水中,攪拌溶解,配制含0.15-0.20mmol/L聚乙烯吡咯烷酮的0.01mol/L的甘露醇水溶液A;
2)將五水合硝酸鉍溶于乙二醇中,室溫下超聲形成0.2mol/L五水合硝酸鉍的溶液B;
3)將氯化鈉溶于乙二醇中,室溫下超聲形成0.2mol/L氯化鈉溶液C;
4)將溶液B和溶液C分別先后加入溶液A中,攪拌均勻,轉移到水熱反應釜中,密封,在160-165℃下保溫7-8h,反應結束后冷卻至室溫;
5)將反應釜內生成的沉淀物經離心分離、蒸餾水洗滌和干燥,即得到氯氧鉍超薄納米片催化劑。
優選地,所述溶液A、溶液B、溶液C的體積比為6:1:1。
催化硝基苯酚氫化還原的催化劑的應用,是將氯氧鉍超薄納米片催化劑超聲分散于濃度為0.1mmol/L的硝基苯酚水溶液中,然后加入硼氫化鈉,室溫下靜置反應,5-10min即可使硝基苯酚全部氫化還原成氨基苯酚,反應結束后催化劑可回收重復利用。
優選地,所述催化劑、硝基苯酚水溶液和硼氫化鈉的質量/體積/質量比(g:L:g)為0.1-0.4:3:0.5。
本發明與現有技術相比,具有以下有益效果:
1、本發明制備的氯氧鉍(BiOCl)超薄納米片,納米片直徑為60-80nm、厚度約5nm,比表面積高達39.2m2/g,用于催化還原鄰、間、對三種硝基苯酚制備相應的氨基苯酚,均具有很高的催化活性;
2、制備BiOCl超薄納米片所采用的原料價廉易得,且制備條件溫、簡單易行;
3、將BiOCl超薄納米片用于催化還原硝基苯酚制氨基苯酚,催化反應條件溫和,常溫常壓下反應,且反應速度快,易于操作;
4、BiOCl超薄納米片催化劑可回收重復使用,循環性好,在催化還原硝基苯酚制氨基苯酚的反應中可以代替貴金屬催化劑,降低成本。
附圖說明
為了更清楚地說明本發明實施例或現有技術中的技術方案,下面將對實施例或現有技術描述中所需要使用的附圖作簡單地介紹,顯而易見地,下面描述中的附圖僅僅是本發明的一些實施例,對于本領域普通技術人員來講,在不付出創造性勞動的前提下,還可以根據這些附圖獲得其他的附圖。
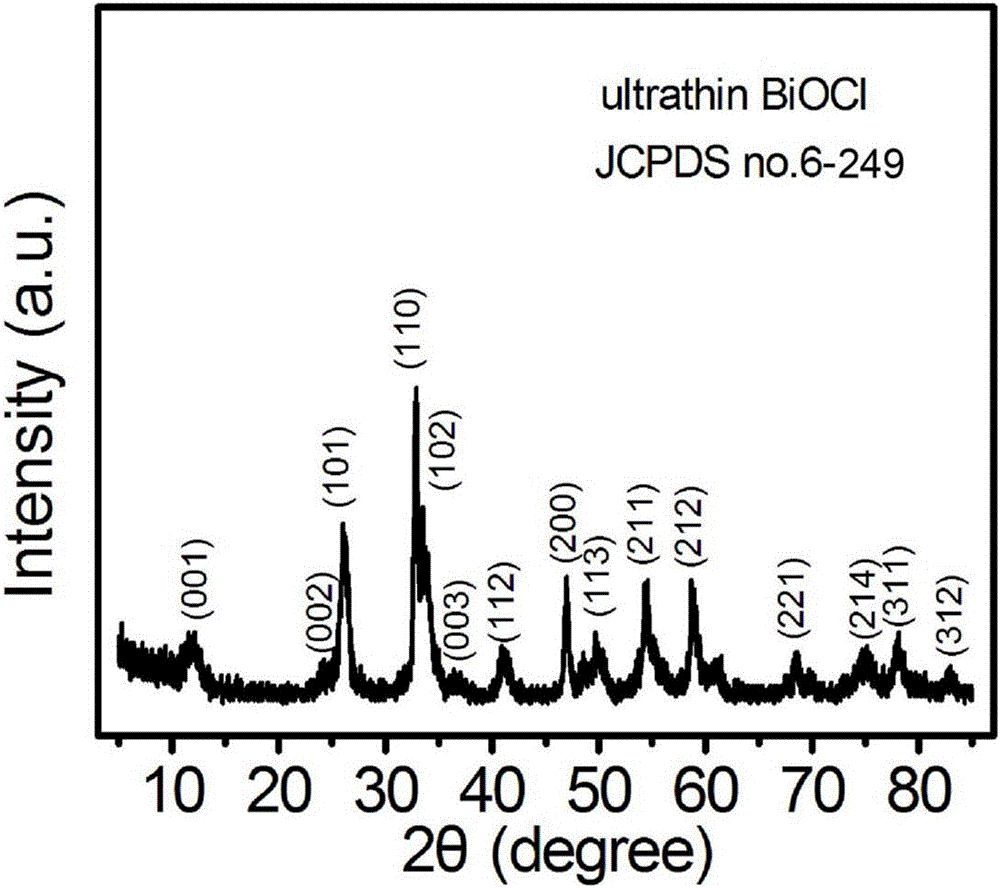
圖1為本發明實施例1制備的氯氧鉍的X射線衍射圖(XRD);
圖2為本發明實施例1制備的氯氧鉍的掃描電鏡圖(SEM);
圖3為本發明實施例1制備的氯氧鉍的透射電鏡圖(TEM);
圖4為本發明實施例1制備的氯氧鉍的原子力顯微鏡圖(AFM)及數據分析;
圖5為本發明實施例1制備的氯氧鉍的氮氣吸附-脫附等溫曲線,插圖為對應的孔徑分布曲線。
圖6為實施例2中制備的氯氧鉍催化還原鄰硝基苯酚的曲線圖,其中圖6a為催化還原鄰硝基苯酚的紫外-可見吸收曲線圖;圖6b為催化還原鄰硝基苯酚體系中鄰硝基苯酚濃度隨時間變化曲線圖。
圖7為實施例3中氯氧鉍催化還原間硝基苯酚的曲線圖,其中圖7a為催化還原間硝基苯酚的紫外-可見吸收曲線圖;圖7b為催化還原間硝基苯酚體系中間硝基苯酚濃度隨時間變化曲線圖。
圖8為實施例4中氯氧鉍催化還原對硝基苯酚的曲線圖,其中圖8a為催化還原對硝基苯酚的紫外-可見吸收曲線圖;圖8b為催化還原對硝基苯酚體系中對硝基苯酚濃度隨時間變化曲線圖。
具體實施方式
為使本發明實施例的目的、技術方案和優點更加清楚,下面將結合本發明實施例中的附圖,對本發明實施例中的技術方案進行清楚、完整地描述,顯然,所描述的實施例是本發明一部分實施例,而不是全部的實施例。基于本發明中的實施例,本領域普通技術人員在沒有作出創造性勞動前提下所獲得的所有其他實施例,都屬于本發明保護的范圍。
實施例1:
氯氧鉍(BiOCl)超薄納米片的制備:
a.將0.6mmol甘露醇和0.4g聚乙烯吡咯烷酮(PVP,K-30)溶于60mL蒸餾水中,攪拌溶解;
b.將2.0mmol五水合硝酸鉍溶于10mL乙二醇中,室溫下超聲形成溶液;
c.將2.0mmol氯化鈉溶于10mL乙二醇中,室溫下超聲形成溶液;
d.將步驟b和步驟c所配制的溶液分別先后加入步驟a的溶液中,攪拌均勻得到反應溶液;
e.將步驟d中的反應溶液移入到容積為50mL的水熱反應釜中,然后將水熱反應釜密封,在160℃保溫8h,反應結束冷卻至室溫,將反應釜內生成的沉淀物經離心分離、蒸餾水洗滌和干燥,即得到BiOCl超薄納米片催化劑。
利用XRD對制備的氯氧鉍樣品物相進行表征,從圖1中可以看出得到的樣品物相很純,為純四方相BiOCl;采用SEM電鏡、TEM、AFM對樣品進行形貌表征,從圖2、圖3和圖4中可以看出制備的氯氧鉍微觀形貌是直徑為50-80nm、厚度約為5nm的超薄納米片,且形貌均一、分布均勻。
對制備的氯氧鉍進行比表面積測試及微孔分布測試,從圖5中可以計算出,氯氧鉍的比表面積為39.2m2/g,大的比表面積和微孔的存在使得樣品具有較大的吸附和催化能力。
實施例2:
催化還原鄰硝基苯酚制鄰氨基苯酚
a.稱量10mg氯氧鉍超薄納米片超聲分散于10mL蒸餾水中;
b.移取0.1mL步驟a配制的懸浮液,加入到2.7mL鄰硝基苯酚水溶液(濃度為0.1mM)中;
c.稱量0.1134g硼氫化鈉溶于10ml冰水中,移取0.4ml加入到步驟b得到的溶液中,快速混合均勻,反應開始;
d.每隔1min用紫外-可見分光光度計檢測步驟c中反應溶液的吸收光譜,實時檢測反應進程,直到400nm左右的峰不再有明顯的變化。
從圖6a中可以看出,鄰硝基苯酚本身的特征吸收峰在351nm處,但加入硼氫化鈉之后,因為在堿性條件下形成鄰硝基酚鹽離子,特征吸收峰紅移到415nm處,隨著催化反應進行并持續,在415nm處的特征吸收峰逐漸降低,同時在265-320nm范圍內產生新的吸收峰并且強度逐漸增加,這是由于鄰硝基苯酚離子轉化成了鄰氨基苯酚,直至最終完全轉化;圖6b為實施例2催化反應體系中鄰硝基苯酚濃度隨時間變化情況曲線,僅需7分鐘就可以將溶液中的鄰硝基苯酚幾乎完全轉化成鄰氨基苯酚,還原率達到95%。
實施例3:
催化還原間硝基苯酚制間氨基苯酚
a.稱量10mg氯氧鉍超薄納米片超聲分散于10mL蒸餾水中;
b.移取0.1mL步驟a配制的懸浮液,加入到2.7mL間硝基苯酚水溶液(濃度為0.1mM)中;
c.稱量0.1134g硼氫化鈉溶于10ml冰水中,移取0.4ml加入到步驟b得到的溶液中,快速混合均勻,反應開始;
d.用紫外-可見分光光度計檢測步驟c中反應溶液的吸收光譜,可實時檢測反應進程。
圖7a為實施例3催化還原間硝基苯酚生成間氨基苯酚過程中反應溶液的紫外-可見吸收光譜圖,間硝基苯酚本身的特征吸收峰在350nm處,但加入硼氫化鈉之后,因為在堿性條件下形成間硝基酚鹽離子,特征吸收峰紅移到400nm處,隨著催化反應進行并持續,在400nm處的特征吸收峰逐漸降低,同時在300nm左右產生新的吸收峰并且強度逐漸增加,這是由于間硝基苯酚離子轉化成了間氨基苯酚,直至最終完全轉化;圖7b為實施例3催化反應體系中間硝基苯酚濃度隨時間變化情況曲線,可以看出僅需2.5分鐘就可以將溶液中的間硝基苯酚完全轉化成間氨基苯酚,還原率達到100%。
實施例4:
催化還原對硝基苯酚制對氨基苯酚
a.稱量10mg氯氧鉍超薄納米片超聲分散于10mL蒸餾水中;
b.移取0.1mL步驟a配制的懸浮液,加入到3.0mL對硝基苯酚水溶液(濃度為0.1mM)中;
c.稱量0.1134g硼氫化鈉溶于10ml冰水中,移取0.4ml加入到步驟b得到的溶液中,快速混合均勻,反應開始;
d.用紫外-可見分光光度計檢測步驟c中反應溶液的吸收光譜,可實時檢測反應進程。
圖8a為實施例4催化還原對硝基苯酚生成對氨基苯酚過程中反應溶液的紫外-可見吸收光譜圖,對硝基苯酚本身的特征吸收峰在317nm處,但加入硼氫化鈉之后,因為在堿性條件下形成對硝基酚鹽離子,特征吸收峰紅移到400nm處,隨著催化反應進行并持續,在400nm處的特征吸收峰逐漸降低,同時在233nm和300nm左右產生兩個新的吸收峰并且強度逐漸增加,這是由于對硝基苯酚離子轉化成了對氨基苯酚,直至最終完全轉化;圖8b為實施例4催化反應體系中對硝基苯酚濃度隨時間變化情況曲線,可以看出僅需7分鐘就可以將溶液中的對硝基苯酚完全轉化成對氨基苯酚,還原率達到100%。
需要說明的是,在本文中,諸如第一和第二等之類的關系術語僅僅用來將一個實體或者操作與另一個實體或操作區分開來,而不一定要求或者暗示這些實體或操作之間存在任何這種實際的關系或者順序。而且,術語“包括”、“包含”或者其任何其他變體意在涵蓋非排他性的包含,從而使得包括一系列要素的過程、方法、物品或者設備不僅包括那些要素,而且還包括沒有明確列出的其他要素,或者是還包括為這種過程、方法、物品或者設備所固有的要素。在沒有更多限制的情況下,由語句“包括一個……”限定的要素,并不排除在包括所述要素的過程、方法、物品或者設備中還存在另外的相同要素。
以上實施例僅用以說明本發明的技術方案,而非對其限制;盡管參照前述實施例對本發明進行了詳細的說明,本領域的普通技術人員應當理解:其依然可以對前述各實施例所記載的技術方案進行修改,或者對其中部分技術特征進行等同替換;而這些修改或者替換,并不使相應技術方案的本質脫離本發明各實施例技術方案的精神和范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 一種手性三齒膦胺酸配體及其在不對稱催化反應中的應用的制造方法與工藝
- 一種手性雙齒氮膦配體及其在不對稱催化反應中的應用的制造方法與工藝
- Pd?C催化氫化脫除4?硝基芐基制備7?ACCA的方法與制造工藝
- 一種固載型路易斯酸硝化催化劑制備芳香硝基化合物的方法與制造工藝
- 一種催化硝基苯酚氫化還原的催化劑及其應用的制造方法與工藝
- 具有良好電催化產氫性能的超薄單層金屬性二硒化釩納米片的宏量制備方法與制造工藝
- 合成氣一步法制低碳烯烴的流化床催化劑及其制備方法與制造工藝
- 合成氣直接制備低碳烯烴的Fe-Mn系催化劑及其制備方法與制造工藝
- 合成氣一步制低碳烯烴的催化劑及其制備方法與制造工藝
- 合成氣一步法制低碳烯烴的流化床催化劑及其制備方法與制造工藝