一種四元復合材料及其制備方法和應用與流程
本發明涉及元素分離
技術領域:
,具體涉及一種四元復合材料及其制備方法和應用。
背景技術:
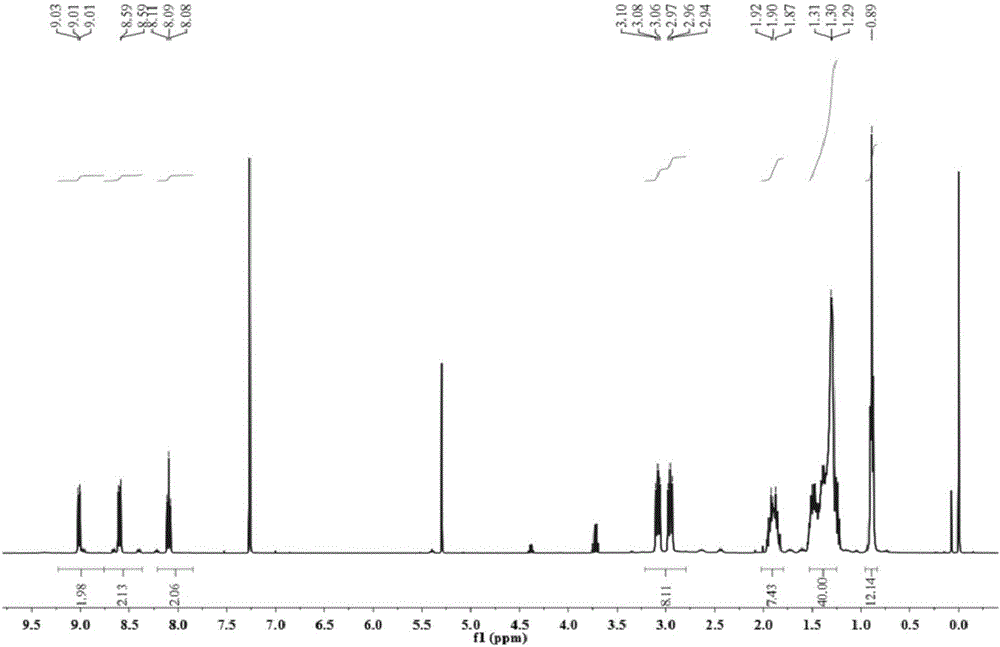
:鈷、鎳是貴重的有色金屬,在國防、航天、原子能、化工、電子等高科技領域都有廣泛的用途。鈷鎳原料除了原生礦物還包括大量的廢棄鐵鎳鈷合金,如報廢的機器、廢舊電池、失效催化劑、廢功能合金、冶煉廢渣等。廢棄鐵鎳鈷合金中含有大量的有價金屬鎳和鈷,對其進行處理回收有利于資源的循環利用,對社會可持續發展具有重要意義。廢棄鐵鎳鈷合金的主要來源是廢可伐合金電子元件、廢高磁合金鋼和廢鎳催化劑等,其常用的處理流程主要包括以下步驟:1)有價金屬的酸性浸出,2)浸出溶液的沉淀除鐵,3)凈化后的鈷鎳溶液萃取分離,4)反萃、沉淀分別得到鈷鎳化合物,5)進一步煅燒、氫氣還原得到鈷粉、鎳粉,該處理流程的關鍵步驟是除鐵和鈷鎳分離。在冶金行業分離工業中,需要將鈷鎳與鐵等其他金屬元素進行分離,現有技術中,尚缺乏簡單可行的技術手段。技術實現要素:本發明提供了一種四元復合材料及其制備方法和應用,四元復合材料吸附能力強,選擇性好,且制備方法簡單易行,適用于冶金行業分離工業中將鈷和鎳同元素鐵進行分離后回收利用。一種四元復合材料,以弱極性大孔樹脂為載體,載體上同時負載如結構式Ⅰ所示的化合物Ⅰ、如結構式Ⅱ所示的化合物Ⅱ和如結構式Ⅲ所示的化合物Ⅲ;本發明中將三種具有特異性吸附功能的化合物與弱極性大孔樹脂相復合,得到的四元復合材料對于鈷和鎳具有特異性吸附作用,用于從含有堿金屬、堿土金屬、稀土元素以及典型過渡金屬的多元素酸性水溶液中,將鈷和鎳分離出來。鈷和鎳的進一步分離可以采用現有技術。作為優選,化合物Ⅰ、化合物Ⅱ和化合物Ⅲ等質量負載在載體上。載體上同時負載相同質量的化合物Ⅰ(雙三嗪雙吡啶衍生物)、化合物Ⅱ(超分子識別試劑杯[4]單冠醚,正丙基-杯[4]單冠-6,簡稱BnPCalix[4]MC6)和化合物Ⅲ(2-叔丁基-2環己基-18-冠-6),三種負載物之間相互協同,產生對鈷和鎳特異性吸附的效果。所述載體為離子交換樹脂XAD-7。離子交換樹脂XAD-7作為一種已經市場化的弱極性大孔樹脂材料,原料易得。作為優選,化合物Ⅰ的與載體的質量比為1:8-10。化合物Ⅱ和化合物Ⅲ的負載量與化合物Ⅰ相同。本發明還提供了一種所述的四元復合材料的制備方法,包括以下步驟:將化合物Ⅰ、化合物Ⅱ和化合物Ⅲ溶于二氯甲烷中,在所得溶液中加入載體混合均勻,經旋蒸干燥后,得到四元復合材料。化合物Ⅰ、化合物Ⅱ和化合物Ⅲ的質量比為1:1:1,每g化合物Ⅰ溶解于450-550mL二氯甲烷中,旋蒸時,使大部分二氯甲烷揮發至近干狀態,在毛細作用以及物理吸附作用下,化合物分子進入載體的空隙中,然后將近干狀態的物料在50-60℃下真空干燥至少24小時,得到四元復合材料。本發明還提供了一種利用所述的四元復合材料分離鈷和鎳的方法,將四元復合材料與含有多種金屬離子的硝酸水溶液混合,硝酸水溶液中的鈷離子和鎳離子被四元復合材料吸附分離,所述硝酸水溶液中含有Co(Ⅱ)、Ni(Ⅱ)和其他金屬離子,其他金屬離子為Li(I)、Na(I)、K(I)、Rb(I)、Ca(Ⅱ)、Mg(Ⅱ)、Ba(Ⅱ)、Nd(Ⅲ)、La(Ⅲ)、Ru(Ⅲ)、Yb(Ⅲ)、Y(Ⅲ)、Fe(Ⅲ)、Zr(Ⅳ)中的至少一種。作為優選,每g四元復合材料與20-30mL硝酸水溶液混合。本發明提供的四元復合材料選擇性好,分離效率高,少量使用,即能達到理想的分離效果。為了保證分離效果,優選地,四元復合材料與含有多種金屬離子的硝酸水溶液在室溫下(25±5℃)混合吸附,吸附時間為120-180min。混合吸附在振蕩條件下進行,振蕩速率為120-150rpm。在進行元素分離時,硝酸水溶液中硝酸的濃度以及硝酸水溶液中金屬離子的濃度均會影響分離效果,優選地,硝酸水溶液中,硝酸的濃度為2-6mol/L。硝酸水溶液中,每種金屬離子的濃度為5.0×10-4-1.0×10-3M。本發明提供的四元復合材料吸附能力強,選擇性好,且制備方法簡單易行,適用于冶金行業分離工業中將鈷和鎳同元素鐵進行分離后回收利用。附圖說明圖1為實施例1合成的目標產物C8-BTBP的MS-ESI陽離子圖譜;圖2為實施例1合成的目標產物C8-BTBP的1HNMR圖譜;圖3為實施例2制備的四元復合材料從硝酸水溶液中分離元素鈷和鎳的分配系數隨硝酸濃度變化的關系圖。具體實施方式實施例1C8-BTBP的合成C8-BTBP合成的化學反應方程式如下所示:具體步驟如下:在500mL單口燒瓶中依次加入450.0mL無水四氫呋喃、5.1g化合物9,10-十八-二酮和10.0mL三乙胺,在攪拌條件下加入2.2g化合物[2,2`]-聯吡啶-6,6`-二甲酰胺腙,在氮氣保護下,69-72℃回流攪拌反應至溶液變澄清(化合物[2,2`]-聯吡啶-6,6`-二甲酰胺腙和化合物9,10-十八-二酮以摩爾比1:2.2進行反應,二酮過量)。停止反應后,過濾除去固體殘渣,濾液經蒸餾除去無水四氫呋喃,得粗產品,然后用無水乙醚研磨,抽濾除去溶劑得到固體,用石油醚/乙酸乙酯作為流動相(體積比4:1)進行柱色譜技術分離和純化,得到目標化合物,在60℃下真空干燥5h,最終得到2.5g金黃色固體,產率40.3%。C8-BTBP化合物表征a.C8-BTBP的元素分析,結果見表1。表1C,%H,%N,%理論值75.739.8614.42實驗值75.489.8214.64C8-BTBP的分子式為C48H74N8,測得C、H、N實驗值與理論值相吻合,說明合成的6,6'-雙(5,6-二–辛基-1,2,4-三嗪-3-基)-2,2'-聯吡啶(C8-BTBP)是要合成的目標化合物。b.MS-ESI分析,結果見圖1。測試了C8-BTBP的MS-ESI陽離子圖譜,分析結果表明:[M+H+]=763.6,[M-2H++Na+]=783.0,[M+Na+]=785.5,計算值m/z為762.6。C8-BTBP的理論分子量為762.6,此結果與C8-BTBP分子量的理論值相符。MS-ESI分析說明合成了目標化合物。c.1HNMR分析,結果見圖2。測試了合成的C8-BTBP化合物的1HNMR圖譜,分析結果表明:(1HNMR(CDCl3,400MHz):δ=0.8-0.9ppm,m,4×CH3,12H;δ=1.2-1.6ppm,m,20×CH2,40H;δ=1.8-1.9ppm,m,4×CH2,8H;δ=2.9-3.0ppm,t,4×CH2,8H;δ=8.1ppm,t,Ar-H,2H;δ=8.7ppm,d,Ar-H,2H;δ=9.0ppm,d,Ar-H,2H。圖2中δ=7.2ppm為氘代氯仿的峰,δ=5.3ppm處的單峰是溶劑二氯甲烷中質子形成的峰,化學位移和氫原子個數等指認結果均與C8-BTBP的結構信息相符。實施例2分別將0.2g實施例1制備的C8-BTBP(結構式Ⅰ所示的化合物)、0.2g冠醚(2-叔丁基-2-環己基-18-冠-6,即結構式Ⅱ所示的化合物)以及0.2g杯芳單冠(正丙基-杯[4]-單冠-6,即結構式Ⅲ所示的化合物)固體溶解于100.0mL二氯甲烷中,充分溶解得到淡黃色澄清溶液;向此淡黃色澄清溶液中加入1.8g離子交換樹脂XAD-7攪拌均勻,并使用旋轉蒸發儀,在減壓條件下旋轉蒸發使二氯甲烷揮發至物料到近干狀態,然后再將近干狀態的物料在55℃下真空干燥24h,將三種有機功能配體負載在離子交換樹脂XAD-7上,得到四元復合材料。實施例3分別將0.2g實施例1制備的C8-BTBP(結構式Ⅰ所示的化合物)、0.2g冠醚(2-叔丁基-2-環己基-18-冠-6,即結構式Ⅱ所示的化合物)以及0.2g杯芳單冠(正丙基-杯[4]-單冠-6,即結構式Ⅲ所示的化合物)固體溶解于90.0mL二氯甲烷中,充分溶解得到淡黃色澄清溶液;向此淡黃色澄清溶液中加入1.6g離子交換樹脂XAD-7攪拌均勻,并使用旋轉蒸發儀,在減壓條件下旋轉蒸發使二氯甲烷揮發至物料到近干狀態,然后再將近干狀態的物料在50℃下真空干燥24h,將三種有機功能配體負載在離子交換樹脂XAD-7上,得到四元復合材料。實施例4分別將0.2g實施例1制備的C8-BTBP(結構式Ⅰ所示的化合物)、0.2g冠醚(2-叔丁基-2-環己基-18-冠-6,即結構式Ⅱ所示的化合物)以及0.2g杯芳單冠(正丙基-杯[4]-單冠-6,即結構式Ⅲ所示的化合物)固體溶解于110.0mL二氯甲烷中,充分溶解得到淡黃色澄清溶液;向此淡黃色澄清溶液中加入2.0g離子交換樹脂XAD-7攪拌均勻,并使用旋轉蒸發儀,在減壓條件下旋轉蒸發使二氯甲烷揮發至物料到近干狀態,然后再將近干狀態的物料在60℃下真空干燥24h,將三種有機功能配體負載在離子交換樹脂XAD-7上,得到四元復合材料。實施例5-11(1)將堿金屬硝酸鹽LiNO3、NaNO3、KNO3、RbNO3;堿土金屬硝酸鹽Mg(NO3)2、Ca(NO3)2、Ba(NO3)2;Ru的硝酸鹽溶液;過渡金屬鹽Fe(NO3)3、ZrO(NO3)2、Co(NO3)2、Ni(NO3)2以及稀土金屬氧化物Y2O3、稀土金屬硝酸鹽La(NO3)3、Yb(NO3)3、Nd(NO3)3溶解于去離子水中配制成硝酸濃度為4.0M且同時含有16種金屬元素的硝酸水溶液,該硝酸水溶液中所含的16種金屬離子的濃度分別約為2.0×10-3-5.0×10-3M。(2)在硝酸水溶液中加入濃硝酸和去離子水進行稀釋,調節硝酸水溶液中的硝酸濃度分別為0.4、1.0、2.0、3.0、4.0、5.0、6.0M,每種金屬離子的濃度為5.0×10-4M。(3)將實施例2制備得到的四元復合材料與步驟(2)得到的不同硝酸濃度的硝酸水溶液分別進行混合,混合時的用量比為:每3.0mL硝酸水溶液對應0.15g四元復合材料。(4)將步驟(3)所得混合液在TAITECMM-10型振蕩器上進行震蕩使固液相充分接觸,振蕩器振蕩速率為120rpm,溫度為298K,為使吸附達到平衡,振蕩時間設置為120min,然后用等離子體電感耦合原子發生光譜(ICP-OES)和原子吸收光譜(AA240)對吸附前后水相中各元素的含量進行檢測。實施例5-11的吸附結果如圖3所示,當硝酸濃度為2.0mol/L時,該四元復合材料同時吸附分離元素鈷和鎳的能力最強,分配系數大于10000cm3/g,即水相中所含的鈷和鎳吸附率為100%。與此同時,該四元復合材料對其他14種共存離子的吸附分配系數均小于20cm3/g,此結果表明該四元復合材料在硝酸濃度大于2.0M條件下,能夠高效地高選擇性地將鈷和鎳與其他金屬,例如鐵、堿金屬、堿土金屬、過渡金屬以及稀土元素相分離,應用前景廣闊。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1