一種污水電化學脫氮除磷方法與流程
本發明屬于廢水處理技術領域,具體涉及一種污水電化學脫氮除磷方法。
背景技術:
氮磷是造成水體富營養化的主要原因之一。一般來說當水體含氮量大于0.2mg/l,含磷量大于0.02mg/l時,水體就會出現富營養化。水體富營養化后會引起藻類的大量繁殖,一方面消耗水中的溶解氧,造成水體中魚蝦等水生動植物的大量死亡。通常情況下,1mg氨氮在硝化細菌的催化下轉化為硝態氮需要消耗水中溶解氧4.57mg。另一方面,死亡的藻類和魚蝦等分解會產生惡臭氣體,不斷釋放氮磷,形成新的污染源,如此惡性循環,造成水水質惡化。藻類生長和分解過程中會釋放某些有毒有害物質,危害水產養殖業,對人類生產和生活造成困擾。
廢水中的氮元素主要以無機氮和有機氮的形式存在,無機氮包括氨氮和硝氮,有機氮包括尿素、蛋白質、氨基酸,有機堿等含氮有機物。目前國內外在水體氨氮處理技術上主要分為物理化學法和生物脫氮法。物理化學法有折點氯化法、化學沉淀法、吸附法、離子交換法、吹脫法和氣浮法、液膜法、電滲析法、催化濕式氧化法等。應用和研究較多的方法主要有:生物法,空氣吹脫法,離子交換法,折點氯化法,吸附法,電催化氧化法和化學沉淀法等。
生物脫氮法:生物脫氮法主要是利用微生物通過同化、氨化、硝化、反硝化等一系列反應使廢水中的氨氮還原為氮氣排放。該法中硝化菌的活性對水溫、溶解氧和有機碳源等比較敏感,且當廢水中碳氮比較低時,需要補充碳源,而當廢水的溫度較低時,微生物生長緩慢,去除效率低。此外,當廢水中氨氮的濃度大于300mg/l時,會對硝化細菌產生抑制作用,不利于氨氮的去除。
空氣吹脫法:氨氮在液體中溶解時,利用吹脫法將其去除的原理是基于氨氮的在水體中的實際濃度高于其平衡時氨氮的濃度,利用空氣在堿性條件下將水體中多余的氨氮從液相中吹脫出去,逸散到空氣中從而達到將污水中污染物去除的目的。但吹脫出的氨氮可能對空氣產生污染,此方法較適用于高濃度氨氮廢水的處理。
吸附法:吸附技術以其高效快速、操作簡單、無二次污染、吸附劑可再生利用等優點,被廣泛應用于中低濃度氨氮廢水的處理。吸附法處理氨氮是較有發展前景的方法之一,近年來在這方面的研究較多,尤其是以沸石為吸附劑對氨氮的吸附去除效果研究為主。此外,以生物炭(如木材、竹子、稻草、秸稈、核桃殼、蔗渣等為原料制成的生物炭)、活性炭、粉煤灰、鋼渣、蛭石等材料為吸附劑,探討其各自對氨氮的吸附性能研究也比較多。同樣,常規的吸附劑去除氨氮也面臨著吸附容量低,吸附劑再生費用高,難以實現氨氮的回收利用,吸附后殘渣處置困難等問題。
電催化氧化法:電催化氧化與生化法相比,電化學方法一般不受反應物生物毒性的影響,可以作為高毒性有機物的有效處理方法,也可以作為生化方法的預處理,使有毒的大分子有機物轉化為小分子有機物,有利于進一步的生化處理。電化學方法以電子作為反應劑,電壓梯度為反應動力,一般不需要外加化學試劑,可以避免過多的二次污染。電化學反應器的結構及外圍設備都相對簡單,合理的設計及安裝有利于實現高效率、低成本要求,另外電化學過程易于實現自動控制。電催化氧化的基本原理是污染物被電極表面或是電場產生的自由基氧化而達到降解去除。一般將能引起電化學反應速率或選擇性發生變化的電極都叫做電催化電極,這樣的反應叫做電催化反應。陽極氧化、陰極間接氧化、陰陽兩極協同作用都能發生電催化反應,其中陽極氧化研究較多。
同時,磷是組成生命物質不可缺少的元素之一,也是地球上農作物重要的營養元素。磷在自然界的循環途徑基本循環途徑是從陸地轉移到海洋的,所以磷在陸地上基本屬于不可再生資源。以目前消耗速度計算,全球磷礦將會在100~250年內消耗殆盡。另一方面,磷礦產資源開采后約80%被用于磷肥生產。攝入人體的磷,除少量被吸收外,絕大部分隨尿液和糞便排泄到污水中。工農業和人類生活中排放的磷進入水體中,造成了嚴重了環境問題。因此,在陸地磷資源日益匱乏的今天,從污水中回收磷具有一舉兩得的功效,具有重要意義。
目前,傳統的污水生物處理工藝無法達到磷回收的效果。利用絮凝沉淀等方法得到的磷回收主要產品形式為磷酸鐵(fepo4)、磷酸鋁(alpo4)、磷酸氨鎂(mgnh4po4·6h2o,又稱鳥糞石,簡寫為map)和羥磷灰石(ca10(po4)6(oh)2,簡寫為hap)等磷酸鹽沉淀物。在各種磷酸鹽回收產物中鳥糞石倍受青睞,原因在于鳥糞石中p含量折算成p2o5標準量后可達51.8%,是品質優異的磷礦。同時,鳥糞石可以直接或間接被用作農業、林業優質肥料。
磷酸銨鎂沉淀法(簡稱map法),就是向廢水中投加mg2+和po43-后,nh4+與其反應生成復鹽mgnh4po4·6h2o(map)結晶沉淀,從而實現將氨氮和磷酸鹽從廢水中分離回用的目的。化學沉淀法去除氨氮的效果受溶液氨氮濃度、反應ph值和沉淀劑投加量等條件的影響。反應產物mgnh4po4·6h2o也稱為鳥糞石,含有氮、磷成分,是一種良好的緩釋肥,可作為土壤改良劑。化學沉淀法可以實現氨氮的回收利用,沉淀反應工藝設計、操作簡單,目前在處理高濃度的氨氮廢水中應用的較多。
化學沉淀法去除效率較高,且不受溫度限制,無需預處理,操作簡單,投資費用低。化學沉淀法的缺點是污水中一般存在氮磷比失調的問題,造成反應過程中磷酸根離子不足;同時由于受到磷酸銨鎂溶度積常數的限制,依靠加大投入藥劑量,氮磷去除效果不明顯,特別是氨氮,在n:p=1:1時,氨氮的去除率不足70%。
技術實現要素:
針對現有技術存在的上述不足,本發明提供一種污水電化學脫氮除磷方法,旨在解決map法處理污水時,因污水中的氮磷比失調(磷的量偏低)導致氨氮的去除率較低的技術問題;以及現有電化學磷酸銨鎂法易使電極表面發生結垢鈍化的問題。
為了實現上述目的,本發明采用的技術方案,可以通過以下步驟實現:
1)將含有銨根離子和磷酸根離子的污水注入反應器,并調節污水的ph值至7;所述的反應器中至少設置有一組電極,每組電極均包括第一電極和第二電極,其中第一電極的材料是鎂或鎂合金,第二電極的材料是石墨、鉑或鈦基金屬氧化物,且鈦基金屬氧化物為鈦/二氧化釕、鈦/二氧化鉛、鈦/二氧化錫或鈦/二氧化銥等。。
2)調節電壓,通過雙向脈沖電源使第一電極和第二電極交替處于高電位和低電位,通電處理污水反應時間為30~180min。
當第一電極處于高電位時,第二電極處于低電位;第一電極電解并釋放出溶解性鎂離子,第二電極產生氫氧根離子,使污水的ph值升高,溶解性鎂離子與水中銨根離子和磷酸根離子反應生成磷酸銨鎂沉淀;當第二電極處于高電位時,銨根離子被氧化,此時第一電極處于低電位,其表面產生氫氣,以緩解鈍化作用。
所述污水含有的銨根離子和磷酸根離子的摩爾濃度之比為1:0.2~1。在此范圍內對可取的較好的污染物去除效果,同時本方法對各類氮磷比污水具有廣泛的適應性。
所述的反應器中還設置有攪拌裝置,用以在步驟2)的反應過程中對污水進行攪拌,攪拌速率為200rpm。在反應過程用攪拌,可以使污水中各部分反應物的傳質過程,有利于反應的進行。
所述反應器采用的電源為:雙向脈沖電源電壓為±10v,偏置為0.0%,占空比為45%,頻率為0.04hz。在上述條件下,本方法對污染物的去除效果明顯優于傳統方法。同時增大電壓可以提高污染物的去除效率。
本方法還包括步驟3):對步驟2)處理后的污水進行沉淀或過濾,得到的固相物質用純水清洗若干次后烘干,即得純度較高的磷酸銨鎂晶體(鳥糞石),可以作為肥料利用。
在步驟1)中,調節污水ph值之前,還宜加入支持電解質如nacl,其在污水中的濃度為0.020moll-1。
當鎂或鎂合金處于高電位,石墨、鉑、或鈦/二氧化釕、鈦/二氧化鉛、鈦/二氧化錫、鈦/二氧化銥等鈦基金屬氧化物電極處于低電位時,此時鎂或鎂合金相當于陽極,石墨、鉑、或鈦/二氧化釕、鈦/二氧化鉛、鈦/二氧化錫、鈦/二氧化銥等鈦基金屬氧化物電極相當于陰極,則反應器中主要發生以下反應來實現磷酸按鎂的生成,從而回收污水中氮磷的目的。
陽極:mg→mg2++2e-(1)
陰極:2h2o+2e-→h2+2oh-(2)
污水中發生的反應:
mg2++nh4++po43-+6h2o→mgnh4po4·6h2o↓(3)
當鎂或鎂合金處于低電位時,石墨、鉑、或鈦/二氧化釕、鈦/二氧化鉛、鈦/二氧化錫、鈦/二氧化銥等鈦基金屬氧化物電極處于高電位時,此時鎂或鎂合金相當于陰極,石墨、鉑、或鈦/二氧化釕、鈦/二氧化鉛、鈦/二氧化錫、鈦/二氧化銥等鈦基金屬氧化物電極相當于陽極。加入氯鹽作為支持電解質,其作用有兩點:(1)增加溶液的電導率,提高電流效率,降低能耗;(2)在電化學氧化過程中cl-的存在會生成hocl和hclo3,從而促進氨氮氧化。反應器中氨氮的氧化過程如式(4)-(11):
鉑電極:2cl-→cl2+2e-(4)
鉑電極:oh-→oh·+e-(5)
污水:oh·+(1/3)nh4+→(1/6)n2+h2o+(1/3)h+(6)
oh·+(1/7)nh4+→(1/7)no3-+(4/7)h2o+(3/7)h+(7)
cl2+h2o→hocl+h++cl-(8)
hocl+(2/3)nh4+→(1/3)n2+h2o+(5/3)h++cl-(9)
hocl+(1/4)nh4+→(1/4)no3-+(1/4)h2o+(3/2)h++cl-(10)
hocl+(1/2)ocl-→(1/2)clo3-+h++cl-(11)
當溶液中不含cl-時,反應器中氨氮的氧化以羥基間接氧化為主,反應過程如(5)-(7)與現有的技術相比,本發明具有如下有益效果:
1、本工藝使用脈沖電源將鳥糞石沉淀法和電化學氧化法結合起來去除氨氮廢水,方法操作簡單,工程投資費用低,氮磷的去除率較高。
2、對廢水中的適應性強,本方法對不同ph和n:p比的廢水有較好的適應性,通過調節運行參數,可同時獲得較高的氮磷去除率。
3、本工藝生成的磷酸銨鎂沉淀純度較高,可以回收用于做農業緩釋肥,不僅解決了廢水中氨氮和磷的污染問題,同時有利于廢物資源化利用,取得了較高的經濟效益和環境效益。
4、電極效率提高。使用雙向脈沖電源,可以減緩極板鈍化,減輕反應器內濃差極化,無論對于電化學沉淀還是電化學氧化,都有利于提高電流效率。
附圖說明
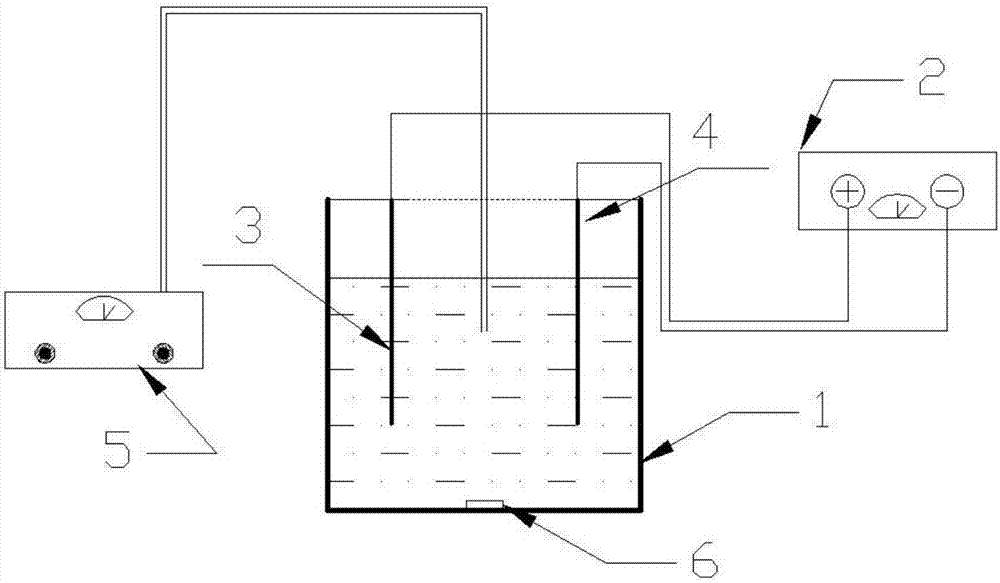
圖1為本發明的反應器的結構示意圖;
圖2a為占空比45%、頻率0.04hz的+10v脈沖波形圖;
圖2b為占空比45%、頻率0.04hz的-10v脈沖波形圖;
圖2c為占空比45%、頻率0.04hz的±10v脈沖波形圖;
圖3a為實施例一的不同波形下氨氮去除率變化趨勢;
圖3b為實施例一的不同波形下磷酸根鹽去除率變化趨勢;
圖4為實施例一的脈沖波形c下生成沉淀的xrd圖譜;
圖5a為實施例二的占空比45%、電壓±10v、頻率0.04hz時不同n:p下銨根離子去除率變化趨勢;
圖5b為實施例二的占空比45%、電壓±10v、頻率0.04hz時不同n:p下磷酸根離子的去除率變化趨勢;
附圖中:1—反應槽;2—雙向脈沖電源;3—第一電極;4—第二電極;5—溫度計及ph計;6—攪拌裝置。
具體實施方式
下面結合具體實施例對本發明作進一步詳細說明。
以下實施例采用圖1中的反應器進行測試,反應槽1為上端敞口的容器,用于盛裝模擬污水。雙向脈沖電源2通過導線分別與第一電極3和第二電極4連接,與污水一起構成成反應裝置。反應槽1中還設置有攪拌裝置6,以及用于實時監控反應狀態的溫度計及ph計5。
實施例一
在濃度為0.010moll-1的磷酸二氫氨模擬廢水中,加入nacl作為支持電解質,使濃度達到0.020moll-1,調節溶液ph=7.0,攪拌速率為200rpm,脈沖電源電壓分別為+10v、-10v、±10v,頻率為0.04hz,偏置為0.0%下,分別電解時間180min。采用mg/pt電極反應器。實驗選用a(﹢10v),b(﹣10v),c(±10v)三種波形(如圖2a—c所示)。
當電壓為正時,材料為鎂的第一電極處于高電位,溶液中發生沉淀反應。當電壓為負時,材料為鉑的第二電極處于低電位時,溶液中發生氧化反應。實驗過程中每30min取樣檢測氨氮和磷酸鹽濃度以計算其去除率。反應結束后,使用0.45μm濾膜過濾溶液,得到沉淀物。
如圖3a所示,在同一波形下,當脈沖電源輸出波形a時,反應60min時達到氨氮最高去除率62.6%;當脈沖電源輸出波形b時,至180min反應結束時氨氮最高去除率僅為12.5%;在波形c下,反應120min時達到氨氮最高去除率為75%。
以上實驗結果表明,波形c下溶液中可能發生了氨氮的電化學氧化和電化學沉淀。在前120min中,隨著溶液中的mg2+和ph不斷增加,生成了磷酸銨鎂沉淀,同時部分氨氮被電化學氧化去除。120min之后,溶液ph過高,磷酸銨鎂的溶解度增加,此時溶液中氨氮的去除以電化學氧化為主,通過二者的聯合作用,氨氮去除率得到提高。
如圖3b所示,波形a條件下磷去除率在120min時基本穩定達到91.7%;波形b下對磷幾乎沒有去除作用;波形c條件下,在反應時間內磷最終去除率為88.4%。
如圖4所示,將波形c(脈沖電解)條件下生成沉淀與xrd標準卡片對比。根據標準圖譜可以看出,波形c(脈沖電解)下生成沉淀的主要成分為mgnh4po4·6h2o和mg3(po4)2·22h2o。
實施例二
設置銨根離子與磷酸根離子摩爾比1:0.2,1:0.5和1:1三個梯度,其中氨氮的濃度為0.010moll-1,磷酸根離子的濃度分別為0.002moll-1,0.005moll-1,0.010moll-1。nacl作為支持電解質,使濃度為0.020moll-1,調節溶液ph=7.0,攪拌速率為200rpm,脈沖電源電壓為±10v,頻率為0.02hz,偏置為0.0%,電解時間180min。如圖5a所示,在n:p為1:0.2,1:0.5和1:1條件下,反應180min后,氨氮的最終去除率分別為32.2%,49.5%和70.8%。如圖5b所示,在n:p分別為為1:0.2和1:0.5條件下,反應60min時磷酸鹽最終去除率分別為96.8%和98.2%,當n:p為1:1時,反應60min時磷酸根去除率為38%,反應180min時最終去除率為88.4%。增大進水氮磷比可以增加溶液中電化學沉淀反應的速度和強度,提高氨氮的去除率,而對磷酸根離子的去除效果則影響不大。
本發明的上述實施例僅僅是為說明本發明所作的舉例,而并非是對本發明的實施方式的限定。對于所屬領域的普通技術人員來說,在上述說明的基礎上還可以做出其它不同形式的變化和變動。這里無法對所有的實施方式予以窮舉。凡是屬于本發明的技術方案所引申出的顯而易見的變化或變動仍處于本發明的保護范圍之列。
- 還沒有人留言評論。精彩留言會獲得點贊!