一種可控發光碳納米粒子及制備方法和應用與流程
本發明屬于發光碳納米粒子技術領域,具體涉及一種可控發光碳納米粒子及制備方法和應用。
技術背景
隨著納米技術的產生與發展,碳材料大家庭不斷壯大。碳納米粒子作為碳材料大家庭中的新成員,是一種性質獨特的發光納米材料,因其具有粒徑小(尺寸小于10nm),毒性低,水溶性好,熒光性能優異和光穩定性強等優點而備受研究者的關注。碳納米粒子(carbonnanoparticles,cnps)自2004年首次發現以來,一直受到科研工作者的青睞,相對于傳統的量子點(qds)及熒光小分子體現出了一些特有的優勢,包括:與qds相比,cds具有較好的生物相容性和環境友好性;相比于有機熒光染料,cds具有熒光穩定、激發波譜寬和成本低等優點。
目前,很多合成方法和材料可以用于碳納米粒子的制備,但仍有一些問題存在,如有些方法步驟過于繁瑣,有的碳納米粒子的量子產率不高,有的制備方法需要添加有毒化學試劑,發光集中在短波長,可控合成的局限性,這限制了碳納米粒子在實際檢測中的應用。因此,發展簡單、快速、綠色和低損耗以及可控其性質的碳納米粒子合成方法是十分必要的。
目前碳納米粒子的研究尚處于起步階段,還有許多實驗和理論方面的問題值得探索和解決。例如尋找更綠色環保的碳源,通過更簡單安全、易操作的方法來合成性能更好,可控制備不同發光的熒光碳納米粒子,碳納米粒子作為新型熒光探針在生物標記以及離子、ph檢測上有更深入的應用。
技術實現要素:
為了克服現有技術存在的缺陷,本發明的目的在于提供一種簡單、快速的方法用于可控熒光碳納米粒子發光的制備,碳納米粒子制備方法簡便、設備簡單、碳源低廉且綠色環保、反應時間短,可控合成不同發光碳納米粒子;所制備的碳納米粒子可應用于金屬離子檢測、ph的檢測以及細胞成像等方面,檢測靈敏度、檢出限以及細胞成像效果均優于當前文獻報道,對碳納米粒子在實際樣品、生物學以及醫學應用有重要的指導意義。
本發明為實現上述目的而采取的技術方案為:
一種可控發光碳納米粒子,通過以下步驟制成:
(1)將鮮丁香花瓣烘干,粉碎成粉末,稱取1-2g于小燒杯中并加入去離子水10ml然后通過加入0-3gnaoh固體攪拌使其充分溶解,加入到高壓反應釜中,放入烘箱150-250℃高溫反應3-5小時;
(2)反應結束后冷卻得到棕色或深棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色或棕色液體即為純凈碳納米粒子溶液;
(3)將步驟(2)中的碳納米粒子溶液冷凍真空干燥得到棕黃色或棕色粉末,即為目的碳納米粒子,溶于水中發出強藍色或者綠色熒光。
本發明可控發光碳納米粒子的制備方法,包括以下步驟:
(1)將鮮丁香花瓣烘干,粉碎成粉末,稱取1-2g于小燒杯中并加入去離子水10ml然后通過加入0-3gnaoh固體攪拌使其充分溶解,加入到高壓反應釜中,放入烘箱150-250℃高溫反應3-5小時;
(2)反應結束后冷卻得到棕色或深棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色或棕色液體即為純凈碳納米粒子溶液;
(3)將步驟(2)中的碳納米粒子溶液冷凍真空干燥得到棕黃色或棕色粉末,即為目的碳納米粒子,溶于水中發出強藍色或者綠色熒光。
本發明可控發光碳納米粒子的應用,作為熒光探針用于檢測水溶液中的fe3+濃度和水溶液的ph值或者通過活細胞熒光成像檢測活細胞中的fe3+濃度和活細胞的ph值。
進一步地,本發明用于檢測水溶液中的fe3+濃度和活細胞中的fe3+濃度時,在制備發光碳納米粒子的步驟(1)中naoh固體的加入量為0g;用于檢測水溶液的ph值和活細胞的ph值時,在制備發光碳納米粒子的步驟(1)中naoh固體的加入量為1-3g。
本發明采用上述技術方案,具有以下有益效果:
(1)本發明操作步驟簡單,只需加入常規普通藥品就可調節碳納米粒子的發光,即發光可以向長波長移動,對于在生物傳感應用有很重要的價值,反應物在同一體系中進行,即可得到目標碳納米粒子。
(2)原材料為丁香花,是很低廉的綠色原料,來源廣泛,經濟環保。
(3)生產設備簡單,成本低,反應周期短,產量高。
(4)合成的碳納米粒子均有良好的水溶性,熒光產率高,生物相容性,良好的光穩定性,適合量產。
(5)應用價值高,制備碳納米粒子可應用于金屬fe3+離子檢測,其檢測靈敏度高,檢出限在相關文獻報道中是最小的;通過簡單調控制備的碳納米粒子還可應用于溶液ph的檢測;所有制備的碳納米粒子都可成功應用于生物標記、活細胞中fe3+離子以及ph檢測,效果明顯,
總之,本發明合成工藝操作簡單,原料來源廣泛且低廉環保,制備條件要求低且溫和,所得碳納米粒子產量高,解決了現有碳納米粒子制備方法因工藝和原料限制而無法規模化生產問題,該碳納米粒子可應用于金屬離子檢測、生物標記、生物影像、光電裝置以及防偽標記等領域。
附圖說明
圖1是本發明將實施例1-8所得到的純凈碳納米粒子進行熒光光譜測試,圖1a、b為實施例1-5的熒光譜圖,圖1c為實施例6-8的熒光光譜圖。
圖2是實施例2中制備的純凈碳納米粒子的紫外吸收光譜、最佳熒光激發和發射光譜。
圖3是實施例7中制備的純凈碳納米粒子的紫外吸收光譜、最佳熒光激發和發射光譜。
圖4是實施例2、實施例7制備的純凈碳納米粒子熒光發射光譜隨激發波長變化的譜圖。
圖5是實施例2、實施例7制備的純凈碳納米粒子的紅外光譜圖。
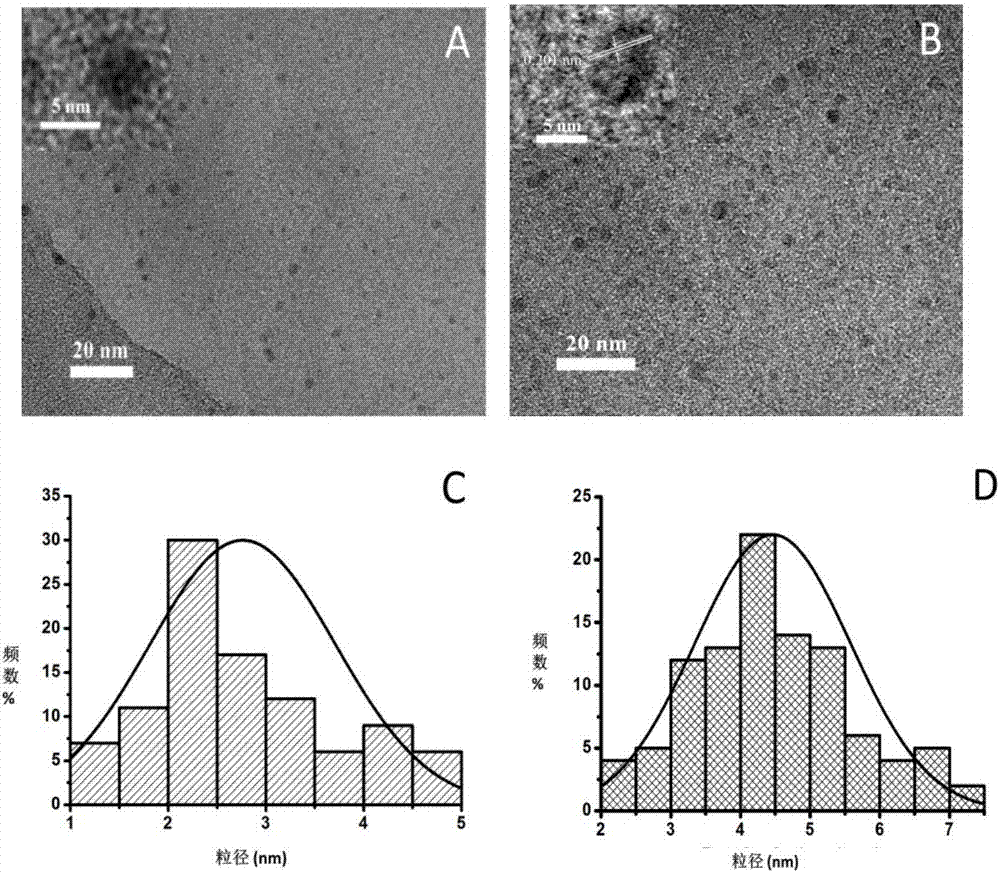
圖6是實施例2、實施例7制備的純凈碳納米粒子的tem、hrtem以及粒徑分布圖。
圖7是實施例2、實施例7制備的純凈碳納米粒子的xps譜圖。
圖8是實施例2、實施例7制備的純凈碳納米粒子的xrd譜圖。
圖9是實施例2、實施例7制備的純凈碳納米粒子對金屬離子選擇以及實施例2制備的純凈碳納米粒子對鐵離子猝滅圖。
圖10是實施例7制備的純凈碳納米粒子在不同ph環境下的熒光圖以及不同循環次數下熒光變化圖。
圖11是實施例2、實施例7制備的純凈碳納米粒子對乳腺癌細胞mcf-7的細胞毒性mtt實驗圖。
圖12是實施例2中制備的純凈碳納米粒子標記乳腺癌細胞mcf-7以及檢測鐵離子的激光共聚焦圖。
圖13是實施例7中制備的純凈碳納米粒子標記不同ph環境下乳腺癌細胞mcf-7激光共聚焦圖。
具體實施方式
以下結合實施例對本發明做詳細的說明,具體的操作過程以及詳細的實施方式通過實施例給出,單本發明的保護范圍不限于以下實施例。
實施例1
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml,加入到高壓反應釜中,放入烘箱150℃高溫反應4小時;
步驟2、反應結束后冷卻得到棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕黃色粉末,即為目的碳納米粒子,溶于水中發出藍色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以硫酸奎寧為標準)為5.8%。
實施例2
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml,加入到高壓反應釜中,放入烘箱200℃高溫反應4小時;
步驟2、反應結束后冷卻得到棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕黃色粉末,即為目的碳納米粒子,溶于水中發出藍色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以硫酸奎寧為標準)為12.9%。
實施例3
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml,加入到高壓反應釜中,放入烘箱250℃高溫反應4小時;
步驟2、反應結束后冷卻得到棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色液體即為純凈碳納米粒子溶液;
步驟3將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕黃色粉末,即為目的碳納米粒子,溶于水中發出藍色熒光;
步驟4將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以硫酸奎寧為標準)為6.8%。
實施例4
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml,加入到高壓反應釜中,放入烘箱200℃高溫反應3小時;
步驟2、反應結束后冷卻得到棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕黃色粉末,即為目的碳納米粒子,溶于水中發出藍色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以硫酸奎寧為標準)為10.9%。
實施例5
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml,加入到高壓反應釜中,放入烘箱200℃高溫反應5小時;
步驟2、反應結束后冷卻得到棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕黃色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕黃色粉末,即為目的碳納米粒子,溶于水中發出藍色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以硫酸奎寧為標準)為7.2%。
實施例6
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml然后加入1gnaoh固體攪拌使其充分溶解,加入到高壓反應釜中,放入烘箱200℃高溫反應4小時;
步驟2、反應結束后冷卻得到深棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕色粉末,即為目的碳納米粒子,溶于水中發出綠色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以羅丹明6g為標準)為4.8%。
實施例7
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml然后加入2gnaoh固體攪拌使其充分溶解,加入到高壓反應釜中,放入烘箱200℃高溫反應4小時;
步驟2、反應結束后冷卻得到深棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕色粉末,即為目的碳納米粒子,溶于水中發出綠色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以羅丹明6g為標準)為8.9%。
實施例8
步驟1、將鮮丁香花瓣烘干,粉碎成粉末,稱取1g于小燒杯中并加入去離子水10ml然后加入3gnaoh固體攪拌使其充分溶解,加入到高壓反應釜中,放入烘箱200℃高溫反應4小時;
步驟2、反應結束后冷卻得到深棕色溶液,通過離心,0.22μm過濾器過濾,然后在500-1000d透析袋中透析3天,得到棕色液體即為純凈碳納米粒子溶液;
步驟3、將步驟2中的碳納米粒子溶液冷凍真空干燥得到棕色粉末,即為目的碳納米粒子,溶于水中發出綠色熒光;
步驟4、將上述熒光碳納米粒子水溶液冷凍干燥后得到熒光碳納米粒子,其相對量子產率(以羅丹明6g為標準)為6.5%。
實施例9
將實施例1-5所得到的純凈碳納米粒子進行熒光光譜測試,如圖1a、b為實施例1-5的熒光譜圖。將實施例6-8所得到的純凈碳納米粒子進行熒光光譜測試,如圖1c為實施例6-8的熒光光譜圖。
實施例10
將藍色熒光量子產率最高的碳納米粒子,即實施例2中得到的碳納米粒子進行紫外光譜測定,熒光激發譜、發射譜測定,如圖2;將綠色熒光量子產率最高的碳納米粒子,即實施例7中得到的碳納米粒子進行紫外光譜測定,熒光激發譜、發射譜測定,如圖3。將實施例2中的碳納米粒子溶液在不同激發波長下的熒光發射譜圖進行測定,如圖4a,在佳發射波長在450nm左右,屬于藍光范疇;將實施例2中的碳納米粒子溶液在不同激發波長下的熒光發射譜圖進行測定,如圖4b,在佳發射波長在520nm左右,屬于綠光范疇。
將實施例2和實施例7中得到高純碳納米粒子進行紅外,tem/hrtem,xps,xrd表征,如圖5-8得到本發明得到的高純碳納米粒子粒徑均小于10nm,發藍光的碳納米粒子含有羧基、羥基以及氨基等基團,發綠光的碳納米粒子含有羧基、羥基等基團,兩種碳納米粒子含有基團略有區別。
實施例11
取實施例2制備的熒光碳納米粒子水溶液(2.8mg/ml)置于熒光比色皿中,分別加17種常見的金屬離子溶液(300mm),充分混合均勻,在熒光光譜儀中掃描發射光譜(λex=340nm,λem=445nm),并記錄加入每一種離子后的熒光強度,如圖9b所示,實施例2的碳納米粒子對fe3+有很好的選擇性,即fe3+可以使實施例2中的碳納米粒子的藍色熒光淬滅。為了計算碳納米粒子對fe3+的檢測范圍,取實施例2制備的熒光碳納米粒子水溶液(2.8mg/ml)置于熒光比色皿中,從低到高分別加入不同濃度的fe3+溶液,充分混合均勻,測定在不同濃度fe3+下實施例2中熒光碳納米粒子的熒光,如圖9a,從圖中繼而得出對fe3+的檢出限為可達3.69×10-7mol/l,檢出線性范圍0-150mol/l。而實施例7中的發綠光的熒光碳納米粒子沒有對某種金屬離子有很好的選擇,如圖9c。
實施例12
取實施例2制備的熒光碳納米粒子水溶液(2.8mg/ml)置于熒光比色皿中,通過利用不同濃度fe3+滴定可以制得c(fe3+)與熒光強度的線性關系,從而可以測定實際水樣中(自來水中)fe3+的含量,所測定值與電感耦合等離子光譜發生儀(icp)測定的結果基本一致,見表1,確定我們的方法具有可靠性。
實施例13
將實施例7中制備的發綠光的碳納米粒子(1.6mg/ml)置于熒光比色皿中,加入不同ph的溶液(1.89-11.92)中測定其熒光,充分混合均勻,在熒光光譜儀中掃描發射光譜(λex=450nm,λem=520nm),并記錄加入到每一種ph后的熒光強度,如圖10a所示,在1.89-8.95范圍內呈線性,即ph越大熒光越強,在1.89和8.95不同重復變換后熒光不受影響,如圖10b,說明實施例7制備的發綠光的熒光碳納米粒子對ph有很好的靈敏度。
實施例14
將實施例7中制備的發綠光的碳納米粒子(1.6mg/ml)置于熒光比色皿中,加入不同ph的溶液(1.89-8.95)中測定其熒光,得出溶液ph與熒光強度的線性關系,從而可以測定未知實際溶液中的ph,所測定值與商業ph測定儀測定值很接近,見表2。
實施例15
將實施例2、7中不同發光的碳納米粒子進行細胞毒性測試,分別配制不同濃度的碳納米粒子溶液(0-50mg/ml)作用于人乳腺癌細胞mcf-7,即通過常規mtt實驗進行分析得出實施例2、7中制備的不同發光的碳納米粒子對細胞毒性很小,如圖11。
實施例16
將實施例2中制備的發射藍色熒光的碳納米粒子水溶液(6mg/ml)用于標記人乳腺癌mcf-7細胞,如圖12,圖12a是只有實施例2中制備的碳納米粒子水溶液(6mg/ml)加入到培養mcf-7細胞中的dmem培養液中,共孵育10分鐘后的激光共聚焦成像(激發波長是405nm,接收的發射波長范圍是425-480nm),顯示藍色熒光很強;圖12b-e是加入實施例2中制備的碳納米粒子水溶液(6mg/ml)加入到培養mcf-7細胞中的dmem培養液中,共孵育10分鐘后,立即加入fe3+(300mm)在不同時間的激光共聚焦成像,顯示隨著時間推移,熒光逐漸減弱;圖12f是加入fe3+在不同時間段的細胞內熒光強度圖,表明實施例2中制備的碳納米粒子可以在活細胞中檢測fe3+。
實施例17
將實施例7中制備的發射綠色熒光的碳納米粒子水溶液(5mg/ml)用于標記人乳腺癌mcf-7細胞,如圖13,表示實施例7中制備的碳納米粒子水溶液(5mg/ml)加入到培養mcf-7細胞中的dmem培養液中,在不同ph環境中共孵育10分鐘后(激發波長是405nm,接收的發射波長范圍是480-545nm)的激光共聚焦成像,顯示在ph較小的酸性環境綠色熒光很弱,而在ph較大的中性和弱堿環境綠色熒光很強,表明實施例7制備的發射綠色熒光的碳納米粒子可以在活細胞中檢測酸堿性。
表1測定自來水中fe3+的含量(n=3).
表2測定未知溶液ph值.
以上實施例描述了本發明的制備方法及應用。本行業的技術人員應該知曉本發明不受上述實施例的限制,在不脫離本發明實質的范圍下,本發明還會有各種變化和改進,這些變化和改進均落入本發明保護的范圍內。
- 還沒有人留言評論。精彩留言會獲得點贊!