一種綠色熒光氮化碳粉末的制備方法與流程
本發明屬于材料技術領域,具體涉及一種綠色熒光氮化碳粉末的制備方法。
背景技術:
近年來,類石墨烯氮化碳納米材料作為新型的材料被廣泛應用于光催、生物成像、載藥以及生物傳感等領域。石墨相氮化碳是一種不需要經過像石墨烯一樣極端處理就具有高熒光產率和良好生物相容性的半導體納米材料,且其可以通過低成本的氰氨、雙氰氨、三聚氰氨和尿素直接聚合而成。由于這種熱解有機物的方法操作相對簡易,反應條件溫和,所以相比石墨烯而言,其具有大規模生產的潛力。
自從報道公開通過在水溶液中剝離氮化碳,得到了超薄氮化碳納米片并發現其具有較強熒光性能以來。熒光氮化碳納米材料的可控制備引起了人們的廣泛興趣。盡管,對氮化碳熒光性能的調控已有不少報道,其通過元素摻雜或者將氮化碳制備成量子點的方法使氮化碳熒光產率得到很大提高,如CN 106006581A、CN 104140084A、CN 105670620A以及CN 105152147A等等。然而,它們所得到的氮化碳的熒光發射基本都在藍色熒光區域,這與氮化碳本體的熒光顏色一致,且人對藍光的視覺敏感度不如綠光、紅光等顏色,這使得氮化碳在一些領域上的應用受到一定的限制,如生物成像、可視化的熒光傳感器的構建、防偽墨水和指紋成像等應用。此外,已有研究(如Applied Catalysis B: Environmental, 2016, 182, 68-73;Energy and Environmental Science, 2014, 7, 1902-1906;ACS Catalysis, 2015, 5 , 5008-5015)報道將芳環引入到氮化碳的結構單元里會引起氮化碳的能帶以及π離域共軛體系發生變化,從而導致氮化碳的吸收光譜和熒光光譜發生紅移,抑制光載流子的復合,提高光催化效率。然而,其所得到的氮化碳的熒光均比未引入芳環的氮化碳來得低,限制了其在光學傳感器等領域的應用。因此,開發一種成本廉價、制備簡便、可發射綠色熒光且熒光產率高的氮化碳就顯得十分必要。
技術實現要素:
本發明的目的在于提供一種高量子產率、高光學穩定的綠色熒光氮化碳粉末的制備方法。
為實現上述目的,本發明采用如下技術方案:
一種綠色熒光氮化碳粉末的制備方法,其包括以下步驟:
1)按質量比10000:1~2稱取尿素與均苯三甲酸,然后將兩者倒入燒杯中,并加入蒸餾水,超聲分散1-5min;
2)將得到的混合液置于100℃油浴中攪拌12h,然后蒸干,得到固體前驅體;
3)將所得前驅體研磨均勻;
4)將研磨后的前驅體于惰性氣體保護下進行高溫聚合反應,其反應初始溫度為30℃,升溫速度為3~10℃/min,500℃~600℃下反應2-4h,反應所得黃色固體經研磨均勻,即為所述綠色熒光氮化碳粉末。
本發明先利用均苯三甲酸與尿素混合制備前驅體,再將該前驅體在惰性氣體保護下經高溫聚合反應制備具有強熒光特性的碳化氮粉末,該碳化氮粉末在320 nm紫外光激發下的熒光發射中心在522 nm左右,為綠色熒光。經對比試驗證實,本發明摻雜均苯三甲酸的氮化碳的熒光強度可較未摻雜的氮化碳粉末提高3倍以上,且其熒光量子產率可由3.8%提高到14%,這說明將均苯三甲酸摻雜到氮化碳的納米結構中,不僅可以提高氮化碳的熒光量子產率,而且可以使氮化碳的熒光發生紅移。
盡管專利CN 106238086A中公開了類似利用均苯三甲酸摻雜氮化碳的技術內容,但由于其中均苯三甲酸摻雜的比例較大,且在空氣氛圍中聚合,會使氮化碳的表面缺陷增多,結構扭曲,這雖然可使光載流子的復合受到抑制,光催化性能增加,但會使其熒光強度大幅度下降,不利于熒光性能的應用。而本發明在惰性氣氛保護下熱縮聚尿素與均苯三甲酸的混合前驅體,由于所摻雜的均苯三甲酸的量極少,可減少氮化碳的結構扭曲,提高氮化碳環內電子離域程度,使得碳化氮的熒光從藍色移到綠色,并且量子產率提高3倍多。
本發明綠色熒光氮化碳粉末的制備方法操作簡單,容易獲得,得到的氮化碳粉末熒光量子產率高,且無毒、環保、生物相容性好,制備成水溶液分散性好,有望應用于光催、生物成像、載藥以及生物傳感等領域。
附圖說明
圖1為均苯三甲酸不同量摻雜的氮化碳粉末與未摻雜的氮化碳粉末的熒光發射光譜對比圖。
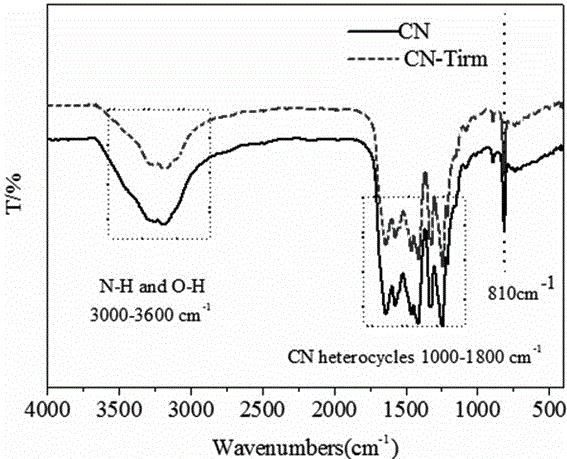
圖2為均苯三甲酸摻雜的氮化碳粉末與未摻雜的氮化碳粉末的紅外吸收光譜圖對比圖。
圖3為均苯三甲酸摻雜的氮化碳粉末與未摻雜的氮化碳粉末的固體核磁碳譜。
具體實施方式
為了使本發明所述的內容更加便于理解,下面結合具體實施方式對本發明所述的技術方案做進一步的說明,但是本發明不僅限于此。
實施例1
1)稱取10g尿素,將其倒入40mL燒杯中,并往燒杯中加入15mL蒸餾水,超聲分散;
2)稱取0.0020g均苯三甲酸,將其加入步驟1)的分散液中,超聲分散3min;
3)將得到的混合液置于100℃油浴中攪拌12h,然后蒸干蒸餾水,得到固體前驅體;
4)將所得前驅體在研缽中研磨均勻,然后倒入25mL坩堝中;
5)將研磨后的前驅體于氮氣保護下進行高溫聚合反應,反應初始溫度30℃,升溫速度為3.0℃/min,500℃下反應2h,反應所得黃色固體經研磨均勻,得到綠色熒光氮化碳粉末。
實施例2
1)稱取10g尿素,將其倒入40mL燒杯中,并往燒杯中加入15mL蒸餾水,超聲分散;
2)稱取0.0015g均苯三甲酸,將其加入步驟1)的分散液中,超聲分散1min;
3)將得到的混合液置于100℃油浴中攪拌12h,然后蒸干蒸餾水,得到固體前驅體;
4)將所得前驅體在研缽中研磨均勻,然后倒入25mL坩堝中;
5)將研磨后的前驅體于氮氣保護下進行高溫聚合反應,反應初始溫度30℃,升溫速度為4.8℃/min,550℃下反應3h,反應所得黃色固體經研磨均勻,得到綠色熒光氮化碳粉末。
實施例3
1)稱取10g尿素,將其倒入40mL燒杯中,并往燒杯中加入15mL蒸餾水,超聲分散;
2)稱取0.0010g均苯三甲酸,將其加入步驟1)的分散液中,超聲分散5min;
3)將得到的混合液置于100℃油浴中攪拌12h,然后蒸干蒸餾水,得到固體前驅體;
4)將所得前驅體在研缽中研磨均勻,然后倒入25mL坩堝中;
5)將研磨后的前驅體于氮氣保護下進行高溫聚合反應,反應初始溫度30℃,升溫速度為10℃/min,600℃下反應4h,反應所得黃色固體經研磨均勻,得到綠色熒光氮化碳粉末。
對比實例
1)稱取10g尿素,將其倒入40mL燒杯中,并往燒杯中加入15mL蒸餾水,超聲分散;
2)將得到的尿素溶液置于100℃油浴中攪拌12h,然后蒸干蒸餾水,得到固體前驅體;
3)將所得前驅體在研缽中研磨均勻,然后倒入25mL坩堝中;
4)將研磨后的前驅體于氮氣保護下進行高溫聚合反應,反應初始溫度30℃,升溫速度為3.0℃/min,500℃下反應2h,反應所得白色固體經研磨均勻,得到藍色熒光氮化碳粉末。
圖1為實施例1-3所得均苯三甲酸不同量摻雜的氮化碳粉末(CN-Trim)與對比實例所得未摻雜的氮化碳粉末(CN)的熒光發射光譜對比圖。從圖1可見,相較于未摻雜的氮化碳粉末,均苯三甲酸摻雜的氮化碳粉末的熒光紅移了65nm。
圖2為實施例1所得均苯三甲酸摻雜的氮化碳粉末(CN-Trim)與對比實例所得未摻雜的氮化碳粉末(CN)的紅外吸收光譜圖對比圖。從圖2可見,均苯三甲酸摻雜的氮化碳粉末和未摻雜的氮化碳粉末在810 cm-1處均有吸收,說明均苯三甲酸摻雜的氮化碳仍然保留了其三嗪環結構。
圖3為實施例1所得均苯三甲酸摻雜的氮化碳粉末(CN-Trim)與對比實例所得未摻雜的氮化碳粉末(CN)固體核磁碳譜。從圖3可見,均苯三甲酸摻雜的氮化碳粉末在130.7 ppm處均有芳環C=C峰,說明摻雜均苯三甲酸后苯環結構保留在氮化碳上。
以上所述僅為本發明的較佳實施例,凡依本發明申請專利范圍所做的均等變化與修飾,皆應屬本發明的涵蓋范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 一種熒光材料4?(N,N′?雙(4?羧基芐基)氨基)苯磺酸鎘配合物及合成方法與流程
- 一種熒光材料4?(N,N′?雙(4?羧基芐基)氨基)苯磺酸鈷配合物及合成方法與流程
- 一種熒光材料4?(N,N′?雙(4?羧基芐基)氨基)苯磺酸錳配合物及合成方法與流程
- 一種熒光材料4?(N,N′?雙(4?羧基芐基)氨基)苯磺酸鋅配合物及合成方法與流程
- 一種熒光材料4?(N,N′?雙(4?羧基芐基)氨基)苯磺酸銅配合物及合成方法與流程
- 一種熒光材料4?(N,N′?雙(4?羧基芐基)氨基)苯磺酸鎘配合物及合成方法與流程
- 一種Eu3+/Mg2+
- 一種熒光皮革材料的制造方法與制造工藝
- 復合襯底、使用該襯底的薄膜電致發光器件以及該器件的生產方法
- 在基材上布置粉末層的方法以及在基材上具有至少一個粉末層的層結構的制作方法