一種鋰離子摻雜磷酸鉍釤熒光粉及其制備方法與流程
本發明涉及稀土發光材料領域,具有涉及一種鋰離子摻雜磷酸鉍釤熒光粉及其制備方法。
背景技術:
稀土發光材料在整個固體發光領域占有很重要的地位,因為特殊的電子層結構使稀土元素具有一般元素無法比擬的性質。近幾年來,因為具有吸收能力強、發光亮度高、合成溫度適中等優點,稀土磷酸鹽在照明、量子光學、彩色電視機和熱釋發光檢測領域應用廣泛,引起了科研工作者廣泛的興趣。因此,尋找制作工藝簡單并且產物多功能化和特殊形貌的稀土磷酸鹽的方法無論是在工業生產還是科學研究上都具有重要價值,也在合成其它納米材料方面具有指導意義。
BiPO4是一種重要的無機磷酸鹽材料,具有六方相、低溫單斜相和高溫單斜相三種不同的結構,被廣泛應用于光催化、離子傳感器、鋰離子電池、放射性元素分離、微波介電、超級電容器等方面。該材料的性能在很大程度上取決于它的形貌,尺寸、結構及其組成。關于BiPO4:Ln3+熒光粉的研究已經取得很大成就,現有固相法、微波水熱法、溶劑熱法、共沉淀法、靜電紡絲法、聲化學法、水熱法等多種方法制備了多種結構形貌的BiPO4:Ln3+晶體。上述合成方法中,水熱法工藝簡單,反應條件溫和,可很好地控制產物的形貌,尺寸、結構,與此同時表面活性劑在控制晶體形貌,結構中也扮演著重要的角色。2008年,Guan等人首次報道了由納米棒組成的海膽狀微球BiPO4:Ln3+(Eu3+,Tb3+,Dy3+)熒光粉具有優異的發光性能,是一種優異的稀土發光材料基質,研究了不同Bi3+離子含量和反應時間對形貌的影響,提出了海膽狀微球的合成機理(Crystal Growth and Design,2008,8(8):2694-2697.);史曉磊等人通過水熱法合成BiPO4:Sm3+橙紅色熒光粉,并研究了不同pH值和Sm3+摻雜量對其發光材料的結構、形貌以及發光性能的影響。(Ceramics International,2015,41:3162–3168)。Joanna Cybinska等人首次使用離子液體輔助的微波合成的方法,研究了BiPO4:Ln3+(Ln=Sm,Eu,Tb,Dy)稀土離子摻雜的顏色可調控的發光材料(Journal of Luminescence,2016,170:641-647)。
迄今為止,現有的合成方法制得的BiPO4:Sm3+熒光粉結晶度低、發光強度不高,還沒有人提出能增強其發光的簡單便捷的方法。
技術實現要素:
本發明的目的在于克服現有技術中存在的缺陷,提供一種鋰離子摻雜磷酸鉍釤熒光粉及其制備方法,該方法工藝流程簡單,成本較低,制得的熒光粉具有結晶度高,發光強度高的優點。
為了達到上述目的,本發明方法采用如下技術方案:
包括以下步驟:
(1)取Bi(NO3)3·5H2O、Sm(NO3)3·6H2O和LiNO3固體粉末混合后加入到硝酸溶液中,攪拌均勻得到混合溶液A;
(2)再向混合溶液A中滴加NH4H2PO4溶液,繼續攪拌直到NH4H2PO4溶液充分溶解,得到混合溶液B;其中Bi(NO3)3·5H2O、Sm(NO3)3·6H2O、LiNO3和NH4H2PO4的比為3.8mmol:0.2mmol:xmmol:4mmol,x=0.1~1.0;
(3)調節混合溶液B的pH值至0.50~0.55,得到混合溶液C;
(4)混合溶液C在180℃~185℃下反應生成沉淀,至沉淀不增加時,自然冷卻到室溫;
(5)將步驟(4)得到的沉淀物離心分離,將離心分離得到的沉淀物洗滌并干燥,得到鋰離子摻雜磷酸鉍釤熒光粉。
進一步地,步驟(1)中硝酸溶液的體積分數為13%~13.6%;步驟(2)中NH4H2PO4溶液是將NH4H2PO4加入去離子水中攪拌20~30min制得的,其濃度為0.2~0.4mol/L;硝酸溶液和NH4H2PO4的比為10mL:4mmol。
進一步地,步驟(1)中攪拌10~15min得到混合溶液A。
進一步地,步驟(2)中攪拌20~30min得到混合溶液B。
進一步地,步驟(4)中,混合溶液C先攪拌40~60min,再轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中密封反應。
進一步地,不銹鋼反應釜體積填充度為80%。
進一步地,步驟(4)中反應12~13h。
進一步地,步驟(5)中離心分離是在轉速為10000r/min的條件下離心分離5~6min;洗滌是用水洗滌兩次,接著用乙醇洗滌一次。
進一步地,步驟(5)中的干燥是在75~85℃干燥箱中干燥10~12h。
一種利用如上所述制備方法制得的鋰離子摻雜磷酸鉍釤熒光粉,其特征在于:該鋰離子摻雜磷酸鉍釤熒光粉為單斜相結構,尺寸在0.5~3μm之間。
與現有技術相比,本發明具有以下有益的技術效果:
本發明制備方法中,具有以下優點:(1)本發明以Bi(NO3)3·5H2O、Sm(NO3)3·6H2O和LiNO3和NH4H2PO4等為原料,采用水熱法合成的BiPO4:Sm3+熒光粉,工藝流程簡單,成本較低,通過調節LiNO3的添加量就可以控制產物的發光強度,適合批量生產。(2)本發明通過添加LiNO3水熱合成BiPO4:Sm3+熒光粉,結果證明,添加LiNO3更能提高BiPO4:Sm3+熒光粉的發光性能。由水熱法添加Li+合成BiPO4:Sm3+熒光粉結晶度高,發光強度高。并且還沒有通過水熱法制備添加Li+可提高BiPO4:Sm3+熒光粉發光性能的相關報道。(4)本發明由水熱法添加Li+合成BiPO4:Sm3+熒光粉,其發光性能顯著提升對研究發光材料有重要意義。
本發明制得的Li+摻雜BiPO4:Sm3+熒光粉為單斜相結構,尺寸在0.5~3μm之間,相對沒有添加Li的BiPO4:Sm3+熒光粉,本發明熒光粉發光強度提高1.07~1.5倍,對開發BiPO4基熒光材料具有重要意義。
【附圖說明】
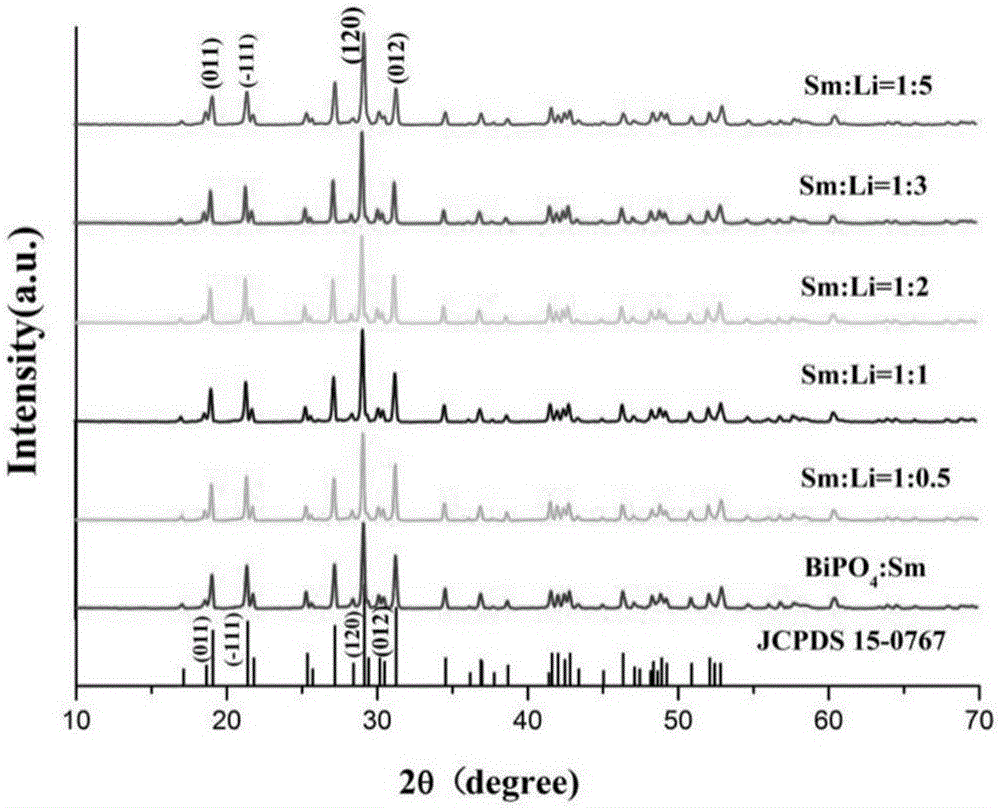
圖1是本發明由不同Li+添加量水熱合成Bi0.95PO4:0.05Sm3+熒光粉的XRD圖;
圖2是本發明由不同Li+添加量水熱合成Bi0.95PO4:0.05Sm3+熒光粉的發光圖譜。
【具體實施方式】
下面結合附圖,對本發明作進一步詳細說明。
本發明以Bi(NO3)3·5H2O、Sm(NO3)3·6H2O和LiNO3和NH4H2PO4等為原料,通過水熱法合成了更高發光強度的BiPO4:Sm3+熒光粉,研究了不同Li+添加量對BiPO4:Sm3+結構及發光性能的影響。
本發明制備方法,包括以下步驟:
(1)Bi(NO3)3·5H2O、Sm(NO3)3·6H2O、0~1.0mmol LiNO3和0.2~0.4mol/L的NH4H2PO4溶液,備用;其中NH4H2PO4溶液是將NH4H2PO4加入去離子水中,攪拌20~30min使其溶解,備用;
(2)取步驟1)備用的Bi(NO3)3·5H2O、Sm(NO3)3·6H2O和0~1.0mmol LiNO3混合,將其溶于體積分數為13%~13.6%的硝酸溶液,伴隨攪拌10~15min至均勻得到混合溶液A,即反應生成Bi0.95NO3:0.05Sm3+,Li+,再向混合溶液A中滴加NH4H2PO4溶液,繼續攪拌20~30min直到試劑充分溶解,得到混合溶液B;其中Bi(NO3)3·5H2O、Sm(NO3)3·6H2O、LiNO3、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:xmmol:10mL:4mmol,x=0.1~1.0;
(3)調節步驟2)得到的混合溶液B的pH值至0.50~0.55,得到混合溶液C;
(4)將步驟3)的混合溶液C攪拌40~60min后,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中密封,且反應釜體積填充度為80%,在180℃~185℃下反應12~13h至生成沉淀,至沉淀不增加時,后自然冷卻到室溫;
(5)將步驟4)得到的沉淀物在轉速為10000r/min的條件下離心分離5~6min,后將離心分離后沉淀物,用水洗滌兩次,接著用乙醇洗滌1次,后放入75~85℃干燥箱中干燥10~12h,最終由水熱法制備出添加Li+增強BiPO4:Sm3+發光性能的熒光粉。
本發明由水熱法制備出添加Li+增強BiPO4:Sm3+發光性能的熒光粉,樣品結晶度良好,屬于純低溫單斜相,其發光性能顯著增強。
下面結合具體的實施例對本發明做進一步詳細說明。
對比例1:
(1)取3.8mmol(1.843g)Bi(NO3)3·5H2O和0.2mmol(0.089g)Sm(NO3)3·6H2O放入燒杯混合,再將其溶于體積分數為13%的10mL硝酸溶液中,磁力攪拌15min,得到混合溶液A;
(2)稱量4mmolNH4H2PO4溶于20mL去離子水中,攪拌30min配制成0.2mol/L的NH4H2PO4溶液,將其滴加到步驟(1)所得的混合溶液A中,攪拌30min,保證其混合均勻,得到混合溶液B;其中Bi(NO3)3、Sm(NO3)3·6H2O、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:10mL:4mmol。
(3)在攪拌條件下用稀硝酸調節混合溶液B的pH=0.5,得到混合溶液C;
(4)將上述混合溶液C攪拌60min,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中,密封,在180℃下反應12h后,自然冷卻到室溫;
(5)將得到的沉淀物離心分離(轉速為10000r/min),離心時間為5min,并用水和乙醇重復洗滌沉淀物,離心分離,洗滌后放入80℃干燥箱中干燥11h,得到水熱法合成的Bi0.95PO4:0.05Sm3+熒光粉。
實施例1
(1)取3.8mmol(1.843g)Bi(NO3)3·5H2O、0.2mmol(0.089g)Sm(NO3)3·6H2O和0.1mmol(0.007g)LiNO3放入燒杯混合,再將其溶于體積分數為13%的10mL硝酸溶液中,磁力攪拌15min,得到混合溶液A;
(2)稱量4mmolNH4H2PO4溶于20mL去離子水中,攪拌30min配制成0.2mol/L的NH4H2PO4溶液,將其滴加到步驟(1)所得的混合溶液A中,攪拌30min,保證其混合均勻,得到混合溶液B;其中Bi(NO3)3、Sm(NO3)3·6H2O、LiNO3、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:0.1mmol:10mL:4mmol。
(3)在攪拌條件下用稀硝酸調節混合溶液B的pH=0.5,得到混合溶液C;
(4)將上述混合溶液C攪拌60min,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中,密封,在180℃下反應12h后,自然冷卻到室溫;
(5)將得到的沉淀物離心分離(轉速為10000r/min),離心時間為5min,并用水和乙醇重復洗滌沉淀物,離心分離,洗滌后放入80℃干燥箱中干燥11h,得到水熱法合成的添加Li+增強BiPO4:Sm3+發光性能的熒光粉。
本實施例是通過改變LiNO3的添加量,以研究LiNO3對形貌及其發光性能的影響。
將物質的量為0.1mmol(0.007g)的LiNO3粉末替換成物質的量為0.2mmol(0.014g)、0.4mmol(0.028g)、0.6mmol(0.041g)、1.0mmol(0.069g)的LiNO3粉末,并分別加入到Bi(NO3)3·5H2O和Sm(NO3)3·6H2O混合固體粉末的燒杯中;其它條件與實施例1相同。結合對比例1,此時LiNO3和Sm(NO3)3·6H2O的比值分別為0、0.5、1、2、3和5。
圖1是不同Li+添加量水熱合成Bi0.95PO4:0.05Sm3+熒光粉的XRD圖。從圖中可以看出,在Li+添加量和Sm3+的比值為0~5時,樣品的衍射峰與PDF標準卡(空間群P21/n(14),JCPDS15-0767)吻合,無其他衍射峰出現,各樣品結構均為低溫單斜相,且結晶度較高。隨著Li+添加量和Sm3+的比值從0增加到5的過程中,結晶度小幅度減小。從晶面(011)、(-111)、(120)、(012)可以看出峰高有所下降,由此得出,適量Li+的添加對Bi0.95PO4:0.05Sm3+熒光粉的結構有一些作用,但并不影響其純的低溫單斜相的本質結構。以上分析表明,需要添加適量的LiNO3,才能得到純低溫單斜相(低溫單斜相有利于提高發光性能),使發光強度達到最高。
圖2是不同Li+添加量水熱合成Bi0.95PO4:0.05Sm3+熒光粉在402nm激發下的發射光譜圖。由圖可知,不同Li+添加量沒有改變發射光譜的發射峰形和峰位,僅發射光譜強度隨Li+添加量出現變化。相對于0.2mmolSm(NO3)3·6H2O來說,當LiNO3添加量在0-0.6mmol范圍內,隨著LiNO3添加量的增加,熒光粉的發射光譜強度逐漸增強,在LiNO3添加量為0.6mmol即Sm(NO3)3·6H2O:LiNO3=1:3時發光性能達到最佳,當LiNO3添加量超過0.6mmol后,發射光譜強度有稍許降低,但是相對于不添加LiNO3時的發光強度還是顯著增強的。當LiNO3添加量在0-0.6mmol范圍內,其添加對發光性能的提升有促進作用,在LiNO3添加量為1.0mmol時,由于樣品中Li+過多,會影響Bi0.95PO4:0.05Sm3+熒光粉的結構,出現結晶度稍許下降的現象,可能是因為Li+占據的氧空位大量增加,使晶格擴張從而導致樣品的結晶度下降,因此發射光譜強度也有所下降。
由此可知,LiNO3添加量對Bi0.95PO4:0.05Eu3+熒光粉發光性能有重要影響,對其結構和形貌也有一定的影響。當LiNO3添加量在0-1.0mmol范圍內時,樣品結構保持為純低溫單斜相,隨LiNO3添加量的增多,熒光粉的發射光譜強度逐漸增強,在LiNO3添加量為0.6mmol即Sm(NO3)3·6H2O:LiNO3=1:3時發光性能達到最佳,當LiNO3添加量超過0.6mmol后,發射光譜強度有稍許降低,但是相對于不添加LiNO3時的發光強度還是顯著增強的,相對沒有添加Li的,其發光強度最少提高到原來的1.07倍,最高提高到原來的1.5倍。
實施例2:
(1)取3.8mmol(1.843g)Bi(NO3)3·5H2O、0.2mmol(0.089g)Sm(NO3)3·6H2O和0.2mmol(0.014g)LiNO3放入燒杯混合,再將其溶于體積分數為13%的10mL硝酸溶液中,磁力攪拌15min,得到混合溶液A;
(2)稱量4mmolNH4H2PO4溶于20mL去離子水中,攪拌25min配制成0.2mol/L的NH4H2PO4溶液,將其滴加到步驟(1)所得的混合溶液A中,攪拌30min,保證其混合均勻,得到混合溶液B;其中Bi(NO3)3、Sm(NO3)3·6H2O、LiNO3、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:0.2mmol:10mL:4mmol。
(3)在攪拌條件下用稀硝酸調節混合溶液B的pH=0.51,得到混合溶液C;
(4)將上述混合溶液C攪拌60min,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中,密封,在182℃下反應12h后,自然冷卻到室溫;
(5)將得到的沉淀物離心分離(轉速為10000r/min),離心時間為5min,并用水和乙醇重復洗滌沉淀物,離心分離,洗滌后放入80℃干燥箱中干燥12h,得到水熱法合成的添加Li+增強BiPO4:Sm3+發光性能的熒光粉。
實施例3:
(1)取3.8mmol(1.843g)Bi(NO3)3·5H2O、0.2mmol(0.089g)Sm(NO3)3·6H2O和0.4mmol(0.028g)LiNO3放入燒杯混合,再將其溶于體積分數為13%的10mL硝酸溶液中,磁力攪拌15min,得到混合溶液A;
(2)稱量4mmolNH4H2PO4溶于20mL去離子水中,攪拌20min配制成0.2mol/L的NH4H2PO4溶液,將其滴加到步驟(1)所得的混合溶液A中,攪拌30min,保證其混合均勻,得到混合溶液B;其中Bi(NO3)3、Sm(NO3)3·6H2O、LiNO3、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:0.4mmol:10mL:4mmol。
(3)在攪拌條件下用稀硝酸調節混合溶液B的pH=0.53,得到混合溶液C;
(4)將上述混合溶液C攪拌60min,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中,密封,在185℃下反應12h后,自然冷卻到室溫;
(5)將得到的沉淀物離心分離(轉速為10000r/min),離心時間為5min,并用水和乙醇重復洗滌沉淀物,離心分離,洗滌后放入80℃干燥箱中干燥10h,得到水熱法合成的添加Li+增強BiPO4:Sm3+發光性能的熒光粉。
實施例4:
(1)取3.8mmol(1.843g)Bi(NO3)3·5H2O、0.2mmol(0.089g)Sm(NO3)3·6H2O和0.6mmol(0.041g)LiNO3放入燒杯混合,再將其溶于體積分數為13.4%的10mL硝酸溶液中,磁力攪拌10min,得到混合溶液A;
(2)稱量4mmolNH4H2PO4溶于16mL去離子水中,攪拌28min配制成0.25mol/L的NH4H2PO4溶液,將其滴加到步驟(1)所得的混合溶液A中,攪拌20min,保證其混合均勻,得到混合溶液B;其中Bi(NO3)3、Sm(NO3)3·6H2O、LiNO3、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:0.6mmol:10mL:4mmol。
(3)在攪拌條件下用稀硝酸調節混合溶液B的pH=0.52,得到混合溶液C;
(4)將上述混合溶液C攪拌40min,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中,密封,在180℃下反應12.5h后,自然冷卻到室溫;
(5)將得到的沉淀物離心分離(轉速為10000r/min),離心時間為5.5min,并用水和乙醇重復洗滌沉淀物,離心分離,洗滌后放入75℃干燥箱中干燥12h,得到水熱法合成的添加Li+增強BiPO4:Sm3+發光性能的熒光粉。
實施例5:
(1)取3.8mmol(1.843g)Bi(NO3)3·5H2O、0.2mmol(0.089g)Sm(NO3)3·6H2O和1.0mmol(0.069g)LiNO3放入燒杯混合,再將其溶于體積分數為13.6%的10mL硝酸溶液中,磁力攪拌12min,得到混合溶液A;
(2)稱量4mmolNH4H2PO4溶于10mL去離子水中,攪拌22min配制成0.4mol/L的NH4H2PO4溶液,將其滴加到步驟(1)所得的混合溶液A中,攪拌25min,保證其混合均勻,得到混合溶液B;其中Bi(NO3)3、Sm(NO3)3·6H2O、LiNO3、硝酸溶液和NH4H2PO4的比為3.8mmol:0.2mmol:1.0mmol:10mL:4mmol。
(3)在攪拌條件下用稀硝酸調節混合溶液B的pH=0.55,得到混合溶液C;
(4)將上述混合溶液C攪拌50min,轉移到帶聚四氟乙烯內襯的不銹鋼反應釜中,密封,在181℃下反應13h后,自然冷卻到室溫;
(5)將得到的沉淀物離心分離(轉速為10000r/min),離心時間為6min,并用水和乙醇重復洗滌沉淀物,離心分離,洗滌后放入85℃干燥箱中干燥11h,得到水熱法合成的添加Li+增強BiPO4:Sm3+發光性能的熒光粉。
經測試,本發明制得的Li+摻雜BiPO4:Sm3+熒光粉為單斜相結構,尺寸在0.5~3μm之間。相對沒有添加Li+的,其發光強度提高到原來的1.07~1.5倍,對開發BiPO4基熒光材料具有重要意義。
以上所述僅為本發明的一種實施方式,不是唯一的實施方式,本領域科研,技術人員通過閱讀本發明,在未背離本工藝過程下所做的任何等效變換,均為本發明的權利要求所涵蓋。
- 還沒有人留言評論。精彩留言會獲得點贊!