一種二價錳離子激活熒光粉、制備方法及應用與流程
本發明涉及熒光粉技術領域,具體而言,涉及一種二價錳離子激活熒光粉、制備方法及應用。
背景技術:
光致發光是指物體依賴外界光源進行照射,并獲得能量,從而激發發光材料導致發光的現象,紫外光、可見光以及紅外輻射均可以引發光致發光。第四代綠色照明光源LED(光致發光二極管),就是利用光致發光的原理制成的(徐舒瑢,蘇勉曾,《發光學與發光材料》,化學工業出版社,2004)。
目前,主要是通過三基色LED混色法以及光轉換法以得到白光LED,其中,光轉換白光LED是現階段國際上白光照明的主流方案,而實現白光轉換的關鍵技術之一就是高效廣轉換材料的合成(X.Q.Piao,T.Horikawa,H.Hanzawa,et al.,Appl.Phys.Lett.88(2007)161908)。
已有現有技術證明二價錳離子可以作為激活離子,從而制備光致發光材料,并能夠發射多種波長的光(參閱文獻:J.C.Zhang,L.Z.Zhao,Y.Z.Long,et al.,Chem.Mater.27(2015)7481)。然而,現有技術中,二價錳離子激活的熒光粉的制備,均需要在還原性氣氛下進行(D.Haranath,S.Mishra,S.Yadav,et al.,Appl.Phys.Lett.101(2012)221905)。而還原氣氛下制備的熒光粉會在長期使用過程中,由于高溫氧化而導致色度坐標偏移(Jong Seong Bae Won and Jung Hyun Jeon,Appl.Phys.B.95(2009)715)。因此,能夠在非還原氣氛下制備出二價錳離子激活的熒光粉,不僅能夠降低制備成本,還能夠進一步提高熒光粉在高溫以及氧化條件下的使用效果。
有鑒于此,特提出本發明。
技術實現要素:
本發明的第一目的在于提供一種二價錳離子激活熒光粉的制備方法,所述方法在非還原氣氛下反應即能夠制得熒光粉,并通過在空氣條件下直接煅燒,實現四價錳離子到二價錳離子的自還原,并得到具有二價錳離子的激活熒光粉,從而解決了現有技術中熒光粉制備必須在還原性氣氛中進行,反應操作復雜且成本高,同時所制得的熒光材料易于高溫氧化等的技術問題。本發明方法具有制備方法便捷,所制得的熒光粉發光性能好、耐高溫氧化優點。
本發明的第二目的在于提供一種由本發明所述方法制備的熒光粉,本發明熒光粉具有發光性能好,且熒光粉不會在高溫環境下被氧化,色度坐標不會偏移等優點。
本發明的第三目的在于提供一種所述的熒光粉的用途,本發明熒光粉具有良好的發光性能,因而能夠作為紅色和黃色熒光粉而用于暖白光LED光致發光器件中。
為了實現本發明的上述目的,特采用以下技術方案:
一種二價錳離子激活熒光粉的制備方法,所述方法包括如下步驟:將堿金屬碳酸鹽,氧化鋅或氧化鎂,二氧化錳和磷酸二氫銨混合后加熱并保溫反應;然后,待反應體系冷卻后,將產物研磨均勻,并再次加熱并保溫燒結反應,待反應體系冷卻后,即得所述二價錳離子激活熒光粉;
其中,所述保溫反應以及保溫燒結反應都是在非還原氣氛下進行的。
可選的,本發明中,所述堿金屬碳酸鹽為碳酸鈉或碳酸鋰。
可選的,本發明中,所述碳酸鈉與氧化鋅的摩爾比為0.5:(0.83~1),所述碳酸鈉與氧化鎂的摩爾比為0.5:(0.83~1);所述碳酸鋰與氧化鋅的摩爾比為0.5:(0.84~1),所述碳酸鋰與氧化鎂的摩爾比為0.5:(0.86~1)。
可選的,本發明中,所述保溫反應的溫度為450~500℃,例如保溫反應的溫度可以為,但不限于460、470、480或者490℃;保溫反應的時間為20~30h,例如保溫反應的時間可以為,但不限于22、25、27或者29h。
可選的,本發明中,所述保溫燒結反應的溫度為600~1000℃,保溫燒結的反應時間為36~48h。優選的,本發明中,所述保溫燒結反應的溫度為800~1000℃,保溫燒結的反應時間為42~48h;例如保溫燒結的反應溫度可以為,但不限于、850、900或者950℃;保溫燒結的反應時間可以為,但不限于43、45或者47h。
本發明中,所述加熱保溫反應以及加熱保溫燒結反應均是在馬弗爐中進行的。
可選的,本發明中,所述二價錳離子激活熒光粉的化學式為NaZn1-x(PO3)3:xMn2+,其中x=0.001~0.17;或者,化學式為NaMg1-x(PO3)3:xMn2+,其中x=0.001~0.17;或者,化學式為LiZn1-xPO4:xMn2+,其中,x=0.001~0.16;或者,化學式為LiMg1-xPO4:xMn2+,其中x=0.001~0.14。
可選的,本發明中,所述堿金屬碳酸鹽,氧化鋅,氧化鎂純度不小于99.9%;二氧化錳純度不小于99.99%,磷酸二氫銨的純度不小于99.5%。
可選的,本發明中,所述保溫反應和所述保溫燒結反應的反應容器為坩堝;所述研磨是在研缽中進行的。進一步的,所述坩堝為鉑坩堝或剛玉坩堝;所述研缽為瑪瑙研缽。
進一步的,本發明反應整體步驟流程如下:
將堿金屬碳酸鹽,氧化鋅或氧化鎂,二氧化錳和磷酸二氫銨混合均勻后放入鉑坩堝或剛玉坩堝中;將鉑坩堝或剛玉坩堝放入馬弗爐中,并將溫度逐步升至450~500℃,并保溫反應20~30小時;反應結束后,將反應體系自然冷卻至室溫,然后,取出產物置于瑪瑙研缽中均勻研磨后,再次放入鉑坩堝或剛玉坩堝中;將坩堝放入馬弗爐中,并加熱至600~1000℃,保溫燒結反應36~48h;然后,保溫反應結束后,將反應體系自然冷卻至室溫,即獲得相應的二價錳離子激活的熒光粉。
其中所述堿金屬碳酸鹽,氧化鋅,氧化鎂純度不小于99.9%;二氧化錳純度不小于99.99%,磷酸二氫銨的純度不小于99.5%;所述堿金屬碳酸鹽為碳酸鈉或碳酸鋰,碳酸鈉與氧化鋅的摩爾為1:(0.83~1),碳酸鈉與氧化鎂的摩爾比為1:(0.83~1),碳酸鋰與氧化鋅的摩爾比為1:(0.84~1)摩爾比,碳酸鋰與氧化鎂的摩爾比為1:(0.86~1)。
本發明中,是以四種晶格結構中帶有三維剛性網狀結構的化合物:多磷酸鈉鋅鹽NaZn(PO3)3、多磷酸鈉鎂鹽NaMg(PO3)3、磷酸鋰鋅鹽LiZnPO4和磷酸鋰鎂鹽LiMgPO4為基質(即模板化合物)。然后,分別對此四種化合物合成的原料進行調整,以MnO2替換了部分用于合成此四種化合物所用的原料ZnO/MgO,從而使得在進一步所制得的新化合物中,Mn離子能夠替代原化合物中的部分Zn/Mg離子,并摻入四種化合物的三維剛性網狀結構的晶格中,并利用錳離子摻入特殊晶格時的自還原現象得到了穩定的二價錳晶格離子,從而獲得了二價錳離子激活熒光粉。
同時,本發明還提供了四種二價錳離子激活熒光粉,所述熒光粉是由本發明所述的方法制備得到的。
進一步的,本發明還提供了所述的熒光粉在光致發光器件中的應用。
本發明中,LiZn1-xPO4:xMn2+(其中,x=0.001~0.16)一種黃色熒光粉,在紫外光激發下,發射黃光。
同時,本發明中,NaZn1-x(PO3)3:xMn2+(其中x=0.001~0.17),NaMg1-x(PO3)3:xMn2+(其中x=0.001~0.17)以及LiMg1-xPO4:xMn2+(其中,x=0.001~0.14)為紅色熒光粉,在紫外光激發下,發射紅光。
與現有技術相比,本發明的有益效果為:
(1)本發明中,利用基質特殊的晶格結構,在非還原氣氛下獲得低價態的二價錳離子激活的熒光粉,并非還原氣氛中;利用錳離子摻入特殊晶格時的自還原現象穩定了二價錳離子,獲得了二價錳離子激活的紅色和黃色熒光粉。本發明方法具有反應產物純度高、成本低廉、設備簡單、易于推廣,且制備出的熒光粉不會在高溫環境下被氧化,色度坐標不會偏移等優點;
(2)本發明二價錳離子激活的熒光粉不會在高溫環境下被氧化,且色度坐標不會偏移,因此適于作為發光材料而用于電致發光器件中。
附圖說明
為了更清楚地說明本發明實施例或現有技術中的技術方案,以下將對實施例或現有技術描述中所需要使用的附圖作簡單地介紹:
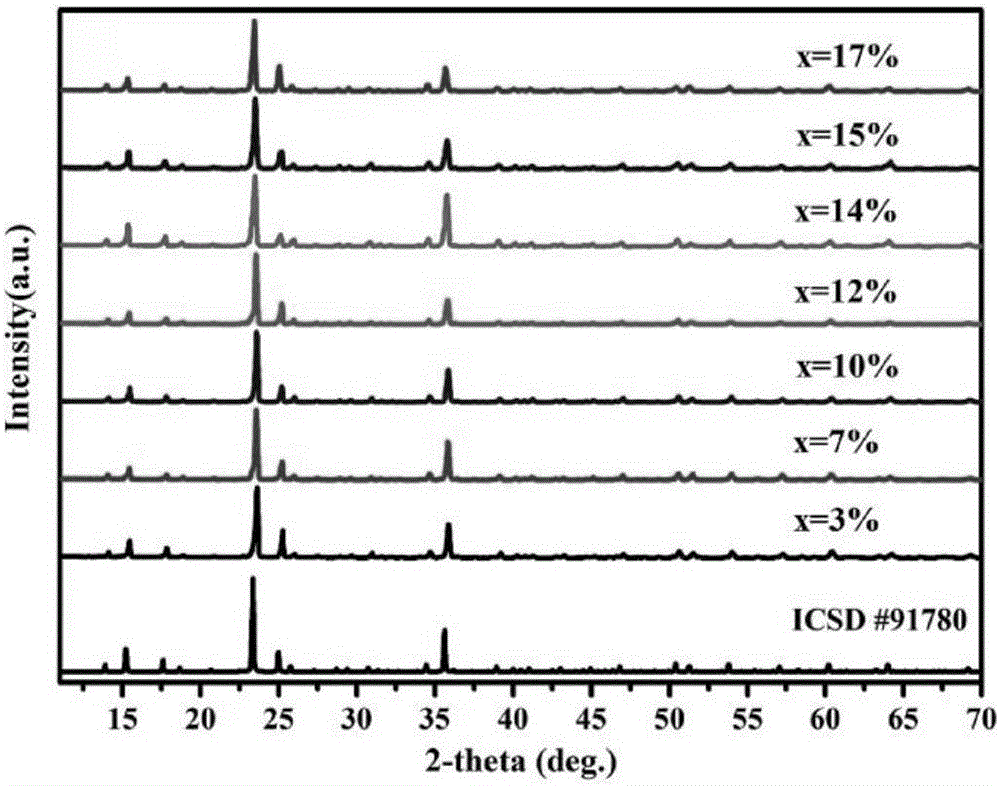
圖1為實施例1的熒光粉的XRD圖譜;
圖2為實施例1的熒光粉的激發和發射光譜;
圖3為實施例2的熒光粉的XRD圖譜;
圖4為實施例2的熒光粉的激發和發射光譜;
圖5為實施例3的熒光粉的XRD圖譜;
圖6為實施例3的熒光粉的激發和發射光譜;
圖7為實施例4的熒光粉的XRD圖譜;
圖8為實施例4的熒光粉的激發和發射光譜。
從圖1、3、5、7可以看出,所合成熒光粉為純相物質,不含氧化物等各種雜質,熒光粉的基質結構并沒有因為摻雜而改變。
從圖2、4、6、8中可以看出,所合成熒光粉出現典型的二價錳離子發光,其中NaZn1-x(PO3)3:xMn2+,NaMg1-x(PO3)3:xMn2+,LiMg1-xPO4:xMn2+發射紅光,LiZn1-xPO4:xMn2+發射黃光。
具體實施方案
下面將結合實施例對本發明的實施方案進行詳細描述,但是本領域技術人員將會理解,下列實施例僅用于說明本發明,而不應視為限制本發明的范圍。實施例中未注明具體條件者,按照常規條件或制造商建議的條件進行。所用試劑或儀器未注明生產廠商者,均為可以通過市售購買獲得的常規產品。
實施例1:
稱取0.005mol純度為99.9%的碳酸鈉,(0.01-x)mol純度為99.9%的氧化鋅,0.03mol純度為99.5%的磷酸二氫銨,(x)mol純度為99.99%的二氧化錳,其中x為0.00001~0.0017。
將上述原料放入研缽研磨均勻后,分別裝入剛玉坩堝和鉑坩鍋,并將坩堝置于馬弗爐中,以4℃/分鐘的速率從室溫升至500℃,并在500℃恒溫24小時,然后自然降溫至室溫。取出樣品置于瑪瑙研缽中再次充分研磨后,放回坩堝內,放入馬弗爐,加熱至800℃,恒溫48小時,自然降溫后取出再次研磨均勻。兩種坩鍋均可得到白色目標產物NaZn1-x(PO3)3:xMn2+(x=0.001~0.17)的粉末。
然后,對實施例1所得的NaZn1-x(PO3)3:xMn2+(x=0.001~0.17)粉末進行XRD表征,表征圖譜如圖1所示。
實施例2:
稱取0.005mol純度為99.9%的碳酸鈉,(0.01-x)mol純度為99.9%的氧化鎂,0.03mol純度為99.5%的磷酸二氫銨,(x)mol純度為99.99%的二氧化錳,其中x為0.00001~0.0017。
將上述原料放入研缽研磨均勻后,分別裝入剛玉坩堝和鉑坩鍋,將坩堝置于馬弗爐中,以4℃/分鐘的速率從室溫升至500℃,并在500℃恒溫24小時,然后自然降溫至室溫。取出樣品置于瑪瑙研缽中再次充分研磨后,放回坩堝內,放入馬弗爐,加熱至800℃,恒溫48小時,自然降溫后取出再次研磨均勻。兩種坩鍋均可得到白色目標產物NaMg1-x(PO3)3:xMn2+(x=0.001~0.17)的粉末。
然后,對實施例2所得的NaMg1-x(PO3)3:xMn2+(x=0.001~0.17)粉末進行XRD表征,表征圖譜如圖3所示。
實施例3:
稱取0.01mol純度為99.9%的碳酸鋰,(0.01-x)mol純度為99.9%的氧化鋅,0.01mol純度為99.5%的磷酸二氫銨,(x)mol純度為99.99%的二氧化錳,其中x為0.00001~0.0016。
將上述原料放入研缽研磨均勻后,分別裝入剛玉坩堝和鉑坩鍋,將坩堝置于馬弗爐中,以4℃/分鐘的速率從室溫升至500℃,并在500℃恒溫24小時,然后自然降溫至室溫。取出樣品置于瑪瑙研缽中再次充分研磨后,放回坩堝內,放入馬弗爐,加熱至800℃,恒溫48小時,自然降溫后取出再次研磨均勻。兩種坩鍋均可得到白色目標產物LiZn1-xPO4:xMn2+(x=0.001~0.16)的粉末。
然后,對實施例3所得的LiZn1-xPO4:xMn2+(x=0.001~0.16)粉末進行XRD表征,表征圖譜如圖5所示。
實施例4:
稱取0.01mol純度為99.9%的碳酸鋰,(0.01-x)mol純度為99.9%的氧化鎂,0.01mol純度為99.5%的磷酸二氫銨,(x)mol純度為99.99%的二氧化錳,其中x為0.00001~0.0014。
將上述原料放入研缽研磨均勻后,分別裝入剛玉坩堝和鉑坩鍋,將坩堝置于馬弗爐中,以4℃/分鐘的速率從室溫升至500℃,并在500℃恒溫24小時,然后自然降溫至室溫。取出樣品置于瑪瑙研缽中再次充分研磨后,放回坩堝內,放入馬弗爐,加熱至800℃,恒溫48小時,自然降溫后取出再次研磨均勻。兩種坩鍋均可得到白色目標產物LiMg1-xPO4:xMn2+(x=0.001~0.14)的粉末。
然后,對實施例4所得的LiMg1-xPO4:xMn2+(x=0.001~0.14)粉末進行XRD表征,表征圖譜如圖7所示。
實驗例1
測定實施例1所得到的二價錳激活的多磷酸鈉鋅鹽樣品的光致發光性質。測定用氙燈光源,功率450W,步長1nm,電壓950V,光柵1nm,波長360nm。將樣品夾在兩個石英片之間,樣品片厚1mm,選定條件后,激發光照射樣品,采集發射光譜線,獲得有效的紅光發射。
實施例1的NaZn1-x(PO3)3:xMn2+(x=0.001~0.17)的激發和發射光譜如圖2所示。
實驗例2
測定實施例2所得到的二價錳激活的多磷酸鈉鎂鹽樣品的光致發光性質。測定用氙燈光源,功率450W,步長1nm,電壓950V,光柵1nm,波長360nm。將樣品夾在兩個石英片之間,樣品片厚1mm,選定條件后,激發光照射樣品,采集發射光譜線,獲得有效的紅光發射。
實施例2的NaMg1-x(PO3)3:xMn2+(x=0.001~0.17)的激發和發射光譜如圖4所示。
實驗例3
測定實施例3所得到的二價錳激活的磷酸鋰鋅鹽樣品的光致發光性質。測定用氙燈光源,功率450W,步長1nm,電壓950V,光柵1nm,波長414nm。將樣品夾在兩個石英片之間,樣品片厚1mm,選定條件后,激發光照射樣品,采集發射光譜線,獲得有效的黃光發射。
實施例3的LiZn1-xPO4:xMn2+(x=0.001~0.16)的激發和發射光譜如圖6所示。
實驗例4
測定實施例4所得到的二價錳激活的磷酸鋰鎂鹽樣品的光致發光性質。測定用氙燈光源,功率450W,步長1nm,電壓950V,光柵1nm,波長407nm。將樣品夾在兩個石英片之間,樣品片厚1mm,選定條件后,激發光照射樣品,采集發射光譜線,獲得有效的紅光發射。
實施例4的LiMg1-xPO4:xMn2+(x=0.001~0.14)的激發和發射光譜如圖8所示。
以上實例表明,以碳酸鈉或碳酸鋰,氧化鋅或氧化鎂,二氧化錳和磷酸二氫銨為原料,均可以有效合成出相應的二價錳激活的多磷酸鈉鋅鹽、二價錳激活的多磷酸鈉鎂鹽、二價錳激活的磷酸鋰鋅鹽和二價錳激活的磷酸鋰鎂鹽熒光粉。
進一步的,以實施例1-4所制得的熒光粉作為發光材料可進一步制備光致發光器件,所制得的光致發光器件的色度坐標不會由于二價錳被氧化而發生偏移。
應該指出,上述的實施例只是用具體的實例來說明本發明,而不應是對本發明的限制。同時,本領域的普通技術人員都知道,在本發明的構思基礎上,對本發明所進行的各種修改和變化均在本專利的保護范圍。
盡管已用具體實施例來說明和描述了本發明,然而應意識到,在不背離本發明的精神和范圍的情況下可以作出許多其它的更改和修改。因此,這意味著在所附權利要求中包括屬于本發明范圍內的所有這些變化和修改。
- 還沒有人留言評論。精彩留言會獲得點贊!