一種基于非對稱疏水尾可電離脂質的脂質納米粒及其制備方法和應用
本發明涉及一種基于非對稱疏水尾可電離脂質的脂質納米粒及其制備方法和應用,屬于藥物遞送。
背景技術:
1、隨著rna干擾(rnai)的發現和小干擾rna(sirna)能瞬時誘導特異性信使rna(mrna)降解的證實,人們在過去的二十年里進行了大量的努力來利用基因沉默進行疾病治療。sirna、mrna等核酸藥物由于能被快速化學合成并以序列依賴性方式直接作用于靶基因而成為理想的候選藥物。原則上sirna能夠靶向包括剪接變異體和突變體在內的所有基因,這表明sirna適用于靶向不可藥物化的蛋白質。因此,sirna對于多種疾病十分有應用前景。
2、由于sirna是多價陰離子和高度親水性的中等大小分子,因此它幾乎不能被細胞攝取。此外,sirna容易被血液中的核酸酶降解,導致sirna不能在靶組織中累積。因此,建立合適的遞送載體對sirna藥物的開發至關重要。脂質納米粒(lnp)因其優異的生物降解性、低毒性、結構靈活性、生物相容性及易于大規模制備等優點,已成為非病毒載體中最具臨床應用前景的載體。lnp可以保護sirna免于降解,并確保其在循環中的穩定性,減少免疫活化,能夠定位于靶組織,并促進細胞內遞送。lnp遞送系統直徑通常約為50~200nm,一般由可電離陽離子脂質、膽固醇、磷脂和聚乙二醇(peg)-脂質組成,可以有效地將sirna遞送到細胞質中,參與rnai機制并隨后抑制特異性mrna翻譯。
3、可電離陽離子脂質在基于lnp的sirna遞送中起關鍵作用。首先,在酸性條件下,脂質帶正電荷,可將帶負電荷的核酸藥物裝載在納米顆粒內。其次,含有可電離脂質lnp的最佳酸解離常數(pka)為6.0~6.9,在生理ph值下總lnp表面電荷接近中性,在體內遞送過程中毒性更低。第三,可電離脂質在內涵體酸性環境中(ph=5-6)中顯示出正電荷,以便與內源性陰離子脂質相互作用釋放sirna進入細胞質。最后,為了有效地使內涵體膜不穩定并將核酸釋放到細胞膜中,脂質必須表現出促進六邊形(hii)脂質相形成的物理形狀。因此,合理的脂質設計與迭代篩選過程相結合,以確定烷基鏈、連接官能團和可電離頭部基團的最佳組合。盡管目前已經報道了一系列可電離陽離子脂質,但是仍然需要更高效和穩定遞送性能的可電離脂質化合物。高效的可電離脂質為rna-lnp提供更好的轉染效果,同時保持低毒性。因此,本項目研究目標旨在設計合成新型可電離陽離子脂質,高效封裝遞送sirna用于疾病的治療。
技術實現思路
1、為改善上述技術問題,本發明提供了一種式(i)所示的化合物:
2、
3、其中,
4、l1選自a1、a2、a3相同或不同,彼此獨立地不存在或者選自無取代或任選被一個、兩個或更多個ra取代的下列基團:亞c1-6烷基、亞c1-6烷基氧基、亞c2-6烯基、亞c3-8環烷基、亞3-8元雜環基、亞c6-10芳基、亞5-10元雜芳基、nh;每個ra相同或不同,彼此獨立地選自c1-10烷基;p和q相同或不同,彼此獨立地選自0、1、2、3、4、5或6;
5、j不存在或者選自h、
6、當j不存在時,b2-j選自-oc(=o)-、-c(=o)o-;當j為h時,b2-j選自-nh-、-nhc(=o)-、-c(=o)nh-;當j為時,b2為n;
7、b1選自n、
8、u1、u2、g1、g2、e1、e2、j1、j2、k1、k2、q1、q2彼此獨立地選自-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-、無取代或任選被一個、兩個或更多個rb取代的下列基團:亞c1-6烷基、亞c1-6烷基氧基、亞c2-6烯基;每個rb相同或不同,彼此獨立地選自oh、c1-10烷基;
9、u1、u2與j1、j2不同;和/或,
10、g1、g2與k1、k2不同;和/或,
11、e1、e2與q1、q2不同;
12、n1、n2相同或不同,彼此獨立地選自2-25的數,例如3、5、7、10、12和13。
13、m1、m2相同或不同,彼此獨立地選自1-25的數,例如2、4、7、9、15、18和22。
14、根據本發明的實施方案,a1、a2、a3相同或不同,彼此獨立地不存在或者選自無取代或任選被一個、兩個或更多個ra取代的下列基團:亞甲基、亞乙基、亞丙基、亞丁基、亞甲氧基、亞乙氧基、亞丙氧基、o、nh、亞哌嗪基、亞苯基。
15、根據本發明的實施方案,每個ra相同或不同,彼此獨立地選自c1-6烷基;例如甲基、乙基。
16、根據本發明的實施方案,l1選自l-1、l-2、l-3、l-4、l-5、l-6、l-7、l-8、l-9、l-10、l-11或l-12;
17、
18、根據本發明的實施方案,u1、u2相同或不同,彼此獨立地選自-ch2-、-(ch2)u-、-ch(oh)-、-ch2o-、-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-;u選自2、3、4、5、6、7、8、9或10;
19、根據本發明的實施方案,j1、j2相同或不同,彼此獨立的選自-ch2-、-(ch2)u-、-ch(oh)-、-ch2o-、-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-、-ch=ch-、-ch2-ch=ch-;u選自2、3、4、5、6、7、8、9或10。
20、根據本發明的實施方案,g1、g2相同或不同,彼此獨立地選自-ch2-、-ch(oh)-、-ch2o-、-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-、-ch=ch-、-ch2-ch=ch-。
21、根據本發明的實施方案,e1、e2相同或不同,彼此獨立地選自-ch2-、-ch(oh)-、-ch2o-、-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-、-ch=ch-、-ch2-ch=ch-。
22、根據本發明的實施方案,k1、k2相同或不同,彼此獨立地選自-ch2-、-ch(oh)-、-ch2o-、-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-、-ch=ch-、-ch2-ch=ch-、-(ch=ch)2-、-(ch2-ch=ch)2-。
23、根據本發明的實施方案,q1、q2相同或不同,彼此獨立地選自-ch2-、-ch(oh)-、-ch2o-、-oc(=o)-、-c(=o)o-、-c(=o)nh-、-nhc(=o)-、-c(=o)s-、-ch=ch-、-ch2-ch=ch-、-(ch=ch)2-、-(ch2-ch=ch)2-。
24、根據本發明的實施方案,相同或不同,彼此獨立地選自-c8h17、
25、根據本發明的實施方案,不同,彼此獨立地選自-c6h13、-c7h15、-c8h17、-c9h19、-c10h21、-c11h23、-c12h25、-c13h27、-c14h29、-c15h31、-c16h33、-c17h35、-(ch2)6-ch=ch-(ch2)7ch3、-(ch2)6-ch=ch-ch2-ch=ch-(ch2)4ch3、-(ch2)6-ch=ch-ch2-ch=ch-ch2-ch=ch-(ch2)2ch3、
26、根據本發明的實施方案,式(i)所示化合物選自以下結構的化合物:
27、
28、其中,l1、b1、b2、u1、u2、g1、g2、e1、e2、j1、k1、q1、n1、n2、m1彼此獨立地具有上文所述的定義。
29、根據本發明的實施方案,式(i)所示化合物選自以下結構的化合物:
30、
31、其中,j、l1、u1、u2、g1、g2、e1、e2、j1、k1、q1、n1、n2、m1彼此獨立地具有上文所述的定義。
32、根據本發明的實施方案,式(i)所示化合物選自以下結構的化合物:
33、
34、本發明提供了一種空白脂質納米粒,包括式(i)所示的化合物、中性磷脂、甾類脂質和聚乙二醇脂質(peg);
35、根據本發明的實施方案,所述中性磷脂選自dspc、dppc、dppe、dmpe、popc、dopg、dope、pope和depc中的至少一種,優選為二硬脂酰基磷脂酰膽堿(dspc);
36、根據本發明的實施方案,所述甾類脂質選自燕麥甾醇、谷甾烷醇、谷甾醇、豆甾烷醇、豆甾醇、β-谷甾醇、菜子甾醇、麥角骨化醇、菜油甾醇、膽甾烷醇、膽固醇、糞甾醇、羥基膽固醇、羊毛甾醇、二氫膽固醇、二氫麥角甾醇、光甾醇、海藻甾醇、膽酸、甘氨膽酸、牛磺膽酸、脫氫膽固醇、鏈甾醇、二氫麥角骨化醇、表膽甾醇、麥角甾醇、巖藻甾醇、六氫光甾醇和脫氧膽酸,優選為膽固醇(cho)。
37、根據本發明的實施方案,所述peg脂質選自dspe-peg、dmg-peg、mg-peg、dag-peg、dsg-peg、dppe-peg和dma-peg至少一種,優選為1,2-二肉豆蔻酰-rac-甘油-3-甲氧基聚乙二醇2000(dmg-peg?2000)。
38、根據本發明的實施方案,式(i)所示的化合物占的摩爾分數為15-65%,例如35-50%,如40%、43%、47%、49%;
39、根據本發明的實施方案,所述peg脂質占的摩爾分數為0.1-6%,例如0.5-3.5%,如0.8%、1%、1.5%、1.7%、2.7%、3.4%;
40、根據本發明的實施方案,所述中性磷脂占的摩爾分數為5-25%,例如10-15%,如11%、13%、14%、15%;
41、根據本發明的實施方案,所述甾類脂質占的摩爾分數為10-50%,例如30-45%,如32%、37%、39%、40%、41%、43%、45%。
42、根據本發明一個實施方案,式(i)所示的化合物、中性磷脂、甾類脂質、peg脂質的摩爾比為50:10:38.5:1.5。
43、本發明所述空白脂質納米粒可以采用本領域常規的脂質納米顆粒制備方法制備得到,例如高壓乳勻法、乙醇注入法、超聲分散法、微流控法等。
44、本發明還提供所述空白脂質納米粒作為藥物載體的應用。
45、本發明還提供一種載藥脂質納米粒組合物,所述載藥脂質納米粒包括所述的空白脂質納米粒、藥學上可接受的輔料和藥物。
46、本發明所述的藥學上可接受的輔料包括佐劑、稀釋劑等。
47、根據本發明的實施方案,所述空白脂質納米粒與所述藥物的質量比為(5-30):1,例如(10-20):1,優選為10:1、15:1、20:1、25:1、30:1、40:1。
48、根據本發明的實施方案,所述藥物可以為小分子化合物、核酸、寡肽等,優選地,所述的藥物為核酸。
49、進一步的,核酸分子可以選自sirna、mrna、aso、質粒和sarna中的至少一種。
50、進一步的,所述核酸用于預防和/或治療癌癥、炎癥、纖維化疾病、自身免疫病、感染、精神性病癥、血液病、染色體疾病、遺傳病、結締組織疾病、消化性疾病、耳鼻喉疾病、內分泌疾病、眼病、生殖性疾病、心臟病、腎病、肺病、代謝性病癥、口部疾病、肌肉骨骼疾病、新生兒篩查、營養性疾病、寄生蟲疾病、皮膚疾病等。
51、本發明還提供了所述載藥脂質納米粒組合物用于遞送sirna至細胞或器官的應用。
52、本發明還提供所述載藥脂質納米粒組合物的制備方法,包括以下步驟:將所述藥物裝載于所述空白脂質納米粒上,得到所述載藥脂質納米粒組合物。
53、根據本發明的實施方案,所述制備方法包括以下步驟:
54、(1)將所述藥物溶于檸檬酸鈉水溶液中,得到藥物溶液;
55、(2)將所述空白脂質納米粒的溶液與檸檬酸鈉緩沖液混合,得到脂質體溶液;
56、(3)將所述藥物溶液加入到所述脂質體溶液中在適當溫度下進行加熱,得到所述載藥脂質納米粒組合物。
57、根據本發明的實施方案,步驟(3)中所述加熱的溫度為25℃-100℃。
58、根據本發明的實施方案,步驟(3)中所述加熱的時間為10min~60min。
59、優選地,所述加熱的溫度為50℃,加熱時間為30min。
60、根據本發明的實施方案,步驟(3)中所述藥物溶液與所述脂質體溶液的體積比為1:(0.5-5),例如1:(0.8-3),優選為1:1。
61、有益效果
62、1.本發明設計合成了一種式(i)所示的新型非對稱可電離脂質;
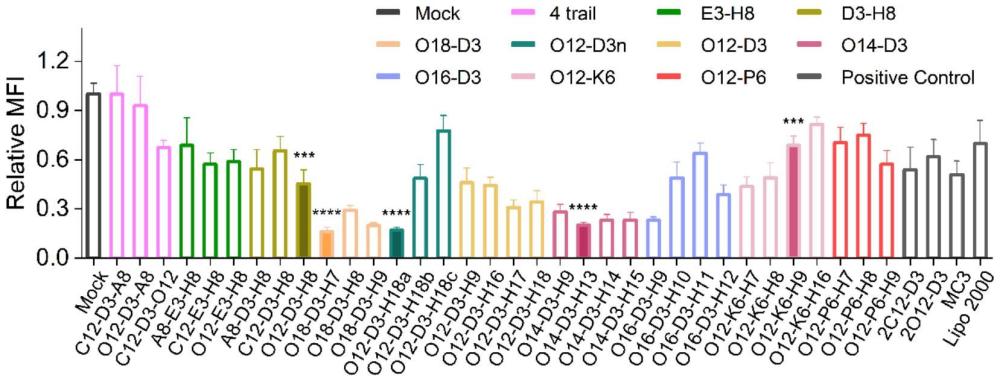
63、2.本發明基于上述非對稱可電離脂質制備的空白脂質納米粒可作為藥物載體,該脂質納米粒具有均一粒徑、高載藥量和低毒性,在內涵體中可電離,具有優異的內涵體逃逸效果。與上市可電離脂質mc3或商品化轉染試劑lipo2000相比,具有更高的體內外轉染效率。
- 還沒有人留言評論。精彩留言會獲得點贊!