一種人凝血因子Ⅷ的制備方法與流程
本發明涉及一種人凝血因子ⅷ的制備方法,屬于生物制藥領域。
背景技術:
甲型血友病(ha)為最常見的遺傳性出血性疾病,系由血漿中凝血因子ⅷ(fⅷ)缺失所致。fⅷ基因位于x染色體,所以患者絕大多數為男性,女性雜合子為攜帶者,而女性患者極少見。重型患者自幼即有反復自發性出血,不經治療者往往造成關節畸形和致殘,嚴重者可因顱內出血死亡。目前仍以替代療法為主,如全血、冷沉淀、人凝血因子ⅷ制劑等,由于全血和冷沉淀純度低、輸注量大、副反應多、存在傳播血液病毒的風險等,臨床全血或冷沉淀替代療法已少用,多用人凝血因子ⅷ制劑替代療法。
人凝血因子ⅷ亦稱抗血友病球蛋白,是一種血漿糖蛋白,在凝血機制中的內部途徑的級聯反應中起著必不可少的作用。臨床上廣泛應用于治療甲型血友病和獲得性凝血因子ⅷ缺乏而致的出血癥狀及這類病人的手術出血治療。
隨著蛋白質純化技術的發展,以冷沉淀或cohn組分i為原料的各種純化方法不斷建立、完善和改良,純度越來越高fⅷ產品相繼產生。低溫乙醇法、凝膠過濾法、離子交換層析法、親和層析等方法都是制備fⅷ制劑的有效方法,特別是幾種方法的聯合使用,使fⅷ的純度甚至比原血漿有較大幅度的提高。純度越來越高的fⅷ制劑在甲型血友病的治療中發揮著巨大的作用。目前一般接受治療的血友病人都能夠進行正常的生活和工作,生活質量和平均壽命基本接近正常人。
fⅷ在血漿中的含量極微,1ml血漿中僅含0.1~0.2μg,故其純品的獲得受到蛋白純化技術發展的限制而極為困難。由于國家對原料血漿的嚴格控制和人凝血因子ⅷ提取困難,國內只有少數幾家公司生產人凝血因子ⅷ,而我國甲型血友病患者保守估計為7~10萬,臨床需求巨大,導致人凝血因子ⅷ臨床供應十分緊張,甚至出現“一藥難求”的現象。國家食品藥品監督管理局批準拜耳醫藥生產的重組人凝血因子ⅷ在國內上市,但其高昂的價格(約6元/iu)讓國內普通的患者難以承受。而國內生產的人凝血因子ⅷ價格(約2元/iu),遠低于進口重組人凝血因子ⅷ,可大大降低患者的醫療成本。本發明為健康人血漿經低溫離心分離得到冷沉淀,再經粗分離、離子交換層析提純、超濾、進行脂包膜病毒滅活(有機溶劑/去污劑法,s/d法)、配制、除菌過濾、分裝凍干,凍干后再進行非脂包膜病毒滅活或去除處理(干熱法,100℃,30分鐘)制成人凝血因子ⅷ。對缺乏人凝血因子ⅷ所致的凝血機能障礙具有糾正作用,主要用于防治甲型血友病和獲得性凝血因子ⅷ缺乏而致的出血癥狀及這類病人的手術出血治療。
傳統人凝血因子ⅷ制備方法中有甘氨酸沉淀法、peg沉淀法、酸沉淀法、離子交換層析法等,制備過程中多采用高速離心法去除雜質不溶物,由于人凝血因子ⅷ易激活、易水解,特別是劇烈條件易導致活性喪失,蛋白激活從而影響制品的質量。其次,人凝血因子ⅷ制備過程顆粒物的去除多采用濾芯過濾去除如用1.0μm、0.65.μm、0.45μm等,該種濾芯可去除蛋白顆粒物,但很難去除可溶性的脂質蛋白。再者人凝血因子ⅷ冷凍干燥過程凍干工藝不成熟易引起蛋白活性損失、質量不合格等。
在人凝血因子ⅷ制備方法中還應該注意到溶解性、復溶時間、效價及比活性等問題。由于人凝血因子ⅷ存在含量低、易激活、易水解等現象,導致在制備過程中存在以下問題(1)純度不高,產品雜質含量偏多,臨床使用易發生皮疹、心動過速、發熱等不良反應;(2)效價及比活性低,由于制備過程中易激活、易水解,導致產品的效價及比活性低,從而影響臨床療效;(3)得率不高,由于血漿中人凝血因子ⅷ含量低,提取困難,導致得率低;(4)可能存在傳播血液病毒的風險。
本申請人是一家經國家認定的血液制品定點生產單位。正在研發人凝血酶原復合物和凝血因子ⅷ等系列產品,力爭成為全國血液制品行業中品種最多、規格最全的廠家之一。先后申請授權了多項有關人凝血因子ⅷ的發明專利并查詢對比國內現有的人凝血因子ⅷ的發明專利,如:
zl201010534849.9《一種人凝血因子ⅷ的制備工藝》,制備工藝包括取冷沉淀:室溫融解1-2h,處理成1.8-2.2cm的方塊;冷沉淀溶解;鋁膠吸附;離心收集上清液;酸沉淀;離心收集上清液;s/d滅活;過濾;deaesepharoseff層析柱平衡;層析;洗滌;洗脫;超濾透析,配液;分裝;凍干;干熱滅活。本發明它采用離子交換層析技術,并在生產工藝采用離心法結合氫氧化鋁凝膠吸附及酸沉淀法去除雜質;此外生產過程中采用s/d法去除脂包膜病毒及99.5±0.5℃干熱法去除非脂包膜病毒,經過這2次病毒滅活步驟顯著提高了臨床用藥的安全性。
cn201510879630.5《一種凍干人凝血因子ⅷ的制備方法》,制備工藝包括取冷沉淀的溶解,50p濾板串聯0.45μm濾芯過濾,收集澄清濾液;deaesephadexa-50凝膠去除維生素k依賴的凝血因子;陰離子交換樹脂柱層析純化fⅷ;超濾透析并濃縮洗脫液;濃縮液中加入穩定劑并調節fⅷ的效價及ph值;納米膜除病毒過濾;除菌過濾及分裝;凍干;干熱病毒滅活。該制備工藝采用deaesephadexa-50凝膠吸附去除維生素k依賴的凝血因子,代替傳統的氫氧化鋁及peg沉淀方式,具有生產穩定、得率高、質量好的優點;采用三步病毒滅除措施使產品的安全性大大提高。
zl201410524351.2《一種從冷沉淀提取凝血因子ⅷ的廢料中提取人纖維蛋白原的制備工藝》,包括:冷沉淀溶解、離心收集上清液、2%氫氧化鋁凝膠吸附、離心收集上清液、調節離子強度、串聯過濾、s/d病毒滅活、離子交換層析、edta除ca2+、甘氨酸沉淀、第一次低溫乙醇沉淀、at-ⅲ抑制凝血酶、第二次低溫乙醇沉淀、納米膜過濾以及干熱滅活。本發明為了確保安全性,除了s/d及干熱滅活外,新增納米膜過濾除病毒;新增at-ⅲ滅活凝血酶及edta除ca2+工藝,有效阻止在生產過程中纖維蛋白原激活成纖維蛋白;用甘氨酸沉淀去除制品中的纖維蛋白單體和多聚體,以獲得高純度的人纖維蛋白原;所得制劑產品安全可靠,復溶時間短,滿足臨床上救急之需,同時間接節約稀缺血漿資源具有重要意義。
cn201610077346.0《一種從冷沉淀提取凝血因子ⅷ的廢料中提取人血管性血友病因子的制備工藝》,用一步q-sepharose陰離子交換層析及一步親和層析純化得到純度較高的vwf:收集冷沉淀提取凝血因子ⅷ的廢料即在冷沉淀提取凝血因子ⅷ的制備中經層析柱流出來的液體作為原料;通過q-sepharose離子交換柱層析后,收集洗脫液,再經明膠親和層析,去除殘余的纖維結合蛋白及雜質,得到血管性血友病因子。本發明獲得高純度的血管性血友病因子,質量可靠,可滿足臨床上血管性血友病人急需的治療用藥需求。同時對于冷沉淀的綜合利用,間接節約稀缺血漿資源具有十分重要的意義。
目前,人凝血因子ⅷ為治療甲型血友病的特效藥,目前國內市場仍處于短缺狀況,開發人凝血因子ⅷ可提高血漿這一寶貴資源的利用率,增加血液制品的附加值,有效降低甲型血友病患者的醫療成本,部分緩解人凝血因子ⅷ臨床用藥的緊張局面。
技術實現要素:
本發明的目的在于提供一種新的人凝血因子ⅷ的制備方法。
本發明的主要技術構思如下:
本發明于人血漿融解后,經二步壓濾粗分離人凝血因子ⅷ;對經前期粗分離后的蛋白液經一步q-sepharose-ff離子交換,效價及比活性進一步提高,再經干熱滅活,進一步提高臨床用藥的安全性;
本發明的制備工藝,依次包括:人血漿的融解、低溫離心收集冷沉淀、冷沉淀溶解、k700濾板進行壓濾,收集壓濾液、調整ph值,加入2%氫氧化鋁凝膠吸附、ek濾板進行壓濾,收集壓濾液、調節ph值,蛋白濃度,cunodelp深層濾芯過濾,收集濾液、s/d法病毒滅活、調整ph值,離子強度、離子交換層析上樣,洗滌,洗脫,收集洗脫液、兩步梯度透析,濃縮,稀配、0.22μm濾芯除菌過濾、無菌分裝、冷凍干燥、干熱病毒滅活、真空檢測、成品入庫。本發明是這樣來實現的,其具體工藝方案如下:
(1)、檢疫期檢疫合格的人血漿領取后,75%乙醇擦拭血漿袋表面,用注射用水沖洗,合并到融漿罐中,用30~35℃以下循環水融化,血漿溫度控制不高于4℃;待融化后,離心,出液溫度控制在0~4℃,收集冷沉淀,稱重;
(2)、將步驟(1)的制得物冷沉淀加入其6倍重量的溶解液中,攪拌至冷沉淀完全溶解,循環水的溫度控制在20~26℃;開始用k700濾板(頗爾公司)進行壓濾,控制壓力不大于0.2mpa,出液溫度為20~26℃,收集壓濾液,稱重;溶解液配制方法:3000iu肝素鈉,2.5g三羥甲基氨基甲烷,0.75g甘氨酸,補加注射用水至1l,調節ph為6.5~7.5,溫度控制在20~26℃;
(3)、將步驟(2)的制得物上清液用0.5mol/lhcl調節ph至6.46~6.66;加入2%氫氧化鋁凝膠,攪拌;開始用ek濾板進行壓濾,控制壓力不大于0.2mpa,出液溫度為20~26℃,收集壓濾液,稱重,測蛋白濃度;
(4)、將步驟(3)的制得物壓濾液用0.5m氫氧化鈉溶液調節ph至6.5~7.5;用蛋白濃度緩沖液調節蛋白濃度不大于15.0g/l;用cunodelp深層濾芯過濾,收集過濾液,稱重;蛋白濃度緩沖液的配制方法:2.5g三羥甲基氨基甲烷,0.9g氯化鈣,4.2g氯化鈉,1.2g甘氨酸,加適量注射用水充分溶解,補加注射用水至1l,調節ph為6.5~7.5;
(5)、按步驟(4)的制得物過濾液體積的1/10加入s/d溶液,攪拌均勻,溫度控制在24~26℃,連續保溫6小時;0.45μm濾芯過濾收集濾液;s/d溶液的配制方法:用清潔容器裝約850ml,70℃以上注射用水,在攪拌情況下加入聚山梨酯80110g,再緩慢加入磷酸三丁酯33g,繼續攪拌至澄清透明后降溫至30℃以下,補加注射用水至1l;
(6)將步驟(5)所得過濾液用2m氯化鈉溶液調整電導至35ms/cm(20℃),再調節ph至6.5~7.5,稱重;
(7)、將步驟(6)的制得物用經平衡液平衡的q-sepharose-ff離子交換柱進行上樣,上樣完畢后用洗滌液洗滌柱子直至成基線,用洗脫液洗脫,收集洗脫液,稱重;平衡液的配制方法:2.5g三羥甲基氨基甲烷,1.0g氯化鈣,17.5g氯化鈉,補加注射用水至1l,調節ph為6.5~7.5;洗滌液的配制方法:2.5g三羥甲基氨基甲烷,1.0g氯化鈣,19.5g氯化鈉,補加注射用水至1l,調節ph為6.5~7.5;洗脫液的配制方法:2.5g三羥甲基氨基甲烷,1.0g氯化鈣,58.5g氯化鈉,補加注射用水至1l,調節ph為6.5~7.5;
(8)將步驟(7)收集的洗脫液用30kd超濾膜超濾濃縮至1/4后,加入透析液①進行等體積超濾透析液3倍,再加入透析液②進行等體積超濾透析液3倍,用0.45um的濾芯過濾得人凝血因子ⅷ原液,送原液樣品檢測效價及ph值;透析液①配制方法:5.85g氯化鈉,0.9g氯化鈣,2.94g枸櫞酸鈉,12g甘氨酸,補加注射用水至1l,調節ph為6.5~7.5;透析液②配制方法:2.94g枸櫞酸鈉,12g甘氨酸,補加注射用水至1l,調節ph為6.5~7.5;
(9)依據人凝血因子ⅷ原液檢測結果,將步驟(8)得到原液加入透析液②進行稀配至24iu/ml,調整ph至6.5~7.5,即為稀配液;
(10)將步驟(9)得到的稀配液經0.22μm除菌濾芯過濾,過濾后進行分裝,分裝規格為10ml/瓶,既得人凝血因子ⅷ半成品;
(11)將步驟(10)得到的人凝血因子ⅷ半成品裝入冷凍干燥機進行冷凍干燥,既得人凝血因子ⅷ凍干品;
凍干工藝:
①制品常溫進柜;
②隔板20分鐘從常溫降至-5℃,在-5℃保持60分鐘;
③隔板120分鐘從-2℃降到-30℃,在-30℃保持60分鐘;
④隔板120分鐘從-2℃降到-10℃,在-10℃保持60分鐘;
⑤隔板120分鐘從-2℃降到-30℃,在-30℃保持60分鐘;
⑥開真空泵到真空達到0.3mbar穩定;
⑦60分鐘隔板升溫到-20℃,保持480分鐘;
⑧90分鐘隔板升溫到0℃,保持240分鐘;
⑨180分鐘隔板升溫到15℃,保持240分鐘;
⑩240分鐘隔板升溫到30℃,保持120分鐘;
(12)將步驟(11)得到的人凝血因子ⅷ凍干品出柜,扎蓋,后將制品裝入水浴滅菌柜進行99~100℃、30分鐘、壓力0.4mpa干熱滅活;
(13)將步驟(12)得到的人凝血因子制品進行真空檢測,真空合格制品送檢,檢驗合格后包裝;
所述百分數除有限定之外,其余為質量百分數。
本發明相比于傳統的人凝血因子ⅷ制備方法,創新點在于:
1、在人凝血因子ⅷ制備過程中采用二步壓濾法(k700壓濾法和ek壓濾法)替代現有的高速離心法,如專利zl201010534849.9、zl201410524351.2、cn201610077346.0均采用二步離心法,專利zl201410496187.9采用一步離心法。由于人凝血因子ⅷ制備過程中采用高速離心法容易引起激活,水解,導致收得率下降,部分產品的外觀不合格等。而采用壓濾法進液速度不需隨時調節,出液溫度幾乎不變,條件溫和,不易導致蛋白變性,可有效提高產品的收得率約10%。專利cn201510879630.5采用一步50p壓濾法結合deaesephadexa-50凝膠去除維生素k依賴的凝血因子,其中采用一步50p壓濾法分離效果有限,deaesephadexa-50凝膠在使用過程中吸附人凝血因子ⅷ導致得率有所下降且工藝復雜,而本方法采用二步壓濾法可提高分離效果,結合氫氧化鋁凝膠吸附法去除維生素k依賴的凝血因子,氫氧化鋁凝膠不吸附人凝血因子ⅷ,產品收得率高。
2、采用cunodelp深層濾芯過濾,提高對內毒素和病毒的脫除能力,能夠吸附帶負電的內毒素、病毒及脂質蛋白,提高產品的純度,為患者安全用藥提供更為可靠的保證。現有制備人凝血因子ⅷ的過程中多采用筒式濾芯過濾,可去除顆粒物,但無對內毒素、病毒、脂蛋白的脫除能力,如專利zl201010534849.9、zl201410524351.2、cn201510879630.5、cn201610077346.0等采用筒式濾芯。
3、采用兩步梯度透析法,不僅可以減少超濾導致的蛋白活性降低,也可有效降低制品中的聚山梨酯80殘留量、磷酸三丁酯殘留量、鋁殘留量。國內大多專利采用一步透析法,超濾過程中可能導致的蛋白活性降低,對聚山梨酯80殘留量、磷酸三丁酯殘留量、鋁殘留量的去除效果低于兩步梯度透析法,如專利zl201010534849.9、zl201410524351.2、cn201510879630.5、cn201610077346.0等均采用一步透析法。
4、將步驟(2)的制得物蛋白上清液用0.5mol/lhcl調節ph至6.46~6.66,進行酸沉淀可去除大量的人纖維蛋白原,提高產品的純度,防止制品的激活。ph過低可去除更多人纖維蛋白原,但人凝血因子ⅷ的穩定性降低;ph過高,去除人纖維蛋白原的量有限,導致產品純度較低,如zl201010534849.9采用調節ph至6.25~6.45。
5、采用自主研究的人凝血因子ⅷ凍干工藝,該凍干工藝增加了復溶復凍工藝,凍干時可保證產品凍結完全,降低最終制品水分,保護制品的活性,提升產品的質量。國內大多人凝血因子ⅷ凍干工藝專利中采用直接凍結過程,有時導致部分產品不能凍結完全,最終制品水分偏高,如zl201010534849.9凍干過程中采用直接凍結過程,產品的合格率約85%,而本凍干工藝增加了復溶復凍工藝,產品的合格率約93%。
本發明制備方法的創新不是簡單替換,是基于到整個工藝的重新設計,創造性地采用了新的技術路線組合,主要表現在積極效果方面:
1、在人凝血因子ⅷ制備過程中采用二步壓濾法替代傳統的高速離心法,可有效提高產品的收得率約10%,提升產品的質量。
2、該專利技術的實施,提升產品質量,人凝血因子ⅷ比活性可提升至20iu/mg以上,高于現行版藥典要求(10iu/mg);復溶時間為10分鐘內溶解完全,高于現行版藥典要求(30分鐘)。
3、采用兩步梯度透析法,不僅可以減少超濾導致的蛋白活性降低,而且可有效去除制品中的聚山梨酯80殘留量、磷酸三丁酯殘留量、鋁殘留量,均高于現行版藥典要求。
4、生產過程采用多種病毒去除/滅活技術,如s/d法滅活脂包膜病毒、干熱法滅活非脂包膜病毒、cunodelp深層濾芯過濾吸附病毒顆粒、離子交換層析吸附病毒顆粒等,可減少傳播病毒的風險,提高臨床用藥的安全性。
5、在血漿原料日趨緊缺的今天,通過從冷沉淀提取凝血因子ⅷ,對冷沉淀的綜合利用,提高市場競爭力具有重大意義,另一方面也能間接節約稀缺血漿資源。
附圖說明
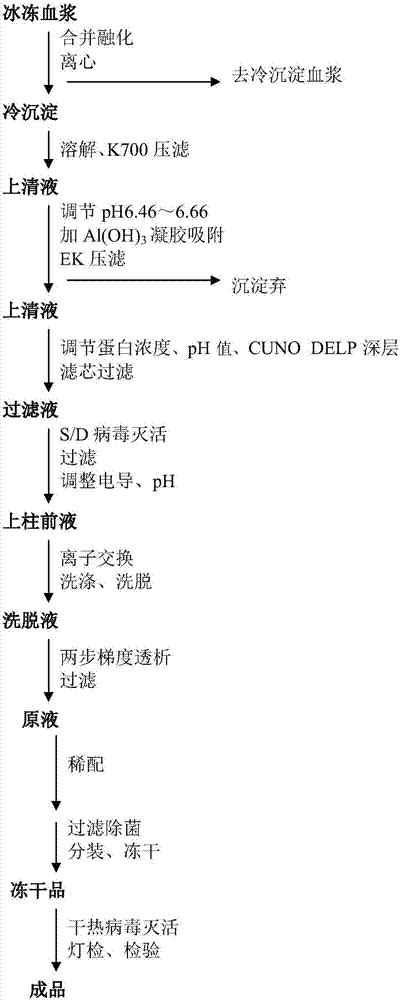
圖1為本發明工藝流程圖。
具體實施方式
本發明通過下面的實施例可以對本發明作進一步的描述,然而,本發明的范圍并不限于下述實施例。
實施例1:以5000升血漿為例,具體制備工藝如下:
(1)、檢疫期檢疫合格的人血漿領取后,75%乙醇擦拭血漿袋表面,用注射用水沖洗,合并到融漿罐中,用30~35℃以下循環水融化,血漿溫度控制不高于4℃;待融化后,離心,出液溫度控制在0~4℃,收集得冷沉淀34.2kg;
(2)、將步驟(1)的制得的冷沉淀加入205l溶解液中,攪拌至冷沉淀完全溶解,循環水的溫度控制在20~26℃;開始用k700濾板進行壓濾,控制壓力不大于0.2mpa,出液溫度為20~26℃,收集壓濾液,稱重236.2kg;
(3)、將步驟(2)的制得物上清液用0.5mol/lhcl調節ph至6.51;加2%氫氧化鋁凝膠80kg,攪拌;開始用ek濾板進行壓濾,控制壓力不大于0.2mpa,出液溫度為20~26℃,收集壓濾液,稱重260.4kg,蛋白濃度為1.6%;
(4)、將步驟(3)的制得物壓濾液用0.5m氫氧化鈉溶液調節上清液ph至6.96;加入蛋白濃度緩沖液17.4kg調節蛋白濃度為15.0g/l;用cunodelp深層濾芯過濾,收集過濾液,稱重278.6kg;
(5)、按步驟(4)的制得物加入s/d溶液27.8kg,攪拌均勻,溫度控制在24~26℃,連續保溫6小時;0.45μm濾芯過濾,收集濾液274.6kg;
(6)將步驟(5)所得過濾液用2m氯化鈉溶液調整電導至35ms/cm(20℃),再調節ph至7.1,稱重308.2kg;
(7)、將步驟(6)的制得物超濾液用經平衡液平衡的q-sepharose-ff離子交換柱進行上樣,上樣完畢后用平衡液洗滌柱子直至成基線,用洗脫液洗脫,收集洗脫液,稱量81kg;
(8)將步驟(7)收集的洗脫液用30kd超濾膜超濾濃縮至20kg,加入透析液①進行等體積超濾透析液3倍,再加入透析液②進行等體積超濾透析液3倍,用0.45um的濾芯過濾得人凝血因子ⅷ原液,稱重17.3kg,檢測效價36.2iu/ml及ph值為6.9;
(9)依據人凝血因子ⅷ原液檢測結果,將步驟(8)得到原液加入透析液②8.8kg進行稀配至24iu/ml,調整ph至7.0,即為稀配液26.1kg;
(10)將步驟(9)得到的稀配液經0.2μm除菌濾芯過濾,過濾后進行分裝,分裝規格為10ml/瓶,既得人凝血因子ⅷ半成品;
(11)將步驟(10)得到的人凝血因子ⅷ半成品裝入冷凍干燥機進行冷凍干燥,既得人凝血因子ⅷ凍干品;
凍干工藝:
①制品常溫進柜;
②隔板20分鐘從常溫降至-5℃,在-5℃保持60分鐘;
③隔板120分鐘從-2℃降到-30℃,在-30℃保持60分鐘;
④隔板120分鐘從-2℃降到-10℃,在-10℃保持60分鐘;
⑤隔板120分鐘從-2℃降到-30℃,在-30℃保持60分鐘;
⑥開真空泵到真空達到0.3mbar穩定;
⑦60分鐘隔板升溫到-20℃,保持480分鐘;
⑧90分鐘隔板升溫到0℃,保持240分鐘;
⑨180分鐘隔板升溫到15℃,保持240分鐘;
⑩240分鐘隔板升溫到30℃,保持120分鐘;
(12)將步驟(11)得到的人凝血因子ⅷ凍干品出柜,扎蓋,后將制品裝入水浴滅菌柜進行99~100℃、30分鐘、壓力0.4mpa干熱滅活;
(13)將步驟(12)得到的人凝血因子ⅷ制品進行真空檢測,真空合格制品送檢,檢驗合格后包裝;
所述百分數除有限定之外,其余為質量百分數。
本發明方法產品的收得率、合格率與傳統的人凝血因子ⅷ制備方法比較如下表1。
表1
本發明方法制備的產品與《中國藥典》(2015年版,三部)中描述的人凝血因子ⅷ在關鍵質量指標的對比如下表2。
表2
- 還沒有人留言評論。精彩留言會獲得點贊!