螺雙芴衍生物及其在有機電致發光領域中的應用的制作方法
本發明屬于有機光電材料技術領域,涉及間位取代螺雙芴化合物和本發明化合物在電子器件特別是在有機電致發光器件、有機場效應晶體管、有機太陽能電池中的用途,尤其是在有機電致發光器件中用作發光主體材料、激子阻擋材料或電子傳輸材料,另外還涉及包含所述化合物的電子器件。
背景技術:
滿足各種信息顯示需求的發光材料在信息時代的今天發展尤其迅速。發光材料主要分為無機和有機
兩類,與無機材料相比,有機材料具有相對更高的發光效率和更寬的發光顏色選擇范圍以及具有大面積成膜的優勢,引起研究者極大的興趣。1987年柯達公司c.w.tang等人首次報道以真空蒸鍍的方法制備出alq3為發光材料的雙層發光器件,有力地推動了有機電致發光材料的發展。經過30多年的發展,有機電致發光在平板顯示、照明方面的應用已經進入產業化初級階段。從發光材料來分類,有機發光二極管(organiclight-emittingdiode,oled)可以分為熒光、磷光以及熱激發延遲熒光發光二極管。
有機電致發光器件一般包括由陽極、金屬陰極和它們之間夾著的有機層組成。有機層主要有空穴注入層、空穴傳輸層、電子阻擋層、發光層、空穴阻擋層、電子傳輸層、電子注入層。另外,發光層大多采用主客體結構,即將發光材料以一定濃度摻雜在主體材料中,以避免濃度淬滅和三線態-三線態湮滅,提高發光效率。因此一般要求主體材料具有較高的三線態能級,并且同時具有較高的穩定性。
現有技術中主體材料多采用咔唑基團,可使得材料具有高額空穴傳輸能力,但咔唑基團c-n鍵容易分解,影響器件的耐久性。為了改善器件的穩定性,有報道設計具有螺環連接鍵的材料可具有加強的形態穩定性。螺雙芴分子具有非平面的空間結構,兩個芴單體以sp3雜化的c原子為中心橋聯在一起,將其引入到具有電致發光特性的分子中,對于提高分子的熱穩定性和光譜穩定性等方面具有很大的應用價值。目前,對于螺雙芴衍生物的研究主要集中在其2位和4位(如cn102077384a和cn104541576a)。然而,2位和4位的衍生物一般具有較大的共軛度,分子的三重態能級較低,大大限制了其在藍色有機電致發光器件中的應用。
技術實現要素:
發明要解決的問題
為了解決以上現有技術的缺點和不足之處,有效提高三線態能級,改善有機電致發光器件的壽命、效率和工作電壓等性能,本發明的目的是提供一種間位取代螺雙芴化合物以及制備方法。
本發明的另一目的在于提供上述螺雙芴類化合物的一種應用,特別是在有機電致發光器件中的應用。
本發明的再一目的在于提供一種包含所述化合物的電子器件。
用于解決問題的方案
令人驚訝地發現,下面描述的化合物能有效提高三線態能級,能夠有效改進有機電致發光器件的壽命、效率和工作電壓等性能。
本發明涉及式(ⅰ)或式(ⅱ)的化合物
其中,
螺雙芴母核通過l1、l2分別連接1個或2個r1或r2基團,-l1-r1和/或-l2-r2以碳原子連接到螺雙芴母核3位和/或6位;
l1、l2分別獨立地選自單鍵、羰基、具有6至18個環原子的芳族或雜芳族環系;
r1、r2分別獨立地為具有6至30個環原子的芳族或雜芳族環系,所述芳族或雜芳族環系可任選地被一個或多個基團r1取代;
r1:在每次出現時相同或不同地選自:氫、氘、鹵素、氰基;具有1至40個c原子的直鏈烷基、烷氧基或硫代烷基基團或者具有3至40個c原子的支鏈或環狀的烷基、烷氧基或硫代烷基基團,所述直鏈烷基或支鏈烷基可任選地被鹵素取代;具有6至30個環原子的芳族環系或具有5至30個環原子的雜芳族環系;
當化合物為式(ⅰ)時,若l1為單鍵或羰基時,螺雙芴母核通過l1連接1個r1;若l1為具有6至18個環原子的芳族或雜芳族環系時,螺雙芴母核通過l1連接2個r1,每個r1可相同或不同;
當化合物為式(ⅱ)時,若l1、l2分別獨立地為單鍵或羰基時,螺雙芴母核通過l1連接1個r1和r2;若l1、l2分別獨立地為具有6至18個環原子的芳族或雜芳族環系時,螺雙芴母核通過l1、l2分別連接2個r1和r2,每個r1、每個r2可相同或不同;
所述化合物不包括式a所示結構的化合物:
優選地,l1、l2分別獨立地為單鍵、羰基、苯基、三嗪基或聯苯基;雜芳族環系中雜原子選自n、o和/或s。
優選地,r1、r2分別獨立地選自如下結構(ar-1至ar-29):
其中虛線表示與l1或l2鍵合的鍵,r1具有上述含義。
優選地,l1、l2分別獨立地為單鍵、羰基、苯基或三嗪基;
r1、r2分別獨立地選自以下芳族或雜芳族環系:苯基、聯苯基、三聯苯基、四聯苯基、五聯苯基、苯并蒽、苯并菲、芴基、螺雙芴基、三嗪基、二苯并呋喃基、二苯并噻吩基、咔唑基、n-苯基咔唑基、茚并咔唑基、苯并咪唑基、二苯基-苯并咪唑基、二苯基-噁二唑基,所述芳族或雜芳族環系可被一個或多個r1取代;
r1在每次出現時相同或不同地選自:氫、具有1至5個c原子的直鏈烷基、苯基、苯并菲、聯苯基、三聯苯基、四聯苯基、五聯苯基、芴基、喹啉基、螺雙芴基、三嗪基、二苯并呋喃基、二苯并噻吩基、咔唑基、茚并咔唑基、苯并咪唑基。
進一步優選地,l1、l2分別獨立地為單鍵、羰基或三嗪基;
r1、r2分別獨立地選自以下芳族或雜芳族環系:苯基、苯并菲、螺雙芴基、三嗪基;所述芳族或雜芳族環系可被一個或多個r1取代,每個r1、每個r2不同時為苯基;r1在每次出現時相同或不同地選自:氫、具有1至5個c原子的直鏈烷基、苯基、苯并菲、聯苯基、三聯苯基、四聯苯基、五聯苯基、芴基、螺雙芴基、三嗪基、二苯并呋喃基、二苯并噻吩基、咔唑基、苯并咪唑基。
進一步優選地,本發明化合物選自:
本發明還提供一種用于制備以上任一項化合物的方法,其特征在于通過3位和/或6位官能化的螺雙芴和含有官能化基團-l1-r1和/或-l2-r2的化合物進行金屬催化偶聯反應引入基團-l1-r1和/或-l2-r2。
更進一步地,本發明提供上述化合物在電子器件特別是在有機電致發光器件、有機場效應晶體管、有機太陽能電池中的用途,尤其是制備有機電致發光器件中的發光主體材料、激子阻擋材料或電子傳輸材料的用途。
本發明還提供一種電子器件,其包括至少一種上述化合物。優選地,該電子器件是有機電致發光器件,所述有機電致發光器件包含有機發光層、激子阻擋層、電子傳輸層,其中任意一層或多層含有上述任一種化合物。
發明的效果
本發明的3位和/或6位取代的螺雙芴衍生物的三線態能級高達2.80ev,較2位(2.54ev)和4位(2.65ev)取代的螺雙芴衍生物的三線態高。因此其可作為主體材料、激子阻擋材料或者電子傳輸材料應用在電致發光器件中,其能有效抑制能量的耗損,有望實現高效率、長壽命的器件性能。本發明以環金屬銥配合物ir(ppy)3為客體制備的發光器件,在10000坎特拉每平方米下,最大外量子效率可達16.8%,同時在10000坎特拉每平方米下,器件保持了極高的穩定性,在衰減到起始亮度的90%時,壽命長達1000個小時。除此之外,以熱激發延遲熒光材料4czipn為客體制備的發光器件,在10000坎特拉每平方米下,最大外量子效率可達15.4%,同時在10000坎特拉每平方米下,在衰減到起始亮度的90%時,壽命長達800個小時。另外,以藍色熒光材料bd1為客體制備的發光器件,在5000坎特拉每平方米下,最大外量子效率可達5.2%,同時在5000坎特拉每平方米下,在衰減到起始亮度的90%時,壽命長達600個小時。而已報道的2位取代的螺雙芴衍生物為主體材料并以藍色熒光材料bd1為客體制備的發光器件,其最大外量子效率僅為2.0%,同時在5000坎特拉每平方米下,在衰減到起始亮度的90%時,壽命為100個小時。由此可見本發明具有有效的技術效果。
附圖說明
圖1為化合物1-75的紫外吸收光譜(uv-vis)、室溫熒光光譜(pl)以及低溫磷光光譜(phos)。
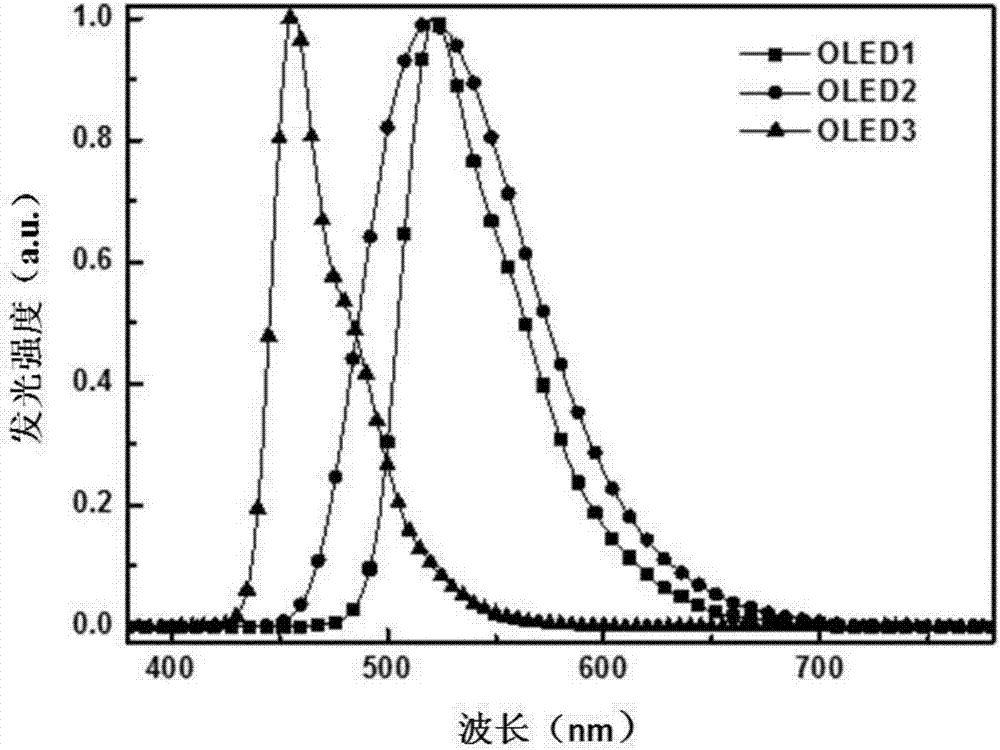
圖2為實施例oled1、oled2和oled3的有機電致發光光譜。
具體實施方式
下面將結合實施例對本發明的技術方案進行詳細的描述。
出于本發明的目的,本發明意義上的芳族環系在該環系中含有6至30個c原子,優選6至18個c原子。本發明意義上的雜芳族環系在該環系中含有5至30個,優選6至18個c原子和雜原子,該雜原子優選地選自n、o和/或s。在本發明中,化合物的雜原子數目可以是1-5個(取整數)。本發明意義上的芳族或雜芳族環系旨在被認為是指如下的體系,該體系并不必須僅含有芳基或雜芳基基團,而是其中多個芳基或雜芳基基團還可以被非芳族單元(優選小于非氫原子的10%)間斷,該非芳族單元例如是c、n或o原子或者羰基基團或者-c(cf3)2-。例如,和兩個或更多個芳基基團例如被直鏈或環狀的烷基基團或者被甲硅烷基基團間斷的體系一樣,9,9’-螺二芴、9,9-二芳基芴、三芳基胺、二芳基醚等的體系也旨在被認為是在本發明意義上的芳族環系。此外,其中兩個或更多個芳基或雜芳基基團相互直接鍵合的體系,例如聯苯、三聯苯或四聯苯,同樣旨在被認為是芳族或雜芳族環系。
芳族或雜芳族環系例如由衍生自以下基團的一種或多種所構成的體系:苯、萘、蒽、苯并蒽、菲、苯并菲、芘、苝、熒蒽、苯并熒蒽、并四苯、并五苯、苯并芘、聯苯、偶苯、三聯苯、四聯苯、五聯苯、三聚苯、芴、螺雙芴、二氫菲、二氫芘、四氫芘、順式或反式茚并芴、順式或反式單苯并茚并芴、順式或反式二苯并茚并芴、三聚茚、異三聚茚、螺三聚茚、螺異三聚茚、呋喃、苯并呋喃、異苯并呋喃、二苯并呋喃、噻吩、苯并噻吩、異苯并噻吩、二苯并噻吩、吡咯、吲哚、異吲哚、咔唑、吲哚并咔唑、茚并咔唑、吡啶、喹啉、異喹啉、吖啶、菲啶、苯并-5,6-喹啉、苯并-6,7-喹啉、苯并-7,8-喹啉、吩噻嗪、吩噁嗪、吡唑、吲唑、咪唑、苯并咪唑、萘并咪唑、菲并咪唑、吡啶并咪唑、吡嗪并咪唑、喹喔啉并咪唑、噁唑、苯并噁唑、萘并噁唑、蒽并噁唑、菲并噁唑、異噁唑、1,2-噻唑、1,3-噻唑、苯并噻唑、噠嗪、苯并噠嗪、嘧啶、苯并嘧啶、喹喔啉、1,5-二氮雜蒽、2,7-二氮雜芘、2,3-二氮雜芘、1,6-二氮雜芘、1,8-二氮雜芘、4,5-二氮雜芘、4,5,9,10-四氮雜苝、吡嗪、吩嗪、吩噁嗪、吩噻嗪、熒紅環、萘啶、氮雜咔唑、苯并咔啉、菲咯啉、1,2,3-三唑、1,2,4-三唑、苯并三唑、1,2,3-噁二唑、1,2,4-噁二唑、1,2,5-噁二唑、1,3,4-噁二唑、1,2,3-噻二唑、1,2,4-噻二唑、1,2,5-噻二唑、1,3,4-噻二唑、1,3,5-三嗪、1,2,4-三嗪、1,2,3-三嗪、四唑、1,2,4,5-四嗪、1,2,3,4-四嗪、1,2,3,5-四嗪、嘌呤、蝶啶、吲嗪、苯并噻二唑等,上述基團可被取代或不被取代。
本發明意義上環狀的烷基、烷氧基或硫代烷氧基基團被認為是指單環、雙環或多環的基團。
<化合物>
在本發明的一種實施方式中,式(ⅰ)或式(ⅱ)的化合物為:
其中,螺雙芴母核通過l1、l2分別連接1個或2個r1或r2基團,-l1-r1和/或-l2-r2以碳原子連接到螺雙芴母核3位和/或6位。取代基r1、r2通過l1、l2連接在螺雙芴母核3位或者6位,這種連接方式可以打斷整個分子的共軛,從而提高分子的三線態能級。
本發明的實施方案可為:
(1)對于l1、l2:
l1、l2分別獨立地選自單鍵、羰基、具有6至18個環原子的芳族或雜芳族環系,所述芳族或雜芳族環系可任選地被一個或多個基團取代;優選地,l1、l2分別獨立地選自單鍵、羰基、具有6至12個環原子的芳族或雜芳族環系;更優選地,l1、l2分別獨立地為單鍵、羰基、苯基、三嗪基或聯苯基。
(2)對于r1、r2:
r1、r2分別獨立地為具有6至30個環原子的芳族或雜芳族環系,所述芳族或雜芳族環系可任選地被一個或多個基團r1取代;
當化合物為式(ⅰ)時,若l1為單鍵或羰基時,螺雙芴母核通過l1連接1個r1;若l1為具有6至18個環原子的芳族或雜芳族環系時,螺雙芴母核通過l1連接2個r1,每個r1可相同或不同;當化合物為式(ⅱ)時,若l1、l2分別獨立地為單鍵或羰基時,螺雙芴母核通過l1、l2連接1個r1和r2;若l1、l2分別獨立地為具有6至18個環原子的芳族或雜芳族環系時,螺雙芴母核通過l1、l2分別連接2個r1和r2,每個r1、每個r2可相同或不同;
優選地,r1、r2分別獨立地選自以下芳族或雜芳族環系:苯基、聯苯基、三聯苯基、四聯苯基、五聯苯基、苯并蒽、苯并菲、芴基、螺雙芴基、三嗪基、二苯并呋喃基、二苯并噻吩基、咔唑基、n-苯基咔唑基、茚并咔唑基、苯并咪唑基、二苯基-苯并咪唑基、二苯基-噁二唑基,所述芳族或雜芳族環系可被一個或多個r1取代;
同樣,優選地,r1、r2分別獨立地選自如上文所述結構ar-1至ar-29;
更優選地,r1、r2分別獨立地選自以下芳族或雜芳族環系:苯基、苯并菲、螺雙芴基、三嗪基;所述芳族或雜芳族環系可被一個或多個r1取代,每個r1、每個r2不同時為苯基。
(3)對于取代基r1:
r1在每次出現時相同或不同地選自:氫、氘、鹵素、氰基;具有1至40個c原子的直鏈烷基、烷氧基或硫代烷基基團或者具有3至40個c原子的支鏈或環狀的烷基、烷氧基或硫代烷基基團,所述直鏈烷基或支鏈烷基可任選地被鹵素取代;具有6至30個環原子的芳族環系或具有5至30個環原子的雜芳族環系;
優選地,r1在每次出現時相同或不同地選自:氫、氘、氟、氰基;具有1至10個c原子的直鏈烷基、烷氧基或者具有3至10個c原子的支鏈或環狀的烷基或烷氧基,所述直鏈烷基或支鏈烷基可任選地被氟取代;具有6至30個環原子的芳族或雜芳族環系;
更優選地,r1在每次出現時相同或不同地選自:氫、氟;具有1至5個c原子的直鏈烷基如甲基、乙基、丙基、丁基,具有3至6個c原子的支鏈或環狀的烷基,具有6至30個環原子的芳族或雜芳族環系如苯基、苯并菲、聯苯基、三聯苯基、四聯苯基、五聯苯基、芴基、喹啉基、螺雙芴基、三嗪基、二苯并呋喃基、二苯并噻吩基、咔唑基、茚并咔唑基、苯并咪唑基。
在本發明的一種特別優選的實施方式中:
l1、l2分別獨立地為單鍵、羰基或三嗪基;
r1、r2分別獨立地選自以下芳族或雜芳族環系:苯基、苯并菲、螺雙芴基、三嗪基;所述芳族或雜芳族環系可被一個或多個r1取代,每個r1、每個r2不同時為苯基;
r1在每次出現時相同或不同地選自:氫、具有1至5個c原子的直鏈烷基、苯基、苯并菲、聯苯基、三聯苯基、四聯苯基、五聯苯基、芴基、螺雙芴基、三嗪基、二苯并呋喃基、二苯并噻吩基、咔唑基、苯并咪唑基。
本發明合適化合物的實例如化合物1-1到1-135、2-1到2-6中的一種或多種。
<化合物的制備方法>
可通過本領域普通技術人員已知的合成步驟,例如溴化、鈴木(suzuki)偶聯、布赫瓦爾德-哈特維希(hartwig-buchwald)偶聯等,來制備根據本發明的化合物。
本發明的化合物合成通常從3位和/或6位官能化的螺雙芴衍生物開始,然后通過金屬催化偶聯反應如鈴木(suzuki)偶聯而引入基團-l1-r1和/或-l2-r2。
在本發明的一種優選實施方式中,所述螺雙芴衍生物是利用硼酸衍生物官能化的化合物,且基團-l1-r1和/或-l2-r2源自鹵素官能化的化合物。在本發明的另一種優選的實施方式中,所述螺雙芴衍生物是鹵素官能化的化合物,且基團-l1-r1和/或-l2-r2源自硼酸衍生物官能化的化合物。
在本發明的第三種優選實施方式中,所述螺雙芴衍生物是鹵素官能化的化合物,在格氏試劑的作用下與氰基化的化合物反應而引入基團-l1-r1和/或-l2-r2。其中,鹵素官能化優選溴化、氯化、碘化,特別是溴化。
具體而言,如上所述的第一種優選實施方式,需先制備硼酸官能化的螺雙芴衍生物(3-硼酸-9,9’螺雙芴,即中間體1),優選的制備步驟示例如下:
通過控制反應條件,m1的收率可達到80-90%,m2的收率可達到60-77%,中間體1的收率可到80-90%。得到中間體1后,在體系中加入可引入基團-l1-r1和/或-l2-r2的鹵素官能化化合物如2,4-二氯-6-苯基-1,3,5-三嗪或三聚氰胺,以及一定量的鈀類催化劑如四(三苯基磷鈀)、無水碳酸鉀、四氫呋喃和水,在氮氣保護下50-80℃下反應30-35小時,反應完畢。蒸去溶劑,用二氯甲烷和水溶解殘留物,水洗,分出有機層,水層用二氯甲烷萃取,合并有機層,用水洗兩次至中性,蒸去溶劑后,柱層析分離,干燥得到產物。中間體1與四(三苯基磷鈀)的摩爾比在15-20:1,優選18:1;通過調節反應條件,收率在65-85%。
如上所述的第二種優選實施方式,優選利用3-溴-9,9’螺雙芴和硼酸衍生物官能化的化合物如2-硼酸苯并菲反應,在體系中加入四(三苯基膦)鈀、無水碳酸鉀、四氫呋喃和水,在氬氣保護下50-80℃下反應30-35小時,反應完畢。后處理同第一種優選實施方式。最終產品收率可達到94%。
如上所述的第三種優選實施方式,優選利用3-溴-9,9’螺雙芴在四氫呋喃中溶解,低溫下滴加正丁基鋰,在-78℃攪拌1小時,然后,將溶解在80ml中的氰基官能化的化合物如2-氰基苯并菲慢慢滴加到反應瓶中,1小時后自動升溫,反應過夜。在反應瓶中加入少量水淬滅反應,減壓蒸去溶劑,加入稀鹽酸,室溫攪拌,加入二氯甲烷萃取,分層,經過洗滌干燥后可得產品,收率可達78%。
<化合物的應用>
本發明還涉及本發明化合物在電子器件中、特別是在有機電致發光器件、有機場效應晶體管、有機太陽能電池中的用途。
本發明另外還涉及包含至少一種本發明化合物的電子器件。所述電子器件優選地選自有機電致發光器件(有機發光二極管、oled)、有機場效應晶體管(o-fet)、有機太陽能電池(o-sc)、有機薄膜晶體管(o-tft)、有機發光晶體管(o-let)、有機集成電路(o-ic)、有機染料敏化太陽能電池(odssc)、有機光學檢測器、有機光感受器、有機場猝熄器件(o-fqd)、發光電化學電池(lec)、有機激光二極管(o-laser)和有機等離子體發射器件等,優選有機電致發光器件(oled)。
一個oled總體上包括:基板,例如(但不限于)玻璃、塑料、金屬;陽極,例如氧化銦錫(ito)陽極;空穴注入層(hil);空穴傳輸層(htl);電子阻擋層(ebl);有機發光層(eml);激光阻擋層(ebl);電子傳輸層(etl);電子注入層(eil),例如lif、cs2co3;陰極,例如al。然而,應該指出,中間每層可以有一層或多層并且每層并非必須存在。
本發明的化合物可以用于該器件的任意一層或多層,但優選用于發光層(eml),更優選為發光層的主體材料,因為其具有高的三線態能級,穩定性好。本發明的化合物也可以用于作為激子阻擋材料或者電子傳輸材料用于激子阻擋層(ebl)和電子傳輸層(etl)中,因其載流子傳輸能力好。
本發明的有機發光層摻雜劑并無特別限定,優選為發光金屬配合物和發光有機分子,發光金屬配合物優選為銥和鉑的配合物,發光有機分子優選熒光化合物和熱激發延遲熒光化合物。為了提高器件效能,摻雜劑質量比例在6%-30%,優選6%-20%,進一步優選6%-15%。
在本發明的優選實施方式中,oled包括:基片/陽極/空穴注入材料(hil1)/空穴傳輸材料1(hil1)/空穴傳輸材料2(hil2)/電子阻擋層(ebl)/有機發光層(eml)/激子阻擋層(ebl)/電子傳輸層(etl)/陰極。其中,基片使用玻璃基板,ito作陽極材料。空穴注入材料使用現有技術中常用的2,3,6,7,10,11-六氰基-1,4,5,8,9,12-六氮雜苯并菲(hat-cn),空穴傳輸材料1使用現有技術中常用的n,n'-二苯基-n,n'-(1-萘基)-1,1'-聯苯-4,4'-二胺(npb);空穴傳輸材料2使用現有技術中常用的9,9',9”-三苯基-9h,9'h,9”h-3,3':6',3”-三咔唑(tris-pcz);電子阻擋層使用現有技術中常用的3,3'-二(n-咔唑基)-1,1'-聯苯(mcbp);有機發光層使用本發明所述化合物摻雜現有技術中常用的環金屬銥配合物ir(ppy)3、熱激發延遲熒光材料4czipn或藍色熒光材料bd1;激子阻擋層使用本發明所述化合物。另外,本發明所述化合物摻雜8-羥基喹啉-鋰或者金屬鋰也可用作電子傳輸層,部分器件也使用現有技術中常用的雙(10-羥基苯并[h]喹啉)鈹(be(bq)2)和三(8-羥基喹啉)鋁(alq3)。陰極采用金屬及其混合物結構,如mg:ag、ca:ag等,也可以是電子注入層/金屬層結構,如lif/al、liq/al和li2o/al。本發明優選電子注入材料為liq,陰極材料為al。
以下列舉實施例來說明本發明,本領域技術人員能夠理解,該例子僅是示例性的說明,并非窮盡性的說明。制備例為化合物合成例,所涉及的化學原料和試劑均為市售或按公開文獻合成,實施例為發光器件oled的制備。
制備例
中間體1的合成:
中間體1的結構式和合成路線如下式所示:
式m1化合物的制備方法為:在裝有溫度計、滴液漏斗和機械攪拌的250ml三口瓶中,加入10.0g(36.21mmol)2-氨基-4’-溴-二苯甲酮及80ml水,在攪拌下慢慢滴加5.0g,98%(50mmol)濃硫酸,攪拌30分鐘,冷卻到0℃,滴加1.5g(21mmol)亞硝酸鈉溶于5ml水的溶液,滴加完畢,保持這個溫度30分鐘后,慢慢升溫到60℃,待氣泡完全放出后,冷卻到室溫,過濾,得到淡黃色結晶狀固體。固體經柱層析分離(350目硅膠,淋洗液為石油醚:二氯甲烷=20:1(v/v)),蒸去溶劑,干燥后,得到淡黃色結晶7.50g,收率80%。ms(ei):m/z257.96[m+]。元素分析計算值c13h7bro(%):c60.26,h2.72;實測值:c60.23,h2.82。
式m2化合物的制備方法為:在200mlschlenk瓶中,在氬氣體保護下,加入2-溴聯苯4.6g(19.73mmol)及四氫呋喃80ml,溶解,冷卻到-78℃,在這個溫度下滴加2.4m,8.63ml(20.7mmol)正丁基鋰,在-78℃攪拌1小時,然后將溶解在80ml中的5.1g(19.73mmol)3-溴芴酮慢慢滴加到反應瓶中,1小時后自動升溫,反應過夜。在反應瓶中加入5ml水淬滅反應,并轉移到單口瓶中,在減壓下,用旋轉蒸發儀蒸去溶劑,分別加入80ml二氯甲烷和80ml水,溶解殘留物,并轉移到分液漏斗中,分層,水層用25ml二氯甲烷萃取兩次,有機層再用80ml水洗兩次至中性。有機層用15g無水硫酸鈉干燥3小時后,減壓蒸去溶劑二氯甲烷。將所得中間體3-溴-9-(2-二苯基)-9-芴醇直接投入到100ml單口瓶中,加入45ml乙酸,及4.5ml36%的濃鹽酸,115℃回流反應4小時,冷卻至室溫,過濾,得白色結晶。用10ml石油醚淋洗一次,干燥后得5.2g,收率67%。ms(ei):m/z394.04[m+]。元素分析計算值c25h15br(%):c75.96,h3.82;實測值:c76.08,h3.75。
所述中間體1的制備方法為:在200mlschlenk反應瓶中,在氬氣保護下,投入3-溴-9,9’螺雙芴2.0g(5.05mmol)及80ml四氫呋喃,溶解后冷卻,在-78℃下滴加2.4m正丁基鋰2.2ml(5.28mmol),滴加完畢攪拌1小時,滴加硼酸三異丙酯1.42g(7.57mmol),攪拌1小時后,自動升溫,反應過夜。加入20ml氯化銨水溶液,淬滅反應。將反應物料轉移到單口瓶中,減壓蒸出溶劑后,在瓶中加入80ml二氯甲烷和80ml水,溶解,水洗,分層,水層用15ml二氯甲烷萃取兩次,合并有機相,再用80ml水水洗兩次,至中性。分去水層,有機層加15g無水硫酸鈉,干燥3小時。減壓蒸去溶劑,得白色固體1.46g,收率80%。ms(ei):m/z360.16[m+]。元素分析計算值c25h17bo2(%):c83.36,h4.76;實測值:c83.41,h4.84。
制備例1:化合物1-75的合成
化合物1-75的結構式及合成路線如下式所示:
在200mlschlenk瓶中,加入3-硼酸-9,9’螺雙芴1.50g(4.16mmol)、2,4-二氯-6-苯基-1,3,5-三嗪0.47g(2.08mmol)、四(三苯基膦)鈀0.26g(0.23mmol)、無水碳酸鉀1.77g(12.8mmol),四氫呋喃50ml,水8ml,在氬氣體保護下,70℃攪拌反應30小時,反應完畢。蒸去溶劑,用50ml二氯甲烷和50ml水溶解殘留物,水洗,分出有機層,水層用15ml二氯甲烷萃取兩次,合并有機層,用50ml水洗兩次至中性,蒸去溶劑后,殘留物經柱層析分離(硅膠為350目,淋洗液為石油醚:三氯甲烷=2.5:1(v/v)),蒸去溶劑,干燥后,得到1.27g白色結晶,收率為78%。ms(ei):m/z785.23[m+]。元素分析計算值c59h35n3(%):c90.16,h4.49;實測值:c90.18,h4.41。
附圖1是產品1-75的紫外吸收光譜、紫外吸收光譜(uv-vis)、室溫熒光光譜(pl)以及低溫磷光光譜(phos)。紫外吸收光譜和室溫熒光光譜在二氯甲烷的稀溶液(1×10-5mol/l)中測得;低溫磷光光譜在2-甲基四氫呋喃溶液(1×10-3mol/l)中測得。
制備例2:化合物1-123的合成
化合物1-123的結構式及合成路線如下式所示:
在200mlschlenk瓶中,加入3-硼酸-9,9’螺雙芴1.50g(4.16mmol)、三聚氯氰0.25g(1.38mmol)、四(三苯基膦)鈀0.26g(0.23mmol)、無水碳酸鉀1.77g(12.8mmol)、四氫呋喃50ml、水8ml,在氬氣體保護下,70℃攪拌反應30小時,反應完畢。蒸去溶劑,用50ml二氯甲烷和50ml水溶解殘留物,水洗,分出有機層,水層用15ml二氯甲烷萃取兩次,合并有機層,用50ml水洗兩次至中性,蒸去溶劑后,殘留物經柱層析分離(硅膠為350目,淋洗液為石油醚:三氯甲烷=2.5:1(v/v)),蒸去溶劑,干燥后,得到1.13g白色結晶,收率為68%。ms(ei):m/z1023.41[m+]。元素分析計算值c78h45n3(%):c91.46,h4.43;實測值:c90.51,h4.41。
制備例3:化合物1-112的合成
化合物1-112的結構式及合成路線如下式所示:
在200mlschlenk瓶中,加入3-溴-9,9’螺雙芴3.95g(10.00mmol)、2-硼酸苯并菲2.72g(10.00mmol)、四(三苯基膦)鈀0.26g(0.23mmol)、無水碳酸鉀2.76g(20.0mmol)、四氫呋喃50ml、水8ml,在氬氣體保護下,70℃攪拌反應30小時,反應完畢。蒸去溶劑,用50ml二氯甲烷和50ml水溶解殘留物,水洗,分出有機層,水層用15ml二氯甲烷萃取兩次,合并有機層,用50ml水洗兩次至中性,蒸去溶劑后,殘留物經柱層析分離(硅膠為350目,淋洗液為石油醚:三氯甲烷=2.5:1(v/v)),蒸去溶劑,干燥后,得到5.11g白色結晶,收率為94%。ms(ei):m/z542.21[m+]。元素分析計算值c43h26(%):c95.17,h4.83;實測值:95.19,h4.80。
制備例4:化合物1-113的合成
化合物1-113的結構式及合成路線如下式所示:
在200mlschlenk瓶中,在氬氣體保護下,加入3-溴-9,9’螺雙芴3.95g(10.00mmol)及四氫呋喃80ml,溶解,冷卻到-78℃,在這個溫度下,滴加2.4m,4.58ml(11.0mmol)正丁基鋰,在-78℃攪拌1小時,然后,將溶解在80ml中的2.53g(10.00mmol)2-氰基苯并菲慢慢滴加到反應瓶中,1小時后,自動升溫,反應過夜。在反應瓶中加入5ml水淬滅反應,并轉移到單口瓶中,在減壓下,用旋轉蒸發儀蒸去溶劑,加入10ml1m稀鹽酸,室溫攪拌2小時,加入30ml二氯甲烷萃取,分層,水層用25ml二氯甲烷萃取兩次,有機層再用30ml水洗兩次至中性。有機層用15g無水硫酸鈉干燥3小時后,減壓蒸去溶劑二氯甲烷。蒸去溶劑后,殘留物經柱層析分離(硅膠為350目,淋洗液為石油醚:三氯甲烷=2.5:1(v/v)),蒸去溶劑,干燥后,得到4.5g白色結晶,收率為78%。ms(ei):m/z570.20[m+]。元素分析計算值c44h26o(%):c92.60,h4.59;實測值:c92.64,h4.59。
制備例5:化合物1-1的合成
化合物1-1的結構式及合成路線如下式所示:
在200mlschlenk瓶中,加入3-硼酸-9,9’螺雙芴3.60g(10.00mmol)、1-溴-3,5-二苯基苯3.08g(10.00mmol)、四(三苯基膦)鈀0.26g(0.23mmol)、無水碳酸鉀2.76g(20.0mmol)、四氫呋喃50ml、水8ml,在氬氣體保護下,70℃攪拌反應30小時,反應完畢。蒸去溶劑,用50ml二氯甲烷和50ml水溶解殘留物,水洗,分出有機層,水層用15ml二氯甲烷萃取兩次,合并有機層,用50ml水洗兩次至中性,蒸去溶劑后,殘留物經柱層析分離(硅膠為350目,淋洗液為石油醚:三氯甲烷=2.5:1(v/v)),蒸去溶劑,干燥后,得到4.82g白色結晶,收率為89%。ms(ei):m/z544.22[m+]。元素分析計算值c43h28(%):c94.82,h5.18;實測值:c94.60,h5.23。
制備例6:化合物1-17的合成
化合物1-17的結構式及合成路線如下式所示:
在200mlschlenk瓶中,加入3-硼酸-9,9’螺雙芴3.95g(10.00mmol)、1-溴-3,5-二(二苯并噻吩基)苯5.20g(10.00mmol)、四(三苯基膦)鈀0.26g(0.23mmol)、無水碳酸鉀2.76g(20.0mmol)、四氫呋喃50ml、水8ml,在氬氣體保護下,70℃攪拌反應30小時,反應完畢。蒸去溶劑,用50ml二氯甲烷和50ml水溶解殘留物,水洗,分出有機層,水層用15ml二氯甲烷萃取兩次,合并有機層,用50ml水洗兩次至中性,蒸去溶劑后,殘留物經柱層析分離(硅膠為350目,淋洗液為石油醚:三氯甲烷=2.5:1(v/v)),蒸去溶劑,干燥后,得到6.24g白色結晶,收率為82%。ms(ei):m/z756.19[m+]。元素分析計算值c55h32s2(%):c87.27,h4.26;實測值:c87.25,h4.22。
實施例
器件制備:將涂布ito透明導電層的玻璃板在商用清洗劑中超聲處理,去離子水中沖洗,在丙酮和乙醇中各清洗三次,在潔凈的環境下烘烤至完全除去水分,用紫外光和臭氧清洗,并用低能陽離子束轟擊表面。把ito導電玻璃置入真空腔內,抽真空至2×10-5-2×10-5pa。然后在上述ito導電玻璃上依次蒸鍍空穴注入材料(hil1)、空穴傳輸材料1(hil1)、空穴傳輸材料2(hil2)、電子阻擋層(ebl)、有機發光層(eml)、激子阻擋層(ebl)、電子傳輸層(etl)以及陰極;其中,有機材料的蒸鍍速率為0.2nm/s,金屬電極的蒸鍍速率為0.5nm/s以上,發光層以雙源共蒸的方法,主體材料蒸鍍速率為0.2nm/s,摻雜材料的蒸鍍速率為0.03nm/s。
器件性能測試:器件的電流-亮度-電壓特性是由帶有校正過的硅光電二極管的keithley源測量系(keithley2400sourcemeter、keithley2000currentmeter)完成的,電致發光光譜是由photoresearch公司pr655光譜儀測量的,器件的外部量子效率通過文獻adv.mater.,2003,15,1043–1048的方法計算可得。以ir(ppy)3和4czipn作為摻雜劑的器件壽命是指以1000坎特拉每平方米為起始亮度,衰減到9000坎特拉每平方米(90%)的時間。而以bd1作為摻雜劑的器件壽命是指以5000坎特拉每平方米為起始亮度,衰減到4500坎特拉每平方米(90%)的時間。所有器件均在氮氣環境中封裝。
實施例涉及的化合物結構如下:
實施例(oled1-11)的結構和各層的膜厚厚度如下:
oled1:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-75:ir(ppy)36wt%(20nm)/1-75(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled2:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-75:4czipn15wt%(20nm)/1-75(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled3:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-75:bd110wt%(20nm)/1-75(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled4:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-75:ir(ppy)36wt%(20nm)/1-75(10nm)/1-75:20%liq(40nm)/liq(2nm)/al(100nm)
oled5:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-112:ir(ppy)36wt%(20nm)/1-75(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled6:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-112:4czipn15wt%(20nm)/1-75(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled7:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-113:ir(ppy)36wt%(20nm)/1-113(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled8:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-113:4czipn15wt%(20nm)/1-113(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled9:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-113:bd110wt%(20nm)/1-113(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled10:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-1:ir(ppy)36wt%(20nm)/host2(10nm)/balq(40nm)/liq(2nm)/al(100nm)
oled11:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/1-17:ir(ppy)36wt%(20nm)/1-75(10nm)/balq(40nm)/liq(2nm)/al(100nm)
比較例
比較例1和2的制備方法與實施例相同,僅是改變主體材料和激子阻擋材料化合物,其比較例1的器件結構如下:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/host1:bd110wt%(20nm)/host1(10nm)/balq(40nm)/liq(2nm)/al(100nm)
比較例2的器件結構如下:
ito/hat-cn(10nm)/npb(40nm)/mcbp(15nm)/host2:ir(ppy)36wt%(20nm)/host2(10nm)/balq(40nm)/liq(2nm)/al(100nm)
器件的性能數據見下表:
表1:器件性能數據
由表1可見,本發明的化合物獲得非常好的性能數據。比較例1和oled9均采用bd1作為摻雜劑,區別僅在于oled9的主體材料和激子阻擋材料為本發明的化合物1-113,通過器件性能數據的對比可見,oled9具有更低的工作電壓,外量子效率相對提高了將近3倍,器件壽命(90%)有顯著提高,從102小時變成625小時。另外,比較例2和oled1均采用ir(ppy)3作為摻雜劑,區別僅在于oled1的主體材料和激子阻擋材料為本發明的化合物1-75,通過器件性能數據的對比可見,oled1具有更長的器件壽命。附圖2是oled1-3的有機電致發光光譜,可以看出其具有很強的發光強度,其中oled3采用藍色熒光材料bd1為客體,其藍光峰值在455nm處且具有非常窄的半峰寬,證明其藍光的色純度較高。由此可見,本發明的化合物相對于現有技術常用的材料可以有效降低工作電壓、提高外量子效率和器件壽命。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 螺[芴?9,9?氧雜蒽]類空穴傳輸材料及其應用的制造方法與工藝
- 可采用環境友好溶劑加工的以螺芴單元為核的雙極性小分子發光材料及其制備方法與應用與流程
- 一種含有氮雜螺芴和含氮六元雜環的化合物及其在OLED上的應用的制造方法與工藝
- 一種含有氮雜螺芴和含氮六元雜環的化合物及其在有機電致發光器件上的應用的制造方法與工藝
- 一種以吖啶螺蒽酮為核心的化合物及其在有機電致發光器件上的應用的制造方法與工藝
- 一種含有吖啶螺蒽酮類化合物的有機電致發光器件及其應用的制造方法與工藝
- 螺雙芴衍生物及其在有機電致發光領域中的應用的制造方法與工藝
- 一種螺硅芴衍生物及其有機發光器件的制造方法與工藝
- 螺芴類衍生物及其制備方法和有機發光器件與制造工藝
- 一種4?溴螺環[芴?9,9’?氧雜蒽]的合成方法與制造工藝