還原/pH雙重響應性阿霉素前藥及其制備方法與應用與流程
本發明屬于生物醫用高分子材料領域,具體涉及一種基于聚乙二醇的還原/ph雙重響應性阿霉素前藥、其制備方法及其應用。
背景技術:
癌癥是機體在多種因素、多個階段和多次突變而導致正常細胞癌變的結果,在醫學上也稱之為惡性腫瘤。癌癥的殺傷力大、易轉移,通過破壞組織和器官的各項功能,最終導致人們因器官功能的衰竭而死亡。據統計,隨著人口的增長,癌癥的發病率也在不斷增長,嚴重危害著人類的健康,因此,癌癥治療方法備受國內外醫學研究者們的重視。
在過去的幾十年里,隨著醫療技術的進步,各種癌癥的治療方法得到了迅速發展,包括手術治療、化學療法、放射療法、免疫治療、激素治療、靶向治療等。但是,化療過程中使用的小分子藥物(如:紫杉醇,阿霉素,喜樹堿等),在殺死腫瘤細胞作用的同時對正常細胞也有很強的損傷作用,因此,會引起嚴重的嘔吐、頭暈、機體機能下降等副作用。同時,小分子藥物在血液循環過程中易被機體識別并排出,加上腫瘤組織附近特殊的環境,如錯綜復雜的血管網絡結構、致密的間質結構以及較高的間質液壓力等,使得藥物很難到達腫瘤細胞內。正是由于這些限制條件影響了抗腫瘤藥物在臨床上的療效。
通過前藥化,可以有效地解決上述問題。前藥(prodrug),也稱藥物前體、前驅藥物,是指經過生物體轉化后具有藥理作用的化合物。聚合物前藥是指具有活性的藥物與起運輸作用的聚合物載體通過共價鍵結合,使藥物不具有活性。但是,當前藥進入機體循環和代謝過程中,可通過水解作用卸除載體,釋放出活性藥物,發揮藥理作用。這種方式可以有效地提高藥物的利用率,增強靶向性,降低藥物的毒副作用。
在聚合物前藥結構中,對于聚合物基底材料的選擇至關重要,生物相容性是材料用于藥物載體的最基本要求。聚乙二醇(peg)具有無毒性、良好生物相容性和生物可降解性,已被美國食品藥品監督管理局(fda)批準使用。通過對peg進行末端官能化修飾,再與疏水性藥物鍵合,可以制備聚合物前藥,賦予藥物分子一些優良性質。盡管聚合物前藥在癌癥治療中具有很大的優勢,但是,如何將更多藥物傳遞到腫瘤細胞內,仍然是一直備受關注的問題。藥物到達病灶位點需要克服各種屏障,應考慮在血液循環過程中如何保持輸運載體的穩定性,延長循環時間;如何高效地進入細胞內,更多地累積在特定的部位;如何對藥物可控釋放等等。如果不解決這些問題,就會大大地降低藥物對癌癥的治療效果。
現有技術中,已有一些關于還原敏感和酸敏感性前藥的報道。但是,作為抗腫瘤前藥,應當具有良好的生物相容性和生物可降解性,并且,作為抗腫瘤前藥,還應當具有下列特征:在水溶液中可以形成穩定的聚合物膠束,親水性外殼起到穩定膠束、提高膠束血液循環時間的作用;前藥膠束在體內循環時,具有抗凝血和抗蛋白吸附的性能;當載藥膠束到達腫瘤或病變組織時,能夠利用局部組織低的ph條件和高的谷胱甘肽濃度的特點,破壞膠束,快速釋放出抗癌藥物。因此,需要尋求更多的藥效明顯、且在腫瘤細胞微環境中具有還原和酸敏感性抗腫瘤前藥。
技術實現要素:
本發明的目的是提供一種基于聚乙二醇的還原/ph雙重響應性阿霉素前藥及其制備方法;該阿霉素前藥具有良好的生物相容性和抑制腫瘤細胞增殖的能力。
本發明具體的技術方案為:一種還原/ph雙重響應性阿霉素前藥,由下列化學結構式表達:
m為3~113,n為3~15。
上述技術方案中,阿霉素前藥具有酸敏感性的基團以及還原敏感性的基團;該具有雙重響應性的阿霉素前藥在結構上含有的疏水性阿霉素部分,用于形成膠束的內核,peg親水性部分包裹在內核外邊形成膠束的外殼,對膠束的穩定性具有很好的作用。在還原和ph條件下,酸敏感基團以及還原敏感基團發生斷裂,膠束被破壞,從而快速地釋放出聚集在膠束內部的疏水性抗癌藥物。
優選的技術方案中,還原/ph雙重響應性阿霉素前藥的數均分子量為4000~80000g·mol-1。
本發明采用結構中含有酸敏感基團以及還原敏感基團的交替共聚物poly(ss-alt-a)作為基本原料,經銅鹽及配體催化化學反應活化后與抗癌藥物阿霉素反應,制備基于聚乙二醇的還原/ph雙重響應性阿霉素前藥dox-hyd-poly(ss-alt-a)-hyd-dox。
上述還原/ph雙重響應性阿霉素前藥的制備方法,包括以下步驟:
(1)以6-疊氮己酰肼與阿霉素鹽酸鹽(dox×hcl)作為原料,無水甲醇為溶劑,冰醋酸為催化劑,通過化學反應獲得阿霉素衍生物;
其中,6-疊氮己酰肼與阿霉素鹽酸鹽的摩爾比為1:(2~6);
所述6-疊氮己酰肼的化學結構式為:
所述阿霉素衍生物的化學結構式為:
(2)惰性氣體氣氛條件下,在銅鹽催化劑和配體的存在下,以3,3’-二硫二炔丁基二丙酸酯與二疊氮乙基二縮醛基聚乙二醇為原料,以無水n,n-二甲基甲酰胺為溶劑,通過反應制備獲得兩端炔基封端的聚乙二醇交替共聚物;
其中,二疊氮乙基二縮醛基聚乙二醇、3,3’-二硫二炔丁基二丙酸酯和銅鹽催化劑的摩爾比為1∶(1.1~1.5)∶(0.5~1.5);銅鹽催化劑和配體的摩爾比為1∶(1~2);
所述3,3’-二硫二炔丁基二丙酸酯的化學結構式為:
所述二疊氮乙基二縮醛基聚乙二醇的結構式為:
上述m為3~113;
所述兩端炔基封端的聚乙二醇交替共聚物的結構式為:
上述m為3~113,n為3~15。
(3)以無水n,n-二甲基甲酰胺作為溶劑,在銅鹽催化劑和配體的存在下,用步驟(2)獲得的兩端炔基封端的的聚乙二醇交替共聚物與步驟(1)獲得的阿霉素衍生物反應,制備得到所述還原/ph雙重響應性阿霉素前藥;
所述兩端炔基封端的聚乙二醇交替共聚物、阿霉素衍生物的摩爾比為1:(2~5)。
上述技術方案中,制備阿霉素衍生物(n3-hyd-dox×hcl),主要通過三個步驟制備而成:
第一步,制備6-疊氮己酸甲酯。以6-溴己酸甲酯與疊氮化鈉(nan3)反應,以dmf為溶劑,進行疊氮化反應,獲得6-疊氮己酸甲酯。其中,6-溴己酸甲酯、疊氮化鈉的摩爾比為1:(1.5~5);
第二步,制備6-疊氮己酰肼。以第一步合成的6-疊氮己酸甲酯與質量分數為85%的水合肼反應,以四氫呋喃(thf)作為溶劑,通過酰胺化反應,獲得6-疊氮己酰肼。其中,6-疊氮己酸甲酯與水合肼的摩爾比為1:(10~30);
第三步,制備阿霉素衍生物(n3-hyd-dox×hcl)。采用第二步合成的6-疊氮己酰肼與阿霉素鹽酸鹽(dox×hcl)作為原料,以無水甲醇為溶劑,冰醋酸為催化劑,獲得阿霉素衍生物。其中,6-疊氮己酰肼與阿霉素鹽酸鹽的摩爾比為1:(2~6);
制備兩端炔基封端的聚乙二醇交替共聚物包括以下幾步:
制備炔基封端的并含有二硫鍵的小分子化合物3,3’-二硫二炔丁基二丙酸酯(b-ss-b)。采用3,3’-二硫代二丙酸與3-丁炔-1-醇為原料,以1-乙基-(3-二甲基氨基丙基)碳二亞胺鹽酸鹽為活化劑,4-二甲氨基吡啶為催化劑,二氯甲烷為溶劑,通過酯化反應,獲得3,3’-二硫二炔丁基二丙酸酯。其中,3,3’-二硫代二丙酸與3-丁炔-1-醇的摩爾比為1:(1.5~3);
制備疊氮基封端的二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3),通過兩步進行:
第一步,合成二氯乙基二縮醛基聚乙二醇(cl-a-peg-a-cl)。采用聚乙二醇(ho-peg-oh)與2-氯乙基乙烯基醚(ceve)為原料、酸催化劑存在下,反應得到末端為氯基的聚乙二醇產物cl-a-peg-a-cl。其中,聚乙二醇的分子量為:400~5000g·mol-1,聚乙二醇與2-氯乙基乙烯基醚的摩爾比為1:(2~6);酸催化劑為對甲基苯磺酸、對甲苯磺酸吡啶鎓、三氟乙酸中的一種;
第二步,合成二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3)。將第一步得到的cl-a-peg-a-cl與疊氮化鈉反應,以二氯甲烷為溶劑,得到二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3)。其中,所述末端含氯基的聚乙二醇(cl-a-peg-a-cl)與疊氮化鈉的摩爾比為1:(2~6);
制備炔基封端的聚合物poly(ss-alt-a)。在氮氣保護下,在銅鹽催化劑和配體的存在下,利用上述合成的3,3’-二硫二炔丁基二丙酸酯(b-ss-b)與二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3)發生化學反應,制備炔基封端的聚合物poly(ss-alt-a)。其中,二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3)與3,3’-二硫二炔丁基二丙酸酯(b-ss-b)的摩爾比為1:(1.1~1.5);
制備雙重響應的阿霉素前藥dox-hyd-poly(ss-alt-a)-hyd-dox包括以下幾步:
利用脫鹽處理的阿霉素衍生物與上步合成的兩端炔基封端的聚乙二醇交替共聚物poly(ss-alt-a)發生化學反應,獲得還原/ph雙重響應性阿霉素前藥dox-hyd-poly(ss-alt-a)-hyd-dox。其中,兩端炔基封端的聚乙二醇交替共聚物與阿霉素衍生物的摩爾比為1:(2~5)。
上述技術方案中,步驟(1)中,反應溫度為60℃~80℃,反應時間為12h~24h;步驟(2)中,惰性氣體為氮氣;反應溫度為25℃~50℃,反應時間為24h~72h;步驟(3)中,反應溫度為25℃~50℃,反應時間為24h~48h。
上述技術方案中,步驟(2)和步驟(3)中,銅鹽催化劑選自五水合硫酸銅、氯化亞銅或溴化亞銅;配體選自:抗壞血酸鈉、聯吡啶、五甲基二亞乙基三胺、四甲基乙二胺或六甲基三亞乙基四胺中的一種。
本發明首次在銅鹽催化劑和配體的存在下,通過原料以及參數的限定,制備得到含有酸敏感基團以及還原敏感基團的聚乙二醇交替共聚物,解決了現有反應體系無法制備出同時含有酸敏感基團以及還原敏感基團的交替共聚物的問題,是一種新型、簡單、高效、快速的合成方法。
進一步的技術方案,在步驟(1)~(3)完成后,分別對產物進行提純處理,所述純化過程包括以下步驟:
(i)阿霉素衍生物n3-hyd-dox×hcl的純化:反應結束后,反應液用棉花過濾除去沉淀物,除去溶劑后在冰乙醚中沉淀三次;采用離心法得到沉淀物,將其放置在真空干燥箱中干燥得到紅色粉末狀的產物n3-hyd-dox×hcl;
(ii)兩端炔基封端的聚乙二醇交替共聚物poly(ss-alt-a)的純化:反應結束后,用dmf透析48h后,置于60℃油浴中,減壓除去dmf;然后用150mlch2cl2重新溶解,用飽和nacl水溶液進行萃取,除去銅鹽;有機層用無水na2so4干燥4h后,旋轉蒸發除去溶劑,再在乙醚溶液中沉淀3次,將沉淀物收集并真空干燥,最終得到粘性產物poly(ss-alt-a);
(ⅲ)還原/ph雙重響應性阿霉素前藥dox-hyd-poly(ss-alt-a)-hyd-dox的純化:反應結束后,采用去離子水透析72h,將透析袋中所得到的紅色透明液體冷凍干燥,獲得深紅色固體產物dox-hyd-poly(ss-alt-a)-hyd-dox。
上述技術方案中,步驟(i)中,采用旋轉蒸發的方法除去溶劑;步驟(ii)中透析時采用截留分子量為1000~14000da的透析袋;步驟(ⅲ)中,透析時采用截留分子量為3500~14000da的透析袋。
具體的提純包括以下步驟:
(i)制備阿霉素衍生物(n3-hyd-dox×hcl)的純化:
第一步,制備6-疊氮己酸甲酯的純化:反應結束后,用中性三氧化二鋁的短柱過濾反應液,并用油泵減壓除去溶劑dmf。隨后,用大量的二氯甲烷溶解粗產物,用30ml的二次水萃取三次,將有機相收集并用無水硫酸鈉干燥4h。最后,用棉花過濾、旋轉蒸發除去溶劑,將產物置于真空烘箱中干燥24h,得到無色的液體產物6-疊氮己酸甲酯;
第二步,制備6-疊氮己酰肼的純化:反應結束后,旋轉蒸發除去thf后換用ch2cl2溶解。在分液漏斗中,采用飽和氯化鈉水溶液萃取粗產物。將有機相用無水na2so4干燥4h,除去溶劑后真空干燥,最終收集到產物6-疊氮己酰肼;
第三步,制備阿霉素衍生物的純化:反應結束后,用棉花過濾除去反應液中的na2so4,將濾液旋轉蒸發除去溶劑后,在冰乙醚中沉淀三次。最終,采用離心法得到下面的沉淀物,將其放置在真空干燥箱中干燥24h,得到紅色粉末狀產物,即為n3-hyd-dox×hcl;
(ii)制備炔基封端的3,3’-二硫二炔丁基二丙酸酯(b-ss-b)的純化:反應結束后,用濾紙過濾,除去反應中生成的鹽,再用150ml的ch2cl2溶解,用1mhcl溶液和飽和氯化鈉(nacl)水溶液的混合溶液萃取2次,每個水層繼續用30ml的ch2cl2萃取3次。將有機層收集后,用無水na2so4干燥4h,除去溶劑后的粗產物繼續采用柱層析法進行分離提純。收集最終產物,真空干燥24h,即得到3,3’-二硫二炔丁基二丙酸酯(b-ss-b);
(ⅲ)制備疊氮基封端的二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3)的純化:
第一步,制備合成二氯乙基二縮醛基聚乙二醇(cl-a-peg-a-cl)的純化:反應結束后,先用ch2cl2稀釋反應液,用10ml的磷酸緩沖溶液(pbs,ph10.0)和飽和nacl水溶液的混合溶液萃取,得到的水層繼續用ch2cl2萃取三次。有機層用無水na2so4干燥4h后,旋轉蒸發除去大量溶劑,剩約3ml粗產物溶液時,將其在正己烷中沉淀三次,收集沉淀物并真空干燥,得到產物cl-a-peg-a-cl;
第二步,制備合成二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3)的純化:反應結束后,用中性al2o3的短柱過濾除去未反應的nan3,60°c油浴減壓條件下除去溶劑dmf。隨后,用ch2cl2溶解粗產物,用ph10.0的pb緩沖溶液萃取提純產物,每個水層繼續用20ml的ch2cl2萃取,最終將有機相收集并用無水na2so4干燥,旋轉蒸發除去溶劑并真空干燥得到棕色的產物n3-a-peg-a-n3;
(ⅳ)兩端炔基封端的聚乙二醇交替共聚物poly(ss-alt-a)的純化:反應結束后,用dmf透析48h后,置于60℃油浴中,減壓除去dmf。然后用150mlch2cl2重新溶解,用飽和nacl水溶液進行萃取,除去銅鹽。有機層用無水na2so4干燥4h后,旋轉蒸發除去溶劑,再在乙醚中沉淀3次,將沉淀物收集并真空干燥,最終得到粘性產物poly(ss-alt-a);
(ⅴ)制備雙重響應的阿霉素前藥dox-hyd-poly(ss-alt-a)-hyd-dox的純化:反應結束后,采用去離子水透析72h,將透析袋中所得到的紅色透明液體冷凍干燥,得到紅色粘性固體產物dox-hyd-poly(ss-alt-a)-hyd-dox。
本發明公開的還原/ph雙重響應性阿霉素前藥dox-hyd-poly(ss-alt-a)-hyd-dox可以在水溶液中自組裝形成前藥膠束,疏水性藥物阿霉素形成膠束的核;親水性peg鏈段形成膠束的外殼,起到穩定膠束的作用。而疏水性內核和親水性peg鏈段之間含有還原響應的二硫鍵和酸敏感的縮醛及酰腙鍵基團,在還原和ph條件下,敏感基團發生斷裂,膠束被破壞,從而快速地釋放出聚集在膠束內部的疏水性抗癌藥物。因此,本發明同時請求保護上述還原/ph雙重響應性阿霉素前藥在制備刺激響應性抗癌納米藥物中的應用。
由于上述方案的實施,本發明與現有技術相比,具有以下優點:
1、本發明采用生物相容性良好的聚乙二醇和疏水性抗癌藥物阿霉素分別作為親水性鏈段和疏水性末端,以在還原條件下和酸性條件下可發生水解的基團作為敏感性連接基團,制備了具有良好生物相容性的還原/ph雙重響應性阿霉素前藥;與原藥阿霉素相比,前藥具有良好的水溶性和貯存穩定性,在腫瘤細胞環境中易于分解,加速藥物釋放,大大增加了其應用價值。
2、本發明獲得的還原/ph雙重響應性阿霉素前藥在水中可自組裝形成穩定的聚合物前藥膠束。疏水性的阿霉素部分聚集形成膠束內核,親水性peg鏈段作為膠束外殼起到穩定膠束、提高膠束血液循環時間的作用。親水部分和疏水部分通過在酸性條件下可裂解化學鍵相連,同時親水的peg鏈段內部含有在還原條件下和酸性條件下可發生水解的基團;當前藥膠束到達腫瘤或病變組織時,由于這些組織微環境的ph值降低,會使酸敏感基團發生斷裂,同時在高的谷胱甘肽的環境中,還原敏感基團也發生斷裂,導致膠束結構被破壞,從而快速釋放出抗癌藥物,增加了藥物的利用率和靶向性,在癌癥的治療方面,具有潛在的應用價值。
3、本發明提供的還原/ph雙重響應性阿霉素前藥結構明確,合成條件不苛刻,具有以下顯著特點:(1)所用原料和試劑容易獲得;(2)反應條件簡單;(3)產率高;(4)立體選擇性好;(5)產物分離簡便;(6)產物穩定性好;制備容易,提純方便,適合工業化生產。
附圖說明
圖1為實施例一中阿霉素衍生物(n3-hyd-dox×hcl)的核磁共振氫譜圖,溶劑為氘代二甲亞砜;
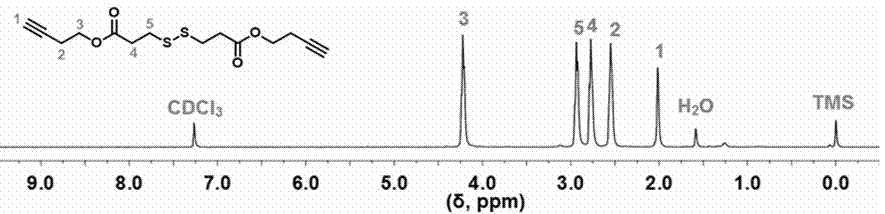
圖2為實施例二中3,3’-二硫二炔丁基二丙酸酯的核磁共振氫譜圖,溶劑為氘代氯仿;
圖3為實施例三中cl-a-peg21-a-cl和n3-a-peg21-a-n3的核磁共振氫譜圖,溶劑為氘代氯仿,其中,下標21代表-ch2ch2o-的重復單元數;
圖4為實施例四中聚合物poly(ss-alt-a)3.6的核磁共振氫譜圖,溶劑為氘代氯仿,其中,下標3.6代表交替共聚物的聚合度;
圖5為實施例五中dox-hyd-poly(ss-alt-a)3.6-hyd-dox的核磁共振氫譜圖,溶劑為氘代氯仿;
圖6為實施例一~五中ho-peg21-oh,cl-a-peg21-a-cl,n3-a-peg21-a-n3,poly(ss-alt-a)3.6,n3-hyd-dox×hcl和dox-hyd-poly(ss-alt-a)3.6-hyd-dox的紅外光譜圖;
圖7為實施例五中dox-hyd-poly(ss-alt-a)3.6-hyd-dox的在ph7.4緩沖溶液中自組裝形成的膠束的動態光散射曲線和透射電鏡照片圖;
圖8為實施例五中dox-hyd-poly(ss-alt-a)3.6-hyd-dox形成的聚合物前藥膠束與裸藥阿霉素在不同ph值的緩沖溶液中的藥物釋放曲線圖;
圖9為dox-hyd-poly(ss-alt-a)3.6-hyd-dox前藥與裸藥阿霉素的抑制腫瘤細胞增殖性能測試圖。
具體實施方式
下面結合實施例和附圖對本發明作進一步描述:
實施例一:阿霉素衍生物(n3-hyd-dox×hcl)的合成
阿霉素衍生物(n3-hyd-dox×hcl)主要通過三個步驟制備而成。第一步,制備6-疊氮己酸甲酯;第二步,制備6-疊氮己酰肼;第三步,對阿霉素鹽酸鹽(dox×hcl)進行修飾得到阿霉素衍生物(n3-hyd-dox×hcl),具體合成方法如下:
合成小分子化合物6-疊氮己酸甲酯。將事先放置于120°c烘箱的裝置取出,放入保干器中,待其冷卻至室溫,取出使用。分別稱取6-溴己酸甲酯(3.54g,16.93mmol)和疊氮化鈉(nan3)(2.75g,42.33mmol),并用20ml的dmf溶解在50ml的圓底燒瓶中,在60°c冷凝水回流條件下反應12h后結束。用中性三氧化二鋁(al2o3)的短柱過濾反應液,除去未反應的nan3,并用油泵減壓除去溶劑dmf。隨后,用大量的二氯甲烷(ch2cl2)溶解粗產物,用30ml的二次水萃取三次,將有機相收集并用無水硫酸鈉(na2so4)干燥4h。最后,用棉花過濾、旋轉蒸發除去溶劑,將產物置于真空烘箱中干燥24h,得到無色的液體產物6-疊氮己酸甲酯(2.47g,產率:53.2%);
在圓底燒瓶中加入已得到的6-疊氮己酸甲酯(0.76g,4.44mmol)和質量分數為85%的水合肼(5.60g,111.1mmol),采用四氫呋喃(thf)作為溶劑。同樣,在80°c油浴并裝有蛇形冷凝管的裝置中,回流反應12h。反應結束后,旋轉蒸發除去thf,用ch2cl2溶解。在分液漏斗中,采用飽和氯化鈉水溶液萃取粗產物。將有機相用無水na2so4干燥4h,除去溶劑后真空干燥,最終收集到產物6-疊氮己酰肼(0.55g,產率:56.2%);
分別稱取6-疊氮己酰肼(102.0mg,0.60mmol),dox×hcl(115.9mg,0.20mmol)和無水na2so4(103mg,0.73mmol)加入帶有冷凝回流裝置的圓底燒瓶中,用30ml的無水甲醇溶解。隨后加入3滴冰醋酸,充分攪拌均勻后,在65°c油浴中避光反應24h。反應結束后,用棉花過濾,除去反應液中的na2so4,除去溶劑后在冰乙醚中沉淀三次。最終,采用離心法得到下面的沉淀物,將其放置在真空干燥箱中干燥24h,得到紅色粉末狀的產物,即為n3-hyd-dox×hcl(93.5mg,產率:62.4%)。
實施例二:炔基封端的3,3’-二硫二炔丁基二丙酸酯(b-ss-b)的合成
首先,以3,3’-二硫代二丙酸與3-丁炔-1-醇為原料,以1-乙基-(3-二甲基氨基丙基)碳二亞胺鹽酸鹽為活化劑,4-二甲氨基吡啶為催化劑,二氯甲烷為溶劑,通過酯化反應,獲得3,3’-二硫二炔丁基二丙酸酯。具體合成方法如下:
將所用玻璃儀器置于120°c烘箱中烘干4h,取出放在保干器中冷卻至室溫待用。首先,向三頸燒瓶中依次加入3,3’-二硫代二丙酸(3.66g,17.40mmol)、1-乙基-(3-二甲基氨基丙基)碳二亞胺鹽酸鹽(edc×hcl)(8.67g,45.23mmol)和4-二甲氨基吡啶(dmap)(3.19g,2.61mmol),用100ml的ch2cl2溶解;其次,將3-丁炔-1-醇(3.17g,45.23mmol)和15ml的ch2cl2加入恒壓滴液漏斗中。在冰水浴中滴加2h,滴加結束后,將裝置移到25°c的油浴中,繼續反應48h;
反應結束后,旋轉蒸發除去少量溶劑,濾紙過濾除去反應生成的鹽,再用150ml的ch2cl2溶解,用1mhcl溶液和飽和氯化鈉(nacl)水溶液的混合溶液萃取2次,收集的水層用30ml的ch2cl2萃取3次。將有機層收集后,用無水na2so4干燥4h,除去溶劑后的粗產物繼續采用柱層析法進行分離提純,淋洗劑為乙酸乙酯和石油醚的混合溶液(乙酸乙酯:石油醚=1:6)。最終產物被收集,真空干燥24h后即得到較純的3,3’-二硫二炔丁基二丙酸酯b-ss-b(3.63g,產率:59.4%)。
實施例三:疊氮基封端的二疊氮乙基二縮醛基聚乙二醇(n3-a-peg21-a-n3)的合成
疊氮基封端的化合物二疊氮乙基二縮醛基聚乙二醇(n3-a-peg21-a-n3),通過兩步反應得到:首先,合成二氯乙基二縮醛基聚乙二醇(cl-a-peg21-a-cl);其次,合成二疊氮乙基二縮醛基聚乙二醇(n3-a-peg21-a-n3)。具體合成方法如下:
第一步,合成二氯乙基二縮醛基聚乙二醇(cl-a-peg21-a-cl)。取分子量為1000的聚乙二醇(ho-peg22-oh)(6.01g,6.01mmol)和對甲苯磺酸吡啶鎓(ppts)(0.30g,1.20mmol)置于100ml的支管燒瓶中,并加入50ml的甲苯,采用兩次常壓甲苯共沸的方法除去雜質水。待其冷卻后,在氮氣保護下,加入30ml干燥的ch2cl2溶解,并在恒壓滴液漏斗中加入10ml的ch2cl2和2-氯乙基乙烯基醚(ceve)(3.20g,30.05mmol),冰水浴滴加完后,室溫下繼續反應1h,加入10ml的質量分數為5%的碳酸鈉(na2co3)水溶液終止反應;
產物的提純采用萃取和沉淀相結合的方法。先用ch2cl2稀釋反應液,用10ml磷酸緩沖溶液(pbs,ph10.0)和飽和nacl水溶液的混合溶液萃取,得到的水層繼續用ch2cl2萃取三次。有機層用無水na2so4干燥4h后,旋轉蒸發除去ch2cl2溶劑。然后,將其在正己烷中沉淀三次,收集沉淀物并真空干燥,得到產物cl-a-peg21-a-cl(5.75g,產率:78.9%);
第二步,合成二疊氮乙基二縮醛基聚乙二醇(n3-a-peg21-a-n3)。將上步得到的cl-a-peg-a-cl(2.37g,1.95mmol)和nan3(0.76g,11.70mmol)溶解在25ml的dmf中,60°c油浴下反應48h。反應結束后,用中性al2o3的短柱過濾除去未反應的nan3,置于60℃油浴中,減壓除去dmf。隨后,用ch2cl2溶解粗產物,用ph10.0的pb緩沖溶液萃取提純產物,收集的水層用20ml的ch2cl2萃取。最終將有機相收集,并用無水na2so4干燥,旋轉蒸發除去溶劑,真空干燥得到棕色的產物n3-a-peg21-a-n3(1.68g,產率:63.9%)。
實施例四:炔基封端的聚合物poly(ss-alt-a)n的合成
在氮氣保護下,將3,3’-二硫二炔丁基二丙酸酯(b-ss-b)與二疊氮乙基二縮醛基聚乙二醇(n3-a-peg21-a-n3)發生化學反應,制備炔基封端的聚合物poly(ss-alt-a)n。具體合成方法如下:
在氮氣的保護下,向含有10ml的dmf的支管燒瓶中加入cubr(0.085g,0.59mmol)和五甲基二乙烯三胺(pmdeta)(0.102g,0.59mmol),攪拌使兩者進行絡合,隨后依次加入已合成的b-ss-b(0.25g,0.79mmol)和n3-a-peg21-a-n3(0.97g,0.79mmol)。抽充氣三次后,裝置在氮氣保護下密封好置于50°c油浴中反應48h,隨后,補加10mol%的b-ss-b繼續反應24h,以確保兩端為丁炔基。粗產物用dmf進行透析(透析袋截留分子量為3500da),每隔一段時間換新的透析液。48h后,60°c油泵減壓除去dmf。然后用150ml的ch2cl2重新溶解,加入飽和nacl水溶液除去銅鹽。分離得到的有機層用無水na2so4干燥4h后,旋轉蒸發除去溶劑,再在乙醚溶液中沉淀3次,將沉淀物收集并真空干燥,最終得到粘性產物poly(ss-alt-a)n(0.74g,產率:60.7%)。
實施例五:雙重響應的阿霉素前藥dox-hyd-poly(ss-alt-a)n-hyd-dox的合成
利用脫鹽處理的阿霉素衍生物與聚合物poly(ss-alt-a)n發生化學反應,獲得還原/ph雙重響應性阿霉素前藥dox-hyd-poly(ss-alt-a)n-hyd-dox。具體合成方法如下:
首先,對阿霉素衍生物(n3-hyd-dox×hcl)進行脫鹽酸處理。在圓底燒瓶中,加入n3-hyd-dox×hcl(0.095g,0.13mmol),用3mldmso溶解,并加入10ml三乙胺(tea)攪拌2h,靜置后吸走上清液再加入新的tea溶液繼續攪拌,如此重復2次,最后留取dmso層的樣品待用。在支管燒瓶中,通氮氣的狀態下,先加入cubr(0.015g,0.104mmol)和pmdeta(0.018g,0.104mmol),用5mldmf溶劑溶解并攪拌5min,再依次向瓶中加入poly(ss-alt-a)n(0.23g,0.052mmol)和上述脫去鹽酸鹽的n3-hyd-dox的溶液,抽充氣三次后,將瓶子密封置于50°c油浴中反應48h。反應結束后,將反應液移到截留分子量為5000da的透析袋中,采用去離子水進行透析,每隔4h后換一次去離子水。透析72h后,將透析袋中溶液取出,在冰箱中冷凍后置于凍干機中凍干,最后得到紅色粘性固體產物dox-hyd-poly(ss-alt-a)n-hyd-dox(0.26g,產率:84.2%)。
分別利用核磁共振氫譜(1hnmr)和紅外光譜(ft-ir)驗證所得小分子化合物、聚合物以及基于聚乙二醇的還原/ph雙重響應性阿霉素前藥的結構。附圖1為阿霉素衍生物(n3-hyd-dox×hcl)的核磁共振氫譜圖、附圖2為聚合物3,3’-二硫二炔丁基二丙酸酯的核磁共振氫譜圖、附圖3為cl-a-peg21-a-cl和n3-a-peg21-a-n3的核磁共振氫譜圖、附圖4為聚合物poly(ss-alt-a)3.6的核磁共振氫譜圖、附圖5為dox-hyd-poly(ss-alt-a)3.6-hyd-dox的核磁共振氫譜圖、附圖6為ho-peg21-oh,cl-a-peg21-a-cl,n3-a-peg21-a-n3,poly(ss-alt-a)3.6,dox-hyd-n3和dox-hyd-poly(ss-alt-a)3.6-hyd-dox的紅外光譜圖。結合附圖1、2、3、4、5、6可以證明反應產物符合實驗設計。
實施例六:采用透析法制備聚合物前藥膠束
取聚合物前藥(dox-hyd-poly(ss-alt-a)3.6-hyd-dox)25mg溶解在2ml的dmf中,攪拌2h后,用微量注射器以2mlh-1的速度向溶液中滴加20ml的去離子水,滴加結束后,繼續攪拌2h。隨后,將溶液裝入截留分子量為5000da的透析袋中,用去離子水透析24h后,將溶液取出并定容至25ml,最終得到濃度為1mgml-1的膠束溶液。附圖7為dox-hyd-poly(ss-alt-a)3.6-hyd-dox在水中自組裝形成的膠束的透射電鏡照片(a)和動態光散射曲線(b);如:附圖7(a)所示為聚合物前藥在水溶液中自組裝形成球形膠束的形貌;附圖7(b)所示為對應膠束粒徑的動態光散射測試曲線圖,可以看出聚合物前藥膠束平均粒徑為48nm。
實施例七:聚合物前藥的體外藥物釋放測試
取4ml預先制備好的膠束溶液(膠束濃度為1mgml-1)置于截留分子量為7000da的透析袋中,兩端封好置于50ml的大離心管中,隨后,向相應的離心管中分別加入30ml不同的緩沖溶液。緩沖溶液分為四種:(1)磷酸緩沖液(ph7.4,10mm);(2)含有10mm的gsh的磷酸緩沖液(ph7.4,10mm);(3)醋酸緩沖液(ph5.0,10mm);(4)含有10mm的gsh的醋酸緩沖液(ph5.0,10mm)。然后,將大離心管置于37.5°c的恒溫振蕩儀中,以160r/min速度進行振蕩。在設定的時間點,依次取出5ml的釋放液并補加相應的緩沖溶液。每組實驗進行3個平衡實驗,最后取平均值。取出的釋放液用熒光分光光度計對dox濃度進行測定。載有阿霉素的聚合物膠束在不同的還原和ph條件下的釋放曲線如附圖8所示,在ph5.0或者在含有10mm的gsh的磷酸緩沖液中,藥物釋放速率明顯快于正常生理條件下;同時,在含有10mm的gsh的ph5.0緩沖溶液中藥物累計釋放率最大。藥物釋放說明該聚合物前藥膠束具有明顯的還原和ph雙重響應性,可以達到控制釋放的目的。
實施例八:聚合物前藥膠束抑制腫瘤細胞增殖性能測試
分別將人子宮頸癌細胞(helacells)和人肝癌細胞(hepg2cells)培養在補充有10%胎牛血清(fbs)的dmem培養基中,置于37℃,5%co2(相對濕度為90%)的培養箱中培養,定期更換培養液。選擇處在生長活躍期的細胞接種于每孔含有100μldmem培養基的96孔板中,培養24h。用透析法配置聚合物前藥dox-hyd-poly(ss-alt-a)3.6-hyd-dox的膠束母液(阿霉素濃度為94mgl-1),將一系列不同濃度的膠束溶液加入到96孔板中,分別繼續培養48h和72h。接著加入25μl的mtt試劑,進一步培養4h后,用酶標儀(bio-radmodel680)在570nm下測量對應的吸光度。細胞存活率的計算方法為:細胞存活率(cellviability)(%)=[a]test/[a]control×100%,其中,[a]test為dox-hyd-poly(ss-alt-a)3.6-hyd-dox聚合物前藥膠束存在下測得的吸光度,而[a]control為不含聚合物前藥的情況下測得的吸光度。每個樣品測試三次,取其平均值。如附圖9所示,(a)和(b)分別為與hela細胞培養48h和72h后細胞的存活率;(c)和(d)分別為與hepg2細胞培養48h和72h后細胞的存活率。結果顯示:與抗癌藥物阿霉素相比,所合成的聚合物前藥具有良好的抑制hela細胞和hepg2細胞增殖的能力。
本發明首先制備阿霉素衍生物(n3-hyd-dox×hcl);再分別制備炔基封端的小分子化合物3,3’-二硫二炔丁基二丙酸酯(b-ss-b)和疊氮基封端的化合物二疊氮乙基二縮醛基聚乙二醇(n3-a-peg-a-n3);然后,通過聚合反應制備含有縮醛鍵和二硫鍵的聚合物poly(ss-alt-a);最后,再通過反應將阿霉素連接在聚合物兩端,獲得具有還原和ph雙重響應的阿霉素前藥dox-hyd-poly(ss-alt-a)3.6-hyd-dox,更換本發明限定的其他催化劑以及配體同樣可以得到產物,更換聚乙二醇的分子量以及本發明限定的原料比例,可以得到不同m值n值的產物;本發明限定的具有刺激響應性聚合物前藥在水溶液中可以組裝成前藥膠束并穩定存在,而在酸性或者是還原條件下,敏感性基團或鏈段會發生斷裂使膠束被破壞,從而可以將聚集在膠束內部的藥物快速地釋放出來,用于治療,取得了如實施例記載的技術效果。
- 還沒有人留言評論。精彩留言會獲得點贊!