一種檢測缺血性腦卒中的分子標志物及其用途的制作方法
本發明涉及生物醫藥領域,具體涉及一種檢測缺血性腦卒中的分子標志物及其用途。
背景技術:
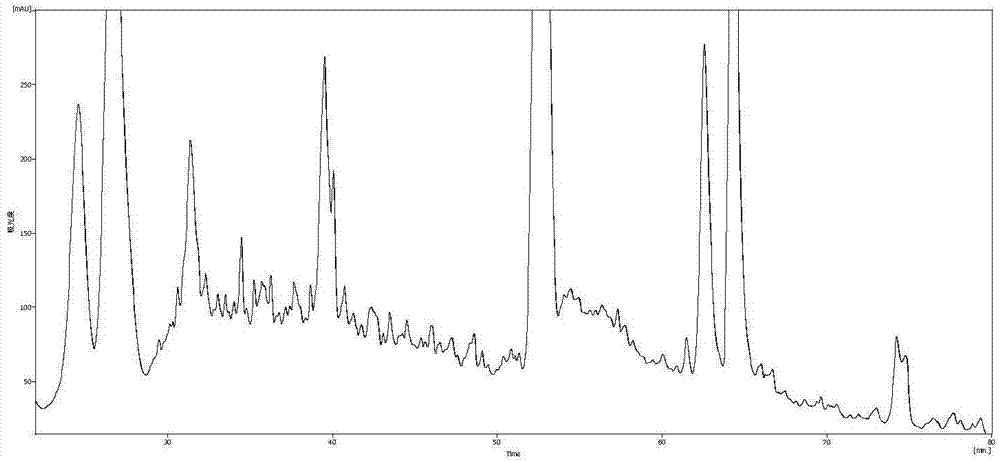
:腦卒中又稱“中風”、“腦血管意外”(cerebralvascularaccident,cva)。是一種急性腦血管疾病,是由于腦部血管突然破裂或因血管阻塞導致血液不能流入大腦而引起腦組織損傷的一組疾病,包括缺血性和出血性卒中。缺血性腦卒中又稱腦梗死,中醫稱之為中風。本病系由各種原因所致的局部腦組織區域血液供應障礙,導致腦組織缺血缺氧性病變壞死,進而產生臨床上對應的神經功能缺失表現。缺血性腦卒中依據發病機制的不同分為腦血栓形成、腦栓塞和腔隙性腦梗死等主要類型。其中腦血栓形成是腦梗死最常見的類型,約占全部腦梗死的60%,因而通常所說的‘腦梗死’實際上指的是腦血栓形成。缺血性腦卒中病因:由于缺血性腦卒中的主要分類——腦血栓形成的病因基礎主要為動脈粥樣硬化,因而產生動脈粥樣硬化的因素是發生腦梗死最常見的病因。由于動脈粥樣硬化好發于大血管的分叉處和彎曲處,故腦血栓形成的好發部位為頸動脈的起始部和虹吸部、大腦中動脈起始部、椎動脈及基底動脈中下段等。當這些部位的血管內膜上的斑塊破裂后,血小板和纖維素等血液中有形成分隨后黏附、聚集、沉積形成血栓,而血栓脫落形成栓子可阻塞遠端動脈導致缺血性腦卒中。近期在全球范圍內進行的interstroke研究結果顯示:腦梗死風險中的90%可歸咎于10個簡單的危險因素,它們依次是高血壓病、吸煙、腰臀比過大、飲食不當、缺乏體育鍛煉、糖尿病、過量飲酒、過度的精神壓力及抑郁、有基礎心臟疾病和高脂血癥。腦卒中是我國繼心血管疾病、惡性腫瘤疾病之后的第三大致死性疾病,每年發病率為150/10萬,死亡率為120/10萬。腦卒中分為缺血卒中和出血性卒中。其中,臨床上缺血性卒中更為常見,約占全部腦卒中的70%。約有50%~75%的腦卒中與高血壓有關,高血壓史使腦卒中的風險增加2.5倍以上。如果應用更嚴格的高血壓定義——血壓>160/90mmhg,這種風險因素的相關性會增加。缺血性腦卒中的病死率約為10%,致殘率可達50%以上。存活者的復發率高達40%,缺血性腦卒中復發可嚴重削弱患者的日常生活和社會功能,而且可明顯增加死亡率。目前,識別引起腦卒中的原因是主要根據頭顱ct掃描,核磁共振成像技術和動脈造影。但ct、mri掃描并不是完全可信的方法,因為在診斷早期ct對缺血性腦卒中只有16%的靈敏度,而對于出血性腦卒中卻有89%的靈敏度。20%缺血性腦卒中并不能夠被mri掃描技術探測到。且影像診斷技術并不存在于所有診療中心中,這些都阻礙了腦卒中的快速診斷和藥物的及時應用。分子標志物是藥物研發過程中的有效工具,它提供了藥物性能及疾病進程的相關信息,反映了具體的藥物治療效果。糖尿病及免疫性疾病等多種疾病都已經根據分子標志物進行治療。然而,在腦血管病中分子標志物仍相對缺乏。因此,探索缺血性腦卒中的分子標志物有著重要的意義。由于傳統診斷不足,找到診斷腦卒中的新穎的生物標志成為了一種迫切的需求。針對辨認生物學標志物用itraq和高分辨率的質譜來進行相對定量是一項很有前途的技術。識別體液中的缺血性腦卒中生物學標志物對于影像學診斷具有輔助性作用。技術實現要素:為了實現腦卒中的早期發現,早期干預,本發明的目的在于提供一種多聚免疫球蛋白受體(polymericimmunoglobulinreceptor(pigr))蛋白在作為缺血性腦卒中分子標志物中的用途。為實現上述目的,本發明首先提供了一種檢測缺血性腦卒中的分子標志物,所述分子標志物包括pigr蛋白或其活性片段;編碼所述pigr蛋白的mrna;編碼所述pigr蛋白的基因。本發明的第二方面提供了所述分子標志物在診斷缺血性腦卒中和/或評估罹患缺血性腦卒中風險的產品中的用途。本發明的第三方面提供了所述分子標志物在評估腦卒中的治療效果或者判斷腦卒中的預后產品中的用途。優選的,所述產品包括芯片或試劑盒。優選的,所述pigr蛋白在缺血性腦卒中生物樣品中表達上調。優選的,所述檢測包括基因水平的檢測和蛋白水平的檢測。如,所述基因水平的檢測包括real-timepcr法、northernblot、southernblot、基因芯片、原位雜交或rna酶保護實驗等。所述蛋白水平的檢測包括免疫檢測、westernblot或蛋白芯片等。為了簡化實驗程序,所述蛋白水平的檢測還包括蛋白檢測試劑盒,如elisa檢測試劑盒、膠體金檢測試劑盒、免疫共沉淀試劑盒、化學發光試劑盒、免疫熒光試劑盒等。所述試劑盒中一般配備有相應的使用說明書,說明書一般包括公司標志及名稱、試劑盒名稱、試劑盒組成、保質期、使用領域、使用方法等項目,用戶按照說明書不需或只需少量的優化即可得到滿意的結果。優選的,所述免疫方法為elisa法檢測和/或膠體金檢測。所述elisa法為使用elisa檢測試劑盒,所述的試劑盒是典型的夾心法酶聯免疫吸附測定試劑盒(elisa)。預先包被的抗體為多克隆抗體。檢測相抗體也為多克隆抗體,經生物素(biotin)標記。樣品和生物素標記抗體先后加入酶標板孔反應后,pbs或tbs洗滌。隨后加入過氧化物酶標記的親和素反應;經過pbs或tbs的徹底洗滌后用底物tmb顯色。tmb在過氧化物酶的催化下轉化成藍色,并在酸的作用下轉化成最終的黃色。顏色的深淺和樣品中的待測因子呈正相關。本發明的第四方面提供了所述分子標志物在篩選預防或治療腦卒中的藥物的用途。優選的,所述pigr蛋白在缺血性腦卒中生物樣品中表達上調。優選的,所述的樣品為血液,如血清、血漿或全血。本發明的第五方面提供了能夠抑制血液中pigr蛋白表達的物質在制備預防或治療腦卒中藥物中的用途。本發明的第六方面提供了用于檢測腦卒中發生的系統,該系統包括檢測pigr蛋白或其活性片段的物質。優選的,所述系統包括數據處理裝置,所述數據處理裝置內設采集比較模塊a和處理模塊b,所述采集比較模塊a的功能為:采集并比較待測者與對照者的組織樣本中所述pigr蛋白或其活性片段的表達量;所述處理模塊b的功能為根據比較的結果按照如下方法確定待測者是否為腦卒中患者:若所述待測者的組織樣本中所述pigr蛋白或其活性片段的表達量顯著高于所述對照組的組織樣本中所述pigr蛋白或其活性片段的表達量,則所述待測者為或候選為腦卒中患者;反之,則所述待測者不為或候選不為腦卒中患者;所述對照者為健康人。優選地,處理模塊b中判斷上調的標準是待測者的組織樣本中所述pigr蛋白或其活性片段的表達量比對照者至少提高30%。優選地,處理模塊b中判斷上調的標準是待測者的組織樣本中所述pigr蛋白或其活性片段的表達量比對照者至少提高60%。優選地,處理模塊b中判斷上調的標準是待測者的組織樣本中所述pigr蛋白或其活性片段的表達量比對照者至少提高90%。本發明的有益效果如下:本發明公開了一種與腦卒中相關的蛋白pigr,并進一步證實該pigr蛋白或其活性片段在腦卒中組織中表達上調。利用該蛋白檢測腦卒中不僅能夠快速有效的做到早期檢測,而且為基因治療、藥物治療等臨床應用提供了治療靶點和重要依據。附圖說明圖1本發明實施例2中的色譜圖;圖2本發明實施例3中的pigr表達量標準曲線。具體實施方式以下實施例用于說明本發明,但不用來限制本發明的范圍。若未特別指明,實施例中所用的技術手段為本領域技術人員所熟知的常規手段,所用的試劑可以商業購買得到。實施例中未注明具體條件的實驗方法,通常為本領域常規方法。本發明的發明人對6例腦卒中樣本及6例對照樣本進行高通量測序,結合生物信息學方法進行篩選,挑選出候選蛋白pigr,現有研究中并沒有pigr蛋白和腦卒中相關的報道,進一步,發明人進行了分子生物學方法驗證,證實了pigr蛋白在缺血性腦卒中組織中表達上調,其相關產品可用于診斷、治療缺血性腦卒中。本發明的pigr蛋白是在本發明之前的已知蛋白,其基本信息如下:genbank:caa51532.1本發明還采用elisa檢測試劑盒檢測上述蛋白在缺血性腦卒中和正常人群中的表達,并驗證了該蛋白為缺血性腦卒中中表達上調。本發明應用itraq聯合質譜的方法鑒定急性缺血性腦卒中患者血清中導致內皮功能紊亂的蛋白標志物。同位素標記相對和絕對定量(isobarictagsforrelativeandabsolutequantitation,itraq)技術由absciex公司研發的一種體外同種同位素標記的相對與絕對定量技術。該技術利用多種同位素試劑標記蛋白多肽n末端或賴氨酸側鏈基團,經高精度質譜儀串聯分析,可同時比較多達8種樣品之間的蛋白表達量,是近年來定量蛋白質組學常用的高通量篩選技術。itraq定量蛋白質組學是蛋白酶切后形成多肽,用itraq同位素試劑標記多肽n末端或賴氨酸側鏈基團。標記后的肽段經過液相分離,進行一級質譜和二級質譜分析,在二級質譜前,被標記的不同樣本中的同一肽段表現為相同的質荷比和其他理化性質。而在二級質譜中,信號離子表現為不同質荷比(114~121)的峰,根據波峰的高度及面積,可以鑒定出蛋白質和分析出同一蛋白質不同處理的定量信息。itraq試劑包括三部分:報告部分、肽反應部分、平衡部分。(1)報告部分有八種:113-121(無120),因此itraq試劑可同時標記8組樣品。(2)肽反應部分:能與肽段n端及賴氨酸側鏈氨基發生共價連接而標記上肽段。(3)平衡部分:保證被標記的同一肽段的質荷比相同。與傳統的雙向電泳定量分析相比,itraq具有以下技術服務優勢:(1)靈敏度高,檢測限低,可檢測出低豐度蛋白;(2)分離能力強,分析范圍廣,itraq可以對任何類型的蛋白質進行分離鑒定,包括高分子量蛋白質、酸性蛋白和堿性蛋白,膜蛋白和不溶性蛋白;(3)高通量:同時對8個樣本進行分析,提高了實驗通量,可同時對多個時間點或不同處理的蛋白質進行分析;(4)結果可靠:定性與定量分析結果更加可靠;(5)自動化程度高:液相與質譜連用,自動化操作,分析速度快,分離效果好。本發明的了pigr基因的核苷酸全長序列或其片段通常可以用pcr擴增法、重組法或人工合成的方法獲得。對于pcr擴增法,可根據已公開的有關核苷酸序列,尤其是開放閱讀框序列來設計引物,并用市售的cdna庫或按本領域技術人員已知的常規方法所制備的cdna作為模板,擴增而得到有關序列。當序列較長時,常常需要進行兩次或多次擴增,然后再將多次擴增出的片段按正確次序拼接在一起。一旦獲得了有關的序列,就可以用重組法來大批量地獲得有關序列。這通常是將其克隆入載體,再轉入細胞,然后通過常規方法從增殖后的宿主細胞中分離得到有關序列。此外,還可用人工合成的方法來合成有關序列,尤其是片段長度較短時。通常,通過先合成多個小片段,然后再進行連接可獲得序列很長的片段。目前,已經可以完全通過化學合成來編碼本發明的蛋白(或其片段,或其衍生物)的dna序列。然后可將該dna序列引入本領域中的各種dna分子(如載體)和細胞中。此外,還可通過化學合成將突變引入本發明蛋白序列中。本發明蛋白的片段除了可用重組法產生之外,還可用固相技術通過直接合成肽而加以生產(stewart等人,(1969)soliod-phasepeptidesynthesis,whfreemanco.,sanfrancisco;merrifieldj.(1963)j.amchem.soc85:2149-2154)。在體外合成蛋白質可以用手工或自動進行。例如,可以用appliedbiosystems的431a型肽合成儀(fostercity,ca)來自動合成肽。可以分別化學合成本發明蛋白的各片段,然后用化學方法加以連接以產生全長的分子。本文使用的術語“表達上調”指對應于所表達基因的序列,其中序列量的測量證明,與從正常個體或從通過腦卒中分期確定與腦卒中不同的已鑒定疾病狀態的個體中分離的生物學樣品中的同一蛋白相比,所述基因在從患腦卒中或通過腦卒中分期確定的腦卒中已鑒定疾病狀態的個體中分離的生物學樣品中的表達水平升高。根據本發明,“表達上調”是指通過本發明方法雜交強度測量的至少1%、2%、3%、4%、5%、6%、7%、8%、9%、10%或更多的表達升高,例如20%、30%、40%、50%、60%、70%、80%、90%或更高。本文使用的術語“表達水平”指通過本領域技術人員已知和本文所述的方法測定的給定核酸或蛋白質的可測量。涉及本發明分子標志物對應的rna、hnrna、mrna或mrna剪接變體時,表達水平可以通過雜交或更多定量測量來測定,例如包括使用sybr綠、taqman和分子信標技術的定量實時rtpcr。本文使用的“對照”指未顯示任何oa癥狀并且未診斷為腦卒中或oa的個體或個體組。優選地,所述對照個體未使用影響oa的藥物,并且未診斷為患有任何其他疾病。更優選地,對照個體具有與測試樣本相比相似的性別、年齡和體重指標(bmi)。根據本發明,“對照”還指分離自正常個體的樣品,包括分離自正常個體的總rna或mrna。取自對照個體的樣品可包括分離自樣本組織的rna,其中rna分離自樣本組織,所述樣本組織分離自組織移除時未診斷為oa并且未顯示任何oa癥狀的個體。本發明的生物學樣品血在本發明的一個方面中,根據本領域熟知的方法從受試者中獲得血樣。可以使用本領域技術人員已知的技術(特別是已知的采血方法)從受試者的任何身體部位(如指、手、腕、臂、腿、足、踝、胃和頸)取血。在一個具體的實施方案中,從受試者獲得靜脈血并根據本發明方法使用。可以使用真空管、注射器或蝶形針取血。采血量將取決于采血部位、本發明方法需要的量和受試者的舒適度而變化。如在多個具體的實施方案中,從受試者收集0.001ml、0.005ml、0.01ml、0.05ml、0.1ml、0.15ml、0.2ml、0.25ml、0.5ml、0.75ml、1ml、1.5ml、2ml、3ml、4ml、5ml、10ml、15ml或更多血。將血保存在k3/edta管中。在一個方面中,根據本領域熟知的采血方法從正常個體或者從診斷為患腦卒中或懷疑患腦卒中的個體取全血。全血包括可直接使用的血,并包括已經根據本領域熟知的方法(例如優選在300-800×g溫和離心5-10分鐘)除去血清或血漿并且已經從剩余血樣中分離了rna或mrna的血。在一個具體的實施方案中,將得自受試者的全血(即未分級血)與裂解緩沖液(如裂解緩沖液(1l):0.6gedta;1.0gkhco2,8.2gnh4cl,用naoh調整至到ph7.4)混合,離心樣品并保留細胞沉淀,根據本領域熟知的方法提取rna或mrna(“裂解血”)(參閱如sambrook等)。優選使用全血,因為它避免了昂貴耗時的分離血中細胞類型的步驟(kimoto,1998,mol.gen.genet258:233-239;chellyj等,1989,proc.nat.acad.sci.usa86:2617-2621;chellyj等,1988,nature333:858-860)。在本發明的一些實施方案中,將收集自受試者的全血進行分級(即分離成組分)。在本發明的一個具體實施方案中,使用本領域已知技術從收集自受試者的全血分離血細胞。例如,可以對收集自受試者的血進行ficoll-hypaque(pharmacia)梯度離心。這種離心將紅細胞(血紅細胞)與各種類型的有核細胞和血漿分離開。具體地,ficoll-hypaque梯度離心可用于分離外周血白細胞(pbl),它們可根據本發明方法使用。其他全血分離方法按照本領域技術人員所熟知的方法進行操作。在根據本發明方法使用前,任選地(但優選)將收集的生物學樣品保存在低溫如4℃下。在一些實施方案中,在第一時間根據本發明方法使用樣品的一部分,而將一個或多個剩余的樣品部分保存一段時間以備后用。該段時間可以是1小時或更長、1天或更長、1周或更長、1月或更長、1年或更長或不確定。就長期保存而言,可以使用本領域熟知的保存方法,例如在冷凍溫度(如低于-80℃)保存。在一些實施方案中,作為保存樣品的補充或替代,將分離的核酸或蛋白質保存一段時間(如1小時或更長、1天或更長、1周或更長、1月或更長、1年或更長或不確定)以備后用。實施例1樣本的收集取2015年06月到2015年12月期間在解放軍火箭軍總醫院就診缺血性腦卒中患者,病例組共收集6例,對照來源于同時期來解放軍火箭軍總醫院體檢但各項指標均正常的健康志愿者,共收集6例,具體信息如表1所示。獲取所有研究對象的肘正中靜脈血,5ml,4度冰箱靜置1h,離心1500rpm、10min,取上清,離心1500rpm、10min,取上清,分裝保存于-80度冰箱。表1樣本信息因素病例組對照組平均年齡61.6760.67性別6男3男,3女平均bmi25.2268423.14447吸煙3是,2否,1已戒6否飲酒2是,3否,1已戒6否糖尿病6否6否高血壓6是6否冠心病6否6否凝血1高凝,5正常6正常實施例2itraq實驗篩選差異蛋白一、所用儀器和試劑渦旋振蕩器(海門市其林貝爾儀器制造有限公司,型號:ql-901)恒溫孵浴器(上海浦東榮豐科學儀器有限公司,型號:hh.s4)真空冷凍干燥機(thermo,型號:spd2010-230)rigoll-3000高效液相色譜系統(北京普源精電科技有限公司),流動相a:98%ddh2o,2%乙腈(ph10);流動相b:98%乙腈,2%ddh2o(ph10)高效液相色譜儀:(thermoscienticeasy-nlc1000system(nanohplc)),流動相a:100%超純水,0.1%甲酸;流動相b:100%乙腈,0.1%甲酸質譜系統(thermo,型號:q-exactive)blue白蛋白igg去除試劑盒(sigma-aldrich,貨號:protba-1kt)dtt(bio-rad,貨號:161-0611,美國)碘乙酰胺(bio-rad,貨號:163-2109,美國)試劑盒中的dissolutionbuffer(absciex,pn:4381664)胰酶(promega,貨號:v5111,美國)10k超濾管(milipore,pn:ufc5010bk)8標試劑盒(absciex,pn:4390812,pn:4381664ziptip(millipore,pn:ztc18m096(2μg))色譜柱:durashell-c18,4.6mm×250mm,5μm,(agela,貨號:dc952505-0)乙腈(merck,貨號:100030,德國)氨水(sigma-aldrich,貨號:17837,美國)二、itraq定量實驗流程2.1樣本蛋白處理2.11、平衡柱子1)緩慢顛倒培養液,渦旋混勻培養液;2)取0.4ml培養液到柱子中,保證培養液是混勻的;3)將柱子放入2ml收集管中,以10000rpm(8000g)的速度離心5-10s;4)加0.4ml平衡緩沖液到柱子中,以10000rpm(8000g)的速度離心5-10s,將2ml收集管中的緩沖液倒掉,并將柱子再次放到原來的2ml離心管中;5)再加0.4ml平衡緩沖液到柱子中,以10000rpm(8000g)的速度離心20-40s,將2ml收集管中的緩沖液倒掉,并將柱子放到一個新的2ml離心管中。2.12、去除血清中的白蛋白和免疫球蛋白g(igg)1)加25-100ul血清樣本到處理過的柱子中,并在室溫下孵育5-10min;2)離心柱子和收集管,10000-12000rpm(8000-12000g)*60s;3)再將收集管中的洗出液加入到柱子中,室溫下孵育5-10min;這一步去除了超過5%的白蛋白;4)在同一個收集管中離心柱子10000-12000rpm(8000-12000g)*60s;5)經過兩次洗脫留在收集管中的血清與第六步清洗步驟的液體混合;6)洗脫柱子中殘余未綁定蛋白:柱子中加入100ul平衡緩沖液,離心;10000-12000rpm(8000-12000g)*60s,將第4、6兩步驟收集管中得到的液體混合;7)去除白蛋白和igg的血清可在-20℃長期貯存。2.2bradford法蛋白定量采用bradford法[marionm.bradford.analyticalbiochemistry,1976,72:248-254]測定樣本提取的蛋白濃度。得到各樣品蛋白濃度(見表2)表2蛋白樣品濃度2.3蛋白酶解(filteraidedsamplepreparation,fasp)1)蛋白定量后取200μg蛋白溶液置于離心管中;2)加入終濃度25mmdtt,60度反應1小時;3)加入終濃度50mm碘乙酰胺,室溫10分鐘;4)將還原烷基化后的蛋白溶液加入10k的超濾管中,12,000轉離心20分鐘,棄掉收集管底部溶液;5)加入itraq試劑盒中的dissolutionbuffer100μl,12,000轉離心20分鐘,棄掉收集管底部溶液,重復3次;6)更換新的收集管,在超濾管中加入胰蛋白酶,總量4μg(與蛋白質量比1:50),體積50μl,37攝氏度反應過夜;7)次日,12,000轉離心20分鐘,酶解消化后的肽段溶液離心于收集管底部;8)在超濾管中加入50μldissolutionbuffer,12,000轉再次離心20分鐘,與上步合并,收集管底部共得到100μl酶解后的樣品。2.4itraq標記1)從冰箱中取出itraq試劑,平衡到室溫,將試劑離心至管底;2)向每管試劑中加入150μl異丙醇,渦旋振蕩,離心至管底;2)取50μl樣品(100μg酶解產物)轉移到新的離心管中;4)將itraq試劑填加到樣品中,渦旋振蕩,離心至管底,室溫反應2小時;5)加入100μl水終止反應;6)為了檢測標記效率及定量準確性,從4組樣品中各取出1μl混合,用ziptip脫鹽后進行maldi-tof-tof(absciex4800plus)鑒定,確認標記反應良好;7)混合標記后的樣品,渦旋振蕩,離心至管底;8)真空冷凍離心干燥;9)抽干后的樣品冷凍保存待用;10)酶解肽段離線預分離及lc-ms/ms質譜分析。2.5高ph條件下的反相色譜分離1)混合標記后的樣品用100μl流動相a溶解,14000g離心20min,取上清待用;2)使用400μg酶解好的bsa進行分離(柱溫45℃,檢測波長214nm),檢測系統情況;3)取100μl準備好的樣本上樣;4)流速0.7ml/min,分離梯度如表3所示,色譜圖如圖1所示。表3反相色譜分離梯度2.6納升級反相色譜-qexactive進行蛋白質分析1)將高ph反相分離得到的組份用20μl2%甲醇,0.1%甲酸復溶;2)12,000轉離心10分鐘,吸取上清上樣;3)上樣體積10μl,采取夾心法上樣;4)loadingpump流速350nl/min,15分鐘;5)分離流速300nl/min,分離梯度如表4所示。表4納升級反相色譜分離梯度三、質譜數據分析和結果數據庫的選擇是以所需物種、數據庫注釋完備性及序列可靠性為參考依據的。在本次實驗中選擇的數據庫來自uniprot(http://www.uniprot.org/),數據庫本版為:uniprot_susscrofa_201510.fasta。itraq的質譜分析是由thermoq-exactive型質譜完成,產生的質譜原始文件*.raw采用thermo公司的配套商用軟件proteomediscoverer1.4處理。本次itraq實驗共鑒定到272個總蛋白,其分析到差異蛋白14個。為了更好的理解差異蛋白的功能,我們對差異蛋白進行了geneonlogy和信號通路分析,并對差異蛋白進行功能注釋和蛋白質互相作用網絡分析,鑒于以上數據分析的結果,結合文獻我們篩選了差異蛋白pigr,該蛋白在缺血性腦卒中樣本中表達上調。實施例3大樣本驗證差異蛋白pigr的表達1、取樣取2015年06月到2016年12月期間在解放軍火箭軍總醫院就診缺血性腦卒中患者,病例組共收集30例,記a組分別標號為a1-a30,對照來源于同時期來解放軍火箭軍總醫院體檢但各項指標均正常的健康志愿者,共收集10例,記b組分別標號為b1-b10。獲取所有研究對象的肘正中靜脈血,5ml,4度冰箱靜置1h,離心1500rpm、10min,取上清,離心1500rpm、10min,取上清,分裝保存于-80度冰箱。2、實驗過程實驗選用人多聚免疫球蛋白受體(pigr)elisa試劑盒(購買自上海康朗生物科技有限公司)該檢測試劑盒操作步驟如下:(1)標準品的稀釋每瓶標準品加入標準品稀釋液1ml,蓋好后室溫靜置大約10分鐘,同時反復顛倒/搓動以助溶解,其濃度為200ng/ml。準備7個稀釋標準品的ep管,每個ep管中加入150μl的標準品稀釋液,稀釋成不同的梯度,標準品稀釋液(0pg/ml)直接作為空白孔。根據預實驗結果判定每個樣品需分別稀釋200倍。(2)加樣:分別設空白孔(空白對照孔不加樣品及酶標試劑,其余各步操作相同)、標準孔、待測樣品孔。在酶標包被板上標準品準確加樣50μl,待測樣品孔中先加樣品稀釋液40μl,然后再加待測樣品10μl(樣品最終稀釋度為5倍)。加樣將樣品加于酶標板孔底部,盡量不觸及孔壁,輕輕晃動混勻。(3)溫育:用封板膜封板后置37℃溫育30分鐘。(4)配液:將20倍濃縮洗滌液用蒸餾水20倍稀釋后備用(5)洗滌:小心揭掉封板膜,棄去液體,甩干,每孔加滿洗滌液,靜置30秒后棄去,如此重復5次,拍干。(6)加酶:每孔加入酶標試劑50μl,空白孔除外。(7)溫育:操作同3。(8)洗滌:操作同5。(9)顯色:每孔先加入顯色劑a50μl,再加入顯色劑b50μl,輕輕震蕩混勻,37℃避光顯色15分鐘.(10)終止:每孔加終止液50μl,終止反應(此時藍色立轉黃色)。(11)測定:以空白空調零,450nm波長依序測量各孔的吸光度(od值)。測定應在加終止液后15分鐘以內進行。3、結果獲得標準品的od值,如表5所示,制作的標準曲線如圖2所示。實驗得到了30個樣本的od值,根據標準曲線,計算樣品中pigr的濃度,其結果如表6所示。其中,樣品的od值為三個副孔去背景后的od均值。根據od均值,計算標準品的濃度c0,按照稀釋倍數200倍相乘,計算實際濃度c1=c0*200。統計學分析表6中數據,可知a組樣本濃度值為81.021±6.144,b組樣本的濃度值為62.895±5.615;a、b兩組樣本進行兩獨立樣本t檢驗統計學分析,差異具有統計學意義(p<0.0001),上述結果表明,pigr蛋白在缺血性腦卒中樣本中表達水平明顯升高。表57個標準品的od值標準品12345678濃度(ng/ml)0.0001.5633.1256.2512.52550100od值0.0620.1230.1340.1560.2280.3600.5731.103表6樣品和對照的od值和濃度值a組a1a2a3a4a5a6a7a8a9a10od均值0.8760.7980.8950.9230.8150.8630.8920.9520.8910.941c0(ng/ml)77.79570.03379.68682.47371.72576.50179.38785.36179.28884.266c1(μg/ml)15.55914.00715.93716.49514.34515.30015.87717.07215.85816.853a組a11a12a13a14a15a16a17a18a19a20od均值0.7960.9950.9540.9860.9620.9810.8670.8980.9650.989c0(ng/ml)69.83489.64385.56088.74786.35788.24976.89979.98586.65589.046c1(μg/ml)13.96717.92917.11217.74917.27117.65015.38015.99717.33117.809a組a21a22a23a24a25a26a27a28a29a30od均值0.9480.8950.9450.9070.8860.7810.8250.9480.9860.892c0(ng/ml)84.96379.68684.66480.88178.79068.34272.72084.96388.74779.387c1(μg/ml)16.99315.93716.93316.17615.75813.66814.54416.99317.74915.877a組b1b2b3b4b5b6b7b8b9b10od均值0.7180.7850.6300.7680.7660.6670.7750.6570.7700.726c0(ng/ml)62.07768.74053.32967.04966.85057.00767.74656.01367.24862.895c1(μg/ml)12.41513.74810.66613.41013.37011.40113.54911.20313.45012.579實施例4elisa評價腦卒中的治療效果樣本選用實施例1中的6例缺血性腦卒中病人,pigr蛋白的elisa操作同實施例3,治療前檢測血清中pigr蛋白水平,跟蹤隨訪這6位患者,療程結束后再檢測血清中pigr蛋白水平,對比血清中pigr蛋白含量變化,具體pigr蛋白的表達水平參見表7。從表7中pigr含量變化與治療效果的比較可以看出,臨床治療效果越顯著的患者,其血清中pigr蛋白水平降低的越多;臨床治療效果不明顯的患者,其血清中pigr蛋白水平無明顯變化。該結果表明,檢測血清中pigr蛋白水平可對缺血性腦卒中治療效果進行評估,即pigr蛋白在評估腦卒中的治療效果或者判斷腦卒中的預后產品中有應用前景。表7臨床檢測缺血性腦卒中治療前后pigr水平由此證明,本發明的試劑盒利用pigr蛋白檢測腦卒中不僅能夠快速有效的做到早期檢測,也能夠有效的評價腦卒中的治療效果。雖然,上文中已經用一般性說明及具體實施方案對本發明作了詳盡的描述,但在本發明基礎上,可以對之作一些修改或改進,這對本領域技術人員而言是顯而易見的。因此,在不偏離本發明精神的基礎上所做的這些修改或改進,均屬于本發明要求保護的范圍。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1
- 一種基于圖像信息的缺血性腦卒中治療監測系統的制作方法
- miR-106b-5p及其檢測引物和其反義核苷酸序列在診斷、治療缺血性腦卒中領域中的應用
- 一種輔助診斷急性缺血性腦卒中的早期生物標志物及其基因芯片和實時熒光定量pcr評 ...的制作方法
- 一種治療髓海不足型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 一種用于治療缺血性腦卒中的藥物組合物的制作方法
- 用于治療和預防腦卒中或缺血、阿爾茨海默病和帕金森病和肌萎縮性側索硬化的甾族硝酮的制作方法
- 一種治療脾腎兩虛型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 缺血性腦卒中診斷標記物的制作方法
- 缺血性腦卒中miRNA標記物的制作方法
- 一種治療瘀血內阻型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 一種基于圖像信息的缺血性腦卒中治療監測系統的制作方法
- miR-106b-5p及其檢測引物和其反義核苷酸序列在診斷、治療缺血性腦卒中領域中的應用
- 一種輔助診斷急性缺血性腦卒中的早期生物標志物及其基因芯片和實時熒光定量pcr評 ...的制作方法
- 瓜蔞桂枝湯在制備治療缺血性腦卒中后遺癥藥物中的應用
- 一種治療髓海不足型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 一種用于治療缺血性腦卒中的藥物組合物的制作方法
- 用于治療和預防腦卒中或缺血、阿爾茨海默病和帕金森病和肌萎縮性側索硬化的甾族硝酮的制作方法
- 一種治療脾腎兩虛型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 缺血性腦卒中診斷標記物的制作方法
- 缺血性腦卒中miRNA標記物的制作方法
- 一種基于圖像信息的缺血性腦卒中治療監測系統的制作方法
- miR-106b-5p及其檢測引物和其反義核苷酸序列在診斷、治療缺血性腦卒中領域中的應用
- 一種輔助診斷急性缺血性腦卒中的早期生物標志物及其基因芯片和實時熒光定量pcr評 ...的制作方法
- 瓜蔞桂枝湯在制備治療缺血性腦卒中后遺癥藥物中的應用
- 一種治療髓海不足型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 一種用于治療缺血性腦卒中的藥物組合物的制作方法
- 用于治療和預防腦卒中或缺血、阿爾茨海默病和帕金森病和肌萎縮性側索硬化的甾族硝酮的制作方法
- 一種治療脾腎兩虛型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 缺血性腦卒中診斷標記物的制作方法
- 缺血性腦卒中miRNA標記物的制作方法
- 一種基于圖像信息的缺血性腦卒中治療監測系統的制作方法
- miR-106b-5p及其檢測引物和其反義核苷酸序列在診斷、治療缺血性腦卒中領域中的應用
- 一種輔助診斷急性缺血性腦卒中的早期生物標志物及其基因芯片和實時熒光定量pcr評 ...的制作方法
- 瓜蔞桂枝湯在制備治療缺血性腦卒中后遺癥藥物中的應用
- 一種治療髓海不足型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 一種用于治療缺血性腦卒中的藥物組合物的制作方法
- 用于治療和預防腦卒中或缺血、阿爾茨海默病和帕金森病和肌萎縮性側索硬化的甾族硝酮的制作方法
- 一種治療脾腎兩虛型缺血性腦卒中后血管性癡呆的中藥組合物的制作方法
- 缺血性腦卒中診斷標記物的制作方法
- 缺血性腦卒中miRNA標記物的制作方法
- 一種用于缺血性腦卒中后神經再生的藥物組合物及其應用的制作方法與工藝
- 一種與抗血小板藥物氯吡格雷治療缺血性腦卒中相關的SNP標志物及其應用的制作方法與工藝
- Nur77在制備改善缺血性腦卒中預后藥物中的應用的制作方法與工藝
- 一種缺血性腦卒中治療藥物的制作方法與工藝
- 反式肉桂醛制備治療缺血性腦卒中的藥物的用途的制作方法與工藝
- LINC01094在診治缺血性腦卒中的應用的制造方法與工藝
- 一種檢測缺血性腦卒中的生物標志物及其應用的制造方法與工藝
- 與缺血性腦卒中組織特異性結合的HGG多肽及其應用的制造方法與工藝
- 一種檢測缺血性腦卒中的分子標志物及其用途的制造方法與工藝
- 肉蓯蓉多糖制備治療缺血性腦卒中的藥物的用途的制造方法與工藝