一種有機熒光顏料及其制備方法與流程
本發明涉及一種有機熒光顏料及其制備方法。
背景技術:
有機熒光顏料作為高性能顏料的主要品種之一,可用于紡織品和塑料制品的著色、熒光墨水、道路標示、國防工業中火箭、軍艦和其它裝備的探傷、以及生物及醫學方面的熒光示蹤(何建偉,楊少平,張旭強;熒光顏料及其應用;杭州科技,2003,(3),43–44)。
香豆素類化合物特別是具有推-拉體系的香豆素衍生物往往表現出很強的熒光,適于作為熒光顏料。但目前現有的制備方法合成的作為熒光顏料的香豆素類化合物熒光性能一般。因此,有必要提出有效的技術方案,解決上述問題。
技術實現要素:
本發明所要解決的技術問題是提供一種有機熒光顏料及其制備方法。該方法反應簡單,原料廉價易得。
本發明解決上述技術問題的技術方案如下:
一種有機熒光顏料,所述有機熒光顏料為如式ii所示的3-三氟乙酰基-7-羥基香豆素:
本發明還提供一種有機熒光顏料的制備方法,包括如下步驟:
(1)將原料2,4-二羥基苯甲醛、三氟乙酰乙酸乙酯以及堿溶解于乙醇或乙腈中,加熱至80℃回流反應6h,反應結束后將溶液冷卻至室溫,過濾出固體產物,經水洗和干燥,得到中間體2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃;
(2)將所述2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃和對甲苯磺酸加入到氯苯或二甲苯中,加熱至130℃回流反應4h,然后將反應混合物冷卻至室溫,過濾出固體產物并進行干燥,得到本發明3-三氟乙酰基-7-羥基香豆素有機熒光顏料。
優選的,步驟(1)中所述堿為哌啶、三乙胺或哌啶-乙酸。
優選的,步驟(1)中所述2,4-二羥基苯甲醛和所述三氟乙酰乙酸乙酯的摩爾比為1:1~1:1.2,最好為1:1.1。
優選的,步驟(1)中所述2,4-二羥基苯甲醛和所述堿的摩爾比為2.5:1~10:1,最好為4:1。
優選的,步驟(1)中所述2,4-二羥基苯甲醛和三氟乙酰乙酸乙酯的總質量占所述乙醇或乙腈的比例為1g:10ml~1g:25ml,最好為1g:14ml。
優選的,步驟(2)中所述2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃和所述對甲苯磺酸的摩爾比為50:1~200:1,最好為100:1。
優選的,步驟(2)中所述2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃與所述氯苯或二甲苯的比例為1g:20ml~1g:50ml,最好為1g:33ml。
有益效果:該化合物結構簡單、制備方便,而且在紫外光照射下顯示出強烈的藍紫色熒光。本發明3-三氟乙酰基-7-羥基香豆素中由于在3和7位分別含有強吸電子基和強供電子基,構成典型的推-拉體系,因此熒光性增強。
附圖說明
圖1為本發明實施例1的中間體2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃的紅外光譜圖;
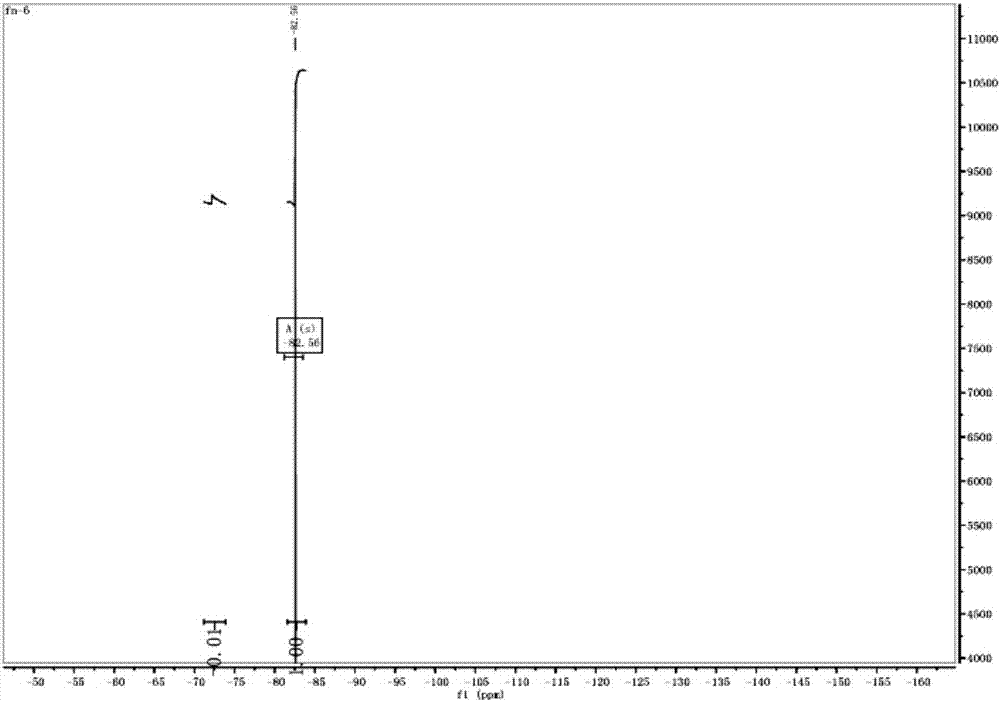
圖2為本發明實施例1的3-三氟乙酰基-7-羥基香豆素的核磁共振氟譜。
具體實施方式
本發明從原料2,4-二羥基苯甲醛和三氟乙酰乙酸乙酯出發,以乙醇或乙腈為溶劑,在堿的存在下發生knoevenagel縮合反應,生成中間體2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃(以下簡稱化合物1);該化合物1在對甲苯磺酸催化下,在氯苯或二甲苯中進行熱重排,生成3-三氟乙酰基-7-羥基香豆素有機熒光顏料(以下簡稱fp2)。所合成的有機熒光顏料fp2可用于熒光油墨、道路或物品標示以及紡織品著色。
本發明的合成路線為:
本發明原料用2,4-二羥基苯甲醛亦可是其它水楊醛類化合物,其與三氟乙酰乙酸乙酯發生knoevenagel縮合反應,得到與化合物1同類結構的中間體;再以對甲苯磺酸為催化劑進行熱重排,可以制得其它具有與fp2類似結構的香豆素類有機熒光顏料。但三氟乙酰基相較乙酰基吸電子能力顯著增強,其熒光強度增大1倍。
本發明制備方法簡便,反應步驟少,原料廉價易得,制備成本低,對環境友好,而且具有很大的結構調節空間,可望產生良好的社會和經濟效益,所合成的新的有機熒光顏料fp2可能用于熒光油墨、道路或物品標示以及紡織品著色。
下面結合具體實施例,進一步闡述本發明。應理解,這些實施例僅用于說明本發明而不用于限制本發明的范圍。此外應理解,在閱讀了本發明講授的內容之后,本領域技術人員可以對本發明作各種改動或修改,這些等價形式同樣落于本申請所附權利要求書所限定的范圍。
實施例1
(1)化合物1的合成:在三頸瓶中加入2,4-二羥基苯甲醛(1.38g,10mmol)、三氟乙酰乙酸乙酯(2.11g,11mmol)和哌啶(215mg,2.5mmol),攪拌下溶解于乙醇(50ml)中,加熱至80℃回流反應6h,反應結束后將溶液冷卻至室溫,過濾出固體產物,經水洗后,在真空干燥箱中50℃下干燥2h,得到1.93g白色固體粉末化合物1,產率為63%,圖1為本發明實施例1的中間體2,7-二羥基-2-三氟甲基-3-乙氧羰基-2h-苯并吡喃的紅外光譜圖。
mp:113-115℃。
ir(kbr)ν=3326,2919,2854,1698,1574,1507,1222,1187,1175,1086cm-1。
1hnmr(400mhz,dmso-d6)δ=7.87(s,1h),7.34(d,j=8.4hz,1h),6.48(dd,j=8.3,1.8hz,1h),6.36(s,1h),4.18(q,j=7.1hz,2h),1.25(t,j=7.1hz,3h)。
13cnmr(101mhz,dmso-d6)δ=163.79(c=o),154.44(ph-c),139.74(ph-c),131.47(=ch),124.46(=c),121.57(ph-c),114.32(cf3),111.51(ph-c),111.18(ph-c),109.23(ph-c),102.45(ph-c),96.92(o-c-oh),60.59(och2),14.58(ch3).
19fnmr(377mhz,dmso-d6)δ=-82.19(cf3)。ms(esi):m/z303.19(m+-1)。
(2)fp2的合成:在100ml三頸瓶中加入化合物1(1.52g,5mmol)和對甲苯磺酸(p-tsoh,10mg,0.05mmol),然后加入50ml氯苯作為溶劑,升溫至大約130℃回流反應4h,得到橘黃色溶液,冷卻至室溫后,有固體析出,過濾出固體產物,在真空干燥箱中50℃下干燥2h,得到1.19g淡黃色粉末狀固體熒光顏料fp2,產率為92%。圖2為本發明實施例1的3-三氟乙酰基-7-羥基香豆素的核磁共振氟譜。
mp:214-216℃。
ir(kbr)ν=3458,2998,2945,2917,2847,1732,1638,1433,1364,1315,1215,1163,1029,900cm-1。
1hnmr(400mhz,dmso-d6)δ=11.56(s,1h),8.85(s,1h),7.92(d,j=8.7hz,1h),6.92(dd,j=8.6,2.1hz,1h),6.79(d,j=1.7hz,1h)。
13cnmr(101mhz,dmso-d6)δ=177.82(c=o),166.73(oc=o),158.55(ph-c),156.64(ph-c),153.17(=ch),134.23(=c),115.31(cf3),113.30(ph-c),111.04(ph-c),102.49(ph-c)。
19fnmr(377mhz,dmso-d6)δ=-72.25(cf3)。
ms(esi):m/z257.16(m+-1)。
實施例2
實施例2與實施例1的制備方法相同。不同之處僅在于,實施例2中步驟(1)化合物1的合成時所選用的堿不是哌啶,而是三乙胺(253mg,2.5mmol)。
實施例2得到的化合物1的產率為43%。
實施例3
實施例3與實施例1的制備方法相同。不同之處僅在于,實施例3中步驟(1)化合物1的合成時所選用的堿不是哌啶,而是哌啶-乙酸(363mg,2.5mmol)。
實施例3得到的化合物1的產率為49%。
實施例4
實施例4與實施例1的制備方法相同。不同之處僅在于,實施例4中步驟(1)化合物1的合成時所選用的溶劑不是乙醇,而是乙腈(50ml)。
實施例4得到的化合物1的產率為54%。
實施例5
實施例5與實施例1的制備方法相同。不同之處僅在于,實施例5中步驟(2)fp2的合成時所選用的溶劑不是氯苯,而是二甲苯(50ml)。
實施例5得到的fp2的產率為26%。
本發明可用其他的不違背本發明的精神或主要特征的具體形式來概述。因此,無論從哪一點來看,本發明的上述實施方案都只能認為是對本發明的說明而不能限制本發明,權利要求書指出了本發明的范圍,而上述的說明并未指出本發明的范圍,因此,在與本發明的權利要求書相當的含義和范圍內的任何改變,都應認為是包括在本發明的權利要求書的范圍內。
- 還沒有人留言評論。精彩留言會獲得點贊!