吲哚菁化合物、其合成及精制法、診斷用組合物、生物體內動態測定裝置及循環可視化裝置的制作方法
本專利申請是申請號為201180006735.x、申請日為2011年1月28日、發明名稱為“新吲哚菁化合物、其合成法及其精制法、使用該吲哚菁化合物的診斷用組合物、使用該診斷用組合物的生物體內動態測定裝置以及循環可視化裝置”的專利申請的分案申請。本發明涉及一種屬于對醫療診斷技術、醫療外科手術技術、科學測定分析技術、印刷技術、筆記技術、涂裝技術、染料技術、染色技術有用的綠色色素,且具有發出近紅外熒光的性質的新吲哚菁(indocyanine)化合物、其合成法及其精制法以及診斷用組合物。詳細而言,涉及一種屬于綠色色素且具有發出近紅外熒光的性質的環狀糖鏈環糊精結合吲哚菁化合物、其合成法及其精制法、使用該吲哚菁化合物的診斷用組合物、使用該診斷用組合物的生物體內動態測定裝置以及循環可視化裝置。
背景技術:
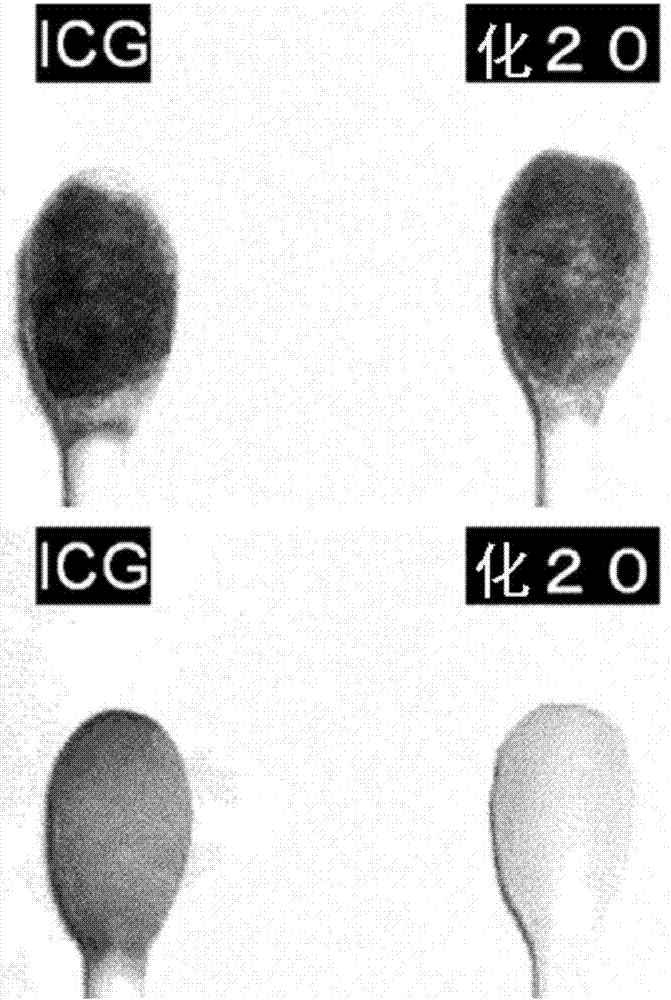
:迄今為止已合成了各種各樣的屬于綠色色素的發出近紅外熒光的吲哚菁化合物,例如,它們在醫療領域中作為眼玻璃體手術用染色用色素,肝功能檢查藥用色素,循環功能檢查藥用色素,外科手術用色素,外科手術用近紅外熒光化合物,在科學領域中作為蛋白質、糖等的染色或熒光化用化合物,在印刷技術中作為色素,具有廣泛的用途。在這些吲哚菁化合物中,被稱為吲哚菁綠(以下,略記為「icg」)的化合物作為肝功能檢查藥及循環功能檢查藥已被使用將近50年。近幾年,作為icg的用途,除了肝功能檢查藥及循環功能檢查藥以外,已嘗試利用icg的從生物體組織的光透過性高這一性質,向體內,例如血管、淋巴管、腦、眼、胃、乳房、食道、皮膚或其他部位,局部地給藥icg,通過觀察icg的近紅外熒光來進行醫療手術及醫療診斷(非專利文獻1)。在先技術文獻非專利文獻非專利文獻1:“icg熒光navigationsurgery的全部”,草野滿夫監制·編輯,インターメディカ社,(2008年11月發行).非專利文獻2:“(商品名)diagnogreen注射用25mg”(第一三共株式會社)的附帶說明書所記載的因特網主頁的url(https://www.daiichisankyo.co.jp/med/contents/di/dg2/pi/pdf/pi_dg2_0909.pdf)非專利文獻3:r.c.benson,h.a.kues,phys.med.biol.,23,159-163(1978).非專利文獻4:s.yoneyama,t.saito,y.komatsu,i.koyama,k.takahashi,j.duvoll-young,iovs,37,1286-1290(1998).非專利文獻5:y.ye,w.p.li,c.j.anderson,j.kao,g.v.nikiforovich,s.achilefu,j.am.chem.soc.,125,7766-7767(2003).非專利文獻6:k.teranishiands.tanabe,itelettersonbatteries,newtechnologies&medicine,1,53-60(2000).非專利文獻7:michaelo’shaughnessyetal:1994wiley-liss,incmicrosurgery15:40s4121994.非專利文獻8:ralphj.p.metal:1997wiley-liss,inc.microsurgery17:402-4081996.技術實現要素:技術問題然而,icg的綠色發色團(呈綠色所需的化學結構體)及近紅外熒光團(發出近紅外熒光所需的化學結構體)是疏水性的,為了使其溶于水在側鏈末端結合磺酰基。因此在現有的icg中存在如下的諸多問題。在醫療上的icg制劑的一般使用中,對icg25mg加蒸留水約5ml~10ml,振動攪拌溶解。icg未能完全溶解的情況下有可能出現惡心,干嘔,發熱,休克等癥狀(非專利文獻2)。另外,因為不溶解,所以不能用生理食鹽水等其他的水溶液進行初期溶解(非專利文獻2)。icg由于如上所述結合有磺酰基所以具有水溶性,但化學結構上疏水性烴基多而具有表面活性,所以具有產生向脂質的吸附的性質。因此,注入到血管、臟器等的生物體組織中時,有時通過附著到注入部位、或誤漏、或逆流而附著到非目標生物體組織上。附著于生物體組織的icg,難以通過擦拭操作、吸取操作從生物體組織除去,有可能成為外科手術、醫療診斷的障礙。icg在水溶液中具有分子締合性質。其作為1個原因,在水溶液中的熒光強度低(非專利文獻3、4)。另外,icg在水中溶解后隨著時間變為不溶,難以作為水溶液長期保存,而且低溫凍結保存會助長不溶解。另外,在icg制劑中含有5%以下的nai,根據情況還存在有可能引起碘過敏癥的問題(非專利文獻2)。另外,icg在靜脈注射時,迅速集積在肝臟被肝排泄,因此其他的器官,例如腎臟、輸尿管、膀胱、尿道、心臟、肺等器官的熒光攝像較困難。另外,icg在靜脈注射時隨血液移動,所以向末梢組織的移動少,難以觀測向間質的移動。本發明以解決如上述的現有的icg的問題為目的。即,以提供一種屬于綠色色素的可發出近紅外熒光的新吲哚菁化合物為目的,其特征為在水或生理食鹽水中的溶解性高,容易從生物體組織除去,水溶液中的分子締合性低,在水溶液中的近紅外熒光強度高,對肝臟以外的器官,例如腎臟、輸尿管、膀胱、尿道、心臟、肺也能進行熒光攝像。另外,提供具有該特征的新吲哚菁化合物的化學合成法以及它的精制法。并且,提供含有上述新吲哚菁化合物的診斷用組合物也屬于所要解決的課題。另外,以提供通過利用這些診斷用組合物而能對與生物體內水分平衡等相關的新吲哚菁化合物體內動態進行評價的生物體內動態測定裝置,以及,使生物體中的血液、淋巴液、尿及其他水分的循環可視化的方法和裝置為課題。解決問題的技術方案本發明人為了解決上述課題經反復潛心研究的結果,發現了可發出近紅外熒光的化合物,其可使用于利用發出近紅外熒光性質的外科手術和醫療診斷中,從而解決了上述的icg的問題。即,發現了一種新吲哚菁化合物,其特征為屬于綠色色素且發出近紅外熒光,在水或生理食鹽水中的溶解性高,容易從生物體組織除去,水溶液中的分子締合低,水溶液中的近紅外熒光強度高,從而完成了本發明。而且還發現了該新吲哚菁化合物的化學合成方法以及精制方法,從而完成了本發明。并且得以提供含有上述新吲哚菁化合物的診斷用組合物。進而得以提供通過利用該診斷用組合物而即使在靜脈給藥時也能對肝臟以外的器官進行熒光攝像的方法。并且,得以提供對與生物體內水分平衡等相關的新吲哚菁化合物體內動態進行評價的方法和生物體內動態測定裝置,以及,使生物體中的血液、淋巴液、尿以及其他水分的循環可視化的方法和裝置。本發明的第一個新吲哚菁化合物是向icg的綠色發色團(呈綠色所需的化學結構體)和近紅外熒光團(發出近紅外熒光所需的化學結構體)使環狀糖鏈環糊精共價結合的化合物。另外,本發明的第二個新吲哚菁化合物的特征是通過在環糊精的空洞內包合屬于吲哚菁結構的疏水性部位的萘基部位,從而用親水性的葡萄糖基披覆屬于疏水性部位的萘基部位,使吲哚菁分子結構的大部分區域成為三維性親水性。因此,相對于icg所具備的因同時具有疏水性部位和磺酰基的親水性帶來的類似表面活性的性質的特征,本發明的化合物的特征為其分子內的疏水性部位被環糊精披覆,所以沒有類似表面活性的性質。具體而言,本發明如下:<1>化學式1表示的環糊精結合吲哚菁化合物,其特征在于,吲哚菁類與環狀糖鏈環糊精共價結合而成;[化學式1](式中的r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13、r14、r15、r16、r17、r18、r19、r20、r21、r22、r23是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。另外也可以是它們的取代基(羧酸、磺酸、磷酸),該取代基中氫離子離解的情況下,其氫離子可被鈉離子、鉀離子、鎂離子、鈣離子等的金屬離子取代。氨基選自伯、仲、叔、季(作為與氮結合的取代可例舉烷基等)。另外r8和r9也可以選擇ch2、ch2ch2、ch2ch2ch2或ch2ch2ch2ch2的環狀結構。另外也可以選擇在這些烷基上氫原子被烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環所取代的官能團。)<2>化學式2表示的環糊精結合吲哚菁化合物,其特征在于,吲哚菁的萘基的至少一部分被環糊精的空洞包合。[化學式2](式中的r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13、r14、r15、r16、r17、r18、r19、r20、r21、r22、r23是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。另外也可以是它們的取代基(羧酸、磺酸、磷酸),該取代基中氫離子離解的情況下,其氫離子可被鈉離子、鉀離子、鎂離子、鈣離子等的金屬離子取代。氨基選自伯、仲、叔、季。另外,r8和r9也可以選擇ch2、ch2ch2、ch2ch2ch2或ch2ch2ch2ch2的環狀結構。另外,也可以選擇在這些烷基上氫原子被烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環取代的官能團。)<3>化學式3表示的環糊精結合吲哚菁化合物,其特征在于,是吲哚菁類和環狀糖鏈環糊精通過酰胺鍵共價結合而成的、化學式1表示的環糊精結合吲哚菁化合物。[化學式3](式中的r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13、r14、r15、r16、r17、r18、r19、r20、r21、r22、r23是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。另外也可以是它們的取代基(羧酸、磺酸、磷酸),該取代基中氫離子在離解的情況下,其氫離子可被鈉離子、鉀離子、鎂離子、鈣離子等金屬離子取代。氨基選自伯、仲、叔、季。m、n是1以上6以下的整數。另外,r8和r9可選擇ch2、ch2ch2、ch2ch2ch2或ch2ch2ch2ch2的環狀結構。另外,也可以選擇在這些烷基上氫原子被烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環取代的官能團。)<4>化學式4表示的是環糊精結合吲哚菁化合物,其特征在于,是吲哚菁類和環狀糖鏈環糊精通過酰胺鍵共價結合而成的、化學式2表示的環糊精結合吲哚菁化合物。[化學式4](式中的r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13、r14、r15、r16、r17、r18、r19、r20、r21、r22、r23是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。另外也可以是它們的取代基(羧酸、磺酸、磷酸),該取代基在氫離子離解的情況下,其氫離子可被鈉離子、鉀離子、鎂離子、鈣離子等的金屬離子取代。氨基選自伯、仲、叔、季。m、n是1以上6以下的整數。另外,r8和r9也可以選擇ch2、ch2ch2、ch2ch2ch2或ch2ch2ch2ch2的環狀結構。另外,也可以選擇在這些烷基上氫原子被烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、磷酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環取代的官能團。)<5>化學式3表示的環糊精結合吲哚菁化合物中的化學式5表示的環糊精結合吲哚菁化合物。[化學式5](式中的m、n、p、q是2以上6以下的整數。r是5以上7以下的整數。s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<6>化學式4表示的環糊精結合吲哚菁化合物中的化學式6表示的環糊精結合吲哚菁化合物。[化學式6](式中的m、n、p、q是2以上6以下的整數。r是5以上7以下的整數。s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<7>化學式3表示的環糊精結合吲哚菁化合物中的化學式7表示的環糊精結合吲哚菁化合物。[化學式7](式中的m、n是2以上6以下的整數。r是5以上7以下的整數。s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<8>化學式4表示的環糊精結合吲哚菁化合物中的化學式8表示的環糊精結合吲哚菁化合物。[化學式8](式中的m、n是2以上6以下的整數。r是5以上7以下的整數。s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<9>化學式3表示的環糊精結合吲哚菁化合物中的化學式9表示的環糊精結合吲哚菁化合物。[化學式9](式中的m、n是2以上6以下的整數。r是5以上7以下的整數。s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<10>化學式4表示的環糊精結合吲哚菁化合物中的化學式10表示的環糊精結合吲哚菁化合物。[化學式10](式中的m、n是2以上6以下的整數。r是5以上7以下的整數。s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<11>化學式3表示的環糊精結合吲哚菁化合物中的化學式11表示的環糊精結合吲哚菁化合物。[化學式11](s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<12>化學式4表示的環糊精結合吲哚菁化合物中的化學式12表示的環糊精結合吲哚菁化合物。[化學式12](s是0以上4以下的整數。r是氫原子、烷基、芳基、鹵素原子、烷氧基、氨基、羧基、甲酰基、磺酰基、磺酸基、烷氧基羰基、芳氧基羰基、烷基羰基、芳基羰基或雜環。)<13>上述的化學式(化學式1、3、5、7、9、11)中的任一項所述的環糊精結合吲哚菁化合物的化學合成法,其特征在于,包括:(1)將吲哚菁羧酸化合物和氨基環糊精在溶劑中混合的工序;(2)加入脫水縮合劑進行脫水縮合反應的工序。<14>上述的化學式(化學式2、4、6、8、10、12)中的任一項所述的環糊精結合吲哚菁化合物的化學合成法,其特征在于,將上述的化學式(化學式1、3、5、7、9、11)中的任一項所述的環糊精結合吲哚菁化合物在水中進行包合反應。<15>上述的化學式(化學式1~12)中的任一項所述的環糊精結合吲哚菁化合物的精制法,是通過將該化合物用含hcl的溶劑進行洗提的柱層析法進行的。<16>一種診斷用組合物,通過向體內注入而使用,是含有上述化學式1~12中的任一項所述的環糊精結合吲哚菁化合物的水溶液。<17>如<16>所述的診斷用組合物,其中,實質上不含碘。<18>一種環糊精結合吲哚菁化合物的生物體內動態測定裝置,具有:激發光照射單元,對于給藥了上述<16>或<17>的診斷用組合物的生物體的一部分,向所述環糊精結合吲哚菁化合物照射激發光;熒光強度測定單元,測定通過上述激發光照射單元激發的上述環糊精結合吲哚菁化合物發出的熒光的強度;以及生物體內動態計算單元,由從上述熒光強度測定單元經時獲取的上述熒光強度,求出該熒光強度的時間變化率的經時變化,從而算出上述環糊精結合吲哚菁化合物在上述生物體的一部分中向間質液中移動的速度和/或向上述間質外移動的速度。<19>一種循環可視化裝置,具有:激發光照射單元,對于給藥了上述<16>或<17>的診斷用組合物的生物體的一部分,向所述環糊精結合吲哚菁化合物照射激發光;熒光成像單元,二維性地獲取通過上述激發光照射單元激發的上述環糊精結合吲哚菁化合物發出的熒光的強度,從而得到上述環糊精結合吲哚菁化合物在生物體內的分布狀態數據;形態成像單元,二維性地獲取除了上述環糊精結合吲哚菁化合物發出的上述熒光波長以外波長的光的強度,從而得到對上述生物體的一部分的形態數據;以及顯示單元,將通過上述形態成像單元得到的上述形態數據和通過上述熒光成像單元得到的上述分布狀態數據進行重疊而顯示上述生物體的一部分中上述環糊精結合吲哚菁化合物的分布狀態。<20>上述<19>記載的循環可視化裝置,其中,上述顯示單元將上述生物體的一部分中上述環糊精結合吲哚菁化合物的分布量低于規定基準的部分,作為壞死部分進行顯示。<21>上述<18>記載的生物體內動態測定裝置,具有:腫脹進展預測單元,從上述生物體的一部分中向間質液內外移動的速度,預測上述生物體的一部分以后進展的腫脹程度。<22>上述<21>記載的生物體內動態測定裝置,其中,上述腫脹進展預測單元是預測與經過規定時間以后的向上述間質液中的移動速度的大小所相應的程度的腫脹進展,所述規定時間是從給藥上述診斷用組合物至上述環糊精結合吲哚菁化合物在全身的血液中分散為止的時間。<23>一種生物體內動態測定裝置,其特征在于,具有:激發光照射單元,對給藥了上述<16>或<17>記載的診斷用組合物的生物體的一部分及對照部位,向上述環糊精結合吲哚菁化合物照射激發光,熒光強度測定單元,測定通過上述激發光照射單元激發的上述環糊精結合吲哚菁化合物發出的熒光的強度,生物體內動態計算單元,通過從上述熒光強度測定單元經時獲取的上述熒光強度,求出其熒光強度的經時變化,從而算出上述環糊精結合吲哚菁化合物在上述生物體的一部分中的、向間質液中移動的速度和/或向上述間質外移動的速度,以及腫脹進展預測單元,從上述生物體的一部分中的向間質液內外移動的速度,預測上述生物體的一部分以后進展的腫脹程度;其中,上述腫脹進行預測單元,從到達規定時間為止的上述生物體的一部分的熒光強度的變化和上述對照部位的熒光強度的變化,求出流動于對照部位的血流量與上述生物體的一部分的血流量的關系,其中,所述規定時間是從給藥上述診斷用組合物至上述環糊精結合吲哚菁化合物在全身的血液中分散為止的時間;將經過上述規定時間以后的、以上述對照部位熒光強度的變化作為對照的上述生物體的一部分的熒光強度的變化程度,用其關系進行計算,根據算出的上述變化程度的大小對腫脹的進展進行預測。<24>一種生物體內動態測定裝置,其特征在于,具有:激發光照射單元,對給藥了上述<16>或<17>記載的診斷用組合物的生物體器官,向上述環糊精結合吲哚菁化合物照射激發光;熒光強度測定單元,測定通過上述激發光照射單元激發的上述環糊精結合吲哚菁化合物發出的熒光的強度;以及生物體內動態計算單元,由上述熒光強度測定單元經時地獲取的上述熒光強度,評價在上述器官中的上述環糊精結合吲哚菁化合物的生物體內動態。<25>上述<24>記載的生物體內動態測定裝置,其中,上述器官為腎臟、輸尿管、膀胱及尿道中的任一個。有益效果根據本發明的化學式1或化學式2表示的環糊精結合吲哚菁化合物,可提供具有如下特征的屬于綠色色素的發出近紅外熒光的化合物:與icg相比,在水或生理食鹽水中的溶解性高,易從生物體組織除去,水溶液中的分子締合低,水溶液中的近紅外熒光強度高,對肝臟以外的器官也能進行熒光攝像,不含碘。另外,根據本發明的環糊精結合吲哚菁化合物的合成法,能夠提供有用的環糊精結合吲哚菁化合物的合成。另外,根據本發明的環糊精結合吲哚菁化合物的精制法,能夠提供有用的環糊精結合吲哚菁化合物的精制。另外,本發明的環糊精結合吲哚菁化合物即使不含碘也具有足夠的溶解性,因此能夠提供不含碘過敏癥的原因的碘的診斷用組合物。這些診斷用組合物表現出與現有的只含icg的診斷用組合物不同的體內行為,因此可利用其性質提供各種各樣的有益的裝置。附圖說明圖1是表示icg及化學式19及20表示的異構化平衡化合物(tk1)向人體皮膚的吸附性試驗結果。表示將icg及化學式19及20表示的異構化平衡化合物(tk1)的1mm水溶液(0.03ml)涂布在手腕后立刻攝取(照片左),5分鐘后水洗后立刻攝取(照片中央),進而擦除水洗后立刻攝取(照片右)的照片。另外,右側的點是用紅色筆作的標記。圖2是表示icg及化學式19及20表示的異構化平衡化合物(tk1)向纖維素纖維的吸附性試驗結果。表示將icg及化學式19及20表示的異構化平衡化合物(tk1)的1mm水溶液(0.05ml)用棉棒涂布后立刻攝取(照片上),3分鐘后用水沖洗5秒后的立刻攝取(照片下)的照片。圖3是表示icg及化學式19及20表示的異構化平衡化合物(tk1)的向生物體肉模型的吸附性試驗結果。表示將icg及化學式20表示的化合物的1mm水溶液(0.05ml)涂布在豬里脊肉的直徑5mm的凹處后立刻攝取(照片左),3分鐘后用水沖洗10秒后立刻攝取(照片右)的照片。圖4是表示icg及化學式19及20表示的異構化平衡化合物(tk1)向生物體的蛋白質模型的吸附性試驗結果。表示將icg及化學式19及20表示的異構化平衡化合物(tk1)的1mm水溶液(0.05ml)涂布于雞胸肉的直徑5mm的凹處后立刻攝取(照片左),3分鐘后用水沖洗10秒后立刻攝取(照片右)的照片。圖5是表示icg及化學式19及20表示的異構化平衡化合物(tk1)向疏水性化學纖維的吸附性的試驗結果。表示將icg及化學式19及20表示的異構化平衡化合物(tk-1)的1mm水溶液(0.05ml)涂布于聚丙烯掩模后立刻攝取(照片左),放置20分鐘后用水沖洗1秒后立刻攝取(照片右)的照片。圖6是表示icg及化學式19及20表示的異構化平衡化合物(tk1)的分子締合試驗結果。左圖是icg,右圖是化學式19及20表示的異構化平衡化合物(tk1)。圖7是表示icg、化學式19及20表示的異構化平衡化合物(tk1)及化學式15及16表示的異構化平衡化合物(tk2)在人體靜脈血中的熒光強度的濃度相關性的曲線圖。圖8是表示將icg、化學式19及20表示的異構化平衡化合物(tk1)及化學式15及16表示的異構化平衡化合物(tk2)給藥大鼠時觀察到的情況的圖。圖9是表示將icg、化學式19及20表示的異構化平衡化合物(tk1)及化學式15及16表示的異構化平衡化合物(tk2)給藥大鼠時在腹腔內的熒光的情況的圖。圖10是表示將化學式15及16表示的異構化平衡化合物的(tk2)0.1mm水溶液0.075ml尾靜脈給藥雄wistar大鼠(14周齡,300g),利用濱松光子學株式會社制近紅外觀察系統pde攝像的圖。左為根據可視光的黑白圖像,右為熒光圖象。圖11是表示將化學式15及16表示的異構化平衡化合物的(tk2)0.1mm水溶液0.075ml尾靜脈給藥雄wistar大鼠(14周齡,300g)的近紅外熒光內視鏡攝像圖。左為根據可視光的黑白圖像,右為熒光圖象。圖12是表示icg、化學式19及20表示的異構化平衡化合物(tk1)及化學式15及16表示的異構化平衡化合物(tk2)給藥大鼠時的足背部的熒光的情況的圖。圖13是表示icg、化學式19及20表示的異構化平衡化合物(tk1)及化學式15及16表示的異構化平衡化合物(tk2)給藥大鼠時的足背部的熒光強度的經時變化的曲線圖。圖14是表示icg、化學式19及20表示的異構化平衡化合物(tk1)及化學式15及16表示的異構化平衡化合物(tk2)給藥大鼠時的足背部的熒光強度的經時變化的曲線圖。圖15是表示大鼠血管的直接觀察手法的圖。圖16是表示大鼠的血管的直接觀察部分(精巣提睪肌皮瓣)的圖。圖17是表示給藥icg的大鼠的血管及其周邊的組織的熒光的情況的圖。圖18是表示將化學式19及20表示的異構化平衡化合物(tk1)給藥大鼠的血管及其周邊的組織的熒光的情況的圖。圖19是表示對進行tk1試驗的群,關于給藥卡拉膠的群(edema)和沒有給藥的群(normal)給藥后立刻(postinjection)和一周后(1wafter)測定的大鼠的左足容積的曲線圖。縱軸是容積(ml)。圖20是表示對進行tk1試驗的群,關于給藥卡拉膠的群(edema)和沒有給藥的群(normal),給藥后立刻(postinjection)和一周后(1wafter)測定的大鼠的左足的vonfreytest的結果的圖。縱軸是發生反應的載重(g)。圖21是表示對給藥卡拉膠的群(edema)和沒有給藥的群(normal),注射卡拉膠后立刻注射tk1后的左足表面的亮度的變化的情況的曲線圖。縱軸是亮度(任意單位),橫軸為時間(秒)。圖22是表示對給藥卡拉膠的群(edema)和沒有給藥的群(normal),注射卡拉膠后經過一周后注射tk1后的左足表面的亮度的變化的情況的曲線圖。縱軸是亮度(任意單位),橫軸是時間(秒)。圖23是表示對icg進行試驗的群,關于給藥卡拉膠的群(edema)和沒有給藥的群(normal),給藥后立刻(postinjection)和一周后(1wafter)測定的大鼠的左足容積的曲線圖。縱軸是容積(ml)。圖24是表示對icg進行試驗的群,關于給藥卡拉膠的群(edema)和沒有給藥的群(normal),給藥后立刻(postinjection)和一周后(1wafter)測定的大鼠的左足的vonfreytest的結果的曲線圖。縱軸是發生反應的載重(g)。圖25是表示關于給藥卡拉膠的群(edema)和沒有給藥的群(normal),注射卡拉膠后立刻注射icg后的左足表面的亮度的情況的曲線圖。縱軸是亮度(任意單位),橫軸是時間(秒)。圖26是關于給藥卡拉膠的群(edema)和沒有給藥的群(normal),注射卡拉膠后經過一周后注射icg后的左足表面的亮度變化的情況的曲線圖。縱軸是亮度(任意單位),橫軸是時間(秒)。具體實施方式本發明的診斷用組合物通過采用后述的本發明的環糊精結合吲哚菁化合物作為色素,不含碘就能夠用于診斷。本診斷用組合物可以代替一直在使用的含有吲哚菁綠的診斷用組合物。例如,肝功能檢查藥,循環功能檢查藥等的用途。另外,通過觀察向體內,例如血管、淋巴管、腦、眼、胃、乳、食道、皮膚、腎臟、輸尿管、膀胱、尿道、肺、心臟或其他的部位給藥而生成的近紅外熒光,從而可應用于醫療手術及醫療診斷。本發明的診斷用組合物所含有的色素與生物體的結合性小,可以長時間標識需要的部位。在診斷用組合物中根據需要也可含有作為等張劑的鹽或其他的添加物。另外,除預先調制的水溶液,還可適宜采用進行溶解而使用的形態。該診斷用組合物可經注射、點滴、塗布、經口給藥等給藥。該診斷用組合物適合在使血液、淋巴液、間質水及尿等的水溶液等的循環情況可視化時使用。通過使血液等的循環可視化,例如,能夠用于通過評價末梢循環的壞死的判斷,血運重建手術、移植手術后的組織成活的評價,血運不良的診斷等。另外,也可應用于迄今進行可視化的眼底造影、腦循環評價、腦外科手術中的術中造影、癌(乳癌、食道癌、胃癌、大腸癌、前列腺癌、皮膚癌等)中的前哨淋巴結鑒定、淋巴浮腫的評價、術中膽管造影、腫瘤的標記、冠動脈造影、腹部血管造影(肝動脈、腹部大動脈、消化管血流等)等。也可對腎臟、輸尿管、膀胱、尿道等腎排泄系進行熒光攝像。<1.非包合型環糊精結合吲哚菁化合物及其合成>作為本發明的非包合型環糊精結合吲哚菁化合物可例舉化學式1、化學式3、化學式5、化學式7、化學式9、化學式11,其合成法是通過使吲哚菁化合物與環糊精化合物在溶液中反應而完成的。在化學式1及3中,考慮與環糊精相當部分的包合,r1~r4及r13~r16優選為不阻礙環糊精包合的體積不大的基團。例如,氫或碳數1~3左右的烷基或烷氧基。優選氫、甲基、甲氧基,最優選氫。出于環糊精的包合,r5、r6、r11及r12也優選體積不大,但不到r1~r4及r13~r16的程度。例如為氫、碳數1~6左右的烷基或烷氧基。r1~r6及r11~r16是由環糊精包合的部位,所以即使在導入親水性的官能團情況下也優選作為其整體為疏水性。r17、r18、r22及r23不太影響環糊精的包合,所以只要是上述的取代基則沒有特別限定。r7、r10、r19及r21從合成容易的觀點來看優選氫。r8、r9及r20只要為上述的取代基則也沒有特別限定。在本發明的非包合型環糊精結合吲哚菁化合物是通過酰胺鍵使吲哚菁化合物與環糊精化合物共價結合的情況下,其非包合型環糊精結合吲哚菁化合物合成法可以是使吲哚菁羧酸化合物與氨基環糊精化合物在溶液中發生脫水縮合反應而實現。<2.包合型環糊精結合吲哚菁化合物>本發明的環糊精結合吲哚菁化合物的特征在于,是化學式2表示的吲哚菁類與環狀糖鏈環糊精共價結合而成的環糊精結合吲哚菁化合物,吲哚菁的萘基的至少一部分包合于環糊精的空洞。另外,只要吲哚菁的萘基被包合在環糊精的空洞,發出近紅外熒光,則吲哚菁基也可以具有取代基。另外,環糊精種類繁多,但吲哚菁的萘基被包合在環糊精的空洞是必要條件。例如,可以例舉α-環糊精,β-環糊精,γ-環糊精。優選為β-環糊精。另外,環糊精可具有取代基。在化學式2及4中,r1~r4及r13~r16優選為不阻礙環糊精包合的體積不大的基團。例如氫、碳數1~3左右的烷基或烷氧基。特別優選氫、甲基、甲氧基,最優選的是氫。出于環糊精的包合,r5、r6、r11及r12雖然不如r1~r4及r13~r16,但也為體積不大。例如氫、碳數1~6左右的烷基或烷氧基。r1~r6及r11~r16是由環糊精包合的部位,所以優選即使導入親水性的官能團的情況下,作為其整體為疏水性。r17、r18、r22及r23不太影響環糊精的包合,所以只要是上述的取代基則沒有特別限定。r7、r10、r19及r21從合成容易的觀點來看優選氫。r8、r9及r20只要為上述的取代基則對其也沒有特別的限定。吲哚菁基和環糊精的結合,只要為共價結合就對其沒有特別限定,例如可例舉烷基鍵、氨鍵、酰胺鍵、雙鍵、三鍵、酯鍵、醚鍵等。但在化學合成上,從注重效率的角度考慮,優選酰胺鍵。為了使吲哚菁的萘基的至少一部分在環糊精的空洞包合,優選使用間隔基使吲哚菁類和環狀糖鏈環糊精介由間隔基進行共價結合而成。此時,可通過調節化學式2中的間隔基的長度來控制吲哚菁的萘基向環糊精的空洞包合的程度。因此,吲哚菁類和環狀糖鏈環糊精介由間隔基通過共價結合而成的環糊精結合吲哚菁化合物且吲哚菁的萘基在環糊精的空洞包合為特征的化合物,優選例舉化學式4的物質。另外,優選例舉化學式6、化學式8、化學式10的物質。另外,優選例舉化學式12的物質。化學式6中,m、n、p及q優選為m+p及n+q分別為5以上7以下。從環糊精包合容易的角度考慮,在所有化學式(化學式1~10)中,優選相當于吲哚菁結構中的氮原子和相當于環糊精結構中的氧原子之間的結構(間隔基)的原子數在7以上9以下。<3.包合型環糊精結合吲哚菁化合物的合成>本發明的包合型環糊精結合吲哚菁化合物為如上所述,其合成法為,以上述合成的非包合型環糊精結合吲哚菁化合物為合成前體,將該化合溶解于水溶液中而完成。在水溶液中,只要不妨礙包合化,可以含有任何物質,對水的含量沒有特別限定。另外,適合包合化的溫度為-20℃~100℃,優選0℃~50℃。另外,包合化需要的時間是在水溶液中添加后立刻開始至1個月左右。包合化反應根據如上的非包合型環糊精結合吲哚菁化合物的性質、包合化反應的溫度、水溶液的組成、濃度等,可以為各種各樣的形態。另外,可以通過使本發明的非包合型環糊精結合吲哚菁化合物溶解于包含水的溶劑而變換為包合型環糊精結合吲哚菁化合物。雖然對溶劑中的水的含量比例沒有特別限定,從原理上講水多時包合更容易,優選為50質量%以上。并且,只要在水溶液以外的溶劑中存有形成包合型環糊精結合吲哚菁化合物的物質,則沒有必要必須在水溶液中進行包合化。另外,在非包合型環糊精結合吲哚菁化合物的合成階段有形成包合型環糊精結合吲哚菁化合物的情況,在此情況下,沒有必要重新進行包合化反應。<4.非包合型環糊精結合吲哚菁化合物的合成法(合成的一例)>將化學式11所示的化合物的合成作為一個例子舉出。化學式11表示的吲哚菁化合物,例如可以通過將以非專利文獻5所述的方法合成的化學式13所述的化合物、非專利文獻6所述的方法合成的化學式14、作為脫水縮合劑的例如水溶性碳化二酰亞胺(wsc:例如,1-乙基-3-(3-二甲基氨基丙基)碳化二酰亞胺鹽酸鹽)或二環己基碳化二酰亞胺(dcc)、以及作為溶劑的吡啶或n,n-二甲基甲酰胺或水溶液進行添加,-20℃~60℃下反應10分鐘~100小時而得到。另外,為了使反應活化作為活化劑例如還可以添加1-羥基苯并三唑(hobt)。脫水縮合劑的量是化學式13表示的化合物的2倍摩爾或其以上,所使用的溶劑,只要可以使反應物溶解,不妨礙脫水縮合反應則對其沒有限制。活化劑只要是能活化脫水縮合反應則對其沒有限制,添加的量只要能使脫水縮合反應進行為所期待的程度的量,則對其沒有限制。[化學式13][化學式14]<5.非包合型環糊精結合吲哚菁化合物的精制法>將以上述的方法合成的含有非包合型環糊精結合吲哚菁化合物的混合物溶解于酸性水溶液中,提供給反相柱層析,作為洗提液例如使用含酸水和甲醇混合液、或含酸水和乙腈混合液、或含酸水和乙醇混合液、或含酸水和丙酮混合液中的任一種進行洗提,分離精制出高純度的非包合型環糊精結合吲哚菁化合物。作為酸只要不使非包合型環糊精結合吲哚菁化合物分解,且能有效洗提,洗提后的處理容易,則對其沒有其他限制,例如優選鹽酸、三氟醋酸、醋酸、硫酸、硝酸、蟻酸等。優選為鹽酸、三氟醋酸、醋酸。最優選鹽酸。酸的濃度,只要非包合型環糊精結合吲哚菁化合物不分解、能有效進行洗提、且洗提后的處理容易,則對其沒有其他限制,優選為0.01mm~10mm,最優選為0.1mm~1mm。通過使濃度在該范圍內,能夠不使目的化合物分解又能夠快速洗提。對于洗提的非包合型環糊精結合吲哚菁化合物,通過去除溶劑可得到其固體。作為溶劑的去除方法也可以進行冷凍干燥。<6.包合型環糊精結合吲哚菁化合物的合成法(合成的一例)及精制法(精制的一例)>以上述的方法合成及精制的化學式11所述的非包合型環糊精結合吲哚菁化合物,例如在dmso中為非包合型,但溶解于水后立即變為包合型的化學式12所述的化合物。該現象能夠使用1hnmr確認。因此,包合型化合物只要是水溶液,就以包合型化合物存在,可作為包合型化合物使用。另外,水溶液中的包合型化合物,可通過除去其水溶液的水成為固體,還可制成包合型化合物的固體。<7.適用于給藥了診斷用組合物的生物體的、生物體內動態測定裝置及循環可視化裝置>·生物體內動態測定裝置本裝置是基于本發明的診斷用組合物所采用的本發明的環糊精結合吲哚菁化合物(以下,有時適當的稱為“本發明化合物”)的、間質內移動程度等體內動態與icg不同而完成的。也就是說,本發明化合物的代謝速度、從血液或淋巴液等的循環系向間質的移動速度與icg不同,從而本發明化合物進入間質的比例與icg相比相對地大,因此可通過分析本發明化合物在生物體內的動態,能夠正確地評價生物體內的體液移動(生物體內動態)的機理。這里,本裝置通過盡量將測定條件(生物體的活動狀態、環境溫度等)設為常定狀態,能夠更準確的測定生物體內動態。生物體內的體液移動的異常的一種形態為發生浮腫。在此,根據所謂stirling假設,生物體內的體液(水分)的移動大體可以認為是由動脈到間質,然后由間質流向靜脈。該從動脈到靜脈的水分移動,可從根據動脈壓與間質壓的壓差流向循環系外的水分移動(a),根據靜脈壓與間質壓的壓差流向循環系內的水分移動(b),根據間質液滲透壓與動脈血滲透壓的壓差從間質流向動脈內的水分移動(c),根據間質液滲透壓與靜脈血滲透壓的壓差從間質流向靜脈內的水分移動(d),作為(a)-(b)-(c)+(d)算出。因此,心力衰竭等而動脈壓與靜脈壓的壓差變小,或者營養失調而使間質液滲透壓變低,則會破壞水分移動(a)~(d)的平衡,產生浮腫。另外,如糖尿病這種毛細血管的透過性存在異常(物質透過的選擇性的異常)的情況下,也會破壞水分移動(a)~(d)的平衡,產生浮腫。在此,沒有直接評價毛細血管的透過性異常的簡便的方法,迄今為止雖然可以用現象檢知浮腫的產生,但現狀是很難確定浮腫發生的詳細原因。根據以上的見解,當在毛細血管血管壁中產生物質透過異常的情況下,可期待本發明化合物的移動,與根據動脈壓與靜脈壓的壓差的降低、細胞內的滲透壓的下降等而發生浮腫的情況相比有變化。因此,當確認有與水分移動相當的量以上(或以下)的本發明化合物質移動的情況下,可以判定為產生毛細血管的透過性異常。因為,可以認為若沒有產生毛細血管的透過性異常,則只能確認到與水分移動的變化相當的程度的本發明化合物的移動,所以可以判別為血管壁上產生異常的情況。特別是采用向間質內的移動速度不同的兩種以上的本發明化合物,通過分別測定這些化合物的生物體內動態并進行比較,從而可以對毛細血管的透過性變化的程度進行評價。也就是說,通過采用在毛細血管血管壁中的透過性不同的2種以上的本發明化合物并測定其透過性,可更準確的評價血管壁透過性異常的發生與否。即,通過采用對于血管壁透過性異常的感受性不同的兩種以上的本發明化合物并測定其體內動態,能夠更準確的評價水分移動的變動因素。另外,除了本發明化合物的水分移動的評價之外還可以利用常法測定水分移動。本發明的生物體內動態測定裝置包括激發光照射單元、熒光強度測定單元、體內動態計算單元和其他的單元。可以根據需要選擇其他的單元,例如根據由熒光強度測定單元測定的熒光強度算出環糊精結合吲哚菁化合物濃度的生物體內濃度計算單元。本裝置是對給藥了上述本發明的診斷用組合物的生物體的至少一部分進行測定的裝置。診斷用組合物的給藥量是在測定部位照射激發光時可觀測到熒光的量。因此,根據測量部位適合量有變化。對診斷用組合物中含有的本發明化合物的種類沒有特別限定。本發明化合物可以使用1種,也可以混合2種以上使用。另外,測量的過程中可以追加相同或者不同組成的診斷用組合物。激發光照射單元是對給藥的診斷用組合物中含有的本發明化合物照射能夠產生熒光的波長的激發光的單元。照射的激發光的波長可以限制在適當的范圍。通過將波長限制在盡量狹小的范圍可以使熒光和激發光進行可靠的分離。關于波長的限制,可以選擇發出適當波長光的光源,或利用濾波器限制波長。關于激發光的照射形態,只要是所產生的熒光能被后述的熒光強度測定單元所測定,則沒有特別限定。例如,作為激發光可例舉連續的光、脈沖狀的光、強度變化的光等。欲變化強度時,可以通過使激發光的脈沖以規定間隔照射等來調制激發光的強度。優選激發光的調制是采用脈沖振幅調制來調制激發光的強度。激發光是通過適當的光學系向應照射的部位照射。應照射的部位是欲進行生物體內動態測定的部位,例如想要評價發生浮腫部位的情況下,優選直接在發生浮腫的部位照射激發光。對激發光照射范圍沒有特別限定。根據需要確定照射范圍。若照射范圍狹窄,則被照射的狹窄的部分中可以對被細分化的生物體內動態進行精密測量。以廣范圍照射,則照射激發光而發出熒光的本發明化合物的相對量將增加,因此可以對熒光強度進行更為精密的測定。并且,利用激發光照射單元的激發光的照射優選在抑制環境光影響的狀態下進行。例如,在黑暗處照射激發光,或對照射激發光部分進行披覆而免受外界光的狀態下照射激發光。熒光強度測定單元是測定由通過激發光照射單元照射激發光的部位發出的熒光強度的單元。關于熒光強度的測定,優選通過將發出的熒光選擇性地透過的濾光器,除去熒光以外的光(環境光、激發光等)而進行測定。作為激發光照射單元采用照射調制強度后的激發光的單元的情況下,可以從測定的光強度中分離顯示與該調制對應的變化的成分后作為熒光強度。例如,在利用脈沖振幅調制來調制激發光強度的情況下,解調根據所調制的脈沖的強度而進行變化的光的成分,并通過測定其強度而能夠分離熒光強度。因此可以降低環境光對熒光強度的測定結果帶來的影響。生物體內濃度計算單元是根據通過熒光強度測定單元測定的熒光強度算出本發明化合物的生物體內濃度的單元。熒光強度與本發明化合物的生物體內濃度的關系可以用適當的方法算出。例如,預先作成標準曲線,可根據該標準曲線計算本發明化合物的生物體內濃度。另外,可將熒光強度的絕對值直接用作為與本發明化合物的生物體內濃度相關的值。生物體內濃度計算單元是經時地算出本發明化合物的生物體內濃度。生物體內動態計算單元是從通過生物體內濃度計算單元經時地得到的本發明化合物的生物體內濃度的數據,求得其生物體內濃度的時間變化率的經時變化的單元。生物體內動態計算單元通過求出的生物體內濃度的時間變化率算出本發明化合物在生物體一部分中由循環系向間質內移動的速度及由間質向循環系移動的速度。也可以不使用生物體內濃度而通過使用熒光強度測定單元經時地得到的熒光強度的變化直接算出向間質內外的移動速度。在此,可以推測向間質內(外)的本發明化合物的移動與體液中的水分移動之間具有很高的相關性,因此通過測定本發明化合物的體內動態而可以評價測量部位中的水分移動的情況。并且,當血管壁出現異常,物質的透過性非正常時,本發明化合物在生物體內的動態也應發生變化,因此,通過評價本發明化合物的動態可以對血管的透過性進行評價。熒光強度(或生物體內濃度)的時間變化率是將熒光強度(或生物體內濃度)的經時變化以時間進行微分求得,或可以算出每規定時間的熒光強度(或生物體內濃度)后作為與規定時間前(規定時間后)的熒光強度(或生物體內濃度)的差來求得。由求得的熒光強度(或生物體濃度)的時間變化率可以算出本發明化合物在所述生物體一部分中的進入間質液中的速度和被排出的速度。在此,進入間質液中的速度和被排出的速度可以由熒光強度作為相對值求出,要求更為精密時,可以根據間質內的本發明化合物的濃度及間質液的量算出。而且此外還考慮血液、淋巴液中的本發明化合物的濃度及其量,則能夠更精密地算出。在血液等中的本發明化合物的濃度可以通過實際采取血液而能夠以良好的精度進行測定。作為算出間質液中濃度的方法可以例舉以下方法。第1方法是將算出的本發明化合物的生物體內濃度直接近似為該生物體一部分中的間質液中的濃度的方法。作為與第1方法相關的方法,也可以考慮間質液的量而算出間質液中的濃度。第2方法是在測定實際血液中存在的本發明化合物的濃度的基礎上,利用使用不向間質移動的其他的標準物質(icg等)等的方法來算出血管內存在的物質對通過熒光強度測定單元測定的測定值的影響比例,通過除去實測的血液中本發明化合物的濃度的影響而算出間質液中的濃度的方法。間質液中的本發明化合物的濃度的時間變化率可以由向間質內移動速度減去向間質外移動速度而算出。在此,能夠假設向間質內(外)的本發明化合物的移動以與體液中的水分移動相關的速度進行,且假設該水分移動達到平衡的話,則可將向間質內的移動速度和向間質外的移動速度視為常數,因此,可以由本發明化合物在血液中的濃度變化(新陳代謝、排出、向組織的移動等引起的變化)與在間質液中的濃度的時間變化率的推移,算出其移動速度。此外,即使在其移動速度變化的情況下,也能夠通過制作與此變化對應的模型并適用來算出它們的移動速度。在算出的移動速度脫離正常的血管壁顯示值的范圍時,可以推測為血管壁出現了異常。另外,血管壁產生異常的結果,本發明化合物的透過性有提高的情況和下降的情況這兩種情況。在此,由于急性炎癥、局部缺血、外傷等各種各樣的組織障礙而引起組織急性腫脹是眾所周知的事實,與領域無關而在醫療現場是極其重要的組織反應。例如,除了純粹的腫脹的發生自身成為問題以外,還有手術時等的腸管等的縫合的評價,肺炎等的炎癥程度的評價,臟器移植的適合性的評價,腦、腎臟等的功能不全的評價等,是涉及全臟器的問題。但是,目前沒有正確的預測組織腫脹的可能性和程度的手段,而只能從組織障礙的程度憑經驗預測。所以絕大部分的情況是只能確認了腫脹的發生后討論對策,成為了治療上的較大制約。若早期能夠以高精度預測腫脹的可能性,可以早期就采取減輕腫脹的措施,將影響控制到最低限度。例如若能夠正確預測腦出血不久之后發生的腦浮腫的程度,則可在早期采取減壓措施、降低血管透過性的對策,可將影響控制到最低限度。同樣如果可以事前預測缺血壓力帶來的影響,就可以將由心肌梗塞和四肢外傷等引起的2次性的障礙降到最低限度。這樣,腫脹的高精度定量預測的技術將會給整個醫療帶來不小的影響。包括浮腫的組織腫脹的定量化,到目前為止一直通過觀測定性地判斷。雖然也嘗試了定量化,但僅可應用極為有限的狀況,并且,存在只能在腫脹產生后才能進行評價的缺點。對于這樣的問題,通過使用本發明的生物體內動態測定裝置,算出間質內外的水分移動速度,從而能夠預測腫脹的進展。如在實施例詳述,已知icg在腫脹進行時不向間質移動。相對于此,本發明的環糊精結合吲哚菁化合物可以在間質內外移動,向間質內的移動則在腫脹的進行時隨著水分的移動能夠進一步被促進。因此,通過對本發明的環糊精結合吲哚菁化合物向間質內的移動的評價,可以預測腫脹的進展。也就是說,可以推測最終形成多大程度大小的腫脹受向間質內外的水分的移動速度的影響,因此通過對與水分的移動速度相關的本發明的環糊精結合吲哚菁化合物的移動速度進行評價而能夠評價最終的腫脹的進行程度。移動速度可以通過環糊精結合吲哚菁化合物的濃度進行算出,也可以直接使用熒光強度算出。另外,自然可以將向間質內外的移動速度作為絕對值算出,也可以將其作為相對值(例如可以將熒光強度的變化率直接作為移動速度相關的值使用)算出,根據該值可以預測腫脹的進展。優選腫脹的進展是以沒有進行腫脹的平常時的向間質內的移動速度為基準來計算。然而,有時也有不知道平常時的向間質內移動速度的情況,在這種情況下,將沒有進行腫脹的部位選擇作為對照部位,求得該部位的移動速度而進行代用。另外,使用在間質內不移動的icg評價血液的循環量和代謝的程度,評價本發明的環糊精結合吲哚菁化合物的向間質內移動的程度。本發明的環糊精結合吲哚菁化合物在間質內移動的程度的測定是向生物體內給藥本發明的診斷用組合物后經過規定時間以后進行的。所述規定時間是指本發明的診斷用組合物在血液中分布所需要的時間。使用規定時間以后的數據進行評價的理由是,給藥診斷用組合物后,經規定的時間而分布到血液中時幾乎不受腫脹進展程度的影響,在血液中的濃度迅速上升,熒光強度的變化的情況不受腫脹進行的有無的影響,幾乎不產生差異。在血中分布后,在間質內移動的速度將根據腫脹的進展的有無而發生變化,因此在移動進行的部位(即進行腫脹的部位)上將有選擇地確認到熒光強度的提高。作為具體的腫脹進展推定方法的例子,可以舉出這樣的方法:由體重等推測血液量,由推測出的血液量算出熒光強度的峰的大小、至峰為止的時間;考慮該時間、強度而測定可能伴隨浮腫發生變化的時間的熒光強度,由其結果可以推測出浮腫的進行的程度,以及將來可能發生的浮腫的程度。循環可視化裝置本裝置是基于本發明的診斷用組合物采用的本發明的環糊精結合吲哚菁化合物(以下有時適當的稱為“本發明化合物”)向間質內移動的程度等體內動態與icg的不同而完成的。也就是說,本發明化合物在間質液中容易移動,可以根據追蹤本發明化合物的行為,使血液循環或者淋巴液循環的情況可視化。本發明的循環可視化裝置具有激發光照射單元、熒光成像單元、形態成像單元和顯示單元。本裝置是對給藥了上述本發明的診斷用組合物的生物體的至少一部分進行測定的裝置。診斷用組合物的給藥量是在測定部位照射激發光時可觀測到熒光的量。因此,根據測量部位適合量有變化。診斷用組合物中含有的本發明化合物的種類沒有特別限定。本發明化合物可以使用一種,也可以2種以上混合使用。另外,在測量的過程中可以追加給藥具有相同或者不同組成的診斷用組合物。激發光照射單元是對給藥的診斷用組合物中含有的本發明化合物照射能夠產生熒光的波長的激發光的單元。照射的激發光的波長可以限制在適當的范圍。通過盡量將波長限制在窄的范圍能夠可靠地分離熒光和激發光。波長的限制可以通過選擇發出適當波長光的光源,或者利用濾波器進行波長限制而實現。關于激發光的照射的形態,只要產生的熒光能夠通過后述的熒光成像單元被測定則沒有特別限定。例如,作為激發光可例舉連續的光、脈沖狀的光、強度變化的光等。欲變化強度時,可以通過使激發光的脈沖以規定間隔照射等來調制激發光的強度。優選激發光的調制是采用脈沖振幅調制來調制激發光的強度。激發光通過適當的光學系,照射應照射的部分。應照射的部分是指生物體中的欲使循環的情況可視化的部位,例如由燙傷或者凍傷、炎癥、創傷、梗塞等導致組織的壞死進行的部位及其周邊部位。在組織中的壞死部分中,血液不循環,放任不管則幾乎沒有益處,因此可以考慮除去。在此情況下,在壞死部分和正常的部分中只將壞死部分完全除去是理想的。以往,對于壞死部分的特定是利用給藥造影劑而進行的血管造影術、檢測伴隨血液循環定價的體溫降低的方法等來進行的,血管造影術有x射線照射裝置等的裝置的使用不便的問題,由體溫的判斷方法有難以進行正確判斷的問題。本發明的裝置用于對壞死部分和正常部分通過有無體液(血液)循環來進行評價的用途。只要能使沒有循環的部分可視化就可以容易地將該部分去除。除了壞死部分的可視化,還可以直接觀察血液循環,因此可以簡便地判別出循環功能發生異常的情況。例如,能夠可視化雖然不至于壞死但發生了梗塞等而循環功能下降的部分。作為激發光照射范圍,以包含欲循環可視化部分的方式根據需要確定照射范圍。并且,利用激發光照射單元的激發光的照射優選是在控制環境光的影響的狀態下進行。例如,在黑暗處照射激發光,或對照射激發光部分進行披覆而免受外界光的狀態下照射激發光。熒光成像單元是二維地獲取利用激發光照射單元激發的本發明化合物發出的熒光的強度,以此獲得本發明化合物在生物體中的分布狀態數據的單元。也就是說,本單元是將生物體一部分的本發明化合物的分布的情況作為二維圖像數據表示的分布狀態數據獲取的單元。例如可由適當的光學系與ccd等攝像元件的組合構成。二維地獲取的數據的分辨率可以根據目的設定為必要的值。熒光強度的測定優選使發出的熒光介由濾片選擇性透過而除去熒光以外的光(環境光、激發光等)來測定。作為激發光照射單元采用照射調制強度后的激發光的情況下,由測量的光的強度將對應調制的變化的成分分離并獲得熒光強度。例如,以脈沖振幅調制對激發光強度進行調制的情況下,通過解調根據被調制脈沖強度來變化的光的成分,并測定其強度,分離出熒光強度。因此,可以降低環境光對熒光強度測定結果的影響。形態成像單元是二維地獲取本發明化合物發出的熒光波長以外的波長的光的強度獲得其在生物體一部分的形態數據的單元。也就是說,本單元是在生物體一部分中,為獲取其形態的二次元圖像數據的單元。形態成像單元可由適當的光學系和ccd等的攝像元件所構成。二維獲取的數據的分辨率可以根據所需的目的設定其值。在這種情況下不測定激發光所發出的熒光(或降低檢測靈敏度)。形態成像單元將前述的熒光成像單元和光學系幾乎都共用的基礎上,最終在導入攝像元件前的光路上利用分光棱鏡等將與熒光對應波長的光引導至熒光成像單元,可將其他波長的光引導至形態成像單元。分光棱鏡通過適當形成雙向色膜,可以合理控制分離光的波長。并且,熒光成像單元和形態成像單元可以共用在同一個攝像裝置。也就是說,熒光和其他的光的分離也可以是得到其二維圖像數據后進行的數學分離。并且,分布狀態數據也可以是從生物體一部分的表面向深層方向的復數圖像數據。熒光成像單元采用的光學焦點在向深層方向移動中在深層方向上得到復數的二維圖像數據。另外,作為激發光照射單元采用可以變化焦點距離的光學系,并非在生物體一部分的表面,而是在深層方向的內部移動焦點,或將激發光聚集細而對生物體一部分照射,并不只在生物體表面而是在生物體的深層內部中可以選擇地發出熒光,可以將此部分循環的情況可視化。顯示單元是通過形態成像單元得到的形態數據和由熒光成像單元得到的分布狀態數據的重疊來表示生物體一部分中的本發明化合物分布狀態的顯示單元。熒光的波長沒有在可見光的范圍內的情況下,優選將熒光的波長轉換為可見光表示。從循環的可視化的觀點來看,分布狀態數據的表示優先于形態數據表示。特別是,可以判別的表示本發明化合物的分布量(即熒光強度)低的部分(低與否,根據循環可視化的目的決定。例如,在將壞死部分可視化目的中,在沒有循環的部分,即確認不到熒光的部分)和其他的部分。例如,能夠將該部分表示成與其他部分不同的顏色或閃爍表示。分布狀態數據和形態數據的疊加可以利用電腦上的邏輯等實現。二維數據的表示可由一般的顯示裝置實現。該顯示裝置設置于生物體和測量者之間,因此可以一邊觀測顯示裝置一邊對生物體進行處置。<8.定義等>在本發明中,“烷基”是指可有取代基的碳數1~20個的直鏈狀或者支鏈狀的烷基,例如,甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、十六烷基、十七烷基、十八烷基、十九烷基、二十烷基等直鏈基團,或者以支鏈狀結合的基團。本發明中,“烷氧基”可例舉例如甲氧基、乙氧基、丙氧基、丁氧基、戊氧基、己氧基,甲氧基乙氧基、甲氧基丙氧基、乙氧基乙氧基、乙氧基丙氧基、甲氧基乙氧基乙氧基等碳數1~20個的烷氧基在直鏈上或者支鏈狀結合的基團。在本發明中,“芳基”可例舉苯基、萘基等碳數6~20個的芳烴。實施例以下通過實施例具體說明本發明的優選實施方式,但本發明的技術范圍并不限于下述實施方式,在本發明范圍內可以進行各種變形來實施。<試驗1:化學式15及化學式16所示的化合物的合成及精制>將化學式13表示的化合物0.20g、化學式14表示的化合物0.94g、wsc0.18g、hobt0.12g、吡啶4.0ml、n,n-二甲基甲酰胺2.0ml的混合物在0℃且在暗處攪拌6小時。其后加入丙酮50ml,析出物經減壓過濾,將析出物溶解于0.1%三氟醋酸水溶液,提供給ods柱層析。洗提液使用含有1mm鹽酸的水及甲醇的混合液,洗提化學式15表示的化合物。洗提液經減壓濃縮得到綠色固體的化學式16表示的包合型化合物0.65g(在洗提液的減壓濃縮中,濃縮的最后,水的含量高,所以自然成為包合型)。[化學式15][化學式16]其次,表示化學式16所示目的物的機器分析數據。1hnmr(500mhz,d2o,26℃,丙酮:2.10ppm)1.43(2h,m),1.55(2h,m),1.99(6h,s),2.09(6h,s),2.63(6h,m),2.80(6h,m),2.92(2h,m),3.02(2h,dd,j=3.7,9.8hz),3.08(2h,t,j=9.2hz),3.2-4.1(m),4.19(2h,t,j=9.8hz),4.26(2h,t,j=9.8hz),4.33(2h,m),4.43(2h,m),4.71(2h,d,j=2.4hz),4.81(4h,d,j=3.7hz),4.91(2h,d,j=3.7hz),4.99(2h,d,j=3.7hz),5.08(2h,d,j=3.7hz),5.13(2h,d,j=3.1hz),6.15(2h,d,j=13hz),6.52(2h,t,j=12hz),7.43(4h,m),7.57(1h,d,j=12hz),7.57(2h,d,j=9.2hz),7.78(2h,m),8.06(3h,m),8.15(2h,d,j=8.5hz).esi-msm/z計算值c131h191n4o722972,實驗值2973[m]+.<試驗2:化學式19及化學式20所示化合物的合成及精制>將化學式17表示的化合物0.17g、甲醇5ml、t-buok0.30g的混合物在室溫攪拌12小時。其后,加入1m鹽酸3ml,并加入水50ml。過濾析出物,用水清洗析出物后,減壓干燥而得到化學式18所示的化合物0.17g。[化學式17][化學式18]將化學式18表示的化合物0.02g、化學式14表示的化合物0.081g、wsc0.016g、hobt0.011g、吡啶0.3ml、n,n-二甲基甲酰胺0.2ml的混合物在0℃暗處攪拌6小時。其后加入丙酮5ml,析出物經減壓過濾,溶解于0.1%三氟醋酸水溶液中,提供給ods柱層析。洗提液中使用含1mm鹽酸的水及甲醇的混合液,洗提化學式19表示的化合物。洗提液經減壓濃縮得到綠色固體的化學式20表示的包合型化合物0.045g(在洗提液的減壓濃縮中,濃縮的最后,水的含有量高,所以自然成為包合型)。[化學式19][化學式20]其次,表示化學式20所示目的物的機器分析數據。1hnmr(500mhz,d2o,40℃,丙酮:2.26ppm)1.54(2h,m),1.68(2h,m),1.98(2h,m),2.19(6h,s),2.20(2h,m),2.30(6h,s),2.6-2.85(10h,m),2.95(2h,m),3.00(4h,m),3.08(2h,t,j=12hz),3.17(2h,dd,j=3.7,9.8hz),3.26(2h,t,j=9.8hz),3.35-4.30(m),4.35(2h,t,j=9.2hz),4.50(2h,t,j=9.2h),4.52(2h,m),4.63(2h,m),4.87(2h,d,j=3.7hz),4.95(d,j=3.1hz),4.97(2h,d,j=3.7hz),5.08(2h,d,j=3.7hz),5.15(2h,d,j=4.3hz),5.25(2h,d,j=3.7hz),5.29(2h,d,j=3.7hz),6.30(2h,d,j=14.6hz),7.58(4h,m),7.73(2h,d,j=8.5hz),7.95(2h,m),8.25(2h,m),8.32(2h,d,j=14.6hz),8.35(2h,d,j=8.5hz).esi-msm/z計算值c135h197n4o733042,實驗值3042[m]+.<試驗3:化學式21表示的化合物的合成及精制>將化學式13表示的化合物0.04g、單-6-氨基-6-去氧-β-環糊精0.18g、wsc0.05g、hobt0.025g、吡啶0.8ml、n,n-二甲基甲酰胺0.4ml的混合物在0℃暗處攪拌3小時。其后加入丙酮10ml,析出物經減壓過濾,溶解于0.1%三氟醋酸水溶液中,提供給ods柱層析。洗提液使用含1mm鹽酸的水及甲醇的混合液,洗提化學式21表示的化合物。洗提液經減壓濃縮得到綠色固體的化學式21表示的化合物0.11g。[化學式21]其次,表示化學式21所示目的物的機器分析數據。1hnmr(500mhz,d2o,29℃,丙酮:2.10ppm)1.79(12h,br.),2.68(4h,br.),3.0-4.5(98h),4.4(4h,br.),4.5-5.3(14h,br.),6.18(2h,br.),6.46(2h,br.),7.3-8.2(15h).esi-msm/z計算值c125h179n4o702856,實驗值2856[m]+.<試驗4:化學式23表示的化合物的合成及精制>將化學式22表示的化合物0.02g、單-6-氨基-6-去氧-β-環糊精0.096g、wsc0.032g、吡啶0.5ml、0.1m磷酸緩沖液0.05ml的混合物在室溫暗處攪拌24小時。其后加入丙酮10ml,析出物經減壓過濾,溶解于0.1%三氟醋酸水溶液中,提供給ods柱層析。洗提液使用水及乙腈的混合液,洗提化學式23表示的化合物。洗提液經減壓濃縮得到綠色固體的化學式23表示的化合物0.014g。[化學式22][化學式23]其次,表示化學式21所示目的物的機器分析數據。1hnmr(500mhz,d2o,26℃,丙酮:2.15ppm)1.26(4h,m),1.5-2.25(24h,br),2.7-4.2(88h),4.82(2h,br),4.90(8h,br),4.97(2h,br),5.03(2h,br),6.11(2h,br),6.36(2h,br),7.3-8.01(15h,br).esi-msm/z計算值c131h191n4o702940,實驗值2940[m]+.<試驗5:化學式24表示的化合物的合成及精制>將化學式22表示的化合物0.20g、3-氨基-3-去氧-β-環糊精0.02g、wsc0.096g、hobt0.013g、吡啶0.4ml、n,n-二甲基甲酰胺0.2ml的混合物在室溫暗處攪拌1小時。其后,加入丙酮10ml,析出物經減壓過濾,溶解于0.1%三氟醋酸水溶液中,提供給ods柱層析。洗提液使用水及甲醇的混合液,洗提化學式24表示的化合物。洗提液經減壓濃縮得到綠色固體的化學式24表示的化合物0.013g。[化學式24]其次,表示化學式24所示目的物的機器分析數據。1hnmr(500mhz,d2o,29℃,丙酮:2.10ppm)1.1-2.5(28h),3.0-4.25(88h),4.5-5.2(14h),7.3-8.02(15h).esi-msm/z計算值c131h191n4o702940,實驗值2940[m]+.<試驗6:化學式25表示的化合物的合成及精制>將化學式22表示的化合物0.02g、化學式14表示的化合物0.1g、wsc0.032g、吡啶0.5ml、0.1m磷酸緩沖液0.05ml的混合物在室溫暗處攪拌24小時。其后加入丙酮10ml,析出物經減壓過濾,溶解于0.1%三氟醋酸水溶液中,提供給ods柱層析。洗提液使用水及甲醇的混合液,洗提化學式25表示的化合物。洗提液經減壓濃縮得到綠色固體的化學式25表示的化合物0.021g。[化學式25]其次,表示化學式25所示目的物的機器分析數據。1hnmr(500mhz,d2o,25℃,丙酮:2.10ppm)1.0-2.5(32h),3.0-4.5(96h),4.8-5.2(14h),6.09(2h,br),6.37(2h,br),7.3-8.02(15h,br).esi-msm/z計算值c137h203n4o723056,實驗值3056[m]+.<試驗7:本發明的環糊精結合吲哚菁化合物的溶解性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)進行了向水及生理食鹽水的溶解性試驗。使用水及生理食鹽水的molecularprobe社的粉末狀的icg的溶解需要1分鐘左右的激烈振動攪拌,本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20所示的化合物不需要振動攪拌即可快速溶解。<試驗8:本發明的環糊精結合吲哚菁化合物向人體皮膚的吸附性>對icg以及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)進行了向人體皮膚的吸附性試驗。將icg以及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別取1mm水溶液(0.03ml)滴在腕上,5分鐘后水洗,擦拭后進行再次水洗。其結果是,icg沒有被完全水洗掉,而本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20所示的化合物容易被水洗掉,顯示本發明的環糊精結合吲哚菁化合物向人體皮膚的吸附性顯著低于icg(圖1)。<試驗9:本發明的環糊精結合吲哚菁化合物向纖維素纖維的吸附性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)進行了向纖維素纖維的吸附性試驗。纖維素纖維的模型用棉棒(株式會社三洋),icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別取1mm水溶液0.05ml塗布,3分鐘后在流水(自來水,1l/min)中水洗5秒鐘。其結果是,icg沒有被完全水洗掉,本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物容易被水洗掉,顯示本發明的環糊精結合吲哚菁化合物表示的化合物在纖維素纖維上的吸附性顯著低于icg(圖2)。<試驗10:本發明環糊精結合吲哚菁化合物向生物體肉模型的吸附性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)進行了向生物體的肉模型的吸附性試驗。生物體肉模型選用市場上販賣的豬里脊肉,在豬里脊肉上制作直徑5mm的凹部,icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別取1mm水溶液0.05ml塗布,3分鐘后在流水(自來水,1l/min)中水洗10秒鐘。其結果是,icg沒有被完全水洗掉,本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物容易被水洗掉,顯示本發明的環糊精結合吲哚菁化合物在生物體肉模型上的吸附性顯著低于icg(圖3)。<試驗11:本發明的環糊精結合吲哚菁化合物向生物體蛋白質模型的吸附性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)進行了向生物體蛋白質模型的吸附性試驗。生物體蛋白質模型選用市場上販賣的雞胸肉,在雞胸肉上制作直徑5mm的凹部,icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別取1mm水溶液0.05ml塗布,3分鐘后在流水(自來水,1l/min)中水洗10秒鐘。其結果,icg沒有被完全水洗掉,本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物容易被水洗掉,顯示本發明的環糊精結合吲哚菁化合物在生物體蛋白質模型上的吸附性顯著低于icg(圖4)。<試驗12:本發明的環糊精結合吲哚菁化合物向疏水性化學纖維的吸附性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)進行了向疏水性化學纖維的吸附性試驗。疏水性化學纖維的模型選用聚丙烯口罩(玉川衛材株式會社),icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別取1mm水溶液0.05ml塗布,放置20分鐘后(樣品中有水分的話就不附著在口罩上,所以為了除去水分放置20分鐘)在流水(自來水,1l/min)中水洗1秒鐘。其結果,icg沒有被完全水洗掉,本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物容易被水洗掉,顯示本發明的環糊精結合吲哚菁化合物向疏水性化學纖維的吸附性顯著低于icg(圖5)。<試驗13:本發明環糊精結合吲哚菁化合物在水溶液中的分子締合性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)在水溶液中的分子締合性進行了研究。分別配制icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)的0.01mm、0.025mm、0.05mm、0.1mm水溶液,裝入光路長1mm的石英比色皿中,測定25℃下600nm至1000nm的光吸收光譜。其結果是,icg在此濃度范圍內產生了被稱作h-聚集的分子締合(圖6左圖),本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物在此濃度范圍內沒有產生被稱作h-聚集的分子締合(圖6右圖)。<試驗14:本發明的環糊精結合吲哚菁化合物在水溶液中的熒光性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)在水溶液中的熒光性進行了研究。icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別取0.1μm水溶液,在25℃裝入1cm見方石英比色皿中,用720nm的激發光(帶通:10nm)激發,測定熒光光譜(帶通:10nm)。熒光效率是以icg的熒光效率0.13(在dmso中,25℃)為基礎計算。其結果,icg的熒光量子效率是0.021,本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物的熒光量子效率是0.054及0.042,熒光量子效率是icg的2.6倍和2倍。<試驗15:本發明的環糊精結合吲哚菁化合物在血液中的熒光性>對icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)在血液中的熒光性進行了研究。將icg及本發明的環糊精結合吲哚菁化合物(化學式16、20、21、23~25)分別溶解于血液(人)中以達到100μm。并在25℃裝入三角石英比色皿中,用760nm的激發光(帶通:10nm)激發,測定表面熒光光譜(帶通:10nm)。極大熒光波長中的熒光強度是,icg為58(任意單位)。本發明的環糊精結合吲哚菁化合物特別是化學式16及化學式20表示的化合物的熒光強度是270(任意單位)及190(任意單位),是icg的4.7倍和3.3倍。這可以認為是因為本發明的環糊精結合吲哚菁化合物在生物體內中不阻礙發光。<試驗16:關于本發明的環糊精結合吲哚菁化合物在生物體內的行為>作為代表例子,關于化學式19及20表示的異構化平衡化合物(tk1)和化學式15及16表示的異構化平衡化合物(tk2),對作為生物體對象物的人類血液以及大鼠體內的行為進行了評價。·人類血液中的熒光行為關于icg、tk1及tk2,對于在三角比色皿中的人類靜脈血中的表面熒光強度的濃度相關性進行了評價。具體地,在三角石英比色皿中加入人類靜脈血液1.0ml,并添加規定濃度的icg、tk1及tk2。在25℃照射760nm(帶通:10nm)的激發光后,測定表面熒光(帶通:10nm)。將結果表示在圖7。從圖7中可以明確知道,tk1及tk2都可以在人類靜脈血中通過激發光的照射發出熒光。·向大鼠體內給藥可能性的研究將icg、tk1及tk2分別配制成濃度1mm的水溶液,各取0.1ml,在開腹大鼠的大腿靜脈剝露出后進行注射。其后,用760nm的激發光照射開腹部,評價有無熒光。其結果,在開腹部中的內臟觀察到了熒光。觀察到tk1及tk2在腎臟的集聚高(如已知icg在肝臟的集聚高)。另外,沒有確認到這些給藥對大鼠的病情非常嚴重的影響,而能夠確認到比較安全的生物體內給藥的可能性。·大鼠體內分布的觀察將wistar雄大鼠(9周齡,體重350g)用乙醚麻醉后,將戊巴比妥鈉(nembutal)0.1ml用26g針腹腔內給藥來麻醉。大鼠的尾巴根部用橡膠帶驅血,用24g留置針確保尾靜脈,并連接3頭方活栓和延長管而確保末梢線。將大鼠以仰臥姿勢固定在平面臺上(圖8)。將濱松光子學株式會社制pde攝像機單元正確設置于離大鼠身體16cm的位置。但對全身范圍攝影時固定在20cm處。觀察范圍是圖8中黒圈表示程度的范圍。其后,通過確保的末梢線,給藥濃度1mm的icg和tk1及tk2。給藥量為0.1ml。將給藥20分鐘后開腹時的腹腔內的熒光的情況表示在圖9,足背部的熒光的情況表示在(達到最高亮度時的畫像)圖12。圖9表示,icg主要在肝臟(圖9(a)),tk1主要在腎臟(圖9(b)),tk2也主要在腎臟(圖9(c))集聚。給藥后立刻對內臟進行近紅外攝像的結果,顯示出能夠鮮明地攝像腎臟、輸尿管、膀胱(圖10)。另外,顯示出能夠應用近紅外內視鏡攝像輸尿管(圖11)。由攝像圖12可知,在足背部中的對應血液流動發出熒光的情況被明確。另外,雖然圖中沒有顯示,對結扎大鼠右大腿動脈的下肢缺血模型同樣給藥icg、tk1及tk2后觀察熒光的結果,由于缺血部分中沒有確認到熒光,因此可以依賴有無熒光來評價血流的程度。在這里,圖13和圖14表示足背部的熒光強度經時間的變化。另外,在表1中表示到達最大熒光強度值(imax)的時間、imax值、達到imax值一半時的時間(t1/2)。[表1]化合物imax到達時間imax*t1/2icg0.5min1242.3mintk-110min16040mintk-215min10655min由表1、圖13和圖14可知,tk1以及tk2的最大熒光強度值達到時間、減半時間與icg比較都要更長。也就是說,能長時間在體內發出熒光。例如,相對于icg給藥后不到10分鐘熒光強度下降到初始值,tk1及tk2在給藥后經過1小時后也顯示高的熒光強度。·血管水平上的觀察根據非專利文獻7及8披露的方法(圖15),在大鼠血管直接露出的狀態下給藥icg、tk1進行觀察。露出后的精巣提睪肌皮瓣的情況如圖16所示。其結果,icg相對于tk1在血管內顯現為不均勻。也就是說,可知tk1從血管向間質液中移動。為了更精密地進行研究,將給藥后血管的顯微鏡照片表示在圖17(icg)和圖18(tk1)。由圖17及18可知,分別比較血管中的熒光強度和其周邊組織中的熒光強度時,icg在間質內幾乎確認不到熒光,相對于此tk1則確認到在間質內的熒光。另外,雖然沒有詳細表示,但確認到間質內的熒光強度是經時增加的。因此,icg幾乎確認不到從血管向間質液中的移動,但tk1確認到從血管向間質液中的移動。·本發明的環糊精結合吲哚菁化合物在間質內移動的程度和浮腫形成的大小之間的關聯的評價(評價方法)選用大鼠(雄性,wister大鼠)10周齡約350g作為試驗動物(n=4)。對大鼠用異氟烷進行全身麻醉,在左后足跖上用26g針注射0.5%λ卡拉膠0.1ml。結果,迅速出現足浮腫。15分鐘后用大鼠足跖體積測量器(室町機械株式會社制:mk-101cmpplethysmometer)測量了大鼠的左足體積。此后關閉異氟烷確認了大鼠覺醒。實施vonfreytest后,再次用異氟烷進行全身麻醉。將大鼠的尾靜脈用24g留置針確保后,以仰臥位姿勢固定在水平臺上。設置濱松光子學株式會社制pde攝像頭,固定在離大鼠足背16cm的高度。用pde攝像頭將測定的部位(roi)設定在足背中央部消燈。測量開始后,將1mmoltk1水溶液0.1ml經尾靜脈注入,用1ml的生理食鹽水沖洗5秒。在注入的最初5分鐘進行連續拍攝,測量roi的亮度。以后以5分鐘間隔測定1分鐘亮度,持續到注入后120分鐘為止。測量結束后,關閉異氟烷返還為覺醒(急性炎癥實驗)。7日后,進行大鼠的vonfreytest后,迅速對大鼠用異氟烷進行全身麻醉,用大鼠足跖體積測量器測量大鼠的左足體積。將大鼠的尾靜脈用24g留置針確保后,以仰臥位姿勢固定在水平臺上。設置濱松光子學株式會社制pde攝像頭,固定在離大鼠足背16cm的高度。將roi設定在足背中央部,消燈后開始測定。將1mmoltk1水溶液0.1ml從尾靜脈注入,用1ml的生理食鹽水沖洗5秒。在注入的最初5分鐘進行連續拍攝,測量roi的亮度。以后間隔5分鐘測量1分鐘亮度,持續到注入后120分鐘為止。測量結束后,關閉異氟烷返還為覺醒。對于沒有注射λ卡拉膠的群也進行了同樣試驗。icg也同樣實行了以上的過程。(結果)在圖19~26表示結果。將對于給藥tk1的群進行測定的大鼠的左足容積表示在圖19(越向縱軸的上方體積越大),將vonfreytest的結果表示在圖20(越向縱軸的下方越是痛覺過敏),將注射后不久的亮度的變化情況表示在圖21(越向縱軸的上方亮度越大),將注射卡拉膠后經過1周后的亮度的變化情況表示在圖23(越向縱軸的上方亮度大)。將對于給藥icg的群進行測定的大鼠的左足容積表示在圖23(越向縱軸的上方體積越大),將vonfreytest的結果表示在圖24(越向縱軸的下方越是痛覺過敏),將注射后不久的亮度的變化情況表示在圖25(越向縱軸上方亮度越大),將注射卡拉膠后經過1周后的亮度的變化情況表示在圖26(越向縱軸上方亮度大)。全部的圖表的縱軸的值是任意單位。確認了icg和tk1之間在roi中的亮度的變化圖案上有大的差異。在icg給藥后的短時間內急速增強的亮度在此后迅速轉為減少,約10分鐘后下降到了基線。相對于此,tk1給藥后的早期的亮度的增強呈現出與icg同樣的軌跡,其后亮度居高不下,恢復到基線需要6小時。根據該結果我們認為icg滯留于血管內沒有向間質內漏出,因此急速的亮度的増強和其后的急速的衰減是由于分布在roi的血管內的通過。相對于此,tk1則反映出了反映一開始的急速向血管內的通過的部分(以后稱“血管相”)和其后逐漸向間質漏出的tk1發出熒光的相(以下稱“間質相”)的兩個相。從血管相向間質相移動的時間對應于規定時間。急性炎癥實驗中對于icg、tk1兩個群而言,大鼠足容積在注射λ卡拉膠后被確認有顯著的容積增加,1周后則恢復正常到與腱側相同(圖19、23)。另外,對icg、tk1兩個群中,在vonfreytest中注射λ卡拉膠后有非常明顯的痛覺過敏,1周后則恢復正常與腱側相同(圖20、24)。關于足背的亮度,tk1群在血管相的亮度變化的情況與對照群之間沒有差距,但間質相中比λ卡拉膠給藥群更迅速增加亮度,在整個評價時間都保持了高的值(圖21)。給藥λ卡拉膠而炎癥消退后的給藥1周后,卡拉膠給藥側與腱側之間在間質相的亮度變化上并無差別(圖22)。如圖21中的曲線明確表示,在間質相的亮度的推移以光滑的曲線推移,該曲線的高度依存于間質相的向上的變化率。換句話說,間質相的值的變化能夠根據時系列解析以高精度預測,是我們在本工作中假設成立的重要根據。icg群則在注射λ卡拉膠后立刻和1周后都未能確認亮度的差異(圖25、圖26)。該結果表示以往應用于臨床的疏水性高的icg即使存在由λ卡拉膠等引起的高度的急性炎癥,也不會發生向血管外的熒光物質的泄漏。由以上結果可知,將tk1給藥生物體后,在與間質相相當的期間,可以對預測腫脹進展部位的熒光強度進行經時測定,由此可以對其后的熒光強度的推移進行預測,其熒光強度的推移與其部位的腫脹的進展有關系。因此tk1可以適用于icg所不能進行的腫脹的預測。產業上的利用可能性根據本發明的化學式1或化學式2表示的環糊精結合吲哚菁化合物,可提供具有如下特征的屬于綠色色素的發出近紅外熒光的化合物:與icg相比,在水或生理食鹽水中的溶解性高,易從生物體組織除去,水溶液中的分子締合低,水溶液中的近紅外熒光強度高,不含碘。另外,根據本發明的環糊精結合吲哚菁化合物的合成法,能夠提供有用的環糊精結合吲哚菁化合物的合成。另外,根據本發明的環糊精結合吲哚菁化合物的精制法,能夠提供有用的環糊精結合吲哚菁化合物的精制。進而,由于本發明的環糊精結合吲哚菁化合物即使不含碘也顯示足夠的溶解性,因此能夠提供不含碘過敏癥的原因的碘的診斷用組合物。這些診斷用組合物表現出與現有的只含icg的診斷用組合物不同的體內行為,因此可利用其性質提供各種各樣的有益的診斷法和診斷裝置。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1