光學活性1,5?戊二醇衍生物及其合成方法和應用與流程
本發明屬于合成醫藥化工領域,主要涉及光學活性1,5-戊二醇衍生物及其化學合成方法和應用。
背景技術:
1,5-戊二醇衍生物是重要的化工中間體,廣泛用于聚酯、聚氨酯、增塑劑、涂料、香料、粘合劑、墨水、纖維、藥物中間體、密封劑以及鉛印等產品。近來,中國專利cn101316508a報道了1,5-戊二醇的組合可以用于減少和/或消除來自哺乳動物的氣味,該氣味如來自尿、糞便、腿部潰瘍液體、褥瘡性潰瘍、血液和汗液的氣味,可以用于制作吸收性產品或一次性衛生產品。因此合成1,5-戊二醇衍生物具有重要意義。
近年來已有大量文獻報道了1,5-戊二醇衍生物的合成方法。中國專利cn1072168a報道了以取代的乙烯基乙醚和取代的丙烯醛反應,生成取代的3,4-二氫吡喃,取代的3,4-二氫吡喃酸催化水解生成取代的戊二醛,然后將鎳負載在氧化鋁上做催化劑進行加氫反應生成取代的戊二醇。中國專利cn101225022a報道了以鎳-a/x負載型催化劑催化的戊二醛加氫反應獲得戊二醇,其中組分a為co、mn、cu、cr等,載體x為分子篩、al2o3、sio2等。但是上述制取1,5-戊二醇衍生物的方法中,其共同存在的問題是催化加氫反應壓力普遍都很高,這樣勢必對反應設備的壓力要求較高,相應地就會使生成裝置的一次性投資增高,生產成本增加,同時也會加大生產中的操作難度。同時,通過上述催化加氫法實現不對稱的合成光學活性1,5-戊二醇衍生物也是很難的。不利于光學活性1,5-戊二醇衍生物在工業和有機合成中的應用及其工業化合成。
技術實現要素:
本發明克服了現有技術合成光學活性1,5-戊二醇衍生物的上述缺陷,提出了一種光學活性1,5-戊二醇衍生物及其制備方法。本發明制備方法中使用三組分的方法構建了比已有兩組份方法更為復雜的光學活性1,5-戊二醇衍生物;本發明制備方法中使用的原料手性二芳基脯氨醇硅醚是天然存在的手性氨基酸衍生物,化學合成價廉易得;本發明制備方法具有高效原子經濟性,高對映選擇性,高產率,底物適用范圍廣,操作簡單安全等有益效果。本發明制備的光學活性1,5-戊二醇衍生物具有高對映選擇性,對hct116(人結腸癌細胞)有明顯抑制作用,適用于抗腫瘤藥物的制備應用。
本發明提出的光學活性1,5-戊二醇衍生物,其結構如式(ia)和式(ib)所示,
其中,ar1為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基、硝基取代的苯基;
ar2為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基;
ar3為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基。
優選地,所述ar1為芳基,選自于苯基、4-氟苯基、4-氯苯基、4-溴苯基、3-溴苯基、4-甲氧基苯基、4-甲基苯基、4-硝基苯基、3-甲基苯基、2-甲基苯基、或3-甲氧基苯基;
ar2為芳基,選自于苯基、2-甲基苯基、2-溴苯基、3-甲基苯基、3-甲氧基苯基、4-甲基苯基、4-溴苯基、4-氟苯基、或4-甲氧基苯基;
ar3為芳基,選自于苯基、2-甲基苯基、2-溴苯基、3-甲基苯基、3-溴苯基、3-甲氧基苯基、4-甲基苯基、4-溴苯基、4-氟苯基、或4-甲氧基苯基。
進一步優選地,所述光學活性1,5-戊二醇衍生物選自:
(2s,3s)-2-芐氧基-2-苯基-3-間甲基苯基-1,5-戊二醇(1a)
(2r,3s)-2-芐氧基-2-苯基-3-間甲基苯基-1,5-戊二醇(1b)
(2s,3s)-2-芐氧基-2-苯基-3-對甲基苯基-1,5-戊二醇(2a)
(2r,3s)-2-芐氧基-2-苯基-3-對甲基苯基-1,5-戊二醇(2b)
(2s,3s)-2-芐氧基-2-苯基-3-對甲氧基苯基-1,5-戊二醇(3a)
(2r,3s)-2-芐氧基-2-苯基-3-對甲氧基苯基-1,5-戊二醇(3b)
(2s,3s)-2-對溴芐氧基-2,3-雙苯基-1,5-戊二醇(4a)
(2r,3s)-2-對溴芐氧基-2,3-雙苯基-1,5-戊二醇(4b)
(2s,3s)-2-間溴芐氧基-2,3-雙苯基-1,5-戊二醇(5a)
(2r,3s)-2-間溴芐氧基-2,3-雙苯基-1,5-戊二醇(5b)
(2s,3s)-2-對甲氧基芐氧基-2,3-雙苯基-1,5-戊二醇(6a)
(2r,3s)-2-對甲氧基芐氧基-2,3-雙苯基-1,5-戊二醇(6b)
(2s,3s)-2-芐氧基-2-間甲氧基苯基-3-苯基-1,5-戊二醇(7a)
(2r,3s)-2-芐氧基-2-間甲氧基苯基-3-苯基-1,5-戊二醇(7b)
(2s,3s)-2-芐氧基-2-鄰溴苯基-3-苯基-1,5-戊二醇(8a)
(2r,3s)-2-芐氧基-2-鄰溴苯基-3-苯基-1,5-戊二醇(8b)
(2s,3s)-2-芐氧基-2-對甲基苯基-3-苯基-1,5-戊二醇(9a)
(2r,3s)-2-芐氧基-2-對甲基苯基-3-苯基-1,5-戊二醇(9b)
(2s,3s)-2-芐氧基-2-對溴苯基-3-苯基-1,5-戊二醇(10a)
(2r,3s)-2-芐氧基-2-對溴苯基-3-苯基-1,5-戊二醇(10b)
本發明提出的光學活性1,5-戊二醇衍生物具有兩個手性中心,包括式(ia)和式(ib)所示的一對光學活性1,5-戊二醇衍生物。
本發明還提出了所述式(ia)和式(ib)光學活性1,5-戊二醇衍生物的合成方法,在有機溶劑中,以式(1)α,β-不飽和醛、式(2)重氮化合物、式(3)芐醇衍生物為原料,以
具體地,所述方法包括以下步驟:在有機溶劑中,以式(1)α,β-不飽和醛、式(2)重氮化合物、式(3)芐醇衍生物為原料,以
其中,ar1為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基、硝基取代的苯基;
ar2為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基;
ar3為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基。
優選地,所述ar1為芳基,選自于苯基、4-氟苯基、4-氯苯基、4-溴苯基、3-溴苯基、4-甲氧基苯基、4-甲基苯基、4-硝基苯基、3-甲基苯基、2-甲基苯基、或3-甲氧基苯基;
ar2為芳基,選自于苯基、2-甲基苯基、2-溴苯基、3-甲基苯基、3-甲氧基苯基、4-甲基苯基、4-溴苯基、4-氟苯基、或4-甲氧基苯基;
ar3為芳基,選自于苯基、2-甲基苯基、2-溴苯基、3-甲基苯基、3-溴苯基、3-甲氧基苯基、4-甲基苯基、4-溴苯基、4-氟苯基、或4-甲氧基苯基。
進一步優選地,所述光學活性1,5-戊二醇衍生物選自:
(2s,3s)-2-芐氧基-2-苯基-3-間甲基苯基-1,5-戊二醇(1a)
(2r,3s)-2-芐氧基-2-苯基-3-間甲基苯基-1,5-戊二醇(1b)
(2s,3s)-2-芐氧基-2-苯基-3-對甲基苯基-1,5-戊二醇(2a)
(2r,3s)-2-芐氧基-2-苯基-3-對甲基苯基-1,5-戊二醇(2b)
(2s,3s)-2-芐氧基-2-苯基-3-對甲氧基苯基-1,5-戊二醇(3a)
(2r,3s)-2-芐氧基-2-苯基-3-對甲氧基苯基-1,5-戊二醇(3b)
(2s,3s)-2-對溴芐氧基-2,3-雙苯基-1,5-戊二醇(4a)
(2r,3s)-2-對溴芐氧基-2,3-雙苯基-1,5-戊二醇(4b)
(2s,3s)-2-間溴芐氧基-2,3-雙苯基-1,5-戊二醇(5a)
(2r,3s)-2-間溴芐氧基-2,3-雙苯基-1,5-戊二醇(5b)
(2s,3s)-2-對甲氧基芐氧基-2,3-雙苯基-1,5-戊二醇(6a)
(2r,3s)-2-對甲氧基芐氧基-2,3-雙苯基-1,5-戊二醇(6b)
(2s,3s)-2-芐氧基-2-間甲氧基苯基-3-苯基-1,5-戊二醇(7a)
(2r,3s)-2-芐氧基-2-間甲氧基苯基-3-苯基-1,5-戊二醇(7b)
(2s,3s)-2-芐氧基-2-鄰溴苯基-3-苯基-1,5-戊二醇(8a)
(2r,3s)-2-芐氧基-2-鄰溴苯基-3-苯基-1,5-戊二醇(8b)
(2s,3s)-2-芐氧基-2-對甲基苯基-3-苯基-1,5-戊二醇(9a)
(2r,3s)-2-芐氧基-2-對甲基苯基-3-苯基-1,5-戊二醇(9b)
(2s,3s)-2-芐氧基-2-對溴苯基-3-苯基-1,5-戊二醇(10a)
(2r,3s)-2-芐氧基-2-對溴苯基-3-苯基-1,5-戊二醇(10b)
具體地,所述方法包括:(1)在有機溶劑中,以式(1)α,β-不飽和醛、式(2)重氮化合物、式(3)芐醇衍生物為原料,以
更具體地,所述方法包括:將α,β-不飽和醛、金屬催化劑、手性二芳基脯氨醇硅醚、取代苯甲酸和
本發明方法中,所述合成光學活性1,5-戊二醇衍生物的反應的溫度為0~50℃;優選地,為25℃、40℃。進一步優選地,所述反應中兩步反應溫度不同,步驟(1)反應的溫度為0~40℃,步驟(2)反應的溫度為20~50℃;優選地,步驟(1)反應的溫度為25℃,步驟(2)反應的溫度為40℃。
本發明方法中,式(2)重氮化合物:式(3)芐醇衍生物:式(1)α,β-不飽和醛:金屬催化劑:手性二芳基脯氨醇硅醚:取代苯甲酸:金屬負氫試劑的摩爾比為1.0-3.0:1.0-2.5:1.0:0.05-0.2:0.15-0.2:0.15-0.5:10。優選地,重氮化合物:芐醇衍生物:α,β-不飽和醛:金屬催化劑:手性二芳基脯氨醇硅醚:取代苯甲酸:金屬負氫試劑的摩爾比為3.0:2.5:1.0:0.2:0.2:0.5:10、1.0:1.0:1.0:0.05:0.15:0.15:10、2.0:2.0:1.0:0.1:0.2:0.4:10。
本發明方法中,還可以包括對反應得到的光學活性1,5-戊二醇衍生物進行分離純化的步驟,第一步反應的分離純化用體積比為乙酸乙酯:石油醚=1:500~1:80洗脫劑進行柱層析,第二步反應的分離純化用體積比為乙酸乙酯:石油醚=1:50~1:8洗脫劑進行柱層析。優選地,第一步反應的分離純化用體積比為乙酸乙酯:石油醚=1:100洗脫劑進行柱層析,第二步反應的分離純化用體積比為乙酸乙酯:石油醚=1:10洗脫劑進行柱層析。
本發明方法中,所述有機溶劑包括二氯甲烷、四氫呋喃、甲苯或氯仿;優選地,為二氯甲烷。
本發明方法中,所述金屬催化劑為銥復合物,銠復合物或鈀復合物;優選地,所述金屬催化劑為銥復合物;進一步優選地,為雙(1,5-環辛二烯)四氟硼酸銥。
本發明方法中,所述手性二芳基脯氨醇硅醚結構如式(ⅲ)所示,
其中,r1為三甲基硅基,三乙基硅基或二甲基叔丁基硅基;ar4為苯基或3,5-雙三氟甲基苯基。優選地,r1為二甲基叔丁基硅基,ar4為苯基。
本發明方法中,所述取代苯甲酸結構如式(ⅳ)所示,
其中,r包括氫、3,5-雙三氟甲基、硝基、甲氧基、鹵素。優選地,r為4-硝基。
本發明方法中,所述金屬負氫試劑為四氫鋁鋰或硼氫化鈉;優選地,為硼氫化鈉。
在一個具體實施方案中,本發明中光學活性1,5-戊二醇衍生物的合成方法為:第一步反應,按重氮化合物、芐醇衍生物、α,β-不飽和醛、銥復合物、手性二芳基脯氨醇硅醚、取代苯甲酸摩爾比為2.0:2.0:1.0:0.1:0.2:0.4稱取原料,以α,β-不飽和醛用量為基準量取
本發明中,所述如式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物為一對高對映選擇性的化合物。
本發明還提出了由本發明所述合成方法制備得到的如式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物;所述式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物具有兩個手性中心。
本發明還提出了如式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物;所述式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物具有兩個手性中心。
本發明還提出了如式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物在制備醫藥中間體中的應用。
本發明還提出了如式(ia)和式(ib)所示的光學活性1,5-戊二醇衍生物在制備抗腫瘤藥物中的應用。其中,所述腫瘤疾病包括結腸癌等。
本發明還提出了如式(ia)和式(ib)所示的一對高對映選擇性的光學活性1,5-戊二醇衍生物在制備抗結腸癌藥物中的應用。
本發明提出的具有兩個手性中心的如式(ia)和式(ib)所示的一對光學活性1,5-戊二醇衍生物是重要的化工和醫藥中間體,在醫藥化工領域廣泛應用,具有很大應用前景。本發明的制備方法以廉價易得的化合物為原料,具有反應條件溫和、反應步驟少、反應快、成本低、產生的廢物少、操作簡單安全、原子經濟性高、選擇性高、產率高等有益效果。
附圖說明
圖1是實施例1所得產物(1a)的1hnmr示意圖。
圖2是實施例1所得產物(1a)的13cnmr示意圖。
圖3為實施例1所得產物(1a)的消旋產物液相圖。
圖4為實施例1所得產物(1a)的手性產物液相圖。
圖5是實施例1所得產物(1b)的1hnmr示意圖。
圖6是實施例1所得產物(1b)的13cnmr示意圖。
圖7為實施例1所得產物(1b)的消旋產物液相圖。
圖8為實施例1所得產物(1b)的手性產物液相圖。
圖9是實施例2所得產物(2a)的1hnmr示意圖。
圖10是實施例2所得產物(2a)的13cnmr示意圖。
圖11為實施例2所得產物(2a)的消旋產物液相圖。
圖12為實施例2所得產物(2a)的手性產物液相圖。
圖13是實施例2所得產物(2b)的1hnmr示意圖。
圖14是實施例2所得產物(2b)的13cnmr示意圖。
圖15為實施例2所得產物(2b)的消旋產物液相圖。
圖16為實施例1所得產物(2b)的手性產物液相圖。
圖17是實施例3所得產物(3a)的1hnmr示意圖。
圖18是實施例3所得產物(3a)的13cnmr示意圖。
圖19為實施例3所得產物(3a)的消旋產物液相圖。
圖20為實施例3所得產物(3a)的手性產物液相圖。
圖21是實施例3所得產物(3b)的1hnmr示意圖。
圖22是實施例3所得產物(3b)的13cnmr示意圖。
圖23為實施例3所得產物(3b)的消旋產物液相圖。
圖24為實施例3所得產物(3b)的手性產物液相圖。
圖25是實施例4所得產物(4a)的1hnmr示意圖。
圖26是實施例4所得產物(4a)的13cnmr示意圖。
圖27為實施例4所得產物(4a)的消旋產物液相圖。
圖28為實施例4所得產物(4a)的手性產物液相圖。
圖29是實施例4所得產物(4b)的1hnmr示意圖。
圖30是實施例4所得產物(4b)的13cnmr示意圖。
圖31為實施例4所得產物(4b)的消旋產物液相圖。
圖32為實施例4所得產物(4b)的手性產物液相圖。
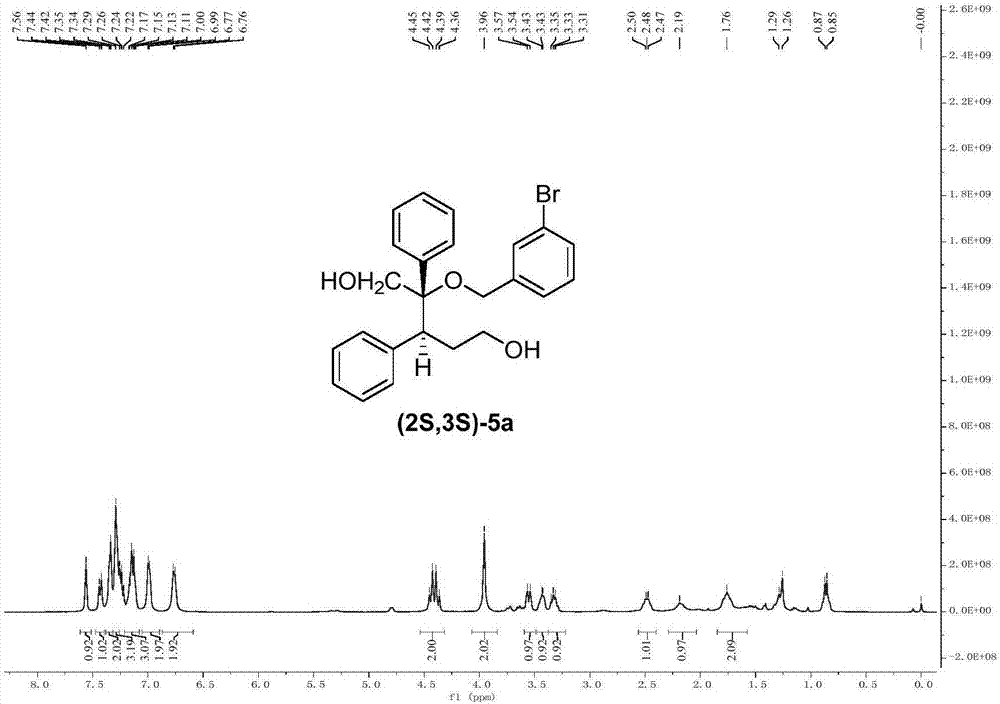
圖33為實施例5所得產物(5a)的的1hnmr示意圖。
圖34為實施例5所得產物(5a)的13cnmr示意圖。
圖35為實施例5所得產物(5a)的消旋產物液相圖。
圖36為實施例5所得產物(5a)的手性產物液相圖。
圖37為實施例5所得產物(5b)的1hnmr示意圖。
圖38為實施例5所得產物(5b)的13cnmr示意圖。
圖39為實施例5所得產物(5b)的消旋產物液相圖。
圖40為實施例5所得產物(5b)的手性產物液相圖。
圖41為實施例6所得產物(6a)的1hnmr示意圖。
圖42為實施例6所得產物(6a)的13cnmr示意圖。
圖43為實施例6所得產物(6a)的消旋產物液相圖。
圖44為實施例6所得產物(6a)的手性產物液相圖。
圖45為實施例6所得產物(6b)的1hnmr示意圖。
圖46為實施例6所得產物(6b)的13cnmr示意圖。
圖47為實施例6所得產物(6b)的消旋產物液相圖。
圖48為實施例6所得產物(6b)的手性產物液相圖。
圖49為實施例7所得產物(7a)的1hnmr示意圖。
圖50為實施例7所得產物(7a)的13cnmr示意圖。
圖51為實施例7所得產物(7a)的消旋產物液相圖。
圖52為實施例7所得產物(7a)的手性產物液相圖。
圖53為實施例7所得產物(7b)的1hnmr示意圖。
圖54為實施例7所得產物(7b)的13cnmr示意圖。
圖55為實施例7所得產物(7b)的消旋產物液相圖。
圖56為實施例7所得產物(7b)的手性產物液相圖。
圖57為實施例8所得產物(8a)的1hnmr示意圖。
圖58為實施例8所得產物(8a)的13cnmr示意圖。
圖59為實施例8所得產物(8a)的消旋產物液相圖。
圖60為實施例8所得產物(8a)的手性產物液相圖。
圖61為實施例8所得產物(8b)的1hnmr示意圖。
圖62為實施例8所得產物(8b)的13cnmr示意圖。
圖63為實施例8所得產物(8b)的消旋產物液相圖。
圖64為實施例8所得產物(8b)的手性產物液相圖。
圖65為實施例8所得產物(9a)的1hnmr示意圖。
圖66為實施例8所得產物(9a)的13cnmr示意圖。
圖67為實施例8所得產物(9a)的消旋產物液相圖。
圖68為實施例8所得產物(9a)的手性產物液相圖。
圖69為實施例8所得產物(9b)的1hnmr示意圖。
圖70為實施例8所得產物(9b)的13cnmr示意圖。
圖71為實施例8所得產物(9b)的消旋產物液相圖。
圖72為實施例8所得產物(9b)的手性產物液相圖。
圖73為實施例8所得產物(10a)的1hnmr示意圖。
圖74為實施例8所得產物(10a)的13cnmr示意圖。
圖75為實施例8所得產物(10a)的消旋產物液相圖。
圖76為實施例8所得產物(10a)的手性產物液相圖。
圖77為實施例8所得產物(10b)的1hnmr示意圖。
圖78為實施例8所得產物(10b)的13cnmr示意圖。
圖79為實施例8所得產物(10b)的消旋產物液相圖。
圖80為實施例8所得產物(10b)的手性產物液相圖。
圖81是不同濃度的兩種本發明化合物(fb1-3-s、fb1-3-x)對hct116(人結腸癌細胞)的濃度-存活率曲線圖。
具體實施方式
結合以下具體實施例和附圖,對本發明作進一步的詳細說明,本發明的保護內容不局限于以下實施例。在不背離發明構思的精神和范圍下,本領域技術人員能夠想到的變化和優點都被包括在本發明中,并且以所附的權利要求書為保護范圍。實施本發明的過程、條件、試劑、實驗方法等,除以下專門提及的內容之外,均為本領域的普遍知識和公知常識,本發明沒有特別限制內容。
本發明的光學活性1,5-戊二醇衍生物的制備方法,第一步反應,將α,β-不飽和醛、金屬催化劑、手性二芳基脯氨醇硅醚、取代苯甲酸和
其中,ar1為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基、硝基取代的苯基;
ar2為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基;
ar3為芳基,選自于苯基、鹵素取代的苯基、甲氧基取代的苯基、c1-c3烷基取代的苯基。
實施例1
第一步反應,將3-甲基肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(1a)的1hnmr示意圖如圖1所示,其13cnmr示意圖如圖2所示,其消旋產物液相圖如圖3所示,其手性產物液相圖如圖4所示。
1hnmr(400mhz,cdcl3)δ7.34(dt,j=14.8,7.2hz,4h),7.23(td,j=5.6,3.8hz,3h),7.19(s,1h),6.96(d,j=3.7hz,2h),6.87(d,j=8.0hz,2h),6.57(d,j=6.8hz,2h),4.37(s,2h),3.86(s,2h),3.46(dd,j=11.6,3.2hz,1h),3.34(ddd,j=20.6,12.5,6.5hz,2h),2.45(ddd,j=10.1,6.7,3.9hz,1h),2.21(s,3h),1.93(s,1h),1.70–1.57(m,1h).
13cnmr(100mhz,cdcl3)δ138.59,137.29,136.48,136.07,129.92,128.58,128.40,127.96,127.66,127.58,127.14,84.08,77.32,77.01,76.69,64.85,62.00,61.83,47.60,31.69,21.03.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=33.13分鐘,tminor=8.15分鐘.
光學活性產物(1b)的1hnmr示意圖如圖5所示,其13cnmr示意圖如圖6所示,其消旋產物液相圖如圖7所示,其手性產物液相圖如圖8所示。
1hnmr(400mhz,cdcl3)δ7.39–7.25(m,6h),7.20(dd,j=12.4,4.5hz,4h),7.06(d,j=7.7hz,2h),6.99(d,j=7.6hz,2h),4.51(q,j=12.1hz,2h),4.08–3.91(m,2h),3.33–3.22(m,1h),3.11(dd,j=15.6,9.2hz,1h),2.99(dd,j=11.4,2.7hz,1h),2.23(d,j=14.4hz,3h),2.05–1.93(m,1h),1.86(s,1h),1.55–1.48(m,2h).
13cnmr(100mhz,cdcl3)δ140.51,139.39,136.62,136.55,129.91,128.80,128.44,128.41,127.34,127.17,126.88,126.75,84.15,77.34,77.02,76.71,65.71,65.66,61.18,52.10,32.81,21.06.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=7.39分鐘,tminor=12.91分鐘.
實施例2
第一步反應,將4-甲基肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(2a)的1hnmr示意圖如圖9所示,其13cnmr示意圖如圖10所示,其消旋產物液相圖如圖11所示,其手性產物液相圖如圖12所示。
1hnmr(400mhz,cdcl3).δ7.39–7.27(m,4h),7.27–7.16(m,4h),6.99–6.84(m,4h),6.44(s,2h),4.37(s,2h),3.86(s,2h),3.44(dd,j=11.6,3.2hz,1h),3.36(ddd,j=11.8,7.5,4.7hz,1h),3.28(dd,j=16.3,8.7hz,1h),2.52–2.38(m,1h),2.11(s,3h),1.98(d,j=24.6hz,1h),1.71–1.61(m,1h),1.38–1.36(m,1h).
13cnmr(100mhz,cdcl3)δ139.15,138.62,137.38,137.05,130.88,128.58,127.99,127.67,127.61,127.59,127.49,127.16,84.04,77.35,77.04,76.72,64.86,62.03,61.79,47.95,31.66,21.34.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=17.58分鐘,tminor=6.54分鐘。
光學活性產物(2b)的1hnmr示意圖如圖13所示,其13cnmr示意圖如圖14所示,其消旋產物液相圖如圖15所示,其手性產物液相圖如圖16所示。
1hnmr(400mhz,cdcl3)δ7.44–7.26(m,9h),7.25–7.23(m,1h),7.14(t,j=7.7hz,1h),7.04(t,j=8.1hz,3h),4.59(dd,j=27.1,12.0hz,2h),4.08(s,2h),3.36(ddd,j=11.1,6.9,4.5hz,1h),3.20(dd,j=15.8,9.4hz,1h),3.08(dd,j=11.6,3.3hz,1h),2.29(s,3h),2.13–2.01(m,1h),1.93(ddd,j=8.9,6.9,3.4hz,1h),1.36–1.34(m,1h),1.09–1.07(m,1h).
13cnmr(100mhz,cdcl3)δ140.37,139.62,139.34,137.43,131.02,128.39,127.87,127.73,127.37,127.19,126.99,126.91,126.83,84.16,77.33,77.21,77.01,76.69,65.67,65.59,61.23,52.29,32.75,21.43.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=7.46分鐘,tminor=9.88分鐘.
實施例3
第一步反應,將4-甲氧基肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(3a)的1hnmr示意圖如圖17所示,其13cnmr示意圖如圖18所示,其消旋產物液相圖如圖19所示,其手性產物液相圖如圖20所示。
1hnmr(400mhz,cdcl3)δ7.47–7.35(m,4h),7.29(t,j=14.9hz,4h),7.02(s,2h),6.67(s,4h),4.43(s,2h),3.93(s,2h),3.76(s,3h),3.52(dd,j=11.5,2.6hz,1h),3.44(dd,j=13.0,8.8hz,1h),3.40–3.29(m,1h),2.63–2.45(m,1h),2.07(s,1h),1.67(dd,j=15.0,9.0hz,2h).
13cnmr(100mhz,cdcl3)δ158.47,138.59,137.27,131.15,131.01,128.59,127.92,127.69,127.67,127.59,127.15,113.04,84.16,77.35,77.03,76.71,64.88,61.94,61.76,55.14,47.06,31.69.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=22.97分鐘,tminor=8.82分鐘.
光學活性產物(3b)的1hnmr示意圖如圖21所示,其13cnmr示意圖如圖22所示,其消旋產物液相圖如圖23所示,其手性產物液相圖如圖24所示。
1hnmr(400mhz,cdcl3)δ7.33(ddd,j=19.0,13.4,7.1hz,8h),7.24(d,j=7.6hz,2h),7.13(d,j=8.3hz,2h),6.79(d,j=8.4hz,2h),4.57(q,j=12.1hz,2h),4.07(s,2h),3.79(s,3h),3.46–3.29(m,1h),3.27–3.13(m,1h),3.08(dd,j=11.4,2.9hz,1h),1.99(dd,j=20.5,14.8hz,2h),1.66(s,2h).
13cnmr(100mhz,cdcl3)δ158.59,140.34,139.36,131.57,131.00,128.42,127.36,127.19,126.90,126.72,113.41,84.22,77.36,77.04,76.72,65.58,65.47,61.13,55.20,51.38,32.83.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=7.97分鐘,tminor=12.59分鐘.
實施例4
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(4a)的1hnmr示意圖如圖25所示,其13cnmr示意圖如圖26所示,其消旋產物液相圖如圖27所示,其手性產物液相圖如圖28所示。
1hnmr(400mhz,cdcl3)δ7.50(d,j=7.7hz,2h),7.32(d,j=22.0hz,5h),7.21–7.07(m,3h),6.99(s,2h),6.76(s,2h),4.39(dd,j=25.7,11.8hz,2h),3.95(s,2h),3.55(d,j=10.6hz,1h),3.43(s,1h),3.33(d,j=6.6hz,1h),2.56–2.40(m,1h),2.12(s,1h),1.73(dd,j=18.4,13.0hz,2h).
13cnmr(100mhz,cdcl3)δ139.10,137.62,137.23,131.65,130.07,128.77,128.54,127.99,127.79,127.71,126.99,126.07,121.36,84.09,77.35,77.04,76.72,64.22,62.22,61.53,48.03,31.59.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=10:1,流速=1.0毫升/分鐘),tmajor=26.81分鐘,tminor=13.34分鐘.
光學活性產物(4b)的1hnmr示意圖如圖29所示,其13cnmr示意圖如圖30所示,其消旋產物液相圖如圖31所示,其手性產物液相圖如圖32所示。
1hnmr(400mhz,cdcl3)δ7.50(d,j=7.9hz,2h),7.43–7.14(m,12h),4.53(dd,j=33.1,12.3hz,2h),4.06(q,j=12.5hz,2h),3.35(d,j=3.7hz,1h),3.25–3.07(m,2h),2.00(dd,j=23.2,17.4hz,2h),1.64(s,2h).
13cnmr(100mhz,cdcl3)δ139.94,139.59,138.33,131.49,130.08,128.52,128.36,128.02,127.51,127.07,126.82,120.94,84.33,77.35,77.03,76.71,65.58,65.03,60.97,51.97,32.71.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=8.0:1,流速=1.0毫升/分鐘),tmajor=19.29分鐘,tminor=14.99分鐘.
實施例5
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(5a)的1hnmr示意圖如圖33所示,其13cnmr示意圖如圖34所示,其消旋產物液相圖如圖35所示,其手性產物液相圖如圖36所示。
1hnmr(400mhz,cdcl3)δ7.56(s,1h),7.43(d,j=7.7hz,1h),7.34(d,j=5.0hz,2h),7.29(s,3h),7.14(dd,j=15.2,7.5hz,3h),6.99(d,j=4.6hz,2h),6.76(d,j=5.7hz,2h),4.41(dd,j=24.6,11.9hz,2h),3.96(s,2h),3.55(d,j=10.3hz,1h),3.43(d,j=3.6hz,1h),3.38–3.22(m,1h),2.56–2.40(m,1h),2.19(s,1h),1.76(s,2h).
13cnmr(100mhz,cdcl3)δ140.99,139.08,137.29,130.59,130.12,130.10,128.53,127.82,127.77,127.71,126.99,126.08,125.61,122.61,84.10,77.37,77.05,76.73,64.15,62.29,61.47,48.09,31.57.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1毫升/分鐘),tmajor=6.15分鐘,tminor=9.43分鐘.
光學活性產物(5b)的1hnmr示意圖如圖37所示,其13cnmr示意圖如圖38所示,其消旋產物液相圖如圖39所示,其手性產物液相圖如圖40所示。
1hnmr(400mhz,cdcl3)δ7.54(s,1h),7.42(d,j=7.7hz,1h),7.36(t,j=7.3hz,2h),7.29(dd,j=14.8,7.2hz,5h),7.22(t,j=5.5hz,5h),4.55(dd,j=33.2,12.5hz,2h),4.15–3.99(m,2h),3.37(dd,j=9.5,5.2hz,1h),3.25–3.11(m,2h),2.03(dt,j=10.9,7.0hz,1h),1.95(dd,j=13.4,5.3hz,1h),1.62(s,1h),1.14(d,j=8.2hz,1h).
13cnmr(100mhz,cdcl3)δ141.67,139.76,139.46,130.22,130.12,129.93,129.68,128.53,128.06,127.53,127.12,126.83,125.12,122.58,84.37,77.34,77.02,76.70,65.50,64.89,60.99,51.80,32.67.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=20:1,流速=1.0毫升/分鐘),tmajor=5.76分鐘,tminor=9.71分鐘.
實施例6
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(6a)的1hnmr示意圖如圖41所示,其13cnmr示意圖如圖42所示,其消旋產物液相圖如圖43所示,其手性產物液相圖如圖44所示。
1hnmr(400mhz,cdcl3)δ7.36–7.28(m,5h),7.20–7.08(m,3h),7.02(d,j=4.2hz,2h),6.93(d,j=8.6hz,2h),6.74(d,j=5.7hz,2h),4.44–4.28(m,2h),3.92(s,2h),3.83(s,3h),3.55(dd,j=11.3,3.4hz,1h),3.43(ddd,j=11.7,7.4,4.7hz,1h),3.36(dd,j=15.9,9.1hz,1h),2.59–2.46(m,1h),2.07(s,1h),1.78–1.67(m,1h).
13cnmr(100mhz,cdcl3)δ159.20,139.38,137.29,130.56,130.07,128.81,127.98,127.67,127.31,126.90,114.04,84.00,77.34,77.02,76.70,64.64,61.94,61.80,55.32,48.02,31.71.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=38.04分鐘,tminor=20.48分鐘.
光學活性產物(6b)的1hnmr示意圖如圖45所示,其13cnmr示意圖如圖46所示,其消旋產物液相圖如圖47所示,其手性產物液相圖如圖48所示。
1hnmr(400mhz,cdcl3)δ7.47–7.28(m,6h),7.27–7.13(m,6h),6.93(d,j=8.5hz,2h),4.50(q,j=11.5hz,2h),4.19–3.98(m,2h),3.83(s,3h),3.45–3.28(m,1h),3.24–3.14(m,1h),3.11(dd,j=11.4,3.3hz,1h),2.13–1.86(m,2h).
13cnmr(100mhz,cdcl3)δ158.91,140.35,139.82,131.36,130.10,128.40,128.30,127.96,127.38,126.94,113.88,84.13,77.34,77.02,76.71,65.42,61.15,55.32,52.31,32.81.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=22.18分鐘,tminor=38.56分鐘.
實施例7
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(7a)的1hnmr示意圖如圖49所示,其13cnmr示意圖如圖50所示,其消旋產物液相圖如圖51所示,其手性產物液相圖如圖52所示。
1hnmr(400mhz,cdcl3)δ7.46–7.27(m,4h),7.26–7.19(m,1h),7.16–6.96(m,4h),6.81–6.62(m,3h),6.58–6.39(m,2h),4.38(s,2h),3.93–3.76(m,2h),3.59(s,3h),3.48(dd,j=11.6,3.1hz,1h),3.41–3.30(m,1h),3.30–3.17(m,1h),2.52–2.35(m,1h),2.11(brs,1h),1.79–1.65(m,1h),1.53(brs,1h).
13cnmr(100mhz,cdcl3)δ158.05,138.23,138.07,137.60,129.12,127.63,127.54,126.60,126.53,126.07,125.89,119.23,112.67,112.16,83.02,63.94,61.17,60.62,54.10,47.01,30.56.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=9.22分鐘,tminor=8.06分鐘.
光學活性產物(7b)的1hnmr示意圖如圖53所示,其13cnmr示意圖如圖54所示,其消旋產物液相圖如圖55所示,其手性產物液相圖如圖56所示。
1hnmr(400mhz,cdcl3)δ7.40–7.34(m,4h),7.31–7.19(m,7h),6.86–6.79(m,2h),6.77(s,1h),4.58(q,j=12.2hz,2h),4.04(q,j=12.7hz,2h),3.64(s,3h),3.40–3.27(m,1h),3.24–3.08(m,2h),2.13–1.98(m,1h),1.99–1.86(m,1h),1.79(brs,1h),1.42(brs,1h).
13cnmr(100mhz,cdcl3)δ159.67,141.84,139.67,139.36,130.21,129.49,128.41,127.93,127.16,126.97,126.65,118.98,112.99,112.86,84.34,65.70,65.43,61.06,55.09,51.81,32.74.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=6.61分鐘,tminor=10.59分鐘.
實施例8
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(8a)的1hnmr示意圖如圖57所示,其13cnmr示意圖如圖58所示,其消旋產物液相圖如圖59所示,其手性產物液相圖如圖60所示。
1hnmr(400mhz,cdcl3)δ7.54–7.36(m,4h),7.34–7.27(m,3h),7.22–7.08(m,3h),7.06–6.97(m,2h),6.88–6.60(m,2h),4.56–4.29(m,2h),3.94(d,j=4.8hz,2h),3.57(dd,j=11.6,3.2hz,1h),3.49–3.26(m,2h),2.63–2.46(m,1h),2.15–2.00(m,1h),1.82–1.67(m,1h),1.36(s,1h).
13cnmr(100mhz,cdcl3)δ139.27,138.57,137.27,130.10,128.59,127.92,127.71,127.67,127.60,127.15,126.93,84.04,64.88,62.05,61.73,48.02,31.66.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=15.82分鐘,tminor=5.99分鐘.
光學活性產物(8b)的1hnmr示意圖如圖61所示,其13cnmr示意圖如圖62所示,其消旋產物液相圖如圖63所示,其手性產物液相圖如圖64所示。
1hnmr(400mhz,cdcl3)δ7.45–7.35(m,5h),7.34–7.26(m,4h),7.25–7.18(m,5h),4.59(q,j=12.2hz,2h),4.17–3.98(m,2h),3.44–3.31(m,1h),3.25–3.16(m,1h),3.13(dd,j=11.6,3.3hz,1h),2.14–2.03(m,1h),2.01–1.90(m,1h),1.09(brs,1h).
13cnmr(100mhz,cdcl3)δ140.23,139.77,139.32,130.10,128.46,128.43,128.01,127.42,127.20,126.99,126.90,126.72,84.21,65.68,65.55,61.13,52.30,32.81.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=5.77分鐘,tminor=8.11分鐘.
實施例9
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(9a)的1hnmr示意圖如圖65所示,其13cnmr示意圖如圖66所示,其消旋產物液相圖如圖67所示,其手性產物液相圖如圖68所示。
1hnmr(400mhz,cdcl3)δ7.53–7.32(m,4h),7.32–7.25(m,1h),7.21–7.01(m,5h),6.88(d,j=7.4hz,2h),6.83–6.52(m,2h),4.40(s,2h),3.88(s,2h),3.54(dd,j=11.3,2.5hz,1h),3.48–3.35(m,1h),3.35–3.21(m,1h),2.64–2.44(m,1h),2.34(s,3h),2.31–2.10(m,1h),1.91–1.49(m,2h).
13cnmr(100mhz,cdcl3)δ139.48,138.70,137.35,134.18,130.16,128.58,128.43,127.88,127.66,127.55,127.18,126.86,83.94,64.74,62.07,61.66,47.95,31.75,21.12.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=18.20分鐘,tminor=6.11分鐘.
光學活性產物(9b)的1hnmr示意圖如圖69所示,其13cnmr示意圖如圖70所示,其消旋產物液相圖如圖71所示,其手性產物液相圖如圖72所示。
1hnmr(400mhz,cdcl3)δ7.47–7.32(m,4h),7.30–7.26(m,1h),7.25–7.17(m,5h),7.15–7.01(m,4h),4.56(d,j=12.2hz,1h),4.50(d,j=12.2hz,1h),4.02(s,2h),3.46–3.26(m,1h),3.12(d,j=7.8hz,2h),2.32(s,3h),2.10–1.84(m,3h),1.69(brs,1h).
13cnmr(100mhz,cdcl3)δ139.81,139.48,137.03,136.88,130.28,129.10,128.41,127.88,127.14,126.96,126.88,126.69,84.13,65.46,65.26,60.96,51.71,32.77,21.08.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=5.91分鐘,tminor=8.33分鐘.
實施例10
第一步反應,將肉桂醛(1.0mmol)、雙(1,5-環辛二烯)四氟硼酸銥(0.1mmol)、手性二苯基脯氨醇二甲基叔丁基硅醚(0.2mmol)、4-硝基苯甲酸(0.4mmol)和
光學活性產物(10a)的1hnmr示意圖如圖73所示,其13cnmr示意圖如圖74所示,其消旋產物液相圖如圖75所示,其手性產物液相圖如圖76所示。
1hnmr(400mhz,cdcl3)δ7.55–7.36(m,6h),7.35–7.30(m,1h),7.22–7.07(m,3h),6.89(d,j=8.2hz,2h),6.83–6.62(m,2h),4.42(dd,j=27.1,11.7hz,2h),3.90(s,2h),3.56(dd,j=11.7,3.0hz,1h),3.51–3.39(m,1h),3.39–3.25(m,1h),2.58–2.40(m,1h),2.11(brs,1h),1.78–1.65(m,1h),1.42(brs,1h).
13cnmr(100mhz,cdcl3)δ138.88,138.29,136.69,130.84,130.05,129.67,128.65,127.85,127.71,127.10,121.89,83.83,64.90,62.07,61.46,47.69,31.48.
hplc(手性ia柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=9.38分鐘,tminor=6.88分鐘.
光學活性產物(10b)的1hnmr示意圖如圖77所示,其13cnmr示意圖如圖78所示,其消旋產物液相圖如圖79所示,其手性產物液相圖如圖80所示。
1hnmr(400mhz,cdcl3)δ7.52–7.43(m,2h),7.42–7.34(m,4h),7.34–7.28(m,1h),7.27–7.19(m,5h),7.13(d,j=8.5hz,2h),4.54(dd,j=43.5,12.1hz,2h),4.05(s,2h),3.38(ddd,j=10.9,6.9,4.3hz,1h),3.27–3.16(m,1h),3.13(dd,j=11.7,3.3hz,1h),2.13–2.00(m,1h),1.98–1.86(m,1h),1.61(s,2h).
13cnmr(100mhz,cdcl3)δ139.50,139.39,138.97,131.50,130.09,128.79,128.49,128.10,127.34,127.13,126.67,121.50,83.96,65.65,65.20,60.94,51.84,32.62.
hplc(手性ic柱,波長等于220納米,正己烷:異丙醇=4.5:1,流速=1.0毫升/分鐘),tmajor=5.37分鐘,tminor=4.66分鐘。
實施例11
本實施例中用cck8法對本發明化合物生物活性進行測試,采用實施例10制備得到的本發明化合物(10a),(2s,3s)-2-芐氧基-2-對溴苯基-3-苯基-1,5-戊二醇(編號為fb1-3-s)和實施例10制備得到本發明化合物(10b),(2r,3s)-2-芐氧基-2-對溴苯基-3-苯基-1,5-戊二醇(編號為fb1-3-x)進行其對腫瘤細胞的抑制作用研究。本實施例具體使用的細胞系為:hct116(人結腸癌細胞)。
1、接種細胞:用含10%胎牛血清、1%青霉素和鏈霉素的mccoy'5a培養液配成單個細胞懸液,以每孔3000個細胞接種到96孔細胞培養板,每孔體積100μl。
2、經過碾磨處理步驟將本發明化合物制備為粉狀藥物,把粉狀藥物配制成終濃度為10mm的母液,而后梯度依次稀釋至0.01mm,0.03mm,0.1mm,0.3mm,1mm,3mm,10mm,30mm。作用于細胞,每組濃度設置三個復孔。
3、給藥:用完全培養基將梯度母液稀釋至終濃度0.01μm,0.03μm,0.1μm,0.3μm,1μm,3μm,10μm,30μm,每孔200μl作用于細胞,每組濃度設置三個復孔,培養液中dmso含量為1‰。
4、培養:5%co2,37℃飽和濕度育孵箱培養72小時。
5、呈色:培養72小時吸出培養基,每孔加入100μl完全1640培養基和10μlcck8,37℃孵育4小時。
6、比色:選擇620、450nm波長,在酶標儀上測定各孔光密度(od)值,記錄結果。
7、同一孔450nm吸光光度值-620nm吸光光度值(背景吸光光度值)作為最終吸光度,代入以下公式。
8、細胞增殖活力(%)=[a(加藥)-a(空白)]/[a(0加藥)-a(空白)]×100
a(加藥):具有細胞、cck溶液和藥物溶液的孔的吸光度
a(空白):具有培養基和cck溶液而沒有細胞的孔的吸光度
a(0加藥):具有細胞、cck溶液而沒有藥物溶液的孔的吸光度
9、實驗結果表明:在濃度為10、30μm本發明化合物的作用下,hct116細胞增殖活性受到明顯抑制。
如圖81所示為hct116(人結腸癌細胞)在本發明化合物(編號fb1-3-s、fb1-3-x)不同濃度下的存活率,以濃度為橫坐標,存活率為縱坐標繪制的濃度-存活率曲線。從曲線上可以獲知,本發明化合物(fb1-3-s、fb1-3-x)對hct116(人結腸癌細胞)的半致死濃度ic50分別為11.87μm、21.99μm。
由此可見,本發明fb1-3-s、fb1-3-x對hct116(人結腸癌細胞)活性具有抑制作用,適用于抗腫瘤藥物的制備應用。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 毛栲利素衍生物的制備方法及其抗菌活性的新用圖
- 6-o-脫甲基側厚殼桂堿衍生物及其制備和抗病毒活性應用及抗癌活性的制作方法
- 一種聚乙二醇中吡啶衍生物的合成方法
- 棉酚衍生物和它們的制備,在農藥上的應用及抗癌活性的制作方法
- 用于治療或預防神經精神病疾病的含有黃酮-6-c-葡萄糖衍生物作為活性成分的藥物組合物的制作方法
- 具有抗癌活性的6-氧代-1,6-二氫-噠嗪衍生物與吉非替尼的組合的制作方法
- 2,3′-脫水-2′-脫氧-5-氟尿苷衍生物與細胞毒活性、制備方法及應用
- 2,3′-脫水-2′-脫氧-5-氟尿苷衍生物與細胞毒活性、制備方法及應用
- 具有抗腫瘤活性的哌啶酮衍生物及其制備方法
- 一種支化聚乙二醇的脂質衍生物及其組成的脂質膜結構體的制作方法