mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2及其應用的制作方法
本發明屬于多肽藥物領域,更具體地說,涉及一種mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2及其應用。
背景技術:
基質金屬蛋白酶(MMPs)是一類鈣離子和鋅離子依賴的內肽酶,它們介導細胞外基質(ECM)的降解和組織重塑,調節宿主防御反應及正常的細胞功能。MMP抑制劑(MMPIs)可用于制備治療各類以基質金屬蛋白酶的過度表達和過度活化為特征的急性炎癥疾病和自身免疫性疾病藥物。
內毒素休克是醫院中經常發生的致死原因,在休克癥狀的發展過程中,多器官衰竭是由于機體對細菌產物(如內毒素)發生了急性的、過度的炎癥反應造成的。在內毒素休克過程中,過度的Toll-like受體活化會導致白細胞的過度活化并產生了大量的炎性介質,包括細胞因子和酶類。近年來有研究表明內毒素休克發展過程中導致多器官衰竭的炎癥反應與基質金屬蛋白酶-9的過度表達有關。基質金屬蛋白酶-9的缺失可增加小鼠對內毒素休克的抵御作用。
中性粒細胞是循環系統中最豐富的白細胞,在機體受到細菌感染時,中性粒細胞可迅速作出反應,首先進入被感染部位,構成了機體免疫系統應對細菌感染的第一道防線。中性粒細胞的細胞顆粒中儲存有不同種預先產生的酶類,包括彈性蛋白酶,基質金屬蛋白酶-8(MMP-8)和基質金屬蛋白酶-9(MMP-9)等。基質金屬蛋白酶-8可切割膠原蛋白,基質金屬蛋白酶-9可繼續把變性的膠原蛋白或明膠切割成更小的片段。基質金屬蛋白酶-9本身也有切割VI型膠原蛋白的活力,VI型膠原蛋白是血管基底層的主要成分。與其它細胞不同,中性粒細胞不表達基質金屬蛋白酶-2和基質金屬蛋白酶抑制因子-1(TIMP-1)。這使得中性粒細胞在受到諸如LPS,IL-8和PMA等的刺激時,迅速釋放胞內顆粒,而釋放的基質金屬蛋白酶-9類可被同時釋放的有氧自由基激活,在局部具有較高的濃度。這些酶除了具有正常的殺菌功能外,在病理條件下可能會對機體造成很大的破壞。這一點可由基質金屬蛋白酶-9缺失小鼠對內毒素休克的抑制作用證明。所以,基質金屬蛋白酶-9可以作為以中性粒細胞為主的炎癥反應的主要靶點。
多發性硬化癥(MS)是一種中樞神經系統慢性炎性疾病。從病理解剖角度,患者出現:(1)血腦屏障周期性、局灶性破壞;(2)血管周圍炎癥細胞的浸潤;(3)髓磷脂灶性破壞;(4)膠質斑塊狀壞死,最終導致軸突斷裂。目前,眾多的實驗研究表明,多種MMPs家族成員,尤其是MMP-9參與介導EAE及MS的以上發病的各個環節。多發性硬化癥中血腦屏障的破壞、炎性細胞浸潤、髓鞘降解以及軸索的損傷等主要病理過程均與MMP-9活性異常增高有關。MMPs在疾病中起著促進作用。
多肽P2由22個氨基酸組成,是具有抑制基質金屬蛋白酶-9活性的多肽,前期研究發現尾靜脈注射P2在實驗中能夠顯著降低小鼠對內毒素休克的敏感性,體內具有顯著的抗內毒素休克效果,有望廣泛應用于基因穩定、機理明確的炎癥治療中(如內毒素休克的治療)。前期實驗還建立了間接競爭ELISA方法,用來檢測P2的血藥濃度,研究發現,多肽P2在小鼠體內的代謝非常快,8分鐘就降低為初始濃度的十分之一,這大大限制了P2在治療急性炎癥中的應用。同時,前期研究發現,P2在多動脈硬化癥的動物模型中沒有治療效果。
對分子結構進行修飾或改造是解決半衰期較短、需連續給藥問題的常用方法,其中以化學修飾應用最為廣泛,常用的化學修飾劑有mPEG-SC5K(polye thylene glycol,PEG)、葡聚糖、聚氨基酸、聚酸酐等。PEG具有無毒、無免疫原性、水溶性好的特點,被美國食品與藥物管理局(FDA)認可作為藥品的輔助原料和修飾劑。多肽類藥物經PEG修飾后,分子量增加,腎小球的濾過率減少,PEG的屏障作用保護了多肽不易被蛋白水解酶水解,同時減少了中和抗體的產生,這些變化極大地改善了多肽類藥物在機體內清除快、免疫原性高、有效血藥濃度持續時間短、需頻繁給藥等缺點。目前已有多種PEG修飾的多肽類藥物上市銷售。但PEG修飾同時也會影響蛋白質和多肽的生物學活性,其影響大小與修飾劑、修飾條件及蛋白質和多肽本身的性質有關,需通過一系列的體內外藥效學試驗確定修飾產物的生物活性。
技術實現要素:
1.要解決的問題
針對現有基質金屬蛋白酶-9抑制劑多肽P2存在半衰期短的缺點,本發明提供一種mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2及其應用,對多肽P2進行了mPEG-SC5K修飾。mPEG-SC5K修飾蛋白質藥物可以在其藥物周圍產生空間屏障作用,降低藥物的免疫降解和酶解作用,延長藥物的循環半衰期,降低藥物在腎臟中的代謝速率,降低免疫原性。同時,為了解決mPEG-SC5K修飾成本高昂的問題,對mPEG-SC5K修飾多肽P2的反應條件進行了多次摸索,從而篩選出修飾物產率高的反應條件;并檢測了mPEG-SC5K-P2的體內半衰期,以及對所得修飾產物進行了多種體內外藥效試驗,證明mPEG-SC5K修飾P2很好的改善或提高其生物活性,可以更好的應用于急性炎癥和自身免疫疾病的預防和治療。
2.技術方案
為了解決上述問題,本發明所采用的技術方案如下:
一種mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2,其特征在于其序列為:
mPEG-SC5K-Pro-(D-Pyr)-(D-Cys)-Bip-Arg-Gly-Glu-Gly-Gly-Gly-Gly-Ile-Val-Arg-Arg-Ala-Asp -Arg-Ala-Ala-Val-Pro。
mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2在動物體內的藥代動力學特征。
mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2在制備治療以基質金屬蛋白酶-9的過度表達和過度活化為特征的急性炎癥疾和自身免疫疾病藥物中的應用。
一種治療急性炎癥藥物,其特征在于:所述的一種mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2,藥物的給藥方式為注射給藥,包括尾靜脈注射和皮下注射。
一種治療自身免疫性疾病的藥物,其特征在于:所述的一種mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2,藥物的給藥方式為注射給藥,包括尾靜脈注射和皮下注射。
mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑P2的制備方法,其步驟為:(1)合成序列Pro-(D-Pyr)-(D-Cys)-Bip-Arg-Gly-Glu-Gly-Gly-Gly-Gly-Ile-Val-Arg-Arg-Ala-Asp-Arg-Ala-Ala-Val-Pro;(2)用mPEG-SC5K修飾Pro-(D-Pyr)-(D-Cys)-Bip-Arg-Gly-Glu-Gly-Gly-Gly-Gly-Ile-Val-Arg-Arg-Ala-Asp-Arg-Ala-Ala-Val-Pro;(3)經分離純化得到聚乙二醇修飾的基質金屬蛋白酶-9抑制劑多肽P2。
研究表明,P2序列Pro-(D-Pyr)-(D-Cys)-Bip-Arg-Gly-Glu-Gly-Gly-Gly-Gly-Ile-Val-Arg-Arg-Ala-Asp-Arg-Ala-Ala-Val-Pro中的Pro-(D-Pyr)-(D-Cys)-Bip-Arg-Gly-Glu為基質金屬蛋白酶-9的多肽抑制劑,P2本身也有抑制基質金屬蛋白酶-9的活性。Pro-(D-Pyr)-(D-Cys)-Bip-Arg-Gly-Glu的缺點是在水溶液中的溶解度低,需要DMSO助溶,而P2在水溶液中的溶解度很好。P2的缺點是在血液中的半衰期很短,這限制了它的應用。聚乙二醇修飾即PEG化,是將活化的PEG分子與蛋白質藥物通過共價鍵偶聯,提高蛋白藥物的生理穩定性。由于mPEG-SC5K分子鏈的空間位阻作用,藥物經過mPEG-SC5K修飾后,對酶解作用的抵抗能力大大提高,同時能夠顯著降低腎臟過濾清除速度。同時,mPEG-SC5K的結構特異性和位阻遮蔽作用可以降低中和抗體的產生,降低免疫清除速率。以上這些作用使得mPEG-SC5K修飾后的藥物分子具有了相對未修飾藥物更為優良的藥理藥代性能。除了能夠延長半衰期和降低免疫原性,蛋白藥物經mPEG-SC5K修飾后,通常還具有以下優點:1.血藥濃度波動降低;2.蛋白酶降解作用降低;3.毒性顯著降低;4.溶解性增加;5.用藥頻率降低,治療費用降低。
多肽P2經過mPEG-SC5K修飾后靶點不變,但同時延長了多肽分子的體內半衰期、清除率低、降低了免疫原性和抗原性,且抗基質金屬蛋白酶-9活性保持不變。
發明人經過大量試驗獲知mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2能夠明顯抗內毒素休克,前期研究發現P2對內毒素休克有治療作用,但它在血液中的半衰期很短,因此使用受到限制,比如,如果尾靜脈注射P2,那么P2必須在注射內毒素之后5分鐘內給藥才有效,這與臨床是不符合的,臨床上我們不能預測病人何時發生內毒素休克;mPEG-SC5K修飾的P2體內半衰期延長,尤其是通過皮下注射,其吸收的峰值出現在2小時,在皮下注射相同劑量P2和mPEG-SC5K修飾的P2時,mPEG-SC5K修飾的P2在血液中的濃度高于P2的濃度,這樣我們通過皮下注射較大劑量的mPEG-SC5K-P2,就可以在幾個小時之內保持對基質金屬蛋白酶-8和基質金屬蛋白酶-9的有效抑制,對急性炎癥有積極的治療和預防作用(注:由于基質金屬蛋白酶-8和基質金屬蛋白酶-9酶活性位點空間結構有高度相似性,所以P2和mPEG-SC5K-P2可同時抑制兩種酶的活性)。
發明人經過大量試驗獲知該mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑多肽P2,在多動脈硬化癥的動物模型(EAE模型)中能夠明顯改善造模組的癱瘓癥狀,降低臨床評分,而P2本身對多發性硬化癥動物模型沒有治療作用。
本發明設計的聚乙二醇修飾的基質金屬蛋白酶-9抑制劑科學合理、可行有效,能作為制備治療人類急性炎癥和自身免疫疾病的治療藥物,拓展了多肽P2的治療譜,為將來藥物開發提供新的思路和前景。
3.有益效果
相比于現有技術,本發明的有益效果為:
(1)本發明采用mPEG-SC5K(PEG)對多肽進行修飾,延長了基質金屬蛋白酶-9抑制劑多肽P2在動物循環系統中的半衰期,且修飾后的多肽P2仍然保持其原有的生物學活性;
(2)本發明中用于修飾多肽P2的PEG的種類為修飾多肽N端氨基的mPEG-SC5K,具有延長P2半衰期,并且保留其體內外活性的特點。本發明針對上述mPEG-SC5K修飾的基質金屬蛋白酶-9抑制劑P2進行了大量的體內外活性研究,研究了其對急性炎癥和多發性硬化癥的治療作用,發現修飾產物在內毒素休克模型中對內毒素休克有治療和預防的作用,并在EAE模型中對多發性硬化癥有治療作用。
附圖說明:
圖1.不同濃度mPEG-SC5K-P2對MMP-9酶活力的抑制作用
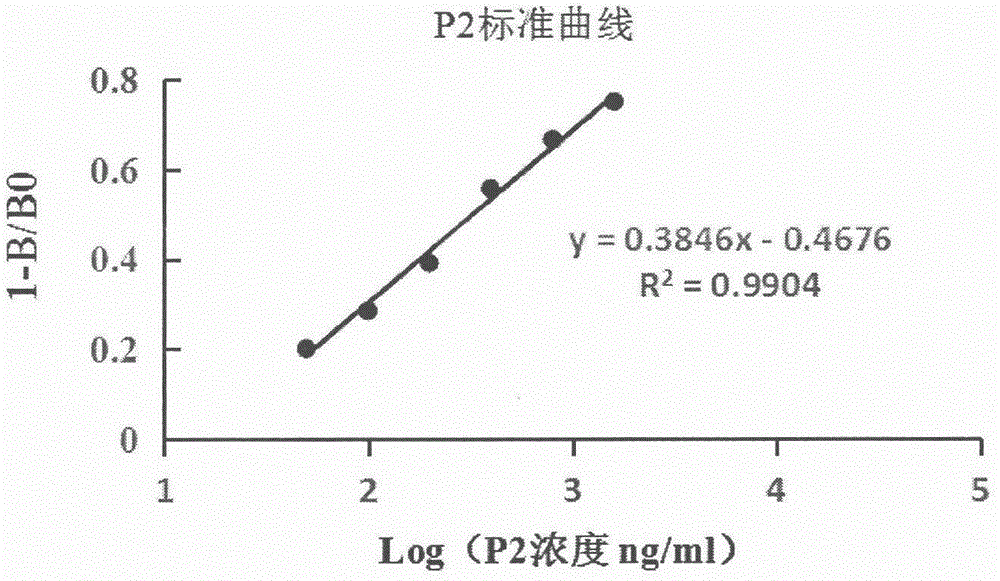
圖2.在ELISA檢測中P2的標準曲線
圖3.在ELISA檢測中mPEG-SC5K-P2的標準曲線
圖4.尾靜脈注射P2和mPEG-SC5K-P2后的濃度-時間(C-T)曲線
圖5.皮下注射注射P2和mPEG-SC5K-P2后濃度-時間(C-T)曲線
圖6.尾靜脈注射P2和mPEG-SC5K-P2的藥效學實驗
圖7.皮下注射注射P2和mPEG-SC5K-P2的藥效學實驗
圖8.皮下注射mPEG-SC5K-P2對EAE造模小鼠的治療作用
具體實施方式
下面結合具體實施例對本發明進一步進行描述。
本發明設計的多肽P2由上海吉爾生化合成。
實施例1
mPEG-SC5K修飾P2的步驟
一、PEGSC5K修飾條件的初步摸索
分別稱取32mg mPEG-SC5K和10mg P2(摩爾比為1.5∶1)濃度為0.05mol/L、0.1mol/L、0.15mol/L、0.2mol/L、0.25mol/L時配制pH7.0的Na2HPO4-NaH2PO4緩沖液,在4℃條件下反應3小時。
二.mPEG-SC5K修飾條件的優化
分別稱取23mg mPEG-SC5K和10mg P2(摩爾比為1.1∶1)、27mg mPEG-SC5K和10mg P2(摩爾比為1.3∶1)、32mg mPEG-SC5K和10mg P2(摩爾比為1.5∶1)、36mg mPEG-SC5K和10mg P2(摩爾比為1.7∶1)、42mg mPEG-SC5K和10mg P2(摩爾比為2.0∶1)置于40mL配好的pH 8.0-8.5的PBS緩沖溶液中,在4℃條件下反應3-12h。
三.對各種PEG修飾條件的再優化
分別稱取128mg mPEG-SC5K和40mg P2(摩爾比為1.5∶1)置于40mL配好的pH 7.7-8.0的PBS緩沖溶液中,在4℃條件下過夜,使其進行反應。
mPEG-SC5K修飾多肽P2的具體過程為:對可能影響修飾反應的各個條件,包括:反應時間、緩沖液的pH、緩沖液的濃度(表2)條件進行了初步摸索及再優化,通過高效液相色譜儀,利用面積歸一化法對單修飾產物的修飾率進行分析,從而獲得mPEG-SC5K修飾多肽P2修飾物產率較高的反應條件。具體色譜條件為:
分析型色譜柱:Welch,250mm×4.6mm(5μm填料);
流動相:A相為水(100%)、B相為乙腈(100%);
上樣量:20μL;
流速:1mL/min;
檢測波長:220nm;
洗脫梯度:見表1。
表1檢測修飾產率的洗脫梯度
mPEG-SC5K修飾條件的初步摸索過程:固定反應溫度為4℃,mPEG-SC5K與P2的摩爾比為1.5∶1,多肽濃度為1mg/mL,進行反應緩沖液種類及濃度的選擇:(1)mPEG-SC5K修飾P2緩沖液濃度的篩選:反應時間為3h,分別在濃度為0.05mol/L、0.1mol/L、0.15mol/L、0.2mol/L、0.25mol/L時配制pH 7.0的Na2HPO4-NaH2PO4緩沖液,并在各不同濃度的緩沖液中進行修飾反應,并檢測修飾產物的修飾率。結果表明,mPEG-SC5K在濃度為0.1mol/L,pH為7.0的Na2HPO4-NaH2PO4緩沖液中修飾物產率最高,最高可達84.0%。因此選用0.1mol/L的Na2HPO4-NaH2PO4緩沖液進行mPEG-SC5K修飾條件的優化。
mPEG-SC5K修飾條件的優化:根據初步摸索的結果,在所選的緩沖液的濃度下對其他關鍵因素進行正交試驗,對mPEG-SC5K的修飾條件進行優化。固定反應溫度為4℃,多肽濃度為1mg/mL,在0.1mol/L的Na2HPO4-NaH2PO4緩沖液中對mPEG-SC5K與P2二聚體的摩爾比,緩沖液的pH和反應時間進行三因素多水平正交試驗(表2)。對正交試驗結果進行極差分析,反應液pH是該反應的關鍵影響因素,pH為7.5、8.0、8.5時的平均修飾率分別為84.18%,92.96%和88.67%,對修飾率的影響顯著,可對緩沖液的pH進行再優化。
表2 PEGSC5K修飾的正交試驗方案
mPEG-SC5K修飾P2條件的再優化:固定反應溫度為4℃,多肽P2濃度為1mg/mL,mPEG與P2的摩爾比為1.5∶1,反應時間為3h,在pH分別為7.7,7.8,7.9,8.0,8.1和8.2的0.1mol/L的Na2HPO4-NaH2PO4緩沖液中對緩沖液的pH進行再優化。結果表明:pH 7.7-8.0時,隨pH的升高修飾物產率升高;pH大于8.0時,隨pH的升高修飾物產率降低,因此應嚴格控制pH不超過8.0。
實施例2
mPEG-SC5K修飾P2的分離純化步驟
一、分離
對反應后的樣品應用半制備型高效液相(HPLC,島津)進行純化,純化條件為:
半制備色譜柱:YMC,250mm×10mm(5μm填料);
流動相:A相為水,B相為乙腈;
上樣量:1mL;
流速:2mL/min;
檢測波長:220nm;
洗脫梯度:見表3。
表3洗脫梯度2
目的峰出峰過程中用離心管收集產物。
二、純化
將經過半制備型HPLC收集的產物經旋蒸后首先于-80℃低溫冰箱預凍過夜,之后于提前預冷的冷凍干燥機凍干,直到目測全為白色粉末為止(48h左右)。收獲凍干產物,稱量并記錄產物重量后于-20℃冰箱保存,并進行鑒定。
1.產物的純度分析
將凍干后的產物,通過分析型高效液相色譜分析純度,分析條件為:
分析型色譜柱:Welch,250mm×4.6mm(5μm填料);
流動相:A相為水(100%)、B相為乙腈(100%);
上樣量:20μL;
流速:1mL/min;
檢測波長:220nm;
洗脫梯度:見表4。
表4修飾產物純度的洗脫梯度
2.修飾產物的SDS-PAGE分析
基本操作參考《分子克隆(第二版)》。濃縮膠濃度為5%,分離膠濃度為15%,濃縮電壓80伏,分離電壓120伏。電泳結束后樣品條帶先進行考馬斯亮蘭R250對蛋白部分染色,染色完畢放入脫色液中至本底透明后掃描分析;然后再使用BaI2對含有PEG的部分染色。
實施例3
酶抑制活力實驗
一、緩沖液的配制:準確稱取2.42g Tris,再準確稱取1.16g NaCl,將這兩個樣品加入到200mL的雙蒸水中溶解,使其完全溶解,用HCl調節PH至7.4,最后準確稱取1.11g CaCl2,加入溶液中使其完全溶解,用0.22μm的微孔濾膜過濾該溶液。
二、通過基質金屬蛋白酶-9對熒光底物(Mca-Pro-Leu-Gly-Leu-Dpa-Ala-Arg-NH2)的切割作用來檢測mPEG-SC5K-P2的酶抑制活力,MMP-9在切割的時候,反應系統的熒光值呈現增加的趨勢(設置激發波長為328nm,發射波長為392nm),分析過程應該在37℃100μL的反應系統中進行,此系統中包括MMP-9溶液,底物溶液,緩沖液以及抑制劑)。反應系統中的溶液都應該加入96孔黑色酶標板中,黑色酶標板是為了防止熒光互相干擾,然后用Tecan平板讀取儀檢測得到相應的實驗結果并分析。
從酶抑制活性圖1中可以看出,隨著mPEG-SC5K-P2濃度的增加,酶活力被明顯的抑制,不加抑制劑的斜率明顯大于加了抑制劑的斜率,且隨著抑制劑濃度的增大,斜率減小,抑制率增大。從抑制曲線圖也可以明顯看出在隨著抑制劑濃度的增大,抑制率開始時快速增加并且最后趨于穩定。當抑制劑量加到1.95μM時,抑制率甚至達到了50%,這說明抑制劑的對酶的具有較強的抑制作用。
通過以上的分析,我們可以看出mPEG-SC5K-P2可以抑制基質金屬蛋白酶-9的酶活性。
實施例4
小鼠體內血藥濃度測定ELISA方法學的建立
實驗方法:
一、偶聯抗原的制備
采用戊二醛二步法:取12mg BSA溶解于1mL 0.1mol/L PBS(pH 7.4),加新鮮配置1.5%戊二醛(GA)溶液1.5mL,于室溫反應約6h。將反應液對0.01mol/L PBS(pH 7.4)于4℃透析過夜。在透析內液中加入6mg PBS溶解的P2,反應10h,對0.01mol/L PBS(pH 7.4)于4℃透析過夜。收集透析內液,EP管分裝每管10μL,于-20℃保存。
二、間接競爭ELISA測定mPEG-SC5K-P2血藥濃度基本程序
1.包被:將P2-BSA用包被液以1∶1600濃度稀釋,加入酶標板中,每孔100μL,4℃過夜。
2.洗板:將包被液棄去,每孔加入400μL洗液,PBST洗滌3次,每次5min,拍干。
3.封閉:每孔加入200μL封閉液,37℃水浴放置1.5h,重復洗板過程,拍干。
4.加待測樣品和抗體:酶標板中先加入50μL待測樣品,再加入50μL 1∶20000濃度稀釋的單抗,設4個復孔,于37℃搖床震蕩混勻2min,再移至37℃水浴鍋放置1h,進行間接競爭ELISA反應。重復洗板過程,拍干。
5.與酶標二抗反應:加入1∶2 000濃度稀釋的HRP酶標山羊抗小鼠IgG,每孔100μL,37℃溫育1h。重復洗板過程,拍干。
6.加入底物:每孔加入100μL TMB底物顯色液,室溫避光顯色20-30min。
7.終止:每孔加入50μL終止液,終止反應。
8.檢測:用酶標儀讀取各孔OD450nm值。
三、標準曲線的繪制
將P2分別稀釋成1600、800、400、200、100、50ng/mL,將mPEG-SC5K-P2分別稀釋成1600、800、400、200、100、50ng/mL,進行間接競爭ELISA測定,制作標準曲線。以各濃度mPEG-SC5K-P2抑制的OD450值記為B,其中無mPEG-SC5K-P2抑制時的OD450記為B0。B/B0%值與Lg[mPEG-SC5K-P2]成線性回歸關系,從而可計算回歸曲線的方程及相關系數。
四、靈敏度的測定
作標準曲線的同時,在包被好的酶標板上隨機選擇10個孔做零標準品間接競爭ELISA檢測。求所得10個OD450值的平均值(OD450)和標準差(SD),按照下式計算靈敏度(Y):Y=[(OD450-2SD)/OD450]×100%。將Y值代人標準曲線回歸方程,計算出對應的mPEG-SC5K-P2濃度,即為該方法理論上的檢測下限。
五、精密度測定
1.批內誤差每一個標準品濃度設置3個重復,以其批內變異系數(CV)表示批內誤差。批內變異系數(CV)表示,即CV=平均值/批內平均結合率×100%。
2.批間誤差重復操作,連續三次以其批間變異系數表示批間誤差。
六、回收率測定
采用高溫水浴法:取P2加入小鼠鼠血漿中,分別為低(100ng/mL)、中(600ng/mL)、高(1280ng/mL)三個劑量,取mPEG-SC5K-P2加入小鼠鼠血漿中,分別為低(100ng/mL)、中(600ng/mL)、高(1280ng/mL)三個劑量,取各10μL與80℃預熱的PBS緩沖液190μL混勻,80℃水浴30min,12000rpm離心2min,取上清液,以小鼠血漿為空白對照進行間接競爭ELISA檢測,計算回收率。每個樣品重復3次取平均值。回收率=(測量值/加入量)×100%。
實驗結果:
一、標準曲線的制作
根據以上優化得到的最佳包被抗原濃度、最佳多克隆抗體稀釋倍數及酶標二抗工作濃度,進行間接競爭ELISA測定,制作標準曲線。
依上述優化條件做間接競爭ELISA測定,并制作標準曲線。由圖2和圖3可見,在小鼠血漿中P2濃度為1600-50ng/mL范圍內,標準曲線線性良好,標曲線性方程為y=0.3846x-0.4676,R2=0.9904;在小鼠血漿中mPEG-SC5K-P2濃度為1600-50ng/mL范圍內,標準曲線線性良好,標曲線性方程為y=0.4256x-0.578,R2=0.9916。
二、靈敏度的測定
采用該方法P2的理論最低檢測限為7.32ng/mL,mPEG-SC5K-P2的理論最低檢測限為13.74ng/mL。
三、精密度和回收率的測定
批內批間精密度和回收率見表5和表6。考察結果顯示,ELISA法測定小鼠血漿中高、中、低濃度的P2樣品,批內變異系數分別為5.11%、3.42%和4.08%;批間變異系數分別為:1.74%、2.88%和5.53%;回收率分別為:104.33%、100.86%和101.49%,均符合相關生物樣品檢測標準。考察結果顯示,ELISA法測定小鼠血漿中高、中、低濃度的mPEG-SC5K-P2樣品,批內變異系數分別為:2.46%、2.55%和2.54%;批間變異系數分別為:4.51%、5.31%和3.72%;回收率分別為:101.51%、99.61%和102.59%,均符合相關生物樣品檢測標準。
表5 P2 ELISA精密度和回收率
表6 mPEG-SC5K-P2 ELISA精密度和回收率
實施例6
P2和mPEG-SC5K-P2小鼠體內血藥濃度變化測定
一、尾靜脈注射修飾多肽mPEG-SC5K-P2在小鼠體內血藥濃度的測定
參照文獻方法,將小鼠隨機隨機分為4組,每組4只。尾靜脈注射給予P2 30mg/kg,各組小鼠分別于給藥后0min,2min,5min,10min,15min,20min,30min,40min,50min,由眼眶靜脈叢采血;或者尾靜脈注射給予mPEG-SC5K-P2 30mg/kg,各組小鼠分別于給藥后0min,2min,5min,10min,15min,20min,30min,40min,50min,由眼眶靜脈叢采血。每點采全血0.1mL,肝素抗凝,12000rpm/2min離心分離血漿,吸取上清血漿各10μL與80℃預熱的PBS(0.05M pH7.4)緩沖液190μL混勻,80℃水浴30min,12000rpm離心2min,取上清液,-20℃低溫保存備用。待室溫溶解后,取50μL上清液按上述操作ELISA方法測定P2和mPEG-SC5K-P2血藥濃度。
圖4為以時間(min)為橫坐標,血藥濃度(ug/mL)為縱坐標,作濃度-時間(C-T)曲線。
二、皮下注射修飾多肽mPEG-SC5K-P2在小鼠體內血藥濃度的測定
參照文獻方法,將小鼠隨機隨機分為4組,每組4只。尾靜脈注射給予P2 30mg/kg,各組小鼠分別于給藥后0h,0.25h,0.5h,1h,2h,3h,4h,5h,8h,由眼眶靜脈叢采血;或者尾靜脈注射給予mPEG-SC5K-P2 30mg/kg,各組小鼠分別于給藥后0h,0.5h,1h,1.5h,2h,3h,4h,5h,8h,由眼眶靜脈叢采血。每點采全血0.1mL,肝素抗凝,12000rpm/2min離心分離血漿,吸取上清血漿各10μL與80℃預熱的PBS(0.05M pH 7.4)緩沖液190μL混勻,80℃水浴30min,12000rpm離心2min,取上清液,-20℃低溫保存備用。待室溫溶解后,取50μL上清液按上述操作ELISA方法測定P2和mPEG-SC5K-P2血藥濃度。
圖5為以時間(h)為橫坐標,血藥濃度(ng/mL)為縱坐標,作濃度-時間(C-T)曲線。
從圖4和圖5中可以看出,P2經mPEG-SC5K修飾后,小鼠體內半衰期得到延長,皮下注射后吸收相延長,效果更明顯。
以上實驗數據均證明mPEG-SC5K修飾能夠顯著改善蛋白多肽藥物在大鼠體內的藥代動力學特征,能夠顯著延長多肽P2的生物半衰期(t1/2)。PEG修飾延長蛋白多肽藥物體內半衰期機制探討主要可以從以下幾方面來分析:①由于mPEG-SC5K大分子的共價偶聯,蛋白或多肽分子量增加,使其不易被腎臟代謝,因而在血液的停留時間延長。P2的分子量為2365Da,分子量較小,經靜脈注射后易積聚在腎小球,在腎臟代謝消除。蛋白或多肽的腎消除速率與其分子量呈負相關,分子量越大,腎消除越慢。mPEG-SC5K修飾增大了P2的有效分子量,腎消除速率減小,半衰期延長;②mPEG-SC5K線性長鏈的屏蔽作用,使蛋白或多肽不易受蛋白酶的降解,從而延長其體內作用時間;③mPEG-SC5K修飾后的蛋白或多肽對網狀內皮系統有抗性,而網狀內皮系統負責外源蛋白的清除。
實施例7
體內藥效學實驗--尾靜脈注射多肽的保護作用
將小鼠分為四組,分別為陰性對照組,造模組,陽性對照組、尾靜脈注射P2組、尾靜脈注射mPEG-SC5K-P2組,對每組小鼠進行編號以及稱重,將相應的體重記錄下來,陰性對照組只尾靜脈注射0.1mL無菌生理鹽水;造模組尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL);陽性對照組首先尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL),5分鐘后尾靜脈注射多肽Regasepin2溶液(Regasepin2溶于無菌生理鹽水中,18mg/mL);尾靜脈注射P2組先尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL),5分鐘后尾靜脈注射多肽P2溶液0.1mL(P2溶于無菌生理鹽水中,6mg/mL);尾靜脈注射mPEG-SC5K-P2組先尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL),5分鐘后尾靜脈注射mPEG-SC5K-P2溶液0.1mL(mPEG-SC5K-P2溶于無菌生理鹽水中,18.7mg/mL)。
小鼠注射后,分別間隔12h、16h、20h、24h、36h、40h觀察各籠小鼠的情況,將每籠老鼠的存活數記錄下來,制成表格;實驗全部結束,將實驗小鼠處死并做好后續的處理。
從實驗結果(圖6)不難看出,10只注射內毒素的小鼠,造模組在12h內數量發生明顯的銳減,12h的時候小鼠已全部死亡。按照90mg/kg劑量注射Regasepin2的陽性組小鼠生存率顯著高于造模組(p=0.000372);30mg/kg注射的P2有一定的保護作用(p=0.0118),與造模組相比有顯著性差異;注射了mPEG-SC5K-P2的小鼠與造模組相比存活率有明顯的提高(p=0.00432),而且好于P2組。
實施例8
體內藥效學實驗--皮下注射多肽的保護作用
將小鼠分為四組,分別為陰性對照組,造模組,陽性對照組、皮下注射P2組、皮下注射mPEG-SC5K-P2組,對每組小鼠進行編號以及稱重,將相應的體重記錄下來,陰性對照組只尾靜脈注射0.1mL無菌生理鹽水;造模組尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL);陽性對照組首先尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL),5分鐘后尾靜脈注射多肽Regasepin2溶液(Regasepin2溶于無菌生理鹽水中,18mg/mL);皮下注射P2組先皮下注射0.1mL P2溶液(P2溶于無菌生理鹽水中,6mg/mL),60min后尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL);皮下注射mPEG-SC5K-P2組先皮下注射mPEG-SC5K-P2溶液0.1mL(mPEG-SC5K-P2溶于無菌生理鹽水中,18.7mg/mL),60min后尾靜脈注射0.1mL LPS(LPS溶于無菌生理鹽水中,4μg/μL)。
小鼠注射后,分別間隔12h、14h、16h、18h、20h、24h、36h、40h觀察各籠小鼠的情況,將每籠老鼠的存活數記錄下來,制成表格;實驗全部結束,將實驗小鼠處死并做好后續的處理。
由實驗結果(圖7)可見,陽性對照組動物生存率顯著高于造模組(p=0.000543);皮下注射多肽P2組雖然生存的只數比較少,也有統計學意義,其生存率顯著高于造模組(p=0.284);皮下注射mPEG-SC5K-P2組動物生存率高于皮下注射P2組(p=0.000147)。
實施例9
體內藥效學實驗--多肽在多發性硬化癥模型上(EAE模型)的保護作用
EAE模型的建立和臨床評分:將100μL PLP139-151水溶液(含PLP139-151150μg)與100μL福(氏)免疫佐劑(含結核桿菌H37RA 400μg)混合,充分乳化制成抗原配劑。第1天經SJL/J小鼠上腹部皮下注射0.2mL抗原配劑,第1天和第3天經其靜脈注射0.60×106百日咳桿菌。
給藥劑量:將小鼠分為六組,分別為造模組,陽性對照組、尾靜脈注射P2組、尾靜脈注射mPEG-SC5K-P2組,皮下注射P2組、皮下注射mPEG-SC5K-P2組,對每組小鼠進行編號以及稱重,從實驗第1天開始給要,至第40天。造模組每天尾靜脈注射0.1mL無菌生理鹽水;陽性對照組從免疫后1周開始按體重10mg/(kg·d)經小鼠皮下注射強的松;尾靜脈注射P2組每天尾靜脈注射0.1mL P2溶液(P2溶于無菌生理鹽水中,6mg/mL);尾靜脈注射mPEG-SC5K-P2組每天尾靜脈注射mPEG-SC5K-P2溶液0.1mL(mPEG-SC5K-P2溶于無菌生理鹽水中,18.7mg/mL);皮下注射P2組每天皮下注射0.1mL P2溶液(P2溶于無菌生理鹽水中,6mg/mL);皮下注射mPEG-SC5K-P2組每天皮下注射mPEG-SC5K-P2溶液0.1mL(mPEG-SC5K-P2溶于無菌生理鹽水中,18.7mg/mL)。
免疫后所有動物每天稱體重并進行神經功能評分:0,不發病;1,尾部張力降低或輕度步態笨拙;2,尾部無張力,和/或中度步態異常,和/或姿態維持缺乏;3,肢體力弱;4,肢體麻痹;5,瀕死狀態。
由圖8可見尾靜脈注射和皮下注射P2和mPEG-SC5K-P2對EAE小鼠臨床神經功能評分的影響:尾靜脈注射P2或mPEG-SC5K-P2的臨床評分與造模組均無顯著性差異;皮下注射P2也沒有顯著性的改善臨床評分,但皮下注射mPEG-SC5K-P2顯著性的改善了臨床評分,發病時間明顯延遲。陽性對照藥強的松治療可顯著改善神經功能評分,并延遲發病時間。
- 還沒有人留言評論。精彩留言會獲得點贊!