溶菌酶納米晶溶膠及采用其制備的蛋白質多晶水凝膠和制備方法與流程
本發明屬于蛋白質超分子自組裝材料的制備技術領域,具體涉及一種溶菌酶納米晶溶膠,以及完全基于溶菌酶蛋白質分子的水凝膠制備,特別是由于該蛋白質水凝膠是由蛋白質納米晶組成,制備的是一種具有抗菌性能各向異性的軟材料。
背景技術:
蛋白質水凝膠是由蛋白質分子相互作用形成的三維網絡和大量水構成的軟材料,能夠在水中溶脹而不溶解,在生物醫學領域,尤其是在藥物的緩釋、組織工程支架、生物傳感、柔性促動器以及人工細胞外基質等方面具有廣泛的應用前景。同時,蛋白質水凝膠材料是一種理想的化學軟模板,可應用于合成具有特殊結構的有機無機復合材料。
目前,一般的蛋白質水凝膠材料都是由具有結合位點的蛋白質和一些大分子如PEG相互作用,或者和金屬離子之間存在絡合作用從而發生凝膠化形成水凝膠材料。因此一般的蛋白質水凝膠材料配方都是基于蛋白質的復配方,即使水凝膠中含有非蛋白質物質如PEG、金屬離子等。這些都限制了蛋白質水凝膠的實際醫用。再者,過多雜質的引入也會影響蛋白質水凝膠作為一類理想的化學軟模板應用于合成具有一定分級結構的復合材料。
技術實現要素:
本發明所要解決的技術問題在于提供一種溶菌酶納米晶溶膠,以及基于該蛋白質納米晶自主裝制備的生物相容性好、具有良好抗菌能力的純蛋白質多晶水凝膠。
本發明的溶菌酶納米晶溶膠由下述方法制備得到:
將溶菌酶和三(2-羧乙基)膦(TCEP)加入pH值為7.3~7.4的tris-HCl緩沖液中,控制tris-HCl緩沖液中溶菌酶的濃度為0.1~5mg/mL、TCEP的濃度為1~10mmol/L,然后用tris水溶液或鹽酸調節pH至6.0~6.9,30~50℃密封靜置6~24小時,用超純水進行透析,得到蛋白質納米晶溶膠。
上述溶菌酶納米晶溶膠的制備方法中,優選控制tris-HCl緩沖液中溶菌酶的濃度為0.5~1mg/mL、TCEP的濃度為2.5~5mmol/L。
上述溶菌酶納米晶溶膠的制備方法中,進一步優選用tris水溶液或鹽酸調節pH至6.5~6.6,35~40℃密封靜置8~12小時。
本發明的蛋白質多晶水凝膠由下述方法制備得到:
將溶菌酶納米晶溶膠與氨水按體積比為1:0.002~0.01混合,在50~80℃下加熱2~10分鐘,溶菌酶納米晶在溶液表面自組裝形成蛋白質多晶水凝膠。
上述蛋白質多晶水凝膠的制備方法中,優選將溶菌酶納米晶溶膠與氨水按體積比為1:0.005~0.008混合,在60~70℃下加熱2~5分鐘。
本發明在較溫和條件下用TCEP還原溶菌酶中的二硫鍵,使溶菌酶分子發生相轉變,即溶菌酶分子中的多肽鏈發生解折疊,溶菌酶由富含α螺旋結構的天然蛋白質結構轉變為富含β片層結構的蛋白聚集體,β片層結構進一步有序堆積形成密實結晶核,解折疊的多肽鏈形成連續相作為殼,形成具有核殼結構的溶菌酶納米晶溶膠。
本發明基于溶菌酶納米晶超分子自組裝形成蛋白質多晶水凝膠,由于制備蛋白質納米晶溶膠時引入的TCEP小分子在透析過程中完全除掉,所以獲得的是純粹的蛋白質水凝膠材料,更有利于其進一步加工和應用。
本發明的蛋白質多晶水凝膠是三維網絡結構,具有良好的生物相容性和抗菌性。同時由于該水凝膠是由溶菌酶納米片晶組成,使其具有各項異性,表現在水分逐漸揮發的過程中會形成多層有序結構,因此,其是一種新型的各相異性軟材料和良好化學軟模板。另外,本發明蛋白質多晶水凝膠還具有一定的力學強度,能夠用作細胞培養基。
附圖說明
圖1是實施例1制備的溶菌酶納米晶溶膠的數碼照片。
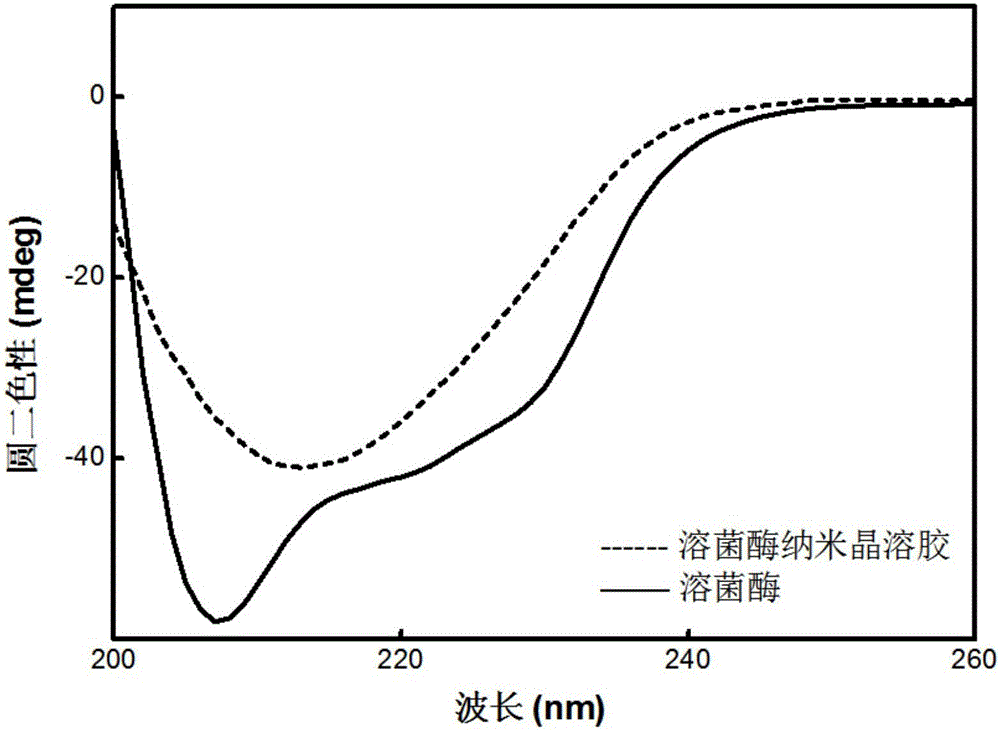
圖2是天然溶菌酶和溶菌酶納米晶溶膠的圓二色譜圖。
圖3是實施例1制備的溶菌酶納米晶溶膠的透射電子顯微鏡圖。
圖4是實施例1制備的溶菌酶納米晶溶膠的X-射線衍射圖。
圖5是實施例4制備的蛋白質多晶水凝膠的照片。
圖6是實施例4制備的蛋白質多晶水凝膠的儲能模量G'和損耗模量G''隨應變的變化圖。
圖7是實施例4制備的蛋白質多晶水凝膠的儲能模量G'和損耗模量G''隨頻率的變化圖。
圖8是實施例4制備的蛋白質多晶水凝膠的斷面掃描電鏡圖。
圖9是實施例4制備的蛋白質多晶水凝膠干燥后的斷面掃描電鏡圖。
具體實施方式
下面結合附圖和實施例對本發明進一步詳細說明,但本發明的保護范圍不僅限于這些實施例。
實施例1
制備溶菌酶納米晶溶膠
將50mg溶菌酶和58.6mg(0.25mmol)TCEP加入100mL pH值為7.4的tris-HCl緩沖液中,tris-HCl緩沖液中溶菌酶的濃度為0.5mg/mL、TCEP的濃度為2.5mmol/L,然后用10mmol/L tris水溶液調節pH至6.5,37℃密封靜置8小時,用超純水進行透析處理,透析袋的截留分子量為2000,得到純凈的溶菌酶納米晶溶膠,見圖1。由圖2可見,溶菌酶發生相轉變后由雙峰變成216nm處的單峰,說明溶菌酶由富含α螺旋結構的天然蛋白質結構轉變成富含β片層結構的蛋白聚集體。由圖3可見,β片層結構有序堆疊,形成具有核殼結構的溶菌酶納米晶,其中β片層結構有序堆積形成密實結晶核,解折疊的多肽鏈形成連續相作為殼。由圖4可見,所得溶菌酶納米晶溶膠含有結晶相。
實施例2
制備溶菌酶納米晶溶膠
將100mg溶菌酶和117.2mg(0.5mmol)TCEP加入100mL pH值為7.4的tris-HCl緩沖液中,tris-HCl緩沖液中溶菌酶的濃度為1mg/mL、TCEP的濃度為5mmol/L,然后用tris水溶液調節pH至6.9,47℃密封靜置6小時,用超純水進行透析處理,透析袋的截留分子量為2000,得到純凈的溶菌酶納米晶溶膠。
實施例3
制備溶菌酶納米晶溶膠
將500mg溶菌酶和234.4mg(10mmol)三(2-羧乙基)膦加入100mL pH值為7.4的tris-HCl緩沖液中,tris-HCl緩沖液中溶菌酶的濃度為5mg/mL、三(2-羧乙基)膦的濃度為10mmol/L,然后用tris水溶液調節pH至6.0,30℃密封靜置24小時,用超純水進行透析處理,透析袋的截留分子量為2000,得到純凈的溶菌酶納米晶溶膠。
實施例4
制備蛋白質多晶水凝膠
將4mL實施例1制備的溶菌酶納米晶溶膠與30μL氨水混合均勻,在65℃下加熱3分鐘,在溶液表面形成蛋白質多晶水凝膠(見圖5),其固含量為4.5%左右。由圖6和圖7可見,所得蛋白質多晶水凝膠具備一定的力學性能,由于水凝膠是由溶菌酶納米片晶自組裝而成,所以水凝膠的儲能模量G'總是大于損耗模量G''。
室溫下將所得蛋白質多晶水凝膠在密閉干燥器中靜置2周,緩慢揮發水溶劑形成蛋白質薄膜。由圖8和圖9可見,干燥前蛋白質多晶水凝膠為三維網絡結構,干燥后所得蛋白質薄膜具有有序多層結構,說明本發明的蛋白質多晶水凝膠是一種各向異性材料。
實施例5
制備蛋白質多晶水凝膠
將4mL實施例1制備的溶菌酶納米晶溶膠與40μL氨水混合均勻,在50℃下加熱10分鐘,在溶液表面形成蛋白質多晶水凝膠。
實施例6
制備蛋白質多晶水凝膠
將4mL實施例1制備的溶菌酶納米晶溶膠與20μL氨水混合均勻,在70℃下加熱3分鐘,在溶液表面形成蛋白質多晶水凝膠。
- 還沒有人留言評論。精彩留言會獲得點贊!