CYP2C19基因多態性檢測引物、探針及試劑盒的制作方法
本發明涉及基因多態性檢測技術領域,具體涉及CYP2C19基因多態性檢測引物、探針及試劑盒。
背景技術:
氯吡格雷英文名稱Clopidogrel,藥品名稱波立維,化學式為C16H16ClNO2S。該藥品為口服抗血小板藥物,可用于防治心肌梗死、缺血性腦血栓、閉塞性脈管炎、動脈粥樣硬化及血栓栓塞引起的并發癥。罹患中風、心肌梗死或確診為外周動脈疾病的患者,用藥后可減少動脈粥樣硬化的發生;經皮冠狀動脈介入治療后的病人,應用氯吡格雷可以降低血栓形成的風險。該藥品經體內P450酶生物轉化后可與血小板表面ADP受體P2Y12發生不可逆的結合,從而抑制ADP誘導的血小板的聚集,達到抗凝血的功效。
在臨床工作中發現,并非所有患者都能在應用氯吡咯雷中獲得預期效果,表現為心血管不良事件的發生,這個現象稱為“氯吡咯雷抵抗”。另外,服用氯吡咯雷也存在出血的風險,嚴重出血事件的發生率為1.4%。氯吡格雷抵抗主要原因是CYP2C19基因突變致使氯吡格雷的活性代謝產物減少。2009年1月,哈佛大學JessicaL.M.等在《新英格蘭醫學雜志》上發表了最新臨床研究結果,證實CYP2C19基因突變所導致的弱代謝個體,其栓塞重新形成的風險增加,心腦血管事件的發生風險增加,病死率升高。目前,公認的與氯吡咯雷代謝減弱相關的CYP2C19基因多態性主要包括CYP2C19*2和CYP2C19*3,與氯吡咯雷代謝增強相關的CYP2C19基因多態性則為CYP2C19*17。基于以上原因,氯吡格雷遭遇了美國食品藥品監督管理局(FDA)的黑框警告,警告內容為“建議服用氯吡格雷的患者做CYP2C19基因檢測”。
目前,針對CYP2C19基因多態性檢測的方法有多種,主要包括DNA測序法、高分辨率溶解曲線法和液相芯片法。DNA測序法雖然是金標準,但步驟繁瑣,耗時長。高分辨率溶解曲線法,快速,簡便,經濟實用,但對儀器的需求較高,絕大部分的實時熒光定量PCR儀無法適用。液相芯片法操作過程復雜,且容易污染,假陽性率高。因此需要建立一種快速操作方便,快速,特異性好、靈敏的基因檢測方法。
技術實現要素:
為了克服現有檢測技術的上述不足,本發明在Taqman探針法的基礎上提供一種具有高靈敏度、高特異性、高準確度、高精確度、操作方法簡單的CYP2C19基因CYP2C19*2(G681A)、CYP2C19*3(G836A)和CYP2C19*17(C-806T)多態性位點的引物和探針,本發明的另一目的是提供包括檢測以上多態性位點的試劑盒,以及檢測方法。
本發明提供的檢測CYP2C19基因多態性的引物和探針,用于檢測第681位點、第836位點以及第806位點基因多態性,其具體核苷酸序列如下:
(1)檢測CYP2C19*2(G681A)基因多態性的引物和探針:
G681A位點突變型ARMS上游引物:
5’-CCCACTATCATTGATTATTTCACA-3’(SEQ ID NO.1),
G681A位點野生型ARMS上游引物:
5’-TTCCCACTATCATTGATTATTGCCGG-3’(SEQ ID NO.2),
G681A位點公用的下游引物:5’-CCATTTTGATCAGGAAGCAATC-3’(SEQ ID NO.3),
G681A位點公用的探針:5’-CCTTGCTTTTATGG-3’(SEQ ID NO.4);
(2)檢測CYP2C19*3(G836A)基因多態性的引物和探針:
G836A位點突變型ARMS上游引物:
5’-GATTGTAAGCACCACCTGA-3’(SEQ ID NO.5),
G836A位點野生型ARMS上游引物:
5’-GATTGTAAGCACCCACTGG-3’(SEQ ID NO.6),
G836A位點公用的下游引物:5’-CTAGGCAAGACTGTAGTATTC-3’(SEQ ID NO.7),
G836A位點公用的探針:5’-CCAGGTAAGGCCAAGT-3’(SEQ ID NO.8);
(3)檢測CYP2C19*17(C-806T)基因多態性的引物和探針:
C-806T位點突變型ARMS上游引物:
5’-GTGTCTTCTGTTCTCAACGT-3’(SEQ ID NO.9),
C-806T位點野生型ARMS上游引物:
5’-GTGTCTTCTGTTCTCAAGGC-3’(SEQ ID NO.10),
C-806T位點公用的下游引物:5’-CTCATAGCTGGCAGAACTGG-3’(SEQ ID NO.11),
C-806T位點公用的探針:5’-CGCCACGATGGGCATC-3’(SEQ ID NO.12);
所述探針均為MGB探針,探針核苷酸序列5’端標記熒光報告基團,3’端標記熒光淬滅基團。
優選地,上述檢測CYP2C19基因多態性的引物和探針,所述熒光你報告基團為FAM。
本發明還提供了一種CYP2C19基因多態性檢測試劑盒,包括以上任一所述的檢測CYP2C19基因多態性的引物和探針。
該試劑盒針對不同基因位點,分別采用上述設計的野生型和突變型ARMS引物和Taqman-MGB探針,結合熒光定量PCR反應,對從人外周血中提取的基因組DNA進行檢測,一次性在一條6聯PCR反應條上實現對CYP2C19*2(G681A)、CYP2C19*3(G836A)和CYP2C19*17(C-806T)基因多態性進行檢測,通過實時熒光PCR儀上收集信號,計算野生型和突變型的△Ct值來確定樣本DNA的基因型,準確度好,操作簡單方便。
優選地,所述CYP2C19基因多態性檢測試劑盒,還包括一組內控基因的檢測引物和探針,具體核苷酸序列如下:
上游引物:5’-GGAAAGTGATATTTTGGAGAA-3’(SEQ ID NO.13),
下游引物:5’-CCATTTTGATCAGGAAGCAA-3’(SEQ ID NO.14),
內控探針:5’-CACCAAGAATCGATGGACATCAACAACCCTCGGGAC-3’(SEQ ID NO.15);
所述內控探針為Taqman探針,探針核苷酸序列的5’端標記熒光報告基團,3’端標記熒光淬滅基團,且熒光報告基團不同于權利要求1所述的MGB探針。
優選地,上述CYP2C19基因多態性檢測試劑盒,內控探針的核苷酸序列5’端標記的熒光報告基團為JOE,3’端標記的熒光淬滅基團為BHQ1。
優選地,所述CYP2C19基因多態性檢測試劑盒,還包括PCR反應液,所述PCR反應液包括dNTPs、PCR緩沖液、Fast Advanced Master Mix、礦物油和超純水。
優選地,所述CYP2C19基因多態性檢測試劑盒,還包括非模板對照和陽性對照。
本發明還提供了上述CYP2C19基因多態性檢測試劑盒的檢測方法,包括以下步驟:
(1)提取待檢測樣品中的DNA;
(2)用權利要求1所述的檢測CYP2C19基因多態性的引物和探針,每個基因型的檢測引物和探針對應一個反應體系,每個反應體系里均含有內控引物和探針,每個反應體系均使用提取的DNA作為模板,進行熒光定量PCR;同時設置非模板對照和陽性對照;
(3)檢測結果分析:
在非模板對照FAM及JOE信號不起線,或Ct>28;陽性對照FAM及JOE信號Ct值≤25;待檢測樣本產生的JOE信號Ct值≤25的情況下,代表擴增正常,按照以下標準判斷基因型:
其中,Ct1為CYP2C19*2G基因型反應體系的FAM信號Ct值,Ct2為CYP2C19*2A基因型反應體系的FAM信號Ct值,Ct3為CYP2C19*3G基因型反應體系的FAM信號Ct值,Ct4為CYP2C19*3A基因型反應體系的FAM信號Ct值,Ct5為CYP2C19*17C基因型反應體系的FAM信號Ct值,Ct6為CYP2C19*17T基因型反應體系的FAM信號Ct值。
本發明具有以下有益效果:
本發明經過大量試驗、研究和分析成功研究出能夠用于快速、靈敏、有效的檢測CYP2C19基因多態性檢測引物、探針和試劑盒。利用這個試劑盒可以檢測出CYP2C19*2(G681A)、CYP2C19*3(G836A)和CYP2C19*17(C-806T)三個位點的基因多態性情況。
與現有技術相比,本發明運用ARMS引物區分野生型和突變型基因,有如下有益效果和顯著進步:
(1)靈敏度高,可以準確檢出低至1ng的基因組DNA。對于保存時間過長,提取濃度很低的樣本能準確檢出。
(2)特異性強,對于高至200ng及以上的基因組DNA不會出現非特異性的結果。
(3)成本低,ARMS分型法相對于Taqman探針分型法,不僅能保留Taqman的高靈敏度和高特異性,而且還能節約成本。
(4)操作簡單,檢測速度快,整個檢測過程只需要120分鐘。
(5)應用Fast Advanced Master Mix預混在反應體系中,減少了酶與樣本混合的步驟,減少了樣本的污染,避免了氣溶膠污染引起的假陽性。
總之,本發明涉及的CYP2C19基因多態性檢測試劑盒適用于臨床多種樣本類型選擇,具有特異性強,靈敏度高,實驗周期短,操作簡單,成本低等顯著優點。
附圖說明
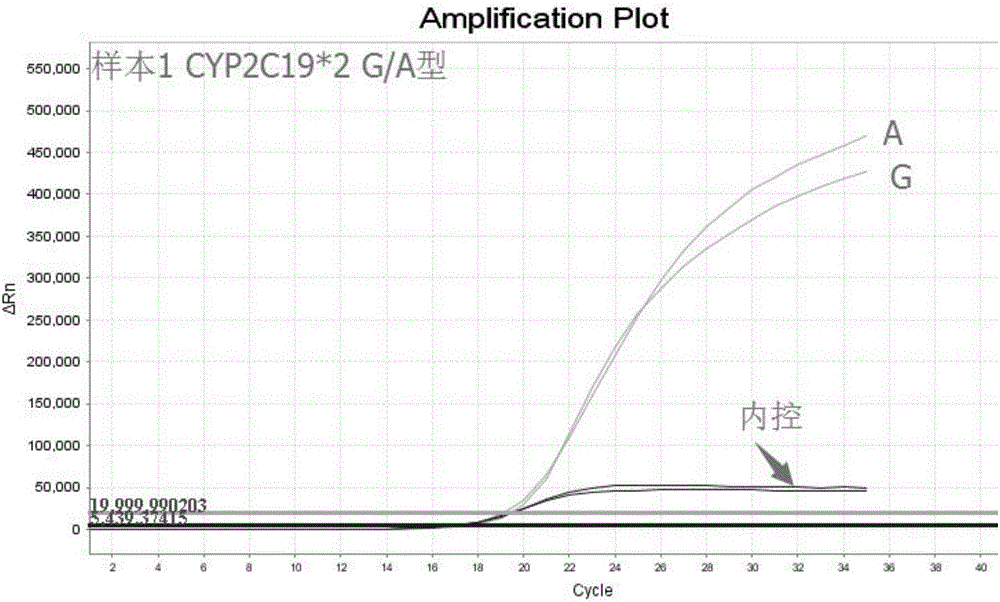
圖1是實施例3中樣本1第1、2孔擴增曲線(CYP2C19*2 G/A);
圖2是實施例3中樣本1第3、4孔擴增曲線(CYP2C19*3 G/G);
圖3是實施例3中樣本1第5、6孔擴增曲線(CYP2C19*17 C/C);
圖4是實施例3中樣本2第1、2孔擴增曲線(CYP2C19*2 G/A);
圖5是實施例3中樣本2第3、4孔擴增曲線(CYP2C19*3 G/A);
圖6是實施例3中樣本2第5、6孔擴增曲線(CYP2C19*17 C/C)。
具體實施方式
下面結合具體實施例對本發明作進一步說明,以使本領域的技術人員可以更好地理解本發明并能予以實施,但所舉實施例不作為對本發明的限定。
實施例1:試劑盒組成
本發明所述的檢測試劑盒組成如下表。
注:Fast Advanced Master Mix(簡稱AB premix),購自美國應用生物系統公司;10×buffer(PCR緩沖液,含Mg2+等)購自寶生物工程(大連)有限公司。試劑盒中,內控探針的核苷酸序列5’端標記的熒光報告基團為JOE,3’端標記的熒光淬滅基團為BHQ1。檢測探針均為MGB探針,探針核苷酸序列5’端標記熒光報告基團FAM,3’端標記熒光淬滅基團。
實施例2:樣本基因組DNA的提取
本實施例中收集人體全血樣本,從中提取基因組DNA。
從EDTA抗凝血中提取基因組DNA,并對其進行定量,作為PCR檢測的模板。采用天根生化科技(北京)有限公司的血液基因組DNA提取試劑盒,按照說明進行,具體詳述如下:
1、處理血液材料:
(1)當血液樣品體積小于200μL時,可加緩沖液GS補足體積至200μL,再進行下一步實驗(如血液樣品體積為200μL,可直接進行下一步實驗,不需加入GS)。
(2)當血液樣品體積超過200μL時,需用細胞裂解液CL處理,具體步驟如下:在樣品中加入1~2.5倍體積的細胞裂解液CL,顛倒混勻,10,000rpm(~11,500×g)離心1min,吸去上清,留下細胞核沉淀(如果裂解不徹底,可重復以上步驟一次),向離心收集到的細胞核沉淀中加200μL緩沖液GS,振蕩至徹底混勻。
2、加入20μL roteinase K溶液,混勻。
3、加200μL緩沖液GB,充分顛倒混勻,56℃放置10min,其間顛倒混勻數次,溶液應變清亮。
4、加200μL無水乙醇,充分顛倒混勻,此時可能會出現絮狀沉淀。
5、將上一步所得溶液和絮狀沉淀都加入一個吸附柱CB3中(吸附柱CB3放入收集管中),12,000rpm(~13,400×g)離心30sec,倒掉收集管中的廢液,將吸附柱CB3放入收集管中。
6、向吸附柱CB3中加入500μL緩沖液GD(使用前請先檢查是否已加入無水乙醇),12,000rpm(~13,400×g)離心30sec,倒掉收集管中的廢液,將吸附柱CB3放入收集管中。
7、向吸附柱CB3中加入600μL漂洗液PW(使用前請先檢查是否已加入無水乙醇),12,000rpm(~13,400×g)離心30sec,倒掉收集管中的廢液,將吸附柱CB3放入收集管中。
8、重復操作步驟7。
9、12,000rpm(~13,400×g)離心2min,倒掉廢液。將吸附柱CB3置于室溫放置數分鐘,以徹底晾干吸附材料中殘余的漂洗液。
10、將吸附柱CB3轉入1.5ml離心管中,向吸附膜中間位置懸空滴加50-200μL洗脫緩沖液TB,室溫放置2-5min,12,000rpm(~13,400×g)離心2min,將溶液收集到離心管中。
11、定量
將提取的DNA用紫外分光光度計進行定量,稀釋DNA濃度到1ng/μL。
實施例3:樣本基因組DNA的檢測
本實施例采用實施例1中所列舉的引物、探針組合來擴增實施例2所提取的基因組DNA樣品。
檢測CYP2C19基因多態性的反應體系組成:
10×buffer(Mg2+Plus):4~8μL,
dNTPs:50~250μM(each),
各條引物:150~300nM,
各條探針:50~200nM,
FastAdvanced Master Mix:6~12μL,
模板:10μL,
總體積:40μL。
PCR反應條件設置:
檢測方法如下:
1、每次PCR反應中,同時進行非模板對照(No Template Control;NTC)、陽性對照和待測樣本的檢測。
2、將陽性對照取出解凍后震蕩混勻,并離心30sec。
3、將6聯PCR反應條取出解凍后離心30sec,防止反應液在開蓋時濺出。
4、將ddH2O(NTC)、實施例1中提取的DNA樣本、陽性對照分別加入6聯PCR反應條,每孔10μL。
5、將以上6聯PCR反應條蓋好管蓋于離心機上離心30sec,確保管壁上不沾有液滴。
6、將6聯PCR反應條放于實時PCR儀器中,用預設的反應程序進行PCR擴增。
檢測結果分析:
根據熒光定量PCR擴增儀Ct值分析檢測結果:以非模板對照(NTC)和陽性對照(STD)FAM及JOE信號Ct值作為實驗數據是否有效的判定標準(非模板對照FAM及JOE信號不起線,或Ct>28;陽性對照FAM及JOE信號Ct值≤25,體系性能良好,結果有效);以待測樣本JOE信號Ct值作為PCR反應是否成功的判定標準(JOE信號Ct值≤25,擴增正常),以待測樣本每組SNP位點檢測孔FAM信號Ct值的差值作為判斷標準。
注:Ct1~Ct6分別表示第1到第6孔的FAM信號Ct值。其中第1、2孔為一組,3、4孔為一組,5、6孔為一組;分別計算三組Ct值的差值。當ct值為Undetermined(無擴增曲線)時,該孔的Ct值記為∞。
附圖1~3中,Ct2-Ct1=-0.39,Ct4-Ct3=∞,Ct6-Ct5=∞。結果顯示樣本1為CYP2C19*2雜合型(G/A),CYP2C19*3純野生型(G/G),CYP2C19*17純野生型(C/C)。
附圖4~6中,Ct2-Ct1=-0.44,Ct4-Ct3=0.2,Ct6-Ct5=17.81。結果顯示樣本2為CYP2C19*2雜合型(G/A),CYP2C19*3雜合型(G/A),CYP2C19*17純野生型(C/C)。
以上所述實施例僅是為充分說明本發明而所舉的較佳的實施例,本發明的保護范圍不限于此。本技術領域的技術人員在本發明基礎上所作的等同替代或變換,均在本發明的保護范圍之內。本發明的保護范圍以權利要求書為準。
SEQUENCE LISTING
<110> 武漢海吉力生物科技有限公司
<120> CYP2C19基因多態性檢測引物、探針及試劑盒
<130> WH1610026-1
<160> 15
<170> PatentIn version 3.3
<210> 1
<211> 24
<212> DNA
<213> 人工序列
<400> 1
cccactatca ttgattattt caca 24
<210> 2
<211> 26
<212> DNA
<213> 人工序列
<400> 2
ttcccactat cattgattat tgccgg 26
<210> 3
<211> 22
<212> DNA
<213> 人工序列
<400> 3
ccattttgat caggaagcaa tc 22
<210> 4
<211> 14
<212> DNA
<213> 人工序列
<400> 4
ccttgctttt atgg 14
<210> 5
<211> 19
<212> DNA
<213> 人工序列
<400> 5
gattgtaagc accacctga 19
<210> 6
<211> 19
<212> DNA
<213> 人工序列
<400> 6
gattgtaagc acccactgg 19
<210> 7
<211> 21
<212> DNA
<213> 人工序列
<400> 7
ctaggcaaga ctgtagtatt c 21
<210> 8
<211> 16
<212> DNA
<213> 人工序列
<400> 8
ccaggtaagg ccaagt 16
<210> 9
<211> 20
<212> DNA
<213> 人工序列
<400> 9
gtgtcttctg ttctcaacgt 20
<210> 10
<211> 20
<212> DNA
<213> 人工序列
<400> 10
gtgtcttctg ttctcaaggc 20
<210> 11
<211> 20
<212> DNA
<213> 人工序列
<400> 11
ctcatagctg gcagaactgg 20
<210> 12
<211> 16
<212> DNA
<213> 人工序列
<400> 12
cgccacgatg ggcatc 16
<210> 13
<211> 21
<212> DNA
<213> 人工序列
<400> 13
ggaaagtgat attttggaga a 21
<210> 14
<211> 20
<212> DNA
<213> 人工序列
<400> 14
ccattttgat caggaagcaa 20
<210> 15
<211> 36
<212> DNA
<213> 人工序列
<400> 15
caccaagaat cgatggacat caacaaccct cgggac 36
- 還沒有人留言評論。精彩留言會獲得點贊!
- 一種快速區分prv中國型、歐美型及疫苗株的雙色熒光檢測方法、引物及探針的制作方法
- 實時熒光pcr技術定量檢測myd88基因l265p突變的方法、引物和探針的制作方法
- 用于定性檢測白血病融合基因的引物、探針、試劑盒及方法
- 在體外檢測或/及定量乙型肝炎病毒的方法及其所使用的引物、探針的制作方法
- 用于檢測多種呼吸道病毒的pcr引物組、探針組及試劑盒的制作方法
- 一種檢測人類met基因14外顯子剪接突變的引物、探針及試劑盒的制作方法
- 使用重疊引物和熔解探針檢測單核苷酸多態性的制作方法
- 用于檢測多種呼吸道病毒的pcr引物組、探針組及試劑盒的制作方法
- 一種檢測人類met基因14外顯子剪接突變的引物、探針及試劑盒的制作方法
- 使用重疊引物和熔解探針檢測單核苷酸多態性的制作方法
- 一種木瑚菌屬食用菌鑒別用分子標記及引物和探針的制造方法與工藝
- 一組用于驢源性的實時熒光PCR檢測的特異性引物和探針的制造方法與工藝
- 一組用于雞源性實時熒光PCR檢測的特異性引物和探針的制造方法與工藝
- 一種快速檢測異鱗蛇鯖和棘鱗蛇鯖源性成分的方法與制造工藝
- 一種檢測食管癌相關標志物的探針組合及其試劑盒的制造方法與工藝
- 一種檢測皮膚癌相關標志物的探針組合及其試劑盒的制造方法與工藝
- 一種檢測骨髓瘤相關標志物的探針組合及其試劑盒的制造方法與工藝
- 一種用于檢測樣品中牛凸隆病毒的熒光RT-PCR引物、探針和試劑盒及檢測方法與制造工藝
- CYP2C19基因多態性檢測引物、探針及試劑盒的制造方法與工藝
- 檢測CYP2C9和VKORC1基因多態性的引物、探針和試劑盒的制造方法與工藝