一種用于病毒基因分型檢測的探針組合、試劑盒以及方法與流程
本發明涉及基因檢測技術領域,具體而言,涉及一種用于病毒基因分型檢測的探針組合、試劑盒以及方法。
背景技術:
宮頸癌是女性生殖道最常見的惡性腫瘤之一,已有研究表明,高危型人乳頭瘤病毒(Human Papillomavirus,HPV)持續感染及多重感染是導致宮頸癌變的重要原因之一,全球范圍的研究結果顯示,在99.7%的宮頸癌患者體內檢測到高危型HPV DNA的存在。目前已經發現的HPV有200多種型別,主要包括低危型和高危型兩大類。不同型別與不同疾病的相關性也不一樣,低危型HPV感染可能會引起生殖道濕疣病變,高危型HPV感染則與宮頸癌、陰道癌相關。目前還缺乏針對HPV公認的有效治療手段,因此宮頸HPV早發現、早預防是阻斷癌變的關鍵。
多年來,國際上通用的宮頸上皮內瘤變及宮頸癌的診斷主要遵循“三階梯式”診斷程序,即宮頸細胞學、陰道鏡及組織病理學檢查。由于HPV不能體外培養,HPV檢測方法主要基于HPV DNA的分子分型。HPV核酸檢測技術主要包括雜交捕獲法,PCR-熒光探針法、轉錄介導的核酸擴增技術以及PCR-雜交法等。
宮頸癌的早期篩查方式是采用巴氏涂片以及改進后的TCT技術,這些方法只能從細胞學病變的角度來評估宮頸癌的發病情況,也就是說需要等到遭受病毒感染的細胞開始出現明顯變化時才可以檢測出來,特異性和靈敏度均不夠理想。隨著對HPV感染導致宮頸癌的認識加深以及分子診斷技術的發展,HPV基因檢測作為宮頸癌的一種篩查手段得到了更廣泛的應用。目前HPV分型檢測技術主要基于聚合酶鏈反應,如熒光定量、反向斑點雜交和基因芯片技術等,這些技術表現出高靈敏度、高特異性,可以進行多重感染檢測等優點,但這些技術對實驗條件和檢驗人員素質要求高,檢測費用也較高,不太適用于大量的臨床檢測和大規模的流行病學篩查。第二代基因雜交捕獲技術檢測采用美國Digene公司的HC2技術試劑盒,HC2是一種應用微孔板化學發光進行信號放大的核酸雜交檢測方法,被公認為評價HPV檢測新技術的金標準。然而,HC2檢測方法價格昂貴,且其方法操作繁瑣,操作過程中容易交叉污染而出現假陽性。
技術實現要素:
本發明的第一目的在于提供一種用于病毒基因分型檢測的探針組合,該探針組合能夠對待測樣本中的病毒進行基因型檢測,具有較強的特異性、較高的靈敏度以及較低的假陽性率,且檢出結果準確可靠。
本發明的第二目的在于提供一種用于病毒基因分型檢測的試劑盒,該試劑盒能夠對待測樣本中的病毒進行基因型檢測,其具有較強的特異性和較高的靈敏度,且檢出結果準確可靠、假陽性率低、操作簡單方便。
本發明的第三目的在于提供一種病毒基因分型檢測的方法,該方法能夠對待測樣本中的病毒進行基因型檢測,具有較強的特異性和較高的靈敏度,且檢出結果準確可靠,檢測方法簡單易操作。
本發明解決其技術問題是采用以下技術方案來實現的。
一種用于病毒基因分型檢測的探針組合,其包括至少一個探針對,每個探針對包括用于結合目標序列的捕獲探針(Capture Probe,CP)和與捕獲探針相對應的且可結合目標序列的檢測探針(Detector Probe,DP),每個探針對的檢測探針的3’端或5’端標記有用于結合催化酶的親和物,催化酶用于催化底物產生化學反應形成電子流。
一種用于病毒基因分型檢測的試劑盒,其包括上述的用于病毒基因分型檢測的探針組合。
一種用于病毒基因分型檢測的方法,其包括如下步驟:
先將用于結合目標序列的捕獲探針通過電場作用固定至檢測孔板的反應孔內;
將待測樣本加入至反應孔內;
加入與捕獲探針對應的且可結合目標序列的檢測探針至反應孔內,檢測探針的3’端或5’端標記有可用于結合用于催化相應底物產生化學反應形成電子流的催化酶的親和物;
加入催化酶和底物,通過電流檢測裝置檢測反應孔內的電流。
本發明提供的用于病毒基因分型檢測的探針、試劑盒以及方法的有益效果是:本發明提供的用于病毒基因分型檢測的探針組合包括至少一個探針對,每個探針對包括有用于結合目標序列的捕獲探針和與捕獲探針相對應的且可結合目標序列的檢測探針,捕獲探針通過堿基互補原則與目標序列結合,將目標序列捕獲固定,進行第一次特異性結合固定;檢測探針通過堿基互補原則與目標序列第二特異性結合,檢測探針被結合固定;檢測探針的3’端或5’端的通過標記的親和物將催化酶結合,催化酶催化底物釋放電流信號,檢測釋放的電流信號,進而檢測出病毒基因型。由于,目標序列只有與捕獲探針和檢測探針同時準確配對后即經過兩次特異性結合,才能有信號的產生,這大大地提高了檢測的特異性,使得檢出結果準確可靠,假陽性率非常低。
附圖說明
為了更清楚地說明本發明實施例的技術方案,下面將對實施例中所需要使用的附圖作簡單地介紹,應當理解,以下附圖僅示出了本發明的某些實施例,因此不應被看作是對范圍的限定,對于本領域普通技術人員來講,在不付出創造性勞動的前提下,還可以根據這些附圖獲得其他相關的附圖。
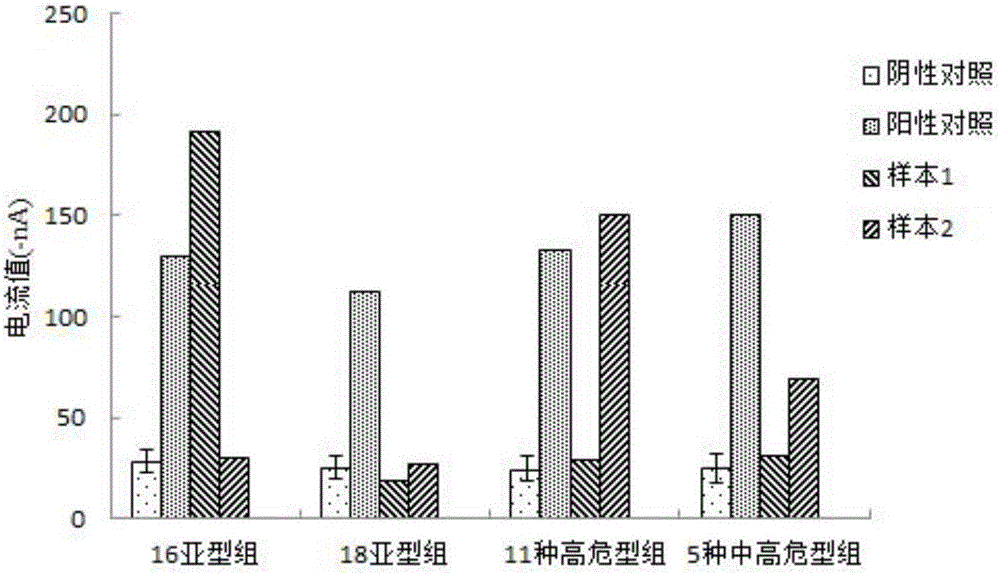
圖1為本發明實施例1的檢測結果;
圖2為本發明實施例2的檢測結果;
圖3為本發明實施例3的檢測結果;
圖4為本發明實施例4的檢測結果;
圖5為本發明實施例5的檢測結果。
具體實施方式
為使本發明實施例的目的、技術方案和優點更加清楚,下面將對本發明實施例中的技術方案進行清楚、完整地描述。實施例中未注明具體條件者,按照常規條件或制造商建議的條件進行。所用試劑或儀器未注明生產廠商者,均為可以通過市售購買獲得的常規產品。
下面對本發明實施例的用于病毒基因分型檢測的探針、試劑盒以及方法進行具體說明。
本發明提供的用于病毒基因分型檢測的探針組合,其包括至少一個探針對。每個探針對包括用于結合目標序列的捕獲探針和與捕獲探針相對應的且可結合目標序列的檢測探針。每個探針對的檢測探針的3’端或5’端標記有用于結合催化酶的親和物,該催化酶用于催化其底物產生化學反應形成電子流。
其中,檢測探針與捕獲探針相對應是指,一個捕獲探針和一個檢測探針組成一個探針對,即可用于檢測某類型的病毒。捕獲探針和檢測探針均根據同一類型的病毒的同一個保守基因或保守DNA片段即目標序列進行設計的,捕獲探針和檢測探針能夠與該病毒類型的同一個保守基因或保守DNA片段的不同區域或結合位點通過堿基互補原則結合,但捕獲探針與檢測探針并不互補,堿基序列也不相同,二者與目標序列的結合位點不重合、也不重疊。另外,捕獲探針和檢測探針與目標序列的結合區域可以是相鄰,也可以是間隔多個堿基。只要捕獲探針和檢測探針能夠與同一類型的病毒的同一個保守基因或同一段保守DNA片段通過堿基互補原則結合即可。
具體地,本發明針對各HPV亞型,根根其DNA保守區域設計出了用于檢測HPV基因型的探針組合,探針組合包括多個探針對,該多個探針對分別是:第1探針對、第2探針對、選自第3~11探針對中的至少一種、以及選自第12~16探針對中的至少一種。以下對各探針對檢測的HPV亞型及其捕獲探針和堿基探針的序列進行詳細說明。
具體地,用于檢測HPV16亞型的第1探針對,其捕獲探針的堿基序列如SEQ ID NO.1所示,其檢測探針的堿基序列如SEQ ID NO.2所示。
用于檢測HPV18亞型的第2探針對,其捕獲探針的堿基序列如SEQ ID NO.3所示,其檢測探針的堿基序列如SEQ ID NO.4所示。
用于檢測HPV31亞型的第3探針對,其捕獲探針的堿基序列如SEQ ID NO.5所示,其檢測探針的堿基序列如SEQ ID NO.14所示。
用于檢測HPV33亞型或52亞型或58亞型的第4探針對,其捕獲探針的堿基序列如SEQ ID NO.6所示,其檢測探針的堿基序列如SEQ ID NO.15所示,該三種亞型共用第4探針對。
用于檢測HPV35亞型的第5探針對,其捕獲探針的堿基序列如SEQ ID NO.7所示,其檢測探針的堿基序列如SEQ ID NO.14所示。
用于檢測HPV39亞型的第6探針對,其捕獲探針的堿基序列如SEQ ID NO.8所示,其檢測探針的堿基序列如SEQ ID NO.16所示。
用于檢測HPV45亞型的第7探針對,其捕獲探針的堿基序列如SEQ ID NO.9所示,其檢測探針的堿基序列如SEQ ID NO.17所示。
用于檢測HPV51亞型的第8探針對,其捕獲探針的堿基序列如SEQ ID NO.10所示,其檢測探針的堿基序列如SEQ ID NO.18所示。
用于檢測HPV 56亞型的第9探針對,其捕獲探針的堿基序列如SEQ ID NO.11所示,其檢測探針的堿基序列如SEQ ID NO.18所示。
用于檢測HPV59亞型的第10探針對,其捕獲探針的堿基序列如SEQ ID NO.12所示,其檢測探針的堿基序列如SEQ ID NO.19所示。
用于檢測HPV68亞型的第11探針對,其捕獲探針的堿基序列如SEQ ID NO.13所示,其檢測探針的堿基序列如SEQ ID NO.16所示。
用于檢測HPV26亞型的第12探針對,其捕獲探針的堿基序列如SEQ ID NO.20所示,其檢測探針的堿基序列如SEQ ID NO.26所示。
用于檢測HPV53亞型的第13探針對,其捕獲探針的堿基序列如SEQ ID NO.21所示,其檢測探針的堿基序列如SEQ ID NO.25所示。
用于檢測HPV66亞型的第14探針對,其捕獲探針的堿基序列如SEQ ID NO.22所示,其檢測探針的堿基序列如SEQ ID NO.25所示。
用于檢測HPV73亞型的第15探針對,其捕獲探針的堿基序列如SEQ ID NO.23所示,其檢測探針的堿基序列如SEQ ID NO.27所示。
用于檢測HPV82亞型的第16探針對,其捕獲探針的堿基序列如SEQ ID NO.24所示,其檢測探針的堿基序列如SEQ ID NO.28所示。
需要說明的是,上述各探針對的捕獲探針序列和檢測探針序列的堿基序列可以是不相互對應的,也就是說,在其他的實施例中,各探針對的捕獲探針序列可以是上述所述的堿基序列,而其相應的檢測探針的堿基序列可以是取自同一檢測亞型病毒的同一DNA保守區域其他的序列的互補;或者在其他的實施例中,各探針對的檢測探針序列可以是上述所述的堿基序列,而其相應的捕獲探針的堿基序列可以是其他的序列選擇自同一檢測亞型病毒的同一DNA保守區域其他的序列的互補序列。但本發明給出的各探針對的捕獲探針和檢測探針的堿基序列,在其進行檢測時,其具有更強的特異性、更高的靈敏度等優點,具有檢測結果可見實施例。
其中,根據各亞型病毒在宮頸癌患者出現的概率大小,一般情況下將上述各亞型病毒作如下分類。HPV16、18亞型是臨床最常見的,也是該兩類型病毒在宮頸癌患者出現的概率最大;HPV31、33、52、58、35、39、45、51、56、59、68亞型是高等風險型型別的(可統稱為高危型組),HPV26、53、66、73、82亞型是中等風險型別的(可統稱為中高危型組)。在對這些亞型病毒檢測中,可以進行分組檢測例如僅檢測出樣本含有某個危險級別(例如高危型組或中高危型組)的病毒,而不必檢測出其含有那個組別中的具體某類型病毒。當然,也可以進行具體亞型的檢測,例如檢測出樣本中具體含有高危型組中的某類亞型例如HPV53亞型病毒。具體采用何種檢測方法檢測至何種程度,得到何種程度的檢測結果,檢測人員可以根據具體情況來選擇,以提供較合理的指導意義,具體分組檢測的情況見實施例。
本發明提供的用于病毒基因分析檢測的探針組合包括第1探針對,第2探針對,選自第3~11探針對中的至少一種,選自第12~16探針對中的至少一種。這樣,本發明的探針組合可對HPV常見亞型的HPV16和18亞型,高危型的HPV31、33、52、58、35、39、45、51、56、59、68亞型中的至少一種,以及中高危型的HPV26、53、66、73、82亞型中的至少一種,共至少4種HPV亞型進行檢測。
當然,在其他的實施例中,用于病毒基因分析檢測的探針組合可以僅包括第1探針對~第16探針對中的一種或二種或三種。
另外,較佳地,上述每個檢測探針的3’端或5’端標記的親和物是生物素,生物素的作用在于與鏈霉親和素標記的催化酶結合,通過催化酶催化底物產生的電流釋放檢測信號。當然,在其他的實施例中,檢測探針可以不通過生物素-鏈霉親和素的識別系統結合催化酶,可以通過其他的例如抗體/抗原、配體/受體等結合系統來結合催化酶,因此,親和物可以抗原/抗體中的一種。例如親和物可以是地高辛或者異硫氰酸熒光素,對應地,催化酶上標記有高辛抗體或異硫氰酸熒光素抗體即可。且親和物可以標記在檢測探針的3’端記,也可以標記在其5’端,二者均可以。
還有需要說明的是,在其他的實施例中,可根據其他病毒例如艾滋病毒(Human Immunodeficiency Virus,HIV)、乙肝病毒(Hepatitis Bvirus,HBV)等病毒基因組序列的保守區域設計出相應的捕獲探針和檢測探針,用于檢測其具體的病毒亞型,其也屬于本發明的保護范圍。
本發明提供的用于病毒基因分型檢測的試劑盒,其包括上述所述的任意一項探針組合。優選地,各探針以溶液的形式獨立存在,例如捕獲探針以含有捕獲探針的捕獲探針溶液的形式存在,檢測探針以含有檢測探針的檢測探針溶液的形式存在。各探針溶液含有的探針濃度為可以根據實際情況設置。優選地,各探針溶液含有的探針終濃度為0.5~1.5μM。
另外,本發明提供的用于病毒基因分型檢測的試劑盒還可包括將探針對的捕獲探針固定至檢測孔板的固定物。固定物包括導電聚合物和離子化合物。導電聚合物選自吡咯、苯胺和噻吩中的一種,當然,導電聚合物也可以是其他的導電聚合物材料。離子化合物選自氯化鈉和氯化鉀中的任一種。導電聚合物帶正電,其在電場的作用下形成網狀交聯結構,被沉積在反應孔的底部,網狀交聯結構能夠穩定地將捕獲探針固定在底部,有助于提高捕獲探針的穩定性和捕獲能力。
另外,本發明提供的用于病毒基因分型檢測的試劑盒還可包括檢測孔板,檢測孔板的反應孔內固定有探針對的捕獲探針。檢測孔板的具體結構可參考如申請號為201620769829.2公開的名稱為檢測電極以及檢測孔板中的檢測孔板所示。
另外,本發明提供的用于病毒基因分型檢測的試劑盒還可包括催化酶,催化酶是帶有標記物的辣根過氧化物酶,優選地,催化酶是帶有鏈霉親和素標記的辣根過氧化物酶。當然,催化酶也可以是帶有標記物的堿性磷酸酶,標記物為地高辛抗體、異硫氰酸熒光素抗體或鏈霉親和素中的任一種,標記物與親和物相對應,其可根據檢測探針上的親和物的類別進行選擇。當親和物是生物素時,標記物為鏈霉親和素;當親和物是地高辛時,標記物為地高辛抗體;當親和物是異硫氰酸熒光素時,標記物為異硫氰酸熒光素抗體。只要親和物與標記物相對應,可相互結合即可。
另外,本發明提供的用于病毒基因分型檢測的試劑盒還可包括底物,底物的類別根據催化酶的類別選擇。
當催化酶為辣根過氧化物酶時,底物是TMB(Tetramethylbenzidine、四甲基聯苯胺)、ABTS(2,2'-Azinobis-(3-ethylbenzthiazoline-6-sulphonate、2,2-聯氮-二(3-乙基-苯并噻唑-6-磺酸)二銨鹽)和OPD(o-Phenylenediamine、鄰苯二胺)中的任一種。TMB、ABTS和OPD均是辣根過氧化物酶的底物,在辣根過氧化物酶的催化作用下發生顯色反應并伴隨電流產生,有助于提高檢測信號的釋放。
當催化酶為堿性磷酸酶時,底物是對BCIP(5-Bromo-4-Chloro-3-Indolyl Phosphate、5-溴-4-氯-3-吲哚基-磷酸鹽)和NBT(Nitrotetrazolium Blue chloride、四唑硝基藍)的組合物、硝基苯磷酸鹽、4-硝基苯磷酸二鈉、萘酚AS-BI磷酸鹽、萘酚-AS-MX-磷酸鹽中的任一種。
另外,本發明提供的用于病毒基因分型檢測的試劑盒還可包括清洗液,清洗液包括洗液A和洗液B,洗液A是含SDS的SSC緩沖液,洗液B是含Tween20的PBS緩沖液。
另外,本發明提供的用于病毒基因分型檢測的試劑盒還可包括稀釋液,稀釋液是含酪蛋白的PBS緩沖液。
本發明提供的用于病毒基因分型檢測的方法,其包括:
捕獲探針固定步驟:先將用于結合目標序列的捕獲探針通過電場作用固定至檢測孔板的反應孔內。捕獲探針在電場作用下,往反應孔底部移動沉積,并被固定在反應孔底部。
樣本雜交步驟:將待測樣本加入至反應孔內。待測樣本中的目標序列與捕獲探針通過堿基互補原則被捕獲固定在反應孔底部;
檢測探針結合步驟:加入與捕獲探針對應的且可結合目標序列的檢測探針至反應孔內,檢測探針的3’端或5’端標記有可用于結合用于催化相應底物產生化學反應形成電子流的催化酶的親和物。檢測探針通過堿基互補原則與目標序列結合固定在反應孔內。
酶催化反應檢測步驟:加入催化酶和底物至反應孔內,通過電流檢測裝置檢測反應孔內的電流。檢測探針通過親和物與催化酶結合,催化酶再催化底物產生電流釋放檢測信號,該信號被電流檢測裝置識別放大,進而檢出結果。
需要說明的是,上述方法中所采用的檢測孔板和電流檢測裝置均可通過市面上購買得到。
本發明的檢測原理是利用電場誘導釋放和測量(Electric Field–Induced Release and Measurement,EFIRM)技術快速檢測病毒基因型,尤其是對18種高危型HPV進行檢測。EFIRM的基本原理是:
在電場作用下捕獲探針被固定在檢測孔板上的反應孔的孔底;CP在電場作用下通過堿基互補配對原則捕獲待測樣本中的目標序列即病毒DNA;帶有生物素標記的檢測探針再與目標序列結合;催化酶通過其標記的鏈霉親合素與生物素識別,結合;往反應孔加入催化酶的底物,產生氧化還原反應,有電流產生,儀器檢測電流信號,進而判斷出待測樣本中有相應的目標序列,由于捕獲探針和檢測探針均是根據特定病毒類型的保守區域進行設計的,進而可知該病毒的類型。
以下結合實施例對本發明的特征和性能作進一步的詳細描述。
實施例1
本實施例以檢測HPV基因型為例,對本實施例提供的用于病毒基因分型檢測的試劑盒進行說明。本實施例對取自兩個不同的宮頸癌患者的宮頸口處的細胞(即待測樣本)檢測其HPV亞型,取自兩個不同患者的待測樣本分別命名為樣本1和樣本2,并對樣本1和樣本2同時檢測,取好的樣本1和樣本2于-20℃存儲。
本實施例提供的病毒基因分型檢測的試劑盒包括探針組合,該探針組合包括16個用于對HPV亞型檢測的探針對,各探針對的捕獲探針和檢測探針以溶液形式獨立存在,探針的終濃度均為1μM。該16個探針對分別是:用于檢測HPV 16亞型的第1探針對,其捕獲探針的堿基序列如SEQ ID NO.1所示,其檢測探針的堿基序列如SEQ ID NO.2所示;用于檢測HPV 18亞型的第2探針對,其捕獲探針的堿基序列如SEQ ID NO.3所示,其檢測探針的堿基序列如SEQ ID NO.4所示;用于檢測HPV 31亞型的第3探針對,其捕獲探針的堿基序列如SEQ ID NO.5所示,其檢測探針的堿基序列如SEQ ID NO.14所示;用于檢測HPV 33亞型或52亞型或58亞型的第4探針對,其捕獲探針的堿基序列如SEQ ID NO.6所示,其檢測探針的堿基序列如SEQ ID NO.15所示;用于檢測HPV 35亞型的第5探針對,其捕獲探針的堿基序列如SEQ ID NO.7所示,其檢測探針的堿基序列如SEQ ID NO.14所示;用于檢測HPV 39亞型的第6探針對,其捕獲探針的堿基序列如SEQ ID NO.8所示,其檢測探針的堿基序列如SEQ ID NO.16所示;用于檢測HPV 45亞型的第7探針對,其捕獲探針的堿基序列如SEQ ID NO.9所示,其檢測探針的堿基序列如SEQ ID NO.17所示;用于檢測HPV 51亞型的第8探針對,其捕獲探針的堿基序列如SEQ ID NO.10所示,其檢測探針的堿基序列如SEQ ID NO.18所示;用于檢測HPV 56亞型的第9探針對,其捕獲探針的堿基序列如SEQ ID NO.11所示,其檢測探針的堿基序列如SEQ ID NO.18所示;用于檢測HPV 59亞型的第10探針對,其捕獲探針的堿基序列如SEQ ID NO.12所示,其檢測探針的堿基序列如SEQ ID NO.19所示;用于檢測HPV 68亞型的第11探針對,其捕獲探針的堿基序列如SEQ ID NO.13所示,其檢測探針的堿基序列如SEQ ID NO.16所示;用于檢測HPV 26亞型的第12探針對,其捕獲探針的堿基序列如SEQ ID NO.20所示,其檢測探針的堿基序列如SEQ ID NO.26所示;用于檢測HPV 53亞型的第13探針對,其捕獲探針的堿基序列如SEQ ID NO.21所示,其檢測探針的堿基序列如SEQ ID NO.25所示;用于檢測HPV 66亞型的第14探針對,其捕獲探針的堿基序列如SEQ ID NO.22所示,其檢測探針的堿基序列如SEQ ID NO.25所示;用于檢測HPV 73亞型的第15探針對,其捕獲探針的堿基序列如SEQ ID NO.23所示,其檢測探針的堿基序列如SEQ ID NO.27所示;用于檢測HPV 82亞型的第16探針對,其捕獲探針的堿基序列如SEQ ID NO.24所示,其檢測探針的堿基序列如SEQ ID NO.28所示。各HPV亞型類別及其檢測對應的捕獲探針和檢測探針的堿基序列見表1。
表1.檢測HPV亞型的捕獲探針和檢測探針的堿基序列
其中,檢測33、52和58亞型的捕獲探針堿基序列相同,檢測33、52和58亞型的檢測探針堿基序列相同,也就是說用SEQ ID NO.6所示的捕獲探針和SEQ ID NO.15所示的檢測探針能夠檢測出HPV33、52和58亞型病毒,檢出結果說明的是樣品具有HPV33、52和58亞型中的至少一種,但具體是該三種亞型病毒中的哪一種亞型病毒并不能檢測出。39和68亞型的檢測探針序列相同,51和56亞型的檢測探針序列相同,53和66亞型的檢測探針序列相同。此外,用于檢測16和18亞型的檢測探針的5’端標記生物素,其余亞型的檢測探針的3’端標記生物素(如表1所示)。
采用本實施例提供的病毒基因分型檢測試劑盒對樣本1和樣本2的具體檢測步驟如下。
1捕獲探針固定
1.1配制吡咯(pyrrole)與CP的混合液
取1個1.5mL離心管,依次加入超純水885μl,離子化合物100μl 3M KCl,渦旋震蕩混勻,離心;加入導電聚合物5μl pyrrole(≥98.0%,購自Sigma,貨號W338605),渦旋震蕩混勻,離心;加入10μl CP(100μM)(在分組檢測的情況下,將每種CP各加入10μl至檢測孔中);渦旋震蕩混勻后離心,備用。
1.2固定捕獲探針
在96孔的檢測孔板(E-plate)(其結構和工作原理可見參考文獻201620769829.2)上,按其操作說明書,往反應孔加入30μl的已配制好的pyrrole與CP的混合液,加樣時槍頭貼近孔的底部,但是不接觸到底部電極,加完后傾斜或拍打E-plate使液體在孔里的電極表面均勻覆蓋,然后立刻到EFIRM儀器上(其工作原理和結構可參考申請日為2016年8月11日、申請號為201610658321.X、名稱為保持結構及包括保持結構的檢測儀的專利文獻),按其操作說明書,進行電場操作。
1.3EFIRM電場處理
在EFIRM軟件上選擇進行實驗的對應列,電場參數設置為:電壓A:350mV,1s;電壓B:950mV,1s;進行9個循環。電場處理完畢,立刻取出,清洗E-plate板。
1.4E-plate板清洗:
在洗板機程序上選擇對應的實驗列,清洗程序選擇(2bottom,2top),清洗液選擇洗液A。清洗完畢,立刻進行下一步,樣本上樣操作。其中,洗液A為含0.05%(質量百分比)SDS的2×SSC緩沖液。
2樣本雜交
2.1雜交buffer預處理
雜交buffer(購自thermo fisher)在水浴鍋中90℃水浴處理10min,然后室溫放置冷卻20min。
2.2配制待測樣本
待測樣本從-20℃冰箱取出,放進4℃冰箱解凍。完全溶解后,使用煮沸法或0.4M NaOH預處理待測樣本,然后將待測樣本與雜交buffer按體積比1:2混合,渦旋振蕩后離心,即可上樣進行檢測。
2.3加待測樣本
在E-plate上,在對應的孔里加入上述待測樣本與雜交buffer混合后的混合液30μl。(需要注意的是:加樣時槍頭貼近孔的底部,但是不接觸到底部電極,加完后傾斜或拍打E-plate使液體在孔里的電極表面均勻覆蓋,然后立刻到EFIRM上進行電場操作。)
在本實施例中,設置4個檢測組,分別是16亞型組、18亞型組、11種高危型組以及5種中高危型組。每個檢測組設置一個陽性對照孔,一個陰性對照孔(重復4次),一個樣本1的檢測孔以及一個樣本2的檢測孔。其中,16亞型組用于檢測HPV16亞型(該組每個孔中對應加入第1探針對),18亞型組用于檢測HPV18亞型(該組每個孔對應加入第2探針對),11種高危型組用于檢測11種高危型HPV中的一種(該組每個孔對應加入第3~11探針對,5種中高危型用于檢測5種中高危型HPV中的一種(該組每個孔對應加入第12~16探針對)。需要說明的是,檢測組的數量可根據需要的檢測結果準確程度進行設計。如果僅需檢測出待測樣本是否含有常見型HPV、高危型病毒以及中高危型病毒,則可按本實施例的檢測組的設置方法進行設置。如果僅需檢測出樣本是否含有HPV,則可僅設置一個檢測組,具體檢測方法參考實施例2。如果需要檢測出樣本具體含有某類型的病毒,則可設置18個檢測組,具體檢測方法參考實施例3。
其中,陽性對照孔中加入對應的30μl含終濃度為1pM的陽性寡核苷酸(其能夠與對應的捕獲探針和檢測探針互補配對結合)的雜交buffer作為陽性對照(需要說明的是,11種高危型組的陽性對照僅選擇52亞型核苷酸序列(表2中的第9行),5種中高危型組的陽性對照僅選擇26亞型核苷酸序列(表2中的第13行),即可起到陽性對照的作用),各HPV亞型對應的陽性寡核苷酸的堿基序列見表2,陰性對照孔中加入30μl雜交buffer作為陰性對照。
表2.用于檢測HPV基因型的陽性對照的陽性寡核苷酸的堿基序列
2.4EFIRM電場處理
在EFIRM軟件上選擇進行實驗的對應列,電場參數設置為:電壓A:300mV,1s;電壓B:500mV,1s;進行150個循環。電場處理完畢,立刻取出,清洗E-plate板。
2.5室溫孵育
蓋上E-plate蓋子,實驗臺上室溫孵育30min。
2.6E-plate板清洗
在洗板機程序上選擇對應的實驗列,清洗程序選擇(2bottom,2top),清洗液選擇洗液A。清洗完畢,立刻進行DP加樣操作。
3DP結合
3.1DP溶液配制
從4℃冰箱取出稀釋液,取1個1.5mL離心管,加入990μl的稀釋液,往各檢測組的反應孔中加入對應的10μl DP(100μM),渦旋震蕩混勻,離心,備用。其中,稀釋液為含0.1%(質量體積比)酪蛋白的PBS緩沖液(pH7.4)。酪蛋白的作用是封閉非特異性位點,以提高檢測的靈敏性和準確度。
3.2加樣
根據實驗設計在對應的孔加入對應DP溶液30μl,加樣時槍頭貼近孔的底部,但是不接觸到底部電極,加完后傾斜或拍打E-plate使液體在孔里的電極表面均勻覆蓋,然后立刻到EFIRM上進行電場操作。
3.3室溫孵育
蓋上E-plate蓋子,實驗臺上室溫孵育30min。
3.4E-plate板清洗
在洗板機程序上選擇對應的實驗列,清洗程序選擇(2bottom,2top),清洗液選擇洗液A。清洗完畢,立刻進行加樣操作。
4鏈霉親和素標記的辣根過氧化物酶(Poly-HRP)與生物素結合
4.1Poly-HRP溶液配制
從4℃冰箱取出稀釋液,取1個1.5mL離心管,加入999μl的稀釋液,加入1μl的酶液(含Poly-HRP,濃度為0.5mg/ml,購自thermo fisher,產品名稱為PierceTMStreptavidin Poly-HRP,貨號為21140,單位規格為0.5mL),渦旋震蕩混勻,離心,備用。
4.2加酶液
在對應的各孔加入上述稀釋液和酶液混合后的混合液30μl,Poly-HRP通過其標記的鏈霉親和素與檢測探針上的生物素識別并結合。
4.3室溫孵育
蓋上E-plate蓋子,實驗臺上室溫孵育30min。
4.4E-plate板清洗
在洗板機程序上選擇對應的實驗列,清洗程序選擇(3bottom,3top),清洗液選擇洗液B。清洗完畢,立刻進行TMB加樣操作。其中,洗液B為含0.1%(質量百分比)Tween20的PBS緩沖液。
5數據讀取
5.1加底物
在對應的各孔加入底物60μl,加樣時槍頭貼近孔的底部,但是不接觸到底部電極。加完立刻到EFIRM上進行電場操作。其中,底物為含TMB的溶液(購自thermo fisher,產品貨號為34028,名稱為1-StepTM Ultra TMB-ELISA)。加入酶的底物,發生氧化還原反應,產生電流,檢測各孔內電流值即完成整個檢測過程。以陰性對照孔重復4次的電流平均值+3倍標準差的和作為陽性判定值,陽性判定值=AVG+3×SD,其中AVG為陰性對照孔重復4次的電流平均值,SD為陰性對照孔重復4次的標準差。若加入有待測樣本的檢測孔的電流值大于或等于該陽性判定值,則判定位陽性結果,說明待測樣本中含有相應的HPV亞型病毒。
5.2 EFIRM電場讀數
在EFIRM軟件上選擇進行實驗的對應列,電場參數設置為:電壓A:-200mV,60s;電壓B:0mV,0s;進行1個循環。電場處理完畢,立刻取出,清洗E-plate板。
儀器將自動完成檢測工作,檢測數據自動上傳到云計算平臺。根據檢測數據繪制柱狀圖,橫坐標為檢測組的類別,縱坐標為各檢測組中各檢測孔的電流值(Current),單位為納安(-nA、負號表示方向)。本實施例的檢測結果如圖1所示。
由圖1可知,在16亞型組中,樣本1的檢測結果呈陽性,其含有HPV16亞型病毒(陰性對照電流值為28.67nA、其標準差為5.62,陽性對照電流值為130.22nA,樣本1的電流值為192.05nA,樣本2的電流值為30.53nA);在11種高危型組中,樣本2的檢測結果呈陽性(陰性對照電流值為24.94nA、其標準差為5.91,陽性對照電流值為132.94nA,樣本1的電流值為29.57nA,樣本2的電流值為151.30nA),說明其含有高危型HPV31、33、52、58、35、39、45、51、56、59、68亞型中的至少一種。
實施例2
本實施例提供的用于病毒基因分型檢測的試劑盒包括同探針組合(同實施例1)、固定物、鏈霉親和素標記的辣根過氧化物酶(以溶液形式存在)及其底物,固定物是導電聚合物和離子化合物,其中,導電聚合物是吡咯,離子化合物是氯化鉀。底物是含TMB的溶液。其余同實施例1。
在本實施例中,檢測組設置為1個,命名為18種亞型同時檢測組,檢測組包括一個陽性對照孔,一個陰性對照孔(重復4次),一個樣本1的檢測孔以及一個樣本2的檢測孔。每個孔中都加入實施例1所述的16種探針對,18種HPV亞型同時檢測)。其余同實施例1。如果有陽性檢出結果,則檢出的結果能說明待測樣本含有HPV16、18、31、33、52、58、35、39、45、51、56、59、68、26、53、66、73、82亞型中的至少一種(如圖2所示)。本實施例的檢測結果如圖2所示。
由圖2說明,樣本1的檢測結果呈陽性(陰性對照電流值為26.59nA、其標準差為7.91,陽性對照電流值為110.46nA,樣本1的電流值為189.66nA),說明其含有HPV16、18、31、33、52、58、35、39、45、51、56、59、68、26、53、66、73、82亞型中的至少一種;樣本2的檢測結果呈陽性(陰性對照電流值為26.59nA、其標準差為7.91,陽性對照電流值為110.46nA,樣本2的電流值為80.60nA),說明樣本2含有HPV16、18、31、33、52、58、35、39、45、51、56、59、68、26、53、66、73、82亞型中的至少一種。
實施例3
本實施例提供的用于病毒基因分型檢測的試劑盒包括同探針組合(同實施例1)、固定物、鏈霉親和素標記的辣根過氧化物酶(以溶液形式存在)及其底物、清洗液。
固定物是導電聚合物和離子化合物,其中,導電聚合物是吡咯,離子化合物是氯化鉀。底物是含TMB的溶液。清洗液包括包括洗液A和洗液B,洗液A是含SDS的SSC緩沖液,洗液B是含Tween20的PBS緩沖液。其余同實施例1。
在本實施例中,檢測組設置為16個組,分別是16亞型組、18亞型組、26亞型組、31亞型組、35亞型組、39亞型組、45亞型組、51亞型組、52亞型組、53亞型組、56亞型組、59亞型組、66亞型組、68亞型組、73亞型組以及82亞型組。每個檢測組設置一個陽性對照孔(每個檢測組分別加入表2中所示的對應的陽性寡核苷酸),一個陰性對照孔(重復4次),一個樣本1的檢測孔以及一個樣本2的檢測孔,每個檢測孔內加入其相應的探針對。其余同實施例1。如果各檢測組有陽性檢出結果,則檢出的結果則能夠說明待測樣本含有的相應的HPV亞型病毒。需要說明的是,由于,HPV 33、52和58亞型的探針對通用,因此52亞型組檢測出的陽性結果說明待測樣本中含有HPV33、52和58亞型中的一種或幾種。本實施例的檢測結果如圖3所示。
由圖3說明,在16亞型組中,樣本1的檢測結果呈陽性(陰性對照電流值為28.67nA、其標準差為5.62,陽性對照電流值為130.22nA,樣本1的電流值為192.05nA,樣本2的電流值為30.53nA),說明樣本1含有HPV 16亞型病毒;在52亞型組中,樣本2的檢測結果呈陽性(陰性對照電流值為25.58nA、其標準差為5.33,陽性對照電流值為75.70nA,樣本1的電流值為23.90nA,樣本2的電流值為166.10nA),另外,在66亞型組中,樣本2的檢測結果呈陽性(陰性對照電流值為25.92nA、其標準差為6.20,陽性對照電流值為115.75nA,樣本1的電流值為34.47nA,樣本2的電流值為72.72nA),說明樣本2含有HPV 33、52、58亞型中的一種和HPV 66亞型。本實施例通過設置18檢測組來檢測待測樣本的檢測結果能夠將其含有的具體病毒亞型檢測出,其檢測結果準確可靠。
實施例4
本實施例提供的用于病毒基因分型檢測的試劑盒包括同探針組合、檢測孔板、異硫氰酸熒光素抗體標記的辣根過氧化物酶(以溶液形式存在)及其底物(ABTS、以溶液形式存在)、清洗液。
其中,探針組合包括9個探針對,該9個探針對分別是:用于檢測HPV 16亞型的第1探針對、用于檢測HPV 18亞型的第2探針對、用于檢測HPV 31亞型的第3探針對、用于檢測HPV 33亞型或52亞型或58亞型的第4探針對、用于檢測HPV 51亞型的第8探針對、用于檢測HPV 56亞型的第9探針對、用于檢測HPV 26亞型的第12探針對、用于檢測HPV 53亞型的第13探針對、用于檢測HPV 73亞型的第15探針對。各檢測探針的3’端帶有異硫氰酸熒光素。各探針對相應的捕獲探針和檢測探針的堿基序列見實施例1中的表1。
檢測孔板的反應孔內固定有上述探針對的捕獲探針,捕獲探針固定至檢測孔板的的方法同實施例1中的“1捕獲探針固定”步驟,當然,在其他的實施例中,采用其他的方法將本發明的捕獲探針固定至檢測孔板上得到的檢測孔板也屬于本發明的保護范圍。
清洗液包括洗液A和洗液B,洗液A是含SDS的SSC緩沖液,洗液B是含Tween20的PBS緩沖液。其余同實施例1。
采用本實施例對樣本1和樣本2同時檢測,檢測步驟與實施例1基本一致,檢測結果如圖4所示。
由圖4可知,在16亞型組中,樣本1的檢測結果呈陽性(陰性對照電流值為25.22nA、其標準差為4.43,陽性對照電流值為108.10nA,樣本1的電流值為166.03nA),說明樣本1含有HPV16亞型病毒;在6種高危型組中,樣本2的檢測結果呈陽性(陰性對照電流值為24.25nA、其標準差為5.27,陽性對照電流值為115.92nA,樣本2的電流值為170.42nA),說明其含有高危型HPV31、33、51、52、58以及56亞型中的至少一種。
實施例5
本實施例提供的用于病毒基因分型檢測的試劑盒包括同探針組合、固定物、地高辛抗體標記的堿性磷酸酶酶(以溶液形式存在)及其底物(以含BCIP和NBT的組合物的溶液存在)、清洗液。
其中,探針組合包括4個探針對,該4個探針對分別是:用于檢測HPV 16亞型的第1探針對、用于檢測HPV 18亞型的第2探針對、用于檢測HPV 33亞型或52亞型或58亞型的第4探針對、用于檢測HPV 26亞型的第12探針對。各檢測探針的5’端帶有地高辛。各探針對相應的捕獲探針和檢測探針的堿基序列見實施例1中的表1。
固定物是導電聚合物和離子化合物,其中,導電聚合物是噻吩,當然,在其他的實施例中可以是苯胺。離子化合物是氯化鈉。清洗液包括包括洗液A和洗液B,洗液A是含SDS的SSC緩沖液,洗液B是含Tween20的PBS緩沖液。其余同實施例1。
采用本實施例對樣本1和樣本2同時檢測,檢測步驟與實施例1基本一致,檢測結果如圖5所示。
由圖5可知,在16亞型組中,樣本1的檢測結果呈陽性(陰性對照電流值為26.31nA、其標準差為5.29,陽性對照電流值為118.74nA,樣本1的電流值為185.47nA),說明樣本1含有HPV16亞型病毒;在3種高危型組中,樣本2的檢測結果呈陽性(陰性對照電流值為27.45nA、其標準差為5.15,陽性對照電流值為122.62nA,樣本2的電流值為150.07nA),說明樣本2含有高危型HPV33、51、52以及58亞型中的至少一種。
綜上,本發明提供的病毒基因分型檢測試劑盒具有以下優點:
1、檢測靈敏度高:傳統的探針固定方法是把探針的一端固定在平面支持物上,此方法由于支持物表面的疏水性等原因會降低探針與待測靶標DNA的雜交效率,本發明通過電荷吸附作用將捕獲探針固定在聚吡咯孔內,可保證捕獲探針具有超高活性;傳統的核酸雜交過程通過控制雜交溫度、鹽離子、反應時間等提高雜交效率,本發明增加電場作為第四個控制條件,在電場的作用下提高了捕獲探針對目的序列DNA的捕獲效率;本方法中通過測定HRP催化TMB氧化過程中產生的電子信號作為檢測結果,由于酶的催化效率很高,間接地放大了雜交反應的結果,增加了測定方法的敏感度。瞬間靶標分子捕獲、超高活性分子探針固定、捕獲分子信號特異放大這三大核心技術保證了本方法具有超高的靈敏性,遠高于巴氏涂片、TCT技術和HC2等技術,與聚合酶鏈反應和基因芯片等技術相當。
2、檢測特異性強:本發明中,每一個亞型HPV的檢測過程均包含一條捕獲探針和一條檢測探針,探針長度在25-40bp之間,雜交效率受錯配堿基的影響明顯,只有目標序列DNA與兩條探針同時準確配對后才能有檢測信號,大大提高了檢測的特異性。
3、操作簡便、反應快速:本發明中電場的引入,一方面省略了雜交過程中對樣品純度要求,使得臨床樣本不經過核酸提取即可直接進行檢測;另一方面降低了雜交過程中對反應時間的要求,加快了反應速率。整個檢測過程可以在半小時內完成,縮短了總體反應時間,減少門診病人的等待時間,為患者爭取寶貴的治療時間。
4、降低了對臨床客戶硬件及人員的要求:本發明中檢測過程中不需要對樣本進行純化和PCR擴增等前處理,有效避免因環境污染造成的假陽性,且試驗操作無需在專門的具有分區的PCR實驗室進行,操作人員亦不需要獲得臨床基因擴增的上崗許可,可以由一般技術人員操作,對實驗環境和操作人員的素質要求較低。
5、成本低:首先,在檢測設備方面,目前無論是ARMS-PCR還是數字PCR都采用熒光信號檢測,檢測設備需配備昂貴的熒光檢測系統,熒光定量PCR儀市場售價都在數十萬元左右,而數字PCR儀更達100多萬元。與之相比,EFIRM平臺采用獨創的電場引導的釋放與測量技術,檢測過程利用電場作用,反應快速,最終結果以電信號的形式檢測,因而設備的成本大幅降低,僅相當于熒光定量PCR儀的一半左右。
其次,在檢測試劑方面EFIRM技術基于核酸雜交的原理,采用獨特設計的電化學技術。本發明中使用的核酸探針長度在25-40bp之間,選擇于HPV亞型之間差異較大的E7區或L1區,均采用人工合成寡核苷酸探針,其中CP無需修飾,DP采用較常見的Biotin修飾方法,探針的制備委托商業化的DNA化學合成公司完成,技術難度低,穩定性較好,且部分亞型別共用CP或DP,減少了總探針數量,降低成本。以PCR為基礎的熒光定量需要對探針進行兩端修飾,且一端為熒光集團,合成成本較高;反向斑點雜交和基因芯片技術大都需要將雜交探針固定到固相載體上,處理工藝復雜,增加了檢測成本,且探針經過固定后活性有一定的降低;HC2使用的探針為全長的RNA探針,長度為7000-8000個堿基,制備工藝復雜,耗時多,成本很高,而且由于探針非常長,雜交效率受錯配堿基的影響小,可能出現亞型間的交叉。此外,在檢測過程中EFIRM技術節省了DNA提取與純化的步驟,因此檢測試劑成本與其它技術相比相比大幅降低。
總之,本方法提供的以EFIRM為基礎的HPV探針檢測方法具有靈敏度高、特異性強、檢測耗時短、實驗場地要求低、成本低等特點,適用于大量的臨床檢測和大規模的流行病學篩查。
以上所述僅為本發明的優選實施例而已,并不用于限制本發明,對于本領域的技術人員來說,本發明可以有各種更改和變化。凡在本發明的精神和原則之內,所作的任何修改、等同替換、改進等,均應包含在本發明的保護范圍之內。
- 還沒有人留言評論。精彩留言會獲得點贊!