一種含希夫堿配體的鉑綠光材料及其制備方法與流程
本發明涉及有機發光材料,具體涉及一種希夫堿鉑配合物的綠光發光材料及其制備方法。
背景技術:
OLEDs的研究始于20世紀60年代,1963年美國紐約大學的Pope教授第一次發現有機材料單晶蒽的電致發光現象。1987年美國Kodak公司的Tang采用超薄膜技術和新型器件結構制成了工作電壓低、發光亮度高的有機電致發光器件,使有機電致發光材料的研究產生根本性變革。隨后,在1990年,英國劍橋大學Cavendish實驗室的Burroughes教授和Friend教授等人以聚對苯乙烯(PPV)為發光材料,制成了聚合物電致發光器件,開辟了聚合物薄膜電致發光器件領域。1997年,美國普林斯頓大學的Forrest教授發現了電致磷光現象[4]。Forrest教授報道的電致磷光(Phosphorescent Organic Light-emitting Devices,PHOLEDs)技術突破了有機電致熒光材料量子效率低于25%的限制。根據量子力學自旋統計理論,形成單線態激子和三線態激子的概率分別為25%、75%。由于自旋禁阻作用,在通常情況下,三線態的磷光發射非常弱,難以測量。然而,在磷光材料中,配合物中由于重金屬原b(Ir,Pt,Os,Au,Cu)的引入,提高了自旋和軌道的耦合,縮短了磷光的壽命,使原有的三線態具有了某些單線態的特性,增強了系間竄越能力,導致禁阻的三線態向基態躍遷變為局部允許,從而使磷光得以順利發射。從原理上,磷光材料可以利用所有的電子和空穴復合能量發光,且器件的內量子效率可以達到100%,因此引起了廣泛關注。
近年來鉑配合物作為磷光發光材料吸引了光電科學家的研究興趣。如本課題組在《J.Mater.Chem.》報道了一系列Schiff堿鉑配合物,這些配合物具有體積較大的取代基(如叔丁基、三苯胺等),可以有效地降低鉑配合物分子之間的聚集或激態二聚體的形成,減慢器件效率隨電流的滑落(roll-off),從而極大地提高器件效率。然而,鉑配合物相比于銥配合物在PHOLEDs上的報道比較少,總體效率也要低很多,更需要進行深入研究。
技術實現要素:
1.本發明的目的是提供一種鉑配合物發光材料和應用。該材料能發射綠光,可作為發光材料應用在光電材料領域。本發明所制備的材料具有很好的熱穩定性和光電性質,所采用的制備方法操作簡單、反應條件溫和。
本發明提供一種鉑配合物發光材料,其結構式為:
2.本發明提供的鉑配合物發光材料包括以下合成步驟:
1)將苯胺和4-(二乙氨基)水楊醛通過縮合作用制備配體HL
2)將希夫堿配體HL和K2PtCl4反應合成鉑配合物PtL·DMSO
3.本發明提供的希夫堿鉑配合物發光材料,具有如下光物理性質:
1)單體分子式為:C19H20BrClF3NO2PtS,分子量為:693.87,PtL·DMSO為2,4,5-三氟苯胺縮5-叔丁基-3-溴水楊醛鉑配合物,屬于單斜晶系,空間群為P2(1)/n,晶胞參數為:α=γ=90.00°,β=95.451(4)°。
2)在三氯甲烷中的最大紫外吸收和熒光發射波長分別為442nm和606nm;
3)熱分解溫度為248℃;
4.以飽和Ag/Ag+電極為參比電極,測試了材料的氧化還原(CV)曲線,所得起始氧化電位為+0.57V,通過經驗公式[HOMO=-(Eox+4.71)]eV計算得到材料的最高占有軌道(HOMO)的能級為-5.28eV,通過公式[LUMO=HOMO+Eg]計算得到最低空軌道(LUMO)的能級為-2.67eV,其中能帶隙[Eg=1240/λmax],Ag/Ag+電極電勢為4.71V。
5.本發明發光材料可以在制備有機光電顯示器中應用。
6.本發明得到的希夫堿鉑配合物發光材料是一種綠光材料,該材料具有好的熱穩定性和電化學性質。該材料能夠作為光電材料在顯示器領域應用。所采用的制備方法反應操作簡單,條件溫和。
附圖說明
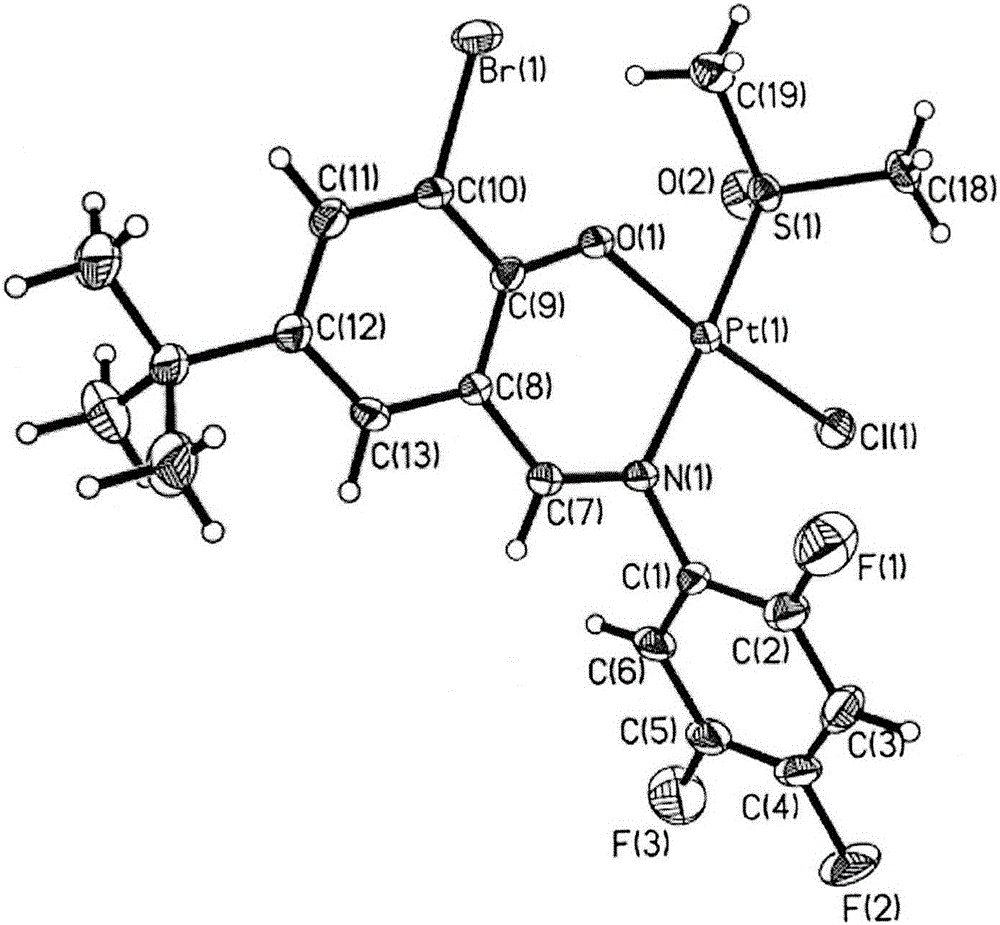
圖1晶體結構圖。
圖2為本發明PtL·DMSO的磷光發射圖。
圖3為本發明PtL·DMSO的紫外可見吸收圖。
圖4為本發明PtL·DMSO的熱重分析圖。
圖5為本發明PtL·DMSO的循環伏安圖。
具體實施方式
實施列1
1)取2,4,5-三氟苯胺(397mg,2.70mmol)和5-叔丁基-3-溴水楊醛(653mg,2.54mmol),置于50ml圓底燒瓶中,加入15ml的無水乙醇,磁力攪拌,在75攝氏度下回流6小時左右,在冷藏室中冷卻至有大量橙黃色固體析出,減壓抽濾。用95%乙醇洗滌2~3次,放在干燥箱中烘干。產品為橙黃色粉末,稱重0.735,產率為74.9%。1HMMR(CDCl3400MHZ)δ13.36(s,1H,OH),8.64(s,1H,HC=N),7.71(d,1H,J=4.0Hz,Ar-H),7.35(d,1H,J=4.0Hz,Ar-H),7.15-7.26(m,1H,Ar-H),7.05-7.11(m,1H,Ar-H),1.33(s,9H,-CH3).IR:3390,3076,2960,1629,1514,1454,1371,1267,1197,1155,881,773.C17H15BrF3NO(386.2063):calcd.C 52.87,H 3.91,N 3.63;found C 52.99,H 3.96,N 3.68.
2)取已經干燥好的席夫堿配體(252mg,0.65mmol)置于50ml圓底燒瓶,加入5mlDMF溶解,再加入干燥的氫氧化鈉(30mg,0.75mmol);同時稱取K2PtCl4(149mg,0.36mmol),并用3ml DMSO加熱溶解再加入反應燒瓶中。在無氧無水環境下反應24小時后,用薄層分析法發現原料基本消失,有新的物質生成,停止反應。待裝置完全冷卻后,在原燒瓶上搭建減壓蒸餾裝置,把溶劑DMF、DMSO蒸出,停止加熱,裝置冷卻后,加入30ml氯仿溶解瓶內固體,用分液漏斗洗滌5次左右,每次使用50ml去離子水洗滌。洗干凈后的下層有機溶劑用旋轉蒸干器蒸干。最后用層析柱分離雜質和產物,重結晶離心后烘干,得到紅色晶體產物40.7mg,產率11.9%,晶體結構見圖1。PtL5·DMSO:1HNMR(400MHz,CDCl3)δ8.10(s,1H,HC=N),7.94(d,J=2.4Hz,1H,Ar-H),7.29(s,1H,Ar-H),7.17-7.00(m,2H,Ph-H),3.49(s,6H,S-CH3),1.30(s,9H,CH3).IR:3446,2358,1606,1589,1519,1444,1300,1255,1155,1110,1026,869,742.C19H20BrClF3NO2PtS(693.8688):calcd.C 32.89,H 2.91,N 2.02;found C 32.78,H 2.94,N 2.06.
實施列2
通過bruker Smart Apex CCD單晶衍射儀對本實施例子的新型配合物進行結構分析。單體分子式為:C19H20BrClF3NO2PtS,分子量為:693.87,PtL5·DMSO為2,4,5-三氟苯胺縮5-叔丁基-3-溴水楊醛鉑配合物,屬于單斜晶系,空間群為P2(1)/n,晶胞參數為:α=γ=90.00°,β=95.451(4)°。
部分鍵長和鍵角(°)數據如下:
Pt(1)-N(1)2.031(4),Pt(1)-O(1)1.993(3),Pt(1)-S(1)2.2328(13),Pt(1)-Cl(1)2.2889(15);O(1)-Pt(1)-Cl(1)175.09(9),S(1)-Pt(1)-N(1)175.19(12),O(1)-Pt(1)-N(1)91.61(14),S(1)-Pt(1)-Cl(1)87.35(5)。
實施列3
準確稱取10mg希夫堿鉑配合物溶解在三氯甲烷中,制得1.0×10-5M溶液,準確移取3.0ml上述溶液加入比色皿中,然后在FLS980熒光儀上測定,激發狹縫和發射狹縫寬度都為10nm,激發波長為446nm。紫外吸收光譜的測定在Shimadzu UV-2450UV/Vis紫外可見吸儀器上測定。測試在室溫和外界大氣壓下進行。發射和吸收測試圖譜歸一化結果見圖2和圖3。從圖可知,最大紫外吸收波長為442nm,最大磷光發射波長為606nm.
實施列4
在氮氣保護下,采用TA Instruments SDTQ600儀器進行該材料的熱重分析(TGA)得到分解溫度為248℃,升溫速率都為10℃/分鐘。測量結果如圖4。
實施列5
準確稱取10mg希夫堿鉑配合物溶解在三氯甲烷中,制得1.0×10-4M溶液。準確取4.0ml溶液加入10.0ml燒杯中,在AUTOLAB三電極系統中測試該化合物的循環伏安曲線,參比電極為飽和甘汞電極,支持電解質為0.1mol/l的四丁基六氟磷酸銨,室溫下掃描速度為50mv/s.測量結果如圖5.
本發明中所描述的具體實施例僅是對本發明精神作舉例說明。本發明所屬技術領域的技術人員可以對所描述的具體實施例做各種各樣的修改或補充或采用類似的方式替代,但并不會偏離本發明的精神或者超越所附權利要求書所定義的范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!