含抗PD?1基因和聚亞精胺的復合物及其在治療腫瘤中的應用的制作方法
本發明涉及腫瘤治療的技術領域,特別涉及一種含抗PD-1基因和聚亞精胺的復合物及其在治療腫瘤中的應用,具體涉及一種將抗PD-1(programmed death-1)基因與聚亞精胺形成的納米復合物通過體外轉染到T細胞,制備自帶分泌抗PD-1抗體-T細胞,能產生PD-1抗體,從而幫助阻斷PD-1信號,可有效幫助衰竭T細胞,促進抗腫瘤免疫應答的T細胞治療腫瘤的方法。
背景技術:
T淋巴細胞靶向殺傷表達這一特異抗原的腫瘤細胞。因其具有靶向殺傷腫瘤細胞的特點,CTL療法已成為腫瘤個體化治療的理想方案,在國際上越來越受到免疫學家們的重視。但是由于PD-1的產生導致T細胞失去活性。為了解決這一難題我們提出了在體外直接將抗PD-1的基因導入體細胞,從而T細胞自身產生抗PD-1的抗體,來提高T細胞的活性,起到治療腫瘤的作用。
基因因其獨特的靶點特異性、結構可設計性和代謝安全性,成為科研界普遍看好的新的治療藥物。然而,在過去的20年里,研究人員設計了一系列的載體用于基因的體內輸送,但僅有極少數進入臨床階段,迄今,仍未有一個載體得到FDA認證,一個有效載體的缺位,導致核酸物質體內輸送仍然處于臨床瓶頸期。
將核酸物質輸送到靶細胞的胞漿或細胞核內,需要克服一系列的體內輸送屏障,因此,核酸載體是否高效,是其能否用于臨床治療的關鍵所在。核酸物質輸送的載體一般為以下兩類:(1)病毒載體:病毒載體(如慢病毒載體、腺病毒載體)作為基因的輸送載體,雖然有較高的體外轉染活性,然而,其免疫原性與易導致突變的缺點為臨床試驗帶來了巨大的安全問題,使得其應用受限。(2)非病毒載體:非病毒載體的優勢主要在于,在保證預期的轉染活性的條件下,可以大大降低病毒載體所帶來的免疫原性與諸多炎癥反應,其一般為以下兩種載體設計:(a)陽離子脂質體;(b)聚陽離子基因載體。而目前研究更多的主要集中于聚陽離子基因載體與陽離子脂質體的修飾,使之適用于基因物質的靶向輸送。陽離子脂質體具有較高的體內外轉染活性,然而,由于表面的正電荷影響其體內的正常分布,同時,由于選用陽離子脂質,免疫原性與炎癥反應在動物試驗中也成為不可避免的缺點之一(Gao,K.&Huang,L.Nonviral methods for siRNA delivery.Molecular pharmaceutics 6,651-658(2008).)。
技術實現要素:
針對現有技術中的缺陷,本發明的目的在于提供一種含抗PD-1基因和聚亞精胺的復合物及其在治療腫瘤中的用途。
本發明的目的是通過以下技術方案實現的:
第一方面,本發明提供了一種含抗PD-1基因和聚亞精胺的復合物,所述復合物包括質量比為1~100:1的聚亞精胺聚合物和抗PD-1基因。
優選地,所述聚亞精胺聚合物和抗PD-1基因的質量比為5~50:1。
優選地,所述聚亞精胺聚合物和抗PD-1基因的質量比為10~30:1。
優選地,所述聚亞精胺聚合物為亞精胺與連接劑形成的聚陽離子聚合物。
優選地,所述連接劑為戊二醛、對苯二甲醛、間苯二甲醛、鄰苯二甲醛、2,5-咪唑二甲醛、2,4-吡啶二甲醛、2,5-吡啶二甲醛、2,6-吡啶二甲醛、2,5-噠嗪二甲醛或2,6-噠嗪二甲醛中的一種。
第二方面,本發明提供了一種含抗PD-1基因和聚亞精胺的復合物的制備方法,包括以下步驟:
所述聚亞精胺聚合物的水溶液和抗PD-1基因的水溶液混合,在室溫靜置20-60分鐘即可制得所述復合物。
第三方面,本發明提供了一種含抗PD-1基因和聚亞精胺的復合物的在治療腫瘤中的應用。
第四方面,本發明提供了一種利用含抗PD-1基因和聚亞精胺的復合物治療腫瘤的方法,包括以下步驟:
將所述含抗PD-1基因和聚亞精胺的復合物與T細胞共培養,制備自帶分泌抗PD-1抗體-T細胞,再將自帶分泌抗PD-1抗體-T細胞注射到腫瘤病人體內即可。
與現有技術相比,本發明具有如下的有益效果:
1、本發明的分泌抗PD-1抗體-T細胞可有效治療腫瘤,可實現腫瘤的免疫治療,并且,不存在體內毒性的問題。
2、本發明制備的含抗PD-1基因和聚亞精胺的復合物轉染T細胞治療腫瘤的方法,可實現抗PD-1基因高效低毒的輸送,由于亞精胺是體內專職凝聚基因的功能,從而有效提高轉染效果。
附圖說明
通過閱讀參照以下附圖對非限制性實施例所作的詳細描述,本發明的其它特征、目的和優點將會變得更明顯:
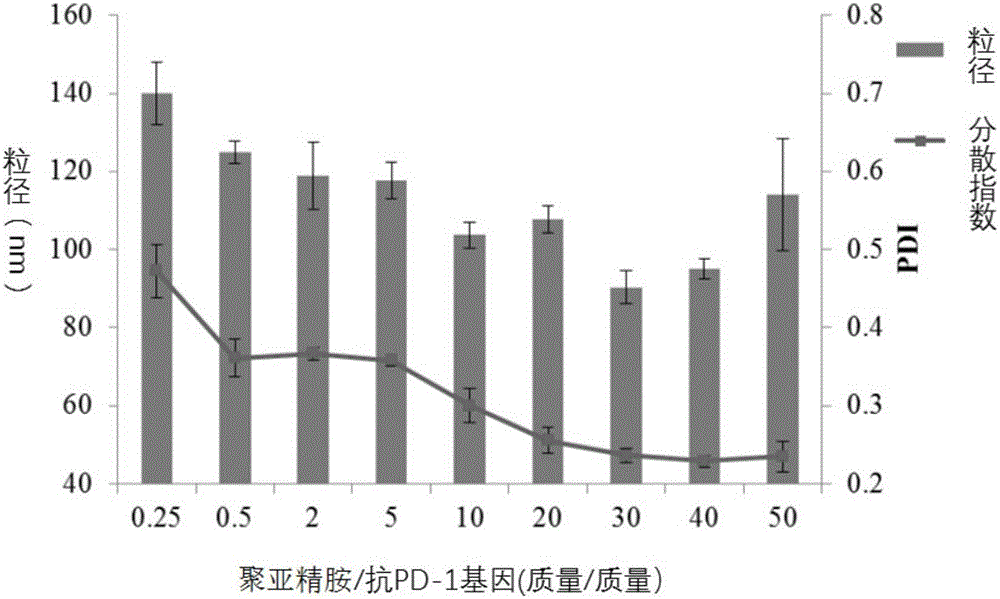
圖1為本發明的復合物的粒徑示意圖;
圖2為本發明的復合物的zeta電位示意圖;
圖3為本發明的復合物的透射電鏡示意圖;
圖4為本發明的復合物的凝膠電泳示意圖;
圖5為本發明的聚亞精胺聚合物的細胞毒性示意圖;
圖6為小鼠腫瘤模型及腫瘤組織切片的示意圖;其中,圖A-D為取下的腫瘤組織,A為生理鹽水組的腫瘤;B為裸DNA組的腫瘤;C為聚亞精胺聚合物(PSAi)組的腫瘤;D為本發明的納米復合物組的腫瘤。
具體實施方式
下面結合具體實施例對本發明進行詳細說明。以下實施例將有助于本領域的技術人員進一步理解本發明,但不以任何形式限制本發明。應當指出的是,對本領域的普通技術人員來說,在不脫離本發明構思的前提下,還可以做出若干變形和改進。這些都屬于本發明的保護范圍。
以下實施例提供了一種含抗PD-1基因和聚亞精胺的復合物,所述復合物包括質量比為1~100:1的聚亞精胺聚合物和抗PD-1基因。
所述聚亞精胺聚合物和抗PD-1基因的質量比為5~50:1。
所述聚亞精胺聚合物和抗PD-1基因的質量比為10~30:1。
所述聚亞精胺聚合物為亞精胺與連接劑形成的聚陽離子聚合物。
所述連接劑為戊二醛、對苯二甲醛、間苯二甲醛、鄰苯二甲醛、2,5-咪唑二甲醛、2,4-吡啶二甲醛、2,5-吡啶二甲醛、2,6-吡啶二甲醛、2,5-噠嗪二甲醛或2,6-噠嗪二甲醛中的一種。
所述含抗PD-1基因和聚亞精胺的復合物的制備方法,包括以下步驟:
所述聚亞精胺聚合物的水溶液和抗PD-1基因的水溶液混合,在室溫靜置20-60分鐘即可制得所述復合物。
所述含抗PD-1基因和聚亞精胺的復合物的在治療腫瘤中的應用。
所述利用含抗PD-1基因和聚亞精胺的復合物治療腫瘤的方法,包括以下步驟:
將所述含抗PD-1基因和聚亞精胺的復合物與T細胞共培養,制備自帶分泌抗PD-1抗體-T細胞,再將自帶分泌抗PD-1抗體-T細胞注射到腫瘤病人體內即可。
實施例1聚亞精胺聚合物(PSAi)和抗PD-1質粒DNA的形成復合物的制備
將聚亞精胺與連接劑2,6-吡啶二甲醛制備的聚亞精胺聚合物配成水溶液,濃度為2μg/μl,用滅菌水稀釋成20ng/μl、40ng/μl、100ng/μl、200ng/μl、1000ng/μl和2000ng/μl溶液。另外將抗PD-1基因質粒DNA配成水溶液,濃度為20ng/μl。將聚亞精胺聚合物水溶液等體積加入至質粒DNA水溶液,渦旋5min,并靜置20min,即得一系列納米復合物的溶液。
實施例2聚亞精胺聚合物(PSAi)和抗PD-1質粒DNA的形成復合物的粒徑與電位的表征
將實施例1制備的一系列復合物溶液放入BIC90plus粒度電位分析儀的測試槽中,該一系列復合物溶液的復合物中PSAi與質粒DNA的質量比0.25、0.5、2、5、10、50,設置測試溫度為25℃,介質為水,粘度為0.89cp,折射率為1.330,光散射角度為90。,檢測波長為659nm,每個樣品測試3次,每次運行時間為2min,記錄粒徑平均值。結果如圖1所示,結果顯示納米復合物的粒徑在200nm以下。其分散指數符合要求。
將實施例1制備的一系列復合物溶液放入BIC90plus粒度電位分析儀的測試槽中,該一系列復合物溶液的復合物中PSAi與質粒DNA的質量比0:1、10:1、20:1、30:1、40:1、50:1,設置測試溫度為25℃,介質為水,粘度為0.89cp,折射率為1.330,介電常數為78.54,pH值為7.0,zeta電位分析模型為Smoluchowski方程,每個樣品測試3次,每次自動運行10次,記錄zeta電位平均值。結果如圖2所示。從圖2的結果可知,其電勢符合要求。
實施例3聚亞精胺聚合物(PSAi)和抗PD-1質粒DNA的形成復合物的透射電鏡測試
按照實施例1的制備方法來配制PSAi/抗PD-1基因質粒DNA質量比為1:l的復合物納米復合物溶液,樣品量為100μL。吸取10μl,滴加在400目的銅網上,自然晾干,最后使用透射電子顯微鏡來觀察樣品的形態,記錄透射電鏡圖。結果如圖3所示,結果顯示納米復合物的粒徑在200nm以下。
實施例4聚亞精胺聚合物(PSAi)和抗PD-1質粒DNA的形成復合物的凝膠電泳測試
稱取1.0g瓊脂糖,加入100ml 1×TAE緩沖液,在微波爐中加熱溶解,待溫度降至65℃,加入溴化乙啶(EB),配制成1.0%瓊脂糖溶液(含0.5μg/ml溴化乙啶),倒入制膠槽中,插入樣品梳,室溫放置0.5-1小時等膠凝固。然后,拔出樣品梳,電泳槽中加入TAE緩沖液沒過凝膠,等待上樣。接著,按照實施例1的制備方法來配制聚亞精胺聚合物與基因物質不同質量比的納米復合物水溶液,PSA與基因物質的質量比依次為0、0.2、0.5、1、5、10、15、20、30、50。Marker選用DSTM5000(100–5000bp),上樣2μl;6×上樣緩沖液(溴酚蘭-甘油指示劑,含0.25%溴酚蘭,40%甘油)1μl與納米復合物水5μl均勻混合,上樣6μl。在110mV電壓下電泳45分鐘,最后,置于紫外凝膠成像系統觀察并記錄電泳圖,結果如圖4所示。從電泳圖可以看出,含有抗PD-1基因的質粒DNA在質量比為1時,復合物在電場的泳動已經被完全阻滯住了。從圖片可以觀察到,隨著質量比的增加,復合物的泳動都被阻滯了。該試驗表明PSAi具有較好的凝聚質粒DNA形成復合物的能力,有效的保護了質粒DNA。
實施例5聚亞精胺聚合物(PSAi)的T細胞毒性檢測
采用MTT法測定細胞毒性,選用T細胞考察細胞毒性,以8000個/孔的細胞密度轉96孔細胞板,置于37℃5%細胞培養箱里培養過夜。配制1、2、4、8、15mg/mL的一系列不同濃度的聚亞精胺聚合物(由實施例1的方法制備)溶液,每孔加入100μL,稀釋介質是DMEM高糖培養基(無血清無酚紅),從培養箱中取出96孔細胞板,吸去培養液,每孔用100μL磷酸鹽緩沖溶液沖洗一次,再棄去磷酸鹽緩沖溶液,將不同濃度的聚亞精胺聚合物溶液依次加入到細胞板中,平行測定3個孔。置于細胞培養箱里培養4小時。然后,吸去培養液,每孔用100μL磷酸鹽緩沖溶液沖洗一次,再棄去磷酸鹽緩沖溶液,每孔加入100μL DMEM高糖培養基(無血清無酚紅)和25μL MTT溶液(5mg/mL),繼續于培養箱里培養。6小時之后,吸去培養液,每孔加入100μL二甲基亞砜,放置充分溶甲瓚,采用多功能酶標儀測定樣品在570nm和630nm處的吸光度值(以630nm處為對照)。結果顯示聚亞精胺聚合物(PSAi)的毒性較低,而高分子的PEI(分子量25000)的毒性明顯高于PSAi。
實施例6本發明的抗PD-1基因與聚亞精胺聚合物形成復合物轉染T細胞治療腫瘤的效果試驗
BALB/c雌性裸鼠(5周齡,體重20±2g),SPF級環境下飼養1周,取SMMC7721生長最佳狀態的傳代細胞,按細胞數4×106個/ml細胞液,0.1ml接種于BALB/c小鼠后肢近背部皮下。繼續飼養2周,使用游標卡尺測量并觀察腫瘤的生長狀況,按照如下公式來計算腫瘤的體積:腫瘤體積(mm3)=(長×寬×寬)/2。當腫瘤體積達到150-200mm3的時候(做腫瘤模型動物實驗),分為A為生理鹽水組的腫瘤,B為裸DNA組的腫瘤,C為亞聚精胺聚合物(PSAi)組的腫瘤,D為本發明的納米復合物組的腫瘤。其中,生理鹽水組注射生理鹽水,裸DNA組注射裸DNA,聚精胺聚合物(PSA)組注射PSA,本發明的納米復合物組注射的是:經本發明實施例1制備的納米復合物(PAS與抗PD-1質粒DNA的質量比為1:40)轉染后的T細胞,該轉染后的T細胞為含自帶分泌抗PD-1抗體-T細胞。
三周后處死小鼠,取腫瘤組織,檢測結果如圖6所示,其中,A-D為取下的腫瘤組織,A為生理鹽水組的腫瘤,B為裸DNA組的腫瘤,C為聚亞精胺聚合物(PSAi)組的腫瘤,D為本發明的納米復合物組的腫瘤。實驗結果顯示:本發明的組治療的效果很好。
本發明具體應用途徑很多,以上所述僅是本發明的優選實施方式。應當指出,以上實施例僅用于說明本發明,而并不用于限制本發明的保護范圍。對于本技術領域的普通技術人員來說,在不脫離本發明原理的前提下,還可以做出若干改進,這些改進也應視為本發明的保護范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!
- 小麥白粉病抗性基因PmR2及其克隆與應用的制造方法與工藝
- 一種受茉莉酸甲酯和白葉枯病菌誘導的啟動子、其制備方法和重組表達載體與流程
- MALDI?TOFMS技術鑒定臨床感染豬腸球菌的方法與流程
- 一種稻瘟病抗性基因Pi2的功能性分子標記及其應用的制造方法與工藝
- 一種與白葉枯病抗性基因Xa7緊密連鎖的SNP分子標記及其應用的制造方法與工藝
- 一種與白葉枯病抗性基因Xa7緊密連鎖的SNP分子標記及其應用的制造方法與工藝
- 一種水稻穗瘟抗性基因的分子標記方法與制造工藝
- OsSAPK9蛋白及其編碼基因在提高水稻白葉枯病抗性中的應用的制造方法與工藝
- 一種硫鏈絲菌素?慶大霉素抗性基因體系及還有其的抗性表達盒和重組質粒的制造方法與工藝
- 含抗PD?1基因和聚亞精胺的復合物及其在治療腫瘤中的應用的制造方法與工藝