一種二芳基乙烯類可光致變色殺蟲化合物及其制備方法和用途與流程
本發明屬于農藥領域。具體地,本發明涉及一種含新煙堿殺蟲劑單元的二芳基乙烯類可光致變色化合物及其制備方法和用途。
技術背景
以吡蟲啉為代表的新煙堿類殺蟲劑因殺蟲活性高,殺蟲譜廣,對哺乳動物和水生動物毒性低,且有良好的系統物性及適當的田間穩定性和環境友好性,成為新農藥創制的重要熱點領域。后來又相繼開發出噻蟲啉、噻蟲胺、噻蟲嗪、啶蟲脒、烯啶蟲胺、呋蟲胺等一系列煙堿類殺蟲劑。
但是由于吡蟲啉過量頻繁使用造成較為嚴重的抗性問題以及由于結構相似性帶來的新煙堿殺蟲劑之間的交互抗性,在一定程度上限制了該類化合物的應用,制約了此類化合物發展,同時新煙堿類殺蟲劑主要對同翅目和鞘翅目害蟲高效,其相對較窄的殺蟲譜也限制了蟲害防治方面的用藥選擇性。
因此,如何對具有高活性的硝基亞甲基化合物進行結構改造,以產生新的、更有效的殺蟲劑,解決新煙堿類殺蟲劑的抗性問題,擴大殺蟲譜,使其應用于殺蟲劑組合物就成為本領域迫切需要解決的技術問題。
技術實現要素:
本發明的目的在于提供一類高效防治害蟲的化合物(如式(A)化合物和式(B)化合物)及其制備方法和用途。
本發明第一方面提供了一種具有式(A)所示結構的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽:
式中:
R1和R2各自獨立地為含氮、氧和/或硫的五元或六元雜環基,或鹵代的含氮、氧和/或硫的五元或六元雜環基,取代或未取代的苯基;
R3,R4各自獨立地為H、C1-4烷基、烯丙基、芐基、C1-4烷氧基-C1-4烷基、C1-4烷基-羰基、C1-4烷氧基-羰基或苯氧羰基;或者R3和R4和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-;
R5,R6各自獨立地為H、C1-4烷基、烯丙基、芐基、C1-4烷氧基-C1-4烷基、C1-4烷基-羰基、C1-4烷氧基-羰基或苯氧羰基;或者R5和R6和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-;
R7為氫、C1-4烷基、鹵素、取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;
R8、R9、R10、R11、R12和R13各自獨立地為氫、鹵素、C1-4烷基、取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;或R8、R9和R10、R11的結合構成取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;或R12、R13和R10、R11的結合構成取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;
R14為C1-4烷基或C1-4烷氧基;
X為硝基、氰基、三氟甲基、三氟乙酰基或三氟甲磺酰基;
Y為N或CH;
Z為S、O或NH;
其中,所述取代是指被選自下組中的一個或多個取代基所取代:鹵素、C1-4烷基或鹵代C1-4烷基、C1-4烷氧基或鹵代C1-4烷氧基、C2-6烯基、C2-6炔基、鹵代的C2-6烯基、鹵代的C2-6炔基、C1-4烷氧基-C1-4烷基、C1-4烷氧基-羰基、C2-6炔基-羰基、C2-6烯基-羰基。
在另一優選例中,R1和R2各自獨立地為吡啶基、噻唑基、嘧啶基、四氫呋喃基、噁唑基,或其鹵代物。
在另一優選例中,R1和R2各自獨立地為鹵代的吡啶基、鹵代的噻唑基、鹵代的嘧啶基、鹵代的四氫呋喃基、或鹵代的噁唑基。
在另一優選例中,所述鹵代物為氯代物。
在另一優選例中,R1和R2各自獨立地為
在另一優選例中,R3,R4各自獨立地為H或C1-3烷基;或者R3和R4和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-;和/或R5,R6各自獨立地為H或C1-3烷基;或者R5和R6和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-。
在另一優選例中,R3,R4各自獨立地為氫、甲基或乙基;或者R3和R4和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-。
在另一優選例中,R5,R6各自獨立地為氫、甲基或乙基;或者R5和R6和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-。
在另一優選例中,R7為氫、C1-3烷基或鹵素。
在另一優選例中,R7為氫。
在另一優選例中,R8、R9、R10、R11、R12和R13各自獨立地為氫、氟、C1-4烷基。
在另一優選例中,R8、R9、R10、R11、R12和R13各自獨立地為氫或氟。
在另一優選例中,R14為C1-2烷基或C1-2烷氧基。
在另一優選例中,R14為甲基。
在另一優選例中,X為硝基或氰基。
在另一優選例中,X為硝基。
在另一優選例中,Y為N或CH。
在另一優選例中,Y為N。
在另一優選例中,Z為S、O或NH。
在另一優選例中,Z為S。
本發明第二方面提供了一種殺蟲劑組合物,其包含:
(a)0.001-99.99重量%的本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽;
(b)農藥學上可接受的載體和/或賦形劑。
在另一優選例中,組分(a)占所述殺蟲劑組合物的0.01-99.9重量%,優選0.05-90重量%。
在另一優選例中,所述殺蟲劑組合物用于殺滅或預防選自如下的害蟲:鞘翅目、鱗翅目、半翅目、直翅目、等翅目、或雙翅目昆蟲。
在另一優選例中,所述害蟲為等翅目或鱗翅目昆蟲。
在另一優選例中,所述害蟲具有刺吸式或銼吸式口器。
在另一優選例中,所述害蟲為蚜蟲、孑孓、飛虱、粉虱、葉蟬、薊馬、棉鈴蟲、菜青蟲、小菜蛾、斜紋夜蛾、粘蟲。
在另一優選例中,所述殺蟲劑還包含其它活性物質,所述其它活性物質選自:殺蟲劑、餌劑、殺菌劑、殺螨劑、殺線蟲劑、殺真菌劑或生長控制劑。
本發明第三方面提供了一種殺蟲和/或防蟲方法,所述方法包括步驟:將本發明第二方面所述的殺蟲劑組合物或本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽施加于遭受或可能遭受蟲害的植物體、其周圍的土壤或環境中。
本發明第四方面提供了一種殺蟲和/或防蟲方法,所述方法包括步驟:將本發明第二方面所述的殺蟲劑組合物或本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽施加于遭受或可能遭受蟲害的植物體、其周圍的土壤或環境中,并用波長為310-380nm的光照射該植物體、其周圍的土壤或環境。
本發明第五方面提供了一種提高殺蟲活性的方法,包括步驟:在使用本發明第二方面所述的殺蟲劑組合物或本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽時,用波長為310-380nm的光照射所述的殺蟲劑組合物或所述的化合物或其光學異構體或順反異構體。
本發明第六方面提供了一種本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽在制備殺蟲劑組合物中的用途。
本發明第七方面提供了一種本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽在殺蟲和/或防蟲中的用途。
本發明第八方面提供了一種本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽的制備方法,
(A)所述方法包括步驟:在惰性溶劑中,將式(1g)化合物與式01化合物和式02化合物進行反應,從而形成式(A)化合物;
或(B)所述方法包括步驟:在惰性溶劑中,將式(2f)化合物與式01化合物和式02化合物進行反應,從而形成式(A)化合物;
各式中,R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12、R13、R14、X、Y、Z定義同前。
本發明第九方面提供了一種具有式(B)所示結構的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽:
式中:
R1和R2各自獨立地為含氮、氧和/或硫的五元或六元雜環基,或鹵代的含氮、氧和/或硫的五元或六元雜環基,取代或未取代的苯基;
R3,R4各自獨立地為H、C1-4烷基、烯丙基、芐基、C1-4烷氧基-C1-4烷基、C1-4烷基-羰基、C1-4烷氧基-羰基或苯氧羰基;或者R3和R4和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-;
R5,R6各自獨立地為H、C1-4烷基、烯丙基、芐基、C1-4烷氧基-C1-4烷基、C1-4烷基-羰基、C1-4烷氧基-羰基或苯氧羰基;或者R5和R6和它們相連的原子共同構成-CH2-CH2-或-CH2-CH2-CH2-;
R7為氫、C1-4烷基、鹵素、取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;
R8、R9、R10、R11、R12和R13各自獨立地為氫、鹵素、C1-4烷基、取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;或R8、R9和R10、R11的結合構成取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;或R12、R13和R10、R11的結合構成取代或未取代的5-6元芳環基、或取代或未取代的5-6元芳雜環基;
R14為C1-4烷基或C1-4烷氧基;
X為硝基、氰基、三氟甲基、三氟乙酰基或三氟甲磺酰基;
Y為N或CH;
Z為S、O或NH;
其中,所述取代是指被選自下組中的一個或多個取代基所取代:鹵素、C1-4烷基或鹵代C1-4烷基、C1-4烷氧基或鹵代C1-4烷氧基、C2-6烯基、C2-6炔基、鹵代的C2-6烯基、鹵代的C2-6炔基、C1-4烷氧基-C1-4烷基、C1-4烷氧基-羰基、C2-6炔基-羰基、C2-6烯基-羰基。
本發明第十方面提供了一種本發明第九方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽的用途,用于高通量篩選殺蟲劑。
本發明第十一方面提供了一種高通量篩選殺蟲劑的方法,所述方法包括步驟:
(a)提供一含有已知濃度的本發明第十方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽和已知濃度的煙堿乙酰膽堿受體的溶液;
(b)在步驟(a)的溶液中加入梯度濃度的煙堿乙酰膽堿受體的競爭性配體;
(c)根據熒光偏振技術測定所述競爭性配體的IC50,從而篩選出有活性或活性高的配體。
在另一優選例中,所述煙堿乙酰膽堿受體的濃度高于所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽的濃度和煙堿乙酰膽堿受體的競爭性配體的濃度。
在另一優選例中,所述化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽的濃度通過熒光偏振結合實驗確定。
本發明第十二方面還提供了一種將本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽和本發明第十方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽互相轉換的方法,包括步驟:
將本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽在光1照射下發生光致異構反應,從而形成本發明第十方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽,其中,所述光1為波長為310-380nm的光;
將本發明第十方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽在光2照射下發生光致異構反應,從而形成本發明第一方面所述的化合物或其光學異構體或順反異構體,或其農藥學上可接受的鹽,其中,所述光2為波長為420-780nm的光;
各式中,R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12、R13、R14、X、Y、Z定義同前。
應理解,在本發明范圍內中,本發明的上述各技術特征和在下文(如實施例)中具體描述的各技術特征之間都可以互相組合,從而構成新的或優選的技術方案。限于篇幅,在此不再一一累述。
附圖說明
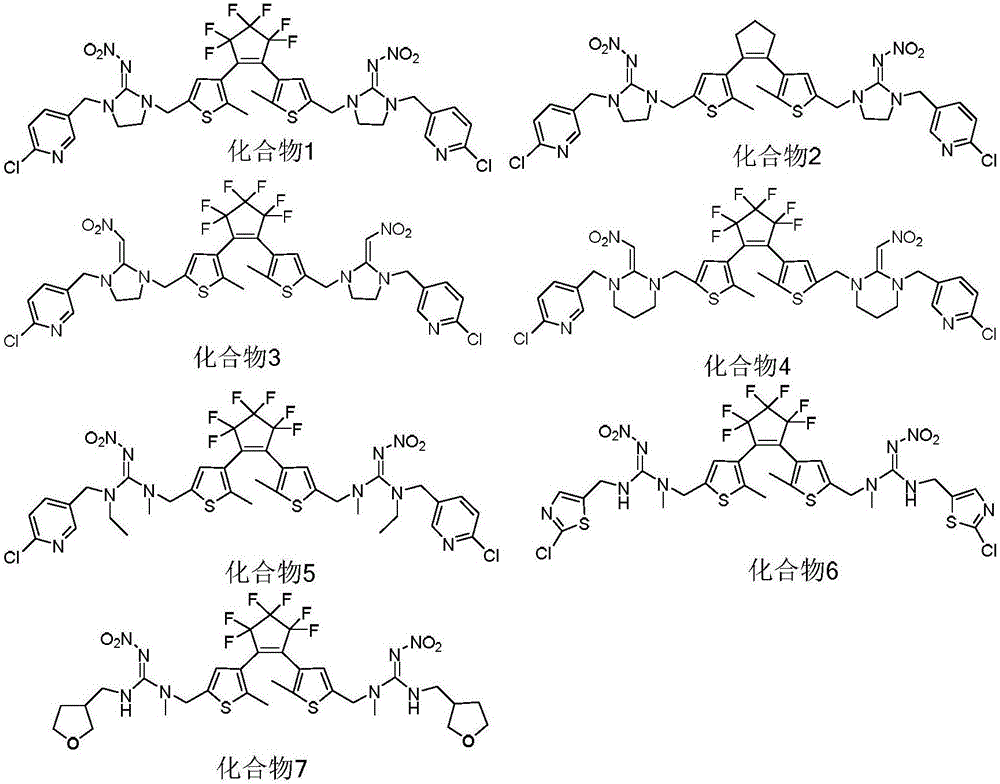
圖1為本發明的光致變色二芳基乙烯化合物的分子式。
圖2為化合物1在乙腈溶液中紫外光照射前后的吸收光譜圖。
圖3為化合物1在特定波長處的抗疲勞性。
圖4顯示了關環化合物1與乙酰膽堿受體結合的最優濃度。
具體實施方式
本發明人通過長期而深入的研究,基于現有的新煙堿殺蟲劑的結構和二芳基乙烯光控開關的結構,將二芳基乙烯片段引入已經商品化的新煙堿類的殺蟲劑,合成了一類含新煙堿殺蟲劑單元的光致變色二芳基乙烯類化合物,該化合物光照關環產物殺蟲活性高,并具有熒光。在此基礎上,發明人完成了本發明。
基團定義
如本文所用,術語“C1-4烷基”指具有1-4個碳原子的直鏈或支鏈烷基,例如甲基、乙基、丙基、異丙基、丁基、異丁基、仲丁基、叔丁基、或類似基團。
術語“C1-4烷氧基”指具有1-4個碳原子的直鏈或支鏈烷氧基,例如甲氧基、乙氧基、丙氧基、異丙氧基、丁氧基、異丁氧基、仲丁氧基、叔丁氧基、或類似基團。
術語“鹵素”指氟、氯、溴、或碘。術語“鹵代的”指被相同或不同的一個或多個上述鹵原子取代的基團,例如三氟甲基、五氟乙基、或類似基團。
術語“五元或六元雜環基”指含一個或多個選自氮、氧或硫的雜原子的五元或六元環,例如吡啶基、噻唑基、嘧啶基、四氫呋喃基、或噁唑基等。
術語“5-6元芳環基”是指5元或6元的芳香基,例如苯基等。
術語“5-6元芳雜環基”是指5元或6元的帶有雜原子(如氮、氧、硫)的芳香基,例如吡啶基等
術語“雜環”指形成所述雜環骨架的原子中至少一個原子不是碳,為氮、氧或硫。通常,雜環包含不超過4個氮、不超過2個氧和/或不超過2個硫。除非另外指明,雜環可以是飽和的、部分不飽和的或完全不飽和的環。
術語“烷基”是指烷烴分子中少掉一個氫原子而成的基團;術語“亞烷基”是指烷烴分子中少掉兩個氫原子而成的基團。類似地,“亞烯基”、“亞炔基”、“亞環烷基”、“亞環烯基”、“亞苯基”、“亞萘基”、“亞雜環基”或“亞雜芳二環或三環環系”的定義類似。
術語“光致變色”是指一個化合物(A),在收到一定波長的光照射時,可進行特定的化學反應或物理效應,獲得產物(B),由于結構的改變導致其(可見部分的)吸收光譜發生明顯的變化。而在另一波長的光照射或熱的作用下,產物(B)又能恢復到原來的形式。
術語“關環產物”是指二芳基乙烯類化合物經特定波長紫外光照射后,發生分子內周環反應關環后得到的化合物。
術語“熒光偏振”是指當熒光分子受平面偏振光激發時,如果分子在受激發時期(對于熒光素約持續4納秒)保持靜止,發射光將位于同樣的偏振平面。如果在受激發時期,分子旋轉或翻轉偏離這一平面,發射光將位于與激發光不同的偏振面。如果用垂直的偏振光激發熒光素,可以在垂直的和水平的偏振平面檢測發射光光強(發射光從垂直平面偏向水平平面的程度與熒光素標記的分子的遷移率有關)。如果分子很大,激發時發生的運動極小,發射光偏振程度較高。如果分子小,分子旋轉或翻轉速度快,發射光相對于激發光平面將去偏振化。
術語“抗疲勞性”是指基于化合物經歷光致變色的呈色和消色之間循環次數的評價指標。
術語“高通量篩選”是指技術是指以分子水平和細胞水平的實驗方法為基礎,以微板形式作為實驗工具載體,以自動化操作系統執行試驗過程,以靈敏快速的檢測儀器采集實驗結果數據,以計算機分析處理實驗數據,在同一時間檢測數以千萬的樣品,并以得到的相應數據庫支持運轉的技術體系,它具有微量、快速、靈敏和準確等特點。
術語“惰性溶劑”指的是不與原料發生反應的各種溶劑,包括各種直鏈、支鏈或環狀的醇,醚或酮,鹵代烷,1,4-二氧六環,乙腈,四氫呋喃,N,N-二甲基甲酰胺(DMF),二甲基亞砜(DMSO)等。
本文所用的“組合物”指任何混合物。可以是溶液、混合液、液體、粉末、油膏、水性的、非水性的或他們的任何組合。
這里使用的任何保護性基團,氨基酸和其他化合物的縮寫,與他們通用的、公認的縮寫或IUPAC-IUB委員會頒布的生化命名一致,除非特別說明。
術語“熒光”,又作"螢光",是指一種光致發光的冷發光現象。當某種常溫物質經某種波長的入射光(通常是紫外線或X射線)照射,吸收光能后進入激發態,并且立即退激發并發出比入射光的的波長長的出射光(通常波長在可見光波段);而且一旦停止入射光,發光現象也隨之立即消失。具有這種性質的出射光就被稱之為熒光。
本發明的化合物可以含有一個或多個不對稱中心,并因此以消旋體、外消旋混合物、單一對映體、非對映異構體化合物和單一非對映體的形式出現。可以存在的不對稱中心,取決于分子上各種取代基的性質。每個這種不對稱中心將獨立地產生兩個旋光異構體,并且所有可能的旋光異構體和非對映體混合物和純或部分純的化合物包括在本發明的范圍之內。本發明包括化合物的所有異構形式。
本發明化合物的制備方法
本發明通式(A)所示化合物可通過如下的方法制得,然而該方法的條件,例如反應物、溶劑、酸堿、所用化合物的量、反應溫度、反應所需時間等并不限于下面的解釋。本發明化合物還可以任選地通過將在本說明書中描述的或本領域已知的各種合成方法組合起來而方便的制得,這樣的組合可由本發明所屬領域的技術人員容易地進行。
本發明通式(A)所示化合物可通過如下的方法(A)合成,所述方法包括步驟:
(1)在惰性溶劑中,將式(1a)化合物與溴化試劑(如溴)進行反應,從而形成式(1b)化合物;
(2)在惰性溶劑中,將式(1b)化合物與乙二醇進行反應(如在對甲基苯磺酸存在下),從而形成式(1c)化合物;
(3)在惰性溶劑中,將式(1c)化合物與進行反應,從而形成式(1d)化合物:
(4)在惰性溶劑中,將式(1d)化合物進行脫保護反應(如在對甲苯磺酸存在下),從而形成式(1e)化合物;
(5)在惰性溶劑中,將式(1e)化合物進行還原反應(如在硼氫化鈉存在下),從而形成式(1f)化合物:
(6)在惰性溶劑中,將式(1f)化合物與氯化試劑(如氯化亞砜)進行反應,從而形成式(1g)化合物:
(7)在惰性溶劑中,將式(1g)化合物與式01化合物和式02化合物進行反應,從而形成式(A)化合物;
本發明通式(A)所示化合物可通過如下的方法(B)合成,所述方法包括步驟:
(1)在惰性溶劑中,將式(2a)化合物與取代的戊二酰氯進行傅克酰化反應(如在三氯化鋁存在下),從而形成式(2b)化合物;
(2)在惰性溶劑中,將式(2b)化合物進行關環反應(如在鋅和四氯化鈦存在下),從而形成式(2c)化合物;
(3)在惰性溶劑中,將式(2c)化合物與二甲基甲酰胺進行反應,從而形成式(2d)化合物;
(4)在惰性溶劑中,將式(2d)化合物進行還原反應(如在硼氫化鈉存在下),從而形成式(2e)化合物;
(5)在惰性溶劑中,將式(2e)化合物與氯化試劑(如氯化亞砜)進行反應,從而形成式(2f)化合物;
(6)在惰性溶劑中,將式(2f)化合物與式01化合物和式02化合物進行反應,從而形成式(A)化合物;
各式中,R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12、R13、R14、X、Y、Z定義同前。
本發明活性物質的殺蟲活性
術語“本發明的活性物質”或“本發明的活性化合物”是指本發明化合物、其光學異構體、順反異構體或農藥學上可接受的鹽,其具有顯著提高的殺蟲活性,以及擴大的殺蟲譜。
術語“農藥學上可接受的鹽”意指該鹽的陰離子在形成殺蟲劑藥學上可接受的鹽時為已了解的和可接受的。該鹽較好的為水溶性的。合適的、由式(A)化合物形成的酸加成鹽包括有無機酸形成的鹽,例如鹽酸鹽、磷酸鹽、硫酸鹽、硝酸鹽;及包括有機酸形成的鹽,如醋酸鹽,苯甲酸鹽。
本發明的活性物質能用作控制和消滅廣泛的農林植物害蟲、貯藏谷類的害蟲、公共衛生害蟲以及危害動物健康的害蟲等。在本說明書中,“殺蟲劑”是具有防治上述提到的所有害蟲的作用的物質的統稱。害蟲的例子包括但不限于:鞘翅目昆蟲:玉米象(Sitophilus zeamais),赤擬谷盜(Tribolium castaneum),馬鈴薯瓢蟲(Henosepilachna vigintioctomaculata),二十八星瓢蟲(Henosepilachna sparsa),細胸叩頭蟲(Agriotes fuscicollis),紅腳綠金龜(Anomala cupripes),四紋麗金龜(Popillia quadriguttata),馬鈴薯葉甲(Monolepta hieroglyphica),松天牛(Monochamus alternatus),稻根象(Echinocnemus squameus),泡桐葉甲(Basiprionota bisignata),星天牛(Anoplophora chinensis),桑天牛(Apripona germari),臍腹小蠹(Scolytus schevy),或細胸金針蟲(Agriotes fuscicollis)。鱗翅目昆蟲:舞毒娥(Lymantria dispar),天幕毛蟲(Malacosoma neustria testacea),黃楊絹野螟(Diaphania perspectalis),大袋蛾(Clania variegata),黃刺蛾(Cnidocampa flauescens),馬尾松毛蟲(Dendrolimus punctatus),古毒蛾(Orgyia gonostigma),白楊透翅蛾(Paranthrene tabaniformis),斜紋夜蛾(Spodoptera litura),二化螟(Chilo suppressalis),玉米螟(Ostrinia nubilalis),粉斑螟(Ephestia cautella),棉卷蛾(Adoxophyes orana),栗子小卷蛾(laspyresia splendana),小地老虎(Agrotis fucosa),大蠟螟(Galleria mellonella),菜蛾(Plutella xylostella),桔潛蛾(Phyllocnistis citrella),或東方粘蟲(Mythimna separata)。同翅目昆蟲:黑尾葉蟬(Nephotettix cincticeps),稻褐飛虱(Nilaparvata lugens),康氏粉蚧(Pseudococcus comstocki),矢尖蚧(Unaspis yanonensis),桃蚜(Myzus persicae),棉蚜(Aphis gossydii),蘿卜蚜(Lipaphis erysimi pseudobrassicae),梨班網蝽(Stephanitis nashi),或粉虱(Bemisia tabaci)。直翅目昆蟲:德國小蠊(Blattella germanica),美國大蠊(Periplaneta american),非洲螻蛄(Gryllotalpa africana),或亞洲飛蝗(Locus migratoria)。等翅目昆蟲:入侵紅火蟻(Solenopsis invicta),或家白蟻(Coptotermes formosanus)。雙翅目昆蟲:家蠅(Musca domestica),埃及伊蚊(Aedes aegypti),種蠅(Delia platura),庫蚊(Culex sp.),或中華按蚊(Anopheles sinensis)。
本發明涉及的化合物尤其對刺吸式、銼吸式口器害蟲如:蚜蟲、葉蟬、飛虱、薊馬、粉虱等農林害蟲有特效以及對衛生害蟲蚊子幼蟲有特效。
含本發明活性物質的殺蟲劑組合物
可將本發明的活性物質以常規的方法制備成殺蟲劑組合物。這些活性化合物可做成常規的制劑,例如溶液劑,乳劑,混懸劑,粉劑,泡沫劑,糊劑,顆粒劑;氣霧劑,用活性物質浸漬的天然的和合成的材料,在多聚物中的微膠囊,用于種子的包衣復方,和與燃燒裝置—塊使用的制劑,例如煙熏藥筒,煙熏罐和煙熏盤,以及ULV冷霧(Cold mist)和熱霧(Warm mist)制劑。
這些制劑可用已知的方法生產,例如,將活性化合物與擴充劑混合,這些擴充劑就是液體的或液化氣的或固體的稀釋劑或載體,并可任意選用表面活性劑即乳化劑和/或分散劑和/或泡沫形成劑。例如在用水作擴充劑時,有機溶劑也可用作助劑。
用液體溶劑作稀釋劑或載體時基本上是合適的,如:芳香烴類,例如二甲苯,甲苯或烷基萘;氯化的芳香或氯化的脂肪烴類,例如氯苯,氯乙烯或二氯甲烷;脂肪烴類,例如環己烷或石蠟,例如礦物油餾分;醇類,例如乙醇或乙二醇以及它們的醚和脂類;酮類,例如丙酮,甲乙酮,甲基異丁基酮或環已酮;或不常用的極性溶劑,例如二甲基甲酰胺和二甲基亞砜,以及水。液化氣的稀釋劑或載體是指在常溫常壓下將成為氣體的液體,例如氣溶膠推進劑,如鹵化的烴類以及丁烷,丙烷,氮氣和二氧化碳。
固體載體可用研磨的天然的礦物質,例如高嶺土,粘土,滑石,石英,活性白土,蒙脫土,或硅藻土,和研磨合成的礦物質,例如高度分散的硅酸,氧化鋁和硅酸鹽。供顆粒用的固體載體是碾碎的和分級的天然告石,例如方解石,大理石,浮石,海泡石和白云石,以及無機和有機粗粉合成的顆粒,和有機材料例如鋸木屑,椰子殼,玉米棒子和煙草梗的顆粒等。
非離子的和陰離子的乳化列可用作乳化劑和/或泡沫形成劑。例如聚氧乙烯-脂肪酸酯類,聚氧乙烯-脂肪醇醚類,例如烷芳基聚乙二醇醚類,烷基磺酸酯類,烷基硫酸酯類,芳基磺酸酯類以及白蛋白水解產物。分散劑包括,例如木質素亞硫酸鹽廢液和甲基纖維素。
在制劑中可以用粘合劑,例如羧甲基纖維素和以粉末,顆粒或乳液形式的天然和合成的多聚物,例如阿拉伯膠,聚乙烯基醇和聚乙烯醋酸酯。可以用著色劑例如無機染料,如氧化鐵,氧化鉆和普魯士藍;有機染料,如有機染料,如偶氯染料或金屬鈦菁染料;和用痕量營養劑,如鐵,猛,硼,銅,鈷,鋁和鋅的鹽等。
本發明的這些活性化合物可與其它活性化合物制成混合物存在于商品制劑中或從這些制劑制備的使用劑型中,所述其它的活性化合物包括但不限于:殺蟲劑,合餌,殺菌劑,殺螨劑,殺線,殺真菌劑,生長控制劑等。殺蟲劑包括,例如磷酸酯類,氨基甲酸酯類,除蟲菊酯類,氯化烴類,苯甲酰脲類,沙蠶毒素類以及由微生物產生的物質,如阿維菌素。
此外,本發明的這些活性化合物也可與增效劑制成一種混合物存在于它們的商品制劑中成從這些制劑制備的使用劑型中。增效劑是提高活性化合物作用的化合物,由于活性化合物本身有活性,也可不必加增效劑。
這些制劑通常含有占所述殺蟲劑組合物0.001-99.99重量%,優選0.01-99.9重量%,更優選0.05-90重量%的本發明的活性化合物。從商品制劑制成使用劑型中的活性化合物的濃度可在廣闊的范圍內變動。使用劑型中的活性化合物的濃度可從0.0000001-100%(g/v),最好在0.0001與1%之間。
本發明的優點主要包括:
發明人創新地將二芳基乙烯片段引入已經商品化的新煙堿類的殺蟲劑中,合成了一類含新煙堿殺蟲劑單元的光致變色二芳基乙烯類化合物,全面探索了這類化合物的兩種異構體在光物理學方面和殺蟲活性方面的差異,實現了通過光來調控殺蟲劑性能的目的。
本發明提供的一類含新煙堿殺蟲劑單元的光致變色二芳基乙烯類化合物,光致變色明顯,熱穩定性好,抗疲勞性好,關環產物殺蟲活性高,可用作殺蟲劑,防治農業害蟲;同時關環產物具有熒光,可利用熒光偏振技術進行藥物的高通量篩選。
下面結合具體實施例,進一步闡述本發明。應理解,這些實施例僅用于說明本發明而不用于限制本發明的范圍。下列實施例中未注明具體條件的實驗方法,通常按照常規條件,或按照制造廠商所建議的條件。除非另外說明,否則百分比和份數按重量計算。其中,r.t.或rt代表室溫。
實施例1化合物1的合成
1.1制備4-溴-5-甲基-2-噻吩甲醛
在100mL圓底燒瓶中加入5-甲基-2-噻吩甲醛(6.3g,50.0mmol)和50mL乙酸,然后用恒壓滴液漏斗稱取Br2(8.78g,55.0mmol)溶于適量乙酸,室溫下慢慢滴加溴的乙酸溶液,室溫攪拌24h,TLC跟蹤反應結束后,加入水停止反應。反應混合物用無水碳酸鈉中和至中性。產物用乙醚萃取三次,有機相用無水硫酸鈉干燥,過濾,減壓除去溶劑得黑色液體,柱層析,用石油醚:乙酸乙酯=40:3(v:v)洗脫。蒸干溶劑得到白色固體3.1g,產率為30.1%。1H NMR(400MHz,CDCl3)δ9.78(s,1H),7.26(s,1H),2.49(s,3H)。13C NMR(101MHz,CDCl3)δ181.60,145.84,140.12,138.73,111.24,15.93。
1.2制備4-溴-5-甲基-2-(1,3-二氧戊環)噻吩
在100mL圓底燒瓶中加入4-溴-5-甲基-2-噻吩甲醛(2.0g,9.75mmol)、乙二醇(1.23g,19.51mmol)和對甲苯磺酸(0.15g,97.53mmol),加入60mL苯溶解,裝上分水器,攪拌回流反應4h,TLC跟蹤反應結束后,將反應液溫度降至室溫,用3.0mol/L的氫氧化鈉溶液洗三次,再用水洗滌三次,有機相用無水硫酸鈉干燥,過濾,減壓除去溶劑得黃色液體,柱層析,用石油醚:乙酸乙酯=20:1(v:v)洗脫。蒸干溶劑得到白色油狀物2.4g,產率為90.8%。1H NMR(400MHz,CDCl3)δ6.96(s,1H),6.00(s,1H),4.18-3.88(m,4H),2.38(s,3H)。13C NMR(101MHz,CDCl3)δ138.70,135.35,128.79,108.45,99.69,65.19,14.86。
1.3制備1,2-二[2-甲基-5-(1,3-二氧戊環)-3-噻吩基]八氟環戊烯
在氮氣及-78℃條件下,在50mL低溫反應瓶中加入4-溴-5-甲基-2-(1,3-二氧戊環)噻吩(2.4g,9.63mmol),加入30mL無水四氫呋喃,攪拌,慢慢用注射器加入2.5mol/L n-BuLi/正己烷(7.7mL,19.27mmol),繼續低溫攪拌反應40min,用預先冷卻的注射器慢慢加入八氟環戊烯(1.23g,5.78mmol),繼續低溫攪拌反應2h,TLC跟蹤反應結束后,將反應液自然升至室溫,用濃度為2M的鹽酸(15mL)淬滅反應,分液,水層用無水乙醚萃取三次,合并有機層,然后用水洗滌三次,有機層用無水硫酸鈉干燥,過濾,減壓除去溶劑得油狀液體2.0g,此粗產物不需要進一步的分離,直接投入下一步脫保護反應。
1.4制備1,2-二(2-甲基-5-甲酰基-3-噻吩基)八氟環戊烯
在250mL圓底燒瓶中加入粗產物1,2-二[2-甲基-5-(1,3-二氧戊環)-3-噻吩基]八氟環戊烯(2.0g,3.90mmol)和對甲苯磺酸(0.4g,2.22mmol),加入混合溶劑水(30mL)和丙酮(80mL)溶解,然后向混合物中加入2.0mL吡啶,攪拌回流反應24h。TLC跟蹤反應結束后,將反應液溫度降至室溫,反應液分別飽和碳酸氫鈉溶液和水洗滌,分液,水層用二氯甲烷萃取,合并有機相,用無水硫酸鈉干燥,過濾,減壓除去溶劑得黃色液體,柱層析,用石油醚:乙酸乙酯=1:5(v:v)洗脫。蒸干溶劑得到藍色固體0.15g,產率為8.7%。1H NMR(400MHz,CDCl3)δ9.86(s,2H),7.74(s,2H),2.03(s,6H)。19F NMR(376MHz,CDCl3)δ-110.30(t,J=5.1Hz,4F),-130.57--133.99(m,2F)。
1.5制備1,2-二(2-甲基-5-羥甲基-3-噻吩基)八氟環戊烯
在氮氣及冰浴條件下,在50mL圓底燒瓶中加入1,2-二(2-甲基-5-甲酰基-3-噻吩基)八氟環戊烯(0.45g,1.06mmol),加入35mL甲醇溶解,然后分批加入硼氫化鈉(0.16g,4.24mmol)。繼續冰浴下攪拌反應1h,TLC跟蹤反應結束后,加入適量的水淬滅反應,然后反應混合物用乙醚(30mL×2)萃取,合并有機相,有機相用飽和氯化鈉溶液洗滌三次,無水硫酸鈉干燥,過濾,減壓除去溶劑得黃色固體,柱層析,用石油醚:乙酸乙酯=1:1(v:v)洗脫。蒸干溶劑得到白色固體0.45g,產率為99%。1H NMR(400MHz,CDCl3)δ6.95(s,2H),4.76(s,4H),1.88(s,8H)。19F NMR(376MHz,CDCl3)δ-110.10(t,J=10.9Hz,4F),-131.48--134.27(m,2F)。
1.6制備1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯
在氮氣及冰浴條件下,在100mL圓底燒瓶中加入1,2-二(2-甲基-5-羥甲基-3-噻吩基)八氟環戊烯(0.25g,0.58mmol)和無水吡啶(1.0mL),加入40mL無水四氫呋喃溶解,攪拌。將氯化亞砜(0.28g,2.33mmol)稱在恒壓滴液漏斗里,慢慢滴加到反應體系中,繼續冰浴攪拌反應2h。TLC跟蹤反應結束后,將反應液慢慢倒入40mL冰水混合物中,攪拌。然后反應混合物用乙醚(30mL×2)萃取,合并的有機相用30mL飽和碳酸氫鈉洗滌,無水硫酸鈉干燥,過濾,減壓除去溶劑得淡黃色固體0.35g,產率為92%。產物不進行純化立即投入下一步反應中。
1.7制備化合物1
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入吡蟲啉(0.40g,1.55mmol)和碳酸銫(0.72g,2.19mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯,繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.35g,產率為60%。m.p.108.7-110.9℃。1H NMR(400MHz,DMSO-d6)δ8.35(d,J=2.0Hz,2H),7.78(dd,J=8.3,2.4Hz,2H),7.55(d,J=8.2Hz,2H),7.10(s,2H),4.53(d,J=28.1Hz,4H),4.46(s,4H),3.77-3.47(m,8H),1.83(d,J=13.4Hz,6H).13C NMR(101MHz,DMSO-d6)δ160.19,149.72,149.53,149.38,142.96,139.42,135.74,130.39,127.34,123.28,46.52,45.57,45.02,44.15,13.90。19F NMR(376MHz,DMSO-d6)δ-109.35(t,J=10.9Hz,4F),-131.11(m,4F)。HRMS(ESI-TOF):m/z C35H3035Cl2F6N10O4S2Na[M+Na]+計算值:925.1072,實測值:925.1080;m/z C35H3035Cl37ClF6N10O4S2Na[M+Na]+計算值:927.1042,實測值:927.1025;m/z C35H3037Cl2F6N10O4S2Na[M+Na]+計算值:929.1013,實測值:929.1030.
實施例2化合物2的合成
2.1制備1,5-二(5-氯-2-甲基噻吩-3-基)戊烷-1,5-二酮
在50mL圓底燒瓶中依次加入無水三氯化鋁(12.1g,90.49mmol)以及硝基甲烷150mL,冰浴條件下,先滴加戊二酰氯(6.37,37.71mmol)的硝基甲烷溶液,再滴加2-氯-5-甲基噻吩(10g,75.41mmol)的硝基甲烷溶液。加完后,繼續反應0.5h,然后撤去冰浴,室溫條件下繼續攪拌反應6h,TLC跟蹤反應結束后,小心慢慢加入60mL冰水混合物,繼續攪拌5min,分液分出有機相,水層用無水乙醚(50mL×2)萃取,合并有機相,用飽和碳酸氫鈉溶液調至中性,然后用水洗滌,飽和氯化鈉溶液洗滌,無水硫酸鎂干燥過夜,旋蒸除去大量溶劑,將得到的粘稠黑色粗產品用石油醚和乙酸乙酯過硅膠柱(7:3,v/v),蒸干溶劑得到16g淡黃色固體粉末,產率為59%。1H NMR(400MHz,CDCl3)δ7.19(s,2H),2.93-2.78(t,J=18Hz,4H),2.66(s,6H),2.06(m,2H)。13C NMR(101MHz,CDCl3):δ194.7,147.6,134.7,126.7,125.2,40.4,18.1,16.0。
2.2制備1,2-二(5-氯-2-甲基噻吩-3-基)環戊烯
在氮氣保護條件下,在250mL三口燒瓶中加入100mL無水四氫呋喃和鋅粉(7.24g,110.71mmol),冰浴,劇烈攪拌條件下,緩慢滴加四氯化鈦溶液(16.80g,88.57mmol),滴加完畢后繼續冰浴攪拌5min,轉移到油浴,升溫至80℃,加熱回流1小時,反應液顏色逐漸由黃綠色變成深黑色。自然冷卻至室溫,用針筒注入40mL含1,5-二(5-氯-2-甲基噻吩-3-基)戊烷-1,5-二酮(16g,44.29mmol)的無水四氫呋喃溶液,繼續加熱回流4小時,停止加熱,冷卻后將反應液倒入10%的碳酸鉀水溶液中,析出大量固體,抽濾,濾餅用無水乙醚反復洗滌,用乙醚(50mL×2)萃取水層,合并有機相,無水硫酸鈉干燥過夜,過濾,旋蒸除掉溶劑,粗品用石油醚為洗脫劑,過硅膠柱,蒸干溶劑后得到無色油狀液體3.3g,低溫靜置成無色蠟狀固體,產率為30%。1H NMR(400MHz,CDCl3)δ6.57(s,2H),2.71(t,J=7.5Hz,4H),2.07-1.96(m,2H),1.88(s,6H)。13C NMR(101MHz,CDCl3)δ134.82,134.41,133.28,126.67,125.18,38.32,22.81,14.16。
2.3制備1,2-二(5-甲酰基-2-甲基噻吩-3-基)環戊烯
在氮氣及-78℃條件下,在50mL低溫反應瓶中加入1,2-二(5-氯-2-甲基噻吩-3-基)環戊烯(1.50g,4.56mmol),加入10mL無水四氫呋喃,攪拌,慢慢用注射器加入2.5mol/L n-BuLi/正己烷(5.5mL),繼續低溫攪拌反應60min,然后用預先冷卻的注射器慢慢加入DMF(2.29mL),繼續低溫攪拌反應1h,TLC跟蹤反應結束后,將反應液自然升至室溫,用濃度為2M的鹽酸(15mL)淬滅反應,分液,水層用無水乙醚(20mL×2)萃取,合并有機層,然后用水洗滌三次,有機層用無水硫酸鈉干燥,過濾,減壓除去溶劑,將得到的粗產品用石油醚和乙酸乙酯過硅膠柱(5:1,v/v),蒸干溶劑得到1.5g藍色固體粉末,產率為46%。1H NMR(400MHz,CDCl3)δ9.74(s,2H),7.43(s,2H),2.84(t,J=7.5Hz,4H),2.17-2.07(m,2H),2.05(s,6H)。13C NMR(101MHz,CDCl3)δ182.38,146.38,140.23,137.42,137.07,134.98,38.41,22.89,15.38。
2.4制備1,2-二(5-羥甲基-2-甲基噻吩-3-基)環戊烯
在氮氣及冰浴條件下,在50mL圓底燒瓶中加入1,2-二(5-甲酰基-2-甲基噻吩-3-基)環戊烯(0.87g,2.75mmol),加入35mL甲醇溶解,然后分批加入硼氫化鈉(0.42g,11.0mmol)。繼續冰浴下攪拌反應1h,TLC跟蹤反應結束后,加入適量的水淬滅反應,然后反應混合物用乙醚(30mL×2)萃取,合并有機相,有機相用飽和氯化鈉溶液洗滌三次,無水硫酸鈉干燥,過濾,減壓除去溶劑得黃色固體,柱層析,用石油醚:乙酸乙酯=6:1(v:v)洗脫。蒸干溶劑得到白色固體0.86g,產率為98%。1H NMR(400MHz,CDCl3)δ6.61(s,2H),4.61(s,4H),2.75(t,J=7.4Hz,4H),2.32(s,2H),2.06-1.98(m,2H),1.95(s,6H)。13C NMR(101MHz,CDCl3)δ139.35,135.33,134.93,134.56,126.91,59.91,38.25,22.98,14.36。
2.5制備1,2-二(5-氯甲基-2-甲基噻吩-3-基)環戊烯
在氮氣及冰浴條件下,在100mL圓底燒瓶中加入1,2-二(5-羥甲基-2-甲基噻吩-3-基)環戊烯(0.86g,2.86mmol)和無水吡啶(1.0mL),加入40mL無水四氫呋喃溶解,攪拌。將氯化亞砜(1.28g,10.73mmol)稱在恒壓滴液漏斗里,慢慢滴加到反應體系中,繼續冰浴攪拌反應2h。TLC跟蹤反應結束后,將反應液慢慢倒入40mL冰水混合物中,攪拌。然后反應混合物用乙醚(30mL×2)萃取,合并的有機相用30mL飽和碳酸氫鈉洗滌,無水硫酸鈉干燥,過濾,減壓除去溶劑得棕色固體。產物不進行純化立即投入下一步反應中。
2.6制備化合物2
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入吡蟲啉(1.37g,5.37mmol)和碳酸銫(2.48g,7.61mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(5-氯甲基-2-甲基噻吩-3-基)環戊烯(0.80g,2.24mmol),繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.61g,產率為34%。m.p.193.4-196.5℃。1H NMR(400MHz,DMSO-d6)δ8.34(d,J=2.0Hz,2H),7.77(dd,J=8.2,2.3Hz,2H),7.55(d,J=8.2Hz,2H),6.73(s,2H),4.45(s,8H),3.68-3.60(m,4H),3.60-3.52(m,4H),2.72(t,J=7.4Hz,4H),1.98(m,2H),1.86(s,6H)。13C NMR(101MHz,DMSO-d6)δ160.16,149.71,149.37,139.42,134.92,134.74,134.10,132.27,130.40,128.99,124.26,46.51,45.50,44.76,44.22,37.68,22.35,13.82。HRMS(ESI-TOF):m/z C35H3635Cl2N10O4S2Na[M+Na]+計算值:817.1637,實測值:817.1635;m/z C35H3635Cl37ClN10O4S2Na[M+Na]+計算值:819.1608,實測值:819.1606;m/z C35H3637Cl2N10O4S2Na[M+Na]+計算值:821.1578,實測值:821.1581。
實施例3化合物3的合成
目標化合物的合成與實施例1的步驟1.1-1.6相同,不同之處在最后一步。
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入(E)-1-((6-氯吡啶-3-基)甲基)-2-(硝基亞甲基)咪唑烷(0.40g,1.55mmol)和碳酸銫(0.77g,2.19mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯,繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.40g,產率為65%。m.p.101.7-103.9℃.1H NMR(400MHz,DMSO-d6)δ8.36(d,J=2.0Hz,2H),7.72(dd,J=8.3,2.4Hz,2H),7.53(d,J=8.2Hz,2H),7.11(s,2H),4.53(d,J=28.1Hz,4H),4.40(s,4H),4.20(s,2H),3.67-3.47(m,8H),1.80(d,J=13.4Hz,6H)。13C NMR(101MHz,DMSO-d6)δ161.19,142.72,142.53,144.38,145.96,138.42,137.74,131.39,126.34,122.28,45.52,45.57,43.02,41.15,12.90。19F NMR(376MHz,DMSO-d6)δ-108.35(t,J=11.9Hz,4F),-130.11(m,4F).HRMS(ESI-TOF):m/z C37H3235Cl2F6N8O4S2Na[M+Na]+計算值:923.1269,實測值:923.1272;m/z C37H3235Cl37ClF6N8O4S2Na[M+Na]+計算值:925.1253,實測值:925.1264;m/z C37H3237Cl2F6N8O4S2Na[M+Na]+計算值:927.1246,實測值:927.1260。
實施例4化合物4的合成
目標化合物的合成與實施例1的步驟1.1-1.6相同,不同之處在最后一步。
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入(E)-1-((6-氯吡啶-3-基)甲基)-2-(硝基亞甲基)六氫嘧啶(0.50g,1.55mmol)和碳酸銫(0.91g,2.19mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯,繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.80g,產率為46%。m.p.110.7-112.9℃.1H NMR(400MHz,DMSO-d6)δ8.31(d,J=2.0Hz,2H),7.72(dd,J=8.3,2.4Hz,2H),7.51(d,J=8.2Hz,2H),7.11(s,2H),4.52(d,J=28.1Hz,4H),4.42(s,4H),4.22(s,4H),3.77-3.47(m,8H),1.85(d,J=13.4Hz,6H)。13C NMR(101MHz,DMSO-d6)δ159.19,143.72,140.53,141.38,140.96,137.42,133.74,129.39,127.34,120.28,45.52,44.57,43.03,40.32,15.55。19F NMR(376MHz,DMSO-d6)δ-112.45(t,J=10.9Hz,4F),-135.11(m,4F).HRMS(ESI-TOF):m/z C39H3635Cl2F6N8O4S2Na[M+Na]+計算值:951.1582,實測值:951.1562;m/z C39H3635Cl37ClF6N8O4S2Na[M+Na]+計算值:953.1437,實測值:953.1440;m/z C39H3637Cl2F6N8O4S2Na[M+Na]+計算值:955.1256,實測值:955.1235。
實施例5化合物5的合成
目標化合物的合成與實施例1的步驟1.1-1.6相同,不同之處在最后一步。
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入烯啶蟲胺(0.50g,1.55mmol)和碳酸銫(0.90g,2.19mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯,繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.60g,產率為35%。m.p.120.7-121.5℃.1H NMR(400MHz,DMSO-d6)δ8.20(d,J=2.0Hz,2H),7.56(dd,J=8.3,2.4Hz,2H),7.46(d,J=8.2Hz,2H),7.03(s,2H),4.45(d,J=28.1Hz,4H),4.37(s,4H),3.5(q,4H),3.27-2.90(m,8H),2.80(t,6H),2.60(s,6H),1.78(d,J=13.4Hz,6H)。13C NMR(101MHz,DMSO-d6)δ169.35,159.21,143.98,142.36,142.78,138.78,137.25,136.20,125.23,116.36,49.37,46.36,45.27,42.28,19.01。19F NMR(376MHz,DMSO-d6)δ-120.36(t,J=10.9Hz,4F),-140.19(m,4F).HRMS(ESI-TOF):m/z C37H3835Cl2F6N10O4S2Na[M+Na]+計算值:957.1803,實測值:957.1805;m/z C37H3835Cl37ClF6N10O4S2Na[M+Na]+計算值:959.1489,實測值:959.1428;m/z C37H3837Cl2F6N10O4S2Na[M+Na]+計算值:961.8954,實測值:961.8937。
實施例6化合物6的合成
目標化合物的合成與實施例1的步驟1.1-1.6相同,不同之處在最后一步。
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入噻蟲胺(0.50g,1.55mmol)和碳酸銫(0.97g,2.19mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯,繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.60g,產率為34%。m.p.123.1-124.5℃.1H NMR(400MHz,DMSO-d6)δ8.35(d,J=2.0Hz,2H),8.25(d,J=1.5Hz,2H),8.10(s,2H),3.77-3.47(m,8H),2.30(s,6H)2.25(d,J=12.4Hz,6H),1.87(d,J=13.4Hz,6H)。13C NMR(101MHz,DMSO-d6)δ158.11,143.31,141.34,140.38,140.29,139.22,137.25,134.23,129.35,128.28,42.68,41.91,40.37,40.41,17.49。19F NMR(376MHz,DMSO-d6)δ-124.17(t,J=10.9Hz,4F),-135.17(m,4F).HRMS(ESI-TOF):m/z C29H2635Cl2F6N10O4S2Na[M+Na]+計算值:903.0301,實測值:903.0311;m/z C29H2635Cl37ClF6N10O4S2Na[M+Na]+計算值:905.1239,實測值:905.1254;m/z C29H2637Cl2F6N10O4S2Na[M+Na]+計算值:907.8375,實測值:907.8371。
實施例7化合物7的合成
目標化合物的合成與實施例1的步驟1.1-1.6相同,不同之處在最后一步。
在氮氣及50℃油浴條件下,在50mL圓底燒瓶中加入噻蟲胺(0.50g,1.55mmol)和碳酸銫(1.20g,2.19mmol),加入30mL二甲基甲酰胺溶解,50℃恒溫攪拌反應半個小時。然后慢慢加入用5mL二甲基甲酰胺溶解的1,2-二(2-甲基-5-氯甲基-3-噻吩基)八氟環戊烯,繼續恒溫反應4h。TLC跟蹤反應結束后,過濾除去沉淀物,減壓除去溶劑得棕紅色固體,柱層析,用二氯甲烷:甲醇=20:1(v:v)洗脫,蒸干溶劑得到白色固體0.80g,產率為42%。m.p.99.7-100.1℃.1H NMR(400MHz,DMSO-d6)δ8.29(d,J=2.0Hz,2H),8.24(d,J=1.5Hz,2H),3.56-3.43(m,8H),3.52-3.41(m,4H),3.31-3.23(m,4H),3.12-3.01(m,4H),2.29(s,6H)2,12(d,J=12.4Hz,6H),1.90(m,2H),1.79(d,J=13.4Hz,6H)。13C NMR(101MHz,DMSO-d6)δ149.12,143.31,141.34,140.31,140.23,139.89,137.48,134.29,129.93,128.19,43.68,41.91,38.37,39.41,11.39。19F NMR(376MHz,DMSO-d6)δ-119.35(t,J=10.9Hz,4F),-141.12(m,4F).HRMS(ESI-TOF):m/z C31H38F6N8O6S2Na[M+Na]+計算值:819.2268,實測值:819.2245。
圖1顯示了上述光致變色二芳基乙烯化合物的分子式。
實施例8本發明化合物的殺蟲活性測試
(1)對蚜蟲的殺蟲活性
蚜蟲俗稱膩蟲或蜜蟲等,屬于同翅目害蟲,是一種常見的農作物害蟲。蚜蟲主要分布在北半球溫帶地區和亞熱帶地區,熱帶地區分布很少。蚜蟲為刺吸式口器的害蟲,常群集于葉片、嫩莖、花蕾、頂芽等部位,刺吸汁液,使葉片皺縮、卷曲、畸形,嚴重時引起枝葉枯萎甚至整株死亡。蚜蟲分泌的蜜露還會誘發煤污病、病毒病并招來螞蟻危害等。蚜蟲繁殖和適應力強,各種防治方法都很難取得根治的效果。對于蚜蟲防治,重要的是抓緊防治,避免蚜蟲大量發生。以豆蚜(Aphis craccivora)為測試對象,采用浸漬法測試。
操作過程:選取健壯的豆蚜無翅成蟲(蟲體呈黑綠色,有光澤,腹部飽滿。各足褪節、脛節、跗節均暗黑色,其余部分黃白色)若干。避光,在黑暗條件下饑餓處理0.5-1h。選取長勢良好,高約3cm的蠶豆豆苗,洗去沙土(注意盡量保持豆皮完整),掐去豆根,插入帶水海綿上,使豆苗保持水分供給的充足。將經過饑餓處理的豆蚜抖落在豆苗周圍,在陽光下讓蚜蟲爬苗,并刺入口針(耗時約2-3h),最終使每棵豆苗爬有蚜蟲約20-30頭。配制所需濃度的化合物溶液,分為兩組,第一組不經紫外光的照射(未光照組),第二組用310nm紫外燈照射一定的時間(光照組,放在黑暗條件下),溶液中DMSO含量不超過5%,溶液中含有少量表面活性劑曲拉通(500ml清水中含曲拉通2-3滴)。采用浸苗法處理蚜蟲,將爬有豆蚜的豆苗在已配好的兩組溶液中浸泡2-3s,連續3次。然后用吸水紙吸干豆苗上多余的溶液,每個濃度3個重復。然后將豆苗插入帶水海綿上,罩上馬燈罩,避光,在25℃恒溫條件下放置48h。48h后觀察并統計光照組和未光照組蚜蟲死亡情況,并根據公式計算死亡率(%):死亡率(%)=(對照活蟲數-處理活蟲數)/對照活蟲數×100%。結果見表1。
(2)對白紋伊蚊4齡幼蟲的殺蟲活性
白紋伊蚊(Aedes albopictus)俗稱黑蚊子、花蚊子、花斑蚊、花腳蚊,生性兇猛、攻擊力強,也被稱為"亞洲虎蚊",屬于長角亞目蚊科,中等大小的黑色蚊蟲,上面具有白色鱗片形成的斑紋,白紋伊蚊源于東南亞,是東南亞和中國的常見蚊種。白紋伊蚊幼蟲(孑孓)無脊椎動物,昆蟲綱,雙翅目蚊類的幼蟲。它是由雌蚊在淡水中產的卵孵化而成,其體細長,胸部較頭部及腹部寬大,游泳時身體一屈一伸,通稱跟頭蟲。白紋伊蚊喜歡在小面積的積水上產卵,而且其幼蟲具有"嗜靜"的特性。水環境安靜、陰涼,不易受打擾,最適合這種伊蚊產卵以及孑孓存活。孑孓身體細長,呈深褐色,在水中上下垂直游動,以水中的細菌和單細胞藻類為食,呼吸空氣。幼蟲主要孳生于人房附近的竹筒、樹洞、石穴、廢輪胎以及缸罐、瓦缽、泡菜缸等容器積水,也見于菠蘿等植物葉腋。孑孓經4次蛻皮后發育成蛹,初期蛹仍可活動,將羽化時則基本不可動,而后羽化為成蚊。白紋伊蚊既是一種攻擊性很強的蚊子,也是一種重要的病毒媒介,它可以傳播很多病原體,包括登革熱、羅斯河病毒和西尼羅病毒。蚊蟲的綜合治理方法包括環境治理、生物防治、化學防治、法規防治和遺傳防治等。化學防治是通過對孳生地投藥,對白紋伊蚊的成蚊直接噴灑起到了較好作用,但是在投入較大的人力、物力、財力的同時對環境造成了不同程度的污染,化學藥物的應用也使蚊蟲產生抗藥性。因此研究高效、低毒的殺蟲劑來殺滅蚊子的幼蟲,可以有效的控制蚊子數量的增加,抑制人類疾病的傳播。
操作過程:選取大小一致的4齡白紋伊蚊幼蟲若干。將待測化合物以DMSO助溶(溶液中DMSO含量不超過5%),用除氯水稀釋,準確配制成800、400、200、100、50、25、12.5、6.25、3.13、1.57ppm溶液,設置兩組實驗,第一組不經紫外光的照射(未光照組),第二組用310nm紫外燈照射一定的時間(光照組,放在黑暗條件下)。然后取配制好的各濃度的化合物2mL加入到4mL的離心管中,再分別轉移30只孑孓進入相應的離心管,最后補加2mL的除氯水,使溶液體積為4mL,最終化合物濃度為400、200、100、50、25、12.5、6.25、3.13、1.57、0.79ppm,并以除氯水溶液處理作空白對照,以吡蟲啉作為陽性對照,每個濃度設3個重復。將光照組和未光照組都放入黑暗條件下,在25℃恒溫條件下放置24h。24h后觀察并統計光照組和未光照組孑孓死亡情況,并根據公式計算死亡率(%):死亡率(%)=(對照活蟲數-處理活蟲數)/對照活蟲數×100%。結果見表1。
表1.式(A)化合物的殺蟲活性
實施例9化合物1的光致變色現象
光致變色現象(photochromism)是指化合物A,在受到特定波長光照射后,能夠進行特定的化學反應,進而生成產物B,而在另一波長光照射或者熱的作用下,又可恢復到原來的狀態的現象。
二芳基乙烯類化合物也是一類基于周環反應的有機光致變色化合物。此類化合物的母體結構是一個6π電子共軛的己三烯。在紫外光激發下,處于反平行狀態的分子發生分子內的順旋關環反應,形成共軛的閉環態分子而呈色。而在可見光的照射后,閉環態分子開環恢復至原來狀態。經過適當的分子結構修飾,此類化合物的閉環態可以呈現出從黃色到綠色的全部顏色。
以化合物1為例說明:采用310nm的紫外光照射化合物1乙腈溶液,在可見光區520nm處出現一個很寬的吸收峰,且隨著照射時間的延長而吸收峰的強度增強,關環產物濃度逐漸增大。大約經過90s照射后,化合物1達到開環閉環的平衡態(圖2),可以觀察到溶液的顏色很快由無色變為紅色,這說明化合物1在紫外光的作用下發生了閉環的光致變色反應。然后用430nm的藍光照射關環化合物1,可以觀察到溶液顏色由紅色變為無色,說明關環化合物1在可見光下發生了開環的光致變色反應,反應式如下:
結合實施例8和實施例9可知:關環化合物的殺蟲效果更好。
實施例10化合物1的耐疲勞性
耐疲勞性是基于化合物經歷光致變色的呈色和消色之間循環次數的評價指標。光致變色反應總是伴隨著化學鍵的改變,在此過程中,副反應的發生不可避免。這無疑會導致化合物的部分降解,降低化合物的耐疲勞度。二芳基乙烯化合物的耐疲勞性除了受到環境因素的影響外,其自身分子結構的差異也會造成其耐疲勞度的不同。在分子結構方面,芳基上取代基的類型會對其耐疲勞性造成很大的影響。
以化合物1為例說明:當采用紫外光和可見光交替照射化合物1的乙腈溶液時,它表現出良好的耐疲勞性。當用310nm紫外光照射時,化合物1的乙腈溶液由無色變為紅色,并且在520nm附近處出現了新的特征吸收峰,這表明它形成了閉環體的化合物。而當大于400nm光照射時,溶液紅色消失,閉環態的化合物發生開環反應變成開環態的化合物。如圖3所示,整個成色和漂白過程可以重復6次以上而未發生大的衰減,這表明化合物1具有良好的耐疲勞性。
實施例11熒光偏振實驗及對新煙堿殺蟲劑進行高通量篩選
本發明的化合物1關環后有熒光,并且與煙堿乙酰膽堿受體有很好的結合力,我們利用熒光偏振實驗確定了化合物及蛋白結合時的最優濃度,并通過競爭性實驗首次對新煙堿殺蟲劑進行高通量篩選。
實驗方法:
制備煙堿乙酰膽堿受體溶液
解剖:選取美洲大蠊雄性成蟲(數量根據實驗需要而定),75%酒精體表消毒,背部向上固定在解剖蠟盤中。在解剖鏡下,沿背中線剪開體壁,去掉背板,剔除消化道、氣管、脂肪體等雜質,剖離出神經節用漂洗2次,整個過程在室溫下操作。解剖過程中要不斷更換生理溶液,使神經索始終浸泡于新鮮生理溶液A中(放在冰上)。
勻漿:將上述含有神經元細胞的溶液用聚四氟乙烯勻漿器勻漿。
離心:將上述勻漿在4℃、25000*g離心30min,沉淀用緩沖溶液A清洗兩遍。然后用緩沖溶液A重新懸浮沉淀(放在冰上30min),再次用相同的條件離心,用pH7.4緩沖液B(50mM Tris-HCl、120mM NaCl)重懸浮沉淀,-80℃保存備用。
測定關環化合物1與蛋白結合時的最優濃度
標準曲線測定:
考馬斯亮藍法測定蛋白標準曲線(8個濃度,每個濃度3個重復,每孔加297μL考馬斯亮藍液和3μL標準蛋白液)。酶標儀檢測。
蛋白濃度檢測:
考馬斯亮藍法測定蛋白的濃度,96孔板,3個平行,每個平行加入297μL考馬斯亮藍液和3μL蛋白液。酶標儀檢測。
熒光偏振結合實驗:
實驗在全黑96孔發光板(上海臥宏生物科技有限公司)中進行,每個濃度3個重復。配置1.95*100、3.91*100、7.81*100、15.625*100、31.25*100、62.50*100和80*100μM梯度濃度的關環化合物1,將制備的蛋白濃度稀釋到229mg/L。首先,在全黑96孔發光板中加入99μl蛋白液(終濃度227mg/L),然后每孔加入1μl梯度濃度的關環化合物1(終濃度為1.95、3.91、7.81、15.625、31.25、62.50和80μM)。將全黑96孔板放入22℃恒溫培養箱中培育1h。Synergy H1酶標儀(Bio-Tek)檢測熒光偏振值,激發波長和發射波長分別設定為420nm和590nm。
實驗結果見表2和圖4:
表2
從圖4可以看出當化合物濃度達到40μM時,FP值達到平衡。
通過競爭性實驗對新煙堿殺蟲劑進行高通量篩選
實驗在全黑96孔發光板(上海臥宏生物科技有限公司)中進行,每個濃度3個重復。配置0.001*101、0.003*101、0.01*101、0.03*101、0.1*101、0.3*101、1*101、3*101和10*101μM梯度濃度的吡蟲啉、噻蟲啉、啶蟲脒、烯啶蟲胺、噻蟲嗪、噻蟲胺、呋蟲胺、煙堿、地棘蛙素、殺螟丹、多殺菌素、氟蟲腈、毒死蜱和高效氯氰菊酯,配置4.04mM關環化合物1,將制備的蛋白液濃度稀釋到232mg/L。首先,在全黑96孔發光板中加入99μl蛋白液(終濃度為227mg/L),然后每孔加入1μl梯度濃度的關環化合物1(終濃度為40μM),最后加入配置好的上述商品化農藥(終濃度為0.001、0.003、0.01、0.03、0.1、0.3、1、3和10μM)。將全黑96孔板放入22℃恒溫培養箱中培育1h。Synergy H1酶標儀(Bio-Tek)檢測熒光偏振值,激發波長和發射波長分別設定為420nm和590nm。
競爭性藥物的IC50值見表3。
表3.煙堿乙酰膽堿受體配體的IC50值
實施例12含有本發明化合物的殺蟲劑組合物的制備
(a)油狀懸浮液
按比例準備以下組分:25%(重量百分比,下同)化合物1-7中任一種化合物;5%聚氧乙烯山梨醇六油酸酯;70%高級脂肪族烴油。將各組分在沙磨中一起研磨,直到固體顆粒降至約5微米以下為止。所得的粘稠懸浮液可直接使用,但也在水中乳化后使用。
(b)水懸浮液
按比例準備以下組分:25%化合物1-7中任一種化合物;3%水合硅鎂土(hydrate attapulgit);10%木質素磺酸鈣;0.5%磷酸二氫鈉;61.5%水。將各組分在球磨機中一起研磨,直到固體顆粒降至約10微米以下為止。該水懸浮液可直接使用。
(c)餌劑
按比例準備以下組分:0.1-10%化合物1-7中任一種化合物;80%小麥面粉;19.9-10%糖蜜。將這些組分完全混合,按需要形成餌形狀。可食用餌可以分散到衛生害蟲所侵染的場所,例如家居或工業場所,諸如廚房、醫院或商店或戶外區域,以通過口服攝入來防治害蟲。
本發明提及的所有文獻都在本申請中引用作為參考,就如同每一篇文獻被單獨引用作為參考那樣。此外應理解,在閱讀了本發明的上述講授內容之后,本領域技術人員可以對本發明作各種改動或修改,這些等價形式同樣落于本申請所附權利要求書所限定的范圍。
- 還沒有人留言評論。精彩留言會獲得點贊!