1?(3?氨基?1,2,4?三唑)?基?3,3?二甲基?2?丁酮及其應用的制作方法
本發明屬于植物生長調節劑領域,涉及一種1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮及其應用。
背景技術:
三唑類植物生長調節劑即指含有三氮唑五元環類化合物,多數三唑類具有內吸性、光譜性、立體選擇性等生理活性特點。高效植物生長調節劑備受人們的關注,近四十年來人們除了在研究內源性植物生長調節劑以外,也在積極的研究外源性植物生長調節劑。
三唑類植物生長調節劑是以上世紀八十年代由日本人開發的三唑酮、烯效唑為主要代表,而且這倆化合物也是目前市場化主流的三唑類植物生長調節劑,尤其是烯效唑,其活性是三唑酮的6-10倍。其作用機理普遍被認為是抑制赤霉素的合成中貝殼杉烯的轉化。其主要的特點是縮短節間伸長,矮化植株。三唑酮、烯效唑除了影響赤霉素的合成,還抑制油菜素內脂的合成,同時還調節植物體內脫落酸、乙烯、IAA的含量。盡管這些化合物具有廣泛的生物活性,其實在實際應用中也因活性廣泛而來了一些生產上的麻煩。比如在調節ABA含量,增加抗逆性的同時,也矮化了植株,可能被認為產生了藥害;在這方面,日本的科學家做了很多工作,以烯效唑為母體結構,通過結構修飾獲得一些具有專一性ABA-8’-羥基化酶抑制劑;另一方面這些化合物水溶性不好,在實際應用過程中,往往需要添加一定量的助劑,不僅增加成本還對環境造成了一定的污染。
氨基-1,2,4-三氮唑-酮類化合物某種程度上屬于多胺類化合物,也是烯效唑、三唑酮合成中間體的類似物,可能具有潛在的植物調節生理活性,同時氨基-三氮唑的存在大大增加了分子的親水性能。根據藥物拼接原理,將兩個或者多個具有不同生物活性的片段連接在同一分子設計合成的藥物分子能通過結合不同的生物靶點發揮良好的藥效作用。本專利選擇3-氨基-1,2,4-三氮唑與叔丁基酮拼接,并進行植物調節活性的測試,結果表明,具有良好的促進植物根系生長發育的效應,這是非常有意義的研究,因為之前發現的大部分三唑類植物調節劑主要是抑制赤霉素的合成,導致植物矮化等效應。在我們的研究中發現1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮不僅沒有矮化植株,而且對植株根系的形成具有很好的調控作用。此化合物不僅活性顯著,且水溶性非常好,合成簡單,成本低廉,因此有望在農藥領域得到廣泛的應用。
技術實現要素:
本發明的第一目的是提供一種1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮,克服目前的大部分三唑類植物調節劑主要是抑制赤霉素的合成,導致植物矮化的問題。
本發明的第二目的是提供上述1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的制備方法。
本發明的第三目的是提供上述1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的應用。
本發明通過以下技術方案來實現:
一、一種1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮,化學結構式為:
該化合物的物理特征:白色屑狀固體,晶體結構的晶型為單斜體,分子式為:C8H14N4O,分子量為:182。
二、一種根據上述的1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的制備方法,該方法包括以下步驟:
(1)0.12-1.19mmol的3-甲基-1,2,4-三氮唑和等量的吡啶混合,吡啶作為催化劑和縛酸劑;
(2)加入10-70mL的乙腈作為反應溶劑;
(3)0.099-0.99mmol的1-叔丁基-2-氯-乙酮和10-20ml的乙腈混溶稀釋,整體加入到上述反應體系中;
(4)微波輻射1-5min,輻射功率為100-600W;
(5)反應結束后冷卻至室溫,減壓濃縮除去乙腈溶劑,產物用乙醇溶解,過濾,并用乙醇洗滌固體3次,每次乙醇用量不超20mL;
(6)將濾液合并并濃縮至5-10mL左右;
(7)濃縮產物用柱層析法進行分離,其中,硅膠細度為200-300目,洗脫液組成及比例:石油醚:乙酸乙酯:甲醇=2:2:0.5,Rf=0.25,熔點152-154℃。
化學反應式為:
三、上述的1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮在促進雙子葉作物根系形成的應用。
四、上述的1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮在促進單子葉作物根系形成的應用。
采用上述技術方案的積極效果:本發明選擇3-氨基-1,2,4-三氮唑與叔丁基酮拼接,并進行植物調節活性的測試,結果表明,本化合物不僅沒有矮化植株,而且對植株根系的形成具有很好的調控作用,并且活性顯著,水溶性非常好,合成簡單,成本低廉,因此有望在農藥領域得到廣泛的應用。
附圖說明
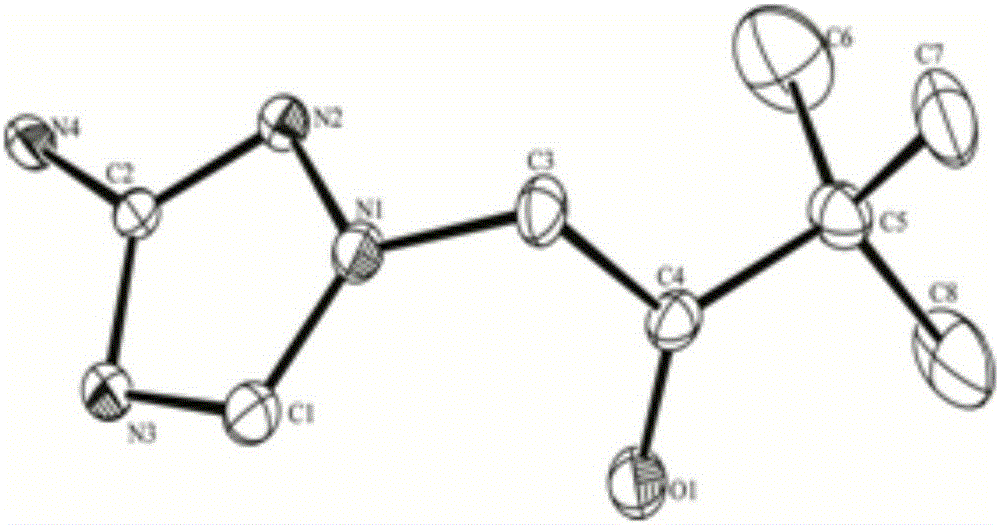
圖1是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的晶體結構;
圖2是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的氫譜;
圖3是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的碳譜;
圖4是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮高分辨質譜;
圖5是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮單晶結構圖;
圖6是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對小麥幼苗(10d)藥效圖;
圖7是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對小麥72小時生長的影響;
圖8是1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對小麥芽生長(96h)藥效圖;
圖9是不同濃度1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對大豆根生長(72h)藥效圖。
具體實施方式
下面結合具體的實施例對本發明的技術方案做進一步的說明,但不應理解為對本發明的限制:
實施例1
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的制備。
0.12mmol的3-甲基-1,2,4-三氮唑和等量的吡啶混合,吡啶作為催化劑和縛酸劑;加入70mL的乙腈作為反應溶劑;0.099mmol的1-叔丁基-2-氯-乙酮和20ml的乙腈混溶稀釋,整體加入到上述反應體系中;微波輻射5min,輻射功率為100W;反應結束后冷卻至室溫,減壓濃縮除去乙腈溶劑,產物用乙醇溶解,過濾,并用乙醇洗滌固體3次,每次乙醇用量不超20mL;將濾液合并并濃縮至5mL左右;濃縮產物用柱層析梯度洗脫法進行分離,其中,硅膠細度為200-300目,洗脫液組成及比例:石油醚:乙酸乙酯:甲醇=2:2:0.5,Rf=0.25,熔點152-154℃。
實施例2
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的制備。
0.8mmol的3-甲基-1,2,4-三氮唑和等量的吡啶混合,吡啶作為催化劑和縛酸劑;加入50mL的乙腈作為反應溶劑;0.6mmol的1-叔丁基-2-氯-乙酮和10ml的乙腈混溶稀釋,整體加入到上述反應體系中;微波輻射4min,輻射功率為200W;反應結束后冷卻至室溫,減壓濃縮除去乙腈溶劑,產物用乙醇溶解,過濾,并用乙醇洗滌固體3次,每次乙醇用量不超20mL;將濾液合并并濃縮至10mL左右;濃縮產物用柱層析梯度洗脫法進行分離,其中,硅膠細度為200-300目,洗脫液組成及比例:石油醚:乙酸乙酯:甲醇=2:2:0.5,Rf=0.25,熔點152-154℃。
實施例3
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的制備。
1.19mmol的3-甲基-1,2,4-三氮唑和等量的吡啶混合,吡啶作為催化劑和縛酸劑;加入10mL的乙腈作為反應溶劑;0.99mmol的1-叔丁基-2-氯-乙酮和15ml的乙腈混溶稀釋,整體加入到上述反應體系中;微波輻射3min,輻射功率為400W;反應結束后冷卻至室溫,減壓濃縮除去乙腈溶劑,產物用乙醇溶解,過濾,并用乙醇洗滌固體3次,每次乙醇用量不超20mL;將濾液合并并濃縮至5mL左右;濃縮產物用柱層析梯度洗脫法進行分離,其中,硅膠細度為200-300目,洗脫液組成及比例:石油醚:乙酸乙酯:甲醇=2:2:0.5,Rf=0.25,熔點152-154℃。
實施例4
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的制備。
0.5mmol的3-甲基-1,2,4-三氮唑和等量的吡啶混合,吡啶作為催化劑和縛酸劑;加入30mL的乙腈作為反應溶劑;0.3mmol的1-叔丁基-2-氯-乙酮和20ml的乙腈混溶稀釋,整體加入到上述反應體系中;微波輻射1min,輻射功率為600W;反應結束后冷卻至室溫,減壓濃縮除去乙腈溶劑,產物用乙醇溶解,過濾,并用乙醇洗滌固體3次,每次乙醇用量不超20mL;將濾液合并并濃縮至10mL左右;濃縮產物用柱層析梯度洗脫法進行分離,其中,硅膠細度為200-300目,洗脫液組成及比例:石油醚:乙酸乙酯:甲醇=2:2:0.5,Rf=0.25,熔點152-154℃。
實施例5
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的結構鑒定。
1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的結構鑒定包括核磁共振氫譜(1HNMR)、核磁共振碳譜(13C NMR)、高分辨質譜(HRMS)和X-射線單晶衍射,具體譜圖見圖1-5,具體數據如下:
1H NMR(DCCl3)δ7.74(s,1H),4.95(s,2H),4.13(s,2H),1.25(s,9H);13C NMR(DCCl3)δ206.7,163.3,144.2,52.7 43.5,26.1(×3);HRMS(ESI)calcd for[M+H]+C8H15N4O:183.124038,found 183.12398.
1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的晶體數據以及結構細化如表1:
表1:化合物的晶體數據及結構細化
1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的晶體結構鍵長及鍵角如表2:
表2化合物3晶體結構鍵長及鍵角
實施例6
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮促進小麥根系發育實驗。
將1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮用蒸餾水分別配置成濃度為:100ppm、50ppm、10ppm三個供試濃度,以清水做對照,每個處理重復4次。培養皿(d=9cm)中放入兩層濾紙,每個皿加入供試液體10mL,貼上標簽備用。
精選小麥種子約400粒,用3%的次氯酸鈉消毒20min,然后用蒸餾水漂洗30分鐘,用濾紙吸干種子表面的水分。然后沿著培養皿周緣整齊地擺放20粒種子,使種子胚朝向培養皿中心,加蓋后置于25℃培養箱中,24h后觀察種子萌發情況,選取發芽整齊的種子10粒繼續培養至第10天。測量個處理種子的根數、根長及芽長,求其平均值,確定1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對根、芽生長具有顯著生物學效應的作用濃度。結果如下:
表3化合物對小麥10d根長(第一條根、第二條根)、根尖數的影響
如表3中數據顯示,1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮的使用濃度在50ppm時,三條種子根的根長促進率分別達到65.3%,66.5%,39.5%。
根據前期小麥幼苗試驗結果,小麥試驗最佳適應濃度為50ppm,以清水做對照,每個處理重復4次。培養皿(d=9cm)中放入兩層濾紙,每個皿加入供試液體10mL,貼上標簽備用。
精選小麥種子約400粒,用3%的次氯酸鈉消毒20min,然后用蒸餾水漂洗30分鐘,用濾紙吸干種子表面的水分。然后沿著培養皿周緣整齊地擺放20粒種子,使種子胚朝向培養皿中心,加蓋后置于25℃培養箱中,24h后觀察種子萌發情況,選取發芽整齊的種子10粒繼續培養至72h。測量個處理種子的根尖數、根長及芽長,求其平均值。
試驗結果如圖6-8所示,在50ppm濃度下,1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮藥劑處理實驗表現出較好的生物學效應,除了根的條數差別較小,三條根的長度及胚芽鞘長度均顯示出較大的差別,此生育時期根尖數對照與藥劑處理之間差異不顯著。
實施例7
本實施例說明1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對大豆幼苗生長的影響。
將化合物1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮配制成濃度分別為:200ppm,100ppm,50ppm,試驗以清水作為對照,以珍珠巖為培養介質,裝入500mL的培養缽中備用。
精選50粒大豆種子,25℃下用以上準備好的各濃度藥液浸種6-8小時,藥劑與種子體積比例范圍為1.5-3;然后瀝水并用濾紙吸取種子表面多余的水分,將種子沿培養缽邊緣擺放并逐步收向缽中心,種子肚臍朝下。然后用保鮮膜封口并放入27℃培養中培養,72h測大豆初生根長度、側根數量,試驗結果見表4及圖9。
表4化合物對大豆72h初生根長度、側根形成的影響
由表4可以看出,1-(3-氨基-1,2,4-三唑)-基-3,3-二甲基-2-丁酮對大豆的初生根和側根都有很好的促進生長的作用。
本發明選擇3-氨基-1,2,4-三氮唑與叔丁基酮拼接,并進行植物調節活性的測試,結果表明,本化合物不僅沒有矮化植株,而且對植株根系的形成具有很好的調控作用,并且活性顯著,水溶性非常好,合成簡單,成本低廉,因此有望在農藥領域得到廣泛的應用。
- 還沒有人留言評論。精彩留言會獲得點贊!