一種二氯甲烷制備三氯乙烯的方法與流程
本發明涉及一種三氯乙烯的制備方法,具體涉及一種二氯甲烷氧化偶聯反應制備三氯乙烯的方法。
背景技術:
三氯乙烯(TCE)是一種重要的有機氯產品,溶解能力極強,在工業上主要用于金屬清洗(脫脂徹底)、纖維脫除油脂、以及電子元件的清洗。其次,三氯乙烯還可作為原料中間體,用于生產四氯乙烯、氯乙酸、二氯乙酰氯、八氯二丙醚、HFC-134a等產品。此外,三氯乙烯還可用作萃取劑和溶劑。
根據所用原料的不同,三氯乙烯的生產方法主要有乙炔法和乙烯法。
根據脫氯化氫方法的不同,乙炔法又可分為皂化法和氣相催化法。皂化法以無水三氯化鐵為催化劑,在減壓狀態下乙炔和氯氣加成反應生成四氯乙烷,四氯乙烷再與石灰乳反應,生成三氯乙烯和氯化鈣,生成的三氯乙烯與水共沸蒸出,經低沸塔和高沸塔精餾除去低沸物和高沸物,即得三氯乙烯產品。皂化法工藝簡單,但皂化殘夜量較多,每生產一噸三氯乙烯產品會產生5-8噸皂化殘夜,環保壓力較大,屬于淘汰工藝。氣相催化法在得到四氯乙烷之前所用工藝條件基本與皂化法相同,之后將四氯乙烷氣化,在200-290℃條件下進入裝有催化劑的固定床反應器脫去氯化氫,生成粗三氯乙烯,再經過多塔分離得到成品三氯乙烯。
與乙炔氯化-皂化脫氯化氫法相比,乙炔氯化-氣相催化脫氯化氫法生產三氯乙烯工藝安全可靠,“三廢”排放量大幅度減少,在產品質量和環保方面具有較強的優勢。然而,該方法所用乙炔原料主要來自電石,依然在環保和經濟性方面存在一些問題:一方面是在電石的生產過程中存在高耗能和高污染問題;另一方面是在電石水解制乙炔過程中會產生大量電石渣,電石渣雖然可以制成水泥出售,但是在中國目前水泥產能嚴重過剩的形勢下,其盈利空間受到了極大的擠壓。實際上,由于電石價格較高,又加上產能嚴重過剩,中國的三氯乙烯行業在目前基本處于虧損狀態。
乙烯法又可分為氯化法和氧氯化法。氯化法是指,乙烯在110℃和0.8MPa壓力下氯化生成四氯乙烷的混合物(通過調節乙烯和氯氣的比例可控制不同的產物),四氯乙烷混合物再在400-500℃條件下裂解生成不同比例的四氯乙烯和三氯乙烯,分離出氯化氫后,未反應的四氯乙烷循環回反應器反應。粗三氯乙烯經精餾、堿洗、脫水等步驟得到成品三氯乙烯。氧氯化法是指,使用金屬氯化物催化劑,在反應溫度365℃條件下,以二氯乙烷(由乙烯直接氯化反應或氧氯化反應合成)、氯氣、氧氣或氯化氫以及循環使用的烴類氯化物為原料,在流化床反應器內反應得到不同比例的三氯乙烯和四氯乙烯。
與乙烯直接氯化法相比,乙烯-二氯乙烷-氧氯化法生產三氯乙烯工藝由于采用了氧氯化反應,避免了通常要產生的大量氯化氫副產物,屬于比較先進的生產工藝。然而,無論是直接氯化法,還是氧氯化法,都需要以乙烯為起始原料,這對于那些乙烯資源緊張的國家,比如中國來說,使用乙烯為原料生產三氯乙烯,常常由于乙烯價格昂貴導致生產成本較高,從而降低了經濟可行性,這也是中國普遍采用電石乙炔-氣相催化脫氯化氫法工藝來生產三氯乙烯的主要原因。
1982年,Keller和Bhasin(Keller G E,Bhasin M M.Synthesis ofethylene via oxidative coupling of methane:I.Determination of active catalysts[J].Journal of Catalysis,1982,73(1):9-19.)報道了使用多種氧化物催化劑在交替進料條件下,可從甲烷制得少量乙烷、乙烯,從而引起各國學者的廣泛關注。研發人員通過幾十年的大量研究發現,變價金屬氧化物、堿土金屬氧化物、稀土金屬氧化物、復合氧化物等催化劑均具有不同程度的甲烷氧化偶聯活性。
受到甲烷氧化偶聯反應的啟發,有研究者開始嘗試以鹵代甲烷為原料,通過氧化偶聯反應合成鹵代烯烴。比如在日本專利JPH05262682中,針對以乙烯或甲烷為起始原料合成氯乙烯的各種技術路線所存在的問題和不足,提供了一種在催化劑和氧氣存在的條件下,鹵代甲烷發生氧化偶聯反應制備鹵乙烯等碳數為2及以上的鹵化碳氫化物的方法。該方法所用催化劑以堿金屬化合物為第一組分,以元素周期表中的第一副族、第二副族、第五副族、第六副族、第七副族、第八族、第三主族、第四主族和第五主族中的金屬化合物中的一種或幾種作為第二組分。該專利還以氯甲烷氧化偶聯合成氯乙烯為例,對其提供的技術方案作了說明。值得注意的是,雖然堿土金屬氧化物和稀土金屬氧化物具有甲烷氧化偶聯反應活性,但是該專利所用的催化劑組分并不包含這兩類化合物。另外,雖然該專利指出,其使用的鹵甲烷,至少含有一個鹵素原子但不限于一個,其所得產物是碳數為2及以上的鹵化碳氫化物,但是該專利并沒有明確指出使用甲烷氯化物可以得到三氯乙烯。
技術實現要素:
本發明的目的就在于針對現有技術存在的不足,提供一種以二氯甲烷為原料通過氧化偶聯反應制備三氯乙烯的新方法,該方法不但所用原料價格低廉,而且具有較高的原料轉化率和三氯乙烯選擇性,其主要副產物四氯乙烯和三氯甲烷也是具有一定市場需求的有用化學品。
為了實現上述目的,本發明采用的技術方案是這樣的:
一種二氯甲烷制備三氯乙烯的方法,在具有甲烷氧化偶聯反應活性的催化劑存在的條件下,二氯甲烷與氧氣反應得到三氯乙烯,其反應方程式為:
4CH2Cl2+O2→2C2HCl3+2H2O+2HCl。
所述二氯甲烷與氧氣的摩爾比為1∶(0.1~2),反應溫度為450~700℃,反應壓力為1~10atm。
本發明反應主反應可能的反應機理為:
O2→[O]([O]代表活性氧物種) (1)
CH2Cl2+[O]→CHCl2·+H2O (2)
2CHCl2·→CHCl2-CH2Cl2(四氯乙烷) (3)
CHCl2-CHCl2→CCl2CHCl+HCl(三氯乙烯) (4)
其副反應可能的反應機理為:
CH2Cl2→CH2Cl·+Cl· (5)
CHCl2·+Cl·→CHCl3(三氯甲烷) (6)
CH2Cl2+HCl+[O]→CHCl3+H2O(三氯甲烷) (7)
CHCl3+[O]→CCl3·+H2O (8)
CCl3·+CHCl2·→CCl3-CHCl2(五氯乙烷) (9)
2CCl3·→CCl3-CCl3(六氯乙烷) (10)
CCl3-CHCl2→CCl2=CCl2+HCl(四氯乙烯) (11)
CCl3-CCl3→CCl2=CCl2+Cl2(四氯乙烯) (12)
CHCl2·+[O]→CCl2·+H2O (13)
2CCl2·→CCl2=CCl2(四氯乙烯) (14)
CH2Cl·+[O]→CHCl·+H2O (15)
2CHCl·→CHCl=CHCl(1,2-二氯乙烯) (16)
根據反應機理,選用合適的催化劑和反應條件,可提高反應的轉化率和三氯乙烯選擇性。
此反應機理中,首先是氧氣的活化,即氧氣變為活性氧物種[O]。選用具有甲烷氧化偶聯制乙烯反應活性的催化劑均可使氧氣分子得到活化,如堿土金屬(鎂、鈣、鍶和鋇)及其化合物催化劑、稀土元素(鑭、鈰、鐠、釹和釤)及其化合物催化劑、過渡金屬(鈧、鈦、釩、鉻、錳、鐵、鈷、鎳、銅、鋅、釔、鋯、鈮、鉬、釕、銠、鈀、銀、鎢、錸、銥、鉑、和金)及其化合物催化劑、以及主族金屬(錫、鉛、鎵、鉍)及其化合物催化劑均對二氯甲烷氧化偶聯制三氯乙烯反應具有活性,所述的化合物包括氧化物、鹵化物、硫酸鹽、磷酸鹽、碳酸鹽、硝酸鹽、絡合物和有機金屬鹽。根據具體的反應條件不同,這些催化劑可在450~700℃之間發揮催化作用。
其次,活性氧物種[O]奪取二氯甲烷分子中的氫原子生成二氯甲基(CHCl2·),在此過程中,通過添加適當的助劑,如堿金屬及其化合物(鋰、鈉、鉀、銣和銫),或通過選擇合適的催化劑載體,調節二氯甲烷分子在催化劑表面的吸附強度和活性氧物種[O]的反應活性,從而控制二氯甲烷分子的活化方式,使其優先斷裂碳氫鍵(C-H)生成二氯甲基(CHCl2·),而不是斷裂碳氯鍵(C-Cl)生成氯甲基(CH2Cl·),需要說明的是,助劑的添加除了可以改善選擇性外,也有可能在一定程度上提高催化劑的活性。
最后,二氯甲基(CHCl2·)自身偶聯生成四氯乙烷分子,四氯乙烷分子再接著脫去一個氯化氫分子生成最終產物三氯乙烯。
對于二氯甲烷氧化偶聯反應,為減少副反應發生,除需使用合適的催化劑來控制二氯甲烷分子的活化方式(使其優先斷裂碳氫鍵)外,選擇合適的反應溫度也很重要,因為反應溫度越高,碳氯鍵斷裂幾率也就越高,則三氯乙烯的選擇性也會相應下降。另外,選擇合適的烷氧比(二氯甲烷/氧氣)不但可以保持相對較高的轉化率,還可避免對二氯甲烷分子的過度活化,從而減少三氯甲烷、四氯乙烯、1,2-二氯乙烯等副產物的生成。一般來說,在較高反應溫度時,宜選用較高的烷氧比,而在較低反應溫度時,宜選用較低的烷氧比。
根據上述分析,提出如下的技術方案來實現本發明的目的。
本發明催化劑具有甲烷氧化偶聯反應活性;所述催化劑活性組分選自堿土金屬及其化合物、稀土元素及其化合物或堿土金屬及其化合物、稀土元素及其化合物、過渡金屬及其化合物、主族金屬及其化合物的組合物中的一種或幾種,所述的組合物中至少包含堿土金屬及其化合物或稀土元素及其化合物中的一種或兩種;所述的化合物包括氧化物、鹵化物、硫酸鹽、磷酸鹽、碳酸鹽、硝酸鹽、絡合物和有機金屬鹽。
所述的堿土金屬為鎂、鈣、鍶和鋇;稀土元素為鑭、鈰、鐠、釹和釤,過渡金屬為鈧、鈦、釩、鉻、錳、鐵、鈷、鎳、銅、鋅、釔、鋯、鈮、鉬、釕、銠、鈀、銀、鎢、錸、銥、鉑、和金;主族金屬為錫、鉛、鎵和鉍。
所述催化劑的助劑為堿金屬及其化合物,堿金屬為鋰、鈉、鉀、銣和銫。
催化劑載體選自活性氧化鋁、硅鋁氧化物、硅膠、二氧化鈦、二氧化鋯、分子篩、堿土金屬氧化物或稀土元素氧化物中的一種或幾種。催化劑可用多種制備方法進行制備,如機械混合法、沉淀法、浸漬法、熱熔融法、浸溶法、離子交換法、溶膠凝膠法等。
在本發明中,二氯甲烷與氧氣的摩爾比為1∶(0.1~2),反應溫度為450~700℃,反應壓力為1~10atm。
與現有的三氯乙烯制備路線相比,本發明的創新點如下:
根據對現有三氯乙烯制備工藝反應機理(乙炔或乙烯→四氯乙烷→三氯乙烯)的深刻認識,提出采用催化氧化脫氫的方法對二氯甲烷分子進行活化,使二氯甲烷分子高效轉化為二氯甲基,二氯甲基再進一步自身偶聯變為四氯乙烷,四氯乙烷再接著脫去氯化氫變為三氯乙烯。
與現有的三氯乙烯制備工藝相比,本發明的主要優點如下:
1、不必使用價格昂貴的電石乙炔或乙烯原料,這不但可以降低三氯乙烯生產成本,還可避免電石生產和使用過程中帶來的高耗能和高污染問題。本發明非常符合綠色、環保、可持續發展的理念。
2、原料資源來源廣泛,如圖1所示,二氯甲烷原料可以從天然氣、頁巖氣、煤層氣、天然氣水合物或煤炭(通過煤基甲醇獲得甲烷氯化物)制取,具有很高的靈活性。
附圖說明
圖1為本發明原料來源示意圖;
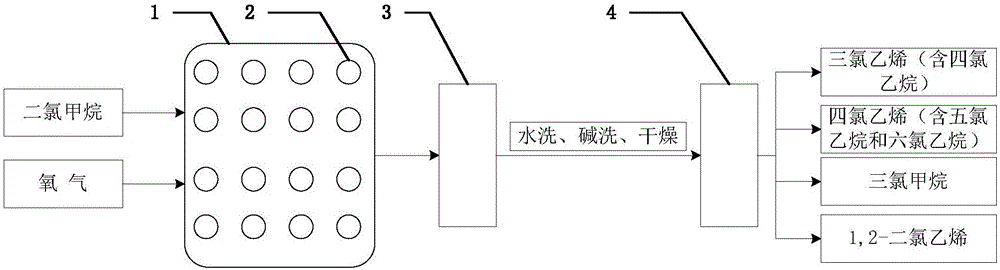
圖2為本發明的生產工藝流程示意圖。
具體實施方式
為了更加清楚地理解本發明的目的、技術方案及有益效果,下面結合具體實施例對本發明做進一步的說明,但并不將本發明的保護范圍限定在以下實施例中。
參見圖2,本發明的生產工藝流程為:氧氣和二氯甲烷進入裝有催化劑2的反應器1中進行反應;從反應器1出來的產物先進入急冷塔3降溫冷卻,然后再經過水洗和堿洗除去氯化氫,接著是冷凝除水干燥處理,最后進入精餾塔4,根據沸點差異分離出未反應的原料(二氯甲烷和氧氣)、目標產物(三氯乙烯和四氯乙烷)、副產物(四氯乙烯、五氯乙烷、三氯甲烷、1,2-二氯乙烯、以及微量的六氯乙烷)。在這些產物中,四氯乙烷和五氯乙烷可以進一步脫去氯化氫生成三氯乙烯和四氯乙烯;1,2-二氯乙烯可以與氯氣反應生成四氯乙烷,四氯乙烷再脫氯化氫生成三氯乙烯;六氯乙烷可以熱裂解生成四氯乙烯。因此,采用本發明提供的技術方案,得到的最終產品是三氯乙烯、四氯乙烯和三氯甲烷。其中,四氯乙烯和三氯甲烷兩者雖然是副產品,但是也具有較大的工業應用價值,可作為商品出售或進一步加工成其他有用化學品,從而提高本發明方法的經濟價值。
根據所用催化劑催化性能的差異,本發明所用反應器可為固定床或流化床。
實施例1
將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:0.5進行混合,通入未裝填催化劑的反應器中,在600℃,1atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為2%,三氯乙烯(含四氯乙烷)選擇性約為27%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為3%,三氯甲烷選擇性約為52%,1,2-二氯乙烯選擇性約為12%。
實施例2
將鍶的前驅體化合物制成水溶液,加入硅膠攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:0.5進行混合,通入裝有催化劑的反應器中,在600℃,1atm下進行反應,反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為35%,三氯乙烯(含四氯乙烷)選擇性約為45%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為5%,三氯甲烷選擇性約為40%,1,2-二氯乙烯選擇性約為8%。
實施例3
將鍶和鎢的前驅體化合物制成水溶液,加入硅膠攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:0.5進行混合,通入裝有催化劑的反應器中,在600℃,1atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為48%,三氯乙烯(含四氯乙烷)選擇性約為42%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為10%,三氯甲烷選擇性約為36%,1,2-二氯乙烯選擇性約為7%。
實施例4
將鍶、鎢和鈉的前驅體化合物制成水溶液,加入硅膠攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:0.5進行混合,通入裝有催化劑的反應器中,在600℃,1atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為65%,三氯乙烯(含四氯乙烷)選擇性約為55%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為10%,三氯甲烷選擇性約為25%,1,2-二氯乙烯選擇性約為5%。
實施例5
將鋇、鈷和鉀的前驅體化合物制成水溶液,加入二氧化鈦攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:0.1進行混合,通入裝有催化劑的反應器中,在700℃,3atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為90%,三氯乙烯(含四氯乙烷)選擇性約為67%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為15%,三氯甲烷選擇性約為5%,1,2-二氯乙烯選擇性約為6%。
實施例6
將鎂、錳、鋰的前驅體化合物制成水溶液,加入氧化鑭攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:2進行混合,通入裝有催化劑的反應器中,在450℃,10atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為35%,三氯乙烯(含四氯乙烷)選擇性約為26%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為20%,三氯甲烷選擇性約為45%,1,2-二氯乙烯選擇性約為6%。
實施例7
將鈰和鉀的前驅體化合物制成水溶液,加入硅膠攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:1進行混合,通入裝有催化劑的反應器中,在530℃,1atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為55%,三氯乙烯(含四氯乙烷)選擇性約為53%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為9%,三氯甲烷選擇性約為30%,1,2-二氯乙烯選擇性約為5%。
實施例8
將鈰、鋇、錫和鋰的前驅體化合物制成水溶液,加入硅膠攪拌均勻,然后烘干、焙燒制得催化劑,將二氯甲烷(加熱氣化)和氧氣按照摩爾比為1:0.3進行混合,通入裝有催化劑的反應器中,在530℃,1atm下進行反應。反應流出物經降溫,水洗堿洗除去氯化氫后,進行組成分析,計算得知二氯甲烷轉化率約為70%,三氯乙烯(含四氯乙烷)選擇性約為65%,四氯乙烯(含五氯乙烷和六氯乙烷)選擇性約為14%,三氯甲烷選擇性約為15%,1,2-二氯乙烯選擇性約為4%。
從以上實施例可以看出,本發明方法制備三氯乙烯,具有較高的二氯甲烷轉化率和三氯乙烯選擇性,同時還可副產具有一定經濟價值的四氯乙烯和三氯甲烷。
- 還沒有人留言評論。精彩留言會獲得點贊!