一種羥乙基纖維素基環糊精水凝膠籠的制備方法與流程
本發明涉及一種環糊精水凝膠的制備方法。
背景技術:
羥乙基纖維素為白色或微黃色的粉末,且無臭無味易流動,大多數的HEC可以溶于水,并且可以溶于由水和水溶性有機溶劑所組成的混合溶劑中,其中水的含量在40%以上。HEC不溶于烴類溶劑中,但在加熱的情況下能夠溶解在如二甲基亞砜、苯酚、乙二胺、二亞乙基三胺、2-氯乙酸、二甲基甲酰胺和甲酸等強極性溶劑。HEC的粘度在pH值為2~12的范圍內變化較小,但超過此范圍后粘度降低。經過乙二醛處理的HEC在冷水中會分散且不凝聚,但溶解速度較慢,一般需要30min左右可完全溶解,將其加熱或在pH值為8~10的環境中可迅速溶解。
環糊精(Cyclodextrin,CD)是由直鏈淀粉在芽孢桿菌產生的環糊精葡萄糖基轉移酶的作用下生成的一系列環狀低聚糖的總稱。環糊精一般含有6-12個D-吡喃葡萄糖單元。其中含有6、7、8個葡萄糖單元的環糊精分子被研究的較多,這三種環糊精分別被稱之α-環糊精、β-環糊精、γ-環糊精。它們呈錐形圓環狀結構,且具有親水外緣和疏水內腔。三種環糊精內腔高度都是0.79nm,直徑分別為0.47,0.60和0.75nm。。這三種環糊精中α-環糊精分子的空隙最小,其次是β-環糊精,γ-環糊精的空隙則最大,其中由于α-環糊精和γ-環糊精比較難提取,導致生產成本較高,所以這兩種環糊精未被大面積使用,和這兩種環糊精相比β-環糊精的提取要容易得多,使其生產成本較低,所以工業上以生產β-環糊精為主,因此也使環糊精的研究主要集中于β-環糊精上。
目前的纖維素/環糊精凝膠產品中,由于環糊精本身在水中的溶解度不好而且本身不能夠形成良好的凝膠,所以主要是化學交聯和輻射誘導接枝將beta環糊精接枝在其他一些載體上面。比如用乙二醇二縮水甘油醚(EDGE)做交聯劑在堿性條件下將環糊精接枝到棉花織物上面的,也有用檸檬酸做交聯劑將環糊精接枝到棉織物上面的,還有用環氧氯丙烷將環糊精接枝到納米微晶纖維素上面的。通常在合成環糊精基質凝膠都是在加熱的過程中進行,這樣會影響環糊精對藥物包合能力,還會導致發生一些副反應,生成一些有毒物質,使其不能用做生物醫學材料。目前合成的環糊精基質凝膠中有膏狀的,也有果凍狀的,前者能夠以任何形態使用,但是會溶于水,后者擁有一定的溶脹能力和機械性能而且不溶于水。但是目前的合成過程也存在一些弊端,比如對未改性的環糊精接枝率太低,或者使用改性后的環糊精大大提高成本還有合成的凝膠沒有合適的機械性能都對合成的凝膠應用照成一定阻礙。
技術實現要素:
本發明是要解決現有羥乙基纖維素基環糊精水凝膠的制備方法復雜,環糊精搭載量低的問題,提供一種羥乙基纖維素基環糊精水凝膠籠的制備方法。
本發明羥乙基纖維素基環糊精水凝膠籠的制備方法,按以下步驟進行:
一、將β-CD溶解于質量分數為15%~25%的NaOH溶液中,之后加入到質量分數為3%~7%的羥乙基纖維素(HEC)水溶液中,攪拌30~40min,然后加入環氧氯丙烷(EPI),攪拌10~20min,得到混合溶液;其中β-CD的質量與NaOH溶液的體積比為(8-16)g:(10-30)mL,β-CD的質量與羥乙基纖維素水溶液的體積比為(8-16)g:(10-30)mL,β-CD的質量與環氧氯丙烷的體積比為(8-16)g:(10-14)mL;
二、將混合溶液在密封的條件下靜止4~6h,形成羥乙基纖維素基環糊精水凝膠。
本發明的有益效果:
本發明在室溫下,以環氧氯丙烷(EPI)為交聯劑并在強堿作用下使羥乙基纖維素(HEC)自交聯形成可以大量包合β-環糊精的水凝膠——(β)CD-g-HEC。其中HEC交聯形成三維網狀結構,像“籠子”一樣,并將環糊精包合在其中,如圖1所示,圖中1為β-CD,2為HEC交聯形成三維網狀結構,3為EPI。因此稱之為羥乙基纖維素基環糊精水凝膠籠。
(β)CD-g-HEC水凝膠具有穩定的適合的HEC鏈空間網狀結構,這可以很容易地包含更多的β-CD并且保證這些被包含其中β-CD不易被透析除去。因此,這也使β-CD的裝載效率可以達到70.50%。
相較于純的羥乙基纖維素凝膠而言,加入環糊精的凝膠籠擁有更好的機械性能和更快的吸水速率。用疏水分子酚酞來評估環糊精凝膠籠中的環糊精的活性,結果顯示,環糊精凝膠籠能夠快速吸收大量酚酞分子并且維持酚酞分子在凝膠中緩慢釋放出來。
另外,本發明可通過控制EPI的加入量來控制水凝膠的機械強度。本發明制備的羥乙基纖維素基環糊精水凝膠擁有可再生性、來源廣、無毒、可降解、生物相容等優點。
本發明的合成方法條件溫和,且方法簡單,且所得到的水凝膠中含有大量的β-CD,所以在工業上存在可以大量生產的實際意義。并且由于這種方法所得到的水凝膠具有透明,易于處理,質地柔軟,無毒等特點,因此適合于與皮膚接觸,這將使其在制藥、食品、化妝品,農業和林業等領域得到更廣泛使用。
附圖說明
圖1為本發明制備的環糊精水凝膠籠的結構模型;
圖2為(β)CD-g-HEC水凝膠與HEC水凝膠的機械強度測定結果;
圖3為干燥的HEC水凝膠與(β)CD-g-HEC水凝膠的溶脹率隨時間變化圖;
圖4為加入不同EPI量下的HEC水凝膠與(β)CD-g-HEC水凝膠的最終溶脹度;
圖5為羥乙基纖維素、β-環糊精、HEC水凝膠的紅外光譜圖;
圖6為羥乙基纖維素、β-環糊精、(β)CD-g-HEC水凝膠的紅外光譜圖;
圖7為HEC水凝膠冷凍干燥后經掃描電鏡所觀察到的表面形貌;
圖8為(β)CD-g-HEC水凝膠冷凍干燥后經掃描電鏡所觀察到的表面形貌;
圖9為水凝膠塊吸收酚酞的速率圖;
圖10為水凝膠塊釋放酚酞的速率圖。
具體實施方式
本發明技術方案不局限于以下所列舉具體實施方式,還包括各具體實施方式間的任意組合。
具體實施方式一:本實施方式羥乙基纖維素基環糊精水凝膠籠的制備方法,按以下步驟進行:
一、將β-CD溶解于質量分數為15%~25%的NaOH溶液中,之后加入到質量分數為3%~7%的羥乙基纖維素水溶液中,攪拌30~40min,然后加入環氧氯丙烷,攪拌10~20min,得到混合溶液;其中β-CD的質量與NaOH溶液的體積比為(8-16)g:(10-30)mL,β-CD的質量與羥乙基纖維素水溶液的體積比為(8-16)g:(10-30)mL,β-CD的質量與環氧氯丙烷的體積比為(8-16)g:(10-14)mL;
二、將混合溶液在密封的條件下靜止4~6h,形成羥乙基纖維素基環糊精水凝膠。
具體實施方式二:本實施方式與具體實施方式一不同的是:步驟一中NaOH溶液的質量分數為18%~22%。其它與具體實施方式一相同。
具體實施方式三:本實施方式與具體實施方式一不同的是:步驟一中NaOH溶液的質量分數為20%。其它與具體實施方式一相同。
具體實施方式四:本實施方式與具體實施方式一至三之一不同的是:步驟一中羥乙基纖維素水溶液的質量分數為4%~6%。其它與具體實施方式一至三之一相同。
具體實施方式五:本實施方式與具體實施方式一至三之一不同的是:步驟一中羥乙基纖維素水溶液的質量分數為5%。其它與具體實施方式一至三之一相同。
具體實施方式六:本實施方式與具體實施方式一至五之一不同的是:步驟一中β-CD的質量與NaOH溶液的體積比為10g:20mL。其它與具體實施方式一至五之一相同。
具體實施方式七:本實施方式與具體實施方式一至六之一不同的是:步驟一中β-CD的質量與羥乙基纖維素水溶液的體積比為10g:20mL。其它與具體實施方式一至六之一相同。
具體實施方式八:本實施方式與具體實施方式一至七之一不同的是:步驟一中β-CD的質量與環氧氯丙烷的體積比為(10-14)g:(11-13)mL。其它與具體實施方式一至七之一相同。
具體實施方式九:本實施方式與具體實施方式一至七之一不同的是:步驟一中β-CD的質量與環氧氯丙烷的體積比為8g:12mL。其它與具體實施方式一至七之一相同。
為驗證本發明的有益效果,進行以下試驗:
實施例1:
一、將20gβ-CD(17.6mmol)溶于40mL 20%的NaOH溶液中,之后加入到40mL 5%的HEC水溶液中,然后攪拌30min,之后分別加入不同量的EPI(2,4,6...24mL,2mL=25.53mmol),攪拌10min,得混合溶液。
二、將混合溶液在密封的條件下靜止4h,形成凝膠((β)CD-g-HEC水凝膠)。
對比例:
以相同的條件制備不含有β-CD的水凝膠(HEC水凝膠)。
一、將40mL 20%的NaOH溶液加入到40mL 5%的HEC水溶液中攪拌30min,之后分別加入不同量的EPI(2,4,6...24mL,2mL=25.53mmol),攪拌10min,得混合溶液。
二、將混合溶液在密封的條件下靜止4h,形成凝膠。
所得到的所有水凝膠產品浸泡在10mmol·L-1的HCl溶液中12h。最后將水凝膠切成3.0×1.5×1.5cm的方塊,并浸泡于蒸餾水中一周,以徹底除去不穩定的β-CD和殘留的NaOH和HCl。然后分別通過真空干燥和冷凍干燥得到干燥的水凝膠。
(一)實施例1的反應機理
水凝膠籠經由HEC和EPI的交聯反應而形成(反應式(1)),為了容納β-CD,通過調節EPI的加入量來控制水凝膠的空間網絡結構。在合成的過程中反應式(2)和反應式(3)都有可能發生,但是從這兩個反應式中可以看出它們并未對形成水凝膠籠起到作用,所以這兩個反應屬于副反應。為了控制交聯反應的發生,本實施例選擇將NaOH的加入量控制在一個固定值——8g上。具體原因如下。
第一,NaOH量過多會造成環糊精自交聯,使凝膠變得易碎;第二,在這個濃度下能夠最好的促進HEC的自交聯反應的進行;第三,NaOH量太少不能提供強堿性環境,不僅不能使環糊精完全溶解,而且由于整個體系堿性不夠強,就不能促使足夠環氧氯丙烷開環,而開環的EPI量較少也就導致了HEC之間交聯過少,形成的凝膠極其柔軟,而且不能進行下一步驟的操作。經試驗,2.4gNaOH的時候20g環糊精能夠完全溶解,按照上面步驟的得到的凝膠幾乎沒有機械強度,即使在水中也不能保持形狀,而加入16gNaOH的時候得到的凝膠變黃,就像捏在一起的沙子,一碰就會碎,沒辦法利用。
(二)水凝膠機械強度測定
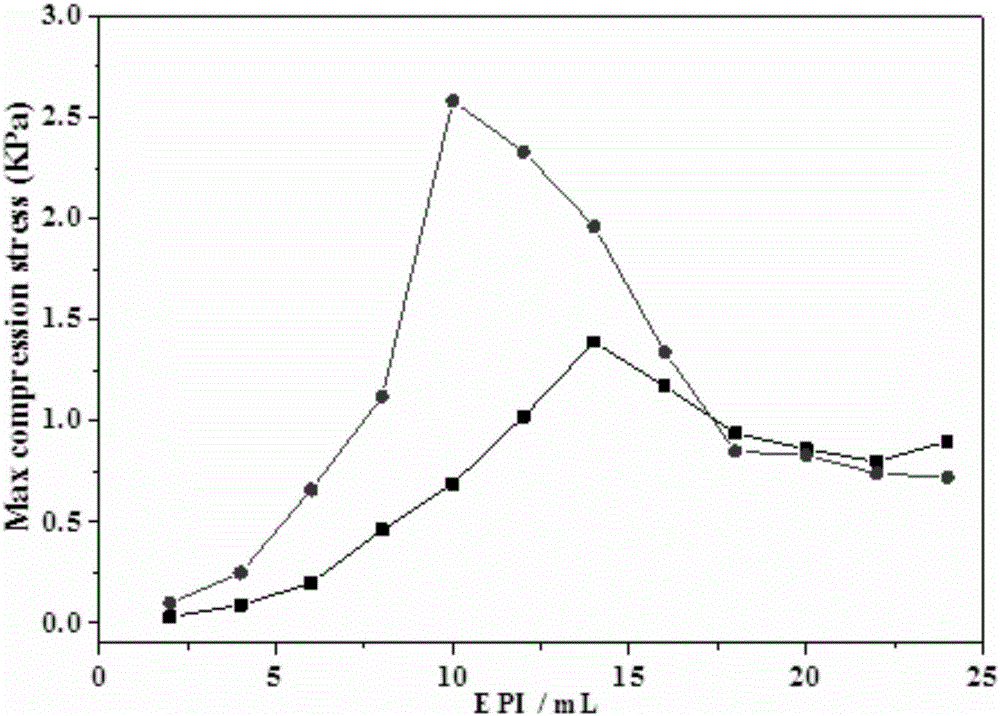
(β)CD-g-HEC水凝膠與HEC水凝膠的機械強度測定結果如圖2所示,■表示HEC水凝膠,●表示(β)CD-g-HEC水凝膠。
從圖2中可以看出(β)CD-g-HEC水凝膠與HEC水凝膠的機械強度都是先增大后減小,且兩者的所能承受的最大壓強分別為2.58KPa和1.39KPa。且從圖2中可以看出兩種水凝膠隨著EPI的加入量從2mL開始以每2mL為一梯度一直加到24mL其機械強度有相當大的差別,從這一現象中可以看出EPI的加入量對水凝膠的機械強度有著相當大的影響。
在機械強度逐漸增加的過程中,(β)CD-g-HEC水凝膠擁有比HEC水凝膠更高的機械強度和機械強度增重速率,這主要是由兩個原因造成的:第一,隨著EPI量的增加HEC之間的交聯度變高,從而導致水凝膠骨架的強度的升高,這就也使水凝膠的內部結構更加穩定,也就使水凝膠的機械強度得到了提升;第二,(β)CD-g-HEC水凝膠有著類似“鋼筋混凝土”的特性,這其中β-CD就相當于鋼筋混凝土里的“鵝卵石”,而交聯在一起的HEC就相當于鋼筋混凝土中的“鋼結構”,另外,水就相當于其中的“水泥”。鋼筋混凝土通過向其中加入鵝卵石以增加其強度,與之同理,向(β)CD-g-HEC水凝膠中加入β-CD就相當于向其三維網狀骨架結構中加入增強劑,并通過這種方法使其機械強度得到顯著提升。當EPI的加入量未超過12mL時,(β)CD-g-HEC水凝膠中的β-CD的裝載量逐步提高,與之對應的(β)CD-g-HEC水凝膠地機械強度也在逐步提高。并且與HEC水凝膠進行對比可以看出在加入相同的EPI量的情況下加入了β-CD的(β)CD-g-HEC水凝膠要比未加入β-CD的HEC水凝膠的機械強度高出很多,這也進一步說明了β-CD的加入確實有效的提高了水凝膠籠的三維網狀結構的骨架強度。
在機械強度逐漸下降的過程中,隨著EPI的量的過量加入(β)CD-g-HEC水凝膠的機械強度迅速下降直至與HEC水凝膠的機械強度相差無幾甚至更低,這種現象大致上也可以用兩種原因對其進行解釋:第一,隨著EPI的過量加入,EPI之間出現自交聯現象,而EPI的自交聯導致了HEC鏈之間的空間變大,這也就使水凝膠籠的三維網狀結構不再像之前那么緊實,骨架的穩定性也不如之前,這也就導致了(β)CD-g-HEC水凝膠的機械強度下降;第二,隨著EPI的加入量超過12mL時β-CD的裝載量也開始下降,而且從第一個原因中可以看出,由于EPI的過量加入導致HEC鏈之間的空間變大,進而導致β-CD更容易被透析除去。隨著(β)CD-g-HEC水凝膠籠中作為增強劑的β-CD流失,本就不再如之前緊實的三維網狀結構變得空隙更大,這也就使其機械強度進一步下降,這也就解釋了為什么當EPI的加入量達到18mL時(β)CD-g-HEC水凝膠的機械強度要比HEC水凝膠的還要低。
(三)溶脹率測定
HEC水凝膠與(β)CD-g-HEC水凝膠的溶脹率測定結果如圖3和4所示。圖3為干燥的HEC水凝膠與(β)CD-g-HEC水凝膠的溶脹率隨時間變化圖(所加入的EPI量都為10mL),圖4為加入不同EPI量下的HEC水凝膠與(β)CD-g-HEC水凝膠的最終溶脹度。其中■表示(β)CD-g-HEC水凝膠,●表示HEC水凝膠。
溶脹性能表示的是水凝膠的持水能力和滲透性能。水凝膠的溶脹以水分子自由擴散進水凝膠的三維網狀結構中為開始,之后與極性親水基團水合并且聚合物開始擴張,到自由水分子與水凝膠網狀結構中的分子達到平衡為止。
從圖3中可以看出HEC水凝膠可以包含更多的水分子,但是其對水的相對吸收速率要比(β)CD-g-HEC水凝膠的慢。這種現象說明了被包裹于(β)CD-g-HEC水凝膠中的β-CD阻礙了水分子擴散進其中,因此導致了(β)CD-g-HEC水凝膠的溶脹性相比于HEC水凝膠要差很多,但這也使其能夠更快的達到其最大溶脹度。
圖4表明了HEC水凝膠與(β)CD-g-HEC水凝膠在不同的EPI加入量下的最終溶脹度,從中可以看出兩種水凝膠的最終溶脹度隨著EPI加入量的增加而發生改變。EPI加入量的不同導致了交聯度的不同,進而導致了水凝膠的三維網狀結構產生了不同的情況。當EPI加入量很少時水凝膠的交聯度比較低,這就導致了水凝膠內部存在很多比較大的孔隙,然后隨著EPI加入量的增加水凝膠的交聯度開始逐漸變高,原本比較大的孔隙也隨之開始不斷變小,這種情況進一步導致水凝膠對水的吸收量不斷變低,之后隨著EPI的過量加入,水凝膠的空間網狀結構的空隙開始變大,這就導致了水凝膠對水的吸收量開始小幅度逐步回升。
(四)β-環糊精裝載量測定
采用重量法和光度滴定法測定樣品中環糊精的含量所得到的數據如表1所示
表1 β-環糊精裝載量數據
表1中可以看出通過重量法所得到的數據要比光度滴定法所得到的高一點,這是因為重量法所測得的是(β)CD-g-HEC水凝膠中β-CD的總重量,而光度滴定法給出的是(β)CD-g-HEC水凝膠中的β-CD的實際封裝能力——由于空間位阻的作用,β-CD之間的交聯使β-CD的封裝能力降低,這表明這部分β-CD不會被光度滴定發檢測出來,這也就導致了重量法所得到的結果要比光度滴定發的高。所以光度滴定發所得到的數據結果更具備研究意義。此外,從表1中可以看出重量法與光度滴定法的結果相差不大,這也說明了β-CD之間的交聯是有限的。
如表1中所示,這兩種方法都表明β-CD的裝載量是隨著EPI的量的增加先增大后減小,并且最大值出現在EPI加入量為12mL時。在EPI的加入量未達到12mL時隨著EPI的加入量的增加水凝膠的交聯度不斷提高,其空間網狀結構變得越來越緊實,進而使水凝膠的內部的空隙變得越來越小,這也就使被包含于其中的β-CD越來越不易被透析除去,進而使(β)CD-g-HEC水凝膠中的β-CD裝載量不斷提高。但是,隨著EPI的過量加入,水凝膠內部的孔隙開始不斷變大,變得不再能有效地阻擋β-CD,β-CD變得越來越容易被透析除去,這就出現了如表1中所示當EPI的加入量大于12mL時β-CD的裝載量不斷降低的現象
(五)傅里葉紅外光譜法(FTIR)表征
圖5為羥乙基纖維素、β-環糊精、HEC水凝膠的紅外光譜圖,其中x表示羥乙基纖維素,y表示HEC水凝膠,z表示β-環糊精。圖6為羥乙基纖維素、β-環糊精、(β)CD-g-HEC水凝膠的紅外光譜圖,其中a表示羥乙基纖維素,b表示(β)CD-g-HEC水凝膠,c表示β-環糊精。
根據干燥的水凝膠凍干粉末的紅外光譜圖,并且以β-CD和HEC的紅外光譜圖為基準,得到以下峰值數據:3397cm-1為O–H的伸縮振動峰,2926cm-1為C–H的反稱伸縮振動峰,1654cm-1為O–H面內彎曲振動峰,1157cm-1為C-O的伸縮振動峰,1030cm-1為C-O-C伸縮振動峰,無論是(β)CD-g-HEC水凝膠還是HEC水凝膠都存在相似的峰值,但當與β-CD和HEC的紅外光譜對比時發現它們的峰的強度和形狀都有所不同。例如,與β-CD和HEC的紅外光譜相比水凝膠的醚鍵的峰(1200和1000cm-1之間)變弱且變成寬峰,產生這種情況的原因是由于交聯反應的發生而導致其生成減少。1384cm-1附近的峰由于交聯反應之后OH基團和氫鍵的產生的而導致強度降低。而且,因為3000cm-1附近沒有檢測出峰的存在,所以可以確定在水凝膠中不存在游離的EPI。
(六)電鏡掃描分析
HEC水凝膠和(β)CD-g-HEC水凝膠冷凍干燥后經掃描電鏡所觀察到的表面形貌如圖7和8所示。
從通過電鏡掃描所得到的圖像中可以看出HEC水凝膠與(β)CD-g-HEC水凝膠的微觀結構是不同的,其中HEC水凝膠呈現出膠狀形態,而(β)CD-g-HEC水凝膠表面則呈現出鋒利的片狀結晶形態。這種鋒利的片狀結晶層是由HEC水凝膠表面上的β-CD結晶棒所形成的,而且與未加入β-環糊精的HEC水凝膠表面完全不同。因此進行了以下實驗:
將干燥的(β)CD-g-HEC水凝膠重新浸泡于去離子水中并且透析1天后,測得β-CD的重量損失為91.3%。這個實驗結果表明,大部分的β-CD是包裹于水凝膠中,而不是接枝于HEC鏈上。
為了減少β-CD經冷凍干燥后的損耗,對(β)CD-g-HEC水凝膠采用了60℃下強制空氣干燥。在經過空氣干燥后,將所得到的干燥產品浸于去離子水中,之后烘干,重復3次。結果顯示這三次烘干過程可以將β-CD的重量損失分別控制在15%,23%和27%。這意味著在60℃下對水凝膠進行強制空氣干燥可以保持水凝膠籠的結構以將β-CD包含其中。
(七)β-CD加入量對β-CD裝載效率的影響
(β)CD-g-HEC水凝膠籠中β-CD的裝載效率可由以下公式求得:
EPI加入量固定為12mL時β-CD的加入量對β-CD的裝載效率的影響的數據結果如表2所示。
表2不同的β-CD加入量下β-CD的裝載效率的數據結果
如表2所示,當加入8gβ-CD時β-CD的裝載效率的裝在效率最高,高達70.50%。從原子經濟性和β-CD的裝載量上考慮,HEC、EPI和β-CD的最合適的加入比例應為1g:6mL:4g,并且NaOH水溶液中NaOH的質量分數應控制在20%。
(八)(β)CD-g-HEC水凝膠和HEC水凝膠對酚酞的吸收與釋放分析
β-CD在溶液中可通過利用β-CD的空腔將酚酞分子的疏水基團包含其中的形式與酚酞形成包合物,并且使酚酞溶液明顯褪色,因此可以清楚的看到酚酞分子進入到了水凝膠中。
將水凝膠塊浸入酚酞/緩沖溶液中4天后,浸有(β)CD-g-HEC水凝膠塊的酚酞/緩沖溶液明顯褪色,然而浸有HEC水凝膠的酚酞/緩沖溶液無明顯變化。這一現象說明(β)CD-g-HEC水凝膠相比于HEC水凝膠可以吸收更多的酚酞,此外通過圖9(圖中◆表示(β)CD-g-HEC水凝膠,■表示HEC水凝膠)可以看出,(β)CD-g-HEC水凝膠相對于HEC水凝膠來說擁有更快的吸收速率并且在相同的時間下可以吸收更多的酚酞。
HEC水凝膠塊和(β)CD-g-HEC水凝膠塊在吸收完酚酞后所呈現出的顏色有所不同,HEC水凝膠塊整體完全變成深紅色,而(β)CD-g-HEC水凝膠塊只在邊緣呈現出淡淡的淺紫色,中心卻為無色透明。產生這種現象的原因是:第一,之所以(β)CD-g-HEC水凝膠塊中心為無色透明是因為當酚酞分子進入到(β)CD-g-HEC水凝膠中后它的疏水性基團被β-CD的空腔結構包含其中,這使酚酞分子的分子結構發生了一定的改變,使其不再顯現顏色;第二,其邊緣呈現出淡淡的淺紫色是因為在水凝膠塊被切割的過程中其邊緣的空間結構遭到破壞,所以當(β)CD-g-HEC水凝膠塊被放入酚酞/緩沖溶液中后,其邊緣的β-CD由于沒有了阻礙便被透析除去,這就導致了凝膠塊邊緣的酚酞分子不會再與β-CD形成包合物,而是僅僅被包裹在水凝膠的空間網狀結構中,酚酞分子也就因此保留了顯色特性。
隨著時間的推進水凝膠塊的酚酞分子累計釋放率百分比的變化如圖10所示(圖中◆表示HEC水凝膠,■表示(β)CD-g-HEC水凝膠),HEC水凝膠在一天之內就幾乎釋放出了所有的酚酞分子,與之相比,(β)CD-g-HEC水凝膠塊在相同的時間段僅釋放了10%的酚酞分子。并且4天后(β)CD-g-HEC水凝膠塊中還存有70%的酚酞分子。這一結果表明,實施例1所合成的(β)CD-g-HEC水凝膠不僅能夠大量包合客體分子,而且還可以對被包含其中的客體分子起到比較強的緩釋作用。
- 還沒有人留言評論。精彩留言會獲得點贊!