抗磷脂酰肌醇蛋白多糖?3的抗體及其應用的制作方法
本發明涉及腫瘤免疫治療或診斷領域,更具體地,涉及特異識別磷脂酰肌醇蛋白多糖-3(GPC3)的抗體及其應用。
背景技術:
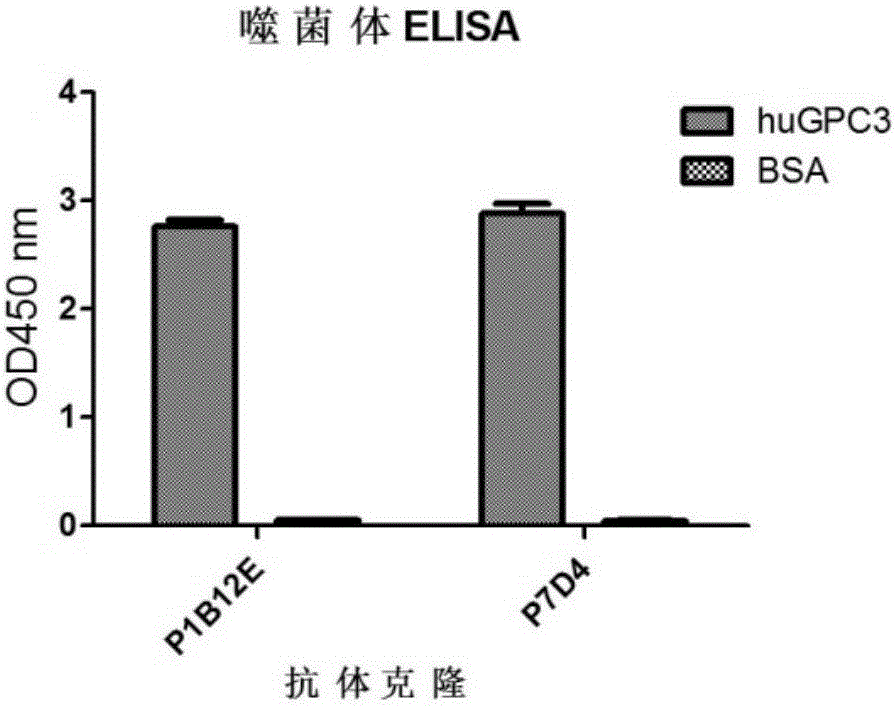
:目前,基于免疫效應細胞的過繼性免疫治療在部分腫瘤中取得了一定的效果,并且該種免疫治療方法可以克服抗體治療的上述缺陷,但在大多數腫瘤的療效仍不能令人滿意[GruppSA,etal.Adoptivecellulartherapy.CurrTopMicrobiolImmunol.,2011;344:149-72.]。近年來,根據細胞毒性T淋巴細胞(cytotoxiclymphocyte,CTL)對靶細胞的識別特異性依賴于T淋巴細胞受體(TCellReceptor,TCR)的發現,將針對腫瘤細胞相關抗原的抗體的scFv與T淋巴細胞受體的CD3ζ或FcεRIγ等胞內信號激活基序融合成嵌合抗原受體(Chimericantigenreceptor,CAR),并將其通過如慢病毒感染等方式基因修飾在T淋巴細胞表面。這種CART淋巴細胞能夠以主要組織兼容性復合物(MajorHistocompatibilityComplex,MHC)非限制性方式選擇性地將T淋巴細胞定向到腫瘤細胞并特異性地殺傷腫瘤。CART淋巴細胞是腫瘤免疫治療領域的一個新的免疫治療策略。設計CAR修飾的免疫效應細胞,特別T細胞時,所靶向的抗原基因實際上是一種關鍵性的選擇,鑒于體內基因表達的復雜性以及各種不可控因素,選擇到一個合適的用于CAR的基因是非常困難的。并且,很多腫瘤特異性的抗原,很難找到針對其的且適合于構建CAR修飾的免疫效應細胞的特異性分子。磷脂酰肌醇蛋白多糖-3(Glypican-3,GPC3,又稱DGSX,GTR2-2,MXR7,OCI-5,SDYS,SGB,SGBS或SGBS1)是一種細胞表面蛋白,屬于硫酸乙酰肝素蛋白多糖家族。GPC3基因編碼產生70-kDa左右的前體核心蛋白,該前體蛋白能夠被弗林蛋白酶(furin)剪切產生40-kDa左右的可溶性的能夠進入血液的氨基端(N末端)肽和30-kDa左右含有2個硫酸乙酰肝素(HS)糖鏈的膜結合的羧基端(C末端)肽。GPC3蛋白通過糖基磷脂酰肌醇(GPI)錨依附在細胞膜上。GPC3高度表達于胎兒肝臟,而不表達于正常成年人的肝組織,但在肝細胞肝癌中恢復表達,與肝癌的發生發展有十分密切的關系,不僅在肝癌發生的早期檢出率較高,而且隨著肝癌的發展,其檢出率也隨之增高。而GPC3的表達在肝腺癌,膽管細胞癌,肝轉移癌和12種常見實體瘤和21種非肝癌細胞系中均未檢測出。此外,GPC3也在例如黑色素瘤,卵巢透明細胞癌、卵黃囊瘤、神經母細胞瘤等腫瘤中表達。考慮到GPC3在肝細胞肝癌,黑色素瘤等腫瘤中特異性的高表達,其被認為是腫瘤免疫治療的一個候選靶標。雖然,利用抗GPC3抗體進行肝癌檢測和利用抗GPC3抗體的抗體依賴的(ADCC)或補體依賴的(CDC)細胞毒性研究方案已有報道,但目前仍沒有藥用的抗GPC3抗體,僅有中外制藥公司在CN200580000807.4公開的GC33抗體在進行一期臨床研究,臨床應用情況仍有待商榷。另外,抗GPC3抗體不僅可以直接作為治療性抗體,而且還有望用于診斷、嵌合抗原受體修飾(CAR)的T淋巴細胞等免疫治療等等。現有研究表明不同的抗體可能會有不同的免疫原性,這種免疫原性會導致抗體或其衍生出來的治療制劑的療效及副作用。如基于小鼠抗mesothelin抗體的CART細胞會導致過敏反應,影響其在人體內的長期存活。基于這些考慮,本領域需要進一步優化及制備新的抗GPC3抗體,使其實體瘤的應用中具有良好的腫瘤殺傷活性和極佳的臨床應用前景,從而使得GPC3抗體可以切實地被用于腫瘤的診斷和治療中,惠及廣大患者。技術實現要素:本發明的目的在于提供抗磷脂酰肌醇蛋白多糖-3的抗體及其應用。在本發明的第一方面,提供一種特異性識別磷脂酰肌醇蛋白多糖-3(GPC3)的抗體,該抗體具有輕鏈可變區和重鏈可變區,且,其輕鏈可變區的CDR1具有選自下組的氨基酸序列:SEQIDNO:16,SEQIDNO:67,SEQIDNO:69;其輕鏈可變區的CDR2具有選自下組的氨基酸序列:SEQIDNO:18,SEQIDNO:68,SEQIDNO:70;其輕鏈可變區的CDR3具有氨基酸序列:SEQIDNO:20;其重鏈可變區的CDR1具有選自下組的氨基酸序列:SEQIDNO:10,SEQIDNO:60,SEQIDNO:62,SEQIDNO:64;其重鏈可變區的CDR2具有選自下組的氨基酸序列:SEQIDNO:12,SEQIDNO:61,SEQIDNO:63,SEQIDNO:65,SEQIDNO:66,SEQIDNO:71;其重鏈可變區的CDR3具有選自下組的氨基酸序列:SEQIDNO:14,SEQIDNO:72。在一個優選例中,所述的抗體包括:抗體(a)(P7D4),其輕鏈可變區具有SEQIDNO:16所示的CDR1、SEQIDNO:18所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:10所示的CDR1、SEQIDNO:12所示的CDR2、SEQIDNO:14所示的CDR3;抗體(b)(am4),其輕鏈可變區具有SEQIDNO:16所示的CDR1、SEQIDNO:18所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:60所示的CDR1、SEQIDNO:61所示的CDR2、SEQIDNO:14所示的CDR3;抗體(c)(am14),其輕鏈可變區具有SEQIDNO:16所示的CDR1、SEQIDNO:18所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:62所示的CDR1、SEQIDNO:63所示的CDR2、SEQIDNO:14所示的CDR3;抗體(d)(am20),其輕鏈可變區具有SEQIDNO:16所示的CDR1、SEQIDNO:18所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:64所示的CDR1、SEQIDNO:65所示的CDR2、SEQIDNO:14所示的CDR3;抗體(e)(am35),其輕鏈可變區具有SEQIDNO:67所示的CDR1、SEQIDNO:68所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:10所示的CDR1、SEQIDNO:66所示的CDR2、SEQIDNO:14所示的CDR3;抗體(f)(am42),其輕鏈可變區具有SEQIDNO:69所示的CDR1、SEQIDNO:70所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:10所示的CDR1、SEQIDNO:66所示的CDR2、SEQIDNO:14所示的CDR3;抗體(g)(T2-23),其輕鏈可變區具有SEQIDNO:16所示的CDR1、SEQIDNO:70所示的CDR2、SEQIDNO:20所示的CDR3;或其重鏈可變區具有SEQIDNO:10所示的CDR1、SEQIDNO:71所示的CDR2、SEQIDNO:72所示的CDR3;抗體(h),其識別與(a)~(g)中任一項所述的抗體所識別的抗原決定部位相同的抗原決定部位。在另一優選例中,所述的特異性識別磷脂酰肌醇蛋白多糖-3(GPC3)的抗體可以是:單鏈抗體(scFV),單克隆抗體,結構域抗體,Fab片段,Fd片段,Fv片段,F(ab’)2片段和其衍生物,或其它形式的抗體;較佳地為單鏈抗體。在另一優選例中,所述的特異性識別磷脂酰肌醇蛋白多糖-3(GPC3)的抗體是人源化的或全人源的;較佳地為全人源的。在另一優選例中,抗體(a)(P7D4)的重鏈可變區的氨基酸序列如SEQIDNO:4中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:4中第137-247位所示;抗體(b)(am4)的重鏈可變區的氨基酸序列如SEQIDNO:25中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:25中第137-247位所示;抗體(c)(am14)的重鏈可變區的氨基酸序列如SEQIDNO:27中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:27中第137-247位所示;抗體(d)(am20)的重鏈可變區的氨基酸序列如SEQIDNO:29中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:29中第137-247位示;抗體(e)(am35)的重鏈可變區的氨基酸序列如SEQIDNO:31中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:31中第137-247位所示;抗體(f)(am42)的重鏈可變區的氨基酸序列如SEQIDNO:33中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:33中第137-247位所示;或抗體(g)(T2-23)的重鏈可變區的氨基酸序列如SEQIDNO:35中第1-121位所示;或所述的抗體的輕鏈可變區的氨基酸序列如SEQIDNO:35中第137-247位所示。在本發明的另一方面,提供一種特異性識別磷脂酰肌醇蛋白多糖-3(GPC3)的抗體,該抗體是人源化的單克隆抗體,含有重鏈可變區和輕鏈可變區,其重鏈可變區包含:SEQIDNO:73所示氨基酸序列的CDR1,SEQIDNO:74所示氨基酸序列的CDR2,SEQIDNO:75所示氨基酸序列的CDR3;或其輕鏈可變區包含:SEQIDNO:76所示氨基酸序列的CDR1,SEQIDNO:77所示氨基酸序列的CDR2,SEQIDNO:78所示氨基酸序列的CDR3。在一個優選例中,該抗體具有:SEQIDNO:58所示氨基酸序列的重鏈可變區,或SEQIDNO:59所示氨基酸序列的輕鏈可變區。在本發明的另一方面,提供編碼前面任一所述的抗體的核酸。在本發明的另一方面,提供一種表達載體,其包含所述的核酸。在本發明的另一方面,提供一種宿主細胞,其包含所述的表達載體或基因組中整合有所述的核酸。在本發明的另一方面,提供前面任一所述的抗體的用途,用于制備特異性靶向表達磷脂酰肌醇蛋白多糖-3的腫瘤細胞的靶向性藥物,抗體藥物偶聯物或多功能抗體;或用于制備診斷腫瘤的試劑,該腫瘤表達磷脂酰肌醇蛋白多糖-3;或用于制備嵌合抗原受體修飾的免疫細胞。在本發明的另一方面,提供一種多功能免疫輟合物,所述的多功能免疫輟合物包括:前面任一所述的抗體;以及與之連接(包括共價連接、偶聯、附著、吸附)的功能性分子;所述的功能性分子選自:靶向腫瘤表面標志物的分子,抑制腫瘤的分子,靶向免疫細胞的表面標志物的分子或可檢測標記物。在一個優選例中,所述的多功能免疫輟合物中,所述的靶向腫瘤表面標志物的分子是結合腫瘤表面標志物的抗體或配體;或所述的抑制腫瘤的分子是抗腫瘤的細胞因子或抗腫瘤的毒素;較佳地,所述的細胞因子包括(但不限于):IL-12、IL-15、IFN-beta、TNF-alpha。在另一優選例中,所述的多功能免疫輟合物中,所述的可檢測標記物包括:熒光標記物、顯色標記物。在另一優選例中,所述的多功能免疫輟合物中,所述的結合腫瘤表面標志物的抗體是指:識別磷脂酰肌醇蛋白多糖-3以外的其它抗原的抗體,所述的其它抗原包括:EGFR,EGFRvIII,mesothelin,HER2,EphA2,Her3,EpCAM,MUC1,MUC16,CEA,Claudin18.2,葉酸受體,Claudin6,WT1,NY-ESO-1,MAGE3,ASGPR1或CDH16。在另一優選例中,所述的多功能免疫輟合物中,所述的靶向免疫細胞的表面標志物的分子是結合T細胞表面標志物的抗體,其與前面任一所述的抗體形成T細胞參與的雙功能抗體(BispecificTcellengager,BiTE)。在另一優選例中,所述的多功能免疫輟合物中,所述的結合免疫細胞表面標志物的抗體是抗CD3抗體。在另一優選例中,所述的抗CD3抗體是單鏈抗體(scFV),單克隆抗體,Fab片段,Fd片段,Fv片段,F(ab’)2片段和其衍生物,或其它形式的抗體;較佳地為單鏈抗體。在另一優選例中,所述的抗CD3抗體是人源化的,嵌合的,全人源的或鼠源的。在另一優選例中,所述的多功能免疫輟合物是融合多肽,前面任一所述的抗體以及與之連接的功能性分子之間,還包括連接肽(接頭)。在另一優選例中,所述的連接肽的序列為(GlyGlyGlyGlySer)n,其中n為1到5的整數;更佳地,n=3。在另一優選例中,所述的多功能免疫輟合物采用多肽給藥或基因給藥的方式。在本發明的另一方面,提供編碼前面任一所述的多功能免疫輟合物的核酸。在本發明的另一方面,提供所述的多功能免疫輟合物的用途,用于制備抗腫瘤藥物,或用于制備診斷腫瘤的試劑,該腫瘤表達磷脂酰肌醇蛋白多糖-3;或用于制備嵌合抗原受體修飾的免疫細胞;較佳地,所述免疫細胞包括:T淋巴細胞、NK細胞或者NKT淋巴細胞。在本發明的另一方面,提供包含前面任一所述的抗體的嵌合抗原受體(Chimericantigenreceptor,CAR),所述的嵌合抗原受體包含順序連接的:前面任一所述的抗體,跨膜區和胞內信號區;所述的胞內信號區選自:CD3ζ,FcεRIγ,CD27,CD28,CD137,CD134,MyD88,CD40的胞內信號區序列,或其組合。在另一優選例中,所述的嵌合抗原受體中,所述的跨膜區包含CD8或CD28的跨膜區。在另一優選例中,所述的嵌合抗原受體中,所述的嵌合抗原受體包括如下的順序連接的抗體,跨膜區和胞內信號區:前面任一所述的抗體、CD8和CD3ζ;前面任一所述的抗體、CD8、CD137和CD3ζ;前面任一所述的抗體、CD28分子的跨膜區、CD28分子的胞內信號區和CD3ζ;或前面任一所述的抗體、CD28分子的跨膜區、CD28分子的胞內信號區、CD137和CD3ζ。在另一優選例中,所述的嵌合抗原受體中,所述的抗體是單鏈抗體或結構域抗體。在另一優選例中,所述的嵌合抗原受體具有:SEQIDNO:49或其中第22-346位所示的氨基酸序列;SEQIDNO:50或其中第22-447位所示的氨基酸序列;SEQIDNO:51或其中第22-491位所示的氨基酸序列;SEQIDNO:52或其中第22-494位所示的氨基酸序列;SEQIDNO:53或其中第22-536位所示的氨基酸序列;SEQIDNO:85所示的氨基酸序列;SEQIDNO:86所示的氨基酸序列;或SEQIDNO:87所示的氨基酸序列。在本發明的另一方面,提供編碼所述的嵌合抗原受體的核酸。在另一優選例中,編碼所述的嵌合抗原受體的核酸具有:SEQIDNO:44或其中第380-1420位或其中第443-1420位所述的核苷酸序列;SEQIDNO:45或其中第380-1723位或其中第443-1723位所述的核苷酸序列;SEQIDNO:46或其中第380-1855位或其中第443-1855位所述的核苷酸序列;SEQIDNO:47或其中第380-1864位或其中第443-1864位所述的核苷酸序列;SEQIDNO:48或其中第380-1990位或其中第443-1990位所述的核苷酸序列;SEQIDNO:85所述的核苷酸序列;SEQIDNO:87所述的核苷酸序列;或SEQIDNO:89所述的核苷酸序列。在本發明的另一方面,提供一種表達載體,其包含編碼所述的嵌合抗原受體的核酸。在另一優選例中,所述的表達載體來源于慢病毒質粒pWPT(或pWPT-eGFP)。在本發明的另一方面,提供一種病毒,所述的病毒包含所述載體。所述的嵌合抗原受體、或編碼其的核酸、或包含該核酸的表達載體或病毒的用途,用于制備靶向表達磷脂酰肌醇蛋白多糖-3的腫瘤的基因修飾的免疫細胞。在另一優選例中,所述的表達磷脂酰肌醇蛋白多糖-3的腫瘤包括(但不限于):肝癌,黑色素瘤,卵巢透明細胞癌、卵黃囊瘤、神經母細胞瘤。在本發明的另一方面,提供一種基因修飾的免疫細胞,其轉導有編碼所述的嵌合抗原受體的核酸,或含有該核酸的表達載體或病毒;或其表面表達所述的嵌合抗原受體。在另一優選例中,所述的免疫細胞還攜帶外源的細胞因子的編碼序列;較佳地,所述的細胞因子包括:IL-12,IL-15或IL-21。在另一優選例中,所述的免疫細胞還表達另一種嵌合抗原受體,該受體不含有CD3ζ,但含有CD28的胞內信號結構域、CD137的胞內信號結構域或者這兩者的組合。在另一優選例中,所述的免疫細胞還表達趨化因子受體;較佳地,所述的趨化因子受體包括:CCR2。在另一優選例中,所述的免疫細胞還表達能降低PD-1表達的siRNA或者阻斷PD-L1的蛋白。在另一優選例中,所述的免疫細胞還表達安全開關;較佳地,所述的安全開關包括:iCaspase-9,TruancatedEGFR或RQR8。在另一優選例中,所述的免疫細胞包括:T淋巴細胞,NK細胞或NKT細胞。在本發明的另一方面,提供所述的基因修飾的免疫細胞的用途,用于制備抑制腫瘤的藥物,所述的腫瘤是表達磷脂酰肌醇蛋白多糖-3的腫瘤。在本發明的另一方面,提供藥物組合物(包括藥物或診斷試劑),其包括:前面任一所述的抗體或編碼該抗體的核酸;或前面任一所述的免疫輟合物或編碼該輟合物的核酸;或前面任一所述的嵌合抗原受體或編碼該嵌合抗原受體的核酸;或前面任一所述的基因修飾的免疫細胞。本發明的其它方面由于本文的公開內容,對本領域的技術人員而言是顯而易見的。附圖說明圖1、在單噬菌體ELISA實驗中抗體P1B12E和P7D4對人類GPC3和對照BSA的結合情況。抗體P1B12E和P7D4對人類GPC3和陰性對照BSA的值證明篩選到的兩個抗體能特異性結合人類GPC3。圖2、人類GPC3的抗體純化電泳圖。圖3、抗體scFv-P1B12E-Fc和scFv-P7D4-Fc對GPC3表達陽性的HepG2細胞結合活性分析。圖4、P7D4系列抗體對GPC3結合能力的SPR分析。圖5、P7D4系列抗體特異性結合重組人GPC3。圖6、表達純化的GPC3蛋白的SDSPAGE電泳鑒定。圖7、抗體Y035對人GPC3的結合動力學分析。圖8、抗體5A5對人GPC3的結合動力學分析。圖9、抗體Y035特異性結合GPC3表達陽性的HepG細胞。具體實施方式本發明人經過深入的研究篩選,獲得了特異性識別GPC3的抗體,包括單鏈抗體和人源化抗體。本發明的抗體可以被應用于制備各種靶向性抗腫瘤藥物以及診斷腫瘤的藥物。抗GPC3抗體本發明人從全人源天然抗體庫中篩選獲得對于GPC3結合性能良好的特異性抗體,進一步還對其進行氨基酸突變獲得了親和力進一步呈現顯著性提高的抗GPC3抗體,并且找到了其發揮結合性能的關鍵CDR區。本發明人還利用雜交瘤技術獲得了抗GPC3的鼠源抗體,對其進行人源化,經過反復比較,獲得對于GPC3結合性能極其優異的人源化抗GPC3抗體,并且找到了其發揮結合性能的關鍵CDR區。本發明的抗體可以是完整的免疫球蛋白分子,也可以是抗原結合片段,包括但不限于Fab片段,Fd片段,Fv片段,F(ab’)2片段、互補決定區(CDR)片段、單鏈抗體(scFv)、結構域抗體,二價單鏈抗體、單鏈噬菌體抗體、雙特異雙鏈抗體、三鏈抗體、四鏈抗體。抗體的抗原結合特性可由位于重鏈和輕鏈可變區的3個特定的區域來描述,稱為互補決定區(complementaritydeterminingregion,CDR),所述的CDR區將可變區間隔成4個框架區域(FR),4個FR的氨基酸序列相對比較保守,不直接參與結合反應。這些CDR形成環狀結構,通過其間的FR形成的β折疊在空間結構上相互靠近,重鏈上的CDR和相應輕鏈上的CDR構成了抗體的抗原結合位點。可以通過比較同類型的抗體的氨基酸序列來確定是哪些氨基酸構成了FR或CDR區域。CDR區是免疫學感興趣的蛋白質的序列,本發明的抗體的CDR區是全新的。所述抗體可包含本文揭示的二、三、四、五或者所有六個CDR區。本發明的另一方面包括本文所述抗體的功能變體。所述變體能與親代抗體競爭特異性結合GPC3,且其識別腫瘤細胞表達的GPC3的能力接近于本發明實施例中提供的具體的抗體。所述功能變體可以具有保守序列修飾,包括核苷酸和氨基酸取代、添加和缺失。這些修飾可以通過本領域己知的標準技術導入,例如定向誘變和隨機PCR介導的誘變,并且可包含天然以及非天然核苷酸和氨基酸。較佳地,序列的修飾發生在所述抗體的CDR區以外的區域上。免疫輟合物本發明還提供了多功能免疫綴合物,其包含本文所述抗體以及進一步包含至少一種其它類型的功能性分子。所述的功能性分子選自但不限于:靶向腫瘤表面標志物的分子,抑制腫瘤的分子,靶向免疫細胞的表面標志物的分子或可檢測標記物。所述抗體與所述功能性分子可以通過共價連接、偶聯、附著、交聯等方式構成輟合物。作為一種優選方式,所述免疫綴合物可包含:本發明的抗體以及至少一種靶向腫瘤表面標志物的分子或抑制腫瘤的分子。所述的抑制腫瘤的分子可以是抗腫瘤的細胞因子,或抗腫瘤的毒素;較佳地,所述的細胞因子包括(但不限于):IL-12、IL-15、IFN-beta、TNF-alpha。所述的靶向腫瘤表面標志物的分子例如可以與本發明的抗體協同作用,更精準地靶向腫瘤細胞。作為一種優選方式,所述免疫綴合物可包含:本發明的抗體以及可檢測標記物。所述的可檢測標記物包括但不限于:熒光標記物、顯色標記物;如:酶、輔基、熒光材料、發光材料,生物發光材料、放射性材料、正電子發射金屬以及非放射性順磁性金屬離子。也可包含一個以上的標記物。為了檢測和/或分析和/或診斷目的用于標記抗體的標記依賴于使用的特定檢測/分析/診斷技術和/或方法例如免疫組織化學染色(組織)樣品、流式細胞計量術等。對于本領域已知的檢測/分析/診斷技術和/或方法合適的標記為本領域技術人員所熟知。作為一種優選方式,所述免疫綴合物可包含:本發明的抗體以及靶向免疫細胞的表面標志物的分子。所述靶向免疫細胞的表面標志物的分子可識別免疫細胞,其攜帶本發明的抗體達到免疫細胞,同時本發明的抗體可將免疫細胞靶向于腫瘤細胞,從而引發免疫細胞特異性地殺傷腫瘤。作為通過直接或間接(例如通過接頭)綴合而化學產生免疫綴合物的一種方式,所述免疫綴合物可以作為融合蛋白而產生,所述融合蛋白包含本發明的抗體及合適的其它蛋白。融合蛋白可以通過本領域已知方法產生,例如通過構建核酸分子以及隨后表達所述核酸分子而重組產生,所述核酸分子包含符合讀框的編碼抗體的核苷酸序列以及編碼合適標記的核苷酸序列。本發明另一方面提供了編碼本發明的至少一種抗體、其功能變體或者免疫綴合物的核酸分子。一旦獲得了有關的序列,就可以用重組法來大批量地獲得有關序列。這通常是將其克隆入載體,再轉入細胞,然后通過常規方法從增殖后的宿主細胞中分離得到有關序列。本發明還涉及包含上述的適當DNA序列以及適當啟動子或者控制序列的載體。這些載體可以用于轉化適當的宿主細胞,以使其能夠表達蛋白質。宿主細胞可以是原核細胞,如細菌細胞;或是低等真核細胞,如酵母細胞;或是高等真核細胞,如哺乳動物細胞。嵌合抗原受體及基因修飾的免疫細胞本發明提供了一種表達于免疫效應細胞(免疫細胞)表面的嵌合抗原受體,所述的嵌合抗原受體包含順序連接的:胞外結合區,跨膜區和胞內信號區,其中所述胞外結合區包含本發明的抗體。將該嵌合抗原受體表達于免疫效應細胞的表面,可使得免疫效應細胞對表GPC3的腫瘤細胞具有高度特異性的細胞毒性作用。如本文所用,所述的“免疫細胞”與“免疫效應細胞”可互換使用,其包括:T淋巴細胞,NK細胞或NKT細胞等,優選的,為NK細胞和T淋巴細胞。作為本發明的優選方式,所述的嵌合抗原受體中,包含的抗體為單鏈抗體,其通過CD8鉸鏈區與CD8或者CD28的跨膜區相連接,跨膜區后緊接胞內信號區。本發明也包括編碼所述嵌合抗原受體的核酸。本發明還涉及上述多核苷酸的變異體,其編碼與本發明有相同的氨基酸序列的多肽或多肽的片段、類似物和衍生物。嵌合抗原受體的跨膜區可以選自CD8或CD28等蛋白的跨膜區。人CD8蛋白是個異二聚體,由αβ或者γδ兩條鏈組成。在本發明的一個實施方案中,跨膜區選自CD8α或者CD28的跨膜區。此外,CD8α鉸鏈區(hinge)是一個柔性區域,因此,CD8或CD28和跨膜區加上鉸鏈區被用于將嵌合抗原受體CAR的靶點識別結構域scFv和胞內信號區連接起來。胞內信號區可以選自CD3ζ,FcεRIγ,CD27,CD28,CD137,CD134,MyD88,CD4蛋白的胞內信號區,及其組合。CD3分子由五個亞單位組成,其中CD3ζ亞單位(又稱CD3zeta,簡稱Z)含有3個ITAM基序,該基序是TCR-CD3復合體中重要的信號轉導區。CD3δZ是截短的不具有ITAM基序的CD3ζ序列,在實踐中一般作為陰性對照的構建。FcεRIγ主要分布在肥大細胞和嗜堿性粒細胞表面,其含有一個ITAM基序,在結構、分布及功能上與CD3ζ類似。此外如前所述,CD28,CD137,CD134是共刺激信號分子,在與各自配體結合后其胞內信號區段產生的共刺激作用引起免疫效應細胞(主要是T淋巴細胞)的持續增殖,并能夠提高免疫效應細胞分泌IL-2和IFN-γ等細胞因子的水平,同時提高CAR免疫效應細胞在體內的存活周期和抗腫瘤效果。本發明的嵌合抗原受體可以按如下方式順序連接:本發明的抗體、CD8和CD3ζ;本發明的抗體、CD8、CD137和CD3ζ;本發明的抗體、CD28分子的跨膜區、CD28分子的胞內信號區和CD3ζ;或本發明的抗體、CD28分子的跨膜區、CD28分子的胞內信號區、CD137和CD3ζ。及其組合,其中相關嵌合抗原受體蛋白中CD28a代表CD28分子的跨膜區,CD28b代表CD28分子的胞內信號區。上述各種嵌合抗原受體統稱為scFv(GPC3)-CAR。本發明還提供了包含上述編碼表達于免疫效應細胞表面的嵌合抗原受體蛋白的核酸的載體。在一個具體實施方案中,本發明使用的載體是一種慢病毒質粒載體pWPT-eGFP。該質粒屬于第三代自滅活慢病毒載體系統,該系統共有三個質粒即編碼蛋白Gag/Pol、編碼Rev蛋白的包裝質粒psPAX2;編碼VSV-G蛋白的包膜質粒PMD2.G;及空載體pWPT-eGFP,其可以用于重組引入目的核酸序列,即編碼CAR的核酸序列。空載體pWPT-eGFP中由延長因子-1α(elongationfactor-1α,EF-1α)啟動子調控增強型綠色熒光蛋白(enhancedgreenfluorescentprotein,eGFP)的表達。而包含編碼CAR的目的核酸序列的重組表達載體pWPT-eGFP-F2A-CAR是通過由來自口蹄疫病毒(food-and-mouthdiseasevirus,FMDV)的核糖體跳躍序列(ribosomalskippingsequence2A)(簡稱F2A)實現eGFP與CAR的共表達的。本發明還包括包含上述載體的病毒。本發明的病毒包括包裝后的具有感染力的病毒,也包括包含包裝為具有感染力的病毒所必需成分的待包裝的病毒。本領域內已知的其它可用于將外源基因轉導入免疫效應細胞的病毒及其對應的質粒載體也可用于本發明。本發明還提供了基因修飾的免疫效應細胞,其被轉導有本發明的核酸或被轉導有本發明的上述包含所述含有該核酸的重組質粒,或包含該質粒的病毒。本領域常規的核酸轉導方法,包括非病毒和病毒的轉導方法都可以用于本發明。基于非病毒的轉導方法包括電穿孔法和轉座子法。近期Amaxa公司研發的Nucleofector核轉染儀能夠直接將外源基因導入細胞核獲得目的基因的高效轉導。另外,基于睡美人轉座子(SleepingBeautysystem)或PiggyBac轉座子等轉座子系統的轉導效率較普通電穿孔有較大提高,將nucleofector轉染儀與睡美人轉座子系統聯合應用已有報道[DaviesJK.,etal.CombiningCD19redirectionandalloanergizationtogeneratetumor-specifichumanTcellsforallogeneiccelltherapyofB-cellmalignancies.CancerRes,2010,70(10):OF1-10.],該方法既具有較高的轉導效率又能夠實現目的基因的定點整合。在本發明的一個實施方案中,實現嵌合抗原受體基因修飾的免疫效應細胞的轉導方法是基于病毒如逆轉錄病毒或慢病毒的轉導方法。該方法具有轉導效率高,外源基因能夠穩定表達,且可以縮短體外培養免疫效應細胞到達臨床級數量的時間等優點。在該轉基因免疫效應細胞表面,轉導的核酸通過轉錄、翻譯表達在其表面。通過對各種不同的培養的腫瘤細胞進行體外細胞毒實驗證明,本發明的免疫效應細胞具有高度特異性的腫瘤細胞殺傷效果(亦稱細胞毒性)。因此本發明的編碼嵌合抗原受體蛋白的核酸,包含該核酸的質粒,包含該質粒的病毒和轉導有上述核酸,質粒或病毒的轉基因免疫效應細胞可以有效地用于腫瘤的免疫治療。本發明所述的免疫細胞還可以攜帶外源的細胞因子的編碼序列;所述的細胞因子包括但不限于:IL-12,IL-15或IL-21等。這些細胞因子具有免疫調節或抗腫瘤的活性,能增強效應T細胞及活化的NK細胞的功能,或直接發揮抗腫瘤作用。因此,本領域技術人員可以理解,這些細胞因子的運用有助于所述的免疫細胞更好地發揮作用。本發明所述的免疫細胞還可以表達除了上述嵌合抗原受體以外的另一種嵌合抗原受體,該受體不含有CD3ζ,但含有CD28的胞內信號結構域、CD137的胞內信號結構域或者這兩者的組合。本發明所述的免疫細胞還可以表達趨化因子受體;所述的趨化因子受體包括但不限于CCR2。本領域技術人員可以理解,所述的CCR2趨化因子受體可以使得體內的CCR2與之競爭性結合,對于阻斷腫瘤的轉移是有利的。本發明所述的免疫細胞還可以表達能降低PD-1表達的siRNA或者阻斷PD-L1的蛋白。本領域技術人員可以理解,競爭性阻斷PD-L1與其受體PD-1的相互作用,有利于恢復抗腫瘤T細胞反應,從而抑制腫瘤生長。本發明所述的免疫細胞還可以表達安全開關;較佳地,所述的安全開關包括:iCaspase-9,TruancatedEGFR或RQR8。藥物組合物本發明的抗體、包含該抗體的免疫輟合物以及基因修飾的免疫細胞可以應用于制備藥物組合物或診斷試劑。所述的組合物除了包括有效量的所述抗體、免疫輟合物或免疫細胞,還可包含藥學上可接受的載體。術語“藥學上可接受的”是指當分子本體和組合物適當地給予動物或人時,它們不會產生不利的、過敏的或其它不良反應。可作為藥學上可接受的載體或其組分的一些物質的具體例子是糖類,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纖維素及其衍生物,如羧甲基纖維素鈉、乙基纖維素和甲基纖維素;西黃蓍膠粉末;麥芽;明膠;滑石;固體潤滑劑,如硬脂酸和硬脂酸鎂;硫酸鈣;植物油,如花生油、棉籽油、芝麻油、橄欖油、玉米油和可可油;多元醇,如丙二醇、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化劑,如潤濕劑,如月桂基硫酸鈉;著色劑;調味劑;壓片劑、穩定劑;抗氧化劑;防腐劑;無熱原水;等滲鹽溶液;和磷酸鹽緩沖液等。本發明的組合物可根據需要制成各種劑型,并可由醫師根據患者種類、年齡、體重和大致疾病狀況、給藥方式等因素確定對病人有益的劑量進行施用。給藥方式例如可以采用注射或其它治療方式。下面結合具體實施例,進一步闡述本發明。應理解,這些實施例僅用于說明本發明而不用于限制本發明的范圍。下列實施例中未注明具體條件的實驗方法,通常按照常規條件如J.薩姆布魯克等編著,分子克隆實驗指南,第三版,科學出版社,2002中所述的條件,或按照制造廠商所建議的條件。實施例1、結合人類GPC3的特異性單鏈抗體(scFv)的制備1.1基于噬菌體展示的GPC3特異性結合抗體的篩選利用噬菌體展示技術,從全人源天然抗體庫中篩選人類GPC3(以下簡稱huGPC3)特異性抗體。為此目的,在400ml2×YT/氨芐青霉素培養基接種噬菌體展示全人源單鏈抗體天然庫的甘油菌(購自上海銳勁生物技術有限公司),使細胞密度達到OD600=0.1,在37℃和200rpm條件下振蕩培養直至細胞密度達到OD600=0.5。用1012pfu的M13KO7輔助噬菌體(購自Invitrogen)感染,在30℃和50rpm條件下培養30分鐘。加入50mg/L卡那霉素后在37℃和200rpm條件下振蕩培養30分鐘后,通過離心(15分鐘,1600×g,4℃)分離沉淀,重懸于400ml2×YT/氨芐青霉素/卡那霉素培養基,在37℃和200rpm條件下振蕩培養16小時。最后細胞通過離心(20分鐘,5000×g,4℃)分離沉淀并丟棄,上清用0.45μm規格濾膜過濾后,加入1/4體積20%(w/v)PEG8000、2.5MNaCl溶液并在冰浴中保溫1小時沉淀噬菌體顆粒。隨后離心沉淀(20分鐘,8000×g,4℃),棄上清,將噬菌體重懸于25ml預冷PBS(137mMNaCl,2.7mMKCl,8mMNa2HPO4,2mMKH2PO4)中,離心(5分鐘,20000×g,4℃)。向上清液加入1/4體積20%(w/v)PEG8000、2.5MNaCl溶液,并冰浴30分鐘再次沉淀噬菌體顆粒。離心沉淀(30分鐘,20000×g,4℃),再次將噬菌體沉淀重懸于2ml預冷PBS中,在冰上保持30分鐘并離心(30分鐘,17000×g,4℃)。上清液與含4%(w/v)BSA的PBS溶液以1:1混合,置于旋轉混合器上,室溫下保溫30分鐘,然后直接用于篩選。利用上述噬菌體抗體庫,針對生物素標記的人類GPC3重組蛋白(購自上海銳勁生物技術有限公司),實施了四輪定向篩選,篩選方案如下:該噬菌體抗體庫與生物素標記的抗原GPC3,在室溫下保溫2小時,然后與經封閉液2%(w/v)BSA(牛血清白蛋白,購自上海生工)封閉過的鏈霉親和素磁珠MyOneC1(購自Invitrogen)在室溫下保溫30分鐘。隨后用PBST(含0.1%吐溫-20)緩沖液洗滌磁珠,除去非特異性結合或結合能力較弱的噬菌體。結合能力強的噬菌體,則用甘氨酸-鹽酸(pH2.2)從磁珠上洗脫下來,用Tris中和液(pH9.1)中和后,用于感染處于對數生長中期的大腸桿菌ER2738,并被用于下一輪篩選。在四輪篩選中,磁珠的用量分別為50μl、20μl、10μl和10μl,生物素標記的抗原GPC3濃度分別為200nM、10nM、5nM和1nM,PBST的洗滌次數分別為10次、10次、15次和20次。1.2GPC3特異性結合抗體的鑒定從第四輪篩選所得的克隆中隨機挑選96個,并用單噬菌體ELISA(酶聯免疫吸附實驗)分析其與人類GPC3的結合能力。為此目的,每個單菌落接種300μl2×YT/氨芐青霉素培養基(含2%葡萄糖)于96孔深孔培養板,并在37℃和250rpm下振蕩培養16小時。用20μl培養物接種到500μl2×YT/氨芐青霉素培養基(含0.1%葡萄糖),在37℃和250rpm下振蕩培養1.5小時。準備輔助噬菌體溶液,取75μl的M13KO7(滴度為3×1012pfu/ml)混入到15ml2×YT培養基中,50μl/孔加到培養板中。在37℃和150rpm條件培養30分鐘,然后加入準備好的卡那霉素溶液50μl/孔(取180μl的50mg/ml卡那霉素,加入到15ml2×YT培養基),在37℃和250rpm下振蕩培養16小時。最后離心沉淀細胞(30分鐘,5000×g,4℃),上清轉移到新的96孔深孔培養板。為進行單噬菌體ELISA,在96孔MediSorpELISA板(購自Nunc)上分別使用100ng/孔抗原GPC3以及陰性對照蛋白BSA(100μl/孔),在4℃包被過夜。每個孔用含2%BSA(w/v)的PBST封閉。隨后用PBST清洗孔三次并排凈。然后加入100μl/孔上面制備的每種噬菌體溶液到板上各孔中。37℃保溫2小時后,用PBST洗滌三次。為了檢測結合的噬菌體,將抗M13抗體過氧化物歧化酶偶聯物(購自GEHealthcare)以1:5000稀釋于PBST中,并取100μl加到每個孔中。37℃保溫1小時后用PBST漂洗孔三次,然后用PBS漂洗三次。最后吸取50μlTMB底物加入到孔中,并在室溫下顯色10分鐘,隨后加入每孔50μl的2MH2SO4終止顯色反應。用酶聯免疫檢測儀(Bio-Rad)在450nm測量消光值。結合測序分析,觀察到兩個不同的單鏈抗體P1B12E(SEQIDNO:1(核苷酸),2(氨基酸))和P7D4(SEQIDNO:3(核苷酸),4(氨基酸)),在ELISA實驗中對人類GPC3(huGPC3)結合信號顯著較強,對BSA沒有結合(圖1)。實施例2、抗GPC3的單鏈抗體的表達和純化根據標準方案,使用引物對V5-P1B12E-F(SEQIDNO:5)和V5-P1B12E-R(SEQIDNO:6)從篩選得到的克隆P1B12E的質粒(pCantab5E-P1B12E)中擴增出scFv-P1B12E片段,使用引物對V5-P7D4-F(SEQIDNO:7)和V5-P7D4-R(SEQIDNO:8)從篩選得到的克隆P7D4的質粒(pCantab5E-P7D4)擴增出scFv-P7D4片段,通過NheI/BamHI(購自NEB)雙酶切,以T4DNA連接酶(購自NEB)于同樣以NheI/BamHI雙酶切載體質粒pCMV-V5-Fc(該載體在多克隆位點下游融合表達人抗體IgG1的Fc片段,以下簡稱V5-Fc,購自上海銳勁生物技術有限公司)連接并轉化于宿主菌TOP10中,挑取克隆通過PCR鑒定陽性克隆并通過測序確認,分別獲得V5-scFv-P1B12E-Fc和V5-scFv-P7D4-Fc真核表達質粒。將上述表達質粒分別轉染生長良好的HEK-293F細胞,37℃,5%CO2,125rpm搖床連續培養7天,4000rpm離心10min,去除沉淀,收集上清,并用0.45μm濾膜過濾,將處理好的樣品以proteinA(購自GE)親和柱進行親和純化,最終獲得純化的抗體-Fc融合蛋白scFv-P1B12E-Fc和scFv-P7D4-Fc,鑒定結果如圖2所示,其分子量在50kD左右。實施例3、流式細胞學分析各個細胞系與抗GPC3單鏈抗體的結合情況通過熒光激活細胞分選儀(FACS)(BD公司,FACSCalibur)分析抗體scFv-P1B12E-Fc和scFv-P7D4-Fc各自與GPC3陽性的肝癌HepG2細胞系(ATCC)的結合能力。具體方法如下:1).取對數生長期的肝癌HepG2細胞系接種到6cm平皿中,接種細胞密度約為90%,37℃孵箱過夜培養。2).使用10mM的EDTA消化細胞,200g×5min離心收集細胞。以1×106~1×107/mL的濃度重懸于1%含小牛血清的磷酸鹽緩沖液(NBSPBS)中,按100ul/管的量加入流式專用管中。3).200g×5min離心,棄上清。4).分別加入待測抗體scFv-P1B12E-Fc和scFv-P7D4-Fc,同時以PBS作為陰性對照,抗體終濃度為10μg/ml,每管加入100ul。冰浴,45分鐘。5).每管加入2ml1%NBSPBS,以200g×5min離心,共二遍。6).棄上清,加入1:50稀釋的FITC熒光標記的羊抗人抗體(來自上海康成生物工程有限公司),每管加入100ul。冰浴,45分鐘。7).每管加入2ml1%NBSPBS,以200g×5min離心,共二遍。8).棄上清,重懸于300ul1%NBSPBS中,流式細胞儀檢測。9).應用流式細胞儀數據分析軟件WinMDI2.9分析數據。結果如圖3,流式細胞分析結果表明,抗體scFv-P7D4-Fc可以特異識別表達GPC3的HepG2細胞,抗體scFv-P1B12E-Fc與HepG2細胞不結合。實施例4、GPC3結合能力提高的P7D4單鏈抗體變體的篩選和制備為提高P7D4單鏈抗體對GPC3結合能力,分別對其重鏈CDR1和CDR2區域、或者輕鏈CDR1和CDR2的部分氨基酸進行隨機突變,并構建對應的親和力成熟文庫H12和L12。4.1、P7D4輕鏈和重鏈及其CDR區P7D4scFv核苷酸序列如下(SEQIDNO:3;其中,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列,第364-408位為(Gly4Ser)3連接序列)。P7D4scFv氨基酸序列如下(SEQIDNO:4):P7D4VHCDR1:核苷酸序列:GGATTCACCTTCAGTAGCTATGCTATGCAC(SEQIDNO:9);氨基酸序列:GFTFSSYAMH(SEQIDNO:10)。P7D4VHCDR2:核苷酸序列:gctattagtggtagtggtggtagcacatactacgcagactccgtgaagggc(SEQIDNO:11);氨基酸序列:AISGSGGSTYYADSVKG(SEQIDNO:12)。P7D4VHCDR3:核苷酸序列:gatcgacgagggagccacgctgatgcttttgatgtc(SEQIDNO:13);氨基酸序列:DRRGSHADAFDV(SEQIDNO:14)。P7D4VLCDR1:核苷酸序列:actggaaccagcagtgacgttggtggttataactatgtctcc(SEQIDNO:15);氨基酸序列:TGTSSDVGGYNYVS(SEQIDNO:16)。P7D4VLCDR2:核苷酸序列:ggtaacagcaatcggccctca(SEQIDNO:17);氨基酸序列:GNSNRPS(SEQIDNO:18)。P7D4VLCDR3:核苷酸序列:cagtcctatgacagcagcctgcgtgtggta(SEQIDNO:19);氨基酸序列:QSYDSSLRVV(SEQIDNO:20)。4.2、H12親和力成熟庫的構建通過對P7D4單鏈抗體進行序列比對和分析,P7D4重鏈第一個和第二個CDR區域的部分氨基酸被選定,通過引物引入隨機化突變,用于構建重鏈親和力成熟文庫。為制備編碼P7D4突變體文庫的DNA片段,以質粒pCantab5E-P7D4為模板,通過PCR方法分別得到兩段DNA片段,隨后通過搭橋PCR的方式拼接而成。具體使用以下操作步驟:為合成基因,在50μl體積中進行PCR反應,每個反應使用質粒pCantab5E-P7D4作為模板,每條引物的終濃度為0.2μM,以及5μl10×KODPlus緩沖液、4μldNTPs(dATP、dCTP、dGTP和dTTP,每種2mM)、2μl25mMMgSO4和1UKODPlus(購自Takara),用水補足體積后,在熱循環儀中開始PCR程序。反應先加熱樣品到94℃預變性5分鐘,然后保溫25個循環,每個循環是94℃30秒、56℃30秒和68℃30秒。最后在68℃保溫10分鐘。第一個片段的擴增利用引物S1(SEQIDNO:21,CAACGTGAAAAAATTATTATTCGC)和74H12F1r(SEQIDNO:22,CCAGCCCCTTGCCTGGAGCCTGGCGGACCCAMNNCATAGCATAMNNACTGAAGGTGAATCCAG),第二個片段利用引物74H12F2f(SEQIDNO:23,GCTCCAGGCAAGGGGCTGGAGTGGGTCTCANNKATTAGTNNKNNKGNTNNKNNKACATACTACGCAGACTCC)和S6(SEQIDNO:21,GTAAATGAATTTTCTGTATGAGG)。預期PCR產物通過分析瓊脂糖凝膠電泳鑒定,并用WizardSVGelandPCRClean-up試劑盒(購自Promega)從樣品中純化回收。兩個片段以等摩爾比加入到第二輪搭橋PCR中作為模板,反應體系仍然使用上述提到的KODPlus體系,反應先加熱樣品到94℃預變性5分鐘,然后保溫10個循環,每個循環反應條件是94℃30秒、60℃30秒和68℃30秒。最后在68℃保溫10分鐘。隨后在反應體系中直接加入終濃度為0.2μM的引物S1和S6,并開始PCR程序。反應先加熱樣品到94℃預變性5分鐘,然后保溫25個循環,每個循環是94℃30秒、56℃30秒和68℃30秒。最后在68℃保溫10分鐘。預期PCR產物通過制備性瓊脂糖凝膠電泳分離,并用WizardSVGelandPCRClean-up試劑盒根據制造商的說明純化回收。完整的文庫DNA片段兩端分別含有sfiI和NotI限制性內切酶識別位點,經限制性內切酶sfiI/NotI進行限制性消化,插入到經過同樣雙酶切的噬菌粒載體pCANTAB5E中。連接產物使用WizardSVGelandPCRClean-up試劑盒分離樣品中的DNA并脫鹽,用于電轉化。在電轉化時,使用電轉化杯和電穿孔儀GenePulserII(購自Bio-Rad),轉化到自制的感受態大腸桿菌ER2738(購自NEB)。最終確認得到一個含有8.9x109個突變體的文庫。4.3、L12親和力成熟庫的構建通過對P7D4單鏈抗體進行序列比對和分析,P7D4輕鏈第一個和第二個CDR區域的部分氨基酸被選定,通過引物引入隨機化突變,用于構建輕鏈親和力成熟突變體文庫。為制備編碼P7D4突變體文庫的DNA片段,以質粒pCantab5E-P7D4為模板,通過PCR方法分別得到兩段DNA片段,隨后通過搭橋PCR的方式拼接而成。具體使用以下操作步驟:為合成基因,在50μl體積重進行PCR反應,每個反應使用質粒pCantab5E-P7D4作為模板,每條引物的終濃度為0.2μM,以及5μl10×KODPlus緩沖液、4μldNTPs(dATP、dCTP、dGTP和dTTP,每種2mM)、2μl25mMMgSO4和1UKODPlus,用水補足體積后,在熱循環儀中開始PCR程序。反應先加熱樣品到94℃預變性5分鐘,然后保溫25個循環,每個循環是94℃30秒、56℃30秒和68℃30秒。最后在68℃保溫10分鐘。第一個片段的擴增利用引物S1和74L12F1r(SEQIDNO:83,GTTTGGGGGCTTTGCCTGGGTACTGTTGGTACCAGGAGACMNNAHNMNNAHNACCAACGTCACTGCTG),第二個片段利用引物74L12F2f(SEQIDNO:84,ACCCAGGCAAAGCCCCCAAACTCCTCATCTATNNKNNKNNKNNKCGGCCCTCAGGGGTC)和S6。預期PCR產物通過分析瓊脂糖凝膠電泳鑒定,并用WizardSVGelandPCRClean-up試劑盒從樣品中純化回收。兩個片段以等摩爾比加入到第二輪搭橋PCR中作為模板,反應體系仍然使用上述提到的KODPlus體系,在沒有引物存在的情況下,反應先加熱樣品到94℃預變性5分鐘,然后保溫10個循環,每個循環反應條件是94℃30秒、60℃30秒和68℃30秒。最后在68℃保溫10分鐘。隨后在反應體系中直接加入終濃度為0.2μM的引物S1和S6,并開始PCR程序。反應先加熱樣品到94℃預變性5分鐘,然后保溫25個循環,每個循環是94℃30秒、56℃30秒和68℃30秒。最后在68℃保溫10分鐘。預期PCR產物通過制備性瓊脂糖凝膠電泳分離,并用WizardSVGelandPCRClean-up試劑盒根據制造商的說明純化回收。完整的文庫DNA片段兩端分別含有sfiI和NotI限制性內切酶識別位點,經限制性內切酶sfiI/NotI進行限制性消化,插入到經過同樣雙酶切的噬菌粒載體pCANTAB5E中。連接產物使用WizardSVGelandPCRClean-up試劑盒分離樣品中的DNA并脫鹽,用于電轉化。在電轉化時,使用電轉化杯和電穿孔儀GenePulserII,轉化到自制的感受態大腸桿菌ER2738。最終確認得到一個含有1.1x1010個突變體的文庫。另外,本發明人也采用errorpronePCR的策略,對整個P7D4片段進行隨機突變,構建了庫容為7.9×109的文庫T2,其中擴增引物對為S1和S6,克隆和構建方式與上述H12和L12一致。以上三個親和力成熟文庫的篩選與實施例1中的篩選過程一致。通過篩選,本發明人鑒定得到六個高親和力P7D4系列突變體克隆am4、am14、am20、am35、am42和T2-23,其序列信息如下:am4核苷酸序列(SEQIDNO:24,其中,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列,第364-408位為(Gly4Ser)3連接序列):am4氨基酸序列(SEQIDNO:25):重鏈CDR1:GFTFSTYAMT(SEQIDNO:60)重鏈CDR2:SISSSGESTYYADSVKG(SEQIDNO:61)重鏈CDR3:DRRGSHADAFDV(SEQIDNO:14)輕鏈CDR1:TGTSSDVGGYNYVS(SEQIDNO:16)輕鏈CDR2:GNSNRPS(SEQIDNO:18)輕鏈CDR3:QSYDSSLRVV(SEQIDNO:20)其中,第1-121位為重鏈氨基酸序列,第137-247為輕鏈氨基酸序列。第122-136為(Gly4Ser)3連接序列。am14核苷酸序列(SEQIDNO:26,其中,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列,第364-408位為(Gly4Ser)3連接序列):am14氨基酸序列(SEQIDNO:27):重鏈CDR1:GFTFSTYAMA(SEQIDNO:62)重鏈CDR2:EISSSGSRTYYADSVKG(SEQIDNO:63)重鏈CDR3:DRRGSHADAFDV(SEQIDNO:14)輕鏈CDR1:TGTSSDVGGYNYVS(SEQIDNO:16)輕鏈CDR2:GNSNRPS(SEQIDNO:18)輕鏈CDR3:QSYDSSLRVV(SEQIDNO:20)其中,第1-121位為重鏈氨基酸序列,第137-247為輕鏈氨基酸序列,第122-136為(Gly4Ser)3連接序列。am20核苷酸序列(SEQIDNO:28,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列。第364-408位為(Gly4Ser)3連接序列):am20氨基酸序列(SEQIDNO:29):重鏈CDR1:GFTFSTYAMA(SEQIDNO:64)重鏈CDR2:AISMSGESTYYADSVKG(SEQIDNO:65)重鏈CDR3:DRRGSHADAFDV(SEQIDNO:14)輕鏈CDR1:TGTSSDVGGYNYVS(SEQIDNO:16)輕鏈CDR2:GNSNRPS(SEQIDNO:18)輕鏈CDR3:QSYDSSLRVV(SEQIDNO:20)其中,第1-121位為重鏈氨基酸序列,第137-247為輕鏈氨基酸序列,第122-136為(Gly4Ser)3連接序列。am35核苷酸序列(SEQIDNO:30,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列。第364-408位為(Gly4Ser)3連接序列):am35氨基酸序列(SEQIDNO:31):重鏈CDR1:GFTFSSYAMH(SEQIDNO:10)重鏈CDR2:AISSSGGSTYYADSVKG(SEQIDNO:66)重鏈CDR3:DRRGSHADAFDV(SEQIDNO:14)輕鏈CDR1:TGTSSDVGHKFPVS(SEQIDNO:67)輕鏈CDR2:KNLLRPS(SEQIDNO:68)輕鏈CDR3:QSYDSSLRVV(SEQIDNO:20)其中,第1-121位為重鏈氨基酸序列,第137-247為輕鏈氨基酸序列。第122-136為(Gly4Ser)3連接序列。am42核苷酸序列(SEQIDNO:32,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列。第364-408位為(Gly4Ser)3連接序列):am42氨基酸序列(SEQIDNO:33):重鏈CDR1:GFTFSSYAMH(SEQIDNO:10)重鏈CDR2:AISSSGGSTYYADSVKG(SEQIDNO:66)重鏈CDR3:DRRGSHADAFDV(SEQIDNO:14)輕鏈CDR1:TGTSSDVGLMHNVS(SEQIDNO:69)輕鏈CDR2:KSSSRPS(SEQIDNO:70)輕鏈CDR3:QSYDSSLRVV(SEQIDNO:20)其中,第1-121為重鏈氨基酸序列,第137-247為輕鏈氨基酸序列。第122-136為(Gly4Ser)3連接序列。T2-23核苷酸序列(SEQIDNO:34,第76-105位為重鏈CDR1,第148-198位為重鏈CDR2,第295-330位為重鏈CDR3;第475-516位為輕鏈CDR1;第562-582位為輕鏈CDR2,第679-708位為輕鏈CDR3;其中,第1-363位為重鏈核苷酸序列,第409-741為輕鏈核苷酸序列。第364-408位為(Gly4Ser)3連接序列):T2-23氨基酸序列(SEQIDNO:35):重鏈CDR1:GFTFSSYAMH(SEQIDNO:10)重鏈CDR2:AISSSGRSTYYADSVEG(SEQIDNO:71)重鏈CDR3:DRRGSHADALNV(SEQIDNO:72)輕鏈CDR1:TGTSSDVGGYNYVS(SEQIDNO:16)輕鏈CDR2:KSSSRPS(SEQIDNO:70)輕鏈CDR3:QSYDSSLRVV(SEQIDNO:20)其中,第1-121位為重鏈氨基酸序列,第137-247為輕鏈氨基酸序列。第122-136為(Gly4Ser)3連接序列。4.4、P7D4系列抗體對GPC3結合能力的SPR分析為定量分析P7D4系列抗體與GPC3的結合,使用BiacoreT200系統(購自GE)通過捕獲法分別測量P7D4系列單鏈抗體的親和力和動力學參數。根據制造商的說明,用NHS/EDC偶聯通過伯氨基將抗人IgG(Fc)的抗體(購自GE)偶聯到傳感器芯片CM5的羧甲基葡聚糖表面。測量在25℃、30μl/min、1×HBS-EP+工作緩沖液中進行,再生條件為3MMgCl2、10μl/min作用30秒。在每一輪測試循環中,待測試抗體首先被捕獲到芯片上,一定濃度的分析物GPC3流過芯片表面,人GPC3與被捕獲的抗體相互作用而導致傳感片表面分子濃度的變化將由SPR信號的改變而得到測定,并以共振單位(RU)表示。以時間對共振單位(RU)連續作圖,得到的傳感圖記錄了整個反應過程包括結合和解離過程(圖4)。在所有的單循環動力學中,GPC3的濃度分別為5nM、10nM、20nM、40nM和80nM。用BiacoreT200evaluationsoftware評估所得作用曲線,并計算親和力KD值。所有P7D4系列單鏈抗體分別對GPC3的結合數據總結在表1中。表1、P7D4系列單鏈抗體對GPC3的結合數據由表1可見,改造獲得的P7D4系列突變體單鏈抗體具有良好的親和力,相對于P7D4單鏈抗體具有極其顯著的提高。4.5、P7D4系列抗體的識別特異性分析為了分析P7D4系列抗體對GPC3蛋白的結合特異性,通過ELISA實驗,分別測定P7D4系列單鏈抗體分別對人GPC家族成員,包括重組人GPC1(rhGPC1)、GPC2(rhGPC2)、GPC3(rhGPC3)、GPC5(rhGPC5)和GPC6(rhGPC6)(購自安迪生物科技(上海)有限公司)的結合活性。為此目的,用0.1MNaHCO3(pH9.6)包被液稀釋以上5種抗原,每孔包被100ng,50μl/孔,4℃包被過夜,并用含2%(w/v)BSA的PBST于室溫下封閉2小時。然后用PBST漂洗平板三次并去除干凈。隨后,向每個孔板加入100ng各抗體蛋白的PBST溶液,每個樣品的測定使用平行復孔分析。37℃保溫2小時后,用PBST漂洗三次,隨后加入1:20000稀釋的HRP標記的兔抗人Fc抗體(購自上海銳勁生物技術有限公司)100μl/孔,37℃反應1小時。為了檢測,用PBST漂洗孔三次,然后用PBS漂洗三次,最后加入TMB顯示10分鐘,用每孔50μl的2MH2SO4終止顯色反應,用酶聯免疫檢測儀(Bio-Rad)在450nm測量消光值。結果如圖5所示,所有P7D4系列的單鏈抗體均只特異性結合人GPC3,不與人GPC1、GPC2、GPC5和GPC6結合。實施例5、人GPC3抗原及抗該抗原的人源化單克隆抗體的制備5.1人GPC3在真核表達系統中表達及純化5.1.1GPC3載體構建及鑒定以人肝癌細胞系Huh-7cDNA為模板,以如下引物GPC3-F:GATCGCTAGCACAGCCCCCGCCGCCGC(SEQIDNO:54),GPC3-R:GTACGGATCCTTCAGCGGGGAATGAACGTTC(SEQIDNO:55)進行PCR擴增,獲得兩端帶有酶切位點NheI/BamHI的GPC3片段(1.6kb),將獲得的PCR片段用內切酶NheI/BamHI(購自Fermentas公司)雙酶切,同時將質粒載體V5H(購自Raygene公司),同樣經內切酶NheI/BamHI雙酶切,瓊脂糖凝膠電泳后回收載體和插入片段,再通過T4DNAligase(購自NEB公司)連接并轉化于宿主菌TOP10(購自LIFE公司)中,經氨芐抗性進行篩選,挑取克隆抽提質粒內切酶NheI/BamHI(購自Fermentas公司)雙酶切鑒定含插入片斷的陽性克隆,并通過測序驗證,得到含有正確的人GPC3基因序列的真核表達質粒V5H-GPC3。5.1.2人GPC3蛋白的表達與純化5.1.2.1.V5H-GPC3質粒的脂質體轉染和培養將生長良好的HEK293F細胞(HEK293F,購自LIFE公司)以1×106細胞/毫升的密度接種于細胞三角培養瓶,37℃5%CO2120rpm培養過夜備用;將上述步驟獲得的質粒V5H-GPC3與脂質體293Fectin(購自LIFE公司)分別用DMEM稀釋并溫和混合,室溫孵育20min,將孵育好的DNA-脂質體復合物加至293F細胞中,37℃5%CO2120rpm培養72h。收集細胞培養液,4500g離心15min,除去細胞,取上清。5.1.2.2.GPC3蛋白純化取1ml的Ni-NTAAgarose親和填料裝柱,將Ni-NTA親和柱用平衡緩沖液(50mMPB、0.3MNaCl、10mM咪唑、pH8.0)平衡10個柱體積。將離心后的細胞培養液上清以1ml/min通過Ni-NTA親和柱,收集流穿液4℃保存。用清洗緩沖液1(50mMPB、0.3MNaCl、20mM咪唑、pH8.0)洗10個柱體積,收集流穿液于4℃保存。用洗脫緩沖液(50mMPB、0.3MNaCl、250mM咪唑、pH8.0)洗4-5個柱體積,收集洗脫液,在透析液(50mMPB,pH7.8,0.3MNaCl,5%甘油)中4℃透析過夜,即獲得GPC3(H)蛋白,取少量進行SDSPAGE電泳(圖6)。5.2人GPC3抗原免疫重組蛋白免疫:將上述實施例5.1中得到的1ml純化人GPC3蛋白GPC3(H)(1.0mg/mL)作為抗原與1mL完全弗氏佐劑(購自Sigma-aldrich公司)充分乳化混合皮下免疫6-8周齡BALB/c小鼠,每只小鼠免疫100μg人GPC3(H)蛋白抗原。4周后人GPC3抗原與不完全弗氏佐劑乳化混合,腹腔注射免疫小鼠,50μg每只小鼠,其后間隔2周,繼續腹腔50μg抗原加強免疫。在第4次加強免疫1周后,以GPC3(H)蛋白進行包被,通過ELISA法檢測小鼠抗血清效價,繼續加強免疫,直至小鼠的抗血清效價達到>105。最后一次加強免疫3周后,脾內免疫上述人GPC3(H)蛋白20μg,備用。5.3抗人GPC3雜交瘤細胞株建立小鼠經脾內加強免疫后4天,在無菌情況下取脾,用100目濾網濾過分離淋巴細胞,與骨髓瘤細胞系SP2/0融合,經次黃嘌呤、氨基蝶呤與胸苷(hypoxathine,aminopterinandthymidine,HAT)選擇性培養3天后,補加HT培養基,繼續培養1周。以GPC3(H)抗原包被,ELISA篩選陽性克隆,以有限稀釋法進行3次亞克隆,繼續連續培養2個月,最后獲得穩定雜交瘤細胞系(克隆號分別命名為:5A5,7C9,11D3)。5.4腹水生產及抗體的純化將8-10周齡F1小鼠腹腔注射100μL降植烷(購自Sigma-aldrich公司),1周后,取上述實施例5.4雜交瘤細胞克隆以5×105細胞/小鼠的量注射小鼠腹腔以制備腹水,7到10天后采集腹水,10000g離心10min,取上清備用。取蛋白G親和柱(購自GE公司)回復室溫,用PBS(0.01MPB,0.15MNaCl,pH7.4)平衡5個柱體積。將腹水上清與等體積用PBS(0.01MPB,0.15MNaCl,pH7.4)混勻,0.22μM濾器過濾,過濾的腹水上清液上蛋白G親和柱,PBS洗5個柱體積。以洗脫緩沖液(0.1MGlycineHCl,pH2.7)洗脫,洗脫液加入1/10體積中和緩沖液(1MNaH2PO4,pH9.0)中和。將溶液用PBS(0.01MPB,0.15MNaCl,pH7.4)透析,其間換液兩次,兩次換液時間間隔時間大于5小時。將透析溶液于10000g離心10min,上清液通過0.22um濾膜過濾保存,得到純化的對應各克隆產生的抗人GPC3單抗的溶液。根據分析5A5具有良好的抗原結合能力。5.5GPC3克隆5A5的人源化5.5.15A5抗體的序列分析5A5具有良好的抗原結合能力。測定5A5抗體基因可變區序列VL與VH,綜合Kabat、Chothia以及IMGT三種抗體CDRs區的命名方案,確定抗體輕鏈與重鏈的六個CDRs區序列。5A5重鏈的核苷酸序列如下(SEQIDNO:56,其中,下劃線的三個區段依次為CDR1、CDR2、CDR3):CAGGTTCAACTGCAGCAGTCTGGGACTGAGCTGGTGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTTGGGCTACACATTTACTGACTATGAAATGCACTGGGTGAAGCAGACACCTGTGCATGGCCTGGAGTGGATTGGAGCTATTCATCCAGGAAGTGGTGATACTGCCTACAATCAGAGGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCTTCCAGCACAGCCTACATGGAGTACAGCAGCCTGACATCTGAGGACTCTGCTGTCTATTACTGTACAAGATTTTATTCCTATGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA5A5輕鏈的核苷酸序列如下(SEQIDNO:57,其中,下劃線的三個區段依次為CDR1、CDR2、CDR3):GATGTTGTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGCCTTGTACACAGTAATGGAAACACCTATTTACAGTGGTACCTGCAGAAGCCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAATCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGAGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTTCTGCTCTCAAAGTATATATGTTCCGTACACGTTCGGAGGAGGGACCAAGCTGGAAATAAAACGG5A5重鏈的氨基酸序列(SEQIDNO:81,其中,下劃線的三個區段依次為CDR1、CDR2、CDR3):QVQLQQSGTELVRPGASVKLSCKALGYTFTDYEMHWVKQTPVHGLEWIGAIHPGSGDTAYNQRFKGKATLTADKSSSTAYMEYSSLTSEDSAVYYCTRFYSYAYWGQGTLVTVSA5A5輕鏈的氨基酸序列(SEQIDNO:82,其中,下劃線的三個區段依次為CDR1、CDR2、CDR3)DVVMTQTPLSLPVSLGDQASISCRSSQSLVHSNGNTYLQWYLQKPGQSPKLLIYKVSNRFSGVPDRFSGRGSGTDFTLKISRVEAEDLGVYFCSQSIYVPYTFGGGTKLEIKR5.5.2抗體模板的選擇抗體模板框架區的選擇主要有4個重要因素:免疫原性,抗原結合特性,表達以及抗體的穩定性。(1)根據專利WO2008021156確定抗體輕重鏈可變區中支持抗體loop結構的氨基酸殘基以及輕重鏈結合區域的氨基酸殘基。(2)將5A5的輕鏈或者重鏈可變區全長與來自IMGT,VBASE或者NCBI的抗體種系進行序列相似性比對。(3)將5A5的輕鏈或者重鏈可變區中CDR區內的loop支持相關的氨基酸殘基去掉,然后與來自IMGT,VBASE或者NCBI的抗體種系進行序列相似性比對。(4)將5A5的輕鏈或者重鏈可變區中CDR區的氨基酸殘基去掉,然后與來自IMGT,VBASE或者NCBI的抗體種系進行序列相似性比對。(5)只保留5A5的輕鏈或者重鏈序列中的與支持loop相關的氨基酸殘基,然后與來自IMGT,VBASE或者NCBI的抗體種系進行序列相似性比對。(6)只保留5A5的輕鏈或者重鏈framework中與支持loop相關的氨基酸殘基,然后與來自IMGT,VBASE或者NCBI的抗體種系進行序列相似性比對。(7)綜合序列相似性比對的結果,選取相似度最高的抗體種系作為抗體模板。(8)重鏈的序列相似度比對結果:根據相似度,選取VH1_69*06(IMGT,Accessionnumbers:L22583)作為5A5重鏈的抗體模板。(9)輕鏈的序列相似對比對結果:根據相似度,選取VK2D_29*02(IMGT,Accessionnumbers:U41644)作為5A5輕鏈的抗體模板。5.5.3CDR移植將5A5抗體的輕鏈或者重鏈CDR區替換掉抗體模板的CDR區。最終確定人源化抗體(Y035)。其氨基酸序列如下:人源化Y035重鏈(SEQIDNO:58):EVQLVQSGAEVKKPGASVKVSCKASGYTFSDYEMHWVRQAPGQGLEWMGAIHPGSGDTAYNQRFKGRVTITADKSTSTAYMELSSLRSEDTAVYYCARFYSYAYWGQGTLVTVSA重鏈CDR1氨基酸序列為:AspTyrGluMetHis(SEQIDNO:73);重鏈CDR2氨基酸序列為:AlaIleHisProGlySerGlyAspThrAlaTyrAsnGlnArgPheLysGly(SEQIDNO:74);重鏈CDR3氨基酸序列為:PheTyrSerTyrAlaTyr(SEQIDNO:75)。人源化Y035輕鏈(SEQIDNO:59):DIVMTQTPLSLPVTPGEPASISCRSSQSLVHSNGNTYLQWYLQKPGQSPQLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSIYVPYTFGQGTKLEIKR輕鏈CDR1氨基酸序列為:ArgSerSerGlnSerLeuValHisSerAsnGlyAsnThrTyrLeuGln(SEQIDNO:76);輕鏈CDR2氨基酸序列為:LysValSerAsnArgPheSer(SEQIDNO:77);輕鏈CDR3氨基酸序列為:SerGlnSerIleTyrValProTyrThr(SEQIDNO:78)。5.5.4表達和純化人源化的抗體(1)根據人源化的抗體(Y035)的氨基酸序列,設計核苷酸序列并合成合成的輕鏈核苷酸序列(SEQIDNO:79,包括信號肽編碼序列):GGATCGATATCCACCATGGACATGATGGTGCTGGCCCAGTTCCTGGCCTTCCTGCTGCTGTGGTTCCCAGGCGCTAGATGCGACATCGTGATGACCCAGACCCCCCTGAGCCTGCCCGTGACCCCCGGCGAGCCCGCCAGCATCAGCTGCCGGAGCAGCCAGAGCCTGGTGCACAGCAACGGCAACACCTACCTGCAGTGGTACCTGCAGAAGCCCGGCCAGAGCCCCCAGCTGCTGATCTACAAGGTGAGCAACCGGTTCAGCGGCGTGCCCGACCGGTTCAGCGGCAGCGGCAGCGGCACCGACTTCACCCTGAAGATCAGCCGGGTGGAGGCCGAGGACGTGGGCGTGTACTACTGCAGCCAGAGCATCTACGTGCCCTACACCTTCGGCCAGGGCACCAAGCTGGAGATCAAACGTACGGTGGCT合成的重鏈核苷酸序列(SEQIDNO:80,包括信號肽編碼序列):GGATCGATATCTGCGGCCTATCTAGCCACCATGCGGGTGCTGATCCTGCTGTGGCTGTTTACCGCCTTCCCCGGCTTCCTGAGCGAGGTGCAGCTGGTGCAGAGCGGCGCCGAGGTGAAGAAGCCCGGCGCCAGCGTGAAGGTGAGCTGCAAGGCCAGCGGCTACACCTTCAGCGACTACGAGATGCACTGGGTGCGGCAGGCCCCCGGCCAGGGCCTGGAGTGGATGGGCGCCATCCACCCCGGCAGCGGCGACACCGCCTACAACCAGCGGTTCAAGGGCCGGGTGACCATCACCGCCGACAAGAGCACCAGCACCGCCTACATGGAGCTGAGCAGCCTGCGGAGCGAGGACACCGCCGTGTACTACTGCGCCCGGTTCTACAGCTACGCCTACTGGGGCCAGGGCACCCTGGTGACCGTGAGCGCCGCTAGCACCAAA(2)把合成的抗體核苷酸序列(信號肽是第16-81位(輕鏈)第31-84位(重鏈)),抗體的可變區,恒定區插入到哺乳動物細胞表達載體中從而分別構建出含有重鏈和輕鏈的抗體表達載體,通過測序鑒定抗體序列跟設計一致。具體為:以EcoRV和BsiWI雙酶切合成的輕鏈以及pIK-hu12L(購自上海銳勁生物技術有限公司),將輕鏈插入pIK-hu12L。以EcoRV和NheI雙酶切合成的重鏈以及改造過的pIH-hu12H(購自上海銳勁生物技術有限公司在CH1上通過同義突變增加了一個NheI酶切位點),將重鏈插入pIH-hu12H。經酶切連接好的載體轉化至TOP10感受態細胞,PCR鑒定陽性克隆,經測序鑒定確定序列正確的克隆。將載體通過293Fectin瞬時轉染至293F細胞中并表達。離心收集293F培養上清,通過0.45um濾器過濾,通過ProteinA柱親和層析。利用分光光度計測定A280來確定純化抗體的濃度。5.6人源化抗體Y035對人GPC3結合能力的SPR分析為定量分析抗體Y035與抗原蛋白人GPC3的結合,使用BiacoreT200系統(購自GE)通過多循環動力學測定方法,測量抗體Y035的親和力和動力學參數。根據制造商的說明,用NHS/EDC偶聯通過伯氨基將抗原蛋白人GPC3(購自上海銳勁生物技術有限公司)偶聯到傳感器芯片CM5的羧甲基葡聚糖表面,配體最終偶聯量為305RU。動力學測量在25℃、30μl/min、1×HBS-EP+工作緩沖液中進行,再生條件為10mMGlycine-HCl(pH2.5)、10μl/min作用25秒。在每一個測量循環中,特定濃度的抗體Y035流過芯片表面,抗體與被固定在芯片上的抗原蛋白人GPC3相互作用而導致傳感片表面分子濃度的變化將由SPR信號的改變而得到測定,并以共振單位(RU)表示。以時間對共振單位(RU)連續作圖,并扣除了未固定抗原的參比通道的RU數值后,得到的傳感圖記錄了整個反應過程包括結合和解離過程。抗體Y035及抗體5A5對人GPC3的結合動力學分析如圖7-8。在動力學測定的不同循環實驗中,抗體Y035的濃度分別為6.25nM、12.5nM、25nM、50nM和100nM。用BiacoreT200evaluationsoftware評估所得作用曲線,并計算親和力KD值。采用同樣的方法,對Y035進行人源化改造前的親本鼠單克隆抗體5A5的親和力和動力學參數也進行了測定分析。抗體Y035和5A5分別對人GPC3蛋白的結合數據總結在表2中,經過人源化改造后的抗體Y035對人GPC3蛋白的結合能力大大優于鼠源的5A5。表2、抗體Y035與5A5對人GPC3的結合動力學參數5.7抗體Y035的細胞結合活性FACS分析通過熒光激活細胞分選儀(FACS)分析抗體Y035與GPC3陽性的肝癌HepG2細胞系(ATCC)的結合能力,使用GPC3表達陰性的293T(ATCC)細胞作陰性對照。具體方法如下:1)取對數生長期的細胞HepG2和293T分別接種到6cm平皿中,接種細胞密度約為90%,37℃孵箱過夜培養。2)使用10mM的EDTA消化細胞,200g×5min離心收集細胞。以1×106~1×107/mL的濃度重懸于1%含小牛血清的磷酸鹽緩沖液(NBSPBS)中,按100ul/管的量加入流式專用管中。3)200g×5min離心,棄上清。4)兩個細胞系的實驗組分別加入待測抗體Y035,另一個對照為不加抗體的PBS空白對照。抗體的終濃度均為20μg/ml,每管加入100ul。冰浴,45分鐘。5)每管加入2ml1%NBSPBS,以200g×5min離心,共二遍。6)棄上清,加入1:100稀釋的羊抗人抗體-FITC(來自上海業力生物科技有限公司),每管加入100ul。冰浴,45分鐘。7)每管加入2ml1%NBSPBS,以200g×5min離心,共二遍。8)棄上清,重懸于300ul1%NBSPBS中,流式細胞儀檢測。應用流式細胞儀數據分析軟件Flowjo7.6分析數據,結果如圖9所示,流式細胞分析結果標明,抗體Y035可以特異性識別表達GPC3的HepG2細胞,與GPC3表達陰性的293T細胞不結合。實施例6、基于P7D4單鏈抗體的CAR表達載體的構建和慢病毒制備作為示例,以下構建本發明的慢病毒質粒載體使用的載體系統屬于第三代自滅活慢病毒載體系統,該系統共有四個質粒:即編碼蛋白Gag/Pol的包裝質粒pMDLgRRE(購自addgene),編碼Rev蛋白的包裝質粒pRSV-REV(購自addgene),編碼VSV-G蛋白的包膜質粒pCMV-VSV-G(購自addgene)及基于空載體pRRLSIN-cPPT.PGK-GFP.WPRE(購自addgene)的編碼目的基因CAR的重組表達載體,該系統可以有效降低形成可復制性慢病毒顆粒的風險。在本系統中,本發明人首先通過常規分子克隆的技術方式,對空載體pRRLSIN-cPPT.PGK-GFP.WPRE進行改造,用延長因子-1α(elongationfactor-1α,簡稱EF-1α)的啟動子替代了原載體的啟動子,并在啟動子和CD8αsp信號肽之間增加了MluI酶切位點。具體地,使用ClaI/SalI(購自NEB)雙酶切載體pWPT-EGFP(購自addgene),回收1.1Kb的DNA片段,用T4DNA連接酶連接于經ClaI/SalI雙酶切的載體pRRLSIN-cPPT.PGK-GFP.WPRE,并轉化于宿主菌TOP10中,挑取克隆通過菌落PCR鑒定陽性克隆并通過測序確認,獲得重組質粒pRRLSIN-cPPT.EF-1α-EGFP.WPRE。利用前述優化獲得的P7D4scFv制備嵌合抗原受體。表3解釋了本發明示例的嵌合抗原受體各部分的連接順序。表3嵌合抗原受體胞外結合區-跨膜區-胞內信號區1-胞內信號區2etc描述P7D4-δZP7D4scFv-CD8-CD3δzeta陰性對照P7D4-ZP7D4scFv-CD8-CD3zeta第一代P7D4-BBZP7D4scFv-CD8-CD137-CD3zeta第二代P7D4-28ZP7D4scFv-CD28a-CD28b-CD3zeta第二代P7D4-28BBZP7D4scFv-CD28a-CD28b-CD137-CD3zeta第三代注:CD28a代表CD28分子的跨膜區,CD28b代表CD28分子的胞內信號區。1、核酸片段的擴增(1)scFv序列的擴增分別以V5-scFv-P7D4-Fc質粒為模板,采用正向引物P7D4fd(SEQIDNO:36,包含部分CD8signalpeptide(CD8sp)的序列,引物序列為:ctccacgccgccaggccgcaggtgcagctgcaggag)和反向引物P7D4re(SEQIDNO:37,包含部分CD8hinge的序列,引物序列為:CGGCGCTGGCGTCGTGGTACCTAGGACGGTGACCTTGG)為引物對,PCR擴增獲得P7D4scFv片段。(2)嵌合抗原受體其他部分的核酸序列抗GPC3嵌合抗原受體蛋白的除P7D4scFv外其它部分的核酸序列以專利申請號為201310164725.X中公開的序列SEQIDNO:26,27,28,29和30為模板通過PCR方式獲得。具體地,其中包含CD8αsp序列的片段F1以本實施例中構建的質粒pRRLSIN-cPPT.EF-1α-EGFP.WPRE為模板,以引物對PWXLF(SEQIDNO:38,引物序列:gcaggggaaagaatagtagaca)和PRRL-CD8SP-R1(SEQIDNO:39,引物序列:CGGCCTGGCGGCGTGGAG)進行PCR擴增獲得。包含CD8-CD3δzeta(δZ)的片段F3-δZ以申請專利201310164725.X中SEQIDNO:26質粒為模板,采用引物對PRRL-CD8hinge(SEQIDNO:40,引物序列:accacgacgccagcgccg)和δZre(SEQIDNO:41,引物序列:GAGGTCGACCTACGCGGGGGCGTCTGCGCTCCTGCTGAACTTCACTCT)通過PCR擴增獲得。包含CD8-CD3zeta(Z)的片段F3-Z、包含CD8-CD137-CD3zeta(BBZ)的片段F3-BBZ、包含CD28a-CD28b-CD3zeta(28Z)的片段F3-28Z和包含CD28a-CD28b-CD137-CD3zeta(28BBZ)的片段F3-28BBZ序列分別以申請專利201310164725.X中SEQIDNO:27、SEQIDNO:28、SEQIDNO:29和SEQIDNO:30對應的質粒為模板,采用引物對PRRL-CD8hinge(SEQIDNO:42,引物序列:accacgacgccagcgccg)和R3R(SEQIDNO:43,引物序列:aatccagaggttgattgtcgacctagcgagggggcagggcctgc)通過PCR擴增獲得。2、核酸片段的拼接分別將如前述獲得的F1核酸片段,與等摩爾的P7D4scFv核酸片段以及等摩爾的F3-δZ或F3-Z或F3-BBZ或F3-28Z或F3-28BBZ核酸片段,進行三片段拼接PCR,拼接條件為:預變性:94℃,4min;變性:94℃,40s;退火:60℃,40s;延伸:68℃,140s,進行5個循環,然后總延伸68℃,10min,補充DNA聚合酶及正向引物PWXLF和反向引物R3R(CD8-CD3δzeta對應的反向引物為δZre,其余的皆為R3R)后PCR擴增30個循環,擴增條件為預變性:94℃,4min;變性:94℃,40s;退火:60℃,40s;延伸:68℃,140s,進行30個循環,然后總延伸68℃,10min。本實施例構建的由F1片段、P7D4scFv或P7D4突變體scFv、以及各類F3片段所組成的片段可以簡稱為CAR片段,擴增獲得的片段分別稱為:3、慢病毒質粒載體的構建本實施例構建了由F1片段、P7D4scFv、以及F3片段組件簡稱為CAR)通過MluI/SalI限制性內切酶雙酶切,連入同樣雙酶切的pRRLSIN-cPPT.EF-1α-EGFP.WPRE載體中,從而構建表達各嵌合抗原受體的慢病毒載體pRRLSIN-cPPT.EF-1α-CAR。構建成功的載體經MluI/SalI酶切鑒定及序列測定正確后,可以準備用于慢病毒包裝。如前所述,相關CAR基因經轉錄翻譯為一條肽鏈,在CD8α信號肽的引導下,抗GPC3嵌合抗原受體將定位在細胞膜上。通過以上構建,分別可獲得五個CAR多肽序列,稱為:P7D4-δZ(SEQIDNO:49);P7D4-Z(SEQIDNO:50);P7D4-BBZ(SEQIDNO:51);P7D4-28Z(SEQIDNO:52);P7D4-28BBZ(SEQIDNO:53)。4、質粒轉染293T包裝慢病毒以6×106的密度接種培養至第6~10代的HEK-293T細胞(ATCC:CRL-11268)于10cm培養皿中,37℃,5%CO2培養過夜準備用于轉染。培養基為含10%胎牛血清和DMEM(均購自Life公司)。轉染的步驟如下:4.1A液配制:將5.2μg的各目的基因質粒pRRLSIN-cPPT.EF-1α-CAR,分別與6.2μg包裝質粒pMDLgRRE和pRSV-REV、以及2.4μg包膜質粒pCMV-VSV-G,溶入800μL的無血清DMEM培養液中,混勻。4.2B液配制:將60μgPEI(聚乙烯亞胺1μg/μl,購自Polysciences公司)溶解于800μL的無血清DMEM培養液中,輕輕混勻,室溫孵育5min。4.3轉染復合物的形成:將A液加入B液中輕輕混合,加入后立即渦旋混合或輕輕混勻,室溫下孵育20min。4.4將轉染復合物1.6ml滴加入HEK-293T細胞中,4-5h小時后,用2%FBS的DMEM培基給轉染的293T細胞換液。在轉染孵育72h后,使用0.45μm濾器(購自Millipore公司)過濾收集病毒,然后采用BeckmanOptimaL-100XP超速離心機28000rpm,4℃離心2小時,棄離心上清,離心所得沉淀用1/10~1/50原液體積的AIM-V培養液(購自Life公司)進行重懸,以100μL/管分裝凍存于-80℃,以待病毒滴定或感染T淋巴細胞。實施例7、重組慢病毒感染CTL細胞由健康人外周血通過密度梯度離心法獲得人外周血單個核細胞(上海市血液中心提供),以約2×106/mL密度加入AIM-V淋巴細胞培養基(購自Invitrogen公司)培養,并以細胞:磁珠比例為1:1加入包被有抗CD3和CD28抗體的磁珠(Invitrogen公司),同時加入終濃度300U/mL的重組人IL-2(購自上海華新生物高技術有限公司)刺激培養48h,然后以用上述重組慢病毒(MOI≈10)感染T細胞。感染后的細胞每隔一天采用5×105/mL的密度進行傳代,同時在淋巴細胞培養液中補加終濃度300U/mL的重組人IL-2。感染的CTL細胞在培養第8天時通過流式細胞檢測各不同嵌合抗原受體表達。采用帶His-tag的人類GPC3重組蛋白(購自上海銳勁生物技術有限公司)進行FACS檢測;首先將細胞與該蛋白(50ug/ml)孵育1hr,D-PBS洗滌2次,然后加入抗His-tag的抗體(1:50稀釋,購自上海睿星生物技術有限公司),孵育1hr,然后用D-PBS洗滌2次,然后加入FITC標記的羊抗鼠二抗(上海康成生物技術有限公司),孵育50min,D-PBS洗滌3次后,FACS檢測。以未感染的T淋巴細胞作為陰性對照,表達不同嵌合抗原受體的病毒感染T細胞其陽性率如表4所示。該陽性率結果表明,通過慢病毒感染的方法能夠獲得一定陽性率的CAR+T細胞。表4轉染有下列CAR的T細胞T細胞轉染陽性率P7D4-δZ(陰性對照)59%P7D4-Z65%P7D4-BBZ53%P7D4-28Z61%P7D4-28BBZ54%T細胞在分別感染包裝有不同嵌合抗原受體的病毒后,以細胞密度為5×105/ml隔天傳代培養、計數、并對傳代的細胞培養液補加IL-2(終濃度為300U/ml),培養第11天約有100~1000倍的擴增,表明表達不同嵌合抗原受體的T細胞在體外能夠進行一定數量的擴增,為后續體外毒性試驗及體內試驗提供了保證。實施例8、表達嵌合抗原受體的T淋巴細胞的體外毒性效果實驗體外毒性實驗使用的材料如下:如表5所示的GPC3陽性肝癌細胞(HepG2和Huh-7)以及GPC3陰性肝癌細胞(SK-HEP-1)作為靶細胞,效應細胞為如實施例7所驗證的體外培養12天的FACS檢測嵌合抗原受體表達的陽性細胞記為嵌合抗原受體陽性(CAR+)的CTL,效靶比視情況分別為3:1,1:1和1:3,靶細胞數量為10000個/孔,根據不同效靶比對應效應細胞。各組均設5個復孔,取5個復孔的平均值。檢測時間為第18h。其中各實驗組和各對照組如下:各實驗組:各靶細胞+表達不同嵌合抗原受體的CTL,對照組1:靶細胞最大釋放LDH,對照組2:靶細胞自發釋放LDH,對照組3:效應細胞自發釋放LDH。檢測方法:采用CytoTox96非放射性細胞毒性檢測試劑盒(Promega公司)進行。該方法是基于比色法的檢測方法,可替代51Cr釋放法。CytoTox檢測定量地測量乳酸脫氫酶(LDH)。LDH是一種穩定的胞質酶,在細胞裂解時會釋放出來,其釋放方式與51Cr在放射性分析中的釋放方式基本相同。釋放出的LDH培養基上清中,可通過30分鐘偶聯的酶反應來檢測,在酶反應中LDH可使一種四唑鹽(INT)轉化為紅色的甲臜(formazan)。生成的紅色產物的量與裂解的細胞數成正比。具體參照CytoTox96非放射性細胞毒性檢測試劑盒說明書。細胞毒性計算公式為:具體如表5所示,本發明的P7D4的單鏈抗體的CAR均有明顯的殺傷GPC3陽性肝癌細胞的活性,其中第二代和第三代的P7D4CART細胞比第一代抗腫瘤活性略強。此外,所有CART細胞對GPC3陰性的SK-HEP-1陽性肝癌細胞均沒有殺傷活性。這些結果表明P7D4可以選擇性地針對GPC3陽性的肝癌細胞,并進行有效的殺傷。此外,本發明的表達P7D4的第一、二、三代CART對GPC3陽性腫瘤細胞呈現效靶比梯度依賴性即效靶比越高細胞毒性作用越強。表5、融合表達單鏈抗體P7D4的CART細胞的細胞毒性實施例9基于Y035和GC33的CAR-T細胞的制備和比較參照實施例6和7的操作,基于Y035的輕鏈可變區和重鏈可變區,分別制備得到Y035-BBZ、Y035-28Z和Y035-28BBZ兩種CAR-T細胞;基于GC33的輕鏈可變區和重鏈可變區,分別制備得到GC33-28Z和GC33-28BBZ兩種CAR-T細胞,作為對照。嵌合抗原受體各部分的連接順序如表6所示。表6其中,Y035-BBZ的核苷酸序列如下所示(SEQIDNO:85):gaggtgcagctggtgcagagcggcgccgaggtgaagaagcccggcgccagcgtgaaggtgagctgcaaggccagcggctacaccttcagcgactacgagatgcactgggtgcggcaggcccccggccagggcctggagtggatgggcgccatccaccccggcagcggcgacaccgcctacaaccagcggttcaagggccgggtgaccatcaccgccgacaagagcaccagcaccgcctacatggagctgagcagcctgcggagcgaggacaccgccgtgtactactgcgcccggttctacagctacgcctactggggccagggcaccctggtgaccgtgagcgccggtggaggcggttcaggcggaggtggttctggcggtggcggatcggacatcgtgatgacccagacccccctgagcctgcccgtgacccccggcgagcccgccagcatcagctgccggagcagccagagcctggtgcacagcaacggcaacacctacctgcagtggtacctgcagaagcccggccagagcccccagctgctgatctacaaggtgagcaaccggttcagcggcgtgcccgaccggttcagcggcagcggcagcggcaccgacttcaccctgaagatcagccgggtggaggccgaggacgtgggcgtgtactactgcagccagagcatctacgtgccctacaccttcggccagggcaccaagctggagatcaaacgtaccacgacgccagcgccgcgaccaccaacaccggcgcccaccatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggccagcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgatatctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaaacggggcagaaagaaactcctgtatatattcaaacaaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggaggatgtgaactgagagtgaagttcagcaggagcgcagacgcccccgcgtacaagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgcY035-BBZ的氨基酸序列如下所示(SEQIDNO:86)EVQLVQSGAEVKKPGASVKVSCKASGYTFSDYEMHWVRQAPGQGLEWMGAIHPGSGDTAYNQRFKGRVTITADKSTSTAYMELSSLRSEDTAVYYCARFYSYAYWGQGTLVTVSAGGGGSGGGGSGGGGSDIVMTQTPLSLPVTPGEPASISCRSSQSLVHSNGNTYLQWYLQKPGQSPQLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSIYVPYTFGQGTKLEIKRTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRY035-28Z的核苷酸序列如下所示(SEQIDNO:87):gaggtgcagctggtgcagagcggcgccgaggtgaagaagcccggcgccagcgtgaaggtgagctgcaaggccagcggctacaccttcagcgactacgagatgcactgggtgcggcaggcccccggccagggcctggagtggatgggcgccatccaccccggcagcggcgacaccgcctacaaccagcggttcaagggccgggtgaccatcaccgccgacaagagcaccagcaccgcctacatggagctgagcagcctgcggagcgaggacaccgccgtgtactactgcgcccggttctacagctacgcctactggggccagggcaccctggtgaccgtgagcgccggtggaggcggttcaggcggaggtggttctggcggtggcggatcggacatcgtgatgacccagacccccctgagcctgcccgtgacccccggcgagcccgccagcatcagctgccggagcagccagagcctggtgcacagcaacggcaacacctacctgcagtggtacctgcagaagcccggccagagcccccagctgctgatctacaaggtgagcaaccggttcagcggcgtgcccgaccggttcagcggcagcggcagcggcaccgacttcaccctgaagatcagccgggtggaggccgaggacgtgggcgtgtactactgcagccagagcatctacgtgccctacaccttcggccagggcaccaagctggagatcaaacgtaccacgacgccagcgccgcgaccaccaacaccggcgcccaccatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggccagcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgatttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggccaacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgcagagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgcY035-28Z的氨基酸序列如下所示(SEQIDNO:88):EVQLVQSGAEVKKPGASVKVSCKASGYTFSDYEMHWVRQAPGQGLEWMGAIHPGSGDTAYNQRFKGRVTITADKSTSTAYMELSSLRSEDTAVYYCARFYSYAYWGQGTLVTVSAGGGGSGGGGSGGGGSDIVMTQTPLSLPVTPGEPASISCRSSQSLVHSNGNTYLQWYLQKPGQSPQLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSIYVPYTFGQGTKLEIKRTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPQRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRY035-28BBZ的核苷酸序列如下所示(SEQIDNO:89):gaggtgcagctggtgcagagcggcgccgaggtgaagaagcccggcgccagcgtgaaggtgagctgcaaggccagcggctacaccttcagcgactacgagatgcactgggtgcggcaggcccccggccagggcctggagtggatgggcgccatccaccccggcagcggcgacaccgcctacaaccagcggttcaagggccgggtgaccatcaccgccgacaagagcaccagcaccgcctacatggagctgagcagcctgcggagcgaggacaccgccgtgtactactgcgcccggttctacagctacgcctactggggccagggcaccctggtgaccgtgagcgccggtggaggcggttcaggcggaggtggttctggcggtggcggatcggacatcgtgatgacccagacccccctgagcctgcccgtgacccccggcgagcccgccagcatcagctgccggagcagccagagcctggtgcacagcaacggcaacacctacctgcagtggtacctgcagaagcccggccagagcccccagctgctgatctacaaggtgagcaaccggttcagcggcgtgcccgaccggttcagcggcagcggcagcggcaccgacttcaccctgaagatcagccgggtggaggccgaggacgtgggcgtgtactactgcagccagagcatctacgtgccctacaccttcggccagggcaccaagctggagatcaaacgtaccacgacgccagcgccgcgaccaccaacaccggcgcccaccatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggccagcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgatttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggccaacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccaaacggggcagaaagaaactcctgtatatattcaaacaaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggaggatgtgaactgagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgcagagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgcY035-28BBZ的氨基酸序列如下所示(SEQIDNO:90)EVQLVQSGAEVKKPGASVKVSCKASGYTFSDYEMHWVRQAPGQGLEWMGAIHPGSGDTAYNQRFKGRVTITADKSTSTAYMELSSLRSEDTAVYYCARFYSYAYWGQGTLVTVSAGGGGSGGGGSGGGGSDIVMTQTPLSLPVTPGEPASISCRSSQSLVHSNGNTYLQWYLQKPGQSPQLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSIYVPYTFGQGTKLEIKRTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPQRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR采用GPC3陽性肝癌細胞Huh-7作為靶細胞,參照實施例8采用的體外毒性實驗方法進行體外測試,在效靶比為1:3時,Y035-28Z和Y035-28BBZ對Huh-7的殺傷率均達35%以上,而GC33-28Z的殺傷率僅為6%,GC33-28BBZ的殺傷率僅為23%,在效靶比為1:1,Y035-28Z對Huh-7的殺傷率達60%以上,而GC33-28Z的殺傷率僅為22%,以上結果表明,本申請Y035-CART細胞的細胞殺傷活性顯著優于GC33-CART細胞。實施例10雙特異性抗體BiTE的制備(1)Y035單鏈抗體核苷酸序列的制備培養分泌單克隆抗體的雜交瘤細胞株至對數生長期時,進行細胞計數,取1×107雜交瘤細胞。按照PlusRNAPurificationkit(Invitrogen,12183-555)說明書,從細胞沉淀中提取總RNA。a.逆轉錄得到cDNA以雜交瘤細胞總RNA做為模板,使用HighcapacityRNAtocDNAkit(Invitrogen,4387406),按照說明書逆轉錄合成cDNA。b.5’-RACE法擴增抗體可變區以cDNA為模板,使用5’-FullRACEkit(TAKARA,D315),用引物tgctttggtttccaggtgcaagatgtgaggtgcagctggtgcaga(SEQIDNO:91)和引物TATCGGATCCACCACCTCCACGTTTGATCTCCAGCTTGGTG(SEQIDNO:92)擴增。PCR產物經1.5%瓊脂糖凝膠電泳分離后,得到的PCR產物為Y035單鏈抗體的核酸。(2)CD3單鏈抗體核酸序列的構建以專利201310025302.X公開的抗EpCAM/CD3雙特異性抗體為模板,通過引物(SEQIDNO:93,gatatcaaactgcagcagtcag)和引物(SEQIDNO:94,GAGAGGGAGTACTCACCCCAAC)進行PCR,具體反應參考KODPLUS酶說明書,膠回收純化,得到的PCR產物為CD3單鏈抗體的核酸。(3)引入NheI酶切位點以載體PIH為模板,通過引物(ggctaactagagaacccactgc,SEQIDNO:95)和PH-R(ACATCTTGCACCTGGAAACCAAAGC,SEQIDNO:96)進行PCR,具體反應參考KODPLUS酶說明書,膠回收純化PCR產物,得到帶有NheI酶切位點的一小段片段。(4)Y035/CD3雙特異性抗體編碼序列核酸的構建步驟(1)、(2)、(3)所得的PCR產物進行OverlapPCR,以引物(SEQIDNO:95)和引物(SEQIDNO:92)進行PCR,膠回收純化PCR產物,即為Y035/CD3雙特異性抗體編碼序列(SEQIDNO:97),序列如下:gaggtgcagctggtgcagagcggcgccgaggtgaagaagcccggcgccagcgtgaaggtgagctgcaaggccagcggctacaccttcagcgactacgagatgcactgggtgcggcaggcccccggccagggcctggagtggatgggcgccatccaccccggcagcggcgacaccgcctacaaccagcggttcaagggccgggtgaccatcaccgccgacaagagcaccagcaccgcctacatggagctgagcagcctgcggagcgaggacaccgccgtgtactactgcgcccggttctacagctacgcctactggggccagggcaccctggtgaccgtgagcgccggtggaggcggttcaggcggaggtggttctggcggtggcggatcggacatcgtgatgacccagacccccctgagcctgcccgtgacccccggcgagcccgccagcatcagctgccggagcagccagagcctggtgcacagcaacggcaacacctacctgcagtggtacctgcagaagcccggccagagcccccagctgctgatctacaaggtgagcaaccggttcagcggcgtgcccgaccggttcagcggcagcggcagcggcaccgacttcaccctgaagatcagccgggtggaggccgaggacgtgggcgtgtactactgcagccagagcatctacgtgccctacaccttcggccagggcaccaagctggagatcaaacgtggaggtggtggatccgatatcaaactgcagcagtcaggggctgaactggcaagacctggggcctcagtgaagatgtcctgcaagacttctggctacacctttactaggtacacgatgcactgggtaaaacagaggcctggacagggtctggaatggattggatacattaatcctagccgtggttatactaattacaatcagaagttcaaggacaaggccacattgactacagacaaatcctccagcacagcctacatgcaactgagcagcctgacatctgaggactctgcagtctattactgtgcaagatattatgatgatcattactgccttgactactggggccaaggcaccactctcacagtctcctcagtcgaaggtggaagtggaggttctggtggaagtggaggttcaggtggagtcgacgacattcagctgacccagtctccagcaatcatgtctgcatctccaggggagaaggtcaccatgacctgcagagccagttcaagtgtaagttacatgaactggtaccagcagaagtcaggcacctcccccaaaagatggatttatgacacatccaaagtggcttctggagtcccttatcgcttcagtggcagtgggtctgggacctcatactctctcacaatcagcagcatggaggctgaagatgctgccacttattactgccaacagtggagtagtaacccgctcacgttcggtgctgggaccaagctggagctgaaa(5)靶向Y035/CD3的雙特異性抗體的表達及純化將Y035/CD3BiTE的質粒瞬時轉染至真核細胞293F中,細胞轉染過程參考293fectin說明書進行。培養上清用金屬親和層析柱NiSepharoseTM6FastFlow(購自GEHealthcareBio-Science公司)進行純化,得到Y035/CD3的雙特異性抗體(SEQIDNO:98),序列如下所示:EVQLVQSGAEVKKPGASVKVSCKASGYTFSDYEMHWVRQAPGQGLEWMGAIHPGSGDTAYNQRFKGRVTITADKSTSTAYMELSSLRSEDTAVYYCARFYSYAYWGQGTLVTVSAGGGGSGGGGSGGGGSDIVMTQTPLSLPVTPGEPASISCRSSQSLVHSNGNTYLQWYLQKPGQSPQLLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSIYVPYTFGQGTKLEIKRGGGGSDIKLQQSGAELARPGASVKMSCKTSGYTFTRYTMHWVKQRPGQGLEWIGYINPSRGYTNYNQKFKDKATLTTDKSSSTAYMQLSSLTSEDSAVYYCARYYDDHYCLDYWGQGTTLTVSSVEGGSGGSGGSGGSGGVDDIQLTQSPAIMSASPGEKVTMTCRASSSVSYMNWYQQKSGTSPKRWIYDTSKVASGVPYRFSGSGSGTSYSLTISSMEAEDAATYYCQQWSSNPLTFGAGTKLELK選擇GPC3表達陽性的HepG2和SK-Hep-1GPC3作為靶細胞,研究了Y035/CD3BiTE在體外的細胞毒性作用,結果顯示,溶度為0.1ng/ml的Y035/CD3BiTE對HepG2的細胞殺傷作用達到約60%,對SK-Hep-1GPC3的細胞作用達到約40%。與CN103833852A所述的GPC3/CD3BiTE相比,細胞毒性顯著增加。在本發明提及的所有文獻都在本申請中引用作為參考,就如同每一篇文獻被單獨引用作為參考那樣。此外應理解,在閱讀了本發明的上述講授內容之后,本領域技術人員可以對本發明作各種改動或修改,這些等價形式同樣落于本申請所附權利要求書所限定的范圍。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1