一種有機合成中間體的合成方法與流程
本發明涉及一種合成方法,特別是一種有機合成中間體的合成方法,具體講本發明是基于Gattermann反應的一種新的合成方法,利用本發明的方法可以合成2個新的有機化合物----有機合成中間體。
背景技術:
Gattermann反應是一個經典的有機人名反應,是在Sandermayer反應基礎上改進的,其參考文獻為基礎有機化學(下冊),作者邢其毅、裴偉偉、徐瑞秋、裴堅,北京高等教育出版社2005出版。該反應是:在少量的金屬銅催化下,芳香族重氮鹽與鹽酸或氫溴酸反應生成氯苯或溴苯。例如:以苯胺為原料合成氯苯,合成路線如下:
。
技術實現要素:
本發明的目的是在現有技術基礎上,提供一種合成方法簡單、一步反應、產率高、成本低的有機合成中間體的合成方法及利用該方法合成新的有機合成中間體,拓寬現有技術的應用范圍。
本發明的有機合成中間體的合成方法,所述的有機合成中間體為2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑,結構式如下:
;
合成步驟如下:
(1)、向干燥的反應瓶中加入2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑、新制的銅粉和濃鹽酸,置于冰水浴中攪拌均勻;
所述的2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑、新制的銅粉和濃鹽酸各成份的用量配比如下:
2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑與新制銅粉的摩爾比為 1∶0.75 ,其中濃鹽酸的用量為過量,所述過量至少為2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑用量的18倍(摩爾倍數);
所述的2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑是熔點為192℃~194℃的白色針狀晶體,苯環上連有甲氧基并且與[1,3,4]噻二唑呈對位;
所述的新制的銅粉是經過稀鹽酸處理并除去其表面氧化膜的銅粉;
所述的濃鹽酸濃度為36-38%;
(2)、取亞硝酸鈉溶于去離子水制成飽和溶液,并置于冰水中;
(3)、以2滴/分鐘的速度向反應瓶中滴加亞硝酸鈉飽和溶液,亞硝酸鈉飽和溶液的用量按如下摩爾比控制:2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑∶亞硝酸鈉∶去離子水= 1∶5∶55;滴加完畢后在室溫下攪拌0.5h,再加熱至60℃,繼續攪拌,至無氣體放出,停止反應;冷卻至室溫,減壓過濾,干燥,用無水乙醇重結晶,除去沒有反應的銅粉,得2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑有機合成中間體;
反應路線如下:
。
本發明的有機合成中間體,為2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑,結構式如下:
。
本發明的合成方法是以 Gattermann 反應為基礎,合成2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑的一種新的合成方法,本發明以 2-氨基-5-(4-甲氧基苯基)-[1,3,4]噻二唑為原料,一步反應,直接合成得到 2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑。在此反應中,反應物分子結構中[1,3,4]噻二唑環上的氨基被氯取代,發生Gattermann 反應;同時,苯環上甲氧基的鄰位氫原子被氯取代,發生了苯環上的親電取代反應。本發明具有合成方法簡單、一步反應、產率高、成本低的優點。
附圖說明
圖1為2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑1H NMR;
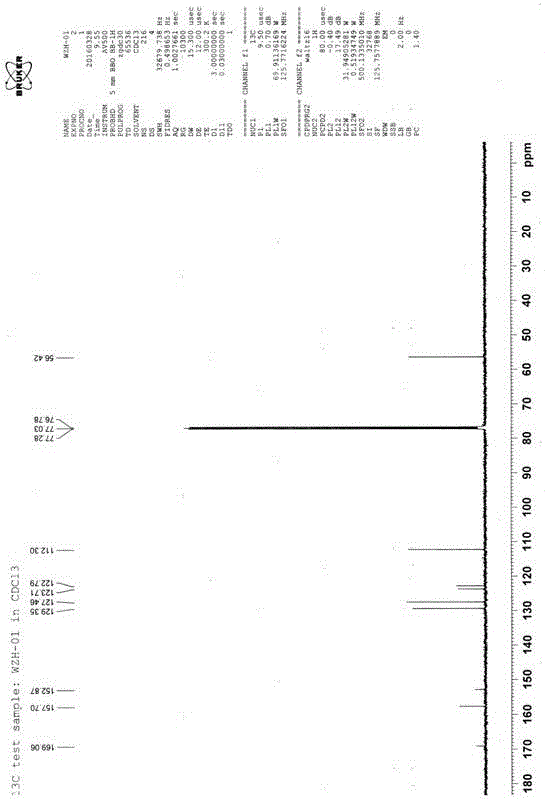
圖2為2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑13C NMR;
圖3為2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑GC-HRMS;
圖4為2-溴-5-(3-溴-4-甲氧基苯基)-[1,3,4]噻二唑1H NMR;
圖5為2-溴-5-(3-溴-4-甲氧基苯基)-[1,3,4]噻二唑13C NMR;
圖6為2-溴-5-(3-溴-4-甲氧基苯基)-[1,3,4]噻二唑GC-HRMS。
具體實施方式
本發明的目的是通過以下技術方案來實現:
1、2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑的合成。
在干燥的反應瓶中,加入2-氨基-5-(4-甲氧基苯基)-1,3,4-噻二唑、新制的銅粉和一定體積的濃鹽酸,置于冰水浴中攪拌均勻。另取一定量的亞硝酸鈉溶于去離子水配制成飽和溶液,置冰水中。然后,緩慢地向反應瓶中滴加亞硝酸鈉飽和溶液,滴加完畢,室溫攪拌0.5h,再加熱至60℃,繼續攪拌,至無氣體放出,停止反應。冷卻至室溫,減壓過濾,干燥,用無水乙醇重結晶,除去過量的銅粉,得到產物,合成路線如下:
。
2、結構確定
所用儀器:X-5型顯微熔點測定儀(溫度未校準,北京泰克儀器有限公司)Avance-500Hz核磁共振儀(瑞士Bruker公司,內標TMS),GCT氣相色譜/飛行時間質譜聯用儀(英國Micromass公司,采集速度10次/秒)。
本發明合成的2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑的相關數據如下:熔點為142~143℃。1H NMR(500Hz,CDCl3)δ7.92(d,J =2.15Hz,1H,2-Ph-H),7.76(dd,J =8.60Hz,2.15Hz,1H,6-Ph-H),7.01(d,J =8.60Hz,1H,5-Ph-H),3.97(s,3H,-OCH3);13C NMR(125Hz,CDCl3)δ169.06, 157.70, 152.87, 129.35, 127.46, 123.71, 122.79, 112.30, 56.42;HRMS (m/z) calcd for C9H6N2OSCl2 [M+H]+ 259.9578, found 259.9582.根據以上數據確定 2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑結構式為:
。
3、合成方法應用
按照本發明的方法,以2-氨基-5-(4-甲氧基苯基)-[1,3,4]噻二唑為原料,氫溴酸替代濃鹽酸,同樣反應條件下,得到2-溴-5-(3-溴-4-甲氧基苯)-[1,3,4]噻二唑。
相關測試數據如下:熔點:168~170℃。1H NMR(500Hz, CDCl3)δ8.1(d, J =2.20Hz, 1H,2-Ph-H),7.81(dd, J =8.55Hz, 2.2Hz, 1H, 6-Ph-H),6.98(d, J =8.60Hz, 1H, 5-Ph-H),3.97(s, 3H,-OCH3);13C NMR(125Hz,CDCl3)δ170.30, 158.52, 137.37, 132.48, 128.30, 122.96, 112.62, 112.05, 56.48;HRMS (m/z) calcd for C9H6N2OSBr2[M+H]+ 349.8547, found.349.8554.確定2-溴-5-(3-溴-4-甲氧基苯基)-[1,3,4]噻二唑結構式為:
。
本發明是通過常規的合成方法,所有試劑均為化學純或分析純。2-氨基-5-(4-甲氧基苯基)-[1,3,4]噻二唑按照文獻合成,白色針狀晶體,熔點192~194℃, 同文獻值,該文獻為GuoGang Tu a,b, ShaoHua Li b, HuiMing Huang b, Gang Li b, Fang Xiong c, Xi Mai b, HuaWei Zhu a, BinHai Kuang b, Wen Fang Xu a,*, Novel aminopeptidase N inhibitors derived from 1,3,4-thiadiazole scaffold, [J]. Bioorganic & Medicinal Chemistry, 16 (2008) 6663–6668。
反應物的具體實驗用量及產物產率:2-氨基-5-(4-甲氧基苯基)-[1,3,4 ]噻二唑2.07g(0.01mol),銅粉0.48g(0.0075mol),亞硝酸鈉3.45g(0.05mol),濃鹽酸30mL,水10mL。產物2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑,橙黃色針狀晶體,1.80g,產率69.08%。
以氫溴酸替代濃鹽酸,相同實驗條件合成得到2-溴-5-(3-溴-4-甲氧基苯基)-[1,3,4]噻二唑,黃色片狀晶體,1.89g,產率54.1%。
本發明反應機理:反應體系中,亞硝酸鈉與鹽酸反應產生亞硝酸,于冰水浴中與2-氨基-5-(4-甲氧基苯基)-[1,3,4]噻二唑反應生成重氮鹽,在銅粉作用下產生氯化亞銅,發生Gattermann反應。過量的亞硝酸與濃鹽酸作用,產生氯氣,以反應中生成氯化亞銅或氯化銅為Lewis酸作催化劑,于苯環上發生氯代反應。由于甲氧基在苯環上是供電子的鄰對位定位基,其苯環對位被富電子的五元雜環噻二唑占據,進一步增加了苯環上電子云密度,從而加熱60℃有利于苯環上發生氯代反應,生成2-氯-5-(3-氯-4-甲氧基苯基)-[1,3,4]噻二唑。也就是說:在此“一鍋反應”中,不僅在[1,3,4]噻二唑環上發生了Gattermann反應,而且同時在苯環上進行了親電取代反應。
- 還沒有人留言評論。精彩留言會獲得點贊!