一種7?氯?2?氧代庚酸乙酯的純化方法與流程
本發明屬于有機化學領域,具體涉及一種西司他丁鈉(CilastatinSodium)關鍵中間體7-氯-2-氧代庚酸乙酯的純化方法。
背景技術:
:西司他丁鈉,結構式如(I)所示,是由美國默克公司在研發β-碳青霉烯類抗生素亞胺培南(imipenem)時研發的一種腎脫氫二肽酶抑制劑,與亞胺培南配伍使用,能有效抑制腎脫氫二肽酶對亞胺培南的降解,并能降低亞胺培南的腎毒性。亞胺培南/西司他丁鈉,已作為一種復合廣譜抗菌制劑被廣泛使用,其在美國的商品名為“Primaxin”。現有技術已經出現多種西司他丁鈉(I)的制備方法,其中以專利US5147868報道的方法最為常用且已實現大規模工業化生產,其工藝路線如下所示:上述方法中,結構式(II)的Z-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸是制備西司他丁鈉(I)的關鍵中間體。在同一篇專利文件中報道了以結構式(III)的7-氯-2氧代庚酸乙酯為起始原料來合成該關鍵中間體的方法,工藝路線如下所示:此外,現有技術中關于7-氯-2-氧代庚酸乙酯(III)也已經出現了多種制備方法的報道,其中最主要的是以下三種方法:I.專利EP48301報道的格氏試劑法,合成路線如下所示:II.文獻J.Med.Chem,1987,30,1074報道的二噻烷法。合成路線如下所示:III.專利US5268501報道的亞硝酰硫酸-甲醛法,合成路線如下所示:由于西司他丁鈉(I)為靜脈注射用藥,臨床制劑對其純度要求很高。但西司他丁鈉(I)為無定形態,本身不易純化。因此,高純度的各中間體,如7-氯-2-氧代庚酸乙酯(III)等能有效減少帶入終產品西司他丁鈉(I)中的雜質。但是,無論是7-氯-2-氧代庚酸乙酯(III),還是上面結構式(IV)的中間體,亦或是制備7-氯-2-氧代庚酸乙酯(III)的起始原料和各中間體,都是液體油狀物,通常只能通過精餾或柱層析的方法進行純化。工業化精餾或柱層析設備投資大、占地大、能耗高且不易得到高純度產物。因此,精餾或柱層析都不是理想的工業化方法。專利US6348617報道了一種7-氯-2-氧代庚酸乙酯的純化方法:先將7-氯-2-氧代庚酸乙酯溶于甲苯等有機溶劑,然后與亞硫酸氫鈉的水溶液反應,得到7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽,然后在酸的作用下分解,得到含量提高的7-氯-2-氧代庚酸乙酯。但是試驗發現該方法得到的7-氯-2-氧代庚酸乙酯仍然含有較多雜質。為了提高西司他丁鈉的純度、保證臨床用藥安全,有必要對7-氯-2-氧代庚酸乙酯(III)的純化方法進行深入研究。技術實現要素:針對上述問題,本發明的一個目的在于提供一種7-氯-2-氧代庚酸乙酯的純化方法。該方法操作簡便、適合工業化生產,得到的7-氯-2-氧代庚酸乙酯純度高,GC檢測純度和含量可達98%以上,總雜不高于2%。為了實現上述發明目的,本發明采用了如下技術方案:一種7-氯-2-氧代庚酸乙酯的純化方法,包含下述步驟:1)將結構式(III)的7-氯-2-氧代庚酸乙酯粗品(油狀物)直接在一定溫度下與亞硫酸氫鹽溶液反應,得到結構式(VI)的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體;或者將結構式(III)的7-氯-2-氧代庚酸乙酯粗品(油狀物)溶于與水相混溶的有機溶劑A,在一定溫度下與亞硫酸氫鹽溶液反應,得到結構式(VI)的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體;2)將步驟1)得到的結構式(VI)的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體過濾,用有機溶劑B洗滌所得固體,干燥;3)將步驟2)得到的所述結構式(VI)的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體溶于水,在一定溫度下加入酸或堿,使7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽分解為結構式(III)的7-氯-2-氧代庚酸乙酯;4)向步驟3)的反應體系加入與水不相溶的有機溶劑C萃取,萃取得到的有機相經脫水后蒸干,得到純度提高的7-氯-2-氧代庚酸乙酯。上述純化方法的反應式,如下所示:其中,M=Na,K,NH4。優選的,所述步驟1)中,所述亞硫酸氫鹽選自亞硫酸氫鈉、亞硫酸氫鉀或亞硫酸氫銨,更優選亞硫酸氫鈉。還優選的,所述步驟1)中,所述亞硫酸氫鹽與7-氯-2-氧代庚酸乙酯的摩爾比可以為1.0~3.0∶1.0,更優選1.2~2.0∶1.0。優選的,所述步驟1)中,所述亞硫酸氫鹽溶液為飽和溶液,通過如下方法制備:將所述亞硫酸氫鹽溶于計算量的水;或將所述亞硫酸氫鹽溶于計算量的水和與水相混溶的有機溶劑A按照一定比例構成的混合溶劑中;所述與水相溶的有機溶劑A選自甲醇、乙醇或四氫呋喃等,更優選乙醇;當優選乙醇時,水和乙醇的體積比為1.0~5.0∶1.0,更優選2.0~3.0∶1.0。優選的,所述步驟1)中,7-氯-2-氧代庚酸乙酯粗品或7-氯-2-氧代庚酸乙酯粗品溶于所述與水相混溶的有機溶劑A得到的溶液采用滴加的方式加入所述亞硫酸氫鹽溶液中;所述與水相溶的有機溶劑A選自甲醇、乙醇或四氫呋喃等,更優選為乙醇,乙醇與7-氯-2-氧代庚酸乙酯粗品的體積重量比(ml:g)為1.0~5.0∶1.0,優選1.0~2.0∶1.0。優選的,所述步驟1)中,反應溫度為0~50℃,更優選為0~30℃。優選的,所述步驟2)中,所述有機溶劑B選自甲醇、乙醇、乙酸乙酯、甲基叔丁醚、二氯甲烷、甲苯、1,2-二氯乙烷和氯仿中的一種或多種;更優選為乙醇或乙酸乙酯。優選的,所述步驟3)中,所述酸與7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽的摩爾比可以為1.0~2.0∶1.0,更優選為1.0~1.5∶1.0。進一步優選的,所述酸選自無機酸,更優選為鹽酸、硫酸和磷酸中的一種或多種,最優選為鹽酸。所述酸可以為濃酸也可以為稀酸。最優選的,所述酸為濃度1.0~6.0mol/L的鹽酸。優選的,所述步驟3)中,所述堿與7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽的摩爾比為1.0~5.0∶1.0,更優選1.0~3.0∶1.0。進一步優選的,所述堿選自無機堿,更優選為碳酸鈉、碳酸氫鈉、碳酸鉀、碳酸氫鉀、氫氧化鈉和氫氧化鉀中的一種或多種,最優選為碳酸鈉。所述堿可以為濃堿也可以為稀堿。最優選的,所述堿為碳酸鈉;碳酸鈉水溶液的重量百分比濃度為5%~10%。優選的,所述步驟3)中,所述溫度為0~60℃,更優選為45~55℃。優選的,上述步驟4)中,所述水不相溶的有機溶劑C選自甲苯、乙酸乙酯、甲基叔丁醚、甲基異丁基甲酮、二氯甲烷、1,2-二氯乙烷和氯仿等中的一種或多種,更優選為甲苯。作為一個可以替代的方案,所述水不相溶的有機溶劑C可以在所述步驟3)中,分解反應開始之前加入7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽的水溶液。為了進一步提高7-氯-2-氧代庚酸乙酯的純度,本發明所述的純化方法還包括7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體的重結晶:在步驟3)之前,將步驟2)得到的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體重結晶一次或多次,得到的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽的精制品再進入步驟3)。優選的,所述重結晶方法為:將步驟2)得到的7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體溶于水中,向所得溶液中滴加與所述水相溶的有機溶劑A,使7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽析出,過濾,干燥,即得7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽的精制品。優選的,所述重結晶步驟中,7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體重量(g)與水的體積(ml)比為1.0∶0.5~5.0,更優選為1.0∶0.5~1.5。所述與水相溶的有機溶劑A選自甲醇、乙醇和四氫呋喃中的一種或多種;更優選為乙醇。所述有機溶劑A與水的體積比為1.0~5.0∶1.0,更優選為2.0~3.0∶1.0。上述重結晶步驟可以重復多次,直至7-氯-2-氧代庚酸乙酯的亞硫酸氫鹽固體的純度達到要求。作為一個優選的實施方式,本發明提供一種7-氯-2-氧代庚酸乙酯的純化方法,包含下述步驟:1)將7-氯-2-氧代庚酸乙酯粗品滴加到亞硫酸氫鈉飽和溶液中,或者將7-氯-2-氧代庚酸乙酯粗品先溶于乙醇,再滴加到亞硫酸氫鈉飽和溶液中,乙醇體積(ml)與7-氯-2-氧代庚酸乙酯粗品的重量(g)比為1.0~5.0∶1.0;0~50℃下反應得到7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉固體;其中,亞硫酸氫鈉與7-氯-2-氧代庚酸乙酯的摩爾比為1.0~3.0∶1.0;亞硫酸氫鈉飽和溶液通過如下方法制備:將所述亞硫酸氫鈉溶于計算量的水;或將所述亞硫酸氫鈉溶于計算量的水和乙醇按照體積比為1.0~5.0∶1.0構成的混合溶劑中;2)將步驟1)得到的7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽過濾,用乙醇或乙酸乙酯洗滌所得固體,干燥;3)將步驟2)所得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉固體溶于水中,向所得溶液中滴加乙醇,使7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽析出,過濾,干燥;得到精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽;其中,7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽固體重量(g)與水的體積(ml)比為1.0:0.5~5.0;乙醇與水的體積比為1.0~5.0:1.0;如有必要,重復上述操作直至所述7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽純度達到要求;4)將步驟3)得到的精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽溶于水,在0~60℃下,加入酸濃度為1.0~6.0mol/L的鹽酸或重量百分比濃度為5%~10%的碳酸鈉水溶液,使7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽分解為7-氯-2-氧代庚酸乙酯;用甲苯萃取一次以上,合并萃取得到的有機相,脫水后蒸干,得到GC檢測純度和含量≥95%的7-氯-2-氧代庚酸乙酯;其中,鹽酸與7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽的摩爾比為1.0~2.0:1.0;碳酸鈉與7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽的摩爾比為1.0~5.0:1.0;每次萃取甲苯的體積(ml)與7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽的重量(g)的比例為0.5~5.0:1.0。作為一個更優選的實施方式,本發明提供一種7-氯-2-氧代庚酸乙酯的純化方法,包含下述步驟:1)將7-氯-2-氧代庚酸乙酯粗品滴加到亞硫酸氫鈉飽和溶液中,或者將7-氯-2-氧代庚酸乙酯粗品先溶于乙醇,再滴加到亞硫酸氫鈉飽和溶液中,乙醇體積(ml)與7-氯-2-氧代庚酸乙酯粗品的重量(g)比為1.0~2.0∶1.0;0~30℃下反應得到7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉固體;其中,亞硫酸氫鈉與7-氯-2-氧代庚酸乙酯的摩爾比為1.2~2.0∶1.0;亞硫酸氫鈉飽和溶液通過如下方法制備:將所述亞硫酸氫鈉溶于計算量的水;或將所述亞硫酸氫鈉溶于計算量的水和乙醇按照體積比為2.0~3.0∶1.0構成的混合溶劑中;2)將步驟1)得到的7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽過濾,用乙醇或乙酸乙酯洗滌所得固體,干燥;3)將步驟2)所得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉固體溶于水中,向所得溶液中滴加乙醇,使7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽析出,過濾,干燥;得到精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽;其中,7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽固體的重量(g)與水的體積(ml)比為1.0:0.5~1.5;乙醇與水的體積比為2.0~3.0:1.0;如有必要,重復上述操作直至所述7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽純度達到要求;4)將步驟3)得到的精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽溶于水,在45~55℃下,加入酸濃度為1.0~6.0mol/L的鹽酸或重量百分比濃度為5%~10%的碳酸鈉,使7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽分解為7-氯-2-氧代庚酸乙酯;用甲苯萃取一次以上,合并萃取得到的有機相,脫水后蒸干,得到GC檢測純度和含量≥95%的7-氯-2-氧代庚酸乙酯;其中,鹽酸與7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽的摩爾比為1.0~1.5:1.0;碳酸鈉與7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽的摩爾比為1.0~3.0:1.0;每次萃取甲苯的體積(ml)與7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽的重量(g)的比例為1.0~2.0:1.0。上述方法中,7-氯-2-氧代庚酸乙酯粗品可以按照現有技術的報道制備,例如
背景技術:
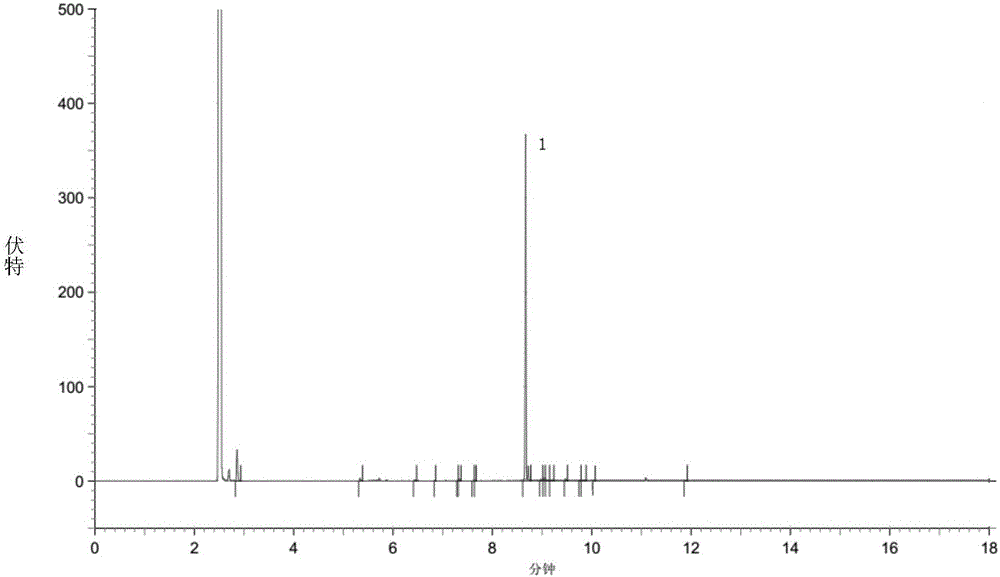
中提到的格氏試劑法(專利EP48301)、二噻烷法(文獻J.Med.Chem,1987,30,1074)或亞硝酰硫酸-甲醛法(專利US5268501)。通過本發明的上述方法制備的7-氯-2-氧代庚酸乙酯的純度和含量可達97%以上,甚至可以高達98%以上、總雜不高于2%。而現有技術中。專利US6348617制備的7-氯-2-氧代庚酸乙酯的純度為85.9%,總雜為13.9%(實施例14)。在下面的具體實施方式部分的對比例1中,發明人重復該現有技術的純化方法,得到的7-氯-2-氧代庚酸乙酯的純度也僅為84.7%(歸一化法),與文獻報道一致。可見,本發明的方法可以顯著提高7-氯-2-氧代庚酸乙酯的純度,減少雜質的含量,并提高下步產物的純度。總之,本發明提供了一種操作簡便、適合工業化生產且能獲得高純度7-氯-2-氧代庚酸乙酯的方法,為制備高純度的西司他丁鈉靜脈注射劑提供了必要的物質基礎,從而可以更好地保證臨床用藥安全。附圖說明以下,結合附圖來詳細說明本發明的實施方案,其中:圖1為實施例1得到的高純度7-氯-2-氧代庚酸乙酯的GC色譜圖,其中1號峰為7-氯-2-氧代庚酸乙酯的吸收峰。圖2為對比例1得到的7-氯-2-氧代庚酸乙酯的GC色譜圖,其中1號峰為7-氯-2-氧代庚酸乙酯的吸收峰。具體實施方式以下參照具體的實施例來說明本發明。本領域技術人員能夠理解,這些實施例僅用于說明本發明,其不以任何方式限制本發明的范圍。下述實施例中的實驗方法,如無特殊說明,均為常規方法。下述實施例中所用的藥材原料、試劑材料等,如無特殊說明,均為市售購買產品。各實施例所用的7-氯-2-氧代庚酸乙酯的粗品(油狀物)可以按照專利US5268501報道的亞硝酰硫酸-甲醛法、專利EP48301報道的格氏試劑法或文獻J.Med.Chem,1987,30,1074報道的二噻烷法制備。高效液相色譜(HPLC)條件:色譜柱以十八烷基硅烷鍵合硅膠為填充劑,規格4.6μm×25cm,以磷酸調節0.05mol/L磷酸氫二鉀溶液pH值至10,加入乙腈配成50/50(V/V)的溶液,以該溶液為流動相,流速1.0ml/min,檢測波長為237nm;氣相色譜(GC)條件:取樣品適量,加乙腈溶解,HP-1型氣相色譜柱;氣化室溫度250℃,檢測器溫度280℃,梯度升溫,初溫60℃,保留3min,再30℃/min,升至230℃,保留10min,分流比30∶1,流速1.2ml/min,進樣量0.2μl。此條件下7-氯-2-氧代庚酸乙酯的保留時間為8.67min。實施例17-氯-2-氧代庚酸乙酯的純化1)室溫下,將50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,GC歸一含量60.6%,外標含量58.3%,相當于含有7-氯-2-氧代庚酸乙酯29.2g,0.14mol)緩慢滴入由21.9g亞硫酸氫鈉(0.21mol)溶于37ml水配成的飽和溶液中,控制滴加速度,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌,約0.5h后析出白色固體。2)將步驟1)得到的反應混合物于0~5℃繼續攪拌2h后過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)40.1g。3)室溫下,將步驟2)所得40.1g白色固體溶于25ml水中,向所得溶液中滴加60ml無水乙醇,逐漸析出白色固體。滴畢,于0~5℃繼續攪拌2h,過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)39.0g,熔點170~172℃,HPLC顯示其歸一含量為98.1%。4)步驟3)所得39.0g白色固體(0.13mol)溶于50ml水中,加入50ml甲苯,加熱至50~55℃,然后緩慢滴入6mol/L鹽酸25ml(0.15mol),滴畢,繼續于50~55℃反應,每隔1h取樣HPLC監測反應進程,約2h反應完畢。將反應液冷至室溫,分液,分出上層甲苯層,向下層水層加入甲苯萃取2次,每次50ml,合并甲苯層;甲苯萃取液加入100ml飽和鹽水洗滌一次,加入無水硫酸鈉干燥,過濾,以少量甲苯洗滌濾渣,收集洗滌液,與干燥后的甲苯萃取液合并,減壓濃縮回收甲苯,得7-氯-2-氧代庚酸乙酯油狀物25.0g,收率86.5%,氣相色譜(GC)歸一含量98.6%(氣相色譜面積歸一化結果,見表1),外標含量98.3%。表1實施例1的氣相色譜面積歸一化結果表保留時間峰高面積分離度(USP)面積百分比8.35520341182980.000.2658.6675552464681514811.0798.6128.982302512793710.950.4049.07942966496613.490.719總計56460226911044—100.00實施例27-氯-2-氧代庚酸乙酯的純化1)室溫下,將18.7g亞硫酸氫鈉(0.18mol)溶于32ml水,然后加入11ml無水乙醇,攪拌均勻;將50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,GC歸一含量64.3%,外標含量62.4%,相當于含有7-氯-2-氧代庚酸乙酯31.2g,0.15mol)緩慢滴入,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌,約0.5h后析出白色固體。2)將步驟1)得到的反應混合物于0~5℃繼續攪拌3h后過濾,以適量乙酸乙酯洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)43.9g。3)室溫下,將步驟2)所得43.9g白色固體溶于30ml水中,向所得溶液中滴加90ml無水乙醇,逐漸析出白色固體。滴畢,于0~5℃繼續攪拌2h,過濾,以適量乙酸乙酯洗滌濾餅,抽干,干燥,得精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)42.1g,HPLC顯示其歸一含量98.3%。4)將上步得到的42.1g白色固體(0.14mol)溶于50ml水中,加熱至45~50℃,然后緩慢滴入6mol/L鹽酸30ml(0.18mol),滴畢,于45~50℃繼續反應,每隔1h取樣HPLC監測反應進程,約2h反應完畢。將反應液冷至室溫,加入50ml甲苯,分液,分出甲苯層(上層),向水層(下層)加入甲苯萃取2次,每次50ml,合并甲苯層,加入100ml飽和鹽水洗滌一次,加入5無水硫酸鈉干燥2h,過濾,以少量甲苯洗滌濾渣,收集甲苯洗滌液,與甲苯萃取液合并,減壓濃縮回收甲苯,得7-氯-2-氧代庚酸乙酯油狀物26.9g,收率86.2%,氣相色譜(GC)歸一含量98.7%,外標含量98.5%。實施例37-氯-2-氧代庚酸乙酯的純化1)室溫下,將50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,GC歸一含量50.8%,外標含量49.6%,相當于含有7-氯-2-氧代庚酸乙酯24.8g,0.12mol)溶于50ml無水乙醇,然后緩慢滴入由16.2g亞硫酸氫鈉(0.16mol)溶于28ml水配成的飽和溶液中,控制滴加速度,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌,約0.5h后析出白色固體。2)將步驟1)得到的反應混合物于0~5℃繼續攪拌2h后過濾,以適量甲苯洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉(白色固體)34.7g。3)室溫下,將步驟2)所得34.7g白色固體溶于30ml水中,向所得溶液中滴加90ml無水乙醇,逐漸析出白色固體。滴畢,于0~5℃繼續攪拌2h,過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉(白色固體)33.3g,HPLC顯示其歸一含量93.6%。4)室溫下,將步驟3)所得33.3g白色固體溶于20ml水中,向所得溶液中滴加60ml無水乙醇,逐漸析出白色固體。滴畢,于0~5℃下繼續攪拌2h,過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉精制品(白色固體)32.1g,HPLC顯示其歸一含量98.8%。5)將步驟4)所得32.1g白色固體(0.11mol)溶于30ml水中,加入30ml甲苯,加熱至50~55℃,然后緩慢滴入6mol/L鹽酸28ml(0.17mol),滴畢,繼續于50~55℃反應,每隔1h取樣HPLC監測反應進程,約2h反應完畢。將反應液冷至室溫,分液,分出上層甲苯層,向下層水層加入甲苯萃取2次,每次50ml,合并甲苯層,加入100ml飽和鹽水洗滌一次,加入無水硫酸鈉干燥2h,過濾,以少量甲苯洗滌濾渣,收集甲苯洗滌液,與甲苯萃取液合并,減壓濃縮回收甲苯,得7-氯-2-氧代庚酸乙酯油狀物20.6g,收率83.2%,氣相色譜(GC)歸一含量98.5%,外標含量98.3%。實施例47-氯-2-氧代庚酸乙酯的純化1)室溫下,將50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,GC歸一含量60.6%,外標含量58.3%,相當于含有7-氯-2-氧代庚酸乙酯29.2g,0.14mol)緩慢滴入由21.9g亞硫酸氫鈉(0.21mol)溶于37ml水配成的飽和溶液中,控制滴加速度,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌,約0.5h后析出白色固體。2)將步驟1)得到的反應混合物于0~5℃繼續攪拌2h后過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)40.1g,HPLC顯示其歸一含量為89.3%。3)將上步反應所得40.1g白色固體溶于50ml水中,加入50ml甲苯,加熱至50~55℃,然后緩慢滴入6mol/L鹽酸25ml(0.15mol),滴畢,繼續于50~55℃反應,每隔1h取樣HPLC監測反應進程,約2h反應完畢。將反應液冷至室溫,分液,分出上層甲苯層,向下層水層加入甲苯萃取2次,每次50ml,合并甲苯層,加入100ml飽和鹽水洗滌一次,加入無水硫酸鈉干燥,過濾,以少量甲苯洗滌濾渣,收集甲苯洗滌液,與甲苯萃取液合并,減壓濃縮回收甲苯,得7-氯-2-氧代庚酸乙酯油狀物25.0g,收率86.5%,氣相色譜(GC)歸一含量88.6%,外標含量87.5%。實施例57-氯-2-氧代庚酸乙酯的純化1)室溫下,將50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,氣相色譜(GC)歸一含量60.6%,外標含量58.3%,相當于含有7-氯-2-氧代庚酸乙酯29.2g,0.14mol)緩慢滴入由21.9g亞硫酸氫鈉(0.21mol)溶于37ml水配成的飽和溶液中,控制滴加速度,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌,約0.5h后析出白色固體。2)將步驟1)得到的反應混合物于0~5℃繼續攪拌2h后過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)40.1g。3)室溫下,將步驟2)所得40.1g白色固體溶于25ml水中,向所得溶液中滴加60ml無水乙醇,逐漸析出白色固體。滴畢,于0~5℃繼續攪拌2h,過濾,以適量無水乙醇洗滌濾餅,抽干,干燥,得精制7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉鹽(白色固體)39.0g,HPLC顯示其歸一含量為98.6%。4)將步驟3)所得39.0g白色固體(0.13mol)溶于50ml水中,加入50ml甲苯,加熱至50~55℃,然后緩慢滴入10%(wt%)碳酸鈉溶液413.4g(0.39mol),滴畢,繼續于50~55℃反應,每隔1h取樣HPLC監測反應進程,約2h反應完畢。將反應液冷至室溫,分液,分出上層甲苯層,向下層水層加入甲苯萃取2次,每次50ml,合并甲苯層,加入100ml飽和鹽水洗滌一次,加入無水硫酸鈉干燥,過濾,以少量甲苯洗滌濾渣,收集甲苯洗滌液,與甲苯萃取液合并,減壓濃縮回收甲苯,得7-氯-2-氧代庚酸乙酯油狀物24.4g,收率83.7%,氣相色譜(GC)歸一含量98.2%,外標含量97.6%。實施例67-氯-2-氧代庚酸乙酯的純化1)室溫下,50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,GC歸一含量60.6%,外標含量58.3%,相當于含有7-氯-2-氧代庚酸乙酯29.2g,0.14mol)溶于30ml四氫呋喃,將該溶液緩慢滴入由20.4g亞硫酸氫鈉(0.20mol)溶于35ml水配成的飽和溶液中,控制滴加速度,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌,約0.5h后析出白色固體。2)將步驟1)得到的反應混合物于0~5℃繼續攪拌2h后過濾,以適量四氫呋喃洗滌濾餅,抽干,干燥,得7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉(白色固體)41.8g。3)室溫下,將步驟2)所得41.8g白色固體溶于30ml水中,向所得溶液中滴加90ml四氫呋喃,逐漸析出白色固體。滴畢,于0~5℃繼續攪拌2h,過濾,以適量四氫呋喃洗滌濾餅,抽干,干燥,得精制的7-氯-2-氧代庚酸乙酯的亞硫酸氫鈉(白色固體)40.1g,HPLC顯示其歸一含量98.6%。4)將步驟3)所得40.1g白色固體(0.13mol)溶于50ml水中,加入50ml甲基叔丁醚,加熱至45~50℃,然后緩慢滴入10%(wt%)碳酸氫鈉溶液252.0g(0.30mol),滴畢,于50~55℃繼續反應,每隔1h取樣HPLC監測反應進程,約2h反應完畢。將反應液冷至室溫,分液,分出上層甲基叔丁醚層,向下層水層加入甲基叔丁醚萃取2次,每次50ml,合并甲基叔丁醚層,加入100ml飽和鹽水洗滌一次,加入無水硫酸鈉干燥2h,過濾,以少量甲基叔丁醚洗滌濾渣,收集甲基叔丁醚洗滌液,與甲基叔丁醚萃取液合并,減壓濃縮回收甲基叔丁醚,得7-氯-2-氧代庚酸乙酯油狀物24.1g,收率82.6%,氣相色譜(GC)歸一含量98.4%,外標含量97.5%。對比例17-氯-2-氧代庚酸乙酯的純化取7-氯-2-氧代庚酸乙酯油狀物粗品(氣相色譜(GC)歸一含量60.6%,外標含量58.3%),按照專利US6348617報道的方法純化。具體操作如下:室溫下,50.0g7-氯-2-氧代庚酸乙酯粗品(油狀物,GC歸一含量60.6%,外標含量58.3%,相當于含有7-氯-2-氧代庚酸乙酯29.2g,0.14mol)溶于50ml甲苯,將該溶液緩慢滴入由17.5g亞硫酸氫鈉(0.17mol)溶于70ml水的溶液中,控制滴加速度,使反應液溫度維持室溫。滴加完畢后,室溫下攪拌2h,然后向反應混合物中加入50ml甲苯,分液,收集水層I,待用。向甲苯層中加入8.7g亞硫酸氫鈉(0.084mol)溶于35ml水的溶液,室溫下攪拌1h,分液,收集水層II,水層II與水層I合并,得到水溶液。向上步所得的水溶液中加入50ml甲苯,將反應混合物加熱至50~55℃,然后緩慢滴入濃鹽酸42ml(0.51mol),約1h滴加完畢。滴畢,保溫50~55℃攪拌40min,分液,加入50ml水洗滌甲苯層,收集甲苯層,加入無水硫酸鈉干燥,過濾,收集濾液,減壓濃縮回收甲苯,得黃色油狀物,氣相色譜(GC)外標法顯示其中含7-氯-2-氧代庚酸乙酯27.1g(收率93.5%),歸一含量84.7%(氣相色譜面積歸一化結果,見表2),總雜15.3%。表2對比例1的氣相色譜結果表保留時間峰高面積分離度(USP)面積百分比2.8612518543721930.0010.1195.335218352655269.220.7226.437113911418334.000.3866.8382556247313.390.0677.3032679250517.570.0687.33515207157101.190.4277.619323836749.710.1007.648149915341.000.0428.6692816926311653135.8984.7318.972108251270810.670.3459.04322210229102.540.6239.1057508172001.530.4689.1999146119892.230.3269.47218391219098.700.5969.758343538249.500.1049.8527920222861.700.60610.042342439293.410.10711.8783484605747.070.165總計32135283678167—100.00試驗例1Z-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸的制備以本發明實施例1所得的純化的7-氯-2-氧代庚酸乙酯,參考專利WO2008138228報道的方法制備Z-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸(II)。具體操作為:將實施例1所得的25.0g7-氯-2-氧代庚酸乙酯(GC歸一含量98.3%,外標含量98.5%),13.5g(+)-S-2,2-二甲基環丙烷甲酰胺和0.15g對甲苯磺酸加入125ml甲苯中,加熱回流,以甲苯與水共沸帶出反應產生的水,帶反應完畢后,降溫至室溫,先后分別以10%的稀鹽酸(100ml×3)和10%的亞硫酸氫鈉溶液(100ml×3)洗滌反應液三次。洗滌完畢后,分出甲苯層,加入無水硫酸鈉干燥。過濾,減壓濃縮回收甲苯,得36.4g棕色粘稠液體,產品不作分離直接用于下步反應。將上一步反應所得36.4g棕色粘稠液體加入60ml乙醇和75g10%的氫氧化鈉溶液中,加熱至45~50℃,保溫攪拌使其反應,HPLC監控反應過程,約10h反應完畢;然后加入叔丁基醚洗滌反應液三次,每次加入叔丁基醚100ml,棄去有機層,向水層中加濃鹽酸酸化,調節pH至3~3.5,加入乙酸乙酯萃取酸化液三次,每次加入乙酸乙酯的量為100ml,棄去水層,向乙酸乙酯層加入無水硫酸鈉干燥,然后過濾,減壓濃縮濾液并回收乙酸乙酯,獲得31.6g棕色粘稠液體。室溫下將31.6g棕色粘稠液體溶于80ml二氯甲烷中,然后加入240ml甲苯,攪拌均勻后將所得溶液置于0℃靜置12h,過濾,抽干,收集溶液中析出的大量固體,真空干燥,得(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸(白色固體)15.6g。同時將結晶后得母液減壓濃縮至恒重,得13.6g棕色粘稠溶液,依照上述方法,在室溫下將13.6g棕色粘稠溶液加入30ml二氯甲烷和75ml甲苯,0℃靜置12h,收集溶液中析出的固體,真空干燥,得(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸(白色固體)3.2g。前后兩次共得(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸(白色固體)18.8g,HPLC測定其純度為98.8%,以7-氯-2-氧代庚酸乙酯計算的(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸的收率為57.8%。試驗例2Z-7-氯-2-(2,2-二甲基環丙基甲酰胺基)-2-庚烯酸的制備以對比例1純化得到的7-氯-2-氧代2庚酸乙酯,參考專利WO2008138228報道的方法制備Z-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸。具體操作如下:將對比例1所得的7-氯-2-氧代庚酸乙酯(GC歸一含量84.8%,總雜15.2%,含7-氯-2-氧代庚酸乙酯27.1g)油狀物,14.8g(+)-S-2,2-二甲基環丙烷甲酰胺和0.16g對甲苯磺酸加入145ml甲苯中,加熱回流,以甲苯與水共沸帶出反應產生的水,帶反應完畢后,降溫至室溫,先后分別以10%的稀鹽酸(100ml×3)和10%的亞硫酸氫鈉溶液(100ml×3)洗滌反應液三次。洗滌完畢后,分出甲苯層,加入無水硫酸鈉干燥。過濾,減壓濃縮回收甲苯,得38.1g棕色粘稠液體,產品不作分離直接用于下步反應。將上一步反應所得38.1g棕色粘稠液體加入60ml乙醇和70g10%的氫氧化鈉溶液中,加熱至45~50℃,保溫攪拌使其反應,HPLC監控反應過程,約10h反應完畢;然后加入叔丁基醚洗滌反應液三次,每次加入叔丁基醚90ml,棄去有機層,向水層中加濃鹽酸酸化,調節pH至3~3.5,加入乙酸乙酯萃取酸化液三次,每次加入乙酸乙酯的量為90ml,棄去水層,向乙酸乙酯層加入無水硫酸鈉干燥,然后過濾,減壓濃縮濾液并回收乙酸乙酯,獲得33.2g棕色粘稠液體。室溫下將33.2g棕色粘稠液體溶于75ml二氯甲烷中,然后加入225ml甲苯,攪拌均勻后將所得溶液置于0℃靜置12h,過濾,抽干,收集溶液中析出的大量固體,真空干燥,得(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸(白色固體)13.2g,HPLC測定其純度為93.5%。將結晶后得母液減壓濃縮至恒重,得14.9g棕色粘稠溶液,依照上述方法,在室溫下將14.9g棕色粘稠溶液加入30ml二氯甲烷和75ml甲苯,0℃靜置12h,溶液中出現粘稠油狀物,未能析出白色固體。后嘗試多種重結晶方法,都未能析出固體。與試驗例1相同的方法和條件下,本試驗例以對比例1純化得到的7-氯-2-氧代2庚酸乙酯制備Z-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸,通過簡單重結晶手段只能得到13.2g白色固體,HPLC測定其純度為93.5%,以7-氯-2-氧代庚酸乙酯計算的(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸(II)的收率為36.8%。本試驗例所得(Z)-7-氯-2-((S)-2,2-二甲基環丙基甲酰胺基)-2-庚烯酸的純度和收率均低于試驗例1。正是由于本發明提供的純化方法提高了油狀7-氯-2-氧代2庚酸乙酯的純度,才顯著提高后續反應產物的純度和產率。以上對本發明具體實施方式的描述并不限制本發明,本領域技術人員可以根據本發明作出各種改變或變形,只要不脫離本發明的精神,均應屬于本發明所附權利要求的范圍。當前第1頁1 2 3
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1