原肌球蛋白相關激酶(TRK)抑制劑的藥物制劑的制作方法
本發明涉及一種原肌球蛋白相關激酶抑制劑(tropomyosin-relatedkinaseinhibitor)(“trk抑制劑”),即3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的藥物制劑,以及3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式,即3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物。所述一水合物形式具有促進將3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制成藥物制劑的期望性質。所述trk抑制劑微晶溶液藥物制劑包含呈一水合物形式的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺,其顯示出相比無水物形式而言改善的特性。本發明還涉及trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的延長釋放藥物制劑,其包含負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球。本發明還涉及使用這些藥物制劑治療疾病包括炎性疾病、自身免疫性疾病、骨代謝缺陷和癌癥,以及治療骨關節炎(oa)、疼痛、術后疼痛和與oa有關的疼痛中的用途。所述trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺和制備所述trk抑制劑的方法披露于國際專利申請pct/us14/69469和美國專利申請14/564,773,各自標題為原肌球蛋白相關激酶(trk)抑制劑,通過引用將其并入本文。
背景技術:
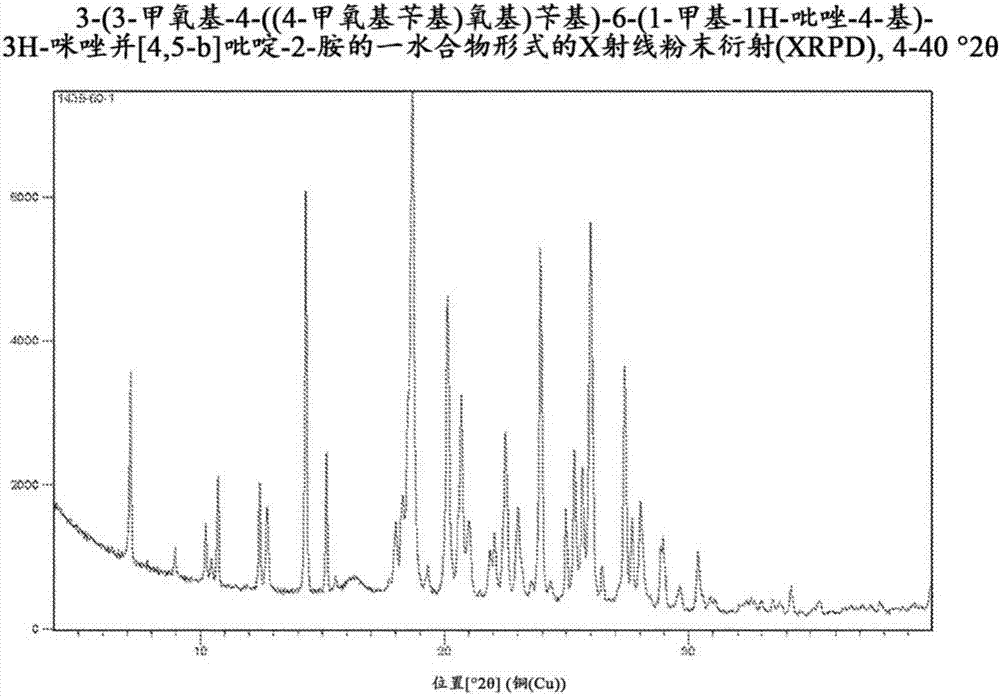
:不適用技術實現要素:本發明的第一方面涉及trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的結晶形式,其中使用cukα輻射測量的x射線粉末衍射圖含有以下2θ峰:7.14、8.89、10.22、12.42、12.73和14.31。本發明的第二方面涉及藥物制劑,其包含trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的結晶形式和藥用賦形劑,其中使用cukα輻射測量的x射線粉末衍射圖含有以下2θ峰:7.14、8.89、10.22、12.42、12.73和14.31。本發明的第三方面涉及trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式。本發明的第四方面涉及藥物制劑,其包含trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式和藥用賦形劑。本發明的第五方面涉及延長釋放藥物制劑,其包含負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球。在第六方面,本發明涉及制備3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的結晶形式的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺與溶劑混合以形成混懸液;b.攪拌混懸液;c.通過過濾收集混懸液中的固體;和d.使固體干燥。在第七方面,本發明涉及制備3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺與溶劑混合以形成混懸液;b.攪拌混懸液;c.通過過濾收集混懸液中的固體;和d.使固體干燥。在第八方面,本發明涉及通過溶劑萃取制備負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶于有機溶劑以形成藥物溶液;b.添加聚合物至藥物溶液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液;c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液混合至水溶液中以形成乳液;d.添加去離子水至乳液;e.通過溶劑萃取從乳液中形成微球;和f.使用表面活性劑溶液篩分所得微球。以及在第九方面,本發明涉及通過溶劑萃取制備負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散于有機溶劑以形成藥物混懸液;b.添加聚合物至藥物混懸液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液;c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液與水溶液混合以形成乳液;d.添加去離子水至乳液;e.通過溶劑萃取從乳液中形成微球;和f.使用表面活性劑溶液篩分所得微球。在第十一方面,本發明涉及通過噴霧干燥制備負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶于有機溶劑以形成藥物溶液;b.添加聚合物至藥物溶液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液;和c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液通過噴霧器泵入干燥器以形成球狀顆粒。在第十二方面,本發明涉及通過噴霧干燥制備負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散于有機溶劑以形成藥物混懸液;b.添加聚合物至藥物混懸液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液;和c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液通過噴霧器泵入干燥器以形成球狀顆粒。附圖說明圖1:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的x射線粉末衍射(xrpd),4-40°2θ。使用cukα測量的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的xrpd顯示出在7.14、8.89、10.22、12.42、12.73和14.312θ峰處的獨特峰。圖2:以10℃/min加熱的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的差示掃描量熱法(dsc)和熱重量分析(tga)熱解曲線。所述dsc熱解曲線展現在76.72、160.13和195.78℃的三個熱事件,所述tga熱解曲線顯示出在25-100℃的3.7%重量損失。圖3:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的結晶結構。展現出trk抑制劑的一水合物形式的結晶結構。圖4:實驗性xrpd圖與由單晶結構計算出的xrpd圖的疊加。該圖展現了實驗性粉末圖與從單晶結構計算出的圖的疊加。強的匹配度表明,單晶結構表示散裝材料(bulkmaterial)。圖5:api載量對ivr分布(profile)的作用-12%api/9:1r202h:752h、16%api/9:1r202h:752h和20%api/9:1r202h:752h微球。該圖比較了3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺負載對不同組成的微球的體外釋放分布的作用。圖6:16%api/9:1r202h:752h和20%api/9:1r202h:752h微球的dsc熱解曲線。所述dsc熱解曲線表明20%微球顯示130-150℃的熔化吸熱,這證實了存在表面藥物晶體。圖7:16%api/9:1r202h:752h微球的掃描電子顯微鏡(sem)視圖(1500x)。所述16%載藥微球未顯示藥物晶體,指示藥物為無定形的。圖8:20%api/9:1r202h:752h微球的掃描電子顯微鏡(sem)視圖(1500x)。所述20%載藥微球顯示表面藥物晶體。圖9:api載量對ivr分布的作用-15%api/r202h、17%api/r202h和19%api/r202h微球。該圖比較了3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺負載對不同組成的微球的體外釋放分布的作用。圖10:api載量對ivr分布的作用-16%api/9.5:0.5r202h:752h、18%api/9.5:0.5r202h:752h和20%api/9.5:0.5r202h:752h微球。該圖比較了3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺負載對不同組成的微球的體外釋放分布的作用。圖11:聚合物共混物對ivr分布的作用-16%api/r202h、16%api/9.0:0.5r202h:rg752h和16%api/9:1r202h:rg752h微球。該圖比較了聚合物共混物對不同組成的微球的體外釋放分布的作用。圖12:聚合物共混物對ivr分布的作用-16%api/r202h、16%api/9.5:0.5r202h:rg502h和16%api/9:1r202h:rg502h微球。該圖比較了聚合物共混物對不同組成的微球的體外釋放分布的作用。圖13:顯示歷時180天的零級ivr分布的制劑-15%api/9:1r203h:rg752h和16%api/9.5:0.5r202h:rg502h微球。使用比率為9:1的r203h:752h聚合物中15%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺以及比率為9.5:0.5的r202h:rg502h聚合物中16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制備的微球展現出歷時6個月的假零級釋放分布。圖14:制備中的共溶劑系統對ivr分布的作用-16%api/9:1r203h:rg752h微球-9:1dcm:meoh、9:0.5:0.5dcm:meoh:ba、9.5:.05dcm:ba、9:1dcm:ba。該圖比較了微球制備中使用的共溶劑系統對含有16%藥物載量和9:1r203h:rg752h的聚合物共混物的微球的體外釋放分布的作用。圖15:用于增加api載量的dcm:ba共溶劑系統對ivr分布的作用-16%api/9:1r202h:rg752h、25%api/9:1r202h:rg752h、30%api/r202h、40%api/r202h、25%api/r203h、30%api/r203h、40%api/r203h、50%api/r203h微球。該圖比較了用于增加藥物載量的微球制備中使用的共溶劑系統對不同聚合物共混物的微球的體外釋放分布的作用。圖16:用微粒化混懸液微囊化方法(micronizedsuspensionmicroencapsulationprocess)制備的微球的掃描電子顯微鏡(sem)視圖(1500x)。通過包囊3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的混懸液產生的微球是球形的,其由于存在嵌入表面的藥物晶體而具有粗糙的表面紋理(texture)。圖17:微粒化混懸液微囊化方法對ivr分布的作用-25%api/9:1r202h:rg752h39ml5%pva+2.6mlea,25%api/9:1r202h:rg752h39ml5%pva+3.25mlea,25%api/r203h39ml5%pva+2.0mlea,30%微流化api/9:1r202h:rg752h39ml5%pva+2.0mlea,40%微流化api/9:1r202h:rg752h39ml5%pva+2.0mlea,30%微流化api/9:1r202h:rg752h39ml5%pva+2.0mlea,30%微流化api/9:1r202h:rg752h39ml5%pva+2.3mlea,30%微流化api/r202s39ml5%pva+2.0mlea,30%微流化api/r203s39ml5%pva+2.0ml微球。該圖比較了在微球制備中使用的微粒化混懸液微囊化方法對具有不同藥物載量的微球的體外釋放分布的作用。圖18:通過溶劑萃取制備的16%api/9:1r202h:rg752h微球的掃描電子顯微鏡(sem)視圖(1000x)。溶劑萃取微球是球形的,具有光滑的表面紋理。圖19:通過噴霧干燥制備的16%api/9:1r202h:rg752h微球的掃描電子顯微鏡(sem)視圖(1000x)。噴霧干燥的微球是球形的,具有一些表面紋理。圖20:微囊化方法對ivr分布的作用-16%api/9:1r202h:rg752h通過溶劑萃取的微球(ow)、16%api/9:1r202h:rg752h通過噴霧干燥的微球(20%和22.5%聚合物)和16%api/9:1r203h:rg752h通過噴霧干燥的微球(22.5%聚合物)。該圖比較了通過溶劑萃取和噴霧干燥制備的負載16%藥物的9:1r202h:rg752h微球的體外釋放分布。圖20:微囊化方法對ivr分布的作用-16%api/9:1r202h:rg752h通過溶劑萃取的微球(ow)、16%api/9:1r202h:rg752h通過噴霧干燥的微球(20%和22.5%聚合物)和16%api/9:1r203h:rg752h通過噴霧干燥的微球(22.5%聚合物)。該圖顯示了微囊化方法對不同制劑的微球的體外釋放分布的作用。圖21:噴霧干燥的16%api/1:1r202h:r203h/無添加劑微球的掃描電子顯微鏡(sem)視圖(1000x)。示出噴霧干燥的16%api/1:1r202h:r203h/無添加劑的微球。圖22:噴霧干燥的16%api/1:1r202h:r203h/31.25mgpeg微球的掃描電子顯微鏡(sem)視圖(1000x)。示出噴霧干燥的16%api/1:1r202h:r203h/31.25mgpeg微球。圖23:噴霧干燥的16%api/1:1r202h:r203h/31.25mg泊洛沙姆407微球的掃描電子顯微鏡(sem)視圖(1000x)。示出噴霧干燥的16%api/1:1r202h:r203h/31.25mg泊洛沙姆407微球。圖24:1%10kdapeg或1%泊洛沙姆407對ivr分布的作用-16%api/1:1r202h:r203h/無添加劑、16%api/1:1r202h:r203h/31.25mgpeg、16%api/1:1r202h:r203h/31.25mg泊洛沙姆407。該圖比較了通過噴霧干燥制備的16%api/1:1r202h:r203h/無添加劑微球、16%api/1:1r202h:r203h/31.25mgpeg微球和16%api/1:1r202h:r203h/31.25mg泊洛沙姆407的體外釋放分布。圖25:體內(大鼠)ivr分布-16%api/9:1202h:rg502h和15%api/9:1r203h:rg752h微球。該圖顯示了歷經約3-4個月和5-6個月對于16%api/9:1202:h:rg502h和15%api/9:1r203h:rg752h微球的體內近零級釋放。圖26:隨時間保留的[14c]3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺(大鼠膝關節)-16%api/9:1202h:rg502h和15%api/9:1203h:rg752h微球。關節內給予至大鼠膝關節后,對于16%api/9:1202:h:rg502h和15%api/9:1r203h:rg752h微球顯示持續5至6個月的藥物釋放;16%api/9:1202:h:rg502h顯示5個月后在關節中保留12%且15%api/9:1r203h:rg752h顯示6個月后保留30%藥物。圖27:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺濃度-時間分布(大鼠血液)-16%api/9:1202:h:rg502h和15%api/9:1r203h:rg752h微球。該圖顯示關節內給予負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球后血液中的藥物濃度-時間分布。圖28:ivr分布-16%api/9:1202:h:rg752h、15%api/9:1r203h:rg752h和40%api/203h微球。圖29:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺濃度-時間分布-16%api/9:1202:h:rg752h、15%api/9:1r203h:rg752h和40%api/203h微球。圖30:形式1至4(無水物和水合物)的測量或模擬xrpd。示出3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的無水物和水合物形式的xrpd。圖31:形式5(乙醇)的xrpd。呈現3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的形式5(乙醇)的xrpd。圖32:形式9(丙酮)的xrpd。呈現3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的形式9(丙酮)的xrpd。圖33:形式10(丙酮)和形式9(丙酮)的xrpd比較。該圖提供了在丙酮中獲得的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的兩種形式的比較。圖34:形式11(乙腈)的xrpd。呈現3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的形式11(乙腈)的xrpd。圖35:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的固體結晶相。該圖提供了實驗中獲得的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的十種結晶形式的比較。具體實施方式本發明涉及一種原肌球蛋白相關激酶抑制劑(“trk抑制劑”),即3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的藥物制劑,以及3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式。所述trk抑制劑微晶溶液藥物制劑包含呈其一水合物形式的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺,其相對于無水物形式而言顯示出改善的特性。本發明還涉及trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的延長釋放藥物制劑,其包含負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球。本發明還涉及使用這些藥物制劑治療疾病包括炎性疾病、自身免疫性疾病、骨代謝缺陷和癌癥,以及治療骨關節炎(oa)、疼痛、術后疼痛和與oa有關的疼痛中的用途。本發明的trk抑制劑的藥物制劑抑制原肌球蛋白相關激酶a(trka)、原肌球蛋白相關激酶b(trkb)、原肌球蛋白相關激酶c(trkc)和c-fms(集落刺激因子-1(csf-1)的細胞受體)。原肌球蛋白相關激酶(trk)是由稱為神經營養因子(neutrophin,nt)的可溶性生長因子活化的高親和力受體。trka也稱為神經營養性酪氨酸激酶受體1型,由神經生長因子(ngf)活化。trkb由腦源性生長因子和nt-4/5活化。trkc由nt3活化。trk的活化導致牽涉細胞信號傳導的下游激酶的活化,包括細胞增殖、存活、血管生成和轉移。trk牽涉許多疾病,包括oa。本發明的trk抑制劑的藥物制劑也可抑制c-fms(集落刺激因子-1(csf-1)的細胞受體)。c-fms在調節巨噬細胞功能中發揮作用,且被認為是在炎性疾病、自身免疫性疾病、骨代謝缺陷和癌癥中發揮作用(burnsandwilks,2011,informahealthcare)。oa是以慢性疼痛和關節軟骨的破壞為特征的流行和使人虛弱的關節疾病。最近的臨床試驗已經證實在oa膝蓋疼痛中阻斷ngf的作用,證明通過靜脈內輸注抗ngf阻斷抗體治療的患者中顯著的疼痛緩解和高像應率(lane,2010,nengljmed)。然而,由于全身抑制ngf信號傳導(fda關節炎咨詢委員會討論與抗神經生長因子因子藥物相關的安全問題會議;http://www.fda.gov/advisorycommittees/calendar/ucm286556.htm),這種方式(modality)可能導致不良事件的風險增加。因此,通過開發trk抑制劑,特別是trka抑制劑,ngf的高親和力受體,采用了靶向ngf介導的oa疼痛的新方法(nicol,2007,molecularinterv)。本發明的trk抑制劑被局部遞送,從而避免了靜脈內抗ngf給予觀察到的全身分布(distribution)。該治療策略通過允許在非局部位點維持生理必需的ngf信號傳導(即感覺/交感神經維持,血管發生)來提供增強的劑量方便性以及更高的安全性。本發明涉及trk抑制劑的藥物制劑和使用trk抑制劑的藥物制劑治療疾病的方法。更具體地,本發明涉及用trk抑制劑的藥物制劑治療疼痛、oa、與oa有關的疼痛、術后疼痛、炎性疾病、自身免疫性疾病、骨代謝缺陷和癌癥的方法。trk抑制劑的藥物組合物可以多種劑型給予,包括作為微晶混懸液和延長釋放制劑的局部遞送的注射劑。trk抑制劑是包含trk抑制劑的藥物組合物中的活性藥物成分。trk抑制劑也可與其他活性成分共同給予和/或共同配制用于治療疾病,包括治療疼痛、oa和與oa有關的疼痛。本發明的trk抑制劑的藥物制劑包含作為活性藥物成分的由式(i)表示的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺也稱為gz389988。式(i):3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺(gz389988)用本發明所要解決的問題是配制包含3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的組合物中的困難。該問題的解決方法是發現3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式與無水物形式相比具有改善的物理和化學性質,包括更佳的物理穩定性和更慢的水溶出度。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的無水物形式證實在溶液中相對不穩定,產生與其配制成藥物組合物相關的問題。無水物形式在某些條件下展現出可變的固體形式變化,包括轉化成水合物。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式容許額外的穩定性且有必要避免經長期儲存和加工期間的無定形轉化,且導致增強的物理穩定性。此外,觀察到一水合物形式在水溶液中更慢的溶出。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式,也稱為gz389988a,由下式(ii)表示。式(ii):3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式(gz389988a)3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的分子量為470.54g/mol,且分子式(elementalformula)為c26h26n6o3。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式是一種灰白色粉末,且在偏振光顯微鏡下其看上去是精細針狀物或纖維狀顆粒。根據實施例1合成3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式。本發明的一個具體實施方案是3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的結晶形式,其中使用cukα輻射測量的x射線粉末衍射圖(xrpd)含有以下2θ峰:7.14、8.89、10.22、12.42、12.73和14.31。獲得xrpd計算結果的方法的詳細內容在實施例1中提供。本發明的另一實施方案是一種藥物制劑,其包含trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的結晶形式和藥用賦形劑。本發明的另一實施方案涉及trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺在其它溶劑中的其它晶體形式,所述溶劑包括乙醇、丙酮、乙腈和混合溶劑。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的其它形式和獲得xrpd計算結果的方法的詳細內容在實施例4中提供。本發明還涉及一種組合物和藥物制劑,所述組合物包含由式(i)表示的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的組合物,所述藥物制劑包含trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式和藥用賦形劑。trk抑制劑的藥物制劑可包含一種或多種藥用賦形劑。trk抑制劑的藥物制劑的給予方式包括口服、舌下、靜脈內、皮下、肌內、關節內、透皮、經直腸、吸入、鞘內/心室內和局部給予。因此,trk抑制劑的藥物制劑可配制成例如膠囊、片劑、粉劑、溶液、混懸液、乳劑、凍干粉末或包含可注射微膠囊的延長釋放制劑。trk抑制劑的藥物制劑中使用的賦形劑將取決于trk抑制劑的藥物制劑預期的給予途徑。合適的賦形劑包括但不限于無機或有機材料,諸如稀釋劑、溶劑、明膠、白蛋白、乳糖、淀粉、穩定劑、熔化劑、乳化劑、助懸劑、鹽和緩沖劑。用于關節內制劑諸如溶液或混懸液的合適的藥用賦形劑包括但不限于市售的惰性凝膠或液體。由于trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺和3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的溶解性低,需要助懸劑來制備用于關節內注射的微晶混懸液制劑,其包含trk抑制劑作為活性藥物成分。常用的藥用助懸劑包括:阿拉伯膠、瓊脂、藻酸、膨潤土、硬脂酸鈣、卡波姆、羧甲基纖維素(鈣和鈉)、角叉菜膠、纖維素(微晶纖維素、微晶纖維素和羧甲基纖維素鈉,粉末狀)、膠體二氧化硅、糊精(destrin)、明膠、瓜爾膠、水輝石、疏水性膠體二氧化硅、羥基乙基纖維素、羥基甲基纖維素、羥基丙基纖維素、羥丙甲纖維素、高嶺土、硅酸鎂鋁、麥芽糖醇溶液、中鏈甘油三酯、甲基纖維素、硼酸苯汞、磷脂、聚卡波非(poycarbophil)、聚乙二醇、聚氧乙烯脫水山梨糖醇脂肪酸酯、聚維酮(聚乙烯基吡咯烷酮)、藻酸丙二醇酯、皂石、麻油、藻酸鈉、脫水山梨糖醇酯、蔗糖、西黃蓍膠、維生素e聚乙二醇琥珀酸酯和黃原膠(handbookofpharmaceuticalexcipients,6thedition)。緩沖劑也可用于關節內給予的溶液的制劑,其中所述活性成分為trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式。藥用緩沖劑包括:己二酸、氨溶液、硼酸、碳酸鈣、氫氧化鈣、乳酸鈣、磷酸鈣、檸檬酸一水合物、磷酸氫二鈉、二乙醇胺、甘氨酸、馬來酸、蘋果酸、甲硫氨酸、磷酸二氫鈉、單乙醇胺、谷氨酸單鈉、磷酸、檸檬酸鉀、乙酸鈉、碳酸氫鈉、硼酸鈉、碳酸鈉、檸檬酸鈉二水合物、氫氧化鈉、乳酸鈉和三乙醇胺(handbookofpharmaceuticalexcipients,6thedition)。因為本發明的trk抑制劑的藥物制劑是關節內給予的制劑,它們也可含有稀釋劑。適用于本發明應用的稀釋劑包括:麥芽糖醇、葵花子油、藻酸銨、碳酸鈣、乳酸鈣、無水磷酸氫鈣、磷酸氫鈣二水合物、磷酸鈣、硅酸鈣、硫酸鈣、纖維素(粉末狀,硅化微晶纖維素)、乙酸纖維素、可壓縮糖、糖粉(confectioner’ssugar)、玉米淀粉和預膠化淀粉、葡聚糖結合劑(dextrate)、糊精、葡萄糖、赤蘚糖醇、乙基纖維素、果糖、富馬酸、棕櫚酸硬脂酸甘油酯、吸入乳糖、異麥芽糖醇、高嶺土、拉克替醇、乳糖(無水、一水合物和玉米淀粉、一水合物和微晶纖維素,噴霧干燥的)、碳酸鎂、氧化鎂、糊精-麥芽糖復合劑、麥芽糖、甘露糖醇、中鏈甘油三酯、微晶纖維素、聚葡萄糖、聚甲基丙烯酸酯、二甲硅油(simethicone)、藻酸鈉、氯化鈉、山梨糖醇、淀粉(預膠化的、可滅菌的玉米淀粉)、蔗糖、糖球、磺丁基醚β-環糊精、滑石、西黃蓍膠、海藻糖、木糖醇(handbookofpharmaceuticalexcipients,6thedition)。含有3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式作為活性成分的trk抑制劑的藥物制劑的微晶混懸液述于實施例2。本發明還涉及制備3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的結晶形式和制備3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的方法,其包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺與溶劑混合以形成混懸液;b.攪拌混懸液;c.通過過濾收集混懸液中的固體;和d.使固體干燥。在該方法中,用于形成混懸液的溶劑可為丙酮和水的混合物。此外,混懸液可攪拌過夜,并且收集的固體可為空氣干燥的。trk抑制劑的延長釋放藥物制劑可包含3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺或3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式,因為在由藥物溶液制備的制劑的情況下,trk抑制劑在微膠包囊和配制之前溶于溶劑中,并且在由藥物混懸液制備的制劑的情況下,trk抑制劑在微膠包囊和配制之前混懸于溶劑中。然后如實施例3所述,將含有活性成分的溶液或混懸液與多種聚合物合并,從而微囊化3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微囊化有助于提供具有延長的效果的制劑,至多且持續3個月,且有助于在患者中提供持續的治療效果。在本發明的具體實施方案中,包含3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的藥物制劑包含藥用稀釋劑、藥用助懸劑和藥用緩沖劑。在本發明的藥物制劑的某些實施方案中,所述稀釋劑為山梨糖醇,所述助懸劑為聚維酮,且所述緩沖劑為磷酸。本發明還涉及延長釋放藥物制劑,其包含負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球。在這些延長釋放制劑中,所述trk抑制劑可為3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺或所述化合物的一水合物形式。所述載藥微球可進一步包含聚合物。在包含聚合物的負載trk抑制劑的微球的具體實施方案中,所述聚合物選自聚(d,l-丙交酯)、聚(d,l-丙交酯-共-乙交酯)及聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)兩者的組合。在本發明的某些實施方案中,延長釋放制劑中使用的聚(d,l-丙交酯)具有0.16-0.35dl/g的固有粘度(inherentviscosity)。在另一實施方案中,聚(d,l-丙交酯)具有0.16-0.24dl/g的固有粘度。在另一實施方案中,所述聚(d,l-丙交酯)具有0.25-0.35dl/g的固有粘度。在本發明的某些實施方案中,所述聚(d,l-丙交酯-共-乙交酯)具有0.14-0.24dl/g的固有粘度。在一個實施方案中,聚(d,l-丙交酯-共-乙交酯)具有0.14-0.22dl/g的固有粘度。在另一實施方案中,所述聚(d,l-丙交酯-共-乙交酯)具有0.16-0.24dl/g的固有粘度。在包含聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)兩者的延長釋放制劑中,所述聚(d,l-丙交酯)具有0.16-0.35dl/g的固有粘度且所述聚(d,l-丙交酯-共-乙交酯)具有0.14-0.24dl/g的固有粘度。在一個實施方案中,所述聚(d,l-丙交酯)具有度0.16-0.24dl/g的比濃對數粘且所述聚(d,l-丙交酯-共-乙交酯)具有0.14-0.22dl/g的固有粘度。在另一實施方案中,所述聚(d,l-丙交酯)具有0.16-0.24dl/g的固有粘度且所述聚(d,l-丙交酯-共-乙交酯)具有0.16-0.24dl/g的固有粘度。在另一實施方案中,所述聚(d,l-丙交酯)具有0.25-0.35dl/g的固有粘度且所述聚(d,l-丙交酯-共-乙交酯)具有0.14-0.22dl/g的固有粘度。且在另一實施方案中,所述聚(d,l-丙交酯)具有0.25-0.35dl/g的固有粘度且所述聚(d,l-丙交酯-共-乙交酯)具有0.16-0.24dl/g的固有粘度。在另一實施方案中,包含負載trk抑制劑的微球的延長釋放藥物制劑包含9:1比率的聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)。在這些延長釋放制劑中,所述聚(d,l-丙交酯)具有0.16-0.35dl/g的固有粘度且所述聚(d,l-丙交酯-共-乙交酯)具有0.14-0.24dl/g的固有粘度。在另一實施方案中,包含負載trk抑制劑的微球的延長釋放藥物制劑包含9.5:0.5比率的聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)。在這些制劑中,所述聚(d,l-丙交酯)具有0.16-0.35dl/g的固有粘度且所述聚(d,l-丙交酯-共-乙交酯)具有0.14-0.24dl/g的固有粘度。在包含負載trk抑制劑的微球的延長釋放藥物制劑中,所述微球負載有1%w/w至99%w/w3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。在一個更具體的實施方案中,所述微球負載有12%w/w至50%w/w3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。在另一實施方案中,所述微球負載有12%w/w至50%w/w3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。在更具體的實施方案中,所述微球負載有12%w/w、15%w/w、16%w/w、17%w/w、18%w/w、19%w/w、20%w/w、25%w/w、30%w/w、40%w/w或甚至50%w/w3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。本發明還涉及通過溶劑萃取和通過噴霧干燥制備負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的方法。本發明的一種溶劑萃取方法涉及由3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的溶液形成負載trk抑制劑的微球。該方法包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶于有機溶劑以形成藥物溶液;b.添加聚合物至藥物溶液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液;c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液混合至水溶液中以形成乳液;d.添加去離子水至乳液;e.通過溶劑萃取從乳液中形成微球;和d.使用表面活性劑溶液篩分所得微球。在該方法中,所述有機溶劑可包括(i)二氯甲烷和甲醇,(ii)二氯甲烷,(iii)苯甲醇和甲醇,(iv)二氯甲烷和苯甲醇,(v)氯仿,(v)氯仿和甲醇,或(vii)氯仿和苯甲醇。該方法中的聚合物可為聚(d,l-丙交酯)、聚(d,l-丙交酯-共-乙交酯)或聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)的組合。該方法中的水溶液可為聚乙烯醇在水中的溶液。該方法中的表面活性劑溶液可為泊洛沙姆407在水中的溶液、聚山梨酯80在水中的溶液或聚山梨酯20在水中的溶液。本發明的另一溶劑萃取方法涉及由3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的混懸液形成負載trk抑制劑的微球。該方法包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散于有機溶劑以形成藥物混懸液;b.添加聚合物至藥物混懸液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液;c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液與水溶液混合以形成乳液;d.添加去離子水至乳液;e.通過溶劑萃取從乳液中形成微球;和f.使用表面活性劑溶液篩分所得微球。在該方法中,所述有機溶劑可包括(i)乙酸乙酯,(ii)二氯甲烷,(iii)氯仿,(iv)乙酸乙酯和二氯甲烷,(v)乙酸乙酯和氯仿,(vi)二氯甲烷和氯仿,或(vii)乙酸乙酯、二氯甲烷和氯仿。該方法中的聚合物可為聚(d,l-丙交酯)、聚(d,l-丙交酯-共-乙交酯)或聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)的組合。該方法中的水溶液可為聚乙烯醇在水中的溶液。該方法中的表面活性劑溶液可為泊洛沙姆407在水中的溶液、聚山梨酯80在水中的溶液或聚山梨酯20在水中的溶液。在另一方面,本發明涉及通過噴霧干燥由負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的溶液形成負載trk抑制劑的微球的方法。該方法包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶于有機溶劑以形成藥物溶液;b.添加聚合物至藥物溶液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液;和c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶液通過噴霧器泵入干燥器以形成球狀顆粒。在該方法中,所述有機溶劑可包括(i)二氯甲烷和甲醇,(ii)二氯甲烷,(iii)苯甲醇和甲醇,(iv)二氯甲烷和苯甲醇,(v)氯仿,(v)氯仿和甲醇,或(vii)氯仿和苯甲醇。該方法中的聚合物可為聚(d,l-丙交酯)、聚(d,l-丙交酯-共-乙交酯)或聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)的組合。該方法的附加參數涉及噴霧器的噴霧速率和霧化氮氣流速。所述噴霧速率可為0.7ml/min;所述霧化氮氣流速可為4l/min。干燥器中各點處的溫度也是可被控制以影響所得微球大小的因素。在該方法中,所述干燥器具有50℃的入口溫度、40-45℃的腔室溫度和20-30℃的排氣溫度。在一個更具體的實施方案中,所述腔室溫度為40-43℃;更具體地,所述腔室溫度為41-43℃。在另一實施方案中,所述排氣溫度為22-28℃。在另一方面,本發明涉及通過噴霧干燥由負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的混懸液形成負載trk抑制劑的微球的方法。該方法包括:a.使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散于有機溶劑以形成藥物混懸液;b.添加聚合物至藥物混懸液以形成聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液;和c.使聚合物/3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺分散液通過噴霧器泵入干燥器以形成球狀顆粒。在該方法中,所述有機溶劑可包括(i)乙酸乙酯,(ii)二氯甲烷,(iii)氯仿,(iv)乙酸乙酯和二氯甲烷,(v)乙酸乙酯和氯仿,(vi)二氯甲烷和氯仿,或(vii)乙酸乙酯,二氯甲烷和氯仿。該方法中的聚合物可為聚(d,l-丙交酯)、聚(d,l-丙交酯-共-乙交酯),或聚(d,l-丙交酯)和聚(d,l-丙交酯-共-乙交酯)的組合。該方法的附加參數涉及噴霧器的噴霧速率和霧化氮氣流速。所述噴霧速率可為0.7ml/min;所述霧化氮氣流速可為4l/min。干燥器中各點處的溫度也是可被控制以影響所得微球大小的因素。在該方法中,所述干燥器具有50℃的入口溫度,40-45℃的腔室溫度和20-30℃的排氣溫度。在一個更具體的實施方案中,所述腔室溫度為40-43℃;更具體地,所述腔室溫度為41-43℃。在另一實施方案中,所述排氣溫度為22-28℃。以下非限制性實施例示例性說明本發明的各種實施方案,包括制備3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式、含有3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的藥物制劑、3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的延長釋放藥物制劑的方法以及制備這些延長釋放制劑的方法。實施例實施例1:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式實施例1-1:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的合成向3-甲氧基-4-(4-甲氧基芐基氧基)苯基)甲胺(2.00g,7.32mmol)和5-溴-2-氯-3-硝基吡啶(1.66g,6.97mmol)于乙腈(50ml)中的經攪拌溶液中添加n,n-二異丙基乙基胺(1.13g,8.71mmol)。將所得混合物加熱至回流并攪拌。64h后,將反應混合物冷卻至室溫并用水稀釋。用二氯甲烷萃取混合物兩次。將合并的有機相以硫酸鎂干燥,過濾并濃縮,得到3.34g(>100%)5-溴-n-(3-甲氧基-4-(4-甲氧基芐基氧基)芐基)-3-硝基吡啶-2-胺,其為黃棕色固體。向攪拌的5-溴-n-(3-甲氧基-4-(4-甲氧基芐基氧基)芐基)-3-硝基吡啶-2-胺于四氫呋喃(40ml)、乙醇(40ml)和水(40ml)中的溶液中添加亞硫酸氫鈉(6.09g,34.99mmol)。將所得混合物加熱至回流并攪拌。4h后,將反應混合物冷卻至室溫并用水稀釋。用二氯甲烷萃取黃色混合物三次。將合并的有機相用鹽水洗滌,干燥(硫酸鎂),過濾并濃縮,得到3.10g黃棕色固體。進行色譜純化(combi-flash40gsio2gold柱,1-2.5%甲醇/二氯甲烷),得到1.28g(51%)5-溴-n2-(3-甲氧基-4-(4-甲氧基芐基氧基)芐基)吡啶-2,3-二胺,其為黃色固體。向經攪拌的5-溴-n2-(3-甲氧基-4-(4-甲氧基芐基氧基)芐基)吡啶-2,3-二胺(0.850g,1.91mmol)于二氯甲烷(30ml)和甲醇(30ml)中的溶液中添加溴化氰(5.0m于乙腈中,573μl,2.87mmol)。將所得溶液在室溫攪拌。24h后,添加第二等份的溴化氰溶液(600μl)并繼續攪拌。48h后,添加第三等份的溴化氰溶液(600μl)并繼續攪拌。總計72h后,濃縮反應混合物,并將殘余物溶于二氯甲烷。將溶液用1n氫氧化鈉溶液洗滌,以硫酸鎂干燥,過濾并濃縮,得到1.17g棕色固體。進行色譜純化(combi-flash,40gsio2gold柱,1-10%2m氨/甲醇/二氯甲烷),得到0.28g(32%)6-溴-3-(3-甲氧基-4-(4-甲氧基芐基氧基)芐基)-3h-咪唑并[4,5-b]吡啶-2-胺,其為棕色固體。向經攪拌的6-溴-3-(3-甲氧基-4-(4-甲氧基芐基氧基)芐基)-3h-咪唑并[4,5-b]吡啶-2-胺(0.25g,0.53mmol)于1,4-二噁烷(10ml)和水(4ml)中的溶液中添加1-甲基-4-(4,4,5,5-四甲基-1,3,2-二氧雜硼雜環戊烷-2-基)-1h-吡唑(0.14g,0.66mmol)、磷酸鉀(0.39g,1.84mmol)、三環己基膦(0.015g,0.052mmol)、乙酸鈀(ii)(0.005g,0.026mmol)。將反應混合物在微波反應器中加熱至125℃。15min后,將反應混合物冷卻至室溫并用水稀釋。用乙酸乙酯萃取混合物兩次。將合并的有機相用鹽水洗滌,以硫酸鎂干燥,過濾并濃縮,得到0.36g,綠棕色固體。進行色譜純化(combi-flash,12gsio2gold柱,1-10%2m氨/甲醇/二氯甲烷),得到0.10g(41%)產物,其為淺綠色固體。將3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺添加至丙酮(2ml)和水(0.1ml)的混合物中。將混懸液在室溫通過磁力攪拌棒攪拌過夜。通過過濾收集固體并在空氣中干燥。通過質子nmr證實結構。差示掃描量熱法(dsc)熱解曲線在76.72、160.13和195.78℃展現三個熱事件,熱重量分析(tga)熱解曲線顯示自25至100℃的3.7%重量損失,x射線粉末衍射分析(xrpd)顯示使用cukα測量的在3.6、7.1、8.9、10.4、10.7、12.4、12.7和14.32θ峰的獨特峰(準確度±0.2°)。實施例1-2:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的結晶結構的鑒定還解析了3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的結晶結構。自丙酮/水中重結晶3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的晶體。當將大小為0.20*0.08*0.03mm的晶體置于mitegenmicromount的頂端時,其符合合適的衍射框。在bruker/axs三圓衍射儀上收集x射線衍射數據,所述衍射儀裝配有smartapex區域探測器(area-detector)、低溫裝置(lt2型)和銅-k微焦點發生器,其在45kv/650μa和具有約250μm圖像焦點直徑的聚焦光束montel多層光學器件操作(wiesmannetal.,2007)。使用程序包smartv5.628(brukeraxs,2001)收集數據,并使用程序saint+release6.45(brukeraxs,2003)進行處理。該分析產生2459次反射(0<h<24,-4<k<0,-19<l<19),其中全部2459次反射均是獨特的(rint=n.a.,rσ=0.1583)。使用1405次反射進行晶胞參數的精修。應用經驗吸收校正并使用apex2套件的“結構-解析(structure-solution)”模塊解析相位問題。使用apex2套件的xl模塊(brukeraxs,2011),通過最小二乘法((fo2–fc2)2的最小化)來精修結構。計算所有氫原子的位置,s擬合優度=1.085,r所有數據=0.1329(1614次反射的robs.數據=0.0920,其中|fobs|>4σ,wr2所有數據=0.2710,wr2觀測數據=0.2377)。差示圖中的最大未分配峰對應于-0.348vs+3.86個電子/c-c鍵的平均估計標準偏差(e.s.d.)為o-c鍵的平均估計標準偏差為且n-c鍵的平均估計標準偏差為平均e.s.d.c-c-c鍵角的平均估計標準偏差為0.7且c-c-c-c扭轉角的平均估計標準偏差為1.004°。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的結晶結構示于圖3。圖4顯示由單晶結構計算出的實驗粉末圖的疊加。強的匹配度表明,單晶結構表示散裝材料。實施例2:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物微晶混懸液制劑開發了trk抑制劑的藥物制劑的微晶混懸液,其中3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式為活性成分。將這些制劑開發成不溶性3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺顆粒的混懸液以使得所述trk抑制劑隨時間持續遞送至體內。該方法依賴于活性成分的差溶解度和用于控制釋放持續時間的劑量;其還顯示3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺約1個月的體內持續遞送。實施例2-1:20mg/ml3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物注射用微晶混懸液制備包含每毫升溶液20mg3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的藥物制劑。20mg/ml微晶混懸液的組合物提供于下表1中。表1:20mg/ml微晶混懸液制劑應用10%的過量填裝(overfilling)實施例2-2:制備20mg/ml3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物微晶混懸液制劑的方法根據以下步驟制備3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的20mg/ml溶液:1.通過以下方式制備磷酸鹽緩沖液10mmph7.4:組合適量注射用水(wfi)和磷酸二氫鈉,攪拌至完全溶解,然后用氫氧化鈉1n溶液調節ph至7.4(±0.2)。2.通過以下方式制備媒介物:組合適量山梨糖醇和聚維酮k17熱原(pyrogen),添加磷酸鹽緩沖液10mmph7.4并攪拌直至完全溶解。3.然后通過0.22μmpvdf[聚偏二氟乙烯]親水型過濾器過濾所得媒介物。4.通過以下方式制備濃縮的混懸液:使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式與媒介物大致混合,以獲得30mg/ml濃縮的混懸液。5.在75μm不銹鋼篩上過濾保持在攪拌下的濃縮的混懸液。6.預過濾的混懸液仍保持攪拌并在40μm不銹鋼篩上過濾,以獲得濃縮物混懸液。7.用經過濾的媒介物濃縮混懸液調節,以獲得20mg/ml混懸液。8.將最終的混懸液填充至無菌和去熱原的無色i型玻璃小瓶中至3.6ml填充體積。用無菌和去熱原的經etfe包覆的溴丁基瓶塞封閉小瓶。將瓶塞用無菌鋁蓋和無菌白色塑料蓋壓接在小瓶上。9.將填充的小瓶在高壓滅菌設備中滅菌。實施例2-3:20mg/ml3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物微晶混懸液制劑的臨床劑量將3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的20mg/ml微晶混懸液進一步修飾,以獲得呈成品藥品構型的將要向患者給予的劑量和體積。必要時由20mg/ml微晶混懸液重構目標劑量。不同的劑量和體積格式的總結在表2中提供。表2:20mg/ml3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物微晶混懸液的臨床處方重構不需要達到所需的最終濃度。2x2.7ml小瓶實施例3:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺延長釋放制劑在一些情況下,期望延長藥物釋放的持續時間,例如延長至大于3個月的暴露時間。因此,使用化合物的無水物或一水合物形式產生和配制的trk抑制劑3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺作為活性成分的延長釋放制劑。所述延長釋放制劑方法使用聚(d,l-丙交酯)(pla)、聚(d,l-丙交酯-共-乙交酯)(plga)聚合物或pla-plga聚合物的組合,以包囊3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺(活性藥物成分[api]或藥物物質[ds]),從而產生可注射微囊的藥品[dp]溶液。這些制劑可提供持續或大于3個月的藥物暴露于體內。該實施例的延長釋放制劑的制備中使用的不同聚合物的總結在表3中提供。表1:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物延長釋放制劑中使用的聚合物*用ubbelhode大小0c玻璃毛細管粘度計以0.1%w/v于chcl3中在25℃測量固有粘度。來源:http://www.resomer.com/product/biodegradable-polymers/en/pharma-polymers/products/pages/bioresorbable-polymer.aspx含有3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺作為活性成分的trk抑制劑的延長釋放藥物制劑使用生物可消化的聚合物,即聚(d,l-丙交酯)和/或聚(d,l-丙交酯-共-乙交酯),以改變活性成分從藥物顆粒溶解至聚合物水解的釋放的控制。使用聚合物與活性成分載量的適當組合,可控制藥物釋放速率以導致3個月或更長的暴露。plga/pla聚合物和3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的具體組合以延長藥物釋放的持續時間大于3個月的方式組合;這些制劑在該實施例中進一步討論。實施例3-1:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺負載對體外釋放分布的作用通過溶劑萃取制備包含3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的藥物組合物。用于制備各批次的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺和pla/pgla聚合物物料的量示于表4。檢查了各種制劑的體外釋放(ivr)動力學。表4:微球的組合物–12%api/9:1r202h:752h、16%api/9:1r202h:752h和20%api/9:1r202h:752h通過溶劑萃取制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg伴隨輕微加熱(約30分鐘),將3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶于2ml9:1二氯甲烷(dcm):甲醇(meoh)。歷經30分鐘添加聚合物并溶解。另外,將39ml冷的無菌過濾的聚乙烯胺(pva)溶液(5%w/v于水中)置于裝配有7.9x38.1mmteflon磁力攪拌棒的250ml燒杯中。將燒杯置于在ikarct基本攪拌平臺設置(basicstirplateset)(500rpm)上的冰浴中。使用連接至5cc玻璃hamilton注射器的pallacrodisc0.2μmptfe注射器過濾器,將聚合物/藥物溶液過濾至pva溶液中。添加后,聚合物/藥物溶液形成乳狀液。1分鐘后,添加160ml冷去離子水。5分鐘后,攪拌速度降至300rpm。歷經3小時通過溶劑萃取法形成微球。通過75μm和38μm疊篩使用冷的0.1%kolliphorp407于去離子水中篩選微球;收集38-75μm級分并除去多余的淋洗液。將微球在-80℃冷凍并凍干。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺自微球制劑中釋放的ivr動力學通過制備與其模擬膝蓋的關節內環境的微球于0.2%透明質酸+0.2%kolliphorp407中的2%(w/v)含水混懸液確定。在一式三份中,將一定體積含有500μg3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的理論載量的混懸液吸入含有0.5%十二烷基硫酸鈉/pbs,ph7.4釋放介質的單獨的50ml玻璃離心管中。將管置于37℃互動搖床培養箱側。在每個時間點,允許微球沉降,取樣1ml釋放介質并置換。為了確定ivr樣品中3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的實際總質量,將用于釋放研究的相同體積的混懸液取樣(一式三份)并添加10ml二甲基亞砜。將樣品進行超聲處理,輕輕加熱并在室溫置于搖臂上以溶解。使用hplc-uv分析這些樣品的總3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺含量。將累積ivr分布對實際3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺載量相對于時間的百分數作圖。3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺包囊效率通過將實際藥物載量除以理論載量來確定。為了確定實際載量,將精確稱重的負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球溶于二甲基亞砜中,并通過hplc-uv測量3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺濃度。ivr分布顯示,高于16%(w/w)的藥物載量水平顯示突然釋放(burstrelease)(圖5)。通過差示掃描量熱法(dsc)和掃描電子顯微鏡(sem)鑒定了該突然釋放的原因。dsc分析表明,高于16%(w/w)的藥物載量水平顯示在微球中藥物結晶,如通過在130-150℃的熔融吸熱所證明(圖6)。藥物結晶也通過sem顯示,其中高于16%的藥物載量水平顯示微球表面上的藥物晶體(圖7)。錯誤!未找到引用源。說明20%微球顯示130-150℃之間的熔化吸熱,確證表面藥物晶體的存在。圖7和圖8顯示負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球在1500x的sem。圖7,16%載藥微球,顯示沒有藥物晶體(藥物為無定形的);圖8,20%載藥微球,顯示表面藥物晶體。使用相關的微球組合物還說明了藥物結晶對ivr的影響。圖9顯示由用r202h聚合物制備的微球的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的ivr。圖10顯示由用9.5:0.5比例的r202h和rg752h聚合物制備的微球的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的ivr。在這些實施例中,高于16%(w/w)的藥物載量水平顯示突然釋放;藥物突然釋放程度與藥物載量水平直接相關。實施例3-2:聚-丙交酯和聚-丙交酯-共-乙交酯聚合物共混物對3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的體外釋放分布的作用實施例3-2-1:16%api/r202h、16%api/9.0:0.5r202h:rg752h和16%api/9:1r202h:752h微球制備包含于r202h、9.0:0.5r202h:rg752h和9:1r202h:752h中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于r202h、9.0:0.5r202h:rg502h和9:1r202h:rg502h中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的藥物組合物,以評估不同聚合物共混物對3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的體外釋放動力學的影響。表5示出用于制備每批的藥物和聚合物質量。用于制備這些制劑的方法描述于實施例3-1。表5:含有聚-丙交酯和聚-丙交酯-共-乙交酯聚合物共混物(16%api/r202h、16%api/9.0:0.5r202h:rg752h和16%api/9:1r202h:rg752h)的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺微球制劑通過溶劑萃取制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg包囊效率和ivr分析如實施例3-1所述進行。制劑4、5和6的包囊效率分別為96.1±2.6%、87.8±6.3%和77.7±8.6%。使用于r202h聚合物中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制備的微球展現出雙相釋放速率,具有0-70天的緩慢初始釋放速率和隨后70-110天的更快二次釋放速率(圖11)。將更親水的聚合物rg752h(75:25plga)混合至pla微球制劑增加了初始釋放速率。該plga聚合物允許更快的水吸收至微球中,導致速率增加。以9:1r202h:rg752h的比率,初始釋放與二次釋放速率相匹配,產生歷時3個月的假零級釋放分布(圖11)。實施例3-2-2:16%api/r202h、16%api/9.5:0.5r202h:rg502h和16%api/9:1r202h:rg502h微球制備含有于r202h、9.0:0.5r202h:rg502h和9:1r202h:rg502h中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的藥物組合物,以評估不同聚合物共混物對3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的體外釋放動力學的影響。表6示出用于制備各批次的藥物和聚合物質量。用于制備這些制劑的方法述于實施例3-1。表6:微球的組合物–16%api/r202h、16%api/9.5:0.5r202h:rg502h和16%api/9:1r202h:rg502h通過溶劑萃取制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg包囊效率和ivr分析如實施例3-1所述進行。制劑7、8和9的包囊效率分別為96.1±2.6%、91.7±3.3%和94.2±2.5%。使用于r202h聚合物中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制備的微球展現出雙相釋放速率,具有0-70天的緩慢初始釋放速率和隨后70-110天的更快二次釋放速率(圖12)。將更親水的50:50plga聚合物(rg752h)混合至pla微球制劑增加了初始釋放速率。rg752h允許更快的水吸收至微球中,導致該速率增加。以9.5:0.5r202h:rg502h的比率,初始釋放與二次釋放速率相匹配,產生歷時6個月的假零級釋放分布(圖12)。實施例3-3:顯示歷時180天的零級體外釋放動力學的微球制劑的制備和表征制備包含于9:1r203h:rg752h中的15%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于9.0:0.5r202h:rg502h中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的藥物組合物并分析體內釋放動力學。表7示出用于制備各批次的藥物和聚合物質量。表7:微球的組合物–15%api/9:1r203h:rg502h和16%api/9.5:0.5r202h:rg502h)通過溶劑萃取制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg包囊效率和ivr分析如實施例3-1所述進行。制劑10和11的包囊效率分別為89.7±2.1%和91.7±3.3%。使用于9:1比率的r203h:752h聚合物中的15%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于9.5:0.5比率的r202h:rg502h聚合物中的16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制備的微球展現出歷時6個月的假零級釋放分布(圖13)。實施例3-4:制備中的共溶劑系統對3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的體外釋放分布的作用實施例3-4-1:如于9:1dcm:meoh、9:0.5:0.5dcm:meoh:ba、9:5dcm:ba和9:1dcm:ba中制備的16%api/9:1r202h:rg752h使用具有不同比率的溶劑二氯甲烷(dcm)、甲醇(meoh)和苯甲醇(ba)的各種共溶劑溶液制備包含于9:1r202h:rg752h中的負載16%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的藥物組合物。所用的比率為9:1dcm:meoh、9:0.5:0.5dcm:meoh:ba、9.5:0.5dcm:ba和9:1dcm:ba。對于用于制備各批次的藥物、聚合物和共溶劑,參見表8。用于制備這些制劑的方法述于實施例3-1。表8:用共溶劑系統制備的微球的組合物–16%api/9:1r203h:rg752h通過溶劑萃取制備(各種共溶劑系統)gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg包囊效率和ivr分析如實施例3-1所述進行。制劑12、13、14和15的包囊效率分別為77.7±8.6%、94.9±2.0%、90.5±2.6%和94.4±1.5%。由于其增強溶解3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的能力,選擇苯甲醇摻入共溶劑系統中。圖14和圖15顯示苯甲醇可用作含有二氯甲烷或二氯甲烷和甲醇的共溶劑的部分,以產生微球而不影響釋放速率。這可用于減少微球產生過程中3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺可能的重結晶。實施例3-4-2:dcm:ba用于提高3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺載量的用途使用不同體積的二氯甲烷(dcm)和苯甲醇(ba)制備藥物組合物,其包含于9:1r202h:rg752h中的16%和25%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于r202h中的30%和40%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于r203h中的25%、30%、40%和50%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。對于用于制備各批次的藥物和聚合物質量及溶劑體積,參見表9。用于制備這些制劑的方法述于實施例3-1。表9:用dcm:ba共溶劑系統制備的微球的組合物–16%api/9:1r202h:rg752h、25%api/9:1r202h:rg752h、30%api/r202h、40%api/r202h、25%api/r203h、30%api/r203h、40%api/r203h、50%api/r203h通過溶劑萃取制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg包囊效率和ivr分析如實施例3-1所述進行。用不同體積二氯甲烷(dcm)和苯甲醇(ba)產生的制劑的包囊效率為:由于其增強溶解3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的能力,選擇苯甲醇摻入共溶劑系統中。圖10顯示苯甲醇可用作含有二氯甲烷的共溶劑的部分,以產生具有高至載量50%(w/w)的微球。一些所示釋放分布具有應當達到3-6月持續時間的最小突然釋放和動力學。方法中使用的苯甲醇的體積影響3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的突然釋放。減少溶劑系統中苯甲醇的量,但仍保持api即3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺在聚合物溶液中的溶解度,降低突然釋放效應(bursteffect)。通過減少向患者給予的聚合物的量,增加api載量提供了益處。這預期提高植入物的生物相容性并減少重復給予后聚合物積聚的可能性。此外,增加的api載量應轉化成較低的每單位制造成本。實施例3-5:微粒化混懸液微囊化方法對3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的體外釋放分布的作用用3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式制備藥物組合物,其包含于9:1r202h:rg752h中的25%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺(一水合物形式)、于9:1r203h:rg752h中的30%和40%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺、于r202h中的25%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺、于r202s中的30%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于r203s中的30%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。對于用于制備各批次的藥物和聚合物質量,參見表10。使用來自生產批次的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制備批次27、28和29,而使用3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制備批次30、31、32、33、34和35,其使用微流化方法進行微粉化以確保粒徑小于10μm直徑。該實施例比較了當聚合物分散在具有或不具有乙酸乙酯(ea)的聚乙烯醇(pva)溶液中獲得的微球中的差異,以及api載量、聚合物組成和不同聚合物溶液濃度(通過改變ea體積)。表10:用微粒化混懸液微囊化方法制備的微球的組合物–16%api/9:1r202h:rg752h、25%api/9:1r202h:rg752h、30%api/r202h、40%api/r202h、25%api/r203h、30%api/r203h、40%api/r203h、50%api/r203h通過溶劑萃取制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mgsem分析顯示,通過包囊3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的混懸液產生的微球由于嵌入表面的藥物晶體的存在而是球形的,具有粗糙的表面紋理(圖16)。包囊效率和ivr分析如實施例3-1所述進行。批號30、31、32、33、34和35的包囊效率分別為103.3±3.8%、101.6±5.3%、94.7±4.0%、97.1±0.2%、35.6±0.8%和62.5±3.0%。沒有在批次27、28或29上進行包囊效率。ivr分布顯示突然釋放范圍為25%至47%,接著是4天后的無釋放(圖17)。對批次進行評估長達21天。實施例3-6:包囊方法對3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的體外釋放分布的作用使用9:1比率的二氯甲烷(dcm):苯甲醇(ba)制備藥物組合物,其包含于9:1r202h:rg752h中的16%和25%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺及于r203h中的25%和30%3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。對于用于制備各批次的藥物和聚合物質量,參見表11。用于制備批次23的方法述于實施例3-1,批次2。通過伴隨輕微超聲處理使3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺溶于5.016g9:1dcm/meoh制備批次24。然后添加兩種聚合物并溶解。表11:通過溶劑萃取和噴霧干燥制備的微球的組合物–16%api/9:1r202h:rg752h和無api/9:1r202h:rg752hgz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg(對于批次23)和1254mg(對于批次24)噴霧干燥使用裝配有具有0.4mm開口的流體噴嘴的procept,4m8裝置進行。噴霧干燥條件和參數如下:sem分析顯示,溶劑萃取微球是球形的,具有光滑的表面紋理,而噴霧干燥微球是球形的,具有一些表面紋理(圖18和圖19)。包囊效率和ivr分析如實施例3-1所述進行。溶劑萃取批次36和噴霧干燥批次37和38的包囊效率分別為107.4±11.6%、91.4±4.3%和92.6±3.6%。兩種微囊化方法產生具有近零級釋放分布的微球。圖18和圖19顯示負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球在1000x的sem。ivr分布顯示不同的釋放速率(圖20);噴霧干燥制劑實現3-6個月遞送的期望持續時間。實施例3-7:1%10kdapeg或1%泊洛沙姆407對16%(w/w)3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的噴霧干燥微球的體外釋放分布的作用進行該實驗以確定添加親水性添加劑是否可用于加速來自pla/pga微球的gz389988的體外釋放速率。在該實驗中,將微球(無添加劑)與用1%10kdapeg或1%泊洛沙姆407制備的微球進行比較。表12詳細說明了用于制備每批的藥物和聚合物質量。表12:用1%10kdapeg或1%泊洛沙姆407制備的微球的組合物–16%api/1:1r202h:r203h/無添加劑、16%api/1:1r202h:r203h/31.25mgpeg、16%api/1:1r202h:r203h/31.25mg泊洛沙姆407通過噴霧干燥制備gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺噴霧干燥使用裝配有具有0.4mm開口的雙流體噴嘴的procept,4m8裝置進行。噴霧干燥條件和參數如下:批號404142gz389988載量(%,w/w)161616plga溶液濃度(%,w/v):22.522.522.5噴霧速率(ml/min):0.70.70.7空氣流速(l/min):0.350.350.35霧化氮氣流速(l/min):444冷卻器溫度(℃):-4-4-4入口溫度(℃):505050腔室溫度(℃):404040排氣溫度(℃):292929預旋流器壓力(mbar):27-3027-3027-30sem分析顯示,用或不用親水性添加劑制備的噴霧干燥微球顯示類似的大小分布和表面紋理;所有噴霧干燥微球均是球形的,具有一些表面紋理(圖21、圖22和圖23)。包囊效率和ivr分析如實施例3-1所述進行。噴霧干燥批號40、41和42的包囊效率分別為102.0±16.3%、101.7±16.3%和100.5±16.1%。不用添加劑制備的微球顯示gz389988的緩慢的近零級釋放,其中歷經35天釋放約20%的活性化合物(圖24)。1%10kdapeg或1%泊洛沙姆407的添加增加了釋放速率;歷經35天釋放約42%的活性化合物。該實施例說明,摻入親水性賦形劑可加速gz389988從pla/pga微球中的體外釋放速率。實施例4:體內研究實施例4-1:關節內注射至大鼠膝關節后負載[14c]-3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球的體內表現選擇兩種制劑來比較體外釋放動力學與大鼠膝關節中的體內藥物持久性。制劑示于表13。使用實施例3-1中所述的方法進行體外釋放測試。使用[14c]-3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺和未標記的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺進行體內藥物持久性測試;兩種藥物形式在微囊化過程中共溶解,以確保微球中藥物分布均勻。向每只大鼠關節給予的放射性活度(radioactivity)總量為約1.2mbq。大鼠膝關節中藥物保留的評價如下進行:在每個時間點處死2-3只大鼠,冷凍研磨膝關節并從研磨的組織提取3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺。通過液體閃爍計數進行定量。通過將每個時間點的放射性計數除以處理后0.1小時處死的大鼠的放射性計數,計算關節中回收的放射性活度的量。將大鼠血液中的放射性藥物的濃度(以neq/g表示)隨時間作圖并與化合物的已知ic50值進行比較。表13:體內測試的微球的組合物–16%api/9:1202:h:rg502h和15%api/9:1r203h:rg752hgz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺*總聚合物量=260mg批次40和41的ivr分布分別顯示歷時近3-4個月和5-6個月的近零級段釋放(圖25)。關節內注射至大鼠膝關節后,批次43和44顯示超過5至6個月的藥物釋放;批次43顯示5個月后關節中12%的保留且批次44顯示6個月后30%的藥物保留(圖26)。相比于可能由于微球在滑膜中的定位而導致的ivr率,體內藥物釋放率略低。圖27顯示血液中的藥物濃度-時間分布。關節內給予負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球后,系統隔室中3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的濃度在第一周內略高于ec50值(基于細胞),但是然后在實驗期間(5-6個月)下降到低于ec50值。該實驗說明,負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球以低系統性(即亞治療性)藥物暴露提供持續的局部藥物遞送至膝關節。實施例4-2:評估單一關節內注射三種負載3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的微球緩釋微球制劑后gz389988的藥物動力學選擇三種制劑來比較大鼠膝關節中關節內注射后系統隔室內的體外和體內藥物動力學。制劑示于表14。使用實施例3-1中所述的方法進行體外釋放測試。通過用給予微球制劑注射3只雄性wistar大鼠(0.1或1mg的gz389988至膝關節)來測量體內表現。在每個時間點,通過頸靜脈插管收集血液樣品(約0.25ml)并置于含有k2edta作為抗凝劑的冷凍管中,混合,并保持在冰上直至離心。將樣品在4℃的溫度收集1小時內,在3,000×g離心5至10分鐘。將血液樣品離心至聚丙烯管后,收集血漿。將血漿樣品在干冰上冷凍,并在lc-ms/ms分析前在-60至-80℃冷凍保存。將gz389988在大鼠血漿中的濃度(以ng/ml表示)對時間(總共28天)作圖。表14:評估gz389988的藥物動力學中測試的微球的組成和劑量gz389988=3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺制劑a和制劑b的ivr分布顯示緩釋,歷經28天約有10%的活性化合物釋放。制劑c在最初5天顯示稍高的初始釋放,接著在剩余的23天顯示降低的釋放率;歷經28天約22%的活性化合物釋放。關節內給予至大鼠膝關節后,制劑a和b歷經28天顯示出類似的血漿-藥物暴露分布;兩種制劑均顯示出在實驗持續時間內具有穩態血漿水平的1-1.5小時的tmax值(對于0.1和1.0mg劑量分別為0.08和0.8ng/ml)。與制劑a和b相比,制劑c在實驗持續時間內顯示出更高的cmax值和更高的穩態血漿水平(對于0.1和1.0mg劑量分別為1.2至12ng/ml)(圖29)。這些結果與ivr實驗結果非常一致。實施例4-3:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺在具有膝蓋的疼痛性骨關節炎的患者中的安全性、耐受性和藥物動力學的臨床研究在兩部分雙盲安慰劑對照臨床研究中,測試3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的一水合物形式的安全性和功效,以評估單次逐步增加的關節內劑量的安全性、耐受性和藥物動力學,隨后評估具有膝蓋的疼痛性骨關節炎的患者中單次關節內劑量的功效、安全性、耐受性和藥物動力學。在第一部分研究中,膝蓋中單次關節內注射各種劑量的根據上述實施例2制備的3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺一水合物微晶混懸液,針對3ml和5ml的安慰劑劑量進行測試。診斷為原發性膝蓋骨關節炎的成年男性和女性有資格參與研究。患者具有癥狀超過6個月并在與研究相關的任何手術之前提供書面知情同意書。在注射后12周,基于安全性和耐受性(不良事件、體檢、體重、體溫、臨床實驗室測試、血壓、心率、12導聯心電圖、局部耐受性)評價功效。還評價了藥物動力學(血漿和(如果可能的話)滑膜液中)和藥效學。在研究藥物或安慰劑給予后,患者被隨訪84±7天,并選擇繼續進行長期觀察性安全性研究而無需額外的研究藥物給予,以評估長期安全性和療效。實施例5:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的多晶型現象研究為了鑒定3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺在純溶劑及溶劑和水的受控混合物中的晶型,進行了gz389988的多晶型現象研究。用作多晶型物的表征工具的技術包括x射線粉末衍射(xrpd)、高分辨率x射線粉末衍射(hr-xrpd)和單晶x射線衍射(xrscd)、熱重量分析(tga)與紅外光譜(ft-ir)或質譜(ms)、水和溶劑的動態蒸氣吸附(dvs)和光學顯微術(om)。這些技術在下文更詳細地描述。高分辨率x射線粉末衍射(hr-xrpd)在panalyticalx'pertprompd粉末衍射儀的環境條件下,使用偶聯有x'celerator檢測器的bragg-brentano(垂直θ-2θ配置)準聚焦幾何圖形記錄高分辨率圖。使用密封的銅陽極x射線管,在45kv和40ma水平運行的。入射光束單色儀(johansson型:對稱切割的彎曲鍺(111)晶體)產生純cukα1輻射對于每組實驗,將產品的薄層沉積在用單晶硅晶片覆蓋的樣品架的表面上。通過系統消光根據si(510)結晶取向切割晶片,阻止硅的任何bragg反射。可用的角度范圍從2延伸到50°2θ,其中步長為0.017°2θ。使用每步100到2500秒的可變計數時間。x射線粉末衍射(xrpd)其他xrpd分析在siemens-bruckerd8advance粉末衍射儀上進行,還使用bragg-brentano(垂直θ-θ配置)準聚焦幾何形狀和anton-paarttk450溫度室。產品的薄層沉積在單晶硅晶片上,通過系統消光根據si(510)結晶取向切割,阻止晶片的任何bragg反射。使用在40kv和35ma水平運行的密封銅陽極x射線管。通常發射兩條線:cukα1和cukα2放置在檢測器和樣品之間的鎳β過濾器并沒有完全消除cukβ輻射,其仍然貢獻了檢測器(制造商的數據)約1%的衍射光束。光束通過soller狹縫發送,以改善其平行度。可變發散狹縫保持樣品面積的照度不變。準直器限制管和樣品之間的擴散。lynxeye線性檢測器完成了設置。它在2θ角度處有一個3.5°寬的檢測窗口。在以下條件記錄圖:在環境溫度,從2至40°2θ角度掃描。積分時間取決于實驗條件。使用以2θ為計的每步0.1秒計數時間進行進化研究和大多數掃描。更長的積分時間(至多5s)可能已被用于表征穩定形式。x射線單晶衍射(xrscd,也稱scxrd)在brukersmartapex單晶衍射儀上記錄xrscd數據。使用鉬iμs微聚焦x射線源,在50kv和0.6ma運行,發射mo-kα輻射電荷耦合元件(ccd芯片:4k,62mm)面積檢測器位于6.0cm處。oxfordcryosystems氮氣低溫恒溫器(cryostreamplus)允許在100k進行xrscd實驗。將晶體從paratonentm油滴安裝到低背景mylarmitegen環上。收集了一個完整的ewald反射球體(3個ω掃描,680幀,幀寬為0.3°)。累積時間取決于晶體。使用apex2(v2014.11-0)程序套件建立取向矩陣和單位晶胞。使用saint(v8.34a)程序進行3d反射分布和所有反射的整合。sadabs(v2014/5)程序用于校正lorentz和極化效應以及通過樣品的吸收。試驗性空間群用xprep(v2014/2)程序確定。shelxtl(v2014/7)套件用于通過內在定相方法解析結構,并通過f2全矩陣最小二乘法精修解決方案。多晶型物鑒定和表征使用上述技術,鑒定3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的晶型。這些形式、使用輻射測量的xrpd2θ峰和形成條件示于下表15。表15:3-(3-甲氧基-4-((4-甲氧基芐基)氧基)芐基)-6-(1-甲基-1h-吡唑-4-基)-3h-咪唑并[4,5-b]吡啶-2-胺的形式一水合物形式1、無水物形式2和3的測量hr-xrpd圖以及倍半水合物形式4的模擬xrpd圖在圖30中繪制在一起。在混合溶劑乙醇/水(99/1)中將20mg/mlgz389988a形式一水合物的混懸液在80℃加熱1小時。然后過濾混懸液。接下來,將溶液在室溫保持過夜。一夜之后,觀察到晶體,隨后鑒定為對應于乙醇溶劑化物形式(標示為形式5)。通過乙醇和水的混合物(99/1)的緩慢蒸發獲得的晶體的物理性質適于通過單晶x射線衍射進行分析。在5x50x200μm3晶體上以100k進行測量,累積時間為300s/幀。衍射圖證實了所分析顆粒的結晶度。圖31顯示了在室溫測量的乙醇溶劑化物粉末的hr-xrpd圖(底部),與由在100k測量的xrscd數據模擬的xrpd圖(上部)相比。在丙酮/水的混合物(99/1)或純丙酮中制備20mg/mlgz389988a形式一水合物1(形式1)的混懸液,并在80℃加熱1小時以實現完全溶解。接下來,過濾混懸液。然后將溶液保持在室溫或5℃。一夜之后,裸眼可見晶體,隨后鑒定為對應于丙酮溶劑化物形式(標示為形式9)。通過丙酮和水的混合物(99/1)的緩慢蒸發獲得的晶體的物理性質適于通過單晶xr衍射進行分析。在100x200x2000μm3晶體上以100k進行測量,累積時間為30s/幀。圖32展現了在室溫測量的丙酮溶劑化物粉末的xrpd圖(底部),并由xrscd在100k模擬的圖(上部)。在另一實驗中,在純丙酮中制備20mg/mlgz389988a形式一水合物1(形式1)的混懸液,并在80℃加熱1小時。接下來,過濾混懸液,然后直接冷卻至5℃并在該溫度儲存。一夜之后,裸眼可見晶體且類似于針對丙酮溶劑化物1,形式9所獲得的那些。將其在研缽中懸浮研磨后,鑒定為對應于另一種丙酮溶劑化物,形式10。圖33比較了兩種丙酮溶劑化物形式的xrpd,形式9(底部)和形式10(上部)。將20mg/mlgz389988a形式一水合物在乙腈(acn)中的混懸液在80℃加熱4小時。然后過濾混懸液。接下來,將溶液在40℃保持過夜,然后放置2小時,冷卻至室溫。一夜之后,在小瓶的底部形成晶體簇。乙腈(acn)溶劑化物形式(形式11)的hr-xrpd圖如圖34所報道。在丙酮/水和乙腈/水混合溶劑中形成的固體結晶相的鑒定50mggz389988a一水合物1補充有三種不同重量比的2ml溶劑(丙酮或乙腈)和去礦物質水的混合物:50/50、80/20和95/5。用丙酮探測比率為99/1和98/2的其他混合物。在80℃2小時后,在標稱孔徑為0.45μm的ptfe注射器過濾器上過濾樣品,過濾后再次在80℃儲存15分鐘。然后將樣品在40℃放置冷卻過夜,然后在室溫再冷卻24小時。然后通過xrpd在用相應溶劑飽和的腔中分析樣品。如果需要,將大晶體在小瓶中用刮刀粉碎成更細的粉末。然后將“濕”粉末的樣品盡可能平坦地沉積在樣品架上。這些分析的結果示于下表16。表16:丙酮/水和乙腈/水混合物中gz389988a的固體結晶相在本實施例中研究并示出了由一水合物1在乙醇、丙酮、乙腈及丙酮/水和乙腈/水混合物中的結晶的溶劑化物和水合物的形成。已經鑒定了十種結晶相:●無水物相1(形式2)●無水物相2(形式3)●無水物相3(形式6/7)●一水合物1(形式1)●一水合物2(形式8)●倍半水合物(形式4)●乙醇溶劑化物(形式5)●丙酮溶劑化物1(形式9)●丙酮溶劑化物2(形式10)●乙腈溶劑化物(形式11)相應的衍射圖在圖35中繪制在一起。從對乙醇、丙酮和乙腈以及溶劑混合物(丙酮/水和乙腈/水)的多晶型現象研究可得出若干結論。所有三種純溶劑導致形成固體結晶溶劑化物相。gz389988a在乙醇和乙腈中重結晶各自導致一種溶劑化物形式。從丙酮中重結晶已經得到兩種溶劑化物形式。在重量比為98:2、97:3、95:5、80:20和50:50的丙酮/水混合溶劑體系中形成的晶體均呈一水合物1結晶相。在重量比為95:5、80:20和50:50的乙腈/水混合溶劑體系中形成的晶體也均為一水合物1晶體。已經觀察到丙酮溶劑化物1經去溶劑化轉化為大部分無定形固體。如果通過混合丙酮和水的蒸氣的存在增加分子遷移率,則初始丙酮溶劑化物1晶體和無定形固體重組成一水合物1。乙醇、乙腈和丙酮溶劑化物1在氮氣下暴露于120℃的溫度去溶劑化成相同的無水結晶相2。對于乙醇、乙腈和丙酮溶劑化物2形式觀察到同晶型現象(isomorphism)(待單晶x射線衍射確證)。它們均可逆地溶劑化成相同的無水物相3。無水物相3水合成一水合物形式,即不同于一水合物1的“一水合物2”。當前第1頁12
相關技術
網友詢問留言
已有0條留言
- 還沒有人留言評論。精彩留言會獲得點贊!
1
- 一種快速檢測BCR/ABL基因融合的探針組、試劑盒及方法與流程
- 酪氨酸激酶抑制劑的制造方法與工藝
- 芳香族酰胺類衍生物、其制備方法及其在醫藥上的應用與制造工藝
- 包含5α?還原酶抑制劑的藥物組合物的制造方法與工藝
- 作為脾酪氨酸激酶抑制劑的二氮雜螺烷酮取代的噁唑衍生物的制造方法與工藝
- 包含熱彈性感覺劑和TRPA1受體抑制劑的皮膚接合剃刮助劑的制造方法與工藝
- 檢測EGFR耐藥性突變的方法和組合物與制造工藝
- 5?溴?7?氮雜吲哚啉?2?酮類化合物及其制備方法與制造工藝
- 3?[(3?{[4?(4?嗎啉基甲基)?1H?吡咯?2?基]亞甲基}?2?氧代?2,3?二氫?1H?吲哚?5?基)甲基]?1,3?噻唑烷?2,4?二酮和EGFR TYR激酶抑制劑的組合的制造方法與工藝
- 一種抗癌藥物的晶體化合物及其制備方法與制造工藝