一種生物法制備莫西沙星側鏈的方法與流程
本發明屬于生物制藥和生物化工技術領域,具體涉及一種生物法制備莫西沙星側鏈的生產方法。
背景技術:
(S,S)-2,8-二氮雜雙環[4.3.0]壬烷(1)及其N-保護衍生物(2)是合成應用廣泛的喹諾酮類抗菌藥莫西沙星的關鍵手性中間體,又稱莫西沙星側鏈或莫西小環:
由于(S,S)-2,8-二氮雜雙環[4.3.0]壬烷含有兩個手性中心,其合成方法通常有拆分法,不對稱合成法和手性源法。拆分法是最主要的應用方法,以2,3-二甲酸吡啶為起始原料,通過高壓氫化等方法獲得芐基保護的1的消旋體,利用酒石酸等拆分劑進行拆分獲得產品,理論收率低于50%,過程復雜,收率低(徐丹丹等,精細與專用化學品,2011,19卷第1期,43-44頁,收率43.3%)。
手性源法使用手性起始物料,如D-苯甘氨醇等合成1。但是由于沒有與1較為接近的手性化合物,存在步驟較長,收率較低(9步總收率27%)等問題(崔棟等,浙江化工,2013,44卷第8期,5-9頁)。
不對稱合成法包括:如US 5703244報道的通過sharpless不對稱環氧化構建手性中心:
和通過手性胺試劑氨化引入手性基團,如CN 201110312411的報道:
不對稱合成法較拆分法和手性源法具有較高的效率,但仍需要使用金屬催化劑和有機溶劑。US 5703244的合成路線需要11步反應,難以工藝化應用。CN 201110312411路線只需要5步反應,但是其關鍵步驟反應底物和產物需要柱層析分離,收率不高(36%-57%),且需要等量的手性反應試劑。綜上所述,化學法制備(S,S)-2,8-二氮雜雙環[4.3.0]壬烷普遍存在步驟長,收率低,條件苛刻,需要手性試劑等問題,導致產物成本較高,生產過程環境壓力較大。
另外一種生物法不對稱合成路線利用轉氨酶進行羰基的氨化(CN 201410418987),如圖所示,由于產物的ee值和得率都較低,且所用的酶來源未知,所以缺乏產業化應用價值。
本領域仍然需要一種能以較高的產品收率和生產效率制備莫西沙星側鏈的方法。
技術實現要素:
本發明公開了一種利用轉氨酶催化制備莫西沙星側鏈的方法,產品收率和生產效率較目前方法具有明顯的優勢。
具體而言,本發明公開一種下式2化合物的制備方法:
該方法包括:
(1)利用轉氨酶催化下式4化合物,形成式3化合物,
和
(2)在允許式3化合物自發閉環的條件下,由式3化合物自發閉環而得到式2 化合物;
其中,式2、3和4中,R選自:
在一個具體實施例中,所述反應在含有有機溶劑、氨基供體、緩沖液、轉氨酶和轉氨酶的輔酶的體系中進行。
在一個具體實施例中,所述有機溶劑選自:DMSO、乙腈、二甲基四氫呋喃、甲基叔丁基醚和DMF。
在一個具體實施例中,所述氨基供體為異丙胺、(R)-甲基芐胺、(S)-甲基芐胺或丙氨酸,優選為異丙胺。
在一個具體實施例中,所述轉氨酶選自:節桿菌(Arthrobacter sp.)、土曲霉(Aspergillus terreus)、河流弧菌(Vibrio fluvialis)、巨大芽孢桿菌(Bacillus megaterium)、少動鞘氨醇單胞菌(Sphingomonas paucimobilis)、海王生絲單胞菌(Hyphomonas neptunium)、青紫色素桿菌(Chromobacterium violaceum)中的ω-轉氨酶。
在一個具體實施例中,所述轉氨酶的序列如SEQ ID NO:1-20中任一所示。
在一個具體實施例中,所述轉氨酶的序列與SEQ ID NO:1-20中任一所示序列具有至少80%相同性。
在一個具體實施例中,所述輔酶選自磷酸吡哆醛。
在一個具體實施例中,所述體系的pH為7.0-10.0,優選8.0-10.0,更優選9.0-10.0。
在一個具體實施例中,所述體系的pH使用選自三乙醇胺緩沖溶液、Tris-HCl緩沖溶液、磷酸鹽緩沖溶液的緩沖液和補加異丙胺維持。
在一個具體實施例中,體系的反應溫度為30~45℃。
在一個具體實施例中,體系的反應溫度為35±3℃,優選35±1℃。
在一個具體實施例中,反應時間為8~24小時。
在一個具體實施例中,所述轉氨酶與式4化合物的用量(重量)配比為0.05~1:1。
在一個具體實施例中,輔酶與轉氨酶的用量(重量)配比為0.02~0.2:1。
在一個具體實施例中,以反應體系總體積計,式4化合物的濃度為1~120g/L。
在一個具體實施例中,化合物2的ee值大于99%,de值大于99%,收率大于95%。
附圖說明
圖1顯示實施例9制備得到的產物的NMR圖譜。
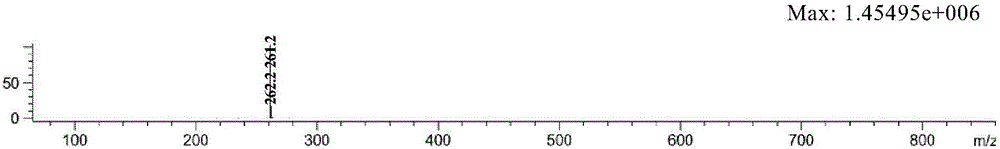
圖2顯示實施例9制備得到的產物的MS圖譜。
具體實施方式
本發明公開了一種利用轉氨酶催化制備2的路線,通過轉氨酶催化易得的底物4(參照路線4,合成只需要2步反應)轉化為中間產物3,3自發閉環得到2,剩余的R-底物5在堿性反應環境中自發消旋回到底物4,可以以>99%de,>99%ee和>90%收率一步獲得光學純的莫西沙星側鏈衍生物,且過程溫和環保。2脫保護基后即得到莫西沙星側鏈1,整個過程只需4步反應,收率高,條件溫和,無需手性試劑,與現有過程比較具有較高的實用性。
其中,
反應通常在含有氨基供體、緩沖溶液、轉氨酶、轉氨酶的輔酶和任選的有機溶劑的體系中進行。
通常,有機溶劑占反應體系總體積的0~30%。適用于本發明的有機溶劑可以是DMSO、乙腈、二甲基四氫呋喃、甲基叔丁基醚和DMF中的一種或多種。
適用于本發明的氨基供體可以是異丙胺、(R)-甲基芐胺、(S)-甲基芐胺和丙氨酸中的一種或多種,優選為異丙胺。在某些實施例中,氨基供體與底物4的摩爾比為1~5:1,優選1~3:1。
通常,使用有機溶劑時,反應體系中,有機溶劑和氨基供體的體積比通常在4~40:1的范圍之內,優選4~20:1。例如,在某些實施例中,使用DMSO和異丙胺的混合物,兩者的體積比為4~40:1,優選為4~20:1。
可用來制備式2化合物的轉氨酶包括但不限于來自節桿菌(Arthrobacter sp.)、土曲霉(Aspergillus terreus)、河流弧菌(Vibrio fluvialis)、巨大芽孢桿菌(Bacillus megaterium)、少動鞘氨醇單胞菌(Sphingomonas paucimobilis)、海王生絲單胞菌(Hyphomonas neptunium)或青紫色素桿菌(Chromobacterium violaceum)的ω-轉氨酶。
在一個具體實施例中,所述轉氨酶的序列如SEQ ID NO:1(來自文獻Appl.Microbiol.Biotechnol.93(4),1563-1573(2012))、SEQ ID NO:2(來自文獻Appl.Microbiol.Biotechnol.61(5-6),463-471(2003))、SEQ ID NO:3(來自文獻Protein Eng.Des.Sel.26(1),25-33(2013))、SEQ ID NO:4(來自文獻Genome Announc 2(5)(2014))、SEQ ID NO:5(來自文獻J.Bacteriol.193(16),4199-4213(2011))、SEQ ID NO:6(Genebank序列號:GAN13094.1)、SEQ ID NO:7(來自文獻J.Bacteriol.188(19),6841-6850(2006))、SEQ ID NO:8(來自文獻J.Bacteriol.188(19),6841-6850(2006))、以及SEQ ID NO:9-19所示。
本發明也包括使用與SEQ ID NO:1-20中任一序列的序列相同性為至少80%、優選至少85%、更優選至少90%、更優選至少95%、更優選至少98%的轉氨酶。優選的是,所述轉氨酶的酶活與SEQ ID NO:1-20中任一所示的轉氨酶的酶活至少相當。可采用本領域周知的方法來確定兩條序列之間的序列相同性,例如BLAST。
在優選的實施例中,本發明使用SEQ ID NO:18-20中任一項所示的轉氨酶。
輔酶通常是磷酸吡哆醛。輔酶與轉氨酶的重量配比為0.02~0.2:1,優選0.05~0.2:1,例如0.08~0.15:1。
轉氨酶與式4化合物的重量配比通常為1:1~20,優選為1:2~20,例如1:5~20。
以反應體系總體積計,式4化合物的濃度為1~120g/L,優選5~100g/L,例如5~80g/L、10~80g/L不等。
生成化合物3的反應通常在pH為7.0~10.0的條件下進行,優選pH為8.0~1.0,更優選為9.0~10.0。通常使用三乙醇胺緩沖溶液、Tris-HCl緩沖溶液、磷酸鹽緩沖溶液的緩沖液來維持反應體系的pH,優選使用三乙醇胺緩沖液。
生成化合物3的反應溫度通常為30~45℃,優選35±3℃,更優選35±1℃。
反應時間通常為8~24小時。在某些實施例中,式4化合物中R為芐氧基羰基;有機溶劑為DMSO,氨基供體為異丙胺,DMSO和異丙胺的體積比為4~40:1,優選為4~20:1;轉氨酶為SEQ ID NO:18-20中任一序列所示;輔酶與轉氨酶的重量配比為00.05~0.2:1;氨基供體與底物式4化合物的摩爾比為1~5:1;式4化合 物的濃度為5~100g/L;體系pH為9.0~10.0,使用三乙醇胺緩沖液調節和/或維持;反應溫度為35±1℃,反應時間為8~24小時。
在其它實施例中,可采用上述反應條件的任意組合來實施本發明的方法。
本發明采用的分析方法如下:
轉化率分析方法:HPLC/MS(安捷倫1260)裝備有C18色譜柱(4.6*50mm,5μm),流動相:0-3min,5%乙腈95%水,3-6min,40%乙腈60%水,6-7min,90%乙腈10%水,7-10min,5%乙腈95%水,流速0.3mL/min,檢測波長214nm,柱溫30度,出峰時間為:產物2c 6.2min,產物3c 5.5min,底物4c 8.3min。
產物光學純度分析方法:HPLC(島津LC-10AT)裝備有AD-H手性色譜柱(4.6*250mm,5μm),流動相:30%乙醇70%正己烷,流速1mL/min,檢測波長214nm,柱溫40度,出峰時間為:RR-2c 14min,SS-2c 17min。
實施例1:氨基保護基團的篩選
底物分別為芐基保護、甲酸乙酯保護和Cbz基團保護的4-(3-氯丙基)-3-吡咯烷酮(4a,4b,4c)10mg,溶解于0.2mL DMSO中,加入0.8mL三乙醇胺緩沖溶液中(pH8.0,0.1M),加入轉氨酶(SEQ ID NO:18)10mg,磷酸吡哆醛(PLP)1mg,異丙胺0.01mL,30度下反應24小時,檢測轉化率>99%,加入1mL乙酸乙酯萃取5次,合并有機相,干燥濃縮之后得到產品2a,2b,2c分別為3.44mg,7.44mg和8.37mg,其摩爾得率分別為40%,88%和95%。
實施例2:芐基保護底物穩定性考察
由于芐基保護底物的穩定性可能存在問題,故對其穩定性進行了考察。底物芐基保護的4-(3-氯丙基)-3-吡咯烷酮(4a)10mg,溶解于0.2mL DMSO中,分別加入0.8mL三乙醇胺緩沖溶液(pH 8.0,0.1M),磷酸鹽緩沖溶液(pH 8.0,0.1M)和去離子水,加入異丙胺0.01mL,30度下震蕩24小時,取樣檢測底物在HPLC中峰面積的變化,如下表:
表明該底物在酶反應條件下不穩定。
實施例3:反應溫度選擇
將10mg底物4c溶解于0.2mL DMSO中,加入0.8mL三乙醇胺緩沖溶液中(pH8.0,0.1M),加入轉氨酶(SEQ ID NO:18)1mg,PLP 0.1mg,異丙胺0.01mL,不同溫度下度下反應24小時,檢測轉化率,結果如下表所示:
實施例4:反應pH選擇
底物4c 10mg溶解于0.2mL DMSO中,加入0.8mL不同pH的緩沖溶液(0.1M),加入轉氨酶(SEQ ID NO:19)1mg,PLP 0.1mg,異丙胺0.01mL,35度下反應8小時,檢測轉化率,結果如下表所示:
實施例5:PLP用量選擇
底物4c 10mg溶解于0.2mL DMSO中,加入0.8mL三乙醇胺緩沖溶液中(pH9.0,0.1M),加入轉氨酶(SEQ ID NO:19)1mg,PLP 0.2-0.02mg,異丙胺0.01mL,35度下反應12小時,檢測轉化率,結果如下表所示:
實施例6:DMSO用量選擇
底物4c 10mg加入1mL三乙醇胺緩沖溶液中(pH 9.0,0.1M),加入轉氨酶(SEQ ID NO:20)1mg,PLP 0.05mg,異丙胺0.01mL,添加入不同量DMSO,35度下反應8小時,檢測轉化率,結果如下表所示:
實施例7:異丙胺用量選擇
底物4c 10mg溶解于0.2mL DMSO中,加入0.8mL三乙醇胺緩沖溶液中(pH9.0,0.1M),加入轉氨酶(SEQ ID NO:20)1mg,PLP 0.05mg,異丙胺0.005-0.02mL,35度下反應8小時,檢測轉化率,結果如下表所示:
實施例8:底物濃度選擇
底物4c 10,20,40,80,100mg溶解于0.2mL DMSO中,加入0.8mL三乙醇胺緩沖溶液中(pH 9.0,0.1M),加入轉氨酶(SEQ ID NO:20)4mg,PLP 0.05mg,異丙胺0.01mL,35度下反應8小時,檢測轉化率,結果如下表所示:
實施例9:產物制備
反應器中加入400mL 100mM pH 9.0三乙醇胺緩沖溶液,底物(3-(3-氯丙基)-4-羰基吡咯烷-1-甲酸苯甲酯)50g,DMSO 100mL,異丙胺25mL,磷酸吡哆醛0.25g,重組轉氨酶(購自蘇州漢酶生物技術有限公司,商品牌號EW094,SEQ ID NO:20) 2.5g,35度下反應24小時,HPLC檢測轉化率99.8%,產物ee值99.9%,de值99.9%。
加入1mL乙酸乙酯萃取5次,合并有機相,干燥濃縮之后得到產品41.9g,收率95%。
產物的NMR圖譜和MS圖譜分別如圖1和2所示。
對比實施例:
將10mg底物4c溶解于0.2mL DMSO中,加入0.8mL三乙醇胺緩沖溶液中(pH8.0,0.1M),加入轉氨酶(SEQ ID NO:1和4)1mg,PLP 0.1mg,異丙胺0.01mL,35度下反應24小時,檢測轉化率,分別為2.8%和5.0%。
- 還沒有人留言評論。精彩留言會獲得點贊!